典型相图分析
相图知识点总结

相图知识点总结相图的类型多种多样,例如散点图、折线图、柱状图、饼图、雷达图、气泡图等等。
每种图表的类型都有其适用的场景和数据类型。
以下是对一些常见相图的介绍和应用场景:散点图:散点图是用来展示两个变量之间的关系的一种图表,将两个变量的数值分别标在横纵坐标上,每一个数据点代表一个观察结果。
散点图适用于展示两个变量之间的相关性和趋势,以及发现异常值。
折线图:折线图是用来展示数据随着时间变化的趋势的一种图表,将时间放在横坐标上,数据值放在纵坐标上,通过连线的方式表示数据的变化趋势。
折线图适用于展示时间序列数据,如销售额、股票价格、气温等随时间的变化趋势。
柱状图:柱状图是用来对比不同类别之间的数据的一种图表,每个类别对应一个柱子,柱子的高度表示数据的数值。
柱状图适用于展示不同类别之间的数量对比,如不同产品的销售量、不同地区的人口数量等。
饼图:饼图是用来展示整体中各个部分占比的一种图表,将整体分成若干个扇形,每个扇形表示一个部分的占比。
饼图适用于展示总体分布中各个部分的比例关系,如各种产品在总销售额中的占比、各种食物在总热量中的占比等。
雷达图:雷达图是用来展示个体在多个维度上的数值的一种图表,以多边形的方式表示各个维度上的数值。
雷达图适用于对比个体在多个维度上的表现,如各种产品在多个特征上的表现、个人在多个能力维度上的表现等。
气泡图:气泡图是用来展示三个变量之间的关系的一种图表,除了横纵坐标表示两个变量外,气泡的大小表示第三个变量的大小。
气泡图适用于展示三个变量之间的关系和趋势,如不同地区的人口数量、GDP和地理面积之间的关系等。
相图的应用场景非常广泛,例如在商业分析中,可以利用相图来展示销售数据、市场趋势、客户行为等信息;在科学研究中,可以利用相图来展示实验数据、观测结果、统计分析等信息;在教育教学中,可以利用相图来展示知识点、考试成绩、学生表现等信息。
相图还可以用于各种报告、论文、展示等场合,帮助读者更好地理解和分析数据和信息。
相图分析ppt课件
当碳在铁中的含量超过溶解度时,多余碳以Fe3C 形式存在于铁碳合金,称为渗碳体。
Fe3C硬度高、强度低(b35MPa), 脆性大, 塑 性几乎为零。
Fe3C是一个亚稳相,在一定条件下可发生分解: Fe3C→3Fe+C(石墨), 该反应对铸铁有重要意义。
42
最新编辑ppt
⒉ 碳在铁中的固溶度
形成稳定化合物的合金: 性能-成分曲线出现拐点。
❖共晶合金
两相机械混合物的合金: 性能与合金成分呈直线关
系,是两相性能的算术平
均值。
混= ∙Q + β∙Qβ
HB混=HB ∙Q +HBβ∙Qβ
(Q 、Qβ为两相相对重量)36
最新编辑ppt
相图铸造性能的关系
固溶体合金:
液固相线间距越大、偏
析倾向大, 树枝晶发达, 流动性降低, 补缩能力 下降, 分散缩孔增加.
三条水平线hjbpskfe55一工业纯铁002二钢002214c高温组织为单相亚共析钢002077c共析钢077c过共析钢077214c214二fefec合金的平衡结晶过程56三白口铸铁214669c铸造性能好亚共晶白口铸铁21443c共晶白口铸铁43c过共晶白口铸铁43669c21457工业纯铁的结晶过程12点间转变为34点间56点间7点开始从中析出fe585921460共析相图与共晶相图相似共析相图与共晶相图相似共析线共析线pskpsk线线共析点共析点s点点共析温度共析温度共析共析成分成分共析合共析合金金共析成共析成分合金分合金亚共析合金亚共析合金共共析线上共析点以左的合析线上共析点以左的合金金过共析合金过共析合金共析线共析线上共析点以右的合金上共析点以右的合金
61
铁碳合金相图
最新编辑ppt
相图分析——精选推荐

相图分析物理化学复习总结之相平衡f组分数,⾃由度,相图,相点,露点,泡点,共熔点,(连)结线,三相线,步冷(冷却)曲线,低共熔混合物(固相完全不互溶)本章主要要求掌握相律的使⽤条件和应⽤,单组分和双组分系统的各类典型相图特征、绘制⽅法和应⽤,利⽤杠杆规则进⾏有关计算1、相律: F = C - P + n , 其中:C=S-R-R’U+ }3 Q0 G- D4 L$ \6 e- D) l(1) 强度因素T,p可变时n=2/ n) \+ r' I3 G" P5 [3 q* A) f(2) 对单组分系统:C=1, F=3-P j(3) 对双组分系统:C=2,F=4-P;应⽤于平⾯相图时恒温或恒压,F=3-P。
Y% z2 ]7 h' z5 d- X- 2、相图(1)相图:相态与T,p,x的关系图,通常将有关的相变点联结⽽成。
(2)实验⽅法:实验主要是测定系统的相变点。
常⽤如下四种⽅法得到。
4 Z r! M- J2 u! s( _. ms 对于⽓液平衡系统,常⽤⽅法蒸⽓压法和沸点法;" A+ d4 S0 D/ v! r液固(凝聚)系统,通常⽤热分析法和溶解度法。
$ l( m3 N$ j5 a" ^3、单组分系统的典型相图对于单组分系统C=1,F=C-P+2=3-P。
当相数P=1时,⾃由度数F=2最⼤,即为双变量系统,通常绘制蒸⽓压-温度(p-T)相图,见下图。
(a) 正常相图(b) ⽔的相图(c) 硫的相图图6-1 常见的单组分系统相图/ ]. g/ W. Y' n* ?" ^# _⼆组分系统的相图j类型:恒压的t-x(y)和恒温的p-x(y)相图。
相态:⽓液相图和液-固(凝聚系统)相图。
5 f% ^( `8 E0 e; h; W! y1 |8 SB(1)⽓液相图根据液态的互溶性分为完全互溶(细分为形成理想混合物、最⼤正偏差和最⼤负偏差)、部分互溶(细分为有⼀低共溶点和有⼀转变温度的系统)和完全不溶(溶液完全分层)的相图。
典型相图分析

第三节 二元共晶相图
二、共晶体的形成
第三节 二元共晶相图
二、共晶体的形成
第三节 二元共晶相图
二、共晶体的形成
第三节 二元共晶相图
三、典型合金的凝固
1. 合金IV(成分在E点附近)
特点
1) 在液体中α 和β 同时具有析 出条件,都可以析出。
2) 由于α 和β 析出过程在成分 上可以互相补充和促进,共 同析出。
第四章 典型相图分析
相图知识 二元匀晶相图与固溶体的凝固 二元共晶相图 二元包晶相图 复杂二元相图的分析方法 三元相图
一、相律 第一节 相图知识
对于恒压条件:f = c – p + 1 系统中有p相,c个组元,则成分引起的变数p(c-1)个。系 统总的变数为p(c-1)+1 在多相平衡时,任一组元在各相间的化学位相等, 每个 组元可写出个p-1等式,平衡条件总数为c(p-1)
第二节 二元匀晶相图与固溶体的凝固
四、固溶体材料非平衡冷却
非平衡凝固的特点有:①凝固过程中,液、固两相的成分偏离液、固相线; ②凝固过程进行到一更低的温度才能完成;③生成固体的成分是不均匀的。 随着冷却速度的加大,这些差别特点表现的愈明显。
结果:生成固体的成分不均匀较偏析,快速冷却时在一个晶粒内部先后结晶 的成分有差别,所以称为晶内偏析,金属的晶体往往以树枝晶方式生长,偏 析的分布表现为不同层次的枝晶成分有差别,因此这种偏析又称枝晶偏析。
在冷却速度较快时的凝固是非平衡凝固,从相图中可见,在略低于开始 凝固温度t 1下开始析出的固体的成分为α 1,到t 2温度晶体表面生长的成分 可为α 2,由于扩散速度跟不上来,心部的成分来不及达到和表面一样就冷却 到下一温度t 3,因此析出的固体的成分表里不一,平均成分也偏离了固相线。 到达平衡和固相线交点的温度t f时还有液相存在,继续冷却到一更低的温度, 固体的平均成分回到合金成分时液体消失,凝固过程才结束。
相图分析——精选推荐

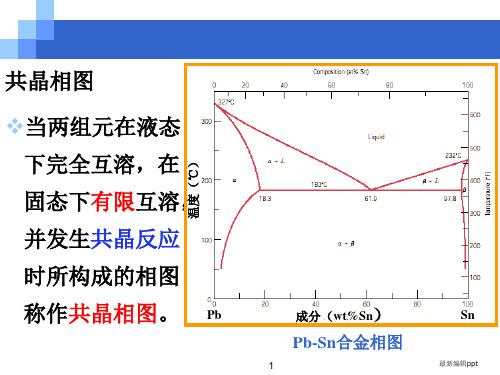
合金相图分析(一)共晶相图分析图1-1 Pb-Sn合金相图一、认识相图Pb-Sn合金相图中有三种相:Pb与Sn形成的液溶体L相,Sn溶于Pb中的有限固溶体α相,Pb溶于Sn中的有限固溶体β相。
相图中有三个单相区:L、α、β三个双相区:L+α、L+β、α+β一条L+α+β的三相共存线(水平线cde )。
这种相图称为共晶相图。
(Al-Si、Ag-Cu合金也具有共晶相图。
)d点为共晶点, 表示此点成分(共晶成分)的合金冷却到此点所对应的温度(共晶温度)时, 共同结晶出c点成分的α相和e点成分的β相。
一种液相在恒温下同时结晶出两种固相的反应叫做共晶反应。
所生成的两相混合物叫共晶体。
发生共晶反应时有三相共存, 它们各自的成分是确定的, 反应在恒温下平衡地进行。
水平线cde为共晶反应线, 成分在ce之间的合金平衡结晶时都会发生共晶反应。
cf线为Sn在Pb中的溶解度线(或α 相的固溶线)。
温度降低, 固溶体的溶解度下降。
Sn 含量大于f点的合金从高温冷却到室温时, 从α相中析出β相以降低α相中Sn含量。
从固态α相中析出的β相称为二次β,记为βII,该过程可表达为:α→ βII。
eg线为Pb在Sn中溶解度线(或β 相的固溶线)。
Sn含量小g点的合金, 冷却过程中同样发生二次结晶, 析出αII。
二、不同成份合金结晶过程1. 合金I的平衡结晶过程图1-2 合金I的平衡结晶过程液态合金冷却到1点温度以后, 发生匀晶结晶过程, 至2点温度合金完全结晶成α固溶体, 随后的冷却(2~3点间的温度), α相不变。
从3点温度开始, 由于Sn在α中的溶解度沿cf 线降低, 从α中析出βII, 到室温时α中Sn含量逐渐变为f点。
最后合金得到的组织为α+ βII。
其组成相是f点成分的α相和g点成分的β相。
运用杠杆定律, 两相的质量分数为:合金室温组织由α和βII组成, α和βII即为组织组成物。
组织组成物是指合金组织中那些具有确定本质, 一定形成机制的特殊形态的组成部分。
相图的绘制和解读方法介绍

相图的绘制和解读方法介绍相图,即相容性图,是描述物质在不同温度和压力下的相变关系的图表。
相图能够帮助科学家们了解物质的相态转变规律,从而在材料研究、工艺制备和能源开发等领域发挥重要作用。
本文将介绍相图的绘制和解读方法,以期帮助读者更好地理解和应用相图。
一、相图的基本概念相图是以温度和压力为坐标轴,将物质的不同相态(如固态、液态、气态等)在相图中进行绘制的图表。
相图中的曲线表示了相变的边界,曲线上方表示一种相态,曲线下方表示另一种相态,曲线上的点表示两种相态共存的状态。
相图中的相变曲线可以分为平衡曲线和非平衡曲线,平衡曲线表示物质在平衡状态下的相变边界,而非平衡曲线则表示物质在非平衡状态下的相变边界。
二、相图的绘制方法相图的绘制需要获取物质在不同温度和压力下的相变数据,然后将这些数据绘制在相图上。
一般来说,相图的绘制可以通过实验和计算两种方法来进行。
实验方法是通过在实验室中对物质进行相变实验,测量不同温度和压力下的相变点,并将这些数据绘制在相图上。
这种方法的优点是准确性高,但是实验过程较为繁琐,需要较长的时间和大量的实验数据。
计算方法是通过利用物质的热力学性质,运用热力学模型和计算软件来计算不同温度和压力下的相变点,并将这些数据绘制在相图上。
这种方法的优点是快速、方便,但是需要准确的热力学参数和计算模型的支持。
三、相图的解读方法相图的解读可以帮助我们了解物质的相态转变规律,从而指导材料研究和工艺制备。
下面介绍几种常用的相图解读方法。
1. 相图的平衡区域解读相图中的平衡区域是指相图中曲线上方的区域,表示两种相态共存的状态。
通过观察平衡区域的形状和大小,可以了解物质的相变稳定性和相变速率。
平衡区域越大,相变稳定性越好,相变速率越慢。
2. 相图的相变温度解读相图中的相变温度是指曲线上的点,表示两种相态共存的状态。
通过观察相变温度的变化趋势,可以了解物质的相变温度范围和相变类型。
相变温度的变化趋势可以帮助我们优化材料研究和工艺制备的温度条件。
铁碳相图详解

三、典型铁碳合金的平衡结晶过程铁碳相图上的合金,按成分可分为三类:⑴ 工业纯铁(〈0.0218% C ),其显微组织为铁素体晶粒,工业上很少应用。
⑵ 碳钢(0.0218%~2。
11%C ),其特点是高温组织为单相A,易于变形,碳钢又分为亚共析钢(0.0218%~0。
77%C)、共析钢(0.77%C )和过共析钢(0。
77%~2.11%C )。
⑶ 白口铸铁(2。
11%~6。
69%C ),其特点是铸造性能好,但硬而脆,白口铸铁又分为亚共晶白口铸铁(2。
11%~4。
3%C )、共晶白口铸铁(4.3%C )和过共晶白口铸铁(4.3-6.69%C)下面结合图3-26,分析典型铁碳合金的结晶过程及其组织变化.图3—26 七种典型合金在铁碳合金相图中的位置㈠ 工业纯铁(图3-26中合金①)的结晶过程合金液体在1~2点之间通过匀晶反应转变为δ铁素体.继续降温时,在2~3点之间,不发生组织转变。
温度降低到3点以后,开始从d 铁素体中析出奥氏体,在3~4点之间,随温度下降,奥氏体的数量不断增多,到达4点以后,d 铁素体全部转变为奥氏体。
在4~5点之间,不发生组织转变。
冷却到5点时,开始从奥氏体中析出铁素体,温度降到6点,奥氏体全部转变为铁素体。
在6-7点之间冷却,不发生组织转变.温度降到7点,开始沿铁素体晶界析出三次渗碳体Fe 3C III 。
7点以下,随温度下降,Fe 3C III 量不断增加,室温下Fe 3C III 的最大量为:%31.0%1000008.069.60008.00218.03=⨯--=ⅢC Fe Q .图3—27为工业纯铁的冷却曲线及组织转变示意图。
工业纯铁的室温组织为a+Fe 3C III ,如图3—28所示,图中个别部位的双晶界内是Fe 3C III 。
图3-27 工业纯铁的冷却曲线及组织转变示意图 图3-28 工业纯铁的显微组织 400× ㈡ 共析钢(图3-26中合金②)的结晶过程共析钢的含碳量为0.77%,超过了包晶线上最大的含碳量0。
相图分析课件
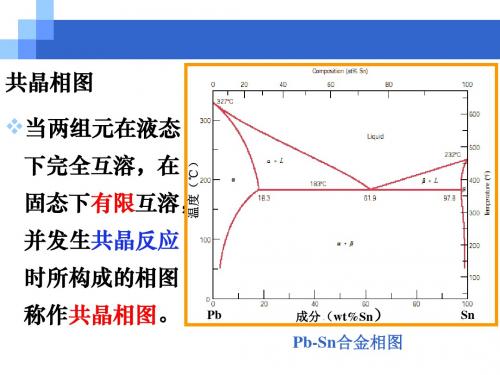
在一定温度下,由一
B
定成分的液相同时结
晶出两个成分和结构
都不相同的新固相的
转变称作共晶转变或
共晶反应。
共晶反应的产物, 即两相的机械混合 物称共晶体或共晶 组织。
发生共晶反应的温 度称共晶温度。
代表共晶温度和共 晶成分的点称共晶 点。
具有共晶成分的合金称共晶合金。在共晶线
上,凡成分位于共晶点以左的合金称亚共晶合 金;位于共晶点以右的合金称过共晶合金。
3、二元包晶相图
当两组元在液态下完全互溶,在固态下有限互溶, 并发生包晶反应时所构成的相图称作包晶相图。 在一定温度下,由一个液相包着一个固相生成另 一新固相的反应称包晶转变或包晶反应。
单相区:L、、β
二相区:L+、 L+、+
三相区:L++
(水平线PDC)
L+
+
共晶组织形态
Pb-Sn共晶组织
在共晶转变过程中,L、 、 三相共存, 三个相 的量在不断变化,但各自 成分固定。 共晶组织中的相称共晶相。
C(19.2)
E(61.9) D(97.5)
共晶转变结束时, 和 相的相对重量百分比为:
Q
ED 100% CD
97.5 61.9 100% 45.4% 97.5 19.2
L
L+
水平线PDC称包晶线。 与该线成分对应的合金在该温度下发生包晶反应:
LC+P⇄βD 。 该反应是液相L包着固相, 新相 β 在L与α的界 面上形核,并向L和两个方向长大。
合金的结晶过程 (1)包晶成分合金:匀晶包晶二次析出。
室温组织为β + II
相图分析

图1-7过共晶合金组织
(二)包晶相图分析
图2-1 Pt-Ag合金相图
一、认识包晶相图
Pt-Ag、Ag-Sn、Sn-Sb合金具有包晶相图。
Pt-Ag合金相图中存在三种相:
Pt与Ag形成的液溶体L相;
Ag溶于Pt中的有限固溶体α相;
Pt溶于Ag中的有限固溶体β相。
e点为包晶点, e点成分的合金冷却到e点所对应的温度(包晶温度)时发生包晶反应L+α →β。发生包晶反应时三相共存,它们的成分确定,反应在恒温下平衡地进行。水平线ced为包晶反应线。
cf为Ag在α中的溶解度线, eg为Pt在β中的溶解度线。
1.合金I的结晶过程
合金冷却到1点温度以下时结晶出α固溶体, α相成分沿ac线变化, L相成分沿ad线变化。合金刚冷到2点温度而尚未发生包晶反应前,由c点成分的α相与d点成分的L相组成。此两相在e点温度时发生包晶反应,L相包围α相而形成β。反应结束后, L相与α相正好全部反应耗尽,形成e点成分的β固溶体。温度继续下降,从β中析出αⅡ。最后室温组织为β+αⅡ。其组成相和组织组成物的成分和质量分数可根据杠杆定律来确定。
图1-3合金II的平衡结晶过程
图1-4共晶合金组织的形态
3.合金Ⅲ的结晶过程
图1-5合金Ⅲ平衡结晶过程
合金Ⅲ是亚共晶合金,合金冷却到1点温度后,由匀晶反应生成α固溶体,叫初生α固溶体。从1点到2点温度的冷却过程中,按照杠杆定律,初生α的成分沿ac线变化,液相成分沿ad线变化;初生α逐渐增多,液相逐渐减少。当刚冷却到2点温度时,合金由c点成分的初生α相和d点成分的液相组成。然后液相进行共晶反应,但初生α相不变化。经一定时间到2点共晶反应结束时,合金转变为α+(α+β)。从共晶温度继续往下冷却,初生α中不断析出,成分由c点降至f点;共晶体形态、成分和总量保持不变。合金的室温组织为初生α+ βⅡ+ (α+β) ,合金的组成相为α和β ,它们的质量分数为:
高中化学物质相图的分析题解析与应用

高中化学物质相图的分析题解析与应用化学是一门研究物质变化和性质的科学,而物质相图是化学中重要的工具之一。
相图可以帮助我们理解物质在不同条件下的相变规律,从而应用于实际问题的解决。
在高中化学考试中,相图的分析题是常见的题型之一,掌握解题技巧对于学生来说至关重要。
本文将通过具体的例子,分析相图题的考点,并给出解题技巧和应用。
首先,我们来看一个具体的例子:某物质在常压下的相图如下图所示。
(图片描述:相图示意图)根据相图,我们可以得出以下信息:1. 在低温和低压下,物质处于固态,随着温度升高,物质从固态转变为液态。
2. 在高温和低压下,物质处于气态,随着温度降低,物质从气态转变为液态。
3. 在高压和高温下,物质处于液态,随着温度降低,物质从液态转变为固态。
根据以上分析,我们可以得出以下解题技巧:1. 根据相图中的斜线,可以确定物质在不同温度和压力下的相变情况。
斜线表示两相共存的平衡线,斜率表示相变的速率。
2. 根据相图中的相变温度和压力,可以判断物质的相变类型。
例如,当相变温度随着压力的增加而升高时,说明物质的相变是正常的。
3. 根据相图中的相变点,可以计算物质的熔点、沸点等性质。
例如,在相图中,固液相变的温度称为熔点,液气相变的温度称为沸点。
接下来,我们来应用相图解决一个实际问题。
假设我们需要在高海拔地区煮鸡蛋,但由于气压较低,水的沸点也会降低。
我们可以通过相图来计算出在该地区水的沸点。
首先,我们需要找到该地区的气压。
假设该地区的气压为80 kPa。
然后,我们查找水的相图,找到对应的气压和沸点。
假设水的相图如下图所示。
(图片描述:水的相图示意图)根据相图,我们可以得出以下信息:1. 在常压下,水的沸点为100℃。
2. 当气压为80 kPa时,水的沸点约为95℃。
根据以上分析,我们可以得出结论:在该高海拔地区,水的沸点约为95℃。
通过以上例子,我们可以看出相图在解决实际问题中的应用价值。
对于高中化学考试中的相图分析题,我们可以总结出以下解题步骤:1. 仔细观察相图,了解相图中的各个区域和线条的含义。
典型铝合金相图 ppt

-
焦宇鸿
焦宇鸿
-
焦宇鸿
焦宇鸿
-
焦宇鸿
焦宇鸿
-
焦宇鸿
焦宇鸿
-
焦宇鸿
焦宇鸿
-
焦宇鸿
焦宇鸿
-
焦宇鸿
焦宇鸿
-
焦宇鸿
焦宇鸿
-
焦宇鸿
焦宇鸿
-
焦宇鸿
焦宇鸿
-
焦宇鸿
焦宇鸿
-
焦宇鸿
焦宇鸿
焦宇鸿
-
焦宇鸿
焦宇鸿
-
焦宇鸿
焦宇鸿
典型的铝合金三元相图
-
焦宇鸿
焦宇鸿
-
焦宇鸿
焦宇鸿
-
焦宇鸿
焦宇鸿
-
焦宇鸿
焦宇鸿
-
焦宇鸿
焦宇鸿
-
焦宇鸿
焦宇鸿
-
焦宇鸿
焦宇鸿
-
焦宇鸿
焦宇鸿
-
焦宇鸿
焦宇鸿
-
焦宇鸿
焦宇鸿
-
焦宇鸿
焦宇鸿
-
焦宇鸿
焦宇鸿
-
焦宇鸿
焦宇鸿
-
焦宇鸿
焦宇鸿
-
焦宇鸿
焦宇鸿
焦宇鸿
典型的铝铝合金相图
-
焦宇鸿
1. 二元合金相图
焦宇鸿
-
焦宇鸿
焦宇鸿
-
焦宇鸿
焦宇鸿
-
焦宇鸿
焦宇鸿
-
焦宇鸿
焦宇鸿
-
焦宇鸿
焦宇鸿
-
焦宇鸿
焦宇鸿
-
焦宇鸿
焦宇鸿
-
焦宇鸿
焦宇鸿
-
冶金物理化学--相图

基本概念回顾v自由度:体系的总变量数减去独立方程数的式,为 独立变量数,也即体系的自由度。
----计算方法冶金物理化学—相图体系总变量数为:(m-1)r+2(考虑温度和压力条件下)其中:假设体系有m个组元,存在r个相,则其中m-1个组元应为独立组 元。
则变量数为:(m-1)r独立方程数:(r-1)m 故自由度: f=m+2-r相律:若C表示组元的数量,P表示相的数量,则 相律常写为f=C-P+2。
冶金物理化学(相图)基本概念回顾 几个定义:v组元:组成系统的独立化学组成物。
合金中元素 视为组元,陶瓷中某一化合物视为组元。
v相:在一个多相体系中由界面分开的物质的均匀 部分,它们具有相同的物理、化学性质和晶体结 构。
v自由度:平衡状态下,在不改变相的类型和数目 时,可以独立变化的状态函数的数量。
冶金物理化学(相图)二元相图的类型v十二个基本类型1、具有最低共溶点或称简单共晶; 2、具有稳定化合物或称同分熔点化合物; 3、具有异分熔点化合物; 4、具有固相分解的化合物; 5、固相晶型转变; 6、液相分层; 7、形成连续固溶体; 8、具有最低点或最高点的连续固溶体; 9、具有低共熔点并形成不连续固溶体; 10、具有转熔反应并形成有限固溶体; 11、具有共析反应; 12、具有包析反应。
冶金物理化学(相图)二元相图的几何元素---面、线v 二元相图由曲线、水平线、垂直线和斜线组成,这些 线把整个图面分成若干区域 区域,形成若干交点 交点。
从而形成相 图中的基本几何元素点、线、面。
v二元相图的几何元素---线二元相图的垂直线:是两组分形成化合物的组成线,可以是 稳定化合物也可以是不稳定化合物。
在化合物的熔点温度,液相和固相有相同的组成,此种化合物 即为稳定化合物,又称同分熔点化合物 同分熔点化合物;若化合物没有固定熔点 仅有分解温度,作为分解产物的固相和液相组成都与原固相化合 物不同,此化合物即为不稳定化合物,也称为异分熔点化合物 异分熔点化合物。
相图的分析

分离应用举例
g
Cl (HNO3+H2SO4) Cl NO2 w = 0.33
246
l+g
精 馏 釜 底 液 送 往 A 结 晶 器
l 送 精 馏 塔 送 精 馏 塔
进 入 混合液 B 结 晶 器
242 82.2
Cl
NO2 w = 0.66 NO2 w = 0.01
Cl
分 分 离 离 l+s 出 32.9 出 邻 对 s+l 硝 硝 14.7 基 基 s(A)+s(B) 氯 氯 苯 苯 0.0 0.2 0.4 0.6 0.8 1.0 xB 邻硝基氯苯 对硝基氯苯 • 邻硝基氯苯(A) - 对硝基氯苯(B)系统 7 结晶与精馏相结合的分离原理示意图
5
溶解度法
由溶解度数据绘制如下所示的相图:
2 3
L 1
M
S
• 状态为L0点的溶液冷却析 出的低共熔混体物称为低 熔冰盐合晶, 在实验室里常 用来制冷, 得到0℃以下的 低温. • 水盐系统相图可应用于结 晶法精制盐类(见图示). • 冷却结晶过程中晶体与母 液的量遵守杠杆规则:
m (盐晶体 ) LM = m ( 母液 ) MS
相图的分析
• 分析相图
“相图”动画
• PL线和QL线分别称为A和B 的凝固点降低曲线, 或溶解度 曲线. • )三相线S1LS2上(除两端点) 的系统点所处相平衡状态 可表示为:
s1 (A) + s 2 (B )
l(L)
• 液相点L称为 低共熔点, 该组 成的液相冷凝得到的固体称为 低共熔混合物. • 常用于结晶分离、熔盐电解等.
0 A
wB (b)
1 B
• 由步冷曲线(a)作Bi(A)-Cd(B)系统的温度-组成图(b)
二元系相图基本类型介绍及分析(自己整理)

图 4 二元连续固溶体相同的两种特殊情况(a)具有最高熔点的二元连续固溶体相 图; (b)具有最低熔点的二元连续固溶体相图
②形成不连续固溶体的二元系统相图
溶质只能以一定的限量溶入溶剂,超过限度便会出现第二相,这种固溶体称 为不连续(也称部分互溶或有限互溶)固溶体。在 A,B 两组元形成有限固溶体 系统中,以 SA(B)表示 B 组元溶解在 A 晶体中所形成的固溶体,SB(A)表示 A 组元 溶解在 B 晶体中所形成的固溶体。根据无变量点性质的不同,这类相图又可以 分为具有“低共熔点”和具有“转熔点”两种类型。 1)具有“低共熔点”的有限固溶体的二元系统相图(共晶体系)
图 2 生成连续固溶体的二元系统分布系数示意图(a)K0<1;(b)K0>1
在形成连续固溶体的系统中,任一组成的熔体的凝固点都介于两个纯组元 的凝固点之间。因此可以从熔体中把两组元分离获得纯粹的 A 和 B。
图 3 分步结晶法示意图
将某熔体 M 冷却到 1 点, 系统由固溶体 S1 和液相 L1 两部分组成。 这时 S1 中 A 的百分含量比原熔体 M 中的 A 百分含量多(横坐标中越靠近 A 点,A 含 量越高) ,L1 中 B 的百分含量比原熔体中 B 的百分含量多。将 L1 分离出来并冷 却到 3 点,则可获得 L3 液相且其 B 的百分含量又比 L1 中 B 的百分含量多。如 此重复,可获得纯 B(确切地讲比较纯的 B) ;另一方面,将 S1 重新熔化,然后 再冷却到2点获得固溶体 S2, 其中 A 的百分含量比 S1 多。 重复几次可得比较纯 的 A。这种办法叫做分步结晶法,可以把固溶体中两组元分离开。 在连续固溶体相图中还有两种特殊情况即具有“最高熔点”和“最低熔点” 的系统, 见图 4。 这两种相图可以看成是由两个简单连续固溶体二元相图构成的。 体系中的平衡关系可由子相图来分析,也可以把相图中的最高熔点 C 和最低熔 点 M 看成是“同成分熔点”/“同成分点” 。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
晶内偏析的程度决定于:相图中液—固相线相距愈远,组元元素原子的迁移 能力愈低(扩散系数小),冷却速度愈大,造成的晶内偏析将愈严重。
消除偏析的方法:前两条原因是不可更改的,但并不是采用慢速冷却,因为 慢速冷却会使晶粒变大,最高和最低成分之间的距离加大消除更困难,而是 快速冷却,细化晶粒,会带来晶内的偏析,即宏观均匀而微观有大的差别, 凝固后重新加热到略低于熔点温度,进行一段时间的保温,让原子在这时进 行扩散迁移,达到均匀,这种方法称为均匀化退火。
f=变数-条件数= p(c-1)+1- c(p-1)=c-p+1
第一节 相图知识
一、相律
二元相图:当存在两个组元时,成分也是变量,但一种组元的含 量为独立,另一组元则为余下部分。为在二维平面上表示, 通常只考虑在常压下,取两个变量温度和成分。横座标用线 段表示成分,纵座标表示温度。平面上以按这时平衡状态下 存在的相来分隔。(如图)
五、固溶体中溶质的分布
例一:定向凝固时溶质分布规律
如果有一长度为L的杆形凝固体,假设凝固过程为一端散热,并且 液体中原子扩散和对流可达到成分均匀,而固体中迁移慢设为凝固后基 本不能变。当合金的成分为C0,开始析出的固体成分为k0C0,变化趋势 如图。已经凝固距离X后,在凝固dx时,按溶质的变化有:
当x 0时,C S (0) C0 CL (0) C0 k0
第二节 二元匀晶相图与固溶体的凝固
三、固溶体材料冷却时组织转变
特点:
1.与纯金属凝固一样由 形核和长大来完成结晶 过程,实际进行在一定 的过冷度下。 2.凝固在一温度范围内 进行。只有在温度不断 下将时固体量才增加, 温度不变,液固数量维 持平衡不变。 3.凝固过程中液体和固 体的成分在不断变化。
在冷却速度较快时的凝固是非平衡凝固,从相图中可见,在略低于开始 凝固温度t 1下开始析出的固体的成分为α1,到t 2温度晶体表面生长的成分 可为α2,由于扩散速度跟不上来,心部的成分来不及达到和表面一样就冷却 到下一温度t 3,因此析出的固体的成分表里不一,平均成分也偏离了固相线。 到达平衡和固相线交点的温度t f时还有液相存在,继续冷却到一更低的温度, 固体的平均成分回到合金成分时液体消失,凝固过程才结束。
第二节 二元匀晶相图与固溶体的凝固
四、固溶体材料非平衡冷却
过程:
从固溶体的凝固特征可知,在晶体长 大过程中,组元元素在析出的固相中不断 的发生迁移。但原子在固体中的迁移相对 结晶过程是较慢的(原子的迁移是扩散过 程,以后专门讨论),可见完全达到平衡 凝固是较困难的,需要相当长的时间,一 般的冷却凝固达不到平衡状态。
第二节
二元匀晶相图与固溶体的凝固
一、图形式
两组元在液态和固态都能无限互溶。如Cu—Ni、Ag—Au形 成二元合金对应的相图就是二元匀晶相图。
相图的构成:由两条曲线将 相图分为三个区。左右两端 点分别为组元的熔点。上面 的一条曲线称为液相线,液 相线之上为液相的单相区, 常用L表示;下面的一条曲 线称为固相线,固相线之下 为固溶体的单相区,常用α 表示;两条曲线之间是双相 区,标记L+α表示。
在TE温度以下仅是固体的冷却
第三节 二元共晶相图
二、共晶体的形成
形核特点
交替形核 在一定的过冷度下,尽管两固相都可能从液体中 形核,由于两固溶体的成分结构的差别,总有一个固相先形核, 它称为领先相,设领先相为α,由于α富A组元,其生长时附 近液体则富B组元,α的存在和液体中B的富集,β相将附着在 α上形核并长大,同理在β相外将附着α的形核长大。这种方 式就是交替形核。此外也有人认为交替形核是以边缘桥接生长 方式来实现的。
典型相图分析
相图知识
二元匀晶相图与固溶体的凝固
二元共晶相图 二元包晶相图
复杂二元相图的分析方法
三元相图
一、相律
第一节 相图知识
对于恒压条件:f = c – p + 1 系统中有p相,c个组元,则成分引起的变数p(c-1)个。系 统总的变数为p(c-1)+1 在多相平衡时,任一组元在各相间的化学位相等, 每个 组元可写出个p-1等式,平衡条件总数为c(p-1)
第三节 二元共晶相图
二、共晶体的形成
过程
成分为E点合金的凝固
在TE温度以上仅是液体的冷却 到达略低于TE的温度,按L+α相区分析应为从液体中析出C成分的α相,而 按L+β相区分析应从液体中析出D成分的β相。如果α和β按一定的比例析 出,最终液体的成分不变,两固相不断同时析出,即共同结晶,故称为共晶 转变,直到液体完全消失,结晶过程完成,得到的是两固相的混合物,称为 共晶体。
第二节 二元匀晶相图与固溶体的凝固
四、固溶体材料非平衡冷却
非平衡凝固的特点有:①凝固过程中,液、固两相的成分偏离液、固相线; ②凝固过程进行到一更低的温度才能完成;③生成固体的成分是不均匀的。 随着冷却速度的加大,这些差别特点表现的愈明显。 结果:生成固体的成分不均匀较偏析,快速冷却时在一个晶粒内部先后结晶 的成分有差别,所以称为晶内偏析,金属的晶体往往以树枝晶方式生长,偏 析的分布表现为不同层次的枝晶成分有差别,因此这种偏析又称枝晶偏析。
相图用途:
1. 由材料的成分和温度预知平衡相; 2. 材料的成分一定而温度发生变化 时其他平衡相变化的规律; 3. 估算平衡相的数量。
预测材料的组织和性能
第一节 相图知识
二、相图与冷却曲线的关系:
成分一定,在冷却过程中,不同的相热容量不相同,如果 系统散热能力一样,温度随时间的变化(冷却)曲线上的斜率将 不同,曲线的转折点对应温度就是某些相开始出现或完全小时 的温度,利用这一特点,由实测的冷却曲线可以作出相图。
第二节 二元匀晶相图与固溶体的凝固
六、成分过冷
成分过冷对凝固过程的影响
3. 中区域的成分过冷可能生成胞 状到树枝晶的各种过渡组织。 4. 成分过冷区较大,凸起发展较 长,在凸起上再生新的凸起, 就可生成树枝晶。 5. 如果成分过冷区域特别大,得到的成分过冷度也十分大,若 达到形核要求的过冷度时,在成分过冷区可能形成新的晶核, 新晶核的生长阻碍原晶粒生长,对柱状晶的发展产生隔断作 用。
第二节 二元匀晶相图与固溶体的凝固
五、固溶体中溶质的分布
由于固溶体凝固中,析出固体的成分与液体不相同,并 且在凝固时达不到平衡,所以凝固后溶质的分布是不均匀的, 当然这种不均匀有时也可带来有利的利用。下面仅就几种特 例讨论。 如图所示相图的一部分,在温度t时,平衡 的液—固相成分的比,称为平衡分配系数。
第二节 二元匀晶相图与固溶体的凝固
五、固溶体中溶质的分布
例二:关于区域熔炼
第二节 二元匀晶相图与固溶体的凝固
六、成分过冷
在正温度梯度下,纯金属的生长方式为平面推进,而固 溶体凝固时,却有树枝状生长和胞状生长存在,这是由于凝 固过程中,成分是在不断变化,液体和固体的成分均不能达 到平衡状态,产生了成分过冷现象。
第三节 二元共晶相图
二、共晶体的形成
生长特点
共同生长 两个相长大时都要 排放相应的溶质组元,排出的溶 质将阻碍自身的生长,但两相同 时生长时,一相排出的组元正是 另一相生长所需要的,所以两相 的生长过程将互相促进,最后是 两相共同携手长大。由于两固相 的成分是固定的,综合成分应和 液体的成分相同,它们的数量反 映在二者的厚度相对比例上。
一般用占总体数量的百分 比的相对值来表示。如果 把线段axc当成一杠杆,则 他们满足杠杆力的平衡原 理,所以称之为杠杆定律。
用杠杆定律来分析在理解和使用都有好的直观性和方便。适用所有两相平衡。
第二节 二元匀晶相图与固溶体的凝固
三、固溶体材料冷却时组织转变
过程:
1点以上液体冷却 1点开始凝固,固体成 分在对应固相线处 1-2之间,温度下降, 液体数量减少,固体数 量增加,成分沿液相线 和固相线变化, 到2点,液体数量为0, 固体成分回到合金原始 成分,凝固完成 2点以下固体冷却,无 组织变化
第三节 二元共晶相图
二、共晶体的形成
组织特点
当两个固相都是金属性较 强相时,共晶体一般生长成层 片状。当两相的相对数量比相 差悬殊时,在界面能的作用下, 数量较小的相将收缩为条、棒 状,更少时为纤维状,甚至为 点(球)状。 当有一相或两相都具有较强的非金属性时,它们表现出较 强的各向异性,不同方向的生长速度不同,并且有特定的角度 关系,同时生长过程要求的动态过冷度也有差异,往往有一个 相在生长中起主导作用,决定了两相的分布,共晶体的形态也 具有独特性,这时常见的形态有针状、骨肋状、蜘蛛网状、螺 旋状等。
第三节 二元共晶相图
二、共晶体的形成
第三节 二元共晶相图
二、共晶体的形成
第三节 二元共晶相图
二、共晶体的形成
第三节 二元共晶相图
三、典型合金的凝固
1. 合金IV(成分在E点附近)
特点
1) 在液体中α和β同时具有析 出条件,都可以析出。
2) 由于α和β析出过程在成分 上可以互相补充和促进,共 同析出。 3) 凝固过程可以在恒温下进行 到结束。
第三节
一、相图形式
二元共晶相图
两组元在液态下无限互溶,固态下有限溶解,一组元溶入 另一组元中时都使凝固温度下降,并发生共晶转变。如Pb—Sn、 Ag—Cu等形成二元合金对应的相图就是二元匀晶相图。 相图的构成:tAE和tBE为两液相线, 与其对应的tAC和tBD为两固相线; CG和DH固溶体α、β的溶解度随温 度变化线;CED为水平共晶线。将 相图分成三个单相区 L、α、β; 三个双相区L+α、L+β、α+β 和 一个三相区L+α+β,即CED 为共晶线。
4) 最终得到两相交替的混合组 织。 结论:合金Ⅳ(成分在E点附近) L →α+β 转变发生在TE温度, 得到的两项交替分布的组织称为共晶体。
第三节 二元共晶相图
三、典型合金的凝固
第二节 二元匀晶相图与固溶体的凝固
