药讯2008年第四期
08医院药讯4

医院药讯☆☆☆☆☆☆☆☆☆☆☆☆☆☆☆☆☆☆☆☆☆☆☆☆☆☆☆☆☆☆☆☆☆☆☆☆☆☆☆【合理用药】把握降糖药使用“时间窗”治疗糖尿病药物可归纳为以下六大类。
磺脲类促胰岛素分泌剂目前常用的有格列苯脲(优降糖)、格列齐特(达美康)、格列吡嗪(唐贝克)、格列喹酮(糖适平)等,通过与胰岛β细胞膜上磺脲类药物受体结合,关闭ATP敏感钾通道,细胞内钾离子外流减少,细胞膜去极化,开放钙通道,细胞内钙离子增加,促进胰岛素释放。
口服0.5~1小时开始起作用,2~6小时作用最强。
该类药物应在餐前30分钟服,作用最强时间与进食后血糖升高时间相一致,从而起到有效的降糖作用。
非磺脲类促胰岛素分泌剂瑞格列耐(诺和龙)、那格列耐(唐力)等,该类药物也是作用于胰岛β细胞,刺激胰岛素分泌,但其作用机制不同于磺脲类。
这类药降糖作用快而短,主要用于控制餐后高血糖。
由于该药“快进快出”的特点,因此应进餐前即刻服用,不进餐不服药。
双胍类降血糖药二甲双胍可增加外周组织(如肌肉、脂肪)对葡萄糖的摄取和利用,通过抑制糖原异生和糖原分解,降低肝糖输出,从而控制餐后血糖。
此类药应在进餐时服用,或在进餐后立即服用,以减少药物对胃肠道的刺激。
α-糖苷酶抑制剂常用药物为阿卡波糖(拜唐苹、卡博平),通过抑制小肠黏膜上皮细胞表面的α葡萄糖苷酶(如麦芽糖、淀粉酶、蔗糖酶),来影响碳水化合物的吸收,从而降低餐后血糖。
其服药方法也比较特别,要与第一口饭同时嚼碎服用。
胰岛素增敏剂如文迪雅(罗格列酮),通过提高外周和肝脏的胰岛素敏感性而控制血糖水平。
可在空腹或进餐时服用。
胰岛素胰岛素是治疗糖尿病最有效、不良反应最小的治疗方法,有利于预防糖尿病的合并症。
胰岛素的类型不同,注射时间也不一样。
基因重组人胰岛素(诺和灵R、诺和灵30R),需在餐前30分钟皮下注射。
胰岛素类似物(诺和锐、诺和锐30),需在餐前15分钟内皮下注射。
要关注社区获得性肺炎病原菌耐药社区获得性肺炎(CAP)是临床常见疾病之一。
100种全球正在研发的新药 ( 2008年8月30)hz

100种全球正在研发的新药2008年8月30新药研发是一个耗资巨大的漫长过程。
目前,发达国家研究开发一个新分子实体药物,平均需要8亿美元,费时10年。
而一个新药一旦成功上市,年销售额可望达10亿美元以上。
因此,新药研发被视为企业增长的驱动力。
国家发改委医药工业信息中心站根据国外医药工业核心杂志上发表的最新资料,整理了100个全球主要在研药物,包括新分子实体药物62个、新生物药物29个、新制剂7个、新适应证用药2个。
这些药物是从数千个在研产品中精选出来的,拥有优于已上市产品的许多特点。
国家发改委医药工业信息中心站诚望国内制药企业能从中了解全球新药研发的最新方向,寻找到适合自己的研发模式,成功地推出新产品,在实现企业利润强劲增长的同时促进我国参与全球药品研发领域的竞争。
1. AGI-1067 82. ALFIMEPRASE 83. ALAGEBRIUM CHLORIDE(ALT-711)94. 阿尼芬净(ANIDULAFUNGIN)95. SORAFENIB(BAY-43-9006)116. BMS-488043 127. GLYMINOX GEL(C31G GEL)138. R-744(CERA)139. NXY-059(CEROVIVE)1310. CLOFARABINE 1411. COMBRETASTATIN A-4 PRODRUG 1612. 盐酸度洛西汀(DULOXETINE HYDROCHLORIDE,CYMBALTA)1713. 地西他滨(DECITABINE,DACOGEN) 1814. DALBAVANCIN 2015. 罗氟司特(ROFLUMILAST,DAXAS)2116. DEXANABINOL 2317. EDIFOLIGIDE SODIUM 2418. XIMELAGATRAN(EXANTA)2419. EXENATIDE 2520. FTY-720 2621. GCS-100LE(GCS-100) 2722. OBLIMERSEN SODIUM(GENASENSE) 2823. ICA-17043 2924. IDN-6556 2925. 伊罗夫文(IROFULVEN)2926. 哌立福新(PERIFOSINE,KRX-0401)3127. LAF-237 3228. LAX-101 3229. 奈拉滨(NELARABINE)3330. NS-2330 3431. 卢比替康(RUBITECAN,ORATHECIN)3432. 2-甲氧雌二醇(2-METHOXYESTRADIOL,PANZEM)3633. PHENSERINE 3634. PLD-118 3735. 普瑞巴林(PREGABALIN)3936. VATALANIB(PTK-787)4037. QAB-149 4138. DIFLOMOTECAN(R-1536) 4239. RAMELTEON 4340. 雷莫拉宁(RAMOPLANIN)4441. 雷诺嗪(RANOLAZINE,RANEXA)4542. 醋酸阿奈可他(ANECORTAVE ACETATE,RETAANE)4643. REVLIMID 4644. RIMONABANT 4845. 阿贝莫司钠(ABETIMUS SODIUM,RIQUENT)4946. ROTIGOTINE 5047. RSD-1235 5148. EFAPROXIRAL SODIUM(RSR-13)5149. 沙铂(SATRAPLATIN)5350. SCIO-469 5451. SPP-100 5552. SQUALAMINE 5553. BATABULIN SODIUM(T-67)5654. ERLOTINIB(TARCEVA)5855. TECADENOSON 5956. TLK-286(TELCYTA)5957. 二盐酸诺拉曲塞(NOLATREXED DIHYDROCHLORIDE,THYMITAQ)6158. 替拉那韦(TIPRANAVIR)63(2004年10月25勃林格殷格翰公司提交tipranavir(替拉那韦)新药)59. 替唑生坦(TEZOSENTAN,VELETRI)6460. VIRULIZIN 6461. 莫特沙芬钆(MOTEXAFIN GADOLINIUM,XCYTRIN)6662. 盐酸考尼伐坦(CONIVAPTAN HYDROCHLORIDE,YM-087) 68个例分析-新生物药物7063. PANITUMUMAB(ABX-EGF)7064. INGN-201(ADVEXIN)7065. AMB A1 LINKED MOLECULE(AIC) 7166. 那他珠单抗(NATALIZUMAB,ANTEGREN)7267. AXOKINE 7368. V-10153(BB-10153) 7469. 癌症疫苗(CANVAXIN)7470. CERTOLIZUMAB PEGOL(CDP870)7571. CTLA4-IG 7672. DX-88 7673. ECULIZUMAB 7774. ETC-216 7775. HSPE7-1ST GENERATION(HSPE7)7876. 人乳头状瘤病毒疫苗(HPV VACCINE) 7977. HUMAX-IL-15 7978. ISEGANAN HYDROCHLORIDE 8079. BELIMUMAB(LYMPHOSTAT-B)8080. 脑膜炎疫苗(MENACTRA)8181. NBI-3001 8282. NBI-6024 8283. 豹蛙酶(RANPIRNASE,ONCONASE) 8384. ONCOPHAGE 8385. OREGOVOMAB(OVAREX)8486. ALX1-11(PREOS)8587. PRO-542 8588. PROVENGE 8689. SPHERAMINE 8690. SA-IGIV(VERONATE)8791. 透明质酸酶(VITRASE)88个例分析-新制剂8992. 紫杉醇纳米制剂(ABRAXANE)8993. 阿托伐他汀+TORCETRAPIB (ATORVASTATIN+TORCETRAPIB)9094. 胰岛素纳米制剂(BASULIN)9095. 吸入型胰岛素(EXUBERA)9196. 长春新碱脂质体制剂(ONCO TCS VINCRISTINE)9197. 普拉睾酮(PRASTERONE,PRESTARA)9298. 聚谷氨酸紫杉醇(PACLITAXEL POLYGLUTAMATE,XYOTAX)93 个例分析-新适应证用药9599. 舒洛地昔(SULODEXIDE,KRX-101)95100. 米那普仑(MILNACIPRAN)95。
2008年第四季度药品监督检查抽验不合格情况公告
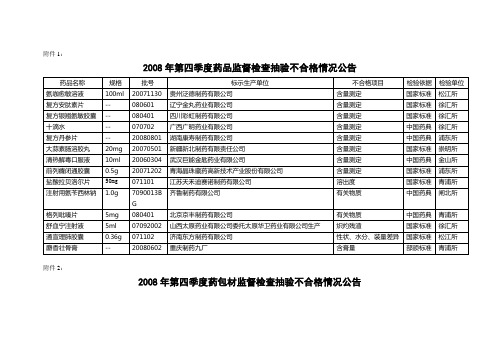
有关物质
中国药典
青浦所
舒血宁注射液
5ml
07092002
ห้องสมุดไป่ตู้山西太原药业有限公司委托太原华卫药业有限公司生产
炽灼残渣
国家标准
徐汇所
通宣理肺胶囊
0.36g
071102
济南东方制药有限公司
性状、水分、装量差异
国家标准
松江所
麝香壮骨膏
--
20080602
重庆制药九厂
含膏量
部颁标准
青浦所
附件2:
附件1:
2008年第四季度药品监督检查抽验不合格情况公告
药品名称
规格
批号
标示生产单位
不合格项目
检验依据
检验单位
氨咖愈敏溶液
100ml
20071130
贵州泛德制药有限公司
含量测定
国家标准
松江所
复方安肽素片
--
080601
辽宁金丸药业有限公司
含量测定
国家标准
徐汇所
复方银翘氨敏胶囊
--
080401
四川彩虹制药有限公司
2008年第四季度药包材监督检查抽验不合格情况公告
药包材产品名称
型号规格
批号或编号
标示生产单位
不合格项目
低硼硅玻璃安瓿
2ml
080606
通州兴扬药用玻璃制品有限公司
折断力、三氧化二硼的含量、121度颗粒法耐水性、内表面耐水性
口服液体药用聚丙烯瓶
500ml
20080601
浙江省海宁县毅峰药业包装有限公司
不挥发物
聚氯乙烯固体药用硬片
98mm
200807211
药品不良反应通讯(第17期)080423

药品不良反应监测通讯2008年4月关于在全国开展反兴奋剂集中宣传活动的通知食药监办[2008]65号各省、自治区、直辖市食品药品监督管理局(药品监督管理局):为了积极配合国家食品药品监督管理局、公安部等8部门开展的兴奋剂生产经营专项治理工作,从即日起至2008年10月底,在全国组织开展反兴奋剂集中宣传活动,并将4月24日至4月30日定为反兴奋剂宣传周。
现将有关事项通知如下:一、工作任务和目标在兴奋剂生产经营专项治理工作小组的组织协调下,积极开展兴奋剂专项治理的正面宣传,充分利用报刊、广播电视、网络媒体,大张旗鼓地宣传反兴奋剂的有关法规和工作部署,宣传合理使用反对滥用兴奋剂的科普知识,组织报道专项治理取得的成效,展示中国政府反兴奋剂的坚强决心和有力措施,做到家喻户晓,深入人心,营造一个全民参与、共同监督的舆论环境。
二、分阶段宣传重点按照兴奋剂生产经营专项治理工作的实施步骤,配合三个阶段的重点任务开展宣传活动。
(一)全面治理阶段的宣传(即日起——5月31日)组织力量集中精力办好反兴奋剂宣传周活动。
1.通过新闻发布会、新闻通气会等形式,组织媒体大张旗鼓地宣传8部门兴奋剂专项治理的部署,做好政策解读和专题访谈。
2.组织全国各零售药店张贴反兴奋剂宣传海报,北京及奥运协办城市零售药店要在店内明显位置摆放反兴奋剂宣传展板。
宣传海报和展板由国家局统一设计制作下发。
3.组织有关学会、协会等力量,进社区、学校等开展反兴奋剂科普宣传,发放张贴反兴奋剂科普资料。
国家局负责设计编印有关资料并向各地提供部分张贴画及宣传折页。
(二)重点督查阶段的宣传(6月1日——7月26日)1.根据各地对专项治理工作的全面检查,组织媒体报道各地取得的阶段性成果。
2.根据8部门对重大案件的查处情况,有重点地曝光一批典型案例,形成强大的舆论声势。
(三)巩固提高阶段的宣传(7月27日——10月底)1.组织相关媒体,深入各地采访,报道专项治理取得的成果。
08年上半年医院用药盘点

08年上半年医院用药盘点发布时间: 2008-12-25 14:10:001 国际抗生素非专利化促进我国市场增长2008年上半年,我国全身用抗感染类药物仍然领跑医院用药市场,市场份额远远高于排在第二位的抗肿瘤和免疫调节剂市场,独自站在医院用药市场的第一梯队。
由于基数大,全身用抗感染类药物在医院用药大类增长率中排名并不突出,但是通过比较亚类的增长贡献率可以看出,全身用抗细菌药增长贡献率仅略低于价格昂贵的抗肿瘤药物,位列增长贡献率榜单第一梯队。
从数据上看我国抗生素市场仍有很大的增长潜力。
与国内抗生素市场不同的是,国际抗生素市场增速正在放缓。
耐药菌感染正以惊人的速度增长,而抗感染药物研发线却接近干涸。
在过去的10年中,FDA 批准了10只新的抗感染药物,但其中只有两只具有创新的作用机制。
正在研发的抗感染药物有14只,但是与25年前每年有十几只抗感染药物处于研发阶段的鼎盛时期相比,已经下降了许多。
为此,2007年底美国专门出台《抗生素临床试验指导原则》,希望能帮助解决抗生素缺乏的问题。
全球抗感染药物市场正从品牌药向非专利药转变,利润受损严重。
与其他类药相比,在未来几年里抗生素医院市场价值的下降可能会较为突出。
2006年抗生素市场销售收入较2004年略微下降了1.8%,2007年比上年增长了6.5%左右,2008年将以5%~6%的速度增长,增速略有降低。
也有预测认为,抗生素市场将在2010年达到一个峰值。
正是由于国际市场抗感染药物从品牌药向非专利药的转变,对于以仿制药为主的我国抗生素市场无疑是一个契机,根据药监局2008年前九个月新药报批数据,在生产批文超过5个的热点报批药物中,抗生素批文占到其中的32%,远远高于其他类药物。
也从另一个角度说明,未来我国抗生素市场将相当活跃。
由于普通抗感染药物的耐药菌层出不穷,使得研发领域对普通抗感染药物已经失去兴趣,而似乎更钟情于如抗HIV-1、乙肝病毒及耐甲氧苯青霉素金黄色葡萄球菌(MRSA)药物,这些药物的市场非常稳定,也因此为大型医药企业和小型生物技术公司带来了开发新药的动力。
药讯(2008年第一期)

药讯2008年第1期一、药物相互作用二、合理用药三、不良反应中山市小榄人民医院药剂科二OO八年三月一、药物相互作用需警惕的药物间相互作用医师在给长期服药的慢性病患者处方其他药物时,应该特别注意可能产生药物相互作用的危险。
前不久,澳大利亚药物不良反应监测委员会告诫临床医师要谨慎处理下列三种配伍。
(AustralianAdverseDrugReactionsBulletin)1、长期服用格列本脲的糖尿病患者加服甲氧苄氨嘧啶/磺胺甲唑导致低血糖。
2例长期服用格列本脲的糖尿病患者因细菌感染而服用甲氧苄氨嘧啶/磺胺甲唑,结果导致低血糖发生。
1例患者以前在服用格列本脲期间曾同时服用过甲氧苄氨嘧啶,但没有不良反应发生。
磺脲类药物通过肝脏中的CYP2C9代谢,磺胺类药物竞争性地抑制了CYP2C9活性,导致磺脲类药物作用增强,产生低血糖。
此外,大剂量磺胺类药物单独使用也可以引起低血糖发生,但比较少见。
2、长期服用地高辛者加服甲基红霉素可增加地高辛毒性。
1例75岁女性患者服用地高辛(250μg/d)长达4年之久,在加服甲基红霉素(250mg,2/d)后的第3天,出现地高辛毒性反应。
地高辛剂量减半并停用甲基红霉素,8天后出院。
地高辛生物利用度大约为70%,因为肠壁中P-糖蛋白可使地高辛返回肠腔,从而减少药物的吸收。
甲基红霉素和其他大环内酯抗生素可抑制P-糖蛋白泵的作用,使地高辛吸收增加。
3、长期服用ACEI加服保钾利尿剂可导致高血钾。
长期服用ACEI治疗的3例患者在加服螺内酯后出现高钾血症2例伴有肾衰,1例血钾升高至8.4mmol/L。
3例患者在撤服两药并接受降血钾治疗后完全恢复。
高血钾症通常发生在ACEI单独服用时,加服保钾利尿剂如螺内酯或阿米洛利,可通过影响肾脏钾的排泄而使这种效应加剧。
专家告诫,除了药物不合理配伍所致相互作用产生的直接严重后果外,有时也可能出现未能正确地识别药物相互作用而将患者长期服用的药物被不必要地停止。
2008“药”闻回顾

察
从C 1 i n
i
c a
l Tr i
a
]S
.
.
g
o v
上 注 册 的 由企 业 资助 的临 床 试 验 数 量 来
。
看
,
肿瘤 已 跃 居 榜 首
—
,
成 为药物 研 发 最 为集 中 的 治 疗 领域
—
在 曾经
最 受关 注 的核 心 领 域 大 幅减 少
心 血 管 疾病
,
,
制药 企 业 却 持续 削减 或 停 止
e
曾经 最 受 关 注 的 核 心 领 域
心 血 管疾 病
,
制药 企 业
,
除 了西 妥 昔 单 抗 ( c
t
u x
i
ma
b
,
却 持续 削 减 或 停 止 了该 领 域 的药 物 研 发 投 入
由企 业
)
,
礼 来 还 获 得 了 3 种 处 于 I I 期或 II I 期 临床 试
。
资助 的 心 脏 病 临床 试 验 的数 量 也 大 幅 减 少
Imc l o
n e
员 削减 开 支
,
些 大型 公 司 则通 过 收购其它 公司来
,
妥昔单抗 ( c
研 药物
。
e
t
u x
im a b
,
e r
b it
u x
公 司 的 靶 向抗 肿 瘤 在
扩 大其业 务领 域
或 者增加 在特 殊 治疗 领 域 的药 物
。
研 发投入 ( 见表 1 )
例如
,
武 田 公司 ( Ta
b
,
Av
2008年医药行业十宗最

2008年医药行业:药品十宗最来源:医药经济报上榜产品最“牛气”:阿托伐他汀最受关注:必存(依达拉奉注射液)最坚强:左氧氟沙星最民族:复方丹参滴丸最老牌:银杏叶制剂最新潮:爱普列特最具成长性:艾素(多西他赛)最具潜力:丹红注射液最具人气:马应龙痔疮膏最时尚:润洁最“牛气”:阿托伐他汀主持人:小小的药片,居然创造出100亿美元的价值,辉瑞的阿托伐他汀真牛!在市场上,这只药片有一个悦耳的名字——立普妥(Lipitor)。
在上市11年的销售中,已经成为世界有史以来销量最大的药品。
身为辉瑞公司安阿伯实验室化学部副总经理的布鲁斯·罗斯做梦都没有想到,其22年前发明的一种降胆固醇药物阿托伐他汀,自2002年以来,一直成为降胆固醇药市场的“顶梁柱”;2004年后,每年都为辉瑞带来100多亿美元的收益。
立普妥是目前全球处方量最多的降胆固醇药物,现由辉瑞公司拥有。
自1997年在全球上市以来,销售额节节攀升。
2002年销售额达到79.72亿美元,成为全球最畅销药物,2004年销售额突破100亿美元大关而独领风骚。
尽管近几年增幅有所放缓,但2007年全球销售额仍有126.75亿美元,同比仅轻微下降了1.64%。
立普妥片剂于1999年9月30日在中国获得药品行政保护(2007年3月30日到期),2000年片剂获准进口。
北京嘉林药业的阿托伐他汀钙片(商品名:阿乐)抢在立普妥片剂获得行政保护前取得生产批文。
2005年,阿托伐他汀钙胶囊剂获准生产,现仅有河南天方药业一家有生产文号(商品名:尤佳)。
在国内,2007年立普妥占据了阿托伐他汀75%左右的市场份额,优势明显。
但近两年,阿乐和尤佳的销售额一直保持增长的势头,逐渐蚕食立普妥的市场。
最受关注:必存(依达拉奉注射液)主持人:谈到必存,不得不提它的主人先声药业,这个诞生才13年的民营制药企业对新药研发甚有眼光。
为了占据在药品市场的制高点,从2000年起,先声就把每年销售额的5%投入到研发中去,远远高于国内同行业的新药研发投入。
药物警戒快讯27

药物警戒快讯2008年10月16日第10期(总第59期)内容提要美国发布药品潜在安全性问题季度报告澳大利亚警告高剂量维生素B6导致周围神经病变澳大利亚发布Vytorin与致癌风险的信息美国加强肿瘤坏死因子抑制剂导致真菌感染的警告美国通报利妥昔单抗治疗类风湿关节炎导致PML病例美国警告纳曲酮引起的注射部位不良反应国家药品不良反应监测中心国家食品药品监督管理局药品评价中心美国发布药品潜在安全性问题季度报告2008年9月5日,美国食品药品监督管理局(FDA)在其网站上发布了首份药品潜在安全性问题季度报告。
报告中列出了一些正在进行评估的具有安全性问题的药品及其潜在风险。
根据美国2007年9月27日颁布的《食品药品管理法修正案》,FDA将对其不良事件报告系统(AERS)进行审查,每个季度向公众告知新的药品安全信息或严重风险的潜在信号。
AERS中包括了由制药商、医务人员和患者提交给FDA的数百万份不良事件报告,FDA审查人员将根据不良事件的严重程度或报告数量来决定是否需要对某个药品进行评估。
根据AERS的审查结果,FDA将于每个季度在其网站发布报告,列出通过AERS发现的具有新的安全信息或严重风险潜在信号的药品。
每季度报告不会重复累积,只会列出上个季度发现的有问题的药品。
药品列于季度报告中并非意味着FDA已经确定这些药品具有所述的风险或与这些风险存在因果关系。
如果FDA在深入评价后认为药品和风险确实存在因果关系,将可能采取相关措施,包括修改说明书、制定“药品评估和风险最小化战略”(REMS)或进一步收集信息来确定风险的特征。
将药品列入季度报告中也不意味着FDA建议处方医师停止处方这些药品或患者停用这些药品。
患者如果有问题,应向处方医师咨询。
FDA将完成每个药品的评估工作,并在适当的时候发布信息。
首份季度报告(2008年1-3月)列有20种药品以及其潜在安全性问题,如下表所示。
(FDA网站)澳大利亚警告高剂量维生素B6导致周围神经病变澳大利亚《药物不良反应公告》2008年8月27卷4期中警告:高剂量的维生素B6可能导致周围神经病变。
2008年至2009年年底国内申报的一类新药

1.1 1.1 1.1 1.1 1.1 1.2 1.2 1.5 1.5 1.5 1.1 1.1 1.1 1.1 1.1 1.1 1.1
天津药物研究院 安徽环球药业股份有限公司 安徽环球药业股份有限公司 江苏恒瑞医药股份有限公司 江苏恒瑞医药股份有限公司 湖南迪诺制药有限公司 湖南迪诺制药有限公司 贵州同济堂制药有限公司 沈阳红旗制药有限公司 沈阳红旗制药有限公司 大连天宇制药有限公司 中国科学院上海药物研究所 江苏正大天晴药业股份有限公司 广东中科药物研究有限公司 浙江医药股份有限公司新昌制药厂 浙江医药股份有限公司新昌制药厂 甘肃玉璞肿瘤心血管病研究所
1.1 1.1 1.6 1.1 1.2 1.2 1.1 1.1 1.5 1.1 1.1 1.1 1.1 1.1 1.1 1.1 1.1
江苏豪森药业股份有限公司 江苏豪森药业股份有限公司 中国人民解放军第二军医大学 福建金山生物制药股份有限公司 浙江海正药业股份有限公司 浙江海正药业股份有限公司 江苏豪森药业股份有限公司 江苏豪森药业股份有限公司 安徽永生堂药业有限责任公司 江苏恒瑞医药股份有限公司 和记黄埔医药(上海)有限公司 和记黄埔医药(上海)有限公司 和记黄埔医药(上海)有限公司 浙江海力生制药有限公司 浙江海力生制药有限公司 浙江海力生制药有限公司 天津药物研究院
65 66 67 68 69 70 71 72 73 74 75 76 77 78 79 80 81
CXHL0800490 硝酸铵 CXHL0800482 伪人参皂苷GQ注射液 CXHL0800481 伪人参皂苷GQ CXHL0800462 绿原酸 CXHL0800461 注射用绿原酸 CXHL0800414 米非司酮片 CXHL0800407 注射用盐酸吡柔比星 CXHL0800406 注射用盐酸吡柔比星 CXHL0800399 甲苯磺酸艾力替尼圆形片 CXHL0800398 甲苯磺酸艾力替尼异形片 CXHL0800397 甲苯磺酸艾力替尼 CXHL0800387 注射用康普瑞丁磷酸二钠 CXHL0800386 注射用河豚毒素 CXHL0800385 河豚毒素 CXHL0800384 康普瑞丁磷酸二钠 CXHL0800371 (5R)-5-羟基雷公藤内酯醇片 CXHL0800370 (5R)-5-羟基雷公藤内酯醇片
2008年二季度通报

2008年第二季度合理用药通报2008年7月2日~7月6日,院纪委、医务科、临床办、药剂科、信息中心联合对部分临床科室及医生的不合理用药病历进行抽查并分析评估,现将结果通报如下:一、2008年第二季度药品销售金额前30位药品排名通报二、2008年第二季度抽查临床科室药占比及异常用药通报三、2008年第二季度部分医生用药情况通报四、2008年第二季度医师典型不合理用药病历分析通报2008.7.7 一、2008年第二季度药品销售金额前30位药品排名二、2008年第一季度抽查临床科室药占比超标及抗菌药物异常用药通报2009年二季度药占比超标严重的科室有心胸外科42.1%(标准40%);神经外科46.5%(标准42%);神经内科44.6%(标准41%);泌尿外科42.1%(标准40%)。
心胸外科和泌尿外科主要是抗菌药物使用异常;神经外科和神经内科主要是脑血管保护剂价格较贵、使用频率较高导致药占比居高不下。
三、2009年第二季度部分医生用药情况通报四、2008年第一季度医师典型不合理用药病历分析通报1. 心胸外科666157 06床60aT 37.2℃P 90 R30 W10kg床位医生:戴君诊断:甲状腺瘤并甲亢,为多发性小息肉。
3.9甲状腺手术盐水+头孢呋辛1.50g QD 4.10-4.14分析:1、乳腺手术为1类切口,如无必要围手术期可不使用抗菌药。
2、围手术期应用头孢呋辛时机不对,应为术前30‘,且应用时间过长。
2. 心胸外科666157 06床42岁T 37.2℃P 90 R30 W10kg,左侧乳腺肿块,乳腺疼痛,乳头溢液、糜烂,左腋窝淋巴结肿大。
诊断:良性纤维瘤床位医生:雷鹏飞手术:左侧乳腺部分切除术盐水+头孢呋辛3.0g QD 3.10-3.14分析:1围手术期应用头孢呋辛应用时间过长。
2、应用头孢呋辛单次剂量过大,超过说明书剂量3、泌尿科方西来女48岁466157 19床反复尿频尿急诊断:膀胱黏膜白斑手术:5.6膀胱黏膜白斑电灼术盐水+加替沙星0.3 g 术前用 5.6术后:盐水+头孢呋辛3.0g QD 5.9-5.13分析:1围手术期选加替沙星预防感染不合理。
2008-4 药源性肝损伤的研究概述

[接受日期] 2008204214[基金项目] 中医药行业科研专项(No.200707008)3通讯作者: 张陆勇,教授;研究方向: 药理学;Tel:025*********; E2ma il:lyzhang@药源性肝损伤的研究概述黄精俸, 江振洲, 王 涛, 姚金成, 张陆勇3(中国药科大学新药筛选中心,江苏南京210038)[摘 要] 随着各种新药的广泛应用以及联合用药的增多,药源性肝损伤的发生率明显增高,按其发病机制可分为药物及其活性代谢物直接造成的可预测的肝损伤及药物特异质反应所致的不可预测的肝损伤两大类。
综述近年来对药源性肝损伤的发病机制的研究进展,为预防药源性肝损伤提供思路。
[关键词] 药源性肝损伤;肝毒性;线粒体;天然性免疫;适应性免疫[中图分类号] R969 [文献标识码] A [文章编号]1001-5094(2008)08-0357-06Overvie w of Research on D rug2induced L iver I njury HUANG J ing2feng, J I A NG Zhen2zhou, WANG Tao, Y AO J in2cheng, Z HANG Lu2yong (Center for D rug S creening,China Pha r m aceutical U niversity,N anjing210038,China)[Abstract] A l ong with the app licati on of ne w drugs and drug combinati on,the incidence of drug2 induced liver injury(D I L I)has increased in recent years.According t o pathogenesy,it can be divided int o t w o kinds of D I L I:injury caused directly by p redictable drugs as well as their reactive metabolites and that caused by unp redictable drug idi osyncratic reacti ons.This paper p r ovides the overvie w of research p r ogresses on the pathogenesy of D I L I,and thus gives thoughts on the p redicti on and p reventi on of D I L I. [Key words] D rug2induced liver injury;Hepat ot oxicity;M it ochondri on;I nnate i m munity; Adap tive i m munity 随着各种新药的广泛应用以及联合用药的增多,药源性肝损伤(drug2induced liver injury,D I L I)已成为医疗卫生工作者、制药工业和药品管理部门共同面对的重要问题。
何谓兴奋剂2008年禁用的兴奋剂有哪几类

何谓兴奋剂兴奋剂在英文中称之为doping。
据称,该词来源于“dope”,指最早由南非人在某些仪式上使用的一种原始的含酒精的饮料,用作兴奋剂。
一般将dope解释为赛马、跑狗、运动员等非法服用的兴奋剂,也有解释为使人感觉愉快或成瘾的药物。
20世纪60年代,国际上将运动员为提高成绩而非法使用的物质和方法统称为doping(兴奋剂)。
需要指出的是,兴奋剂不等同于兴奋药。
兴奋药又称为刺激剂,英文为stimulants,通常指有兴奋作用的药物,如苯丙胺、麻黄素、士的宁等。
而兴奋剂除有兴奋药(刺激剂)外,还包括有其他作用的物质,如蛋白同化制剂、利尿剂等。
虽然近年运动员禁用物质种类日益增多,但兴奋剂(doping)一词沿用至今。
兴奋剂禁用于运动员,世界反兴奋剂机构定期发布禁用目录,规定运动员禁用的物质和方法。
为充分理解doping一词的含义,现将1999年国际奥委会对该词的定义抄录如下,供参考:“doping is defined as the use of an artifice, whether substance or method, potentially dangerous to athletes’ health and/or capable of enhancing their performance。
”2008年禁用的兴奋剂有哪几类世界反兴奋剂机构(world Anti-Doping Agency, WADA)发布的2008年兴奋剂禁用目录包含禁用物质和禁用方法2部分。
禁用物质有9类,其中前5类为赛内和赛外禁用物质,后4类为赛内禁用物质;禁用方法有3类。
现将禁用物质介绍如下。
1蛋白同化制剂(1)蛋白同化雄性激素类固醇a外源性蛋白同化雄性激素类固醇:达那唑、孕三烯酮、甲睾酮及诺龙等46种b内源性蛋白同化雄性激素类固醇:雄(甾)烯二醇、雄(甾)烯三酮、双氢睾酮、普拉睾酮以及17种代谢产物和异构体。
(2)其他蛋白同化制剂克伦特罗、替勃龙、选择性雄激素受体调节剂、泽仑塔及齐帕特罗。
临床药讯2008年第4

临床药讯2008年第(4)期●药品常识讲座药品不良反应知识(4)●行业信息通报药监局关于“协和降糖胶囊”为假药的通告●药品不良反应通报关注皂酸双酯钠的严重不良反应★药品常识讲座药品不良反应知识(4)药品不良反应监测3、医院集中监测:一定的范围内对某一医院或某一地区内所发生的ADR及药物利用详细记录,以探讨ADR的发生规律。
优点:资料详尽、数据准确可靠。
缺点:数据样本偏小,数据代表性差、缺乏连续性,且费用高。
4、病例对照研究:是通过调查一组发生了某种ADR的人群和一组未发生ADR的人群,了解过去有无使用某一可疑药物的历史,然后比较两组暴露于该药物的百分比,以验证该药物与这种ADE间的因果关系。
5、队列研究:将人群按是否使用某药物分为暴露和非暴露组,然后对两组人群都同样地追踪随访一定时期,观察在这一时期两组ADE的发生率,从而验证因果关系的假设。
6、自动记录数据库在药物不良反应监测中的应用对于一些潜在的发生率较低的ADR已难以从小样本人群观察到。
故药物与ADR的因果假设的检验常依靠大型的记录数据库,借助记录联结技术,把病人分散的诊断、用药】剂量、不良反应及其他信息通过病人唯一的确定号码联结起来,进而开展各种形式的流行病学研究,已发现与药物有关的不良事件。
从而高效率地获取ADR监测所需的数据。
(完)★行业信息通报北京市药监局关于“协和降糖胶囊”为假药的通告协和降糖胶囊曾在多家电视台进行广告宣传,目前已被定性为假药,北京市药监局发出通告,提醒公众切勿购买服用。
经检验,这种宣称可以取代胰岛素的神奇中成药,只是添加西药成分的假药。
目前各种媒体在广告中不断进行所谓的一些中成药的宣传,往往打着“协和”、“同仁”等字样,来吸引患者的眼球,并且在某些连锁药店设立专柜进行促销,或通过社区所谓健康教育讲座进行非法销售,使许多老年患者上当受骗,希望群众对这类药进行举报,一般情况这些中成药并非药品,而是保健食品,并且非法添加西药成分来保证有某些疗效,价格不菲,但安全性无法保证。
2008,中国药品安全事件回顾

2008,中国药品安全事件回顾综述:2008年的中国食品药品安全监管领域,充满了警示和反思。
即将过去的一年中,我国在汶川地震灾后救援和北京奥运会成功的食品药品安全保障令人难忘,问题奶粉、刺五加注射剂等严重不良事件的警钟更响彻全国。
伴随着国家食品安全立法、建立基本药品制度等改革步伐的加快,让我们共同期待吃药更安全、餐桌更绿色。
1.甲氨蝶呤注射液事件“结案”,60年名厂被“摘牌”4月11日,国家食品药品监督管理局发布信息,注销上海医药(集团)有限公司华联制药厂甲氨蝶呤注射液的药品批准文号,依法吊销药品生产许可证,这起严重药物损害事件正式“结案”。
去年7月,由于现场操作人员将硫酸长春新碱尾液混于注射用甲氨蝶呤、盐酸阿糖胞苷等批号药品中,导致多个批次的药品被硫酸长春新碱污染,造成这起重大的药品生产质量责任事故。
事故不仅导致广西、上海部分医院的白血病患儿出现下肢疼痛、乏力、行走困难等不良反应症状,也使上海华联这家拥有60多年历史的知名药厂被最终“摘牌”。
点评:一批名企、老厂的“落马”固然令人痛心,但是更让人体会到我国严格药品安全监管的决心和勇气。
相关人员隐瞒违规生产的事实,折射出药品生产企业社会责任的缺失。
要切实保障食品药品安全,光靠企业自律还远远不够,需要更刚性的综合手段促使企业把安全责任真正落到实处。
2.江西博雅问题免疫球蛋白注射液致人死亡江西省食品药品监督管理局新闻办公室6月1日向媒体通报,江西省食品药品监督管理局5月28日接到报告,5月22日至28日,先后有6名在南昌大学第二附属医院就诊的患者,在使用标示为江西博雅生物制药公司生产的批号为20070514、规格为5%2.5g的静脉注射用人免疫球蛋白(PH4)(液体)发生死亡。
”3. 完达山药业刺五加注射液致人死亡10月,云南省红河州6名患者使用了完达山药业公司生产的刺五加注射液出现严重不良反应,其中3例死亡。
调查发现这是一起由药品污染引起的严重不良事件。
药事信息

医院药学通讯2008. Sep. V ol. 4 No.3 ·药事信息·2008年7月30日“药品和治疗品管理委员会”会议纪要一、关于增补药剂科马珂主任为药事委员会常任委员:会议同意增补马珂主任为药事委员会常任委员。
二、治疗性材料讨论:共有31个治疗性材料临床申请使用。
会议通过下列5个产品:1.先天性心脏病伞片封堵系统心内科2.普理灵疝修补装置PHS 普外科3.百多力起搏器心内科4.DIAG可调控冠状窦电极导管心内科5.颈动脉保护伞普外科其余26个产品暂缓,如本院有同类产品的,要求科室提出具体价格或产品性能上的优势。
无同类产品的,要求提供更为详细的产品说明材料,下次会议讨论。
三、邵医党委(2008)4号文件《关于加强医院药品监督管理的实施办法》黄东胜副书记详细解释该文件实施细则,要求参加会议的各科代表将文件主要内容带回科室传达并落实。
四、浙江省医疗机构药事管理专项检查结果反馈:反馈内容主要包括三方面:抗生素管理、处方管理办法执行情况、精麻药品管理。
药剂科将负责协调相关科室对需要改进的环节采取措施。
其中麻醉科麻醉药品的存放问题,由钟泰迪主任负责改进,确保麻醉药品贮存的安全性。
五、关于“头孢菌素类抗生素的过敏试验”原则讨论:会议讨论并原则上通过《医院内注射用β-内酰胺类抗生素皮试原则》,将由药剂科下发相关科室执行。
(见附件4)六、2008年1-6月全院药品/抗生素消耗数量/金额排序:会议回顾了1-6月全院用药情况,并作出如下决定:1.“头孢替安针1g”、“头孢米诺针(进口)”增幅分别为62.11%、51.75%。
会议决定限量使用。
(限量比例为异常波动前3-6个月平均使用量的60%以下),并口头警告。
1医院药学通讯2008. Sep. V ol. 4 No.32.“潘托拉唑针(进口)”增幅为86.77%。
会议决定限量使用。
(限量比例为原基础用药量的50%,并提出口头警告。
同时要求药剂科分析该药使用科室及医生分布情况。
2008 年我国新药研发现状

2008年新药研发2008年药品注册情况通报药品注册,是国家食品药品监督管理局根据药品注册申请人的申请,依照法定程序,对拟上市销售药品的安全性、有效性、质量可控性等进行审查,并决定是否同意其申请的审批过程。
其根本目的是通过科学评价保证上市药品安全有效,保障和促进公众健康。
在药品研制、生产、流通、使用一系列环节中,药品注册管理处于药品监管的起始阶段,是从源头上对药品安全性和有效性进行评估和实施监管的重要手段。
改革开放30年来,我国药品注册管理的模式从分散审批到集中审批,从审评审批一体化到受理、审评、审批三分离,药品注册工作在改革与发展中不断完善。
特别是2007年修订施行的《药品注册管理办法》,以科学监管理念为指导,通过整合药品注册管理资源,深化注册审评机制改革,严格注册审批程序,强化药品的安全性,实现对药品注册全过程的监督管理,逐步建立起统一高效、运行顺畅的药品注册管理体系。
去年是新修订的《药品注册管理办法》实施的第一年,为贯彻执行新办法,将立法精神和要求真正落到实处,我们又相继出台了《中药注册管理补充规定》、《药品注册现场核查管理规定》、《新药注册特殊审批管理规定》等一系列的配套文件以及几个药品研究技术指导原则。
总之,从法制、机制和技术方面规范和完善了药品注册管理工作。
一、药品注册批准情况2008年,我局共受理药品注册申请3413件,与06年和07年同期相比分别下降75%和18%,主要是由于仿制药申请和简单改剂型等申请数量的大幅度下降所致,(其中仿制药申请分别同比下降了85%和46%),这在一定程度上反映出注册申报数量开始趋于正常,注册申请人更加趋于理性,药品研发秩序逐步好转。
2008年,我局共批准新药临床申请434件,其中有52种属于新化合物;批准新药生产申请165件,涉及119种药品,其中包括1类新药5个;批准仿制药生产申请1502件,涉及614种药品;批准药品进口申请99件,涉及83种药品。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
药讯2008年第4期(抗菌素合理使用专辑)第一部分:合理使用抗生素问题的提出第二部分合理使用抗生素中山市小榄人民医院药剂科二O O八年十二月第一部分:合理使用抗生素问题的提出因为原来来源于微生物的抗生素现在大都来源于人工合成或半合成,因此国内外都有学者主张―凡是抑制细菌生长繁殖或杀灭细菌的药物都可称之为抗生素或抗菌药‖。
比如不列颠百科辞典就把喹诺酮类列为抗生素(a n t i b i o t i c s)。
但早期抗菌药磺胺类一般按习惯仍称为抗菌药,而不称抗生素。
1928年,英国细菌学家弗莱明发明青霉素,1940年用于临床,开创了感染性疾病治疗的新纪元。
几十年来,青霉素挽救了数以千百万计的生命,使人类平均寿命从40岁提高到了65岁。
然而仅仅60年间,很多细菌就对抗生素已产生了严重的耐药,有的甚至产生了多重耐药。
例如,耐青霉素的肺炎链球菌,过去对青霉素、红霉素、磺胺等药品都很敏感,现在几乎―刀枪不入‖;绿脓杆菌对阿莫西林、西力欣等8种抗生素的耐药性达100%;多重耐药菌引起的感染更是对人类健康造成了严重的威胁。
20世纪50年代在欧美首先发生了耐甲氧西林金黄色葡萄球菌的感染,这种感染很快席卷全球,有5000万人被感染,50多万人死亡。
耐药菌的出现是人类不合理使用抗生素的直接后果,并且细菌产生耐药性的速度远远快于人类新药开发的速度,如不遏止,人类将进入―后抗生素时代‖,也即回到抗生素发现之前的人们面对细菌性感染束手无策的黑暗时代!为何细菌对抗生素的耐药如此严重?美国哈佛大学的研究人员针对46477份儿童病历的一项调查表明,当前抗生素使用的频繁度极高,平均每个儿童一年间接受3次抗生素处方,其中有一半的抗生素是用于处理中耳炎等问题的正常使用,而有12%是用在感冒、上呼吸道感染、气管炎等并不需要使用抗生素的感染治疗。
在美国,医生每天的抗菌药物处方中有50%是不必要的。
美国在1982年~1992年间死于传染性疾病的人数上升了40%,死于败血症者上升了89%,其主要原因是耐药菌带来的治疗困难,仅1992年全美就有13300名患者死于抗生素耐药性细菌感染。
法国每年大约有900万~1000万人次罹患咽炎,其中90%的人在患病期间服用抗生素,而实际上,只有约22.2%的咽炎属于细菌感染,其他均为病毒感染,服用抗生素根本没有任何作用。
此外,医生也常对鼻炎、支气管炎等多为病毒感染的疾病错用抗生素治疗。
中国是世界上滥用抗生素最为严重的国家之一,W H O在国际范围内的多中心调查显示,住院患者抗菌药物使用约30%,而我国住院患者中使用抗生素的占80%~90%,其中使用广谱抗生素或联合使用两种以上抗生素的占58%,就连门诊感冒患者都有75%应用抗生素,大大超过了已经很不正常的国际平均水平。
根据对全国14家综合性医院的专项调查显示,在最常用的15种药物中,10种是抗生素,住院患者50%左右的费用是用在抗生素上。
在相当一部分的医生处方单上,患者的疾病不论是细菌性感染还是病毒性感染,或者是发热,都千篇一律地使用抗生素,使患者的耐药性大为增加。
而且,使用的抗生素也越来越高级,形成一个恶性循环,这种抗生素滥用造成我国的细菌耐药性问题尤为突出:我国临床分离的一些细菌对某些药物的耐药性已居世界首位。
除了上面提到的耐青霉素的肺炎链球菌、耐甲氧西林的金黄色葡萄球菌、肠球菌、真菌等多种耐药菌外,喹诺酮类抗生素进入我国仅20多年,可其耐药率已经达60%~70%。
上海人群感染的金黄色葡萄球菌中,80%已经产生了对青霉素G的耐药性。
凯福隆、头孢三嗪等第三代的头孢类菌抗生素的应用已日趋普遍,抗生素品种的选用明显超前。
造成我国抗生素滥用的原因:一是医疗卫生系统对医务人员如何正确使用抗生素缺乏行政与法律的界定。
这导致医院不重视病原学检查,抗生素药敏试验过少;抗生素适应症掌握不严,选用广谱抗菌药物偏多,联合用药过多,预防性用药时间过长;不了解抗生素药物代谢动力学特点,在给药剂量、途径、间隔时间上存在不规范操作。
二是抗生素在畜牧、养殖业中的大量使用,导致在环境中大量的抗生素释放和耐药细菌的驯化与进化。
滥用抗生素导致的另一严重恶果是院内感染率已高达40%左右。
如院内获得性肺炎在滥用抗生素48小时后就会出现,这在老年护理院、康复院内尤为突出。
如果是免疫力低下的患者,会直接导致死亡。
中国、世界;各国人民、政府……对于―不合理使用、甚至泛用抗生素,以及由此造成的严重恶果‖这一背景已经到了不能再充耳不闻、视而不见的时候了!我国政府为制止滥用抗生素采取的措施:2004年7月1日起,抗生素再次被明确规定为处方用药;国家食品药品监督管理局(S F D A)下发的《关于开展抗菌药物合理使用的宣传活动的通知》,就是为了加强专业医务人员合理使用抗生素的素质,也促使普通民众和患者建立合理使用抗生素的意识。
中华医学会、中华医院管理学会药事管理专业委员会、中国药学会医院药学专业委员会在其联合制定、发布的―抗菌药物临床应用指导原则‖前言中指出:―抗菌药物的不合理应用表现在诸多方面:无指征的预防用药,无指征的治疗用药,抗菌药物品种、剂量的选择错误,给药途径、给药次数及疗程不合理等。
为提高细菌性感染的抗菌治疗水平,保障患者用药安全及减少细菌耐药性,特制订《抗菌药物临床应用指导原则》‖(附后)卫生部正在起草《合理使用抗生素指南》,不久将会出台。
这将是我国政府首次使用行政手段指导和控制医生对某类药品的使用,也是我国首次为某一类药品制订使用指南;第二部分合理使用抗生素合理使用抗生素的原则确认抗生素药效,―对症‖选用抗生素;经验治疗与药敏检查相结合,结合患者全身情况选用适宜抗生素,尽早实现目标用药;了解药代动力学和药效学制定合理用药方案;针对患者特殊病理情况谨慎用药,密切监察/及时处理抗生素的不良反应。
针对患者特殊病理情况谨慎用药,密切监察/及时处理抗生素的不良反应。
一确认抗生素药效对症选用抗生素(一)ß内酰胺类1、青霉素类*青霉素对葡萄球菌以外的G r+球菌和奈瑟菌属感染,应为首选药!*苯唑西林、氯唑西林、氟氯西林、双氯西林等耐酶青霉素对ß-内酰胺酶稳定,主要用于产酶葡萄球菌所致各种感染;*以氨苄西林和阿莫西林为代表的氨基青霉素,对G r+菌效果不如青霉素,但对流感杆菌、肠球菌及部分肠杆菌有抗菌作用。
2、头孢菌素类第一代头孢菌素对耐青霉素葡萄球菌、其它G r+菌、大肠杆菌、奇异变形杆菌、伤寒杆菌、痢疾杆菌、流感杆菌等有交叉抗菌活力:其中头孢氨苄、头孢羟氨苄、头孢拉啶等口服品种,适用于各种轻-中度感染;而注射用药血药浓度较高,对敏感菌重度感染有效;第二代头孢菌素对G r+菌的活性与一代头孢比较相近或稍差,而对G r-菌的活性作用则增强,但对部分肠杆菌耐药。
用于G r+和G r–菌敏感的各种感染。
常用品种有:头孢呋辛/克洛/孟多/替安等。
前两者的片剂是口服代表品种。
第三代头孢菌素对ß-内酰胺酶更稳定,抗菌谱更广泛,对肠杆菌科细菌、奈瑟氏菌、流感杆菌、肺炎球菌、溶血性链球菌、部分厌氧菌有强大抗菌活力。
但对葡萄球菌的作用较一代和二代头孢菌素差。
第三代头孢菌素注射后,血药浓度高、脑脊液中能达到有效血药浓度、对肝/肾毒性较低,为其三个特点,故适用于:严重G r–及敏感G r+菌感染、病因不明感染的经验治疗、以及院内感染。
常用品种:头孢噻肟/凯福隆、头孢曲松/菌必治(半衰期达8h可q d用药)、头孢哌酮/先锋必(抗铜绿假单孢菌)、头孢他啶/复达欣(抗铜绿假单孢菌活力最强);其口服品种有头孢特仓酯、头孢克肟、头孢泊肟酯等。
第四代头孢菌素同三代头孢菌素比较:对ß内酰胺酶更稳定,抗菌谱进一步扩大,其中:头孢匹美/马斯平---用于G r+/-菌感染,如金葡菌、链球菌、铜绿假单孢菌、克雷伯菌及流感嗜血杆菌引起的肺炎、菌血症及败血症。
头孢匹罗---用于耐药的金葡菌/铜绿假单孢菌/肠杆菌/柠檬酸菌感染。
头孢立定---对铜绿假单孢菌有特效,是头孢哌酮抗菌活力的32倍。
3、其他ß内酰胺类1)头酶素对ß-内酰胺酶稳定,抗菌谱与二代头孢相近,对肠杆菌作用强,对厌氧菌包括脆弱类杆菌也有良好活性。
主要品种有:头孢西丁/美唑/替坦/拉腙等。
适用于:厌氧菌或厌氧菌与需氧菌混合感染,如腹腔感染、盆腔感染、肺脓肿等。
2)单环ß-内酰胺类对多种ß-内酰胺酶稳定,对G r–菌作用强,对G r+菌及厌氧菌作用差,属窄谱抗菌素!以安曲南为代表。
适应证:G r–菌感染或三代头孢无效的G r–菌感染。
3)碳青霉素类抗菌谱极广,对对G r-菌、G r+需氧菌和厌氧菌有强大活性,对ß-内酰胺酶稳定。
代表品种为亚安培南/泰能,美洛培南/美平。
适应证:各种细菌所致严重感染;病因不明的感染;院内感染;免疫缺陷感染者。
4)ß-内酰胺酶抑制剂有克拉维酸、舒巴坦、三唑巴坦,其中以三唑巴坦作用最强;临床产品有:阿莫西林—克拉维酸、替卡西林—克拉维酸。
氨苄西林—舒巴坦,以上产品适用于产酶金葡菌、肠杆菌、流感杆菌、淋球菌、卡他莫拉菌、脆弱类杆菌等感染。
哌拉西林—三唑巴坦还适用于铜绿假单孢菌引起的严重感染。
(二)喹诺酮类第一代奈啶酸仅对G r-菌有效/吸收差/反应多;第二代吡哌酸对G r-杆菌有效可用于尿路感染;第三代氟喹诺酮类(氟哌酸/环丙/依若/氧氟/左氟/洛美/培氟沙星等),对G r-/+菌、铜绿假单孢菌均有效。
体内分布广、半衰期长、反应轻、耐药率低,可用于各种感染;第四代莫西/加替/司帕/左氧氟沙星,对G r-/+菌及需氧/厌氧菌、支/衣原体作用强,能安全、有效地治疗各种感染。
(三)新大环内酯类特点是:均为依托红霉素的衍生物,对胃酸稳定、生物利用度高、半衰期长,如罗红、地红、克拉、阿奇霉素等,抗菌谱加宽,对葡萄球菌、链球菌、流感杆菌、支原体、衣原体、非结核分支杆菌均有效;不良反应轻而少;可q d用药;组织浓度高、分布广,如阿奇在前列腺的浓度是血的10倍、是治疗呼吸道感染如社区获得性肺炎、尿路感染的常用药。
(四)氨基糖苷类对G r-杆菌如大肠/肺炎/流感杆菌抗菌活力强;对沙雷菌、肠杆菌、拘橼酸菌、铜氯假单孢菌、不动/产碱杆菌敏感。
对葡萄球菌和G r-杆菌有3h或更长久的后续作用(P A E)。
主要品种:链霉素主用于结核病;卡那霉素趋于淘汰;庆大耐药率较高;阿米卡星耐药率最低;妥布和西索米星与庆大有交叉耐药;此外外还有核糖霉素、小诺霉素、奈替米星、新霉素。
(五)糖肽类万古霉素和去甲万古霉素1.万古霉素及去甲万古霉素适用于耐药革兰阳性菌所致的严重感染,特别是甲氧西林耐药金葡菌(M R S A)或甲氧西林耐药凝固酶阴性葡萄球菌(M R C N S)、肠球菌属及耐青霉素肺炎链球菌所致感染;也可用于对青霉素类过敏患者的严重革兰阳性菌感染。
