紫外吸收光谱法测定苯甲酸
苯甲酸电离常数三种测定方法的比较

2.3.2苯甲酸pKa 值的预测定
3·O
在( 25±O.5) ℃,将苯甲酸和NaOH按摩
尔数比1:1混合,在水溶液中 进行反应. 由于
2.5
反应完全后[ HA] 一[ A一] ,则pKa一- pH,此时
2·0
用pH计测其反应液的pH,即得粗测的pKa.
测得的苯 甲酸反应液的pH=4.16. 2.3.3苯甲酸pKa 值的精确测定 移取储备液1.00 mL 5份置 于50 mL
摘要:本文采用电位法、电导法、紫外分光光度法测定了苯甲酸的电离常数.用三种方法测得 的 pKa分 别为 :4 .03 ,4. 08 和4. 20. 结果 表明 : 用紫 外分 光光 度法 测得 的苯 甲酸 电离 常数 值最 为准 确,但三种方法各有特点,可根据具体的实验要求和实验目的选择合适的测定方法.
2结果与讨 论
2.1 电位法测定苯甲酸的电离常数 把稀释的苯甲 酸溶液和原苯甲酸溶液共6种不同浓度溶 液,分别放入6个干燥的50 mL烧杯中( 烧杯编 成l 一6) ,按由稀到浓分别用pH计测定它们的pH值,实验记录和计算结 果见表1.从表1.可以看出用电位 法测定的苯甲酸的pKa 值为4.03,而苯甲酸的pKa理论值为4.21,相对标准偏差( RSD) 为7.47%.这个实 验结果误差比较大,主要原因由于仪器本身的误差,在实验的过程中发现玻璃电极在长时间使用后( 一般两 个小时以后) 会出现钝化现象,其主要原因是玻璃电极的水化层在长时间浸泡在溶液中,造成H+交换受阻. 这时候应将电极在KCl 溶液中浸泡一夜.使其水化层恢复.
收稿日期:2008一12—3l
修改日期:2009—03—16
作者 简介:徐 雯( 1979一) ,女 ,安徽安 庆人, 安徽黄山 学院化学 系讲师 ,主要从 事物理 化学的教 学与研究 .
紫外光谱分析实验数据处理部分
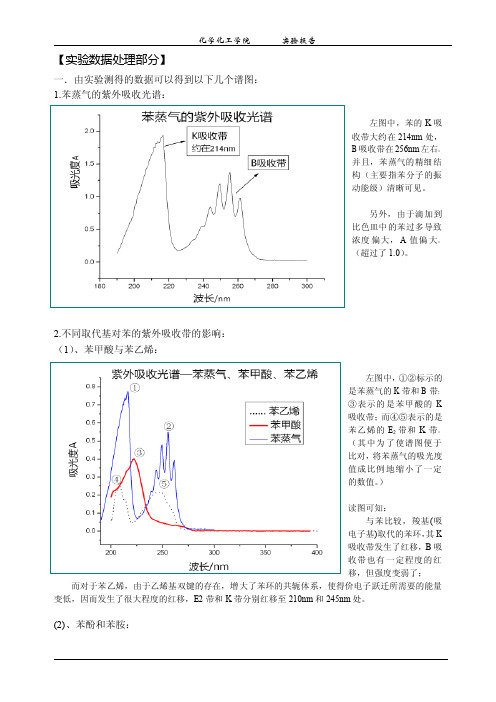
【实验数据处理部分】一.由实验测得的数据可以得到以下几个谱图:1.苯蒸气的紫外吸收光谱:左图中,苯的K吸收带大约在214nm处,B吸收带在256nm左右。
并且,苯蒸气的精细结构(主要指苯分子的振动能级)清晰可见。
另外,由于滴加到比色皿中的苯过多导致浓度偏大,A值偏大。
(超过了1.0)。
2.不同取代基对苯的紫外吸收带的影响:(1)、苯甲酸与苯乙烯:左图中,①②标示的是苯蒸气的K带和B带;③表示的是苯甲酸的K吸收带;而④⑤表示的是苯乙烯的E2带和K带。
(其中为了使谱图便于比对,将苯蒸气的吸光度值成比例地缩小了一定的数值。
)读图可知:与苯比较,羧基(吸电子基)取代的苯环,其K吸收带发生了红移,B吸收带也有一定程度的红移,但强度变弱了;而对于苯乙烯,由于乙烯基双键的存在,增大了苯环的共轭体系,使得价电子跃迁所需要的能量变低,因而发生了很大程度的红移,E2带和K带分别红移至210nm和245nm处。
(2)、苯酚和苯胺:图中,①②标示的是苯蒸气的K带和B带;③④表示的是苯酚的K吸收带和B吸收带;而⑤⑥⑦则表示苯胺的E2带、K带和B带。
读图可知:苯酚的E2吸收带与K吸收带合并了,原因是酚羟基的助色作用使得吸收带发生红移,同样地,与苯相比,苯酚的B吸收带也发生了红移;苯胺的氮原子上含有孤对电子,也和酚羟基一样具有助色效应,因此苯胺的各个吸收带也发生了一定程度的红移(相比较于苯而言)。
二、溶液性质对取代苯紫外吸收的影响:1.苯酚与其碱性溶液:图中:①②③分别标示的是苯酚在碱性溶液中的E2吸收带、K吸收带和B吸收带的大致位置;而④⑤则分别标示苯酚在中性溶液中的K吸收带和B吸收带的位置。
读图可知:由于碱性溶液中的酚羟基以氧负离子形式存在,使得酚羟基的助色作用大大增强,因而苯环的吸收带均发生较大的红移。
例如:原本在苯酚的紫外吸收图谱中未能读出的E1、E2吸收带,此时可以大致从图中读出;另外,碱性溶液中,苯酚的K带红移至245nm左右,B带红移至290nm左右。
紫外分光光度法测定饮料中的苯甲酸

紫外分光光度法测定饮料中的苯甲酸TYYGROUP system office room 【TYYUA16H-TYY-TYYYUA8Q8-实验三紫外分光光度法测定饮料中的防腐剂—苯甲酸1 实验试剂与仪器试剂苯甲酸(AR),雪碧汽水仪器日立UV-3010紫外-可见光谱仪,1cm石英比色皿2 实验原理与方法为了防止食品在储存、运输过程中发生腐败、变质,常在食品中添加少量防腐剂。
防腐剂使用的品种和用量在食品卫生标准中都有严格的规定,苯甲酸及其钠盐、钾盐是食品卫生标准允许使用的主要防腐剂之一。
我国规定了苯甲酸(盐)在碳酸饮料中最大使用量为0.2g/kg。
苯甲酸具有芳香结构,在波长225nm和272nm处有强吸收由于食品中苯甲酸用量很少,同时食品中其它成分也可能产生干扰,因此一般需要预先将苯甲酸与其它成分分离。
从食品中分离防腐剂常用的方法有蒸馏法和溶剂萃取法等。
本实验测定雪碧中苯甲酸,含有人工合成色素、甜味剂等,但一般在紫外区无吸收,故不干扰测定,样品不用处理,苯甲酸(钠)在225nm处有最大吸收,可在225nm波长处测定标准溶液及样品溶液的吸光度,绘制标准曲线法,可求出样品中苯甲酸的含量。
3 实验步骤苯甲酸标准储备液配制称取0.1000g苯甲酸于100mL容量瓶中,加适量蒸馏水定容,配制成1mg/mL溶液,吸取此液5mL于50mL容量瓶中,用蒸馏水定容至刻度,每毫升溶液相当于苯甲酸100ug。
标准曲线绘制取苯甲酸标准储备液、、、、,分别置于50mL容量瓶中,用蒸馏水溶液稀释至刻度。
以水为对照液,测定其中5号标准溶液的紫外可见吸收光谱(测定波长范围为200~350nm),找出λmax ,然后在λmax处测定五个标准溶液的吸光度A。
样品处理和测定雪碧饮料除二氧化碳后,准确移取于100mL容量瓶中,用蒸馏水定容,在λ处测定max吸光度。
4 实验结果测得苯甲酸在227nm波长处有最大吸光值表1 标准液吸光度测定标准液(μg/ml) 0 2 4 8 12吸光度图1 苯甲酸标准溶液标准曲线测得雪碧样品的苯甲酸吸光度为=μg/ml从曲线上找出相应的苯甲酸浓度Cx: 样品定容后体积为100mlV1: 所取样品体积为 25mlV2因为雪碧的密度约等于1kg/m3,故μg/ml≈μg/g=kg根据中华人民共和国国家标准《食品添加剂使用卫生标准一》对汽水类食品中苯甲酸的最大使用量做了规定:苯甲酸<=0.2g/Kg,本实验使用的雪碧样品苯甲酸浓度Kg<0.2g/Kg,即低于国家标准,符合国家标准。
吸收光谱法苯甲酸的含量标准曲线的绘制

吸收光谱法苯甲酸的含量标准曲线的绘制
绘制吸收光谱法测定苯甲酸含量的标准曲线,主要包括以下步骤:
1. 准备一系列浓度已知的苯甲酸标准溶液,比如使用质量浓度为0.1 g/L、0.2 g/L、0.3 g/L 等不同浓度的溶液。
确保样品的每个浓度都有足够的重复性。
2. 使用分光光度计,将波长设置在苯甲酸最大吸收峰的位置。
根据实验条件,苯甲酸的最大吸收峰通常在220-240 nm之间。
3. 依次测量各个标准溶液的吸光度值,并记录下所测得的吸光度值。
确保每次测量时之前进行零点校准。
4. 将吸光度值作为纵坐标,苯甲酸的浓度作为横坐标,绘制出标准曲线。
将所测得的数据点用直线或者曲线连接起来。
5. 根据所绘制的标准曲线,可以推算出待测样品中苯甲酸的浓度。
将待测样品的吸光度值代入标准曲线中,根据吸光度值和标准曲线的关系,可以得到样品中苯甲酸的浓度。
需要注意的是,在进行实验测定之前,应确保实验仪器的准确性和正确性。
同时,在进行测定过程中,按照实验室安全规范进行操作,避免对身体和环境造成伤害。
教案:紫外可见分光光度计 法测定食品中苯甲酸钠的含量

紫外可见分光光度计法测定食品中苯甲酸钠的含量一、实验目的1、了解和熟悉紫外-分光光度计的原理、结构和操作方法;2、掌握紫外分光光度法测定苯甲酸的吸收光谱图;3、掌握标准曲线法测定样品中苯甲酸钠的含量。
二、实验原理为了防止食品在储存、运输过程中发生腐蚀、变质,常在食品中添加少量防腐剂。
防腐剂使用的品种和用量在食品卫生标准中都有严格的规定,苯甲酸及其钠盐、钾盐是食品卫生标准允许使用的主要防腐剂之一,其使用量一般在0.1%左右。
苯甲酸及苯甲酸钠具有芳香结构在近紫外光区具有较强的吸收。
通过实验证实,苯甲酸在230nm处具有最大吸收。
另一方面,它在水中具有适当的溶解度,所以,可将标样和样品处理成水溶液,采用紫外分光光度计,通过标准曲线法而实现酸性食品中苯甲酸(钠)含量的测定。
由于食品中苯甲酸用量很少,同时食品中其它成分也可能产生干扰,因此一般需要预先将苯甲酸与其它成分分离。
从食品中分离防腐剂常用的方法有蒸馏法和溶剂萃取法等。
本实验测定雪碧、可口可乐、醒目等饮料中苯甲酸(钠),样品不用处理,在230nm波长处测定标准溶液及样品溶液的吸光度,绘制标准曲线法,可求出样品中苯甲酸的含量。
3、仪器和试剂仪器:紫外可见分光光度计 TU-1810(北京普析通用仪器有限公司),1.0cm石英比色皿,50ml容量瓶11个,吸量管5mL一支、1mL两支。
试剂:苯甲酸钠标准贮备液(1.000g/L):准确称量经过干燥的苯甲酸钠1.000g(105℃干燥处理2h)于1000mL容量瓶中,用适量的蒸馏水溶解后定容。
该贮备液可置于冰箱保存一段时间;0.1mol/L NaOH溶液;市售饮料。
四、实验步骤1、标准曲线的制作苯甲酸钠标准溶液(100.0mg/L):准确移取苯甲酸储备液5.00mL 于50mL容量瓶中,加入蒸馏水稀释定容。
苯甲酸钠系列标准溶液的配制:分别准确移取苯甲酸钠标准溶液0.00mL、1.00mL、2.00mL、3.00mL、4.00mL和5.00mL于6个50mL容量瓶中,各加入0.1mol/LNaOH溶液1.00mL蒸馏水稀释定容,摇匀。
有机化合物的紫外吸收光谱实验报告

有机化合物的紫外吸收光谱实验报告实验目的:1. 了解有机化合物紫外吸收光谱的基本原理以及使用方法。
2. 掌握实验操作的基本技能,正确操作分光光度计。
3. 通过实验,了解有机化合物的分子结构与紫外吸收光谱之间的关系,为分析有机分子结构提供基础。
实验原理:有机化合物的紫外吸收光谱可以为有机分子结构的研究提供很大的帮助。
在紫外光谱中,通常对于各种功能团体都存在特定的波长范围的吸收峰。
通过分析有机化合物在特定波长的紫外吸收峰的大小以及形状,我们就能够推断出分子中存在的功能团体。
实验步骤:1. 准备实验所需物品:分光光度计、苯甲酸溶液、四乙酸酯溶液、环己酮溶液等。
2. 打开分光光度计,调试好仪器,使其能夠正常工作。
3. 取一定量苯甲酸溶液,加入分光光度计比色皿中,并做好参照物质的设置。
4. 按照波长扫描模式,设定扫描范围,并进行扫描。
5. 记录下吸收峰的最大吸收波长及吸光度值,并对红外光谱进行分析解释。
6. 重复上述实验步骤,分别对于四乙酸酯溶液和环己酮溶液进行的操作。
7. 对实验结果进行分析,分别阐明各个实验组操作中存在的异同之处,并对每种化合物的分子结构和吸收峰进行解释。
实验结果分析:通过实验,我们得到了三种不同有机化合物的紫外吸收光谱,并对各个实验组操作中存在的异同之处进行了分析。
对于苯甲酸、四乙酸酯和环己酮这三种化合物,它们的特定吸收峰分别对应的波长区间如下:1. 苯甲酸:250nm至270nm2. 四乙酸酯:270nm至290nm3. 环己酮: 230nm至255nm可以看出,这三种化合物的吸收峰波长的区间是不同的,这表现出不同化合物分子结构之间的差异。
我们还可以通过分析各个吸收峰的峰值和峰形,来推断出分子中存在的官能团体,这也有利于我们理解化合物分子结构和有机分子之间的结构相互关系。
结论:通过实验,我们对于有机化合物的紫外吸收光谱有了更深入的了解。
通过观察分析不同化合物的吸收峰,我们可以推断出分子结构中所存在的官能团体以及它们在分子中位置的不同,从而为分析有机分子结构和进行有机合成提供帮助。
紫外吸收光谱法测定苯甲酸(精)

因此紫外光谱可用于判别有机化合物中发色团和助色团的种类、位
置、数目,以及区别饱和与不饱和化合物,测定分子中共轭程度等。但
是仅依靠紫外光谱来推断未知化合物的结构是困难的。
4 苯甲酸与山梨酸的性质与用途
苯甲酸别名安息香酸,白色单斜晶系片状或针状结晶体,略带安息
紫外吸收光谱法测定苯甲酸 山梨酸和未知物
化学生物系 吴 丹
பைடு நூலகம்
一、实验目的
1 通过实验了解苯甲酸,山梨酸的紫外吸收特征,并利用这些 特征对未知物进行定性鉴定。
2 通过测定有机化合物紫外吸收光谱,掌握鉴别化合物中发色
团及其化合物类型的方法。
3 掌握有机化合物结构与紫外吸收光谱之间内在联系的规律。
二、实验原理
苯甲酸具有环状共轭结构,在波长 228nm 和272nm 处有 E吸收带和B 吸收带 (芳香族化合物的特征吸收) ;
山梨酸(2,4-己二烯酸)无色针状结晶或白色结晶性粉末,无嗅或稍
带刺激性臭味。分子量112.13。熔点132-135℃。沸点228℃(分解)。微溶于 水。溶于有机溶剂。对光、热稳定,但在空气中长期放置易被氧化着色。
波长 (nm)
310
吸光 度(A)
吸光度(A)从吸收曲线上确定未知物的最大波长λmax = 所以该化合物为???
nm
六、数据处理
1
利用谱图进行定性分析
从紫外光谱仪上读出各波长的吸光度,以波长
为横坐标,吸光度为纵坐标作图,就得紫外吸收光
谱图。由光谱图可定出λmax ,并将未知物谱图与
已知化合物的谱图对照,推测未知物为苯甲酸或山
实验一 紫外分光光度法测定苯甲酸

的含量 取10.00ml样品液,放入50ml容量瓶中,用 0.01mol/L的NaOH溶液定容,摇匀得稀释好的样 品液X。 在上述曲线中找出最大吸收波长,以此作测定波 长。以0.01mol/L的NaOH溶液为参比液。在完全 相同的条件下测出稀释好的样品液X的吸光度值。 3、按下式计算样品液中苯甲酸的浓度:
比色皿使用注意事项
1、拿取比色皿时,只能用手指接触毛玻璃面,避免接触 光学面,注意保护,防止摔破。 2、盛装溶液时,高度为比色皿的2/3处即可,光学面如有 残液可先用滤纸轻轻吸附,然后再用擦镜纸擦拭。 3、 不可随时调换参比用的比色皿和承载样品比色皿,也 就是说参比比色皿应该固定。 4、使用比色皿时, 还应特别注意通光方向。一般比色皿 的毛玻璃面上都刻有箭头, 或在透光面上蚀刻有标记, 以供 使用者辨认通光方向。 5、不能把装有溶液的比色皿放在仪器上以防止溅湿仪器。 6、比色皿在使用后,应立即用水冲洗干净,收好。
实验报告的格式
一、实验目的 二、实验原理 三、实验步骤 四、实验数据与处理 五、结果与讨论
作图统一用Excel格式并打印粘帖
Ax
Cs
Cx
五、结果与讨论
结果如何?是否符合预期? 分析失败的原因:仪器因素?溶液因素? 人为因素?环境因素?
紫外分光光度计的使用方法
1.打开电源,预热20分钟 2.按MODE键设为吸光度方式 显示器显示“---nm,----Abs” 3.设定波长,如220nm 显示器显示“220nm,----Abs” 4.打开样品室盖,将参比液比色皿和待测液比色皿放入样 品室盖上样品室盖 5.将参比液比色皿拉入光路中,按100%T键调零 调零完成时显示器显示“220nm,0.000Abs” 6.将待测溶液拉入光路中,直接读数 注意:每改变波长,必须重新调零 注意倒溶液时远离仪器,避免溅湿仪器
仪器分析实验报告

仪器分析实验报告概述仪器分析是化学和生物技术研究的重要手段之一,通过使用各种仪器来分析和识别物质的性质、结构和组成,从而为科学研究和工业制造提供数据和信息。
本实验旨在通过对三种常用分析仪器的使用与操作,掌握仪器分析的基本方法和技能。
实验一:紫外可见分光光度计紫外可见分光光度计是一种常用的分析仪器,可以用于测定分子的吸光度,从而确定其浓度。
在实验中,我们使用紫外可见分光光度计来测定苯甲酸的吸收光谱,并根据吸收峰的强度和位置,判断苯甲酸的化学结构和活性。
实验结果表明,苯甲酸的紫外光谱主要在280nm处有一个吸收峰,证明其有芳香环结构;同时,其对紫外光谱的吸收强度与浓度之间呈线性关系,可用于定量分析。
实验二:原子吸收光谱仪原子吸收光谱仪是一种常用的分析仪器,可以用于分析痕量金属元素的含量。
在实验中,我们使用原子吸收光谱仪来测定硬度水样品中钙和镁的含量。
实验结果表明,硬度水样品中钙和镁的含量分别为0.4mg/L和0.5mg/L,与标准值相接近,说明该方法可靠。
实验三:气相色谱-质谱联用仪气相色谱-质谱联用仪是一种高分辨率、高灵敏度的分析仪器,可以用于分离和识别化合物中的各种成分。
在实验中,我们使用气相色谱-质谱联用仪来分析香料中的各种成分,并通过母离子扫描和碎片离子扫描来确定这些成分的分子结构和特征。
实验结果表明,香料中含有多种成分,其中醛类、酮类和酯类物质含量较高,可以作为该香料的主要特征。
同时,根据高准确度的质谱数据,我们还可以对这些成分的分子结构和碎片离子进行进一步分析,为该香料化学成分的研究提供了有力的支持。
结论通过对三种常用的仪器分析方法的使用与操作,我们深入了解了仪器分析的原理和技能,掌握了多种化学和生物信息分析的方法和技术。
同时,我们还进一步加深了对化学和生物学的认知和理解,为今后的科学研究和实践奠定了坚实的基础。
紫外可见分光光度计测定食品中苯甲酸钠的含量

紫外可见分光光度计测定⾷品中苯甲酸钠的含量紫外可见分光光度计法测定⾷品中苯甲酸钠的含量⼀、实验⽬的1.进⼀步了解和熟悉紫外-分光光度计的原理和结构,学习UV2550的操作。
2.掌握紫外分光光度法测定苯甲酸钠的吸收光谱图。
3.掌握标准曲线法测定样品中苯甲酸钠的含量。
⼆、实验原理为了防⽌⾷品在储存、运输过程中发⽣腐蚀、变质,常在⾷品中添加少量防腐剂。
防腐剂使⽤的品种和⽤量在⾷品卫⽣标准中都有严格的规定,苯甲酸及其钠盐、钾盐是⾷品卫⽣标准允许使⽤的主要防腐剂之⼀,其使⽤量⼀般在0.1%左右。
苯甲酸具有芳⾹结构,在波长225nm和272nm处有K吸收带和B吸收带。
根据苯甲酸(钠)在225nm处有最⼤吸收,测得其吸光度即可⽤标准曲线法求出样品中苯甲酸的含量。
三、仪器和试剂1.紫外可见分光光度计UV2550(⽇本岛津),1.0cm⽯英⽐⾊⽫,50ml容量瓶。
2.NaOH溶液(0.1mol/L)3.苯甲酸钠标准溶液的配制(1)苯甲酸钠标准贮备液(1.000g/L):准确称量经过⼲燥的苯甲酸钠1.000g(105℃⼲燥处理2h)于1000mL容量瓶中,⽤适量的蒸馏⽔溶解后定容。
该贮备液可置于冰箱保存⼀段时间。
(2)苯甲酸钠标准溶液(100.0mg/L):准确移取苯甲酸钠储备液10.00mL于100mL容量瓶中,加⼊蒸馏⽔稀释定容。
(3)系列标准溶液的配制:分别准确移取苯甲酸钠标准溶液1.00mL、2.00mL、3.00mL、4.00mL和5.00mL于6个50mL容量瓶中,各加⼊0.1mol/LNaOH溶液1.00mL后,⽤蒸馏⽔稀释定容。
得到浓度分别为2.0 mg/L、4.0mg/L、6.0mg/L、8.0mg/L和10.0mg/L的苯甲酸钠系列标准溶液。
4.市售饮料的配制准确移取市售饮料0.5ml于50mL容量瓶中,⽤超声脱⽓5min驱赶⼆氧化碳后,加⼊0.1mol/LNaOH溶液1.00mL,⽤蒸馏⽔稀释定容。
紫外吸收光谱法测定苯甲酸含量

紫外吸收光谱法测定苯甲酸含量
紫外吸收光谱法是一种常用的分析方法,可以用于测定化合物在紫外光区域的吸光性质。
苯甲酸(benzoic acid)通常在紫外区域(200 nm至400 nm)具有吸收峰,因此可以利用紫外吸收光谱法对其含量进行测定。
以下是使用紫外吸收光谱法测定苯甲酸含量的一般步骤:
1.样品制备:将含有苯甲酸的样品溶解在适当的溶剂中,以获得
均匀的溶液。
2.波长选择:选择苯甲酸在紫外光区域的一个特定波长进行测量。
典型的波长可能在200 nm至300 nm之间。
3.基准溶剂:准备一个不含苯甲酸的基准溶剂,以进行基线校正。
4.测量:使用紫外吸收分光光度计,将样品溶液和基准溶剂的吸
光度分别测量在选择的波长。
记录吸光度值。
5.计算含量:通过比较样品吸光度与基准溶剂吸光度的差异,结
合标准曲线或已知浓度的苯甲酸溶液,计算出苯甲酸的含量。
请注意,为了提高测量的准确性,建议制备一系列不同浓度的标准溶液,绘制标准曲线,以便在测量时用于计算未知样品的苯甲酸含量。
具体的测定条件和步骤可能会根据仪器、溶剂以及实验室设备的不同而有所变化。
在进行实验之前,请参考相关的分析方法和仪器操作手册。
实验紫外分光光度法测定饮料中的防腐剂

实验紫外分光光度法测定饮料中的防腐剂实验目的:1.掌握蒸馏操作;2.掌握紫外可见分光光度法测定苯甲酸的方法和原理。
实验原理:为了防止食品在储存、运输过程中发生腐败、变质,常在食品中添加少量防腐剂。
防腐剂使用的品种和用量在食品卫生标准中都有严格的规定,苯甲酸及其钠盐、钾盐是食品卫生标准允许使用的主要防腐剂之一。
其使用量一般在0.1%左右。
苯甲酸具有芳香结构,在波长225nm和272nm处有K吸收带和B吸收带。
由于食品中苯甲酸用量很少,同时食品中其它成分也可能产生干扰,因此一般需要预先将苯甲酸与其它成分分离。
从食品中分离防腐剂常用的方法有蒸馏法和溶剂萃取法等。
本实验采用蒸馏法对鲜橙多中的苯甲酸进行了测定,苯甲酸(钠)在225nm处有最大吸收,可在225nm波长处测定标准溶液及样品溶液的吸光度,绘制标准曲线法,可求出样品中苯甲酸的含量。
仪器与试剂:紫外分光光度计,蒸馏装置;无水硫酸钠,磷酸,硫酸,氢氧化钠,重铬酸钾,苯甲酸;鲜橙多。
操作步骤:1、样品前处理:准确称取10.0g均匀的样品,置于250 mL蒸馏瓶中,加1mL H3PO4,20g无水Na2SO4,70mL水,三粒玻璃珠进行第一次蒸馏。
用预先加有5mL 0.1mol﹒L-1 NaOH的50mL容量瓶接收馏出液,当蒸馏液收集到45mL时,停止蒸馏,用少量水洗涤冷凝器,最后用水稀释至刻度。
吸取上述蒸馏液25mL,置于另一个250mL蒸馏瓶中,加入25mL 0.033mol﹒L-1 K2Cr2O7溶液,6.5mL 2mol﹒L-1H2SO4溶液,连接冷凝装置,水浴上加热10min,冷却,取下蒸馏瓶,加入1mL H3PO4、20g无水Na2SO4、40mL水和三颗玻璃珠,进行第二次蒸馏,用预先加有的5mL 0.1mol﹒L-1 NaOH的50mL容量瓶接收蒸馏液,当蒸馏瓶收集到45mL左右时,停止蒸馏,用少量洗涤冷凝器,最后用水稀释至刻度。
根据样品中苯甲酸含量,取第二次蒸馏液5~20mL,置于50mL容量瓶中,用0.01mol﹒L-1 NaOH定容,以0.01mol﹒L-1 NaOH作为对照液,于紫外分光光度计225nm处测定吸光度。
紫外吸收光谱法测定苯甲酸

紫外吸收光谱法测定苯甲酸
紫外吸收光谱法测定苯甲酸
பைடு நூலகம்
紫外吸收光谱法测定苯甲酸 山梨酸和未知物 化学生物系 吴 丹 一、实验目的 1 通过实验了解苯甲酸,山梨酸的紫外吸收特征,并利用这些 特征对未知物进行定性鉴定。 2 通过测定有机化合物紫外吸收光谱,掌握鉴别化合物中发色 团及其化合物类型的方法。 3 掌握有机化合物结构与紫外吸收光谱之间内在联系的规律。 二、实验原理 1 电磁波谱范围表 光谱名称 X射线 远紫外光 紫外光 可见光 近红外光 中红外光 远红外光 微波 无线电波 波长范围 0.01--10 nm 10--200 nm 200-- --400 nm -- 400-- --750 nm -- 0.75--2.5 ?m 2.5--5.0 ?m 5.0-- 1000 ?m 0.1--100 cm 1--1000 m 跃迁类型 K和L层电子 中层电子 价电子 价电子 分子振动 分子振动 分子转动和低位振动 分子转动 分析方法 X射线光谱法 真空紫外光谱法 紫外光度法 比色及可见光度法 近红外光谱法 中红外光谱法 远红外光谱法 微波光谱法 核磁共振光谱法 2 用紫外或可见光照射含有共轭结构的不饱和化合物 共轭结构的不饱和化合物时,分子中的 共轭结构的不饱和化合物 价电子会从基态向激发态跃迁,此时,电子吸收了某一波长的紫外(可 见)光。能级跃迁所需的能量与被吸收的紫外(可见)光波长之间的关 系,可按下式计算: E = hf = hc / λ 式中: h---普郎克常数 △E—电子能级的能量差(KJ·mol-1) f , λ—被吸收光的频率和波长 电子跃迁主要有σ→σ* ,n→σ*, π→π*, n→π* 四种形式,它们跃迁所需能量大小为: σ→σ* > n→σ* ≥ π→π* > n→π* 其中σ→σ* 及n→σ* 的跃迁能量大,吸收的光 的
紫外分光光度法测定食品中苯甲酸钠的含量

紫外分光光度法测定食品中苯甲酸钠的含量【摘要】利用紫外分光光度法测定食品中苯甲酸钠含量。
在222nm处有最大吸收,可通过紫外分光光度法进行测定。
该法检测成本低,不需要大型仪器及特殊试剂,具有简便快速的特点,可应用于一般工厂实践中。
【关键词】紫外分光光度法;苯甲酸钠;含量测定食品防腐剂是在食品工业中使用比较广泛的一种食品添加剂,其主要作用是抑制微生物的生长繁殖,以提高食品的保质期。
苯甲酸钠是目前国内外广发应用的一种食品防腐剂,具有水中溶解度大,防腐效果好的特点。
从保证食品安全的角度来说,研究简便快速测定食品中苯甲酸钠的方法具有重要的现实意义。
[1]紫外分光光度法是利用物质分子对紫外可见光谱区的辐射吸收来进行分析的一种仪器分析方法,本文研究通过紫外分光光度法来测定各类食品中防腐剂苯甲酸钠的含量,不但操作方便,而且实验条件简单,适合于食品防腐剂的快速检测。
[2]1.仪器与试剂1.1仪器TU—1810紫外分光光度计、FA1004 型电子天平、石英比色皿、水浴装置,容量瓶、分液漏斗、移液管、吸耳球、量筒、烧杯、玻璃棒等。
1.2试剂苯甲酸钠(分析纯),40g/L氢氧化钠溶液,50%浓度的盐酸,乙醚(分析纯),蒸馏水酱油、水塔陈醋、美年达、甘草杏肉(超市购入)。
2.实验方法2.1最大吸收波长的确定配置(1.000g/L)的苯甲酸钠标准溶液1000mL,准确吸取1.00mL于100mL 容量瓶中,用蒸馏水稀释成浓度为10mg/L的苯甲酸钠溶液,摇匀,以蒸馏水为参比,在波长200—300nm波长范围内测定吸光度,记录苯甲酸钠的最大吸收波长,结果如图1所示:由图1分析可知,在200—300nm的波长范围内,苯甲酸钠的波长在222nm 处,有最大吸收波长,则222nm即为吸收测定波长。
2.2标准曲线的绘制吸取苯甲酸钠标准溶液0mL、0.1mL、0.2mL、0.5mL、1.0mL、1.5mL、2.0mL、3.0mL于100mL容量瓶中,分别加入1mL0.1mol/L的氢氧化钠溶液,用蒸馏水定容至刻度,摇匀,在222nm处测其吸光度,并以吸光度(A)为纵坐标,浓度(C)为横坐标,绘制标准曲线,结果如图2所示。
紫外可见分光光度计法测定食品中苯甲酸钠的含量

紫外可见分光光度计法测定食品中苯甲酸钠的含量一、实验目的1.进一步了解和熟悉紫外-分光光度计的原理和结构,学习UV的操作。
2.掌握紫外分光光度法测定苯甲酸钠的吸收光谱图。
3.掌握标准曲线法测定样品中苯甲酸钠的含量。
二、实验原理为了防止食品在储存、运输过程中发生腐蚀、变质,常在食品中添加少量防腐剂。
防腐剂使用的品种和用量在食品卫生标准中都有严格的规定,苯甲酸及其钠盐、钾盐是食品卫生标准允许使用的主要防腐剂之一,其使用量一般在0.1%左右。
苯甲酸具有芳香结构,在波长225nm和272nm处有K 吸收带和B吸收带。
根据苯甲酸(钠)在225nm处有最大吸收,测得其吸光度即可用标准曲线法求出样品中苯甲酸钠的含量。
三、仪器和试剂1.紫外可见分光光度计UV,1.0cm石英比色皿,50ml容量瓶。
2.NaOH溶液(0.1mol/L)3.苯甲酸钠标准溶液的配制(1)苯甲酸钠标准贮备液(1.000g/L):准确称量经过干燥的苯甲酸钠1.000g(105℃干燥处理2h)于1000mL容量瓶中,用适量的蒸馏水溶解后定容。
该贮备液可置于冰箱保存一段时间。
(2)苯甲酸钠标准溶液(100.0mg/L):准确移取苯甲酸钠储备液10.00mL于100mL容量瓶中,加入蒸馏水稀释定容。
(3)系列标准溶液的配制:分别准确移取苯甲酸钠标准溶液1.00mL、2.00mL、3.00mL、4.00mL和5.00mL于5个50mL容量瓶中,各加入0.1mol/LNaOH溶液1.00mL后,用蒸馏水稀释定容。
得到浓度分别为 2.0 mg/L、4.0mg/L、6.0mg/L、8.0mg/L和10.0mg/L的苯甲酸钠系列标准溶液。
4.市售饮料的配制准确移取市售饮料0.5ml于50mL容量瓶中,用超声脱气5min驱赶二氧化碳后,加入0.1mol/LNaOH溶液1.00mL,用蒸馏水稀释定容。
5.蒸馏水四、实验步骤1.开机2.吸收光谱的测定:从170nm-370nm扫描测定最大吸收波长。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2、移液管的使用 、 (1)洗涤 (2)润洗 使用前用吸水纸将尖端内外的水除去 吸水纸将尖端内外的水除去,然后用待吸液润洗三次:左手持洗耳球,右手 吸水纸将尖端内外的水除去 拇指和中指拿住标线以上部分,将移液管管尖插入约溶液1~2cm,将待吸液吸至球部 吸至球部1/4 吸至球部 处,移出,荡洗,弃去(切记从尖口放出 从尖口放出,应保持上管口和食指干燥)。 从尖口放出 (3)移液: 左手持洗耳球,右手拇指和中指拿住标线以上部分,将移液管管尖插入约溶液 ~2cm, 移液管管尖插入约溶液1~ 移液管管尖插入约溶液 将待吸液吸至标线以上,迅速移去洗耳球,同时用右手食指堵住管口,左手改拿盛待吸液 的容器。然后,将移液管往上提起,使之离开液面,并将原深入溶液部分沿容器内部轻转 两圈,以除去管壁上的溶液。使容器倾斜 度,其内壁与移液管尖紧贴,同时右手食指微 容器倾斜45度 容器倾斜 微松动,使液面缓慢下降,直到管内溶液的弯月面与标线相切,这时应立即用食指按紧管 口,停留15秒左右,移开待吸液容器,左手改拿接受溶液的容器,并将接受容器倾斜,使 秒 内壁紧贴移液管尖,成45度左右,然后放松右手食指,使溶液自然顺壁流下,待液面下降 度 到管尖后,等15秒左右,移出移液管。(除特别注明,管尖残留溶液不吹入接受容器中)。 秒
nm
六、数据处理 1 利用谱图进行定性分析
从紫外光谱仪上读出各波长的吸光度,以波长 为横坐标,吸光度为纵坐标作图,就得紫外吸收光 谱图。由光谱图可定出λmax ,并将未知物谱图与 已知化合物的谱图对照,推测未知物为苯甲酸或山 梨酸。
表1 苯甲酸吸收曲线的测定
波长 (nm) 吸光 度(A) 200 210 220 230 240 250 260 270 280 290 300
波长 (nm) 吸光 度(A)
310
从吸收曲线上确定苯甲酸的最大波长λmax = ?? nm
表2 山梨酸吸收曲线的测定
波长 (nm) 吸光 度(A) 210 220 230 240 250 260 270 280 290 300 310
紫外吸收光谱法测定苯甲酸 山梨酸和未知物
化学生物系 吴 丹
一、实验目的
1 通过实验了解苯甲酸,山梨酸的紫外吸收特征,并利用这些 特征对未知物进行定性鉴定。 2 通过测定有机化合物紫外吸收光谱,掌握鉴别化合物中发色 团及其化合物类型的方法。 3 掌握有机化合物结构与紫外吸收光谱之间内在联系的规律。
二、实验原理
三、实验技能
1、容量瓶的使用 、 (1)使用前检漏: 加水至标线附近,盖好瓶塞后,左手用食指按住塞子,其余手指拿住瓶颈标线以上部 分,右手指尖托住瓶底,将瓶倒立 分钟 倒立2分钟 转动瓶塞180°,再倒立 倒立 分钟,如不漏水,将瓶直立,转动瓶塞 转动瓶塞 ° 2分钟 分钟,如不漏可使用。(使用中,玻璃塞不应放在桌面上,以免玷污,操作时可用一手 分钟 的食指和中指夹瓶塞的扁头,当操作结束后随手将瓶盖盖上,也可用橡皮筋或细绳将瓶塞 系在瓶颈上)。 (2)洗涤: 一般先用自来水洗,最后用蒸馏水水洗3次备用。 (3)定量稀释溶液: 用移液管移取一定体积的溶液于容量瓶中,加水至距标线约 加水至距标线约1cm处,等1~2分钟 分钟,使 加水至距标线约 处 ~ 分钟 附在瓶颈内壁的溶液流下后,再用滴管滴加水至弯液面下缘与标线相切,然后盖上瓶塞, 左手用食指按住塞子,其余手指拿住瓶颈标线以上部分,右手指尖托住瓶底,将容量瓶倒 转,使气泡上升到顶,使瓶振荡,正立后再次倒转进行振荡,如此反复15~20次以上,使 瓶内溶液混合均匀。
四、实验仪器与试剂
1 仪器
UV-9100紫外可见分光光度计 容量瓶(50ml) 烧杯(250ml) 洗耳球 玻璃比色皿(1cm) 洗瓶
吸量管(1ml, 2ml, 5ml, 10ml)
2 试剂
山梨酸 苯甲酸 乙醇 未知物
五、实验内容
1 配制溶液 取10 mg苯甲酸,用乙醇溶解,移入100 mL容量瓶中,用乙醇定容 (实验室已配好 实验室已配好)。吸取该溶液0.50 mL ,用乙醇稀释至25 mL ,此溶 实验室已配好 液浓度为2×10-3 mg·mL-1。 同上方法分别配制浓度为2×10-3 mg·mL-1 的山梨酸及未知物的乙醇溶液。 2 测定和纪录 用1cm 比色皿,以乙醇为参比 乙醇为参比,在波长210---310 nm的范围,分别 乙醇为参比 测定苯甲酸、山梨酸和未知物三种溶液的紫外吸收光谱。
有机化合物的紫外吸收光谱具有少数几个宽的吸收带,缺乏精细结 构,它只能反映分子中生色团和助色团(生色基团就是可以吸收光子而 生色基团就是可以吸收光子而 产生跃迁的原子基团, 产生跃迁的原子基团,主要指化合物分子内能吸收紫外及可见光的原子 基团。助色基团是指含有未成对电子的非生色基团。 基团。助色基团是指含有未成对电子的非生色基团。当它与某一生色基 团相连时,能使该生色基团的吸收波长位置向长波方向移动且光谱强度 团相连时, 有所增大) 有所增大)及附近的结构特征,而不能反映整个分子的特征。 。 因此紫外光谱可用于判别有机化合物中发色团和助色团的种类、位 置、数目,以及区别饱和与不饱和化合物,测定分子中共轭程度等。但 是仅依靠紫外光谱来推断未知化合物的结构是困难的。
电子跃迁主要有σ→σ* ,n→σ*, π→π*, n→π* 四种形式,它们跃迁所需能量大小为: σ→σ* > n→σ* ≥ π→π* > n→π* 其中σ→σ* 及n→σ* 的跃迁能量大,吸收的光 的波长落在真空紫外部分,而n→σ* 和共轭体系 π→π* 跃迁能量较小,落在紫外可见光的范围内。
3 有机化合物的紫外波谱性质
2
用紫外或可见光照射含有共轭结构的不饱和化合物 共轭结构的不饱和化合物时,分子中的 共轭结构的不饱和化合物
价电子会从基态向激发态跃迁,此时,电子吸收了某一波长的紫外(可 见)光。能级跃迁所需的能量与被吸收的紫外(可见)光波长之间的关 系,可按下式计算: E = hf = hc / λ
式中: h---普郎克常数 △E—电子能级的能量差(KJ·mol-1) f , λ—被吸收光的频率和波长
利用紫外吸收光谱鉴定有机物,其主要依据是化合物的吸收光谱特 征,如吸收曲线的形状,吸收峰数目以及各吸收峰波长及摩尔吸收系数 等。 一般来说同一化合物浓度不同时,光吸收曲线形状相同, 一般来说同一化合物浓度不同时,光吸收曲线形状相同,最大吸收 波长不变,只是相应的吸光度大小不同。 波长不变,只是相应的吸光度大小不同。 本实验将通过测定苯甲酸、山梨酸及未知物的紫外吸收光谱,根据 它们的紫外吸收光谱特征鉴定未知物是苯甲酸还是山梨酸。
1 电磁波谱范围表
光谱名称 X射线 远紫外光 紫外光 可见光 近红外光 中红外光 远红外光 微波 无线电波 波长范围 0.01--10 nm 10--200 nm 200-- --400 nm -- 400-- --750 nm -- 0.75--2.5 µm 2.5--5.0 µm 5.0-- 1000 µm 0.1--100 cm 1--1000 m 跃迁类型 K和L层电子 中层电子 价电子 价电子 分子振动 分子振动 分子转动和低位振动 分子转动 分析方法 X射线光谱法 真空紫外光谱法 紫外光度法 比色及可见光度法 近红外光谱法 中红外光谱法 远红外光谱法 微波光谱法 核磁共振光谱法
波长 (nm) 吸光 度(A)
从吸收曲线上确定山梨酸的最大波长λmax = ?? nm
表3 未知物吸收曲线的测定
波长 (nm) 200 210 220 230 240 250 260 270 280 290 300
吸光 度(A)
波长 (nm)
31确定未知物的最大波长λmax = 所以该化合物为???
苯甲酸具有环状共轭结构,在波长 228nm 和272nm 处有 E吸收带和B 吸收带 (芳香族化合物的特征吸收 ; 芳香族化合物的特征吸收) 芳香族化合物的特征吸收
山梨酸(2,4-己二烯酸)无色针状结晶或白色结晶性粉末,无嗅或稍 带刺激性臭味。分子量112.13。熔点132-135℃。沸点228℃(分解)。微溶于 水。溶于有机溶剂。对光、热稳定,但在空气中长期放置易被氧化着色。 用途:化妆品防腐剂。属有机酸类防腐剂。添加量一般在0.5%以下。防 腐活性与溶液pH值有密切关系。当溶液pH值为4时,离解率为14%,当pH 值为6时,离解率即高达94%。因此通常在酸性范围内(pH值4.0-5.5)使用。 在pH值为8以下防腐和杀毒作用稳定,毒性低,我们常用其钾盐作为食品防 食品防 腐剂。 腐剂 山梨酸CH3-CH=CH-CH=CH-COOH,具有α,β-不饱和羰基结构,在波 长250 nm 处有π→π* 跃迁的K 吸收带。
3 . 9100型紫外可见分光光度计操作规范 型紫外可见分光光度计操作规范
①开机 关好样品室门,打开仪器电源开头,预热10分钟。将左边紫外灯开关打开,并将后背 的扳手打到“UV”处。 ②测量 A 调节波长旋钮,使波长显示窗显示所需波长值。 B 将挡光板、装有空白液和样品的比色皿(注意:拿住比色皿的毛玻璃面,四面透光的石 英比色皿应拿斜对角;比色皿内的溶液面高度约为比色皿高度的2/3不应低于25毫米且每 次量相当;比色皿的透光部分表面不能有指印、溶液痕迹;用镜头纸擦比色皿时,应按一 个方向从上往下擦。)放入样品室中(注意:不要硬塞以免刮伤比色皿,比色皿不能放在 仪器面板上),关闭样品室门。 C 拉动拉手将挡光板置于光路中,按0%键,等待显示T:0.0%;A:3.000(理论值为∞) D 拉动拉手将空白液置于光路中,按100%键,等待显示T:100.0%;A:0.000 E 拉动拉手将待测溶液置于光路中,则显示器上显示样品的吸光度值。 ③关机 测量完毕,先检查样品室内是否有溶液洒落,若有应将溶液用滤纸擦干后再关好样品 室门,关闭仪器电源开关,拔下插头。特别强调实验完毕,比色皿应用自来水与蒸馏水冲 洗干净,以免染色。
4 苯甲酸与山梨酸的性质与用途
苯甲酸别名安息香酸,白色单斜晶系片状或针状结晶体,略带安息 香或苯甲醛气味。熔点122.4 ℃.在100℃时迅速升华,它的蒸气有很强 的刺激性,吸入后易引起咳嗽。苯甲酸在常温下微溶于水,石油醚,但 溶于热水,水溶液呈酸性;易溶于醇、醚、丙酮等有机溶剂,也溶于非挥发 性油。对霉菌,酵母和细菌等有较好的抑制作用,因而对微生物有强烈 毒性,但对人体毒害不明显。 苯甲酸及其钠盐可用作乳胶、牙膏、果酱或其他食品的抑菌剂 防 抑菌剂和防 抑菌剂 腐剂,也可作染色和印色的媒染剂。 腐剂
