化学中常用的物理量——物质的量PPT课件14(3份打包) 鲁科版
合集下载
鲁科版高中化学必修一《化学中常用的物理量――物质的量》认识化学科学PPT(第2课时)

[自学新教材] 阅读教材,回答下列问题: 1.配制50 g质量分数为6%的NaCl溶液,过程如图:
(1)计算:需要NaCl的质量为___3_____g,需要水的质量为 ___4_7____g。
(2)称量:使用托盘天平称取所需的NaCl,放入烧杯中。(称 量时天平___左_____盘加NaCl,____右____盘加砝码)
3.将 4 g NaOH 溶于水配制成 200 mL 溶液,取出 10 mL,
这 10 mL 溶液的物质的量浓度是
()
A.2 mol·L-1
B.1 mol·L-1
C.0.1 mol·L-1
Байду номын сангаас
D.0.5 mol·L-1
4g 解析: c(NaOH)=Vn=40 0g.·2mLol-1=0.5 mol·L-1。溶液具有均
C.100 g 溶液中含有 0.9 mol NaCl
D.100 g 水中含有 0.9 mol NaCl
解析:溶液的质量分数指的是溶质质量与溶液质量的比值,
则质量分数为 0.9%的 NaCl 溶液指的是 100 g 溶液中含有
0.9 g NaCl。 答案:A
2.下列关于1 mol·L-1 K2SO4溶液的说法正确的是 ( ) A.溶液中含有1 mol K2SO4 B.1 mol K2SO4溶于1 L水中 C.溶液中c(K+ )=2 mol·L-1 D.1 L 溶液中含2 mol K+、2 mol SO24- 解析:因溶液的体积不确定,故无法求解 K2SO4 的物质的量, A 错误;水是 1 L,溶液的体积不是 1 L,B 错误;据 K2SO4 的组成可知,K+与 SO24-的个数比是 2∶1,所以溶液中 c(K+ ) =2 mol·L-1,1 L 溶液中含 2 mol K+、1 mol SO24-,C 正确、D 错误。 答案:C
鲁科版化学必修1《化学中常用的物理量-物质的量》课件

02 物质的量简介
物质的量的定义
物质的量
表示一定数目粒子的集合体,符号为n, 是国际单位制中7个基本物理量之一。
物质的量的计算公式为
n=N/NA,其中N表示微粒数目,NA 表示阿伏伽德罗常数。
物质的量的单位
01
摩尔是物质的量的单位,符号为 mol,用于表示物质所含有的微粒 数目。
02
1摩尔的任何物质所包含的该物质 的微粒个数都是相同的,这个数 目被称为阿伏伽德罗常数。
1 2
计算所需物质的质量
通过已知的摩尔质量和所需的物质的量,计算所 需物质的质量。
计算反应物和生成物的物质的量
通过已知的反应方程式和所需的物质的量,计算 反应物和生成物的物质的量。
3
计算反应速率
通过已知的反应时间和反应物的物质的量变化, 计算反应速率。
化学实验中如何计算反应物和生成物的物质的量
根据反应方程式计算
阿伏伽德罗定律是化学中的重要定律之一,它指出在同温、同压下,相同体积的任何气体都含有相同数目的分子。
详细描述
阿伏伽德罗定律是气体化学中的基本定律,它指出在同温、同压下,相同体积的任何气体都含有相同数目的分子, 而不是原子或离子。这个定律是由意大利化学家阿伏伽德罗在19世纪初提出的,因此得名。根据阿伏伽德罗定律, 气体的物质的量、体积和分子数目之间存在一定的关系。
应用,与日常生活息息相关。
物质的量与其他物理量的关系
03
物质的量与其他物理量如质量、体积、浓度等有密切的联系,
是化学计算的基础。
学习目标
01
02
03
04
理解物质的量的概念及其单位 。
掌握物质的量与质量、体积、 浓度等物理量的换算关系。
化学中常用的物理量——物质的量PPT课件 鲁科版

»
• • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • •
第3节 化学中常用的物理量— 物质的量
第一课时
联想· 质疑
水是大家非常熟悉的物质,它是由水分
子构成的。一滴水(约0.05ml)大约含有 1.7万亿个水分子。如果一个个地去数,即 使分秒不停,一个人一生也无法完成这项 工作。那么,怎样才能既科学又方便地知 道一定量水中含有多少个水分子呢?
物质的量是把微观粒子和宏观物质联系起来的一座桥梁
根据组成而定。
交流· 研讨4
(1)1 mol Na2SO4含有 2 mol Na+ mol SO42- 个氧原子 mol Na+ mol SO42-
1
4×6.02×1023 (2) 0.5 mol Na2SO4含有 1 0.5 2×6.02×1023 物质的量 (n) =
个氧原子
物质所含粒子数目 (N)
阿伏加德罗常数 (NA)
(3) 0.1 mol KClO3 和 0.1 mol KClO 中所含粒子
数相等的是 ( A C )
(A) 钾离子 (C) 氯原子 (B)氯离子 (D)氧原子
KClO3 = K+ + ClO3- KClO = K+ + ClO-
小 结
(1) 一个概念及单位:物质的量 摩尔 一个常数和数值:阿伏加德罗常数 6.02×1023mol-1
化学课件《化学中常用的物理量——物质的量》优秀ppt3 鲁科版

m
cB =
nB V
=
M V
m
=
MV
17
m
2. 根据:
cB =
nB V
=
M V
操作
NaCl中含有杂质
容量瓶洗涤后未干燥
烧杯和玻璃棒未洗涤
摇匀后发现凹液面的最低点低 于刻度线,再加水至刻度线 把溶液向容量瓶中转移,溶液洒了
定容时俯视
定容时仰视
溶液未冷却就定容
水的凹液面超过标线部分用滴管吸去
m
=
MV
CB
――[阿萨·赫尔帕斯爵士] 115.旅行的精神在于其自由,完全能够随心所欲地去思考.去感觉.去行动的自由。――[威廉·海兹利特]
116.昨天是张退票的支票,明天是张信用卡,只有今天才是现金;要善加利用。――[凯·里昂] 117.所有的财富都是建立在健康之上。浪费金钱是愚蠢的事,浪费健康则是二级的谋杀罪。――[B·C·福比斯] 118.明知不可而为之的干劲可能会加速走向油尽灯枯的境地,努力挑战自己的极限固然是令人激奋的经验,但适度的休息绝不可少,否则迟早会崩溃。――[迈可·汉默] 119.进步不是一条笔直的过程,而是螺旋形的路径,时而前进,时而折回,停滞后又前进,有失有得,有付出也有收获。――[奥古斯汀] 120.无论那个时代,能量之所以能够带来奇迹,主要源于一股活力,而活力的核心元素乃是意志。无论何处,活力皆是所谓“人格力量”的原动力,也是让一切伟大行动得以持续的力量。――[史迈尔斯] 121.有两种人是没有什么价值可言的:一种人无法做被吩咐去做的事,另一种人只能做被吩咐去做的事。――[C·H·K·寇蒂斯] 122.对于不会利用机会的人而言,机会就像波浪般奔向茫茫的大海,或是成为不会孵化的蛋。――[乔治桑] 123.未来不是固定在那里等你趋近的,而是要靠你创造。未来的路不会静待被发现,而是需要开拓,开路的过程,便同时改变了你和未来。――[约翰·夏尔] 124.一个人的年纪就像他的鞋子的大小那样不重要。如果他对生活的兴趣不受到伤害,如果他很慈悲,如果时间使他成熟而没有了偏见。――[道格拉斯·米尔多] 125.大凡宇宙万物,都存在着正、反两面,所以要养成由后面.里面,甚至是由相反的一面,来观看事物的态度――。[老子]
鲁科版高中化学必修一《化学中常用的物理量——物质的量》认识化学科学PPT(第二课时物质的量浓度)

3.注意事项 (1)进行有关物质的量浓度的计算时要注意 V 表示的是溶液的
体积,不是溶剂的体积,其常用单位为 L,计算时经常需要 与 mL 相互转化。 (2)从一定物质的量浓度的溶液中取出任意体积的溶液,其浓 度不变,但所含溶质的量因体积不同而不同。 (3)结晶水合物溶于水时,结晶水作为溶剂。例如,CuSO4·5H2O 溶于水时,其中的 CuSO4 作为溶质,结晶水与其他蒸馏水 均作为溶剂。
学的重要作用。 2.能运用物质的量、物质的量浓度之间的相互关系进行简
单计算。
第二页,共五十三页。
第三页,共五十三页。
ቤተ መጻሕፍቲ ባይዱ
[自学新教材] 阅读教材,回答下列问题: 如图所示,图 1 为实验室分析纯盐酸试剂瓶上的标签,图 2 为医院某患者血液化验单的一部分。
第四页,共五十三页。
(1)图 1 盐酸标签中“含量(HCl)——35.38%”表示 _1_0_0_g_盐__酸__中__含__有__3_5_._3_8_g__H_C__l _。 (2)图 2 化验单中表示 K、Na 含量的物理量是物_质__的__量__浓__度___,该 物 理 量 表 示单__位__体__积__溶__液__中__所__含__溶__质__B__的__物__质__的__量_______ , 符 号:__c_B__,常用单位有__m_o_l_·L__-_1、__m__o_l_·m__-_3、__m__m__o_l·_L_-_1___。
第十页,共五十三页。
2.下列关于 1 mol·L-1 K2SO4 溶液的说法正确的是
()
A.溶液中含有 1 mol K2SO4 B.1 mol K2SO4 溶于 1 L 水中 C.溶液中 c(K+ )=2 mol·L-1
D.1 L 溶液中含 2 mol K+、2 mol SO24-
化学课件《化学中常用的物理量——物质的量》优秀ppt13鲁科版

√ ⑤标准状况下1mol氧气与氮气的混合气体体积约为22.4L (
)
标准状况下,1mol任何气体的体积约是22.4L
气体摩尔体积
【练习二】N、n、V之间的关系 在标准状况下: 1、44.8L氧气的物质的量是多少? 2mol
2、0.5mol氧气的体积是多少?11.2L
3、33.6L的氮气中含有多少个氮气分子?9.03×1023
在相Fe同的条固件体下,5不6g同固体7.8、6g液/cm体3 的体积7.1不cm3
相N等aCl 固体 58.5g 2.167g/cm3 27.0cm3
H2O 液体 18OH 液体 46g
0.789g/ml
58.3ml
物质
状态
质量
密度 (0℃,101KPa)
体积
――[阿萨·赫尔帕斯爵士] 115.旅行的精神在于其自由,完全能够随心所欲地去思考.去感觉.去行动的自由。――[威廉·海兹利特]
116.昨天是张退票的支票,明天是张信用卡,只有今天才是现金;要善加利用。――[凯·里昂] 117.所有的财富都是建立在健康之上。浪费金钱是愚蠢的事,浪费健康则是二级的谋杀罪。――[B·C·福比斯] 118.明知不可而为之的干劲可能会加速走向油尽灯枯的境地,努力挑战自己的极限固然是令人激奋的经验,但适度的休息绝不可少,否则迟早会崩溃。――[迈可·汉默] 119.进步不是一条笔直的过程,而是螺旋形的路径,时而前进,时而折回,停滞后又前进,有失有得,有付出也有收获。――[奥古斯汀] 120.无论那个时代,能量之所以能够带来奇迹,主要源于一股活力,而活力的核心元素乃是意志。无论何处,活力皆是所谓“人格力量”的原动力,也是让一切伟大行动得以持续的力量。――[史迈尔斯] 121.有两种人是没有什么价值可言的:一种人无法做被吩咐去做的事,另一种人只能做被吩咐去做的事。――[C·H·K·寇蒂斯] 122.对于不会利用机会的人而言,机会就像波浪般奔向茫茫的大海,或是成为不会孵化的蛋。――[乔治桑] 123.未来不是固定在那里等你趋近的,而是要靠你创造。未来的路不会静待被发现,而是需要开拓,开路的过程,便同时改变了你和未来。――[约翰·夏尔] 124.一个人的年纪就像他的鞋子的大小那样不重要。如果他对生活的兴趣不受到伤害,如果他很慈悲,如果时间使他成熟而没有了偏见。――[道格拉斯·米尔多] 125.大凡宇宙万物,都存在着正、反两面,所以要养成由后面.里面,甚至是由相反的一面,来观看事物的态度――。[老子]
)
标准状况下,1mol任何气体的体积约是22.4L
气体摩尔体积
【练习二】N、n、V之间的关系 在标准状况下: 1、44.8L氧气的物质的量是多少? 2mol
2、0.5mol氧气的体积是多少?11.2L
3、33.6L的氮气中含有多少个氮气分子?9.03×1023
在相Fe同的条固件体下,5不6g同固体7.8、6g液/cm体3 的体积7.1不cm3
相N等aCl 固体 58.5g 2.167g/cm3 27.0cm3
H2O 液体 18OH 液体 46g
0.789g/ml
58.3ml
物质
状态
质量
密度 (0℃,101KPa)
体积
――[阿萨·赫尔帕斯爵士] 115.旅行的精神在于其自由,完全能够随心所欲地去思考.去感觉.去行动的自由。――[威廉·海兹利特]
116.昨天是张退票的支票,明天是张信用卡,只有今天才是现金;要善加利用。――[凯·里昂] 117.所有的财富都是建立在健康之上。浪费金钱是愚蠢的事,浪费健康则是二级的谋杀罪。――[B·C·福比斯] 118.明知不可而为之的干劲可能会加速走向油尽灯枯的境地,努力挑战自己的极限固然是令人激奋的经验,但适度的休息绝不可少,否则迟早会崩溃。――[迈可·汉默] 119.进步不是一条笔直的过程,而是螺旋形的路径,时而前进,时而折回,停滞后又前进,有失有得,有付出也有收获。――[奥古斯汀] 120.无论那个时代,能量之所以能够带来奇迹,主要源于一股活力,而活力的核心元素乃是意志。无论何处,活力皆是所谓“人格力量”的原动力,也是让一切伟大行动得以持续的力量。――[史迈尔斯] 121.有两种人是没有什么价值可言的:一种人无法做被吩咐去做的事,另一种人只能做被吩咐去做的事。――[C·H·K·寇蒂斯] 122.对于不会利用机会的人而言,机会就像波浪般奔向茫茫的大海,或是成为不会孵化的蛋。――[乔治桑] 123.未来不是固定在那里等你趋近的,而是要靠你创造。未来的路不会静待被发现,而是需要开拓,开路的过程,便同时改变了你和未来。――[约翰·夏尔] 124.一个人的年纪就像他的鞋子的大小那样不重要。如果他对生活的兴趣不受到伤害,如果他很慈悲,如果时间使他成熟而没有了偏见。――[道格拉斯·米尔多] 125.大凡宇宙万物,都存在着正、反两面,所以要养成由后面.里面,甚至是由相反的一面,来观看事物的态度――。[老子]
物质的量PPT课件34-鲁科版

思考探究
结合前面解决一堆硬币个数的方法模型,尽可能多地列举出解决一定质量的宏观物质中所含粒子数的方法或途径。
序号
方法或途径
1
2
3
4
5
一个一个地数
先称量出1个微观粒子的质量,然后再用宏观物质的质量除以1个微观粒子的质量,计算出微观粒子个数
先称量出由某一数目的微观粒子所组成的微粒集体的质量,然后再用宏观物质的质量除以微粒集体的质量,再乘以微粒集体所含有的微粒数,计算微观粒子个数
解决问题
N=n•NA
物质的量作为桥梁将宏观的质量与微观的粒子数目联系起来
2H2 +O2 = 2H2O
质 量:
4g 32g 36g
微粒物质的量:
2mol 1mol 2mol
化学反应中各物质物质的量的关系
结论:
化学反应方程式中各物质前的系数之比等于各物质在反应过程中的个数比,也是每种物质的物质的量之比。
微观粒子的数目
宏观物质的质量
问题提出
水是大家很熟悉的物质,由水分子组成,那我们怎么可以迅速知道1滴水(0.05ml,0.05g)有多少个水分子?
生活借鉴
假定我们有一堆面值一元的硬币,假定每一硬币的形状、体积、质量是相同的,我们通过哪些方法或途径可以知道这堆硬币的个数?
序号
方法或途径
第 1 课 时物 质 的 量
do
something
2个H2和1个O2在点燃条件下反应生成2个H2O
建立认识物质的新视角
联系生活,类比借鉴
因为米粒小,不便单个计量购买。生活经验:对于越小的东西用集团来表示它们的数量更方便。
单个计量购买
集团计量购买
可乐
米
√
×
结合前面解决一堆硬币个数的方法模型,尽可能多地列举出解决一定质量的宏观物质中所含粒子数的方法或途径。
序号
方法或途径
1
2
3
4
5
一个一个地数
先称量出1个微观粒子的质量,然后再用宏观物质的质量除以1个微观粒子的质量,计算出微观粒子个数
先称量出由某一数目的微观粒子所组成的微粒集体的质量,然后再用宏观物质的质量除以微粒集体的质量,再乘以微粒集体所含有的微粒数,计算微观粒子个数
解决问题
N=n•NA
物质的量作为桥梁将宏观的质量与微观的粒子数目联系起来
2H2 +O2 = 2H2O
质 量:
4g 32g 36g
微粒物质的量:
2mol 1mol 2mol
化学反应中各物质物质的量的关系
结论:
化学反应方程式中各物质前的系数之比等于各物质在反应过程中的个数比,也是每种物质的物质的量之比。
微观粒子的数目
宏观物质的质量
问题提出
水是大家很熟悉的物质,由水分子组成,那我们怎么可以迅速知道1滴水(0.05ml,0.05g)有多少个水分子?
生活借鉴
假定我们有一堆面值一元的硬币,假定每一硬币的形状、体积、质量是相同的,我们通过哪些方法或途径可以知道这堆硬币的个数?
序号
方法或途径
第 1 课 时物 质 的 量
do
something
2个H2和1个O2在点燃条件下反应生成2个H2O
建立认识物质的新视角
联系生活,类比借鉴
因为米粒小,不便单个计量购买。生活经验:对于越小的东西用集团来表示它们的数量更方便。
单个计量购买
集团计量购买
可乐
米
√
×
化学中常用的物理量—物质的量PPT课件 鲁科版

配制方法
配制方法 现欲配制0.5L 0.4 mol/L NaCl溶液, 请你利用实验室中的固体氯化钠试剂, 完成配制任务。 第一步:计算 第二步:称量
称 量
注意事项: (1)使用前要调零 (2)两个托盘上各放一张大小相同的 称量纸 (3)称量时遵循左物右码的原则 (4)用镊子夹取砝码应按照从大到小的顺序 (5)当天平接近平衡时,用左手轻拍右手手腕,使 少量固体慢慢抖入,直至天平平衡为止 (6)称量完毕应将砝码放回盒中,游码归零 思考:称量NaOH固体应如何操作?
配制方法 现欲配制0.5L 0.4 mol/L NaCl溶液, 请你利用实验室中的固体氯化钠试剂, 完成配制任务。
计 算 现欲配制0.5L 0.4 mol/L NaCl溶液, 请你利用实验室中的固体氯化钠试剂, 完成配制任务。
计 算 现欲配制0.5L 0.4 mol/L NaCl溶液, 请你利用实验室中的固体氯化钠试剂, 完成配制任务。 第一步:计算
溶 解
注意事项: 应在烧杯中溶解,不能在容量瓶 中溶解。 因为在容量瓶上标有温度和体积, 这说明容量瓶的体积受温度影响。 而物质的溶解往往伴随着一定的热效应,如果用容量 瓶进行此项操作,会因热胀冷缩使它的体积不准确, 严重时还可能导致容量瓶炸裂。
提问:除了烧杯外还需要哪些仪器?使用中应注意什么? 还需要玻璃棒。 搅拌时沿着一定的方向,玻璃棒不要碰烧杯底和 烧杯壁,不要把玻璃棒放在实验台上,以免弄脏。
符号:cB 单位: mol/L(或mol· L-1)
表达式:
nB cB = V
形成练习
nB cB = V
1. 用 40gNaOH 配成 2L 溶液,其物 0.5 质的量浓度________mol/L 2.58.5gNaCl 配成 500mL 溶液,其 2 物质的量浓度________mol/L
鲁科版化学必修1《化学中常用的物理量-物质的量》ppt课件
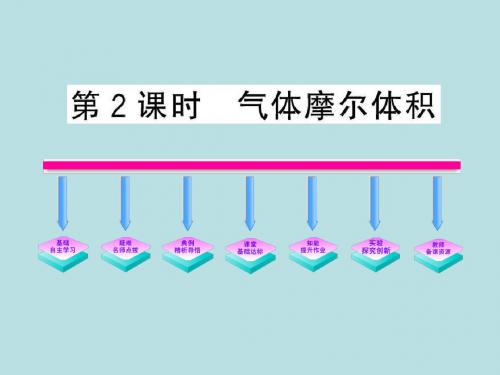
2.在标准状况下,如果1.6 L氧气含n个氧分子,则阿伏 加德罗常数的数值为( )
A.28n
B.14n
C.n/28
D.n/14
1.6 L n , -1 22.4 L mol NA
【解析】选B。由于物质的量=
1.6
则 N A 22.4n mol-1 14n mol-1。
3.同温同压下,等质量的下列气体所占有的体积最大的
体的体积比为______________。
【解析】由 n 据如下表:
m N V 可以计算各量的数 M N A 22.4 L / mol
所以有:(1)n(CO2)>n(H2)>n(N2),m(CO2) >m(N2)>m(H2);
(2)物质的量之比等于分子数之比,所以N(CO2)>
N(H2)>N(N2),所含原子数目最少的是N2; (3)V(CO2)∶V(H2)∶V(N2)=3∶2∶1,体积最大 的是CO2。 答案:(1)CO2 H2 (2)CO2 N2 (3)CO2
是( A.O2 ) B.CH4 C.CO2 D.SO2
【解析】选B。质量相等的气体,摩尔质量越小,其物 质的量越大,同温同压下所占有的体积越大。四个选项
中CH4的摩尔质量最小,所以选B。
4.下列说法正确的是(
)
A.32 g O2占有的体积约为22.4 L B.22.4 L N2含有阿伏加德罗常数个氮分子 C.在标准状况下,22.4 L水的质量约为18 g D.22 g CO2与标准状况下11.2 L HCl含有相同的分子数
V(CO2)∶V(H2)∶V(N2)=3∶2∶1
A (30分钟
组 50分)
一、选择题(本题包括4小题,每小题6分,共24分)
1.2 mol Cl2和2 mol CO2相比较,下列叙述中正确的是
化学中常用的物理量1 鲁科版精选教学PPT课件

与0.0012kg一种碳原子(12C)所含的碳原子 数相等。 科学上把0.0012kg一种碳原子(12C)所含的 碳原子数称为阿伏加德罗常数(NA 单位: mol-1),其近似值为6.02×1023。
物质的量(mol)=
物质所含微粒数 阿伏伽德罗常数
n= N NA
微粒数目之比=物质的量之比
使用摩尔概念时的注意事项
与气体物质的量之间的关系:
气体的体积(L)
气体的物质的量(mol)=
V(L)
摩尔体积(L/mol)
n(mol)= Vm(L/mol)
标准状况下:
V(L) n(mol)= 22.4(L/mol)
V(L) n(mol)=
22.4(L/mol)
使用注意事项:
❖1、对象:气体 ❖2、条件:标准状况(0℃,101kP) ❖3、数据:近似值 ❖【思考】
对分子质量!
2、摩尔质量、物质的量
m
M 与物质的质量之间的关系: n=
〖问题〗 1、1mol不同物质的质量为什么不同? 2、Na和 Na +的摩尔质量是否相同?为什么?
例题1 24.5gH2SO4 物质的量是多少?
解: H2SO4的相对分子质量为98,则 H2SO4的摩尔质量为98g/mol 。
溶质的质量 溶质的质量分数=
溶液的质量
三、物质的量浓度 问题探究 一定体积溶液的组成
探究:配制100mL含0.2mol NaCl的溶液。
实验步骤:
需要溶质质 量为多少?
计算
下 一 步
0.2mol×58.5g/mol =11.7g
需要哪些仪 器? 容量瓶上有 哪些标识?
如何洗涤仪 器?
准备 仪器
下 一 步
物质的量(mol)=
物质所含微粒数 阿伏伽德罗常数
n= N NA
微粒数目之比=物质的量之比
使用摩尔概念时的注意事项
与气体物质的量之间的关系:
气体的体积(L)
气体的物质的量(mol)=
V(L)
摩尔体积(L/mol)
n(mol)= Vm(L/mol)
标准状况下:
V(L) n(mol)= 22.4(L/mol)
V(L) n(mol)=
22.4(L/mol)
使用注意事项:
❖1、对象:气体 ❖2、条件:标准状况(0℃,101kP) ❖3、数据:近似值 ❖【思考】
对分子质量!
2、摩尔质量、物质的量
m
M 与物质的质量之间的关系: n=
〖问题〗 1、1mol不同物质的质量为什么不同? 2、Na和 Na +的摩尔质量是否相同?为什么?
例题1 24.5gH2SO4 物质的量是多少?
解: H2SO4的相对分子质量为98,则 H2SO4的摩尔质量为98g/mol 。
溶质的质量 溶质的质量分数=
溶液的质量
三、物质的量浓度 问题探究 一定体积溶液的组成
探究:配制100mL含0.2mol NaCl的溶液。
实验步骤:
需要溶质质 量为多少?
计算
下 一 步
0.2mol×58.5g/mol =11.7g
需要哪些仪 器? 容量瓶上有 哪些标识?
如何洗涤仪 器?
准备 仪器
下 一 步
《化学中常用的物理量——物质的量》认识化学科学(第二课时物质的量浓度)-鲁科版化学必修一PPT课件

符号:cB,单位:mol·L-1、mol·m-3、mmol·L-1。 2.关系:溶质 B 的物质的量(nB)、溶液的体积(V)、溶质 B 的
物质的量浓度(cB)之间的关系:cB=nVB。
3.注意事项 (1)进行有关物质的量浓度的计算时要注意 V 表示的是溶液的
体积,不是溶剂的体积,其常用单位为 L,计算时经常需要 与 mL 相互转化。 (2)从一定物质的量浓度的溶液中取出任意体积的溶液,其浓 度不变,但所含溶质的量因体积不同而不同。 (3)结晶水合物溶于水时,结晶水作为溶剂。例如,CuSO4·5H2O 溶于水时,其中的 CuSO4 作为溶质,结晶水与其他蒸馏水 均作为溶剂。
第3节 化学中常用的物理量——物质的量
第二课时物质的量浓度
[新课程标准是什么] 1.了解物质的量浓度的含义和应用,体会定量研究对化学科
学的重要作用。 2.能运用物质的量、物质的量浓度之间的相互关系进行简
单计算。
[自学新教材] 阅读教材,回答下列问题:
如图所示,图 1 为实验室分析纯盐酸试剂瓶上的标签,图 2
(3)量取:用___5_0_m__L_(填“10 mL”“50 mL”或“100 mL”)的量筒 量取所需体积的水,量取时视线要跟量筒内 _液__体__的__凹__液__面__最__低__处____保持水平,并将其沿烧杯内壁倒入 盛有 NaCl 的烧杯中。
C.100 g 溶液中含有 0.9 mol NaCl
D.100 g 水中含有 0.9 mol NaCl
解析:溶液的质量分数指的是溶质质量与溶液质量的比值,
则质量分数为 0.9%的 NaCl 溶液指的是 100 g 溶液中含有
0.9 g NaCl。 答案:A
2.下列关于 1 mol·L-1 K2SO4 溶液的说法正确的是 ()
物质的量浓度(cB)之间的关系:cB=nVB。
3.注意事项 (1)进行有关物质的量浓度的计算时要注意 V 表示的是溶液的
体积,不是溶剂的体积,其常用单位为 L,计算时经常需要 与 mL 相互转化。 (2)从一定物质的量浓度的溶液中取出任意体积的溶液,其浓 度不变,但所含溶质的量因体积不同而不同。 (3)结晶水合物溶于水时,结晶水作为溶剂。例如,CuSO4·5H2O 溶于水时,其中的 CuSO4 作为溶质,结晶水与其他蒸馏水 均作为溶剂。
第3节 化学中常用的物理量——物质的量
第二课时物质的量浓度
[新课程标准是什么] 1.了解物质的量浓度的含义和应用,体会定量研究对化学科
学的重要作用。 2.能运用物质的量、物质的量浓度之间的相互关系进行简
单计算。
[自学新教材] 阅读教材,回答下列问题:
如图所示,图 1 为实验室分析纯盐酸试剂瓶上的标签,图 2
(3)量取:用___5_0_m__L_(填“10 mL”“50 mL”或“100 mL”)的量筒 量取所需体积的水,量取时视线要跟量筒内 _液__体__的__凹__液__面__最__低__处____保持水平,并将其沿烧杯内壁倒入 盛有 NaCl 的烧杯中。
C.100 g 溶液中含有 0.9 mol NaCl
D.100 g 水中含有 0.9 mol NaCl
解析:溶液的质量分数指的是溶质质量与溶液质量的比值,
则质量分数为 0.9%的 NaCl 溶液指的是 100 g 溶液中含有
0.9 g NaCl。 答案:A
2.下列关于 1 mol·L-1 K2SO4 溶液的说法正确的是 ()
优秀课件鲁科版高一化学必修一 1.3化学中常用的物理量——物质的量 (共24张PPT)

化学中常用的物理量——物质的量
归纳公式: 之间的关系。 N n= NA
阿伏加德罗常数
Байду номын сангаас
物质的量(n)、阿伏加德罗常数(NA)、微粒数(N)
N=n×NA
规律:物质的粒子数之比 = 物质的量之比
一、物质的量的单位——摩尔
化学中常用的物理量——物质的量
阿伏加德罗常数
例1.在0.5 mol O2中含有的氧原子数目是多少?
化学中常用的物理量——物质的量
2、物质的量的单位 基本单位: 符号: mol 摩尔(简称摩)
“摩尔”起源于希腊文,原意为“堆量”,一个粒子无 法称量,“一堆”大量的粒子当然可以称量。
化学中常用的物理量——物质的量
1 打 12个
铅笔 筷子 别针
宏观物质
1 双 2支 1 盒 100枚
1 令 500张
鲁科版化学 · 必修 1
1.3化学中常用的物理量——物质的量
化学中常用的物理量——物质的量
一、物质的量及其单位——摩尔
化学中常用的物理量——物质的量
有哪些方法可以测出一筐质量体积形状都相同的一元硬币的数目是 多少? 太繁了! 1、可以数它的数目 2、如果知道每100个硬币的质量是一定 的(m1),利用这个关系也可以求出100×m总/m1
解:每个O2分子中含有两个氧原子,氧原子数为:
N(O) = n(O2)×2 × NA
= 0.5 mol×2× 6.02 ×1023mol-1 = 6.02 × 1023 答: 0.5 mol O2的氧原子数为6.02 × 1023个。 注意解题格式:先公式、后数字;标明每一个量 的所属;带单位计算。
经过大量的科学实验证明:这种原子性 质很稳定,0.012kg(12g) 12C 所含有的原 子数是恒定的常数,叫阿伏加德罗常数 (NA)
《化学中常用的物理量——物质的量》认识化学科学(第3课时物质的量浓度)-鲁科版化学必修一PPT课件

栏目 导引
第1章 认识化学科学
2.(2019·宿迁高一期末)下列溶液中 Cl-浓度最小的是( ) A.25 mL 1 mol·L-1 AlCl3 溶液 B.30 mL 3 mol·L-1 KCl 溶液 C.20 mL 2 mol·L-1 MgCl2 溶液 D.30 mL 2 mol·L-1 NaCl 溶液
栏目 导引
第1章 认识化学科学
4.(2019·抚顺省重点高中协作校高一期末)某溶液中只含有四
种离子,已知其中三种离子 Na+、Mg2+、NO-3 的物质的量浓
度分别是 2 mol/L、1 mol/L、1 mol/L,则溶液中另一离子及
其物质的量浓度是( )
A.CO23- 1.5 mol/L C.OH- 3 mol/L
栏目 导引
第1章 认识化学科学
表达式 cB=nVB中,V 表示溶液的体积,不是溶剂的体积。
栏目 导引
第1章 认识化学科学
有关物质的量浓度的计算 1.根据定义式计算
栏目 导引
第1章 认识化学科学
2.物质的量浓度与溶质质量分数的关系
(1)推导过程
设溶液体积为 1 L,溶液密度为 ρ g·mL-1,溶质的质量分数
栏目 导引
第1章 认识化学科学
解析:选 D。A.25 mL 1 mol·L-1 AlCl3 溶液中 c(Cl-)=3c(AlCl3) =1 mol·L-1×3=3 mol·L-1; B.30 mL 3 mol·L-1 KCl 溶液中 c(Cl-)=c(KCl)=3 mol·L-1; C.20 mL 2 mol·L-1 MgCl2 溶液中 c(Cl-)=2c(MgCl2)= 2mol·L-1×2=4 mol·L-1; D.30 mL 2 mol·L-1 NaCl 溶液中 c(Cl-)=c(NaCl) =2 mol·L-1; 所以氯离子浓度最小的是 2 mol·L-1。
第1章 认识化学科学
2.(2019·宿迁高一期末)下列溶液中 Cl-浓度最小的是( ) A.25 mL 1 mol·L-1 AlCl3 溶液 B.30 mL 3 mol·L-1 KCl 溶液 C.20 mL 2 mol·L-1 MgCl2 溶液 D.30 mL 2 mol·L-1 NaCl 溶液
栏目 导引
第1章 认识化学科学
4.(2019·抚顺省重点高中协作校高一期末)某溶液中只含有四
种离子,已知其中三种离子 Na+、Mg2+、NO-3 的物质的量浓
度分别是 2 mol/L、1 mol/L、1 mol/L,则溶液中另一离子及
其物质的量浓度是( )
A.CO23- 1.5 mol/L C.OH- 3 mol/L
栏目 导引
第1章 认识化学科学
表达式 cB=nVB中,V 表示溶液的体积,不是溶剂的体积。
栏目 导引
第1章 认识化学科学
有关物质的量浓度的计算 1.根据定义式计算
栏目 导引
第1章 认识化学科学
2.物质的量浓度与溶质质量分数的关系
(1)推导过程
设溶液体积为 1 L,溶液密度为 ρ g·mL-1,溶质的质量分数
栏目 导引
第1章 认识化学科学
解析:选 D。A.25 mL 1 mol·L-1 AlCl3 溶液中 c(Cl-)=3c(AlCl3) =1 mol·L-1×3=3 mol·L-1; B.30 mL 3 mol·L-1 KCl 溶液中 c(Cl-)=c(KCl)=3 mol·L-1; C.20 mL 2 mol·L-1 MgCl2 溶液中 c(Cl-)=2c(MgCl2)= 2mol·L-1×2=4 mol·L-1; D.30 mL 2 mol·L-1 NaCl 溶液中 c(Cl-)=c(NaCl) =2 mol·L-1; 所以氯离子浓度最小的是 2 mol·L-1。
鲁科化学必修一第1章3、化学中常用的物理量——物质的量第1课时物质的量(共15张PPT)

3. 不因幸运而固步自封,不因厄运而一蹶不振。真正的强者,善于从顺境中找到阴影,从逆境中找到光亮,时时校准自己前进的目标。易卜 生
4、办事贵有定见,不贵有成见,定见者,在我之知识学问,不与世为推移者也。 27、人生只有三天,活在昨天的人迷惑,活在明天的人等待,活在今天的人最踏实。 11. 有志者自有千方百计,无志者只感千难万难。 29、只有不断找寻机会的人才会及时把握机会。 13、力争上游,龙腾虎跃朝气蓬勃;壮志凌云,你追我赶誓夺第一。 43. 如果你希望成功,以恒心为良友,以经验为参谋,以小心为兄弟,以希望为哨兵。 7、少玩游戏,这不是韩国,你打不出房子车子还有资本。可以有爱好,但要把握尺度,少玩农场,牧场,斗地主等一些高度吸引人思想的晋 级游戏,也许你的级别很高,但不代表你有多么成功,反而会影响和占据你成功的时间。
迁移·应用(p23)
对于气体:n = V/ Vm
概括·整合
适用于任 何物质
只适用于 STP时的气
体
n= N NA
n= m M
V
n=
Vm
任何物质所 含的微粒数
任何物质 的质量
气体物质在 STP时的体积
在标准状况下,CO和CO2的混合气体共39.2L, 质量为 61g,求两种气体的物质的量和各自的体积。
7.2 cm3
NaCl
58.5 58.5g
27.0 cm3
H2O
18
C2H5OH
46
H2
2
O2
32
CO2
44
18g
46g
2g
22.4 L
32g 22.4 L
44g 22.3 L
18.0 cm3 58.3 cm3
24.0 L 24.0 L 23.9 L
物质的量 鲁科版精选教学PPT课件
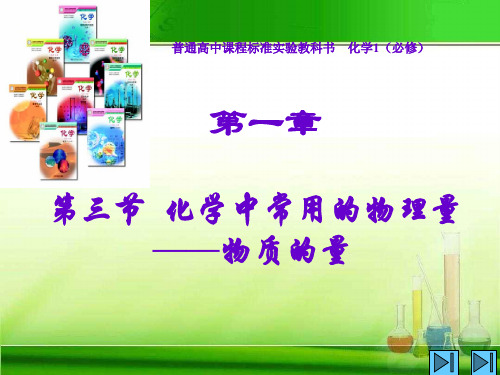
2、物质的量的单位:摩尔,符号mol
1 mol 任何粒子所含有的粒子数同0.012kg12C所含碳原子数目相等
3、阿伏加德罗常数(NA):
0.012kg 12C所含碳原子数目为6.02×1023 , 6.02×1023 mol--1 称为阿伏加德罗常数。
这样规定有什么好处?
① NA个微观粒子所形成的微粒集体的质量在几克 到几百克 之间,质量大小适宜,可以称量,便于换算。
作为标准来衡量其他微粒集体所含微粒数目多 少的物理量
使用摩尔概念时的注意事项
⑴适用范围:微观粒子或它们的特定组合 ⑵使用准则:必须指明微粒符号或化学式 ⑶大: 1mol物质所含微粒数巨大 ⑷小: 摩尔计量的是肉眼无法看到的微观粒子 ⑸广: 应用范围极广,是联系微粒个体与微粒集体、不可称
量的反应微粒与可称量的宏观物质的桥梁。
m
n=
M
只适用于 STP时的气
体
V
n=
Vm
任何物质所 含的微粒数
任何物质 的质量
气体物质在 STP时的体积
问题探究 一定体积溶液的组成
探究:配制0.1 L NaCl溶液,其中溶质的物质的 量为0.04 mol。
实验步骤: 基本步骤: 算—称—溶—转—定—装
计算
准备仪器
称量
溶解
转移
定容摇匀
装瓶贴签
问题探究
⑵ 1mol H2的体积约是22.4L
(×)
⑶ 1mol CO2和1mol CO所含的分子数和体积都相同(×)
⑷ 1mol O2在20℃时的体积一定大于22.4L (×)
⑸在标准状况下,0.5mol N2和1mol O2 的混合气体的
体积约是33.6L
(√ )
1 mol 任何粒子所含有的粒子数同0.012kg12C所含碳原子数目相等
3、阿伏加德罗常数(NA):
0.012kg 12C所含碳原子数目为6.02×1023 , 6.02×1023 mol--1 称为阿伏加德罗常数。
这样规定有什么好处?
① NA个微观粒子所形成的微粒集体的质量在几克 到几百克 之间,质量大小适宜,可以称量,便于换算。
作为标准来衡量其他微粒集体所含微粒数目多 少的物理量
使用摩尔概念时的注意事项
⑴适用范围:微观粒子或它们的特定组合 ⑵使用准则:必须指明微粒符号或化学式 ⑶大: 1mol物质所含微粒数巨大 ⑷小: 摩尔计量的是肉眼无法看到的微观粒子 ⑸广: 应用范围极广,是联系微粒个体与微粒集体、不可称
量的反应微粒与可称量的宏观物质的桥梁。
m
n=
M
只适用于 STP时的气
体
V
n=
Vm
任何物质所 含的微粒数
任何物质 的质量
气体物质在 STP时的体积
问题探究 一定体积溶液的组成
探究:配制0.1 L NaCl溶液,其中溶质的物质的 量为0.04 mol。
实验步骤: 基本步骤: 算—称—溶—转—定—装
计算
准备仪器
称量
溶解
转移
定容摇匀
装瓶贴签
问题探究
⑵ 1mol H2的体积约是22.4L
(×)
⑶ 1mol CO2和1mol CO所含的分子数和体积都相同(×)
⑷ 1mol O2在20℃时的体积一定大于22.4L (×)
⑸在标准状况下,0.5mol N2和1mol O2 的混合气体的
体积约是33.6L
(√ )
相关主题
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
上一页 下一页
课堂练习
1.(1)在同温同压下,决定气体体积大小的因素是气体 分子数目的多少。( )
提示:√ 在同温同压下,任何气体分子间的距离几
乎相等,故决定气体体积大小的因素是气体分子数目 的多少。
上一页 下一页
课堂练习
(2)在常温常压下,0.5 mol N2的体积约为11.2 L。(
)
提示:× 常温常压下,不是标准状况,故0.5 mol
图示:
相同温度压强下,气体分子间平均距离相
同,体积基本相同。
上一页 下一页
新知学习
气体摩尔体积
定义:
在一定温度和压强下,单位物质的量的气 体所占有的体积。
气体
22.4L (标准状况)
上一页 下一页
新知学习
气体摩尔体积 n =V/ Vm L/mol (L· mol-1) 和 m3/mol (m3· mol-1) Vm =V/n V=n•Vm
上一页 下一页
新知学习
换算关系
N
÷NA ×NA
n
× ÷
上一页 下一页
新知学习
换算关系 计算填空: 1.标准状况下,0.5molH2占有的体积都约 为 11.2L 2.标准状况下,11.2LN2中含有N2的分子
23 3.01 × 10 数为
上一页 下一页
新知学习
阿伏加德罗定律 定义:同温、同压下,相同体积的任何气
一、我们因梦想而伟大,所有的成功者都是大梦想家:在冬夜的火堆旁,在阴天的雨雾中,梦想着未来。有些人让梦想悄然绝灭,有些人则细心培育维护,直到它安然度过困境,迎来光明和希望,而光明和希望 总是降临在那些真心相信梦想一定会成真的人身上。——威尔逊
二、梦想无论怎样模糊,总潜伏在我们心底,使我们的心境永远得不到宁静,直到这些梦想成为事实才止;像种子在地下一样,一定要萌芽滋长,伸出地面来,寻找阳光。——林语堂 三、多少事,从来急;天地转,光阴迫。一万年太久,只争朝夕。——毛泽东 四、拥有梦想的人是值得尊敬的,也让人羡慕。当大多数人碌碌而为为现实奔忙的时候,坚持下去,不用害怕与众不同,你该有怎么样的人生,是该你亲自去撰写的。加油!让我们一起捍卫最初的梦想。——柳岩 五、一个人要实现自己的梦想,最重要的是要具备以下两个条件:勇气和行动。——俞敏洪 六、将相本无主,男儿当自强。——汪洙 七、我们活着不能与草木同腐,不能醉生梦死,枉度人生,要有所作为。——方志敏 八、当我真心在追寻著我的梦想时,每一天都是缤纷的,因为我知道每一个小时都是在实现梦想的一部分。——佚名 九、很多时候,我们富了口袋,但穷了脑袋;我们有梦想,但缺少了思想。——佚名 十、你想成为幸福的人吗?但愿你首先学会吃得起苦。——屠格涅夫 十一、一个人的理想越崇高,生活越纯洁。——伏尼契 十二、世之初应该立即抓住第一次的战斗机会。——司汤达 十三、哪里有天才,我是把别人喝咖啡的工夫都用在工作上的。──鲁迅 十四、信仰,是人们所必须的。什麽也不信的人不会有幸福。——雨果 十五、对一个有毅力的人来说,无事不可为。——海伍德 十六、有梦者事竟成。——沃特 十七、梦想只要能持久,就能成为现实。我们不就是生活在梦想中的吗?——丁尼生 十八、梦想无论怎样模糊,总潜伏在我们心底,使我们的心境永远得不到宁静,直到这些梦想成为事实。——林语堂 十九、要想成就伟业,除了梦想,必须行动。——佚名 二十、忘掉今天的人将被明天忘掉。──歌德 二十一、梦境总是现实的反面。——伟格利 二十二、世界上最快乐的事,莫过于为理想而奋斗。——苏格拉底 二十三、“梦想”是一个多么“虚无缥缈不切实际”的词啊。在很多人的眼里,梦想只是白日做梦,可是,如果你不曾真切的拥有过梦想,你就不会理解梦想的珍贵。——柳岩 二十四、生命是以时间为单位的,浪费别人的时间等于谋财害命,浪费自己的时间,等于慢性自杀。——鲁迅 二十五、梦是心灵的思想,是我们的秘密真情。——杜鲁门· 卡波特 二十六、坚强的信念能赢得强者的心,并使他们变得更坚强。——白哲特 二十七、既然我已经踏上这条道路,那么,任何东西都不应妨碍我沿着这条路走下去。——康德 二十八、青少年是一个美好而又是一去不可再得的时期,是将来一切光明和幸福的开端。——加里宁 二十九、梦想家命长,实干家寿短。——约· 奥赖利 三十、青年时准备好材料,想造一座通向月亮的桥,或者在地上造二所宫殿或庙宇。活到中年,终于决定搭一个棚。——佚名 三十一、在这个并非尽善尽美的世界上,勤奋会得到报偿,而游手好闲则要受到惩罚。——毛姆 三十二、在科学上没有平坦的大道,只有不畏劳苦,沿着陡峭山路攀登的人,才有希望达到光辉的顶点。——马克思 三十三、在劳力上劳心,是一切发明之母。事事在劳力上劳心,变可得事物之真理。——陶行知 三十四、一年之计在于春,一日之计在于晨。——萧绛 三十五、没有一颗心会因为追求梦想而受伤,当你真心想要某样东西时,整个宇宙都会联合起来帮你完成。——佚名 三十六、梦想不抛弃苦心追求的人,只要不停止追求,你们会沐浴在梦想的光辉之中。——佚名 三十七、一块砖没有什么用,一堆砖也没有什么用,如果你心中没有一个造房子的梦想,拥有天下所有的砖头也是一堆废物;但如果只有造房子的梦想,而没有砖头,梦想也没法实现。——俞敏洪 三十八、如意算盘,不一定符合事实。——奥地利 三十九、志向不过是记忆的奴隶,生气勃勃地降生,但却很难成长。——莎士比亚 四十、如果失去梦想,人类将会怎样?——热豆腐 四十一、无论哪个时代,青年的特点总是怀抱着各种理想和幻想。这并不是什么毛病,而是一种宝贵的品质。——佚名 四十二、梦想绝不是梦,两者之间的差别通常都有一段非常值得人们深思的距离。——古龙 四十三、梦想家的缺点是害怕命运。——斯· 菲利普斯 四十四、从工作里爱了生命,就是通彻了生命最深的秘密。——纪伯伦 四十五、穷人并不是指身无分文的人,而是指没有梦想的人。——佚名 四十六、不要怀有渺小的梦想,它们无法打动人心。——歌德 四十七、人生最苦痛的是梦醒了无路可走。做梦的人是幸福的;倘没有看出可以走的路,最要紧的是不要去惊醒他。——鲁迅 四十八、浪费别人的时间是谋财害命,浪费自己的时间是慢性自杀。──列宁 四十九、意志薄弱的人不可能真诚。——拉罗什科 五十、梦想绝不是梦,两者之间的差别通常都有一段非常值得人们深思的距离。——古龙 五十一、得其志,虽死犹生,不得其志,虽生犹死。——无名氏 五十二、所虑时光疾,常怀紧迫情,蹒跚行步慢,落后最宜鞭。——董必武 五十三、梦想只要能持久,就能成为现实。我们不就是生活在梦想中的吗?——丁尼生 五十四、很难说什么是办不到的事情,因为昨天的梦想,可以是今天的希望,并且还可以成为明天的现实。——佚名 五十五、要用你的梦想引领你的一生,要用感恩真诚助人圆梦的心态引领你的一生,要用执著无惧乐观的态度来引领你的人生。——李开复 五十六、人类也需要梦想者,这种人醉心于一种事业的大公无私的发展,因而不能注意自身的物质利益。——居里夫人 五十七、一个人的理想越崇高,生活越纯洁。——伏尼契 五十八、梦想一旦被付诸行动,就会变得神圣。——阿· 安· 普罗克特 五十九、一个人追求的目标越高,他的才力就发展得越快,对社会就越有益。——高尔基 六十、青春是人生最快乐的时光,但这种快乐往往完全是因为它充满着希望,而不是因为得到了什么或逃避了什么。——佚名 六十一、生命里最重要的事情是要有个远大的目标,并借助才能与坚毅来完成它。——歌德 六十二、没有大胆的猜测就作不出伟大的发现。──牛顿 六十三、梦想,是一个目标,是让自己活下去的原动力,是让自己开心的原因。——佚名 六十四、人生太短,要干的事太多,我要争分夺秒。——爱迪生 六十五、一路上我都会发现从未想像过的东西,如果当初我没有勇气去尝试看来几乎不可能的事,如今我就还只是个牧羊人而已。——《牧羊少年的奇幻之旅》 六十六、一个人越敢于担当大任,他的意气就是越风发。——班生 六十七、贫穷是一切艺术职业的母亲。——托里安诺 六十八、莫道桑榆晚,为霞尚满天。——刘禹锡 六十九、一切活动家都是梦想家。——詹· 哈尼克 七十、如果一个人不知道他要驶向哪个码头,那么任何风都不会是顺风。——小塞涅卡 七十一、人性最可怜的就是:我们总是梦想着天边的一座奇妙的玫瑰园,而不去欣赏今天就开在我们窗口的玫瑰。——佚名 七十二、一个人如果已经把自己完全投入于权力和仇恨中,你怎么能期望他还有梦?——古龙 七十三、一个人有钱没钱不一定,但如果这个人没有了梦想,这个人穷定了。——佚名 七十四、平凡朴实的梦想,我们用那唯一的坚持信念去支撑那梦想。——佚名 七十五、最初所拥有的只是梦想,以及毫无根据的自信而已。但是,所有的一切就从这里出发。——孙正义 七十六、看见一个年轻人丧失了美好的希望和理想,看见那块他透过它来观察人们行为和感情的粉红色轻纱在他面前撕掉,那真是伤心啊!——莱蒙托夫 七十七、努力向上吧,星星就躲藏在你的灵魂深处;做一个悠远的梦吧,每个梦想都会超越你的目标。——佚名 七十八、正如心愿能够激发梦想,梦想也能够激发心愿。——佚名 七十九、梦想一旦被付诸行动,就会变得神圣。——阿· 安· 普罗克特 八十、对于学者获得的成就,是恭维还是挑战?我需要的是后者,因为前者只能使人陶醉而后者却是鞭策。——巴斯德 八十一、冬天已经到来,春天还会远吗?——雪莱 八十二、一个人想要成功,想要改变命运,有梦想是重要的。……我觉得每个人都应该心中有梦,有胸怀祖国的大志向,找到自己的梦想,认准了就去做,不跟风不动摇。同时,我们不仅仅要自己有梦想,你还应该用自己的梦想去感染和影响别人,因为成功者一定是用自己的梦想去点燃别人的梦想,是时刻播种梦想的人。——李彦宏 八十三、梦想是人们与生俱来的重要宝物之一,它等待你的珍视和实践。——邹金宏 八十四、心存希望,幸福就会降临你;心存梦想,机遇就会笼罩你。——佚名 八十五、第一,有梦想。一个人最富有的时候是有梦想,有梦想是最开心的。第二,要坚持自己的梦想。有梦想的人非常多,但能够坚持的人却非常少。阿里巴巴能够成功的原因是因为我们坚持
体积大小的影响因素 通过计算比较1mol下列各物质的体积(V):
(公式:V = m / = n· M / ) 物质 O2 H2 物质 Fe Al 状态 g g 状态 s s
/g· L-1
1.429 0.0899
课堂练习
1.(1)在同温同压下,决定气体体积大小的因素是气体 分子数目的多少。( )
提示:√ 在同温同压下,任何气体分子间的距离几
乎相等,故决定气体体积大小的因素是气体分子数目 的多少。
上一页 下一页
课堂练习
(2)在常温常压下,0.5 mol N2的体积约为11.2 L。(
)
提示:× 常温常压下,不是标准状况,故0.5 mol
图示:
相同温度压强下,气体分子间平均距离相
同,体积基本相同。
上一页 下一页
新知学习
气体摩尔体积
定义:
在一定温度和压强下,单位物质的量的气 体所占有的体积。
气体
22.4L (标准状况)
上一页 下一页
新知学习
气体摩尔体积 n =V/ Vm L/mol (L· mol-1) 和 m3/mol (m3· mol-1) Vm =V/n V=n•Vm
上一页 下一页
新知学习
换算关系
N
÷NA ×NA
n
× ÷
上一页 下一页
新知学习
换算关系 计算填空: 1.标准状况下,0.5molH2占有的体积都约 为 11.2L 2.标准状况下,11.2LN2中含有N2的分子
23 3.01 × 10 数为
上一页 下一页
新知学习
阿伏加德罗定律 定义:同温、同压下,相同体积的任何气
一、我们因梦想而伟大,所有的成功者都是大梦想家:在冬夜的火堆旁,在阴天的雨雾中,梦想着未来。有些人让梦想悄然绝灭,有些人则细心培育维护,直到它安然度过困境,迎来光明和希望,而光明和希望 总是降临在那些真心相信梦想一定会成真的人身上。——威尔逊
二、梦想无论怎样模糊,总潜伏在我们心底,使我们的心境永远得不到宁静,直到这些梦想成为事实才止;像种子在地下一样,一定要萌芽滋长,伸出地面来,寻找阳光。——林语堂 三、多少事,从来急;天地转,光阴迫。一万年太久,只争朝夕。——毛泽东 四、拥有梦想的人是值得尊敬的,也让人羡慕。当大多数人碌碌而为为现实奔忙的时候,坚持下去,不用害怕与众不同,你该有怎么样的人生,是该你亲自去撰写的。加油!让我们一起捍卫最初的梦想。——柳岩 五、一个人要实现自己的梦想,最重要的是要具备以下两个条件:勇气和行动。——俞敏洪 六、将相本无主,男儿当自强。——汪洙 七、我们活着不能与草木同腐,不能醉生梦死,枉度人生,要有所作为。——方志敏 八、当我真心在追寻著我的梦想时,每一天都是缤纷的,因为我知道每一个小时都是在实现梦想的一部分。——佚名 九、很多时候,我们富了口袋,但穷了脑袋;我们有梦想,但缺少了思想。——佚名 十、你想成为幸福的人吗?但愿你首先学会吃得起苦。——屠格涅夫 十一、一个人的理想越崇高,生活越纯洁。——伏尼契 十二、世之初应该立即抓住第一次的战斗机会。——司汤达 十三、哪里有天才,我是把别人喝咖啡的工夫都用在工作上的。──鲁迅 十四、信仰,是人们所必须的。什麽也不信的人不会有幸福。——雨果 十五、对一个有毅力的人来说,无事不可为。——海伍德 十六、有梦者事竟成。——沃特 十七、梦想只要能持久,就能成为现实。我们不就是生活在梦想中的吗?——丁尼生 十八、梦想无论怎样模糊,总潜伏在我们心底,使我们的心境永远得不到宁静,直到这些梦想成为事实。——林语堂 十九、要想成就伟业,除了梦想,必须行动。——佚名 二十、忘掉今天的人将被明天忘掉。──歌德 二十一、梦境总是现实的反面。——伟格利 二十二、世界上最快乐的事,莫过于为理想而奋斗。——苏格拉底 二十三、“梦想”是一个多么“虚无缥缈不切实际”的词啊。在很多人的眼里,梦想只是白日做梦,可是,如果你不曾真切的拥有过梦想,你就不会理解梦想的珍贵。——柳岩 二十四、生命是以时间为单位的,浪费别人的时间等于谋财害命,浪费自己的时间,等于慢性自杀。——鲁迅 二十五、梦是心灵的思想,是我们的秘密真情。——杜鲁门· 卡波特 二十六、坚强的信念能赢得强者的心,并使他们变得更坚强。——白哲特 二十七、既然我已经踏上这条道路,那么,任何东西都不应妨碍我沿着这条路走下去。——康德 二十八、青少年是一个美好而又是一去不可再得的时期,是将来一切光明和幸福的开端。——加里宁 二十九、梦想家命长,实干家寿短。——约· 奥赖利 三十、青年时准备好材料,想造一座通向月亮的桥,或者在地上造二所宫殿或庙宇。活到中年,终于决定搭一个棚。——佚名 三十一、在这个并非尽善尽美的世界上,勤奋会得到报偿,而游手好闲则要受到惩罚。——毛姆 三十二、在科学上没有平坦的大道,只有不畏劳苦,沿着陡峭山路攀登的人,才有希望达到光辉的顶点。——马克思 三十三、在劳力上劳心,是一切发明之母。事事在劳力上劳心,变可得事物之真理。——陶行知 三十四、一年之计在于春,一日之计在于晨。——萧绛 三十五、没有一颗心会因为追求梦想而受伤,当你真心想要某样东西时,整个宇宙都会联合起来帮你完成。——佚名 三十六、梦想不抛弃苦心追求的人,只要不停止追求,你们会沐浴在梦想的光辉之中。——佚名 三十七、一块砖没有什么用,一堆砖也没有什么用,如果你心中没有一个造房子的梦想,拥有天下所有的砖头也是一堆废物;但如果只有造房子的梦想,而没有砖头,梦想也没法实现。——俞敏洪 三十八、如意算盘,不一定符合事实。——奥地利 三十九、志向不过是记忆的奴隶,生气勃勃地降生,但却很难成长。——莎士比亚 四十、如果失去梦想,人类将会怎样?——热豆腐 四十一、无论哪个时代,青年的特点总是怀抱着各种理想和幻想。这并不是什么毛病,而是一种宝贵的品质。——佚名 四十二、梦想绝不是梦,两者之间的差别通常都有一段非常值得人们深思的距离。——古龙 四十三、梦想家的缺点是害怕命运。——斯· 菲利普斯 四十四、从工作里爱了生命,就是通彻了生命最深的秘密。——纪伯伦 四十五、穷人并不是指身无分文的人,而是指没有梦想的人。——佚名 四十六、不要怀有渺小的梦想,它们无法打动人心。——歌德 四十七、人生最苦痛的是梦醒了无路可走。做梦的人是幸福的;倘没有看出可以走的路,最要紧的是不要去惊醒他。——鲁迅 四十八、浪费别人的时间是谋财害命,浪费自己的时间是慢性自杀。──列宁 四十九、意志薄弱的人不可能真诚。——拉罗什科 五十、梦想绝不是梦,两者之间的差别通常都有一段非常值得人们深思的距离。——古龙 五十一、得其志,虽死犹生,不得其志,虽生犹死。——无名氏 五十二、所虑时光疾,常怀紧迫情,蹒跚行步慢,落后最宜鞭。——董必武 五十三、梦想只要能持久,就能成为现实。我们不就是生活在梦想中的吗?——丁尼生 五十四、很难说什么是办不到的事情,因为昨天的梦想,可以是今天的希望,并且还可以成为明天的现实。——佚名 五十五、要用你的梦想引领你的一生,要用感恩真诚助人圆梦的心态引领你的一生,要用执著无惧乐观的态度来引领你的人生。——李开复 五十六、人类也需要梦想者,这种人醉心于一种事业的大公无私的发展,因而不能注意自身的物质利益。——居里夫人 五十七、一个人的理想越崇高,生活越纯洁。——伏尼契 五十八、梦想一旦被付诸行动,就会变得神圣。——阿· 安· 普罗克特 五十九、一个人追求的目标越高,他的才力就发展得越快,对社会就越有益。——高尔基 六十、青春是人生最快乐的时光,但这种快乐往往完全是因为它充满着希望,而不是因为得到了什么或逃避了什么。——佚名 六十一、生命里最重要的事情是要有个远大的目标,并借助才能与坚毅来完成它。——歌德 六十二、没有大胆的猜测就作不出伟大的发现。──牛顿 六十三、梦想,是一个目标,是让自己活下去的原动力,是让自己开心的原因。——佚名 六十四、人生太短,要干的事太多,我要争分夺秒。——爱迪生 六十五、一路上我都会发现从未想像过的东西,如果当初我没有勇气去尝试看来几乎不可能的事,如今我就还只是个牧羊人而已。——《牧羊少年的奇幻之旅》 六十六、一个人越敢于担当大任,他的意气就是越风发。——班生 六十七、贫穷是一切艺术职业的母亲。——托里安诺 六十八、莫道桑榆晚,为霞尚满天。——刘禹锡 六十九、一切活动家都是梦想家。——詹· 哈尼克 七十、如果一个人不知道他要驶向哪个码头,那么任何风都不会是顺风。——小塞涅卡 七十一、人性最可怜的就是:我们总是梦想着天边的一座奇妙的玫瑰园,而不去欣赏今天就开在我们窗口的玫瑰。——佚名 七十二、一个人如果已经把自己完全投入于权力和仇恨中,你怎么能期望他还有梦?——古龙 七十三、一个人有钱没钱不一定,但如果这个人没有了梦想,这个人穷定了。——佚名 七十四、平凡朴实的梦想,我们用那唯一的坚持信念去支撑那梦想。——佚名 七十五、最初所拥有的只是梦想,以及毫无根据的自信而已。但是,所有的一切就从这里出发。——孙正义 七十六、看见一个年轻人丧失了美好的希望和理想,看见那块他透过它来观察人们行为和感情的粉红色轻纱在他面前撕掉,那真是伤心啊!——莱蒙托夫 七十七、努力向上吧,星星就躲藏在你的灵魂深处;做一个悠远的梦吧,每个梦想都会超越你的目标。——佚名 七十八、正如心愿能够激发梦想,梦想也能够激发心愿。——佚名 七十九、梦想一旦被付诸行动,就会变得神圣。——阿· 安· 普罗克特 八十、对于学者获得的成就,是恭维还是挑战?我需要的是后者,因为前者只能使人陶醉而后者却是鞭策。——巴斯德 八十一、冬天已经到来,春天还会远吗?——雪莱 八十二、一个人想要成功,想要改变命运,有梦想是重要的。……我觉得每个人都应该心中有梦,有胸怀祖国的大志向,找到自己的梦想,认准了就去做,不跟风不动摇。同时,我们不仅仅要自己有梦想,你还应该用自己的梦想去感染和影响别人,因为成功者一定是用自己的梦想去点燃别人的梦想,是时刻播种梦想的人。——李彦宏 八十三、梦想是人们与生俱来的重要宝物之一,它等待你的珍视和实践。——邹金宏 八十四、心存希望,幸福就会降临你;心存梦想,机遇就会笼罩你。——佚名 八十五、第一,有梦想。一个人最富有的时候是有梦想,有梦想是最开心的。第二,要坚持自己的梦想。有梦想的人非常多,但能够坚持的人却非常少。阿里巴巴能够成功的原因是因为我们坚持
体积大小的影响因素 通过计算比较1mol下列各物质的体积(V):
(公式:V = m / = n· M / ) 物质 O2 H2 物质 Fe Al 状态 g g 状态 s s
/g· L-1
1.429 0.0899
