未混合的D或DL-泛酸及其衍生物(不论是否溶…(HS 293624)2017 乌克兰
未混合的D或DL-泛酸及其衍生物(不论是否…(HS 293624)2017 厄瓜多尔

5
PROCESADORA NACIONAL DE ALIMENTOS C.A. PRONACA
6
TADEC TECNICOS AGROPECUARIOS DEL ECUADOR CIA LTDA
7
PROCESADORA NACIONAL DE ALIMENTOS C A PRONACA
8ቤተ መጻሕፍቲ ባይዱ
QUIMICA SUIZA INDUSTRIAL DEL ECUADOR QSI SA
按采购金额排序 Ranked by import amount
排名 Rank
1
公司名称/Company Name DSM NUTRITIONAL PRODUCTS ECUADOR SA
2
ECUADPREMEX SA
3
VIMIN VITAMINAS Y MINERALES CA
4
ADITIVOS Y ALIMENTOS SA ADILISA
瀚闻资讯 Dalian Infobank Co., Ltd.
厄瓜多尔 2017 年度真实 买家/进口商/收货人/采购商 排名 ECUADOR Active and Exact Importers
更多买家信息、采购信息、进出口交易记录、进出口贸易数据、真实交易记录、请与瀚闻资讯联系 Please visit our website to get more import and export trade information
全球最大的贸易统计数据库 – GTA2017 年终统计结果显示:2017 年 1-12 月 未混合的 D 或 DL-泛酸及其衍 生物(不论是否溶于溶剂)(商品编码 293624)厄瓜多尔进口商共计 34 个
GTA (Global Trade Analysis System), the world's largest trade intelligence database shows that there are 34 ECUADOR Importers of --D-or DL-Pantothenic acid (Vitamin B3 or Vitamin B5) and its derivatives (HS CODE 293624) in 2017
IMDS材料数据系统使用指南(10.0版本)

1.4 1.5 1.6 127 日 2013 年 4 月 23 日
2013 年 5 月 24 日 2013 年 6 月 27 日
2013 年 12 月 12 日 2014 年 3 月 17 日 2014 年 7 月 13 日 2015 年 2 月 27 日 2015 年 4 月 27 日 2015 年 6 月 10 日 2015 年 6 月 11 日 2015 年 7 月 10 日
第3页
目录
1 IMDS – 简介.............................................................................................................................................................................................................. 7 2 IMDS – 使用入门 ...................................................................................................................................................................................................... 8
IMDS 服务中心 欧洲 | 电话: +36 1778-9821 | 电子邮件: imds-helpdesk-english@ 中国 | 电话: + 86 27 8743-1668 | 电子邮件: imds-eds-helpdesk-china@
羟丙基纤维素质量标准

目的:建立一个羟丙甲纤维素的质量标准范围:适用于羟丙甲纤维素责任者:内容:品名:羟丙甲纤维素拼音名:Qiangbingjia Xianweisu英文名:Hypromellose本品为2-羟丙基醚甲基纤维素。
根据甲氧基与羟丙氧基含量的不同将羟丙甲纤维素分为四种取代型,即1828、2208、2906、2910型。
按干燥品计算,各取代型甲氧基(-OCH3)、羟丙氧基(-OCH2CHOHCH3)的含量应符合附表的规定。
【性状】本品为白色或类白色纤维状或颗粒状粉末;无臭。
本品在无水乙醇、乙醚或丙酮中几乎不溶;在冷水中溶胀成澄清或微浑浊的胶体溶液。
【鉴别】(1)取本品1g,加热水(80~90℃)100ml,不断搅拌,在冰浴中冷却,成黏性液体;取2ml置试管中,沿管壁缓缓加0.035%蒽酮的硫酸溶液1ml,放置5分钟,在两液界面处显蓝绿色环。
(2)取鉴别(1)项下的黏性液体适量,倾注在玻璃板上,俟水分蒸发后,形成一层有韧性的薄膜。
【检查】酸碱度取本品1.0g(以干燥品计),边搅拌边加入90℃的水50g中,冷却后,用水调节溶液至100g,搅拌至溶解完全,依法测定(附录ⅥH),pH 值应为5.0~8.0。
黏度取本品10.00g,按干燥品计算,加90℃的水使样品与水总重为500.0g,制成2.0%(g/g)的混悬液,充分搅拌约10分钟,直至颗粒得到完全均匀的分散和润湿,置冰浴中冷却,冷却过程中继续搅拌40分钟,离心除去气泡,必要时加冷水调节重量;用旋转式黏度计(NDJ-5),在20℃±0.1℃,依法测定(附录ⅥG第二法),黏度应为标示黏度的80%~120%(标示粘度为5)。
第 1 页共2 页羟丙甲纤维素质量标准第 2 页 共 2 页 水中不溶物 取本品1.0g ,置烧杯中,加80~90℃的热水100ml ,溶胀约15分钟后,在冰浴中冷却,加水300ml (必要时可适当增加水的体积,确保溶液滤过),并充分搅拌,用经105℃干燥至恒重的1号垂熔玻璃坩埚滤过,烧杯用水洗净,洗液并入上述垂熔玻璃坩埚中,滤过,在105℃干燥至恒重,遗留残渣不得过5mg (0.5%)。
无食安标准有进口记录

酶制剂 酶制剂 着色剂 复合添加剂 香精香料 复合添加剂 复合添加剂 复合添加剂 胶基 香精香料 抗氧化剂 香精香料 香精香料 香精香料 助剂 香精香料 香精香料 香精香料 香精香料 香精香料 香精香料 香精香料 营养强化剂 持水剂 营养强化剂 持水剂 酶制剂 胶基 香精香料 营养强化剂 着色剂 着色剂 香精香料 助剂 香精香料 香精香料 香精香料 营养强化剂 香精香料 SH/T 0767-2005 食品 级凡士林 GB2760-附录B GB2760-附录B GB2760-附录B GB 14880 GB2760-附录B 卫生部公告(2008年第 17号) 卫生部公告(2008年第 27号) 卫生部公告(2007年第 12号) 卫生部公告(2008年第 13号) GB2760-附录B GB2760-附录B GB2760-附录B GB2760-附录B HG/T 2750-2006 靛蓝
3
食品安全法实施前已有进口记录但尚无食品安全国家标准的食品添加剂目录
130 131 132 133 134 135 136 137 138 橙香精 橙叶油 橙油香料 虫胶溶液 除酸保水剂 除萜白柠檬油 除萜甜橙皮油 除萜甜橙油 刺槐豆胶 香精香料 香精香料 香精香料 被膜剂 复合添加剂 香精香料 香精香料 香精香料 胶基 稳定剂 增稠剂 营养强化剂 乳化剂 营养强化剂 香精香料 香精香料 酶制剂 乳化剂 胶姆糖基础 剂 乳化剂 酸度调节剂 酶制剂 营养强化剂 营养强化剂 营养强化剂 稳定和凝固 剂 酶制剂 酶制剂 酶制剂 酶制剂 酶制剂 酶制剂 酶制剂 酶制剂 香精香料 卫生部公告(2007年第 12号) 卫生部公告(2007年第 营养强化剂 12号) 甜味剂 香精香料 《中华人民共和国药 2010年第18号公告 营养强化剂 典》(2010年版) GB 14880 营养强化剂 卫生部公告(2007年第 5号) 卫生部公告(2007年第 5号) LY/T1641-2005食用单 宁酸 卫生部公告(2008年第 26号) GB 14880 卫生部公告(2008年第 26号) GB2760-附录B
口溶膜类新药的开发与评价探讨

药事管理㊀作者简介:王璐ꎬ女ꎬ硕士ꎬ主管药师ꎬ研究方向:化学药品技术审评ꎬE-mail:wanglu@cde.org.cn通信作者:王亚敏ꎬ男ꎬ硕士ꎬ主任药师ꎬ研究方向:化学药品技术审评ꎬTel:010-80996309ꎬE-mail:wangym@cde.org.cn口溶膜类新药的开发与评价探讨王璐ꎬ胡延臣ꎬ王亚敏(国家药品监督管理局药品审评中心ꎬ北京100076)摘要:膜剂系指原料药物与适宜的成膜材料经加工制成的膜状制剂ꎬ口溶膜系指在口腔可迅速溶化的膜剂ꎮ口溶膜具有剂量准确㊁携带方便㊁可提高特定适应证人群患者依从性等特点ꎮ本文结合注册法规要求及近年来国内外口溶膜药物的开发和审评审批情况ꎬ对口溶膜新药的开发立项㊁处方工艺㊁质量研究和控制等方面的评价进行了探讨ꎮ研究建议企业在立项开发时应全面评估ꎬ合理选择申报策略和路径ꎮ处方工艺开发时ꎬ根据剂型特点关注影响产品质量的关键因素ꎬ并有针对性地进行质量研究和控制ꎮ希望通过本文能够指导现阶段口溶膜类新药产品的开发和评价ꎬ助力有临床需求的㊁高质量的口溶膜类新药的获批上市ꎮ关键词:口溶膜ꎻ口腔速溶膜ꎻ新药ꎻ处方工艺ꎻ质量控制ꎻ开发与评价中图分类号:R95㊀文献标志码:A㊀文章编号:2095-5375(2024)03-0302-007doi:10.13506/j.cnki.jpr.2024.03.017DiscussiononthedevelopmentandevaluationofnewdrugsoforalsolublefilmWANGLuꎬHUYanchenꎬWANGYamin(CenterforDrugEvaluationꎬNationalMedicalProductsAdministrationꎬBeijing100076ꎬChina)Abstract:Filmsrefertothefilm-likepreparationmadebyprocessingtherawmaterialandtheappropriatefilm-form ̄ingmaterial.Oralsolublefilmreferstothefilmthatdissolvesrapidlyinthemouth.Thecharacteristicsoftheoralsolublefilmincludeaccuratedoseꎬeasytocarryꎬandimprovingthecomplianceofpatientswithspecificindications.Basedontherequire ̄mentsofregistrationregulationsandapprovaloforalsolublefilmsathomeandabroadinrecentyearsꎬtheevaluationoforalsolublefilmswereputforwardintermsofdevelopmentꎬformulationꎬmanufacturingprocessandqualityresearchandcontrol.Theapplicationstrategyandpathshouldberationallyselectedaftercomprehensiveevaluation.Duringformulationandprocessdevelopmentꎬfocusonthekeyfactorsaffectingproductqualityaccordingtothecharacteristicsofdosageformsꎬandconducttargetedqualityresearchandcontrol.Thesediscussionsareexpectedtoguidethedevelopmentandevaluationoforalsolublefilmsꎬandpromotetheapprovalandmarketingofhigh-qualityoralsolublefilmnewdrugswithclinicalneeds.Keywords:OralsolublefilmꎻOrodispersiblefilmsꎻInnovativedrugsꎻFormulationandmanufacturingprocessꎻQualitycontrolꎻDevelopmentandevaluation㊀㊀2016年原国家食品药品监督管理总局发布了«关于发布化学药品注册分类改革工作方案的公告»(2016年第51号)[1]ꎬ提出新药的定义ꎮ国家药品监督管理局关于发布化学药品注册分类及申报资料要求的通告(2020年第44号)[2]中明确化学药品注册分类中1类为境内外均未上市的创新药ꎬ指含有新的结构明确的㊁具有药理作用的化合物ꎬ且具有临床价值的药品ꎻ2类为境内外均未上市的改良型新药ꎬ具体是指在已知活性成分的基础上ꎬ对其结构㊁剂型㊁处方工艺㊁给药途径㊁适应证等进行优化ꎬ且具有明显临床优势的药品ꎮ新药的开发中ꎬ口溶膜类药物在特定疾病及人群方面具有一定优势ꎬ可解决传统口服制剂(如片剂㊁丸剂㊁胶囊剂等)对于口服困难的患者以及需要服药但会产生抵抗情绪的患者(如精神疾病患者)的诸多不便ꎬ因此愈发受到关注ꎮ本文对口溶膜类新药产品上市情况及开发立项建议㊁处方工艺开发㊁质量控制等方面进行探讨ꎬ希望对此类产品的开发和评价提供借鉴ꎮ需要注意的是ꎬ并不是所有药物都适合开发成为口溶膜ꎬ企业进行口溶膜类新药的开发立项时ꎬ应对拟开发品种进行全面评估ꎬ充分考虑剂型适用性及临床优势是否充分ꎬ确认是否符合创新药或改良型新药注册分类的相关要求ꎬ降低注册风险ꎮ1㊀基本情况1.1㊀口溶膜的定义和特点㊀«中国药典»2020年版(四部)通则中[3]ꎬ膜剂系指原料药物与适宜的成膜材料经加工制成的膜状制剂ꎬ供口服或黏膜用ꎮ2023年3月14日国家药典委员会发布关于征求«中国药典»丸剂和膜剂通则修订草案公开征求意见[4]ꎬ进一步将膜剂进行分类ꎮ膜剂根据给药部位不同ꎬ可分为口用膜㊁眼用膜㊁阴道膜等ꎻ其中口用膜可分为口溶膜㊁口颊膜㊁舌下膜和口腔贴膜ꎮ此外ꎬ草案增补口溶膜㊁口颊膜㊁舌下膜和口腔贴膜的定义ꎮ其中口溶膜系指在口腔可迅速溶化的膜剂ꎻ口颊膜系指黏贴于口腔ꎬ经黏膜吸收后起全身作用的膜剂ꎻ舌下膜系指置于舌下能迅速溶化ꎬ药物经舌下黏膜吸收发挥全身作用的膜剂ꎻ口腔贴膜系指黏贴于口腔ꎬ发挥局部作用的膜剂ꎮ«美国药典»中的膜剂定义为置于口腔内的薄片ꎬ可能含有一层或多层ꎬ层中可含有原料药也可不含原料药ꎮ通常情况下ꎬ这些薄膜通常是通过涂膜法制备ꎬ各组分在薄膜中分散ꎮ膜剂按药物释放位置进行分类ꎬ包括直接释放药物到口腔中或到胃肠道吸收的口腔膜(oralfilms)ꎬ通过近端黏膜吸收以避免首过代谢或胃肠道降解ꎬ并快速起效的口颊膜(buccalfilms)和舌下膜(sublingualfilms)ꎮ«欧洲药典»口腔分散膜(orodispersiblefilms)通则中指出ꎬ口腔分散膜是用于口腔内给药的固体口腔黏膜制剂ꎬ它们在口腔内迅速分散以递送活性物质ꎮ口腔分散膜由单层或多层膜片组成ꎮ口溶膜具有的优点包括[5]:可制备成不同的尺寸和形状ꎬ剂量准确ꎻ几分钟内即可在口腔内快速释放和分解ꎻ无须用水送服ꎬ无须吞咽ꎻ体积小㊁质量轻ꎬ便于携带ꎻ可通过掩味剂的加入改善药物本身的不良味道ꎻ服用后在口腔中几乎无残留物ꎻ部分疏水性药物可迅速分散和溶解ꎬ可能提高生物利用度等ꎮ口溶膜适用于需要快速起效的情况ꎬ如突然发作的过敏或哮喘ꎻ适用于需要改善患者依从性的情况ꎬ如具有呕吐症状的吞咽困难患者以及需服药但会产生抵抗情绪的患者服用ꎻ口溶膜适用于儿童ꎬ其计量精准灵活㊁入口立即溶解ꎬ可防止儿童吐药ꎬ且可设计为不同的颜色和口味ꎬ对儿童吸引力更大ꎮ然而ꎬ口溶膜也存在其缺点和局限性ꎬ包括:在口腔pH值环境中不稳定的药物不适用ꎻ不适宜大剂量药物ꎻ易碎且必须防止进水ꎬ需要特殊包装ꎻ对黏膜有刺激作用的药物不适用等ꎮ1.2㊀口溶膜药物国内外上市产品及开发立项建议㊀2006年ꎬ日本上市了第一个口溶膜处方药伏格列波糖口溶膜ꎮ2010年ꎬ美国和欧洲分别上市第一个口溶膜处方药昂丹司琼口溶膜(Rapidfilm和Seto ̄film)ꎮ2020年ꎬ国家药品监督管理局批准了第一个口溶膜化学药品奥氮平口溶膜上市ꎮ目前ꎬ全球已有多个口溶膜产品上市ꎬ查询美国[6]㊁欧洲[7]㊁日本[8]药品监管机构网站ꎬ部分品种信息见表1ꎮ表1㊀国外已上市的部分口溶膜品产品上市地区药品名称活性成分规格适应证临床对照药美国OndansetronOralSolubleFilm昂丹司琼4mg㊁8mg化疗及术后呕吐昂丹司琼口崩片KetoprofenOralSolubleFilm酮洛芬12.5mg风湿㊁类风湿关节炎㊁骨关节炎等酮洛芬片RiluzoleOralFilm利鲁唑50mg肌萎缩性脊髓侧索硬化症利鲁唑片表1㊀(续)上市地区药品名称活性成分规格适应证临床对照药欧盟RabestromOrodispersibleFilm枸橼酸西地那非25mg㊁50mg㊁75mg㊁100mg勃起功能障碍枸橼酸西地那非口崩片OlanzapinRenantosOrodispersibleFilm奥氮平5mg㊁10mg㊁15mg精神分裂症奥氮平口崩片Donepezil-HClSandozSchmelzFilm盐酸多奈哌齐5mg㊁10mg轻度或中度阿尔兹海默病盐酸多奈哌齐薄膜包衣片RizaportSchmelzFilm苯甲酸利扎曲普坦5mg㊁10mg偏头痛发作的头痛期急性治疗苯甲酸利扎曲普坦口崩片ZolmitriptanRenantosOrodispersibleFilm佐米曲坦2.5mg㊁5mg中㊁重度偏头痛佐米曲坦口服分散片RisperidoneSandozSchmelzFilm利培酮0.5mg㊁1mg㊁3mg精神分裂症利培酮薄膜包衣片SetofilmOrodispersibleFilms昂丹司琼4mg㊁8mg恶心㊁呕吐昂丹司琼口崩片㊀㊀通过国家药品监督管理局网站查询[9]ꎬ统计了我国批准的口溶膜药物(见表2)ꎬ共15个批准文号ꎬ按照注册分类统计ꎬ其中10个为2.2类改良型新药ꎬ占大多数ꎻ按适应证统计ꎬ其中6个为精神障碍疾病药物㊁3个为生殖系统疾病药物㊁2个为精神神经系统药物㊁2个为呼吸系统疾病及抗过敏药物㊁2个消化道及代谢药物ꎮ结合目前口溶膜类药品的审评情况以及对上述已上市品种的特点分析ꎬ以下情形比较适宜开发口溶膜剂型ꎮ①在精神分裂症等特定适应证中口溶膜可充分发挥其剂型特点ꎮ例如ꎬ藏药是精神病患者依从性差的最常见表现ꎮ口溶膜具有口腔速溶性质ꎬ融化后易于吞咽ꎬ相比于已上市的口服剂型(如普通片㊁口崩片)具有更好的防藏药特性ꎬ利于精神病患者藏药行为的控制ꎬ对于提高患者依从性有益ꎻ②部分品种现有剂型有限或剂型存在缺陷ꎬ口溶膜可发挥相应特定剂型特点ꎮ例如ꎬ部分治疗哮喘㊁呕吐类产品仅有片剂㊁咀嚼片㊁颗粒剂上市ꎬ口溶膜更利于吞咽ꎬ具有更优的患者依从性ꎮ对于其他情形ꎬ基于目前的审评认知和实践ꎬ建议企业慎重开发ꎮ关于品种立题合理性ꎬ建议开发前期与药品审评中心临床审评团队沟通ꎮ表2㊀国内批准上市的口溶膜药物批准文号/注册证号药品名称规格上市许可持有人注册分类批准日期适应证国药准字H20220012盐酸美金刚口溶膜5mg齐鲁制药有限公司2.22022-06-23国药准字H20220013盐酸美金刚口溶膜10mg齐鲁制药有限公司2.22022-06-23治疗中重度至重度阿尔茨海默型痴呆国药准字H20220014阿立哌唑口溶膜10mg齐鲁制药有限公司2.22022-06-23国药准字H20220015阿立哌唑口溶膜15mg齐鲁制药有限公司2.22022-06-23用于治疗精神分裂症国药准字H20223056昂丹司琼口溶膜4mg江苏恒瑞医药股份有限公司32022-01-30国药准字H20223055昂丹司琼口溶膜8mg江苏恒瑞医药股份有限公司32022-01-30预防高致吐性化疗㊁中度致吐化疗㊁放疗和手术后恶心呕吐国药准字H20220004他达拉非口溶膜2.5mg齐鲁制药有限公司原52022-01-30国药准字H20220006他达拉非口溶膜10mg齐鲁制药有限公司原52022-01-30国药准字H20220005他达拉非口溶膜5mg齐鲁制药有限公司原52022-01-30治疗勃起功能障碍国药准字H20210009孟鲁司特钠口溶膜4mg齐鲁制药有限公司2.22021-03-09国药准字H20210010孟鲁司特钠口溶膜5mg齐鲁制药有限公司2.22021-03-09适用于1岁至14岁儿童哮喘的预防和长期治疗ꎬ包括预防白天和夜间的哮喘症状ꎬ阿司匹林敏感的哮喘症状ꎬ以及预防运动诱发的支气管收缩ꎮ适用于2岁至14岁儿童季节性过敏性鼻炎和常年性过敏性鼻炎ꎬ减轻过敏性鼻炎引起的症状国药准字H20210004奥氮平口溶膜5mg齐鲁制药有限公司2.22021-01-19国药准字H20210005奥氮平口溶膜10mg齐鲁制药有限公司2.22021-01-19精神分裂症㊁双相情感障碍的躁狂发作国药准字H20200011奥氮平口溶膜5mg江苏豪森药业集团有限公司2.22020-11-24国药准字H20200012奥氮平口溶膜10mg江苏豪森药业集团有限公司2.22020-11-24精神分裂症㊁双相情感障碍的躁狂发作㊀㊀«关于发布化学药品注册分类改革工作方案的公告»中指出ꎬ2类新药需具有明显临床优势[1]ꎮ企业拟按照2.2类进行口溶膜产品开发立项时ꎬ应对品种进行全面评估ꎬ充分考虑剂型适用性及临床优势是否充分ꎬ确认是否符合2.2类注册分类相关要求ꎮ建议企业紧紧围绕临床需求及临床优势进行开发立项ꎬ开发前期与药品审评中心做好沟通交流工作ꎬ降低注册风险ꎮ此外企业还应详细调研拟开发产品国内外上市情况及同品种的国内外注册进展ꎬ应符合注册管理法规的相关要求并选择合理的申报路径ꎮ避免注册分类不符合要求无法受理或审批的情况发生ꎮ比如ꎬ某口溶膜产品已在韩国㊁印度等国家上市ꎬ如在国内按照2.2类进行申报ꎬ则与现行注册分类中相关要求不符ꎬ无法按2.2类改良型新药进行审评审批ꎮ2㊀口溶膜的开发及评价关注点2.1㊀处方开发㊀典型的口溶膜处方通常包括:药物活性成分(5%~30%W/W)㊁成膜材料(40%~50%W/W)㊁增塑剂(0~20%W/W)ꎬ必要时添加表面活性剂(适量)㊁甜味剂(3%~6%W/W)㊁唾液刺激剂㊁填充剂㊁香精和色素等[10]ꎮ国内批准上市的产品处方中ꎬ一般主要包括成膜材料(如羟丙甲纤维素)㊁增塑剂(如甘油㊁聚乙二醇400)㊁矫味剂(如三氯蔗糖㊁香精)㊁着色剂等ꎮ调研美国食品药品监督管理局(FoodandDrugAdministrationꎬFDA)批准上市的口溶膜处方如表3所示ꎮ其中羟丙甲纤维素㊁羟丙基纤维素为常用的成膜材料ꎬ甘油㊁甘油单油酸酯为常用的增塑剂ꎬ三氯蔗糖㊁香精为常用的矫味剂ꎮ表3㊀FDA批准上市的口溶膜产品公开处方信息药品名称及商品名辅料组成奥氮平口溶膜Zu ̄plenz [11]丁羟甲苯㊁碳酸钙㊁胶体二氧化硅㊁赤四糖醇㊁羟丙甲纤维素㊁甘草酸铵㊁薄荷香精㊁聚氧乙烯㊁碳酸氢钠㊁三氯蔗糖㊁二氧化钛㊁黄原胶氯巴占口溶膜Sym ̄pazan [12]薄荷香精㊁柠檬酸㊁甘油单油酸酯㊁羟丙基纤维素㊁麦糖醇㊁苦味掩味剂㊁树莓香精㊁聚氧乙烯㊁水㊁磷酸氢二钠㊁三氯蔗糖利鲁唑口溶膜Ex ̄servan [13]FD&C黄#6㊁果糖㊁甘油㊁甘油单油酸酯㊁羟丙基纤维素㊁蜂蜜香精㊁柠檬香精㊁聚丙烯酸树脂㊁聚氧乙烯㊁多聚糖㊁三氯蔗糖㊁黄原胶㊁木糖醇酮洛芬口溶膜Nex ̄cede [14]羟丙基纤维素㊁三氯蔗糖㊁聚乙二醇400㊁木糖醇㊁麦芽糊精㊁薄荷香精/肉桂香精㊁氢氧化钠㊁安赛蜜㊁磷酸氢二钠㊁FD&C蓝#1/FD&C红色#40㊁白色油墨ꎮ㊀㊀通过以上已上市产品处方的梳理ꎬ可了解口溶膜产品处方的常规组成ꎬ对研发和评价具有一定参考价值ꎮ处方研究中需重点关注成膜材料和增塑剂的选择和用量㊁矫味剂种类和用量对口感的影响等ꎮ成膜材料是药物活性成分的载体ꎬ是口溶膜处方中最重要的成分之一ꎬ一般为亲水聚合物(如羟丙甲基纤维素等)ꎮ成膜材料聚合物的种类和用量影响口溶膜的拉伸强度ꎬ聚合物的分子量影响口溶膜的溶化时限ꎮ增塑剂可提高口溶膜的机械性能ꎬ包括拉伸强度和延伸率ꎬ常见的增塑剂有甘油㊁聚乙二醇(PEG400)等ꎮ增塑剂的选择取决于其与聚合物的相容性和溶剂性质等ꎮ有研究表明ꎬ处方中增塑剂与成膜材料的比例对口溶膜的机械性能(断裂伸长率㊁杨氏模量㊁折叠耐久性)㊁厚度㊁溶出度等关键质量属性产生显著影响[15]ꎮ表面活性剂一般用于增强口溶膜的溶解度和润湿性ꎬ使药物活性成分更快释放ꎮ甜味剂用于掩盖药物活性成分的难闻气味和苦味ꎮ唾液刺激剂可刺激唾液腺产生唾液ꎬ帮助口溶膜快速分解ꎮ处方开发过程及临床试验期间ꎬ应关注口感指标的收集与评价(尤其活性成分味道难以掩盖的品种)ꎬ并根据需要优化处方ꎮ对于用于儿童人群的口溶膜ꎬ应特别关注辅料种类及用量在应用于儿童时的口感和安全性ꎮ儿童在不良感觉的耐受性方面有别于成人ꎬ口感不佳所导致的不良用药行为风险也相应增高ꎬ因此ꎬ相比于成人用药ꎬ儿童用药口感评价具有更强的临床意义与价值ꎬ也逐渐成为该类药品临床价值综合评价的重要内容[16]ꎮ由于儿童人群的特殊性ꎬ辅料可能会对正在发育的器官产生不同程度的影响ꎬ且成人与儿童之间㊁不同年龄的儿童之间可能具有不同的暴露量ꎬ导致毒性反应可能不同ꎮ因此ꎬ即使是已常规用于成人药品或在已获批儿童药品中使用的辅料ꎬ仍然需要评估现有资料是否支持在拟定儿童人群中使用ꎮ应结合辅料的已有信息ꎬ并参照相关指南进行儿童药品中辅料的安全性评估ꎮ如果支持该辅料用于拟定的儿童人群的资料不充足ꎬ则需要进一步的安全性试验[17]ꎮ在处方开发时ꎬ还需关注原料药粒度及晶型的研究ꎬ尤其是难溶性药物ꎮ当药物活性成分在制剂中间体药液中呈混悬状态ꎬ关注原料药粒度分布的控制ꎬ以保证配液药液及成品含量均一性ꎬ以及成品膜表面光滑平整ꎮ建议结合粒度对制剂特性(如性状外观㊁含量均匀性㊁溶出度)㊁生产工艺(如分散均匀性㊁存放稳定性)等的影响ꎬ制定粒径控制策略ꎮ除应对口溶膜的原辅料进行合理控制外ꎬ还建议关注离型膜的材质和型号的选择㊁质控ꎬ评估其对产品产生的影响ꎮ2.2㊀生产工艺及过程控制㊀膜剂的制备工艺主要包括涂膜法㊁热熔挤出法㊁半固体溶剂浇铸法㊁固体分散挤压法和滚圆法等[18]ꎮ其中涂膜法是目前商业化生产口溶膜较为普遍的方法ꎮ涂膜法首先将成膜材料溶解于水或有机溶剂或两者的混合溶剂中ꎬ形成具有一定黏度的透明状溶液ꎮ当药物活性成分为水溶性时ꎬ应与成膜材料制成具有一定黏度的溶液ꎻ当药物活性成分为水不溶或难溶时ꎬ应将其粉碎并与成膜材料等混合均匀ꎮ再将药物和其他辅料溶解或分散到上述溶液中ꎬ真空脱气ꎬ倒入涂膜机中涂膜ꎬ真空干燥除去水分ꎬ脱模后裁剪成所需规格ꎬ即得ꎮ涂膜法是制备口溶膜常用的方法ꎬ该方法制备工艺简单ꎬ加工成本低ꎬ易于使用[19]ꎮ工艺开发时应对参照ICHQ8[20]对生产工艺和工艺参数进行全面的筛选研究ꎬ以加强对产品性能和工艺的理解ꎬ建立工艺参数与制剂关键质量属性(如薄膜厚度㊁溶化时限㊁溶出度㊁水分㊁吸湿性㊁含量和含量均匀度㊁机械性能等)之间的关系ꎬ并采取有效的过程控制措施ꎮ在采用涂膜法生产口溶膜时ꎬ影响药品关键质量属性的高风险工艺步骤通常为配液㊁脱泡㊁涂布和干燥ꎮ配液工序建议关注对配料温度㊁加料顺序㊁混合参数的研究和控制ꎮ脱泡工序ꎬ建议考虑胶液中的气泡残留对涂布工艺和产品质量的影响ꎮ涂布和干燥工序ꎬ建议关注风量㊁干燥温度等参数的研究和控制ꎬ尤其当药物活性成分在胶液中呈混悬状态时ꎬ建议重点关注在工艺过程中产品的均一性ꎬ包括胶液放置过程中的均一性㊁涂布过程中胶液的均一性等ꎮ此外关注生产过程中是否会出现离型膜换卷或涂布过程中设备停机等情形ꎬ若存在ꎬ则建议进行风险评估ꎬ并提出相应的处理方式及其合理性依据ꎮ涂膜法制备口溶膜生产过程中的制剂中间产品通常包括胶液㊁涂布干燥后药膜㊁裁切后药膜㊁内包后药膜等ꎮ应根据不同工艺的风险点ꎬ针对性地开展过程控制㊁中间体控制ꎮ其中胶液中间体关注样品的性状㊁气泡㊁黏度㊁含量㊁微生物限度等ꎻ涂布干燥后药膜关注样品的性状㊁片重㊁含量及含量均匀性㊁水分㊁机械性能等ꎻ裁切后和内包后药膜关注样品的尺寸㊁片重差异㊁密封性㊁机械性能等ꎮ在工艺开发过程中ꎬ企业应认真分析生产规模放大对产品质量可能产生的影响ꎬ结合拟定的商业生产规模ꎬ合理选择临床试验用样品批量ꎮ建议商业化样品处方工艺㊁批量与关键临床试验样品保持一致ꎬ不低于10万片ꎮ2.3㊀口溶膜的质量研究及评价关注点㊀«中国药典»2020年版(四部)0125膜剂通则中规定[3]ꎬ膜剂外观应完整光洁㊁厚度一致㊁色泽均匀㊁无明显气泡ꎮ多剂量的膜剂ꎬ分格压痕应均匀清晰ꎬ并能按压痕撕开ꎮ除另有规定外ꎬ膜剂应进行重量差异(凡进行含量均匀度检查的膜剂ꎬ一般不再进行重量差异检查)㊁微生物限度(微生物计数法和控制菌检查法及非无菌药品微生物限度标准检查ꎬ应符合规定)的检查ꎮ国家药典委员会发布关于征求«中国药典»丸剂和膜剂通则修订草案公开征求意见[4]中对膜剂在生产与贮藏期间的要求进行修订ꎬ增加了口感㊁口腔黏膜刺激性㊁水分㊁机械性能㊁微生物限度㊁溶出度㊁含量均匀度及残留溶剂方面的要求ꎮ在口溶膜定义中还指出ꎬ口溶膜应进行溶化时限检查ꎬ对于难溶性原料药物制成的口溶膜ꎬ还应进行溶出度检查ꎮ«美国药典»膜剂通则中指出ꎬ薄膜必须足够坚固ꎬ在生产和包装过程中保持其完整性ꎬ保障患者使用ꎮ由于膜剂溶解迅速ꎬ味道和口感是重要的考虑因素ꎮ«欧洲药典»口腔分散膜通则中指出ꎬ在生产口腔分散膜时ꎬ应采取措施确保其具有适当的机械强度ꎬ以免被损坏ꎮ除非另有理由或授权ꎬ否则应进行合理的试验以证明活性物质的适当释放ꎮ综上ꎬ除常规质量控制项目外ꎬ根据膜剂的特点及关键质量属性ꎬ建议重点关注评价口溶膜的水分㊁口感㊁溶化时限㊁溶出度以及机械性能ꎮ水分:口溶膜中应含有适量的水分ꎬ以保障口溶膜具有适宜的机械性能ꎬ以免包装㊁运输过程中发生磨损或破碎ꎮ口感:口溶膜应口感良好ꎬ为了满足依从性需要ꎬ建议在临床研究过程中关注给药方式(口腔放置位置㊁溶化时限等)㊁黏膜黏附性和刺激性㊁口腔局部不良反应㊁口感评价等[4]ꎮ溶化时限:现行«中国药典»膜剂通则项下并未规定溶化时限检查相关要求ꎬ但溶化时限是口溶膜产品药学质量研究及控制中需关注的重要质量指标之一ꎮ审评工作中发现ꎬ部分药品生产企业参考口崩片的检查方法和限度拟定口溶膜产品的相关方法和限度ꎮ如采用900mL水作为介质ꎬ与口溶膜药物在口腔内的实际使用环境有较大差异ꎮ因此建议模拟口溶膜使用方法及口腔环境ꎬ建立可行的溶化时限检查方法(少量溶剂)ꎬ结合临床试验中在受试者口腔中的溶化时限及相关性考察ꎬ为方法及限度提供合理性依据ꎮ溶出度:口溶膜需要快速释放药物ꎬ以确保活性药物成分在服用后可被吸收ꎮ在口溶膜开发的初期风险评估中ꎬ溶出度通常是高风险质量属性ꎬ应重点关注ꎮ在开展口溶膜溶出度方法开发时ꎬ建议考虑口溶膜膜片质轻易漂浮等制剂特点ꎬ关注溶出装置㊁溶出试验参数㊁取样时间点等选择的合理性ꎬ建立合适的㊁具有一定区分能力的溶出度方法ꎮ证明溶出方法区分能力时ꎬ可制备关键物料属性㊁关键处方组成㊁关键工艺参数发生变化(例如ꎬ参数在设定值ʃ10%ʃ20%的变化)的样品ꎬ提供不同样品溶出曲线对比数据[21]ꎮ对于难溶性药物制备的口溶膜ꎬ溶出方法建议对不同粒径的处方具有一定的区分能力[22]ꎮ机械性能:口溶膜产品机械性能的研究不容忽视ꎬ机械性能在口溶膜药物的操作性㊁给药便利性和稳定性方面均有重要影响[11]ꎮ建议根据口溶膜的临床使用场景和特点ꎬ关注产品商业包装和运输装载方式ꎬ进行模拟装载㊁运输㊁随身携带(可能涉及跌落㊁撞击㊁皱褶等情况)研究ꎬ注意对可能产生的膜片碎裂等情况进行考察ꎮ口溶膜的机械性能的评价指标可参考但不限于[10]:①抗拉强度(tensilestrength):是薄膜样品在某一点断裂时施加的最大应力ꎬ计算方式为用断裂时施加的力除以薄膜的横截面积ꎻ②伸长率(percentelongation):当施加拉力时ꎬ薄膜样品会拉伸产生形变ꎮ伸长率为薄膜伸长量占原来长度的百分率ꎮ薄膜伸长率一般随增塑剂含量的增加而增加ꎻ③抗撕裂性(tearresistance):撕裂薄膜所需的最大力ꎬ记录为抗撕裂值(单位为牛顿或磅)ꎻ④杨氏模量(youngᶄsmodulus):杨氏模量或弹性模量是衡量薄膜刚度的参数ꎮ表示为弹性变形区域的应力与应变之比ꎻ⑤耐折度(foldingendur ̄ance):耐折度是通过将薄膜在同一位置反复折叠直至薄膜破裂来确定的ꎬ薄膜折叠不断裂的次数计为耐折度值ꎮ耐折度可用于模拟临床实际使用㊁运输㊁贮藏过程对薄膜性能的影响ꎮ建议结合口溶膜生产工艺过程控制㊁稳定性过程中的机械性能研究结果ꎬ合理拟定可接受标准ꎬ并考虑是否订入质量标准ꎮ3㊀结语与展望化学药品注册分类中2类为境内外均未上市的改良型新药ꎬ具体是指在已知活性成分的基础上ꎬ对其结构㊁剂型㊁处方工艺㊁给药途径㊁适应证等进行优化ꎬ且具有明显临床优势的药品ꎮ口溶膜具有剂量准确㊁携带方便㊁患者依从性良好等特点ꎬ在部分疾病及适应证人群治疗中ꎬ口溶膜能很好解决其他剂型所带来的不便ꎬ提高患者用药依从性ꎮ需要注意的是ꎬ并不是所有药物都适合开发成为口溶膜ꎮ企业在立项开发时应全面评估适应证和剂型特点ꎬ充分调研产品国内外上市情况ꎬ充分考虑剂型适用性及临床优势是否充分ꎬ合理选择申报策略和路径ꎮ本文还重点探讨了口溶膜产品开发过程中的关注点和相关评价考虑ꎮ在口溶膜处方工艺开发时ꎬ应根据产品特点ꎬ关注影响药品剂量准确性㊁药物快速释放㊁良好的口感㊁满足使用需求的机械强度等相关因素的评估和研究ꎮ在口溶膜质量控制中ꎬ根据剂型特点注意水分㊁口感㊁溶化时限㊁溶出度㊁机械性能的研究ꎬ尤其应关注溶化时限方法合理性以及溶出度方法具有一定的区分能力ꎮ希望上述对口溶膜产品开发立项建议㊁处方工艺开发㊁质量研究和控制等方面的探讨ꎬ能够指导现阶段对此类产品的开发和评价ꎬ助力有临床需求的㊁高质量的口溶膜类新药的获批上市ꎮ参考文献:[1]㊀国家药品监督管理局.化学药品注册分类改革工作方案的公告[EB/OL].(2016-03-09)[2023-9-27].ht ̄tps://www.nmpa.gov.cn/xxgk/ggtg/ypggtg/ypqtggtg/20160309151801706.html.[2]国家药品监督管理局.化学药品注册分类及申报资料要求的通告[EB/OL].(2020-06-30)[2023-9-27].https://www.nmpa.gov.cn/xxgk/ggtg/ypggtg/ypqtggtg/20200630180301525.html.[3]国家药典委员会.中华人民共和国药典2020年版(四部)[S].北京:中国医药科技出版社ꎬ2020.[4]国家药典委员会.征求«中国药典»丸剂和膜剂通则修订草案意见[EB/OL].(2023-03-14)[2023-9-27].https://www.chp.org.cn/#/business/standard. [5]KAURMꎬRANAACꎬSETHN.FastDissolvingOralFilm:ANovelandInnovativeDrugDeliverysystem[J].IntJPharmResAlliedSciꎬ2013ꎬ2(1):14-24. [6]FDA.FDA-ApprovedDrugs[DB/OL].(2023-9-27)[2023-9-27].https://www.accessdata.fda.gov/scripts/cder/daf/. [7]EMA.Medicines[DB/OL].(2023-9-27)[2023-9-27].https://www.ema.europa.eu/en/medicines.[8]PDMA.MedicalChemicalsInformationSearch[DB/OL].(2023-9-27)[2023-9-27].https://www.pmda.go.jp/PmdaSearch/iyakuSearch/.(下转第312页)。
中国R o H S拟“扩物质”,4种邻苯类有害物质须关注

2022/4准与认证40标STANDARD & CERTIFICATION标准修订先行目前,中国RoHS 有害物质包括铅及其化合物、汞及其化合物、镉及其化合物、六价铬化合物、多溴联苯(PBB)、多溴二苯醚(PBDE)以及国家规定的其他有害物质。
对于纳入《电器电子产品有害物质限制使用达标管理目录(第一批)》(以下简称《达标管理目录》)的12类产品,铅、汞、锅、六价铬、多溴联苯和多溴二苯醚的含量应该符合电器电子产品有害物质限制使用限量要求等相关标准,并纳入电器电子产品有害物质限制使用合格评定制度管理范围。
标准作为中国RoHS 制度的技术支撑文件,主要指向GB/T 26572-2011《电子电气产品中限用物在不远的将来,4种邻苯类有害物质或将纳入中国电器电子产品有害物质限制使用管理。
2022年3月14日,工业和信息化部电器电子产品污染防治标准工作组(以下简称标准工作组)以视频会议的形式组织召开了深化电器电子产品有害物质限制使用管理工作启动会。
这次会议不仅分析了当前电器电子领域有害物质限制使用的国内外行业执行情况,更明确传递出一个信息——中国RoHS 的管控物质将扩容,拟将4类邻苯二甲酸酯类物质(包含DEHP、BBP、DBP、DIBP)纳入《电器电子产品有害物质限制使用管理办法》(以下简称《管理办法》)有害物质清单。
本刊记者 于璇中国R o H S 拟“扩物质”,4种邻苯类有害物质须关注41质的限量要求》、GB/T 26125《电子电气产品六种限用物质(铅、汞、镉、六价铬、多溴联苯和多溴二苯醚)的测定》等。
中国RoHS“扩物质”的第一步,正是对GB/T 26572-2011《电子电气产品中限用物质的限量要求》进行修订,新增4种邻苯类有害物质的限量要求。
根据标准工作组的技术,这次标准修订工作预计于2022年9月底完成。
在完成标准修订后,中国RoHS此次“扩物质”将进入“政策文件发布及修订”阶段。
《电器》记者从会上获悉,新增4种邻苯类有害物质政策文件或将以部文或部公告的形式发布,并将向WTO/TBT 通报,计划的实施过渡期为180天。
实验室有毒常用药品及中毒解决方法

实验室有毒常用药品及中毒解决方法实验室有毒常用药品0.溴化乙锭(EB):大家都比较熟悉了。
具有强诱变致癌性,使用时一定要戴一次性手套,注意操作规范,不要随便触摸别的物品。
1.DEPC(焦碳酸二乙酯):闻起来香香甜甜的,可是害人不眨眼!一种强有力的蛋白质变性剂,而且怀疑是致癌剂.开瓶时将瓶子远离你,内压可导致溅泼.操作时戴合适的手套,穿工作服,并在化学通风橱里进行.2.PMSF(苯甲基磺酰氟):老板说是神经毒!!!是一种高强度毒性的胆碱酯酶抑制剂.它对呼吸道黏膜,眼睛和皮肤有非常大的破坏性.可因吸入,咽下或皮肤吸收而致命.戴合适的手套和安全眼镜,始终在化学通风橱里使用.在接触到的情况下,要立即用大量的水冲洗眼镜或皮肤,已污染的工作服丢弃掉.3.乙腈,易挥发易燃,是一种刺激物和化学窒息剂,通风橱中远离热、火。
4.放线菌素D,是一种致畸剂和致癌剂,通风橱中操作。
5.alpha-鹅膏蕈毒环肽,具有强毒性,可能致命。
6.NN-亚甲双丙烯酰胺,有毒,影响中枢神经系统,切勿吸入粉末。
7.甲醇,有毒,能引起失明。
8.乙酸(浓的):可能因为吸入或皮肤吸收而受到伤害,要戴手套和护目镜,最好在化学通风橱中操作。
9.过硫酸铵:对粘膜和上呼吸道、眼睛和皮肤又较大危害性,吸入可致命。
操作时戴手套、护目镜。
始终在通风橱中操作。
10.氯化铯:可因吸入、咽下或皮肤吸收而危害健康。
操作时戴手套和护目镜。
DTT: 很强的还原剂,散发难闻的气味。
可因吸入、咽下或皮肤吸收而危害健康。
当使用固体或高浓度储存液时,戴手套和护目镜,在通风橱中操作。
11.甲醛:毒性较大且易挥发,也是一种致癌剂,易通过皮肤吸收,对眼睛、粘膜和上呼吸道有刺激和损伤作用。
避免一如其挥发的气雾。
戴手套和护目镜。
始终在通风橱中操作。
远离热、火花及明火。
12.TRIzol ,对眼睛有刺激性,腐蚀皮肤。
有一次不小心溅出一小滴在脸上,马上就红了,过一会儿感觉到疼,一周之后才好。
医疗器械未知可沥滤物评价方法建立及表征技术审查指导原则

医疗器械未知可沥滤物评价方法建立及表征技术审查指导原则—•刖S对医疗器械进行充分的化学表征是医疗器械产品设计开发环节中重要内容,可以为材料的选择、工艺优化等提供证据,同时医疗器械的化学表征提供了医疗器械生物学评价和毒理学风险评估所必须的信息”除此之外”化学表征还可以:1.支持再处理医疗器械的生物学安全性;2.临床使用条件下可沥滤物的识别和量的确定可用于支持毒理学风险评估;3.在临床接触性质相同时,支持医疗器械与市售器械的等同性;4.支持生产工艺(如灭菌工艺、清洁工艺等)、生产地址、材料或组件、供应商等发生变更时,与市售器械的等同性;5.支持拟用材料与市售器械/材料在材料组成或浸出物谱(extractable profile )方面的等同性;6.支持器械终产品与原型器械(prototype device )的等同性评估;7.针对器械的临床预期应用,支持新材料的筛选等。
需要说明的是,单纯的化学表征一般不足以证明器械/材料的等同性,也不足以确定器械/材料的生物相容性,需要由具备专门知识且经验丰富的人评估其充分性,必要时需要结合毒理学资料、器械/材料的物理学特征、后续处理、临床用途等进行综合评估。
医疗器械的化学表征一般包括确定产品组分成分研究(如产品结构、成分、理化特性等),浸提研究(extractable study )、可沥滤物硏究(leachable study )等,可沥滤物研究是医疗器械化学表征的重要内容。
医疗器械可沥滤物(Leachables )是指医疗器械或材料在临床使用过程中释放出的物质的统称,一般包括灭菌残留剂、工艺残留物、降解产物以及材料中的单体及添加剂(包括稳定剂、抗氧化剂、增塑剂、着色剂等)等。
作为医疗器械生物学评价的一部分,需要评估医疗器械产品在与人体直接或间接接触并发挥作用的过程中,可沥滤物对人体安全性方面的潜在风险。
根据可沥滤物研究体系不同,分为根据相关信息识别的已知可沥滤物(Target Leachables )和根据未知可沥滤物硏究体系鉴别的未知可沥滤物(Unspecified or Unknown Leachables)o本指南即提供了未知可沥滤物研究体系的一般要求。
化妆品微生物标准检验方

如有均质器,则采用无菌样品袋,将上述水溶性膏、霜、粉剂等,称10g样品加入90mL灭菌生理盐水,均质1min~2min;疏水性膏、霜及眉笔、口红等,称10g样品,加10mL灭菌液体石蜡,10mL吐温80,70mL灭菌生理盐水,均质3min~5min。
菌落总数
1范围
本标准规定了化妆品中菌落总数的检验方法。
本标准适用于化妆品菌落总数的测定。
2术语和定义
下列术语和定义适用于本标准:
菌落总数aerobic bacterial count化妆品检样经过处理,在一定条件下培养后(如培养基成分、培养温度、培养时间、pH值、需氧性质等),1g(1mL)检样中所含菌落的总数。所得结果只包括一群本方法规定的
条件下生长的嗜中温的需氧性和兼性厌氧菌落总数。测定菌落总数便于判明样品被细菌污染
10-1 10-2 10-3两稀释度
菌数之比
菌落总数
(CFU/mL或CFU/g)
报告方式
(CFU/mL或CFU/g)
1 1365 164 20─16400 16000或1.6×104 2 2760 295 46 1.6 38000 38000或3.8×104 3 2890 271 60 2.2 27100 27000或2.7×104 4不可计4650 513─513000 510000或5.1×105 5 27 11 5─270 270或2.7×102 6不可计305 12─30500 31000或3.1×104 7 0 0 0─<1×10
3仪器
3.1恒温水浴箱或隔水式恒温箱:44℃±0.5℃。
3.2温度计。
3.3显微镜。
3.4载玻片。
3.5接种环。
3.6电磁炉。
3.7三角瓶,250mL。
危险化学品目录表二

有机过氧化物,C型
单过氧马来酸叔丁酯[含量≤52%,糊状物]
tert-butyl monoperoxymaleate (not more than 52% as a paste)
107-08-4
易燃液体,类别3
185
2-碘丙烷
异丙基碘;碘代异丙烷
2-iodopropane;isopropyl iodide;iodo-iso-propane
75-30-9
易燃液体,类别3
186
1-碘丁烷
正丁基碘;碘代正丁烷
1-iodobutane;n-butyl iodide;iodo-n-butane
严重眼损伤/眼刺激,类别1
特异性靶器官毒性-一次接触,类别3(呼吸道刺激)
190
碘化亚汞
一碘化汞
mercurous iodide;mercurous monoiodide
15385-57-6
急性毒性-经口,类别2*
急性毒性-经皮,类别1
急性毒性-吸入,类别2*
特异性靶器官毒性-反复接触,类别2*
危害水生环境-急性危害,类别1
遇水放出易燃气体的物质和混合物,类别3
严重眼损伤/眼刺激,类别2
皮肤致敏物,类别1
生殖毒性,类别2
危害水生环境-急性危害,类别1
危害水生环境-长期危害,类别1
171
单过氧马来酸叔丁酯[含量>52%]
tert-butyl monoperoxymaleate (more than 52%)
化妆品中灰黄霉素等9种抗真菌类禁用物质的检测方法
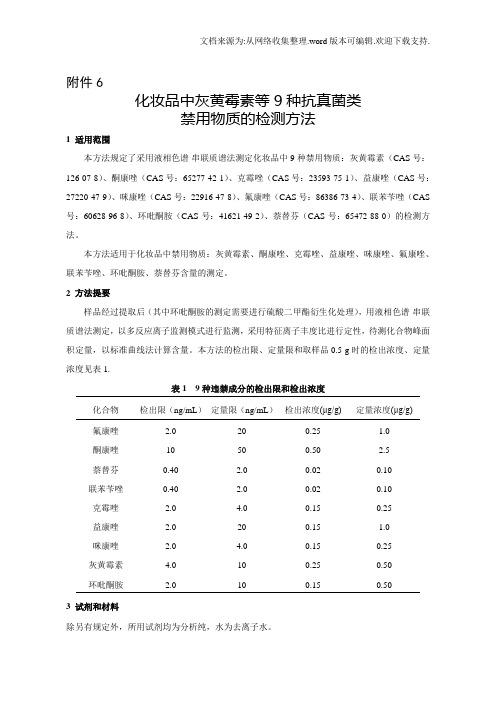
附件6化妆品中灰黄霉素等9种抗真菌类禁用物质的检测方法1 适用范围本方法规定了采用液相色谱-串联质谱法测定化妆品中9种禁用物质:灰黄霉素(CAS号:126-07-8)、酮康唑(CAS号:65277-42-1)、克霉唑(CAS号:23593-75-1)、益康唑(CAS号:27220-47-9)、咪康唑(CAS号:22916-47-8)、氟康唑(CAS号:86386-73-4)、联苯苄唑(CAS 号:60628-96-8)、环吡酮胺(CAS号:41621-49-2)、萘替芬(CAS号:65472-88-0)的检测方法。
本方法适用于化妆品中禁用物质:灰黄霉素、酮康唑、克霉唑、益康唑、咪康唑、氟康唑、联苯苄唑、环吡酮胺、萘替芬含量的测定。
2 方法提要样品经过提取后(其中环吡酮胺的测定需要进行硫酸二甲酯衍生化处理),用液相色谱-串联质谱法测定,以多反应离子监测模式进行监测,采用特征离子丰度比进行定性,待测化合物峰面积定量,以标准曲线法计算含量。
本方法的检出限、定量限和取样品0.5 g时的检出浓度、定量浓度见表1.表19种违禁成分的检出限和检出浓度化合物检出限(ng/mL)定量限(ng/mL)检出浓度(μg/g)定量浓度(μg/g)氟康唑 2.0 20 0.25 1.0酮康唑10 50 0.50 2.5萘替芬0.40 2.0 0.02 0.10联苯苄唑0.40 2.0 0.02 0.10克霉唑 2.0 4.0 0.15 0.25益康唑 2.0 20 0.15 1.0咪康唑 2.0 4.0 0.15 0.25灰黄霉素 4.0 10 0.25 0.50环吡酮胺 2.0 10 0.15 0.503 试剂和材料除另有规定外,所用试剂均为分析纯,水为去离子水。
3.1 乙腈,色谱纯。
3.2 硫酸二甲酯,分析纯。
3.3 三乙胺,分析纯。
3.4 乙酸,色谱纯。
3.5 氯化钠,分析纯。
3.6 氢氧化钠,分析纯。
3.7 灰黄霉素、酮康唑、克霉唑、益康唑、咪康唑、氟康唑、联苯苄唑、环吡酮胺、萘替芬对照品(纯度大于97 %)。
化妆品组分限用物质、组分中英对照

46 47 48 49 50 51 52 53 54 55 56 57 58 59 60 61 62 63 64 65 66 67 68 69 70 71 72 73 74 75 76 77 78
麝香二甲苯 水溶性锌盐(苯酚磺酸锌和吡硫鎓锌除外) 2-溴-2-硝基丙烷-1,3二醇 5-溴-5-硝基-1,3-二噁烷 7-乙基双环噁唑烷 烷基(C12-C22)三甲基铵溴化物或氯化物(2) 苯扎氯铵,苯扎溴铵,苯扎糖精铵(2) 苄索氯铵 苯甲酸及其盐类和酯类(2) 苯甲醇(2) 甲醛苄醇半缩醛 溴氯芬 氯己定及其二葡萄糖酸盐,二醋酸盐和二盐酸盐 三氯叔丁醇 苄氯酚 氯二甲酚 氯苯甘醚 氯咪巴唑 脱氢乙酸及其盐类 双(羟甲基)咪唑烷基脲 二溴己脒及其盐类,包括二溴己脒羟乙磺酸盐 二氯苯甲醇 二甲基噁唑烷 DMDM乙内酰脲 甲醛和多聚甲醛(2) 甲酸及其钠盐 戊二醛 己脒定及其盐,包括己脒定二个羟乙基磺酸盐和己脒定 对羟基苯甲酸盐 海克替啶 咪唑烷基脲 无机亚硫酸盐类和亚硫酸氢盐类(2) 碘丙炔醇丁基氨甲酸酯 甲基异噻唑啉酮 甲基氯异噻唑啉酮和甲基异噻唑啉酮与氯化镁及硝酸 镁的混合物(甲基氯异噻唑啉酮:甲基异噻唑啉酮为3:1) 邻伞花烃-5-醇 邻苯基苯酚及其盐类 4-羟基苯甲酸及其盐类和酯类(3) 对氯间甲酚 苯氧乙醇 苯氧异丙醇(2) 吡罗克酮和吡罗克酮乙醇胺盐 聚氨丙基双胍 丙酸及其盐类 水杨酸及其盐类(2) 苯汞的盐类,包括硼酸苯汞
307 308 309 310 311 312 313 314 315 316 317 318 319 320 321 322 323 324 325 326 327 328 329 330 331 332 333 334 335 336 337 338 339 340 341 342 343 344 345 346 347 348 349 350 351 352 353 354 355 356
ICH残留溶剂指南(中文翻译)

5.4 残留溶剂在活性物质、赋形剂和药品中残留溶剂的级别限度International Conference on Technical Requirements for Registration of Pharmaceuticals for Human Use (ICH)已采用了关于残留溶剂的杂质指南,它规定了生产后允许残留在活性物质、赋形剂和药品中溶剂的含量限度。
本指南(文本复制见下文)不包括已上市的产品。
然而欧洲药典应用了存在的活性物质、赋形剂和药品指南中同样的原理,无论它们是否药典专论主题。
所有物质和产品都需要测定可能存在于物质或产品中的残留溶剂的含量。
如果异类溶剂的使用已被证明其合理性也已授权,那么它会在各个专论的测试部分受限定。
通常,药典专论不包括单一二类溶剂的测试限度,因为该类溶剂随生产商的不同变化很大。
因而生产工艺中使用该类溶剂时应通知主管当局。
这个通知也应随用于证明欧洲药典的实用型的档案一同提交,并在证明中提及。
当生产工艺中只使用了三类溶剂,可应用干燥失重测试,该测试应在单一专论中叙述。
如果三类溶剂的限度大于0.5%,并已经证明合理性和授权,那么还要求有该溶剂的指定的检测方法。
在这种情况下,限度在单一专论中给出,因为定义指的是无水和无溶剂的物质。
在所有情况下,应巴使用的溶剂通知主管当局。
至于二类溶剂,该通知已在适用性证明中提及。
当使用了一类残留溶剂或二类残留溶剂(或三类残留溶剂超过0.5%),应尽可能使用在一般方法(2.4.24)中叙述的方法学。
否则应使用经适当验证的方法。
杂质:残留溶剂指南CPMP/ICH/283/95)1. 引言2. 指南的范围3. 一般原则3.1. 危险评估对溶剂的分类3.2. 规定暴露限度的方法3.3. 二类溶剂的限度叙述的选择3.4. 分析规程3.5. 残留溶剂的报告水平4. 残留溶剂的限度4.1. 避免使用的溶剂4.2. 规定限度的溶剂4.3. 低毒性潜能的溶剂4.4. 未发现充分毒性数据的溶剂词汇表附录1. 溶剂列表包括指南附录2. 附加背景资料附录2.1: 有机挥发性溶剂的环境规程附录2.2: 药物中的残留溶剂附录3. 规定暴露限度的方法1. 引言⋯⋯(原文不清楚)。
化妆品中地氯雷他定等15种物质的检测方法

化妆品中地氯雷他定等15种物质的检测方法1 范围本方法规定了采用高效液相色谱-串联质谱法测定化妆品中地氯雷他定(CAS No:100643-71-8)、氯苯那敏(CAS No:132-22-9)、阿司咪唑(CAS No:68844-77-9)、曲吡那敏(CAS No:91-81-6)、溴苯那敏(CAS No:86-22-6)、苯海拉明(CAS No:58-73-1)、异丙嗪(CAS No:60-87-7)、羟嗪(CAS No:68-88-2)、奋乃静(CAS No:58-39-9)、西替利嗪(CAS No:83881-51-0)、氟奋乃静(CAS No:69-23-8)、氯丙嗪(CAS No:50-53-3)、氯雷他定(CAS No:79794-75-5)、特非那定(CAS No:50679-08-8)、赛庚啶(CAS No:129-03-3)等15种抗组胺类物含量的方法。
本方法适用于膏霜、乳液、水剂和啫喱等类型化妆品中地氯雷他定、氯苯那敏、阿司咪唑、曲吡那敏、溴苯那敏、苯海拉明、异丙嗪、羟嗪、奋乃静、西替利嗪、氟奋乃静、氯丙嗪、氯雷他定、特非那定、赛庚啶含量的测定。
2 方法提要以甲醇为溶剂提取化妆品中抗组胺类物质,用高效液相色谱仪分离,质谱检测器检测,采用保留时间和特征离子对丰度比定性,以待测物质相对应离子峰面积定量,以标准曲线法计算含量。
本方法对15种抗组胺类物质的检出限均为1 ng/mL,定量下限均为2 ng/mL,如以取样0.2 g计,检出浓度均为250 ng/g,定量下限浓度均为500 ng/g。
3 试剂和材料除另有规定外,试剂均为分析纯,水为一级实验用水。
3.1 甲醇,色谱纯。
3.2 甲酸,色谱纯。
3.3 甲酸铵,色谱纯。
3.4 甲酸铵-甲酸水溶液:称取甲酸铵(3.3)6.3 g,加1 mL甲酸(3.2),加水1000 mL溶解,用0.22 µm滤膜过滤。
3.5 标准品,参考附录A。
进口药品注册标准目录2

C
冰片 苯甲醇 苯甲酸钠 苯扎氯铵 苯扎溴铵 倍他环糊精 薄荷脑 薄荷素油(薄荷油) 薄膜包衣预混辅料(胃 温州小伦包衣技术有限公司 溶型) 薄膜包衣预混剂(胃溶 上海新菲尔生物制药工程技术有限公司 型) 上海现代制药股份有限公司 (欧巴代) 上海卡乐康包衣技术有限公司 薄膜包衣预混剂(肠溶 上海现代制药股份有限公司 型) (欧巴代) 上海卡乐康包衣技术有限公司 川蜡 沧州森林蜡业有限公司 醋酸钠 台山市新宁制药有限公司 北京市燕京药业有限公司 肠溶空心胶囊 安徽黄山胶囊有限公司
聚乙二醇400
聚乙二醇4000 聚乙二醇6000 聚乙烯吡咯烷酮 聚丙烯酸树脂Ⅱ 交聚维酮
药品生产企业使用药用辅料调查情况汇总表
交联聚维酮 交联羧甲基纤维素钠 焦亚硫酸钠 枸橼酸 International Specialty Products Inc.(美国进口) Fmc Corporation (美国进口) 湖南尔康制药有限公司 湖南华日制药有限公司 无锡市第二制药厂 台山市新宁制药有限公司 湖南尔康制药有限公司 无锡市第二制药厂 苏州胶囊有限公司 上海广得利胶囊有限公司 安徽黄山胶囊有限公司 镇江力凡胶囊有限公司 新昌县沃洲胶丸有限公司 浙江省新昌县天姥山胶囊有限公司 江苏省勤奋药业有限公司 湖南九典制药有限公司 湖南九典制药有限公司 湖州展望药业有限公司 湖州展望药业有限公司 上海宝达化工有限公司 Shin-Etus Chemical Co.,Ltd.(日本进口) 潍坊盛泰药业有限公司 潍坊盛泰药业有限公司 华北制药康欣有限公司 上海医药(集团)有限公司 自贡鸿鹤制药有限责任公司 台山市新宁制药有限公司 进口药品注册证号:H20030418 进口药品注册证号:H20030197 湘食药辅准字F20050004 国药准字H43020597 国药准字H32023986 国药准字H44020360 湘食药辅准字F20050005 国药准字H32022214 苏卫药准字(88)第3010-15号 沪卫药准字(1995)第197001号 皖药准字(2001)J005675号 苏卫药准字(1983)第301003号 国药准字F20020012 国药准字F20050018 国药准字H32020718 国药准字H20054379 国药准字H20050387 国药准字H33020093 浙卫药准字(1996)第174701号 国药准字H31021940 进口药品注册证号:H20060056 国药准字H37022663 国药准字H37022664 国药准字H13022450 国药准字H31020173
气相色谱-质谱法测定化妆品中10种防腐剂

气相色谱-质谱法测定化妆品中10种防腐剂王改香;张磊;唐晓军;张锁慧;赵鑫;胡国胜【摘要】采用气相色谱-质谱法(GC-MS)同时测定化妆品中10种防腐剂含量.样品经甲醇超声提取,无水硫酸钠脱水后过滤进样检测.采用Agilent HP-5MS毛细管色谱柱(30 m×0.25 mm,0.25μm)分离,程序升温,分流进样进行测定.结果表明:17 min内即可完成10种防腐剂的测定,各防腐剂的质量浓度均在5.00~100 mg · L-1范围内与峰面积呈线性关系,方法的检出限(3S/N)为0.30~0.70 ng.方法用于化妆品测定,加标回收率在96.5%~105%之间,测定值的相对标准偏差(n=6)在0.66%~3.2%之间.【期刊名称】《理化检验-化学分册》【年(卷),期】2015(051)001【总页数】4页(P35-38)【关键词】气相色谱-质谱法;防腐剂;化妆品【作者】王改香;张磊;唐晓军;张锁慧;赵鑫;胡国胜【作者单位】上海相宜本草化妆品股份有限公司,上海200444;上海相宜本草化妆品股份有限公司,上海200444;上海相宜本草化妆品股份有限公司,上海200444;上海相宜本草化妆品股份有限公司,上海200444;上海相宜本草化妆品股份有限公司,上海200444;上海相宜本草化妆品股份有限公司,上海200444【正文语种】中文【中图分类】O657.7尼泊金酯类是对羟基苯甲酸酯的总称,此类防腐剂是目前应用最为广泛的防腐剂之一,用量相对较大,随着其碳链的增长,抗菌效果提升,但其水溶性逐渐变差,一般都是一种或者几种尼泊金酯与其他防腐剂如苯氧乙醇、甲基异噻唑啉酮、甲基氯异噻唑啉酮、碘丙炔醇丁基氨甲酸酯(IPBC)等复配使用[1]。
近年来,人们对尼泊金酯类的关注越来越多,主要集中于两点:一是对羟基苯甲酯类的苯环,在极低的浓度能被检测出来,而且由于其是亲脂性的,所以在脂肪组织中的某种累积可能会发生。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
乌克兰 2017 年度真实 买家/进口商/收货人/采购商 排名 UKRAINE Active and Exact Importers 更多买家信息、采购信息、进出口交易记录、进出口贸易数据、真实交易记录、请与瀚闻资讯联系 Please visit our website to get more import and export trade information
数据来源:全球最大贸易统计数据库—GTA
登录 查询更多贸易大数据
click to get more information
按采购金额排序 Ranked by import amount
排名 Rank 1 2 3 4 5 6 7 8 9 10 公司名称/Company Name ТОВ "Галеан ",Лтд ТОВ "Інбел" ТОВ "М ІКРОФАРМ " ТОВ "БАЛКОРМ " ТОВ "КРЕМ ІКС" ТОВ "ТД "СВІТ-АГРО " ТОВ "ЛЕКО СТАЙЛ " ТОВ "ЛЕКО ФАРМ " ТОВ "АЛЬФА -ВЕТ" ТОВ "РЕВАДА -УКРАЇНА "
全球最大的贸易统计数据库 – GTA2017 年终统计结果显示: 2017 年 1-12 月 未混合的 D 或 DL-泛酸及其衍 生物(不论是否溶于溶剂) (商品编码 293624)乌克兰进口商共计 31 个 GTA (Global Trade Analysis System), the world's largest trade intelligence database shows that there are 31 UKRAINE Importers of --D-or DL-Pantothenic acid (Vitamin B3 or Vitamin B5) and its derivatives (HS CODE 293624) in 2017
未混合的 D 或 DL-泛酸及其衍生物(不论是否溶于溶剂) (HS 293624) 乌克兰(31 个)进口商排名(按进口额排名) --D-or DL-Pantothenic acid (VitБайду номын сангаасmin B3 or Vitamin B5) and its derivatives (HS 293624)2017 UKRAINE Importer Rankings
