201512药讯.
2015年1季度药讯整体最终

【药事动态】国办印发《关于完善公立医院药品集中采购工作的指导意见》近日,国务院办公厅印发了《关于完善公立医院药品集中采购工作的指导意见》(以下简称《意见》),这是深化医药卫生体制改革的一项重大举措,对于加快公立医院改革,规范药品流通秩序,完善国家药物政策,建立健全以基本药物制度为基础的药品供应保障体系具有重要意义。
《意见》全面贯彻落实党的十八大和十八届二中、三中、四中全会精神,按照市场在资源配置中起决定性作用和更好发挥政府作用的总要求,借鉴国际药品采购通行做法,充分吸收基本药物采购经验,围绕“招什么、怎么招,怎么配送,怎么结算,如何监管”等关键环节,提出了一系列有针对性的具体措施:一是放管结合,根据药品供应保障情况实行分类采购,对不同药品分别采取双信封制公开招标采购、谈判采购、医院直接采购、定点生产等方式,调动药品生产企业积极性,增强医院参与度。
这是完善公立医院药品集中采购政策的一大亮点。
二是改进药款结算方式。
明确药款结算时限,强化合同约束。
鼓励药品生产企业与医院直接结算药品货款,与配送企业结算配送费用,进一步减少中间环节。
三是加强药品配送管理。
强化生产企业主体责任,确保药品配送及时到位,重点保障偏远、交通不便地区药品供应配送,鼓励各地结合实际探索县乡村一体化配送。
四是规范采购平台建设。
拓展省级药品集中采购平台功能,推动药品采购编码标准化,实现药品采购数据共享和互联互通。
公立医院使用的所有药品(不含中药饮片)均应通过省级药品集中采购平台采购。
五是强化综合监督管理。
全面推进信息公开,确保药品采购各环节在阳光下运行,严格执行诚信记录和市场清退制度,严肃查处医院和药品生产经营企业违法违规行为。
《意见》强调,药品集中采购要有利于破除以药补医机制、加快公立医院特别是县级公立医院改革,有利于降低药品虚高价格、减轻人民群众用药负担,有利于预防和遏制药品购销领域腐败行为、抵制商业贿赂,有利于推动药品生产流通企业整合重组、公平竞争,促进医药产业健康发展。
药讯第2期

头孢替安使用注意事项从医院规定皮试用原液后不久,泌尿科和心内科均反映了注射用盐酸头孢替安按新的皮试方法进行皮试后的假阳性率明显升高。
从病历及处方抽查结果来看,头孢替安使用几乎涉及到每个临床科室和大部分医务人员,其中也不乏一些不合理的用药情况。
鉴于此情,我们收集并整理了头孢替安的一些相关知识,现介绍给大家,希望有所帮助。
头孢替安系半合成第二代头孢菌素,抗菌作用机制与其他头孢类抗生素相似,最早由日本武田公司开发研制成功,1981年以商品名Pansporin在日本及台湾上市,以后在东南亚及欧美多国上市,USP24版有收载,国外上市规格有0.25g、0.5g、1.0g。
目前我院将其纳入限制级抗菌药物管理,与之同属二代头孢或相当于二代头孢的药物还有有头孢呋辛(非限制)、头孢丙烯(限制级)和头孢西丁(限制级)。
一、作用特点对革兰阳性菌的作用与头孢唑林接近,对革兰阴性菌,如嗜血杆菌、大肠埃希菌、克雷伯杆菌、奇异变形杆菌等作用较优,对肠杆菌、枸橼酸杆菌、吲哚阳性变形杆菌等也有抗菌作用。
可用于全身感染,具体见说明书。
二、用法用量通常,成年人一日0.5~2g,分2~4次;小儿一日40~80mg/kg,分3~4次, 静脉给药。
本品可随年龄和症状的不同适当增减,对成年人败血症一日量可增至4g,对小儿败血症等重症和难治性感染,一日量可增至160mg/kg。
肾功能不全时剂量,肌酐清除率等于或大于16.6ml/min者,不需调整剂量;肌酐清除率小于16.6ml/min者,每6~8小时用量应减为常用剂量的75%。
静脉注射及静脉滴注。
静脉注射时,可用生理盐水或葡萄糖注射溶液溶解后使用。
此外也可将本品的一次用量0.25~2g添加到葡萄糖注射液、电解质或氨基酸等输液中于30分钟至2小时内静脉滴注,对小儿则可参看前面所述给药量,添加到补液中后于30分钟至1小时内静脉滴注。
三、毒理作用毒理研究显示对肾脏的影响与头孢噻吩大致相同,偶尔出现急性肾功能衰竭等严重肾障碍,因而应定期实行检查,充分观察,出现异常情况时,应中止给药,并做适当处置。
2015年2月药物快讯

年月药物快讯新药批准. 年月日,勃林格殷格翰和礼来宣布已通过()治疗型糖尿病的申请。
. 年月日爱尔康宣布通过了用于缓解眼部过敏致痒的申请。
. 年月日,卫材宣布批准卢非酰胺用于岁儿童综合征的辅助治疗。
. 年月日,辉瑞宣布加速批准了用于晚期乳腺癌的治疗。
. 年月日,宣布已批准联合利妥昔单抗、环磷酰胺、阿霉素和泼尼松用于未经治疗且不适合进行造血干细胞移植的套细胞淋巴瘤的治疗。
. 年月日,宣布已批准来尼珠单抗用于糖尿病性黄斑水肿患者的糖尿病性视网膜病变。
. 年月日,宣布已批准用于急性外耳道炎的治疗。
. 年月日,卫材宣布批准乐伐替尼用于甲状腺癌的治疗。
. 年月日,诺华报道授予加速批准资格,批准其与硼替佐米和地塞米松联合治疗多发性骨髓瘤,早前年月日被授予治疗多发性骨髓瘤的孤儿药资格。
. 年月日,报道已获欧盟有条件上市许可,用于因(物理或化学因素所致)眼部灼伤导致的中度至重度角膜缘干细胞缺乏症,这也是世界首个干细胞治疗产品。
. 年月日,宣布通过用于岁季节性过敏性鼻炎的患者治疗的申请。
. 年月日,宣布已通过来那度胺治疗新发多发性骨髓瘤的补充申请。
早前年月日也批准了该治疗的申请。
. 年月日,阿特维斯宣布批准了用于和的治疗。
其日期也是年第一季度。
. 年月日,赛诺菲宣布批准了用于治疗、型糖尿病。
突破性疗法. 年月日,罗氏的获得突破性疗法资格,用于的治疗。
. 年月日,授予了蓝鸟治疗重型β地中海贫血的突破性疗法资格。
. 年月日,宣布授予治疗阳性成胶质细胞瘤的突破性疗法资格。
快速审评. 年月日,宣布授予其研发的一种盐酸纳洛酮鼻腔制剂快速审评资格,该药物用于阿片类药物过量。
. 年月日,生物医药于宣布授予了治疗原发性胆汁性肝硬化的快速审评资格,欧盟也授予了该药物孤儿药资格。
优先审评. 年月日,宣布授予治疗晚期软组织肉瘤的优先审评资格。
. 年月日,诺华报道已受理治疗心衰的申请,并授予了优先审评资格,日期为年月。
. 年月日,宣布授予优先审评资格,该公司年月日提交了与威罗菲尼联合治疗黑色素瘤的申请,预计获批日期为年月日。
2015年第一季度药讯汇编

玛纳斯县人民医院药讯(2015年第01期)玛纳斯县人民医院药剂科 2015-3 内部资料目录静水深流看医改……………………………………………………………2-4页欧盟评估氨溴索和溴己新的严重过敏反应风险…………………………4-5页复方氨基酸注射液的合理使用……………………………………………5-9页补钾的基本常识…………………………………………………………10-12页抗菌药物监测指标相关知识介绍………………………………………12-14页警惕苯溴马隆的肝损害风险……………………………………………15-18页详解各类降糖药优缺点比较……………………………………………19-21页第一季度抗菌药物及其合理用药统计分析汇总………………………22-33页第一季度合理用药及细菌耐药预警提示………………………………33-页俗话说:“没啥别没钱,有啥别有病”。
一人生病全家忙,有担忧,有叹息,有无奈,有眼泪。
看病难、看病贵,成了每个人心中的痛点。
又是一年岁尾时,医改究竟改了啥?有一个词叫“静水深流”,意思是水面风平浪静,水下激流涌动,这种变化往往不易觉察。
如今,医改进入“深水区”,不会总是波澜壮阔、风起云涌,而是静中有动、由浅及深,这也是一种新常态。
2014 年,医改迎难而上,可圈可点,真的很给力。
医改是一道世界性难题,公立医院改革又是难中之难。
看病难、看病贵,主要集中在城市大城市。
2014 年,我国拉开城市公立医院改革序幕。
浙江省所有公立医院取消药品加成,率先告别“以药补医”时代。
全国已有 2300 多个县级公立医院取消了药品加成,调整了医疗服务价格。
福建省三明市打出漂亮的“组合拳”,让公立医院回归公益性质、让医生回归看病角色、让药品回归治病功能,实现了百姓可接受、基金可运行、财政可持续,工资总额核定不与药品、耗材、检查、化验挂钩,扭转了医院和医生的逐利行为。
事实证明,“三明模式”提供了城市公立医院综合改革的生动范例。
2015版药典变化统计.

2015版新药典变化总结1.药典一部收载药材和饮片、植物油脂和提取物、成方制剂和单味制剂等,品种共计2598种,其中新增440种,修订517种,不收载7种。
2.重新建立规范的编码体系,并首次将通则、药用辅料单独作为《中国药典》四部。
3.完善了“药材和饮片检定通则”“炮制通则”和“药用辅料通则”。
4.制定了中药材及饮片中二氧化硫残留量限度标准,建立和完善重金属及有害元素、黄曲霉毒素、农药残留量等物质的检测限度标准。
5.中药材增加专属性的显微鉴别检查、特征氨基酸含量测定等。
6.不再新增处方中含羚羊角、豹骨、龙骨、龙齿等濒危物种和化石的中成药品种。
历届药典中药收载数量对比:新药典增减药材情况:新增:新增药材品种来源:原标准木芙蓉叶,锦葵科木芙蓉Hibiscus mutabilis L.的干燥叶部颁中药材1册红花龙胆,龙胆科植物红花龙胆Gentiana rhodantha Franch.的干燥全草药典1977版岩白菜虎耳草科植物岩白菜Bergenia purpurascens(Hook. F. Et Thoms.)Engl.的干燥根茎药典1977版删除:紫河车新药典“来源”修订情况:品种(2015药典-2010药典)火麻仁本品为桑科植物大麻Cannabis sativa L.的干燥成熟果实。
本品为桑科植物大麻Cannabis sativa L.的干燥成熟种子。
花蕊石本品为变质岩类岩石蛇纹大理岩。
主含碳酸钙(CaCO3)本品为变质岩类岩石蛇纹大理岩附子……浸入胆巴的水溶液…………浸入食用胆巴的水溶液……菊花来源增加“怀菊”芦荟本品为百合科植物库拉索芦荟Aloe barbadensis Miller、好望角芦荟Aloe ferox Miller或其它同属近缘植物叶的汁液浓缩干燥物。
本品为百合科植物库拉索芦荟Aloe barbadensis Miller叶的汁液浓缩干燥物新药典“性状”修订情况品种:上为2015药典,下为2010药典切面白色或红棕色切面类白色至淡红棕色山银花灰毡毛忍冬……表面黄色或黄绿色……灰毡毛忍冬……表面绿棕色至黄白色华南忍冬……华南忍冬……子房有毛……川芎表面灰褐色或褐色表面黄褐色天麻表面黄白色至黄棕色表面黄白色至淡黄棕色太子参表面灰黄色至黄棕色表面黄白色断面较平坦,周边淡黄棕色,中心淡黄白色,角质样。
2015年第2季度11药讯

【药事动态】卫计委解读公立医院药品集中采购细则为进一步细化落实公立医院药品集中采购相关政策措施,增强对实际工作的指导性、操作性,近日,国家卫生计生委印发了《关于落实完善公立医院药品集中采购工作指导意见的通知》,要求各地充分发挥省级药品集中采购工作领导小组作用,落实部门责任分工,抓紧制订具体实施办法,明确时间进度表和技术路线图,确保今年内启动新一轮药品集中采购工作。
《通知》中的具体要求主要包括:一是合理确定药品采购范围。
由医院按照不低于上年度药品实际使用量的80%制定采购计划,药品采购预算一般不高于医院业务支出的25%-30%,报省级药品采购机构统一汇总。
省级药品采购机构在汇总分析医院药品采购计划基础上确定本省(区、市)的药品采购范围。
二是细化药品分类采购措施。
省级药品采购机构根据全省(区、市)上一年度公立医院所有药品采购总金额,按照每个品规采购金额的百分比排序,将占比排序累计不低于80%、且有3家及以上企业生产的基本药物和非专利药品纳入招标采购范围。
对专利药品和独家生产药品实行谈判采购,建立公开透明、多方参与的价格谈判机制,实行国家和省级谈判联动。
直接挂网采购药品包括妇儿专科非专利药品、急(抢)救药品、基础输液、常用低价药品以及暂不列入招标采购的药品,由省级药品采购机构将具备相应资质条件的企业集中挂网,医院直接与企业议价采购。
三是坚持双信封招标制度。
药品招标采购由生产企业直接投标,按照商务标书报价由低到高选择中标企业和候选中标企业。
根据仿制药质量一致性评价技术要求,科学设定竞价分组,促进有效竞争,从严控制中标企业数量。
明确各地开标时间统一集中在每年11月中下旬。
四是改进医院药款结算管理。
鼓励医院公开招标选择开户银行,通过互惠互利、集中开设银行账户,由银行提供相应药品周转金服务,加快医院付款时间,降低企业融资成本和药品生产流通成本。
医院将药品费用支出纳入预算管理,逐步实现药占比(不含中药饮片)总体降到30%以下。
2015年度药品审评报告

2015 年度药品审评报告国家食品药品监督管理总局药品审评中心2015 年,在国家食品药品监督管理总局的领导下,药品审评中心(以下简称药审中心)紧紧围绕“改革审评制度,解决审评积压,提高审评质量,完善审评体系”,不断推进各项工作,切实维护和促进公众健康。
根据国家食品药品监督管理总局有关工作要求,现将《2015 年度药品审评报告》予以发布。
一、2015 年主要工作措施及进展2015 年,药审中心深化制度改革,加强审评管理,消除审评积压,提升审评效率,确保审评质量,各项工作举措取得积极进展,为更好保障公众用药安全有效,促进公众健康奠定了基础。
(一)推进审评制度改革按照国务院、总局党组关于药品审评制度改革的要求和工作部署,2015 年,药审中心在改革审评管理制度、改进用人机制、强化审评质量管理等方面推出了多项改革举措,以全力推进审评制度改革。
改革审评管理制度。
在对创新药实行一次性批准临床试验、加强后续沟通交流与监管,以及有条件批准临床试验方面取得实质性进展;组织研究肿瘤适应症创新药临床试验备案管理的可行性;完善“立卷审查”快速审评方法,加快淘汰存在重大缺陷的注册申请,并为承接药品注册申请受理工作奠定了基础;强化以临床价值为导向的审评管理,完善适应症团队审评制度,探索建立项目管理人制度;逐步完善有关药品注册申请的优先审评制度,起草了《临床急需儿童用药申请优先审评审批品种评定的基本原则》,并上网征求意见。
改进用人机制。
制定首席审评员招聘方案,探索建立首席专业岗位制度,构建科学化、与国际接轨的审评体系;制定《审评员薪酬管理暂行办法》,探索研究多劳多得、优劳优得的动态评估绩效分配体系,以调动工作人员的创造性和积极性;平稳完成三至七级专业技术岗位设置工作,保证了审评人才梯队建设;起草完成《药审中心解决审评积压尽职免责与违规追责暂行规定》,为稳定与激励审评队伍,不断提高审评质量和效率进行探索;探索引入外部咨询机构和专业人员参与中心的管理制度建设等。
2015年版药典二部拟新增品种名单

曾用名
乳酸米力农注射液
克林霉素磷酸酯溶液
利培酮口腔崩解片
L-谷氨酰胺 L-谷氨酰胺胶囊 L-谷氨酰胺颗粒
第 3 页,共 10 页
序号 158 159 160 161 162 163 164 165 166 167 168 169 170 171 172 173 174 175 176 177
品种名称(2015年版药典名称) 谷胱甘肽片 妥布霉素地塞米松眼膏 妥布霉素地塞米松滴眼液 肝素钙 肝素钙注射液 尿素软膏 阿仑膦酸钠 阿仑膦酸钠片 阿仑膦酸钠肠溶片 阿卡波糖 阿卡波糖片 阿卡波糖胶囊 阿立哌唑 阿立哌唑口崩片 阿立哌唑片 阿立哌唑胶囊 阿昔洛韦葡萄糖注射液 阿昔莫司 阿昔莫司胶囊 阿那曲唑
附件1: 序号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51
品种名称(2015年版药典名称) 盐酸阿普林定片 盐酸纳美芬 盐酸纳美芬注射液 注射用盐酸纳洛酮 盐酸林可霉素滴耳液 盐酸林可霉素滴眼液 盐酸非那吡啶 盐酸非那吡啶片 盐酸罗哌卡因 盐酸罗哌卡因注射液 注射用盐酸罗哌卡因 盐酸舍曲林 盐酸舍曲林片 盐酸舍曲林胶囊 盐酸金刚乙胺 盐酸金刚乙胺片 盐酸金刚乙胺颗粒 盐酸法舒地尔 盐酸法舒地尔注射液 盐酸氟西汀 盐酸氟西汀片 盐酸氟西汀胶囊 盐酸氟桂利嗪片 盐酸氟桂利嗪分散片 盐酸班布特罗 盐酸班布特罗片 盐酸氨溴索注射液 盐酸氨溴索糖浆 盐酸特比萘芬 盐酸特比萘芬片 盐酸特比萘芬乳膏 盐酸特拉唑嗪 盐酸特拉唑嗪片 盐酸特拉唑嗪胶囊 盐酸羟考酮 盐酸羟考酮片 盐酸替扎尼定 盐酸替扎尼定片 盐酸硫必利 盐酸硫必利注射液 盐酸氮卓斯汀 盐酸氮卓斯汀片 盐酸氮卓斯汀鼻喷雾剂 盐酸瑞芬太尼 注射用盐酸瑞芬太尼 盐酸雷尼替丁泡腾颗粒 格列吡嗪缓释胶囊 格列美脲 格列美脲片 格列美脲胶囊 恩曲他滨 恩曲他滨胶囊 氨苄西林丙磺舒颗粒 第 7 页,共 10 页
2015农药百强企业销售业绩平稳
2015年第09期甘肃农业GAN SU AGRICULTURE 商道·营销资讯我国是农业生产大国同时也是农药生产大国,近年来我国由原先的农药进口大国变成现在的农药出口大国。
近年来农药行业竞争激烈,各个农药企业都在激流勇进中成长。
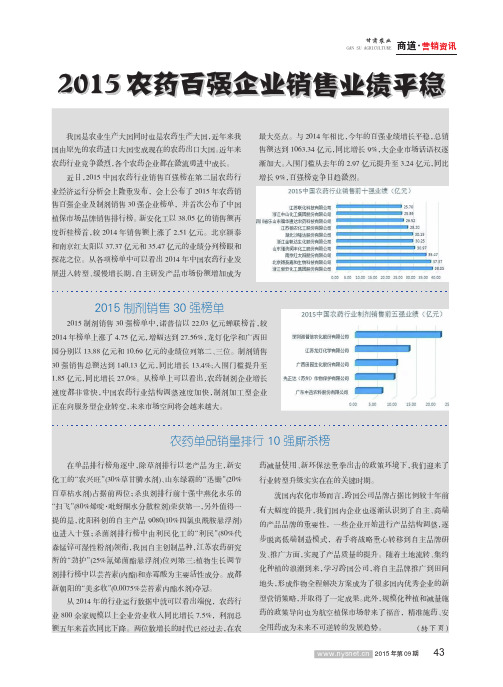
近日,2015中国农药行业销售百强榜在第二届农药行业经济运行分析会上隆重发布,会上公布了2015年农药销售百强企业及制剂销售30强企业榜单,并首次公布了中国植保市场品牌销售排行榜。
新安化工以38.05亿的销售额再度折桂榜首,较2014年销售额上涨了2.51亿元。
北京颖泰和南京红太阳以37.37亿元和35.47亿元的业绩分列榜眼和探花之位。
从各项榜单中可以看出2014年中国农药行业发展进入转型、缓慢增长期,自主研发产品市场份额增加成为最大亮点。
与2014年相比,今年的百强业绩增长平稳,总销售额达到1063.34亿元,同比增长9%,大企业市场话语权逐渐加大。
入围门槛从去年的2.97亿元提升至3.24亿元,同比增长9%,百强榜竞争日趋激烈。
在单品排行榜角逐中,除草剂排行以老产品为主,新安化工的“农兴旺”(30%草甘膦水剂)、山东绿霸的“迅锄”(20%百草枯水剂)占据前两位;杀虫剂排行前十强中燕化永乐的“扫飞”(80%烯啶·吡蚜酮水分散粒剂)荣获第一,另外值得一提的是,沈阳科创的自主产品9080(10%四氯虫酰胺悬浮剂)也进入十强;杀菌剂排行榜中由利民化工的“利民”(80%代森锰锌可湿性粉剂)领衔,我国自主创制品种,江苏农药研究所的“劲护”(25%氰烯菌酯悬浮剂)位列第三;植物生长调节剂排行榜中以芸苔素(内酯)和赤霉酸为主要活性成分。
成都新朝阳的“美多收”(0.0075%芸苔素内酯水剂)夺冠。
从2014年的行业运行数据中就可以看出端倪,农药行业800余家规模以上企业营业收入同比增长7.5%,利润总额五年来首次同比下降。
两位数增长的时代已经过去,在农药减量使用、新环保法重拳出击的政策环境下,我们迎来了行业转型升级实实在在的关键时期。
2015年药讯第一期

成都平安医院药讯二〇一五年第一期(总第09期)目录一、药事管理《一》抗菌药合理应用三部曲…01…二、药物不良反应《一》加拿大发布静脉注射用甲泼尼龙和肝损伤的安全性信息…06…《二》欧盟评估氨溴索和溴己新的严重过敏反应风险…09…《三》警惕苯溴马隆的肝损害风险…10…《四》加拿大发布关于多潘立酮的重要安全性信息…11…《五》警惕丙硫氧嘧啶的严重不良反应…13…三、药物与临床《一》甲氧氯普胺与其他药物的相互作用…17…《二》欧盟不推荐肾素-血管紧张素系统药物的联合使用…19…《三》静脉补钾溶媒须规范…23…《四》须警惕的八大临床常用配伍禁忌…25…四、医药资讯《一》埃博拉疫苗试验引发伦理争议…29…《二》美国FDA批准第二个抗MRSA抗生素…32…《三》口服胰岛素并非遥不可及…33…一、药事管理《一》抗菌药合理应用三部曲“处方集中药品品规的选择不仅要考虑临床常规各类感染的治疗需要,还应该考虑药品的安全性、价格以及细菌耐药情况”,药师的作用主要反映在对抗菌药治疗的干预、临床应用管理以及教育与培训三个方面。
干预药物治疗第一步:审核处方和医嘱审核处方和医嘱是患者用药安全的重要保障措施,是《处方管理办法》赋予药师的权力,也是药师不可推卸的责任。
药师应当对抗菌药物处方用药适宜性进行审核,审核内容包括:有无使用抗菌药物的指征,若有,选择用药是否合理;选用剂型与给药途径的合理性;药物的剂量、用法是否正确;是否有潜在临床意义的药物相互作用和配伍禁忌;患者用药是否有需要特别提醒关注的事项;医生的处方权限等。
药师经处方(或医嘱)审核后,认为存在用药不适宜时,应告知处方医师,请其确认或者重新开具处方。
当发现严重不合理用药或者用药错误时,药师可拒绝调剂,同时,及时告知处方医师,并进行记录,按照有关规定报告。
第二步:点评处方和医嘱处方和医嘱用药点评是一种事后干预方式,但对于药物治疗的持续改进具有重要作用。
抗菌药物专项点评是临床药师的重要职责,通过点评可以发现临床治疗中不合理使用抗菌药物的具体问题,将点评发现的问题提交医务部门进行干预。
2015年12月基本药物网上采购供应情况

流水号 82736 82735 80915 67194 74415 62698 63024 71148 67284 63638 71705 71269 74160 63589 64484 69331 63120 74448 60566 73225 65625 63693 60246 73226 63694 60249 84733 85025 70902 70740 60305 67283 67288 64400 63512 83734 85244 82692 81821 82856 85245 81886 63604 61299 60597 71683 70856 64217 68385 73811 69022 68427 64890 65593 76399 74636 84299 63202 60277 67617 82485 63370 73552 66963 65473 60892 60264 64734 66181 72701 71927 62372 64438 67632 70748 74863 73439 81152 82865 82864 68374 72054 70700 61141 72296 84991 82078 82080 75239 65876 65877 65880 85140 83166 81661 85519 63033 62129 68783 74738 74874 82639 83209 80107 84768 84213 84769 84894 85390 84893 82192 85009 84585 85412 83421 81108 81481 84891 82194 85064 80079 82147 80860 82045 81482 82992 82260 81105 80881 81772 84820 80044 80046 84843 84846 71595 60799 71596 60803 60206 60531 85008 83420 85570 82011 84880 84881 84700 82430 84838 81197 83688 81237 84699 84837 85623 84697 84835 64009 71337 64202 84079 81268 68653 65258 81555 81556 81552 81596 65328 65336 65353 65374 60506 72919 65929 82511 80568 81076 82804 80092 80517 83847 82657 84204 84205 85787 82199 82198 82165 82173 81000 82292 81001 83791 83794 72637 82848 82869 82870 80594 81302 84006 81546 85820 80301 85818 66702 64855 70314 60336 74164 60880 71146 65385 63852 75407 63678 66703 66462 68348 74105 68923 64425 60291 74403 66957 76030 71944 76759 71743 76001 70035 61471 80098 70866 70838 65512 72946 61464 70169 69240 65945 62031 75928 64118 62434 65349 61007 70147 73625 68380 74135 67393 81639 81796 81748 81635 80937 80846 67655 69458 61920 62191 65439 67763 60899 75525 67761 63545 65652 74361 73894 67515 65007 85155 83959 80077 80054 84441 83853 80332 81942 81806 83961 81905 85099 81102 80708 82673 83123 83954 81993 81288 80916 81103 81750 85229 83615 85379 83957 82897 83502 80832 81992 83061 80710 81317 81595 82682 80575 84428 82774 82742 81604 84254 80078 80769 81220 85488 81800 60729 66466 63199 63544 66513 82645 83976 83811 82197 80629 74534 69463 76676 76373 75727 66259 64047 70552 63200 64221 69283 67760 64319 64919 72491 71144 71488 66077 64984 61273 64032 67762 62890 71202 74237 71873 76305 73543 74162 66899 64164
2015版_中国药典目录.

558 椿皮 559 槐花 560 槐角 561 滇鸡血藤 562 满山红 563 煅石膏 564 矮地茶 565 蒲公英 566 蒲黄 567 蒺藜 568 蓍草 569 蓖麻子 570 蓝布正 571 蜂房 572 蜂胶 573 蜂蜜 574 蜂蜡 575 蜈蚣 576 路路通 577 锦灯笼 578 雷丸 579 榧子 580 榼藤子 581 槟榔 582 漏芦 583 磁石 584 罂粟壳 585 蓼大青叶 586 蔓荆子 587 蜘蛛香 588 蝉蜕 589 豨莶草 590 辣椒 591 酸枣仁 592 僵蚕 593 墨旱莲 594 暴马子皮 595 槲寄生 596 熟地黄 597 稻芽 598 蕤仁 599 蕲蛇 600 赭石 601 鹤虱
74 75 76 77 78 79 80 81 82 83 84 85 86 87 88 89 90 91 92 93 94 95 96 五加皮 五味子 五倍子 化橘红 升麻 天山雪莲 天仙子 天仙藤 天冬 天花粉 天竺黄 天南星 天麻 天然冰片(右旋龙脑) 天葵子 太子参 巴豆 巴豆霜 巴戟天 月季花 木瓜
514 鹿衔草 515 麻黄 516 麻黄根 517 黄山药 518 黄芩 519 黄芪 520 黄连 521 黄柏 522 黄精 523 黄蜀葵花 524 黄藤 525 斑蝥 526 棕榈 527 楮实子 528 款冬花 529 湖北贝母 530 滑石 531 滑石粉 532 焦栀子 533 焦槟榔 534 番泻叶 535 硫黄 536 筋骨草 537 紫石英 538 紫花地丁 539 紫花前胡 540 紫苏子 541 紫苏叶 542 紫苏梗 543 紫草 544 紫珠叶 545 紫菀 546 紫萁贯众 547 萹蓄 548 葛根 549 葶苈子 550 蛤壳 551 蛤蚧 552 锁阳 553 雄黄 554 鹅不食草 555 黑芝麻 556 黑豆 557 黑种草子 9
高警示药品目录2015

序号 药物类别
67 68 69 70 71 72 73 74 75 76 77 78 79 80 81 82 83 84 85 86 87 88 89 90 脂肪乳类药物 脂肪乳类药物 脂肪乳类药物 止血药 抗凝血药 口服降糖药 口服降糖药 口服降糖药 口服降糖药 口服降糖药 口服降糖药 口服降糖药 口服降糖药 口服降糖药 口服降糖药 口服降糖药 口服降糖药 口服降糖药 口服降糖药 麻醉药品 麻醉药品 麻醉药品 麻醉药品 皮肤科外用药
分级
A A A A A A A A A A A A A A A A A A A A A B B B B B B B B B B B
复方氨基酸注射液(18AA-Ⅱ) 250ml:21.25g 丙氨酰谷氨酰胺注射液 复方氨基酸(15)双肽(2)注射 液 复方氨基酸注射液(15AA) 复方氨基酸注射液(18AAVII) 复方氨基酸注射液(3AA) 复方氨基酸注射液(9AA) 利多卡因注射液 异丙嗪注射液 阿替普酶注射剂 低分子肝素钙注射液 100ml:20g 500ml:67g 250ml:20g 200ml 250ml:10.65g 250ml:13.98g 5ml:100mg 2ml:50mg 50mg 1ml:5000iu
2015年高警示药品目录
序号 药物类别
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 调节水、电解质及 酸碱平衡药物 调节水、电解质及 酸碱平衡药物 调节水、电解质及 酸碱平衡药物 调节水、电解质及 酸碱平衡药物 妇产科用药 精二药品 抗高血压药 抗心力衰竭 抗休克药物 抗休克药物 抗休克药物 抗休克药物 抗肿瘤药物 抗肿瘤药物 抗肿瘤药物 抗肿瘤药物 抗肿瘤药物 抗肿瘤药物 抗肿瘤药物 平喘药 神经系统用药 氨基酸类药物 氨基酸类药物 氨基酸类药物 氨基酸类药物 氨基酸类药物 氨基酸类药物 氨基酸类药物 局麻药品 抗变态反应药 抗凝血药 抗凝血药
【国际药讯】2015年9月14日-9月18日

【国际药讯】2015年9月14日-9月18日导读:艾尔建卡利拉嗪FDA首批;Nivolumab获第四个突破性疗法认定;VT-1129、CEM-102获QIDP资格;DTX101、CF102进入FDA快速通道;CAT-1004获罕见儿科疾病认定。
一、新药批准1.2015年9月15日消息,FDA批准Octapharma凝血因子VIIINuwiq(Simoctocog alfa)用于成人及儿童血友病A,此前该药已在欧盟等地获批。
2.2015年9月16日消息,FDA批准勃林格殷格翰SPIRIVA Respimat(噻托溴铵吸入剂)新适应症,用于12岁及以上哮喘患者维持治疗,该适应症此前已在欧日等国获批。
3.2015年9月17日消息,FDA批准艾尔建卡利拉嗪(Cariprazine)用于治疗成人躁狂或混合发作的双相情感障碍I型和精神分裂症,该药PDUFA日期为2015年9月。
二、突破性疗法认定1.2015年9月16日消息,FDA授予BMS PD-1免疫疗法Nivolumab治疗晚期或转移性肾细胞癌突破性疗法认定,此前Nivolumab还曾获非鳞NSCLC、恶性黑色素瘤及霍奇金病突破性疗法认定。
三、QIDP资格1.2015年9月16日消息,FDA授予Viamet羊毛甾醇14α-去甲基化(CYP51)酶抑制剂VT-1129治疗隐球菌脑膜炎QIDP资格,去年该疗法曾在美获孤儿药资格。
2.2015年9月18日消息,FDA授予Cempra CEM-102(口服夫西地酸片)QIDP资格,用于治疗ABSSSI,2013年FDA曾授予CEM-102孤儿药资格。
四、快速通道1.2015年9月17日消息,Dimension Therapeutics血友病B基因疗法DTX101进入FDA快速通道。
除DTX101外该公司还有血友病A基因疗法DTX201、鸟氨酸氨甲酰基转移酶缺乏基因疗法DTX301和糖原贮积病I型基因疗法DTX401。
药讯

药讯目录【合理用药】※哪些中西药不宜同服? (2)【药事瞭望】※国家基本药物制度介绍 (3)【用药知识】※如何提高小儿用药的依从性 (5)【药学文摘】※人血白蛋白的合理临床应用 (6)【合理用药】※哪些中西药不宜同服?在生活中,不少人都有中西药同服的习惯,认为可以加强疗效。
其实这种做法不科学。
(1)中成药舒肝丸不宜与西药胃复安合用,因舒肝丸中含有芍药,有解痉、镇痛作用,而胃复安则能加强胃的收缩,二者合用作用相反,会相抵药效。
(2)中成药止咳定喘膏、麻杏石甘片、防风通圣丸与西药复方降压片、优降宁不能同服。
前三种含有麻黄素,会使动脉收缩升高血压,影响降压效果。
(3)中成药蛇胆川贝液与西药吗啡、杜冷丁、可待因不能同服。
因为前者含有苦杏仁甙,与西药的毒性作用一样,都抑制呼吸,两者同服易导致呼吸衰竭。
(4)中成药益心丹、香莲丸、川贝枇杷含有生物碱,与西药阿托品、咖啡因同服会增加毒性,引起药物中毒。
(5)中成药益心丹、麝香保心丸、六味地黄丸不宜与西药心律平、奎尼丁同服,因可导致心脏骤停。
(6)中药虎骨酒、人参酒、舒筋活络酒与西药鲁米那等镇静止痛药同服可加强对中枢神经的抑制作用而发生危险。
(7)丹参片不宜与胃舒平合用,丹参片的主要成分是丹参酮、丹参酚、与胃舒平所含的氢氧铝化形成铝结合物,不易被肠道吸收,降低疗效。
(8)昆布片不宜与异烟肼合用,昆布片中含碘,在胃酸条件下,与异烟肼发生氧化反应,形成异烟酸、卤化物和氮气,失去抗结核杆菌功能。
(9)活络丹、香连片、贝母枇杷糖浆不宜与阿托品、咖啡因、氨茶碱合用。
因前者含乌头、黄连、贝母等生物碱成分,与后者同服,很易增加毒性,出现药物中毒。
(10)止咳片、通宣理肺丸、消咳宁片不宜与地高辛合用,因前者均含麻黄,麻黄碱对心脏有兴奋作用,能加强地高辛对心脏的毒性,引起心律失常。
(11)国公酒、壮骨酒、骨刺消痛液不宜与阿司匹林同服。
因前者含乙醇,合用则增加消化道的刺激性,引起食欲不振、恶心呕吐、严重时可导致消化道出血。
2015年二季度药讯正文

[医学动态]中东呼吸综合征常见问题本文摘自医脉通一、什么是中东呼吸综合征(MERS)?中东呼吸综合征(Middle East respiratory syndrome,MERS)是由一种新型冠状病毒(MERS-CoV)感染而引起的病毒性呼吸道疾病,2012年在沙特阿拉伯首次被发现。
冠状病毒是一组能够导致人类和动物感染发病的病毒,能够引起人类发生从普通感冒到严重急性呼吸综合征(SARS)的多种疾病。
二、中东呼吸综合征(MERS)发生在哪里?以下国家已经报告了MERS病例:中东地区的沙特阿拉伯、阿联酋、约旦、科威特、阿曼、卡塔尔、也门和黎巴嫩;非洲的埃及和突尼斯;欧洲的法国、德国、荷兰、希腊、意大利和英国;亚洲的菲律宾和马来西亚;以及北美的美国。
MERS-CoV似乎在整个阿拉伯半岛广泛循环。
近期中东以外地区报告的所有病例最初感染地均在中东,然后输入到中东以外地区。
这些旅行相关病例输入各国后似乎没有感染其他人。
2013年法国和英国的输入性病例曾导致有限的人与人之间的传播。
三、中东呼吸综合征(MERS)有那些症状?病例典型症状包括发热、咳嗽和气短等,检查中常可发现肺炎。
腹泻等胃肠道症状也有报道。
重症病例可导致呼吸衰竭,需要机械通气和重症监护。
部分病例可出现器官衰竭,尤其是肾衰竭和感染性休克。
已报告的MERS病例大约有27%已经死亡。
免疫力低下、老年人和伴有慢性病(如糖尿病、癌症和慢性肺部疾病)的人群更易发展为重症。
四、人类可以感染MERS-CoV而不发病么?是的。
在对病例密切接触者的随访和标本检测中发现,部分人感染MERS-CoV后并不出现症状。
五、人类是如何感染MERS-CoV的?还未确切了解MERS-CoV通过何种方式感染人类。
在一些病例中,MERS-CoV可通过与病例密切接触而传播。
这种情况常出现在家庭成员、病人和医务人员中,尤其最近医务人员感染病例增加。
一些社区病例未找到可能的传染源,其感染可能来源于动物、人或者其他传染源。
2015年国家药品质量公告2期

南充市食品 药品检验所 自贡市食品 药品检验所 广元市食品 药品检验所 绵阳市食品 药品检验所 绵阳市食品 药品检验所 广元市食品 药品检验所 乐山市食品 药品检验检 测中心 资阳市食品 药品检验所 达州市食品 药品检验所 巴中市食品 药品检验所 宜宾市食品 药品检验所 宜宾市食品 药品检验所 资阳市食品 药品检验所
附件1
2015年第二期四川省药品质量公告(总第29期)抽样检验不符合标准规定的药品名单(基本药物)
序 号 1 2 3 4 药品名称 标示药品生产企业 生产批号 规格 检验依据 不合格项目 检品来源 检验机构 绵阳市食品 药品检验所 雅安市食品 药品检验所 雅安市食品 药品检验所 广元市食品 药品检验所
硫普罗宁肠 江苏.亚邦爱普森药业有 1305004 溶片 限公司 醋酸曲安奈 浙江仙琚制药股份有限 德注射液 公司 湖北亿雄祥瑞药业有限 穿心莲片 公司 复方丹参片 江苏苏南药业实业有限 公司 131122 20140302 130701
5
三黄片
湖北仁悦药业有限公司
Байду номын сангаас
131001
6
复方丹参片 湖北仁悦药业有限公司
131107
7
金匮肾气丸 辽宁金丹药业有限公司 通化颐生药业股份有限 公司
20130706
8
通窍鼻炎片
131006
国家药品标准WS1(X-054)-2002- 含量测定 绵阳高新区医院 2006Z 中国药典2010年版 5ml:50mg pH值 雅安市中医医院 二部 每片含穿心莲 中国药典2010年版 (芦山县)芦阳镇黎 崩解时限 干浸膏0.105g 一部 明村一卫生室 每片重0.32g 中国药典2010年版 苍溪陵江镇胡文波中 重量差异 (相当于饮片 第一增补本 西医结合诊所 0.6g) 中国药典2010年版 一部及国家药品标 乐山市市中区广善堂 准药品检验补充检 每片重0.26g 重量差异 药店 验方法及检验项目 批准件2007002 (修订版) 薄膜衣小片 每 中国药典2010年版 合江县百信药业29连 重量差异 片重0.32g(相 第一增补本 锁店 当于饮片 宜宾中宏药业皮仁堂 国家药品标准WS3每丸重6g 重量差异 零售连锁有限公司一 B-3892-98-2011 一四分店 宜宾时珍大药房零售 国家药品标准(试 每片重0.35g 重量差异 连锁店有限公司筠连 行)YBZ06582005 县四方连锁店 0.1g
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
药学动态美国警告DPP-4抑制剂类降糖药可引起关节痛2015年8月28日,美国食品药品管理局(FDA)发布警示信息,称治疗2型糖尿病的药物西格列汀、沙格列汀、利格列汀和阿格列汀可引关节痛,而且可能是重度或致残性的。
FDA已要求相关药品说明书中添加关于该风险的警告和注意事项。
此类药物亦称为二肽基肽酶-4(dipeptidyl peptidase-4 ,DPP-4)抑制剂。
DPP-4抑制剂用于改善2 型糖尿病患者的血糖控制,一般配合饮食控制和运动,作为单药治疗或与其他降糖药(如二甲双胍)联合治疗。
美国FDA在检索了其不良事件报告系统(FAERS)数据库和医学文献后,确定了与使用DPP-4抑制剂相关的重度关节痛病例。
患者从开始用药的第一天至用药后数年不等开始出现症状,停药后通常在1个月内关节疼痛症状缓解。
重新开始使用相同药物或其他DPP-4抑制剂后,一些患者再次发生重度关节痛。
FDA警告,如果发生重度持续性关节痛,患者不应停用DPP-4抑制剂药物,而应立即联系医疗卫生专业人员。
医疗卫生专业人员应考虑DPP-4抑制剂为严重关节痛的可能原因,并视情况嘱患者停药。
(美国FDA网站)美国加强非甾体类抗炎药物心血管安全性警告2015年7月9日,美国食品药品管理局(FDA)发布信息称,正在加强阿司匹林以外所有非甾体类抗炎药(NSAIDs)说明书中关于心脏病发作和脑卒中的安全性警告。
使用NSAIDs可引发心脏病发作或脑卒中风险,这两种风险均可导致死亡,相关内容于2005年在处方药说明书的黑框警告以及“警告和注意事项”部分首次进行了说明。
自此以后,FDA对NSAIDs的处方药和非处方药的多种新的安全信息进行了审查,包括观察研究、临床试验的大型合并分析以及其他科学文献。
2014年2月10-11日关节炎咨询委员会和药物安全与风险管理咨询委员会举行的联合会议,对这些研究也进行了讨论。
FDA对新的安全信息进行了全面审查,并根据审查结果要求更新所有NSAIDs处方药的说明书内容。
与NSAID处方药的现行说明书一样,阿司匹林以外的非处方NSAIDs的药品说明已经含有心脏病发作和脑卒中风险的信息。
此外,FDA还将要求更新除阿司匹林以外的NSAIDs非处方药的说明书和标签。
FDA建议:NSAIDs的整个用药过程中,患者和医护人员应对心脏相关副作用保持警惕。
患者一旦出现胸痛、呼吸短促或呼吸困难、一个部位或身体一侧无力或口齿不清中任何一种症状,应立即就医。
NSAIDs处方药说明书的更新内容包括以下方面:在使用NSAIDs药品的最初数周内,就存在心脏病发作或脑卒中的风险。
使用时间越长,风险越大;剂量越高,风险也越大。
以往认为所有NSAIDs均具有相似风险。
然而,最新信息不能表明所有NSAIDs均具有相似的心脏病发作或脑卒中风险;但也不足以证明某种NSAIDs的风险肯定高于或低于其他NSAIDs。
NSAIDs可加大患者的心脏病发作或脑卒中风险,无论患者是否已患心脏病或存在心脏病风险因素。
大量研究支持这一结果,但学者对风险加大幅度的估计值则存在差异,具体取决于所研究药物和所使用剂量。
一般而言,对于心脏病患者或存在心脏病风险因素的患者而言,使用NSAIDs后发生心脏病或脑卒中的几率将高于无风险因素的患者,因为前者的基线风险相对较高。
首次心脏病发作之后接受NSAIDs治疗的患者与首次心脏病发作后未接受NSAIDs治疗患者相比,前者更有可能于心脏病发作后一年内死亡。
使用NSAIDs还可导致心力衰竭风险加大。
(美国FDA网站)加拿大公布2014年对乙酰氨基酚过量和肝损害报告对乙酰氨基酚在加拿大使用50余年,广泛用于镇痛解热,遵医嘱使用安全有效。
尽管对乙酰氨基酚的安全性早已确定,但这种药物依然是加拿大急性肝功能衰竭的主要诱因。
在加拿大和其他国家,仍然不断发生与对乙酰氨基酚相关的严重肝损害事件。
多年前就已认识到了对乙酰氨基酚对肝脏的影响,过去十年内,加拿大卫生部针对对乙酰氨基酚的安全性相关信息,采取了多种应对措施。
2009年,应“制定更严厉标签警告内容,以减少对乙酰氨基酚非故意过量事件”的要求,加拿大卫生部进行了一次初步安全审查。
审查结束后,于2009年发布了一份指导文件《对乙酰氨基酚标签标准》,以更新对乙酰氨基酚非处方药的标签。
加拿大卫生部努力减少加拿大用药者的健康风险因素,为此实施了一次更为深入的科学审查,以评估补充证据及加拿大用药现状。
《加拿大对乙酰氨基酚过量和肝损害报告(2 014)》(下文简称为《对乙酰氨基酚报告》)含有关键性调查结果,并提供了进一步减少加拿大用药者肝损害风险的建议。
一、背景信息长期以来,对乙酰氨基酚处方药与非处方药一直用于镇痛解热,在加拿大的使用历史可追溯至1961年。
市售对乙酰氨基酚包括单方和复方产品,例如感冒咳嗽药或麻醉镇痛药。
超过475种不同的对乙酰氨基酚产品被许可上市,其中绝大多数为非处方药。
目前,加拿大和其他许多国家的对乙酰氨基酚的最大推荐日剂量为4 g,建议镇痛的最长持续用药时间为5天,解热为3天。
虽然通常认为遵医嘱服用时对乙酰氨基酚是一种安全药物,但是,服用过量的对乙酰氨基酚(即超过标签的规定用量),无论是有意或无意,均可造成严重肝损害,包括急性肝衰竭。
一般认为成人剂量超过每天10 g(或每天150 mg/ kg)即可造成肝损害。
然而,也有极少数报告表明使用低于最大推荐剂量造成成人肝损害,这种情况多见于已有肝脏疾病的患者。
有证据表明使用对乙酰氨基酚所引发的肝损害风险在某些情况下可能会增加,例如酗酒、营养不良、某些肝脏疾病或超过推荐的持续使用时间。
加拿大卫生部采取了许多措施来调查并减少对乙酰氨基酚相关的肝损害风险。
加拿大卫生部就对乙酰氨基酚的安全使用问题发布了2个公告:1份于2003年2月发布,另1份于2011年1月发布。
此外,于2009年完成了对乙酰氨基酚诱导肝损害的初步安全性审查。
加拿大卫生部于2009年11月发布了《对乙酰氨基酚标签标准》,内容包括改进后的警告内容,提示药物过量可能导致严重肝损害以及潜在致死性肝损害,同时还包括依据体重和年龄的儿童用药指南。
2009年安全性审查也建议加拿大卫生部设立跨局工作组,以进一步研究对乙酰氨基酚诱发的肝损害风险。
这些活动与其他国家的工作方向相一致。
二、目的这份报告的目的是评估加拿大国内的对乙酰氨基酚相关肝损害风险。
考察范围包括发表的科学和医学文献、管理部门文件、加拿大卫生部收到的药品不良反应报告、来自加拿大医院和验尸官办公室的数据、用户信息调查。
三、主要发现(一)加拿大对乙酰氨基酚使用情况加拿大每年销售逾40亿份对乙酰氨基酚,其中约15%为处方药。
复方产品包括感冒咳嗽药(OTC)以及含麻醉剂的镇痛药,占全部售出对乙酰氨基酚产品的一半以上。
(二)对乙酰氨基酚过量、肝损害和住院1.对乙酰氨基酚过量该报告发现,加拿大每年有4000多例对乙酰氨基酚过量导致住院的病例。
约1/5病例是由于患者用药无意间超过了推荐剂量。
还有一项重要发现,即加拿大非故意过量导致的住院人次呈上升趋势。
青少年和年轻成人是最有可能发生对乙酰氨基酚过量(包括故意过量和非故意过量)的年龄组。
报告还发现,与男性相比,对乙酰氨基酚过量在女性中更为常见。
处方药中复方制剂(对乙酰氨基酚+麻醉剂)过量造成的肝损害病例数量相对较多,因其使用时间较长或者可能被误用/滥用。
2.对乙酰氨基酚与肝损害在很多国家,如加拿大、美国、英国和澳大利亚,对乙酰氨基酚是引发包括急性肝衰竭在内的全部严重肝损害事件的主要诱因。
报告指出,加拿大每年发生的250多例对乙酰氨基酚相关严重肝损害病例中,一半以上与非故意过量有关。
这意味着非故意过量造成的严重肝损害可能比故意过量造成的严重肝损害更为普遍。
多数病例涉及对乙酰氨基酚单方产品或含麻醉剂的复方产品。
另外,加拿大药物警戒委员会收到的对乙酰氨基酚相关肝损害报告的病例中,1/5病例所提及的剂量处于推荐剂量范围内(即低于4g/天,相当于8片加强型对乙酰氨基酚500mg 片剂)。
许多病例中,患者存在着可识别的对乙酰氨基酚肝损害风险因素,例如酗酒或病毒性肝脏疾病。
四、结论虽然对乙酰氨基酚是一种安全有效的药物,但若不遵医嘱使用(例如超过推荐剂量或推荐疗程),依然存在着严重肝损害风险。
让人们意识到某些药品中存在对乙酰氨基酚并且不按照产品标签使用时对乙酰氨基酚可导致肝损害风险,有助于减少可造成严重肝损害的非故意过量事件。
2014年《对乙酰氨基酚报告》为减少对乙酰氨基酚相关肝损害,特别是非故意过量肝损害,提出了多种参考建议。
这些建议包括限制消费者一次可以购买的对乙酰氨基酚总量;降低最大推荐日剂量;降低某些产品中的对乙酰氨基酚含量;减少每份包装中的单位数量;重新评估对乙酰氨基酚和麻醉剂复方产品的作用。
此外还专门推荐了加强儿童安全用药的具体措施,例如要求所有儿童液体药品配备准确的给药装置。
五、完成《对乙酰氨基酚报告》后加拿大卫生部采取的行动2014年7月,加拿大卫生部就《对乙酰氨基酚报告》和建议的风险最小化方案,与包括患者安全组、药剂师、零售药房和行业协会在内的各方利益相关者举行了讨论。
此次讨论的成果是,加拿大卫生部和利益相关者代表组成一个指导委员会,共同开发和实施促进对乙酰氨基酚安全使用的教育模式。
此次协作促成了关键性教育资讯的开发,于2015年夏季开始,利益相关者将通过各种传播渠道与公众分享这些教育资讯。
加拿大卫生部还将使用社交媒体来传播这些关键性讯息,Healthy Canadians Web(健康加拿大人)网站上已经发布了一个网页,告知公众安全使用对乙酰氨基酚。
另外,加拿大卫生部发布了一个Next 链接,引导读者前往另一个信息更新网页,帮助教育和提醒加拿大人安全使用对乙酰氨基酚。
2014年10月,加拿大卫生部设立了一个内部小组,评估其余方案中哪个最具有可行性,该小组还将针对这些方案征求外部意见。
加拿大卫生部对健康系统、政策、监管、国际观点进行了考察,以确定风险最小化方案的可行性。
讨论过程中,《对乙酰氨基酚报告》完成后出现的新信息,连同其他国际监管机构所采取的行动(主要为美国FDA),均被纳入了考虑范围。
为了反映出这些进展,《对乙酰氨基酚标签标准》在进行修订,以协助教育消费者使用对乙酰氨基酚可能带来的风险。
六、后续步骤加拿大卫生部正在与其利益相关者合作,对《对乙酰氨基酚报告》中提出的其余风险最小化方案的可行性和预期有效性进行深入分析。
正在考虑减少所有含对乙酰氨基酚产品口服和直肠给药剂型的最大推荐日剂量,并减少某些产品的单位剂量。
正在考虑改进产品说明书和包装,包括所有出售的儿童液体产品需配备准确的给药辅助装置的要求。
《对乙酰氨基酚标签标准》一旦更新,将于2015年夏天在网站上发布,征求利益相关者意见后定稿。
