精品 课后习题及参考答案-药物合成反应-闻韧-第三版-课后习题答案(全)
《药物合成反应(闻韧主编第三版)》人名反应整理

《药物合成反应(闻韧主编第三版)》人名反应整理一、卤化反应1、Hunsdriecke反应(汉斯狄克反应):羧酸银盐和溴或碘反应,脱去二氧化碳,生成比原反应物少一个碳原子的卤代烃。
2、Sandmeyer反应(桑德迈尔反应):用氯化亚铜或溴化亚铜在相应的氢卤酸存在下,将芳香重氮盐转化成卤代芳烃。
3、Gattermann反应(加特曼反应):将Sandmeyer反应条件改为铜粉和氢卤酸。
4、Schiemann反应(席曼反应):将芳香重氮盐转化成不溶性的重氮氟硼酸盐或氟磷酸盐,或将芳胺直接用亚硝酸钠和氟硼酸进行重氮化,此重氦盐再经热分解(有时在氟化钠或铜盐存在下加热),就可以制得较好收率的氟代芳烃。
二、烃化反应5、Willamson合成(威廉姆森合成):醇在碱(钠,氢氧化钠,氢氧化钾等) 存在下与卤代烃反应生成醚的反应。
6、Gabriel合成(盖布瑞尔合成):将氨先制备成邻苯二甲酰亚胺,利用氮上氢的酸性,先与氢氧化钾形成钾盐,然后与卤代烃作用,得N-烃基邻苯二甲酰亚胺,肼解或酸水解即可得纯伯胺。
7、Delepine反应(德勒频反应):用卤代烃与环六亚甲基四胺(乌洛托品Methenamine)反应得季铵盐,然后水解可得伯胺。
8、Leuckart-Wallach反应(鲁卡特-瓦拉赫反应):用甲酸及其铵盐可以对醛酮进行还原烃化,得各类胺。
9、Ullmann反应(沃尔曼反应):卤代芳烃与芳香伯胺在铜或碘化铜及碳酸钾存在并加热的条件下可得二苯胺及其同系物。
三、酰化反应10、Friedel-Crafts反应(傅列德尔-克拉夫茨反应,也称傅-克酰基化反应):羧酸及羧酸衍生物在质子酸或Lewis酸的催化下,对芳烃进行亲电取代生成芳酮的反应。
11、Hoesch反应(赫施):腈类化合物与氯化氢在Lewis 酸催化剂ZnCl2的存在下与烃基或烷氧基取代的芳烃进行反应可生成相应的酮亚胺,再经水解则羟基或烷氧基取代的芳香酮。
12、Gattemann反应(伽特曼反应):将羟基或烷氧基取代的芳烃在AlCl3、ZnCl2催化下与氰化氢及氯化氢反应生成牙胺盐酸盐,再经水解生成相应芳香醛的反应。
药物合成反应习题及答案

药物合成反应习题及答案一、举例解释下列概念:1,官能团保护;为什么保护?当分子中有多个官能团,想在某一官能团进行转换反应,为了不使其他官能团影响反应,需对这些官能团进行衍生化,这就是官能团的保护。
达到反应目的后再还原这些官能团。
理想保护基:试剂易得、无毒,保护基稳定,引入和脱去反应选择性好,收率高。
2,相转移催化剂; 一种与水相中负离子结合的两性物质,可以把亲核试剂转移到有机相进行亲核反应。
相转移催化剂优点:克服溶剂化作用;不需无水操作;可用无机碱代替有机金属碱;降低反应温度。
3,重排反应;重排反应是指在同一分子内,某一原子或基团从一个原子迁移至另一原子而形成新分子的反应。
按反应机理可分为亲电重排、亲核重排、自由基重排和协同重排。
4,合成子;合成子:组成靶分子或中间体骨架的各个单元结构的活性形式.包括:离子合成子、自由基或周环反应所需的中性分子。
离子合成子:包括 d 合成子和a合成子d 合成子: 亲核性的离子合成子d---donor of electrond 合成子等价试剂a合成子:氧化性或亲电性的离子合成子a合成子:等价试剂5,协同反应协同反应:在反应过程中,若有两个或两个以上的化学键破裂和形成时,都必须相互协调地在同一步骤中完成。
6, 非均相催化氢化: 催化剂、反应物、试剂和氢供体在两项或多项中反应,催化剂自成一相,称为非均相催化氢化。
催化剂自成一相称为非均相催化剂如Pd/C为催化剂,氢气为氢供体,在反应液中还原双键的反应。
1) DMAP2) DMF3) DCC4) TBAF1) Aromatic Electrophilic Substitution; 芳香亲电取代2) Phase-transfer catalyst; 相转移催化剂3) Carbocations; 碳负离子4) trifluoroacetic anhydride.三氟乙酸酐Ryoji Noyori was awarded the Nobel Prize in 2001, What did he discover?Ryoji Noyori日本名古屋大学的野伊良治因在手性催化氢化反应方面做出了突出贡献而被授予2001年Nobel化学奖。
(完整word版)药物合成反应(闻韧_第三版)课后翻译(word文档良心出品)

1、About 216–224 g. (1.62–1.68 moles) of powdered anhydrous aluminum chloride is added to a 1Lthree-necked flask.在1L的三口烧瓶中加入大约216-224g(1.62–1.68 moles)的无水三氯化铝。
While the free-flowing catalyst is stirred (Note 3), 81 g. (0.67 mole) of acetophenone is added from the dropping funnel in a slow stream over a period of 20–30 minutes. 自由流动的催化剂边搅拌边用滴液漏斗缓慢滴加81g苯乙酰。
Considerable heat is evolved, and, if the drops of ketone are not dispersed, darkening or charring occurs. 放热反应,假如滴加的酮不能被分散,就会变黑或是碳化。
When about one-third of the acetophenone has been added, the mixture becomes a viscous ball-like mass that is difficult to stir.当三分之一的乙酰苯被滴加,反应混合物变成一个很难搅拌的粘性的球状团块。
Turning of the stirrer by hand or more rapid addition of ketone is necessary at this point. 在这时,改用手动搅拌或快速滴加酮是非常必要的。
The addition of ketone, however, should not be so rapid as to produce a temperature above 180°. 然而,速度不能太快,当反应温度超过180℃时。
药物合成反应(第三版_闻韧)第一章卤化反应

Organic Reactions for Drug Synthesis
例1.
C6H5 H
CC
H
COOC2H5
Br2 / CCl4
Br
C6H5
C
H C
H Br COOC2H5
C6H5 H CC
H Br COOC2H5
1. 卤素与烯烃的亲电加成反应
(1)反应历程: 第一步:卤正离子向π 键进攻,形成三员环卤正离子 或开放式碳正离子的过渡态。
R1 R3
R2
R4
δ +δ XX
Organic Reactions for Drug Synthesis
R1 R3 CC
R2 X R4
(1)
R1 R3
CC
R2
X R4
(2)
第二步:
反应类型
亲电加成 亲电取代 亲核取代 自由基反应
Organic Reactions for Drug Synthesis
常用的卤化剂 卤素(X2):Cl2、Br2
次卤酸(HOX):HOCl、HOBr
N-卤代酰胺:
如 N-溴(氯)代乙酰胺( NBA,NCA) N-溴(氯)代丁二酰亚胺(NBS,NCS)
Ph H CC
H CH3
NBS / DMSO / H2O
OH
Ph
H
CC
H
Br CH3
NBS / 干燥的DMSO
O H
Ph C C Br CH3
Organic Reactions for Drug Synthesis
五、卤化氢与烯烃的加成
最新《药物合成反应(闻韧主编第三版)》人名反应整理资料

《药物合成反应(闻韧主编第三版)》人名反应整理一、卤化反应1、Hunsdriecke反应(汉斯狄克反应):羧酸银盐和溴或碘反应,脱去二氧化碳,生成比原反应物少一个碳原子的卤代烃。
2、Sandmeyer反应(桑德迈尔反应):用氯化亚铜或溴化亚铜在相应的氢卤酸存在下,将芳香重氮盐转化成卤代芳烃。
3、Gattermann反应(加特曼反应):将Sandmeyer反应条件改为铜粉和氢卤酸。
4、Schiemann反应(席曼反应):将芳香重氮盐转化成不溶性的重氮氟硼酸盐或氟磷酸盐,或将芳胺直接用亚硝酸钠和氟硼酸进行重氮化,此重氦盐再经热分解(有时在氟化钠或铜盐存在下加热),就可以制得较好收率的氟代芳烃。
二、烃化反应5、Willamson合成(威廉姆森合成):醇在碱(钠,氢氧化钠,氢氧化钾等) 存在下与卤代烃反应生成醚的反应。
6、Gabriel合成(盖布瑞尔合成):将氨先制备成邻苯二甲酰亚胺,利用氮上氢的酸性,先与氢氧化钾形成钾盐,然后与卤代烃作用,得N-烃基邻苯二甲酰亚胺,肼解或酸水解即可得纯伯胺。
7、Delepine反应(德勒频反应):用卤代烃与环六亚甲基四胺(乌洛托品Methenamine)反应得季铵盐,然后水解可得伯胺。
8、Leuckart-Wallach反应(鲁卡特-瓦拉赫反应):用甲酸及其铵盐可以对醛酮进行还原烃化,得各类胺。
9、Ullmann反应(沃尔曼反应):卤代芳烃与芳香伯胺在铜或碘化铜及碳酸钾存在并加热的条件下可得二苯胺及其同系物。
三、酰化反应10、Friedel-Crafts反应(傅列德尔-克拉夫茨反应,也称傅-克酰基化反应):羧酸及羧酸衍生物在质子酸或Lewis酸的催化下,对芳烃进行亲电取代生成芳酮的反应。
11、Hoesch反应(赫施):腈类化合物与氯化氢在Lewis 酸催化剂ZnCl2的存在下与烃基或烷氧基取代的芳烃进行反应可生成相应的酮亚胺,再经水解则羟基或烷氧基取代的芳香酮。
12、Gattemann反应(伽特曼反应):将羟基或烷氧基取代的芳烃在AlCl3、ZnCl2催化下与氰化氢及氯化氢反应生成牙胺盐酸盐,再经水解生成相应芳香醛的反应。
药物合成反应第三版第五章答案

药物合成反应第三版第五章答案【篇一:药物合成反应作业答案】on(克莱森-施密特反应) p40,不对称酮与芳香醛反应,hoo5% aq. naoh+(2)p56,reformatsky(瑞福马斯基)反应othf, reflux+etoo(3)knoerenagel反应(诺文格尔),p67.o2nbaseo2ncn+(4)darzens缩水甘油酸酯缩合反应,p59pho+2 eq. liohh4 ℃, 60hph(5)mannich(曼尼希)反应,p87;acid catalyst+h+h2nonh(6)p72,perkin (珀金斯)反应,h1) koh, ac2o2) aq. hcl, rt.2ho(7)p65,o+na, etohoo+ofecl3-6h2o2% moloo(9)ho+nh2+acid catalyst(10)friedlander反应,ohnh2oh-+nh2ohcnarcho++10% [bmim]oh100 ℃(11) ophome35% mol incl31.5~3 eq. hsime2phdcm, r.t, 2 hohphome+【篇二:药物合成反应(闻韧_第三版)课后翻译】16–224 g. (1.62–在1l的三口烧瓶中加入大约grams of heavy dark residue by distillation at reduced pressure. 乙醚在常压下蒸馏,微量的溴苯乙酮通过减压蒸馏的方法从大量深色残渣中被分离出来。
the colorless distillate is carefully fractionated to obtain 94–100 g.通过分馏,得到无色的流出液94-100g2、反应式:3、is prepared in a 2-l. three-necked, round-bottomed flask fitted with a–硫酸钠抽滤后用乙醇(150–200 ml)洗涤。
《药物合成反应(闻韧主编第三版)》人名反应整理(新)

《药物合成反应(闻韧主编第三版)》人名反应整理一、卤化反应1、Hunsdriecke反应(汉斯狄克反应):羧酸银盐和溴或碘反应,脱去二氧化碳,生成比原反应物少一个碳原子的卤代烃。
☆☆☆☆☆2、Sandmeyer反应(桑德迈尔反应):用氯化亚铜或溴化亚铜在相应的氢卤酸存在下,将芳香重氮盐转化成卤代芳烃。
☆☆3、Gattermann反应(加特曼反应):将Sandmeyer反应条件改为铜粉和氢卤酸。
☆☆4、Schiemann反应(席曼反应):将芳香重氮盐转化成不溶性的重氮氟硼酸盐或氟磷酸盐,或直接将芳胺用亚硝酸钠和氟硼酸进行重氮化,此重氮盐再经热分解(有时在氟化钠或铜盐存在下加热),就可以制得较好收率的氟代芳烃。
☆二、烃化反应5、Willamson合成(威廉姆森合成):醇在碱(钠、氢氧化钠、氢氧化钾等)存在下与卤代烃反应生成醚的反应。
☆☆☆☆6、Gabriel合成(盖布瑞尔合成):将氨先制备成邻苯二甲酰亚胺,利用氮上氢的酸性,先与氢氧化钾形成钾盐,然后与卤代烃作用,得N-烃基邻苯二甲酰亚胺,再经过肼解或酸水解即可得纯伯胺。
☆☆☆☆☆7、Delepine反应(德勒频反应):用卤代烃与环六亚甲基四胺(乌洛托品Methenamine)反应得季铵盐,然后水解即可得伯胺。
8、Leuckart-Wallach反应(鲁卡特-瓦拉赫反应):用甲酸及其铵盐可对醛酮进行还原烃化,得各类胺。
☆9、Ullmann反应(沃尔曼反应):卤代芳烃与芳香伯胺在铜或碘化铜及碳酸钾存在并加热的条件下可得二苯胺及其同系物。
三、酰化反应10、Friedel-Crafts反应(傅列德尔-克拉夫茨反应,也称傅-克酰基化反应):羧酸及羧酸衍生物在质子酸或Lewis酸的催化下,对芳烃进行亲电取代生成芳酮的反应。
☆☆☆☆☆11、Hoesch反应(赫施反应):腈类化合物与氯化氢在Lewis酸催化剂ZnCl2等的存在下与烃基或烷氧基取代的芳烃进行反应可生成相应的酮亚胺,再经水解则得到羟基或烷氧基取代的芳香酮。
药物合成习题答案
C2H5ONa
(COOC2H5)2CH(CH2)6CH(COOC2H5)2 Na, NH3 PhCH3 (CH2)2 HO O O (CH2)2
C2H5OOC(CH2)8COOC2H5
O
O
②试由
O
OCH3 合成
。
OH 0.25 NaBH4 OCH3 H2O H+ OCH3
OH H+ O O
H COOEt CH2CH 2COOH
HO
2.完成下列合成过程 (1)
O CHO CN PCC NaOAc O O O NaOH H3O O O COOH OH
O
(2)
CH3 O CH2OH + CH3 CHO O OC2H5 O O CH3 Claisen
Cope O
CH3 CHO
H2, Pd-C O
CHO CH3
(3)
C2H5 CH3 OCH3 OCH3 C2H5 O CO2CH3 + H3CO2C CH3 CH3 Claisen Rearrangement OH 2,4-O2NC6H5OH Tol C2H5 CH3 CO2CH3 O
药物合成反应习题
参考答案
第一章 卤化反应
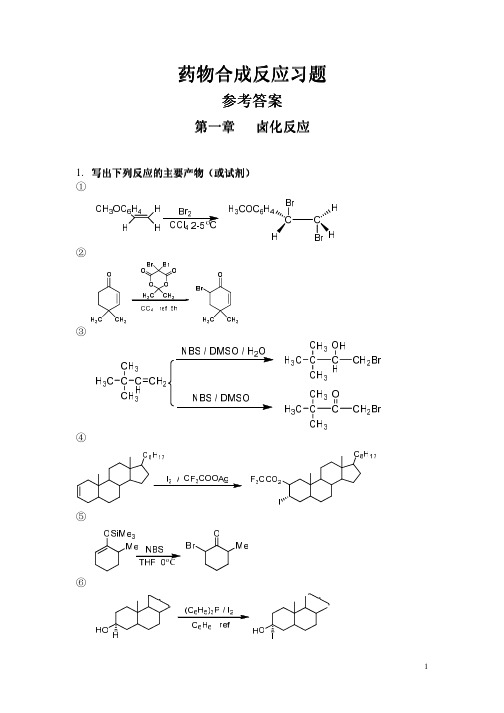
1. 写出下列反应的主要产物( 写出下列反应的主要产物(或试剂) 或试剂) ①
②
③
④
⑤
⑥
1
⑦
⑧
⑨
⑩
2.写出下列反应的可能产物
①
②
2
③
④
3.
①
写出下列反应的主要试剂及条件
②
③ቤተ መጻሕፍቲ ባይዱ
④
第二章 1.
① 完成下列反应
烃化反应
药物合成课后习题答案
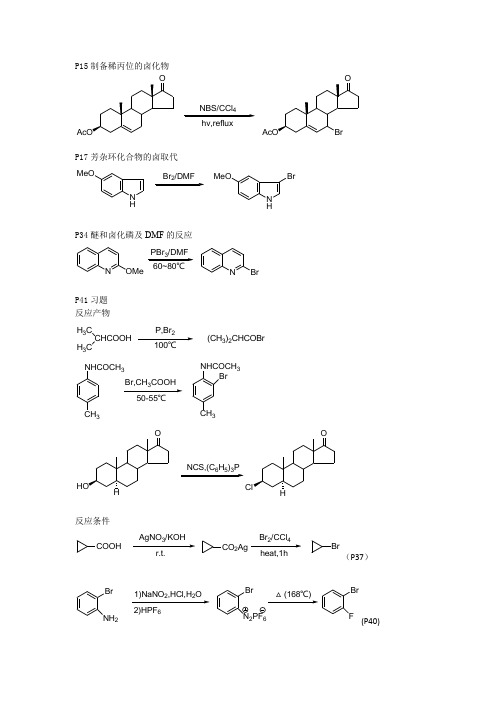
P15制备稀丙位的卤化物4hv,refluxP17芳杂环化合物的卤取代N HMeOBr /DMFN HMeOBrP34醚和卤化磷及DMF 的反应NOMe3NBrP41习题 反应产物 H 3C CHCOOHH 3CP,Br (CH 3)2CHCOBrCH 3NHCOCH 3Br,CH COOH 50-55℃CH 3NHCOCH 3Br653反应条件COOHAgNO /KOHCO 2AgBr /CCl Br(P37)Br NH 21)NaNO ,HCl,H O Br F2)HPF 6Br N 2PF 6△(168℃)(P40)P52有位阻或螯合酚的烃化O HOO OH OMeOMeOO OHOMeP54 DCC缩合法HOR HHOArNHCONH+ArORP56伯胺的制备——Gabriel反应(肼解法)NH OO KOH/EtOHNOOK NOORNH NHOONHNH+RNH2P62还原烃化法的应用NH23N CHMeH/Raney NiNHCH2CH3P63 Ullmann反应:芳胺的N-芳烃化CF3NH2+ClCOOH无水K23105-110℃F3CNHHO2CP65 芳烃的烃化:Friedel-Crafts反应R1+R C AlCl3XR'R''R'CR''RRAlCl3XR1CR'R R''+AlCl3+HXP79稀胺的C-烃化N H +OCH3NCH3P84习题反应产物KNO O+OON OOPhHN OOPhHN OONH222.2+OOBrOMeSnCl0℃OOMeO反应条件2OLi(P77 )P853(P77)O原子上的酰化反应P92羧酸为酰化剂——伯醇酯的制备+NO2CO2HDEAD/Ph3r.t.,1h2N CO22NNHOO P95活性酯用于大环内脂合成NS SN/PPh3PhH/r.t.HOP98酸酐为酰化剂H 3C NCH 3OH1)(CH 3CH 2CO)2O/Py2)HClH 3C NCH 3OCOCH 2CH 3.HCl(Anadol)P101酰氯为酰化剂——仲醇的酰化NNNO OHNClClONNCH 3.HClpy/CH 2Cl 2NNNON ClONN OCH 3(Zopiclone)N 原子上的酰化反应P107 酸酐为酰化剂O O O+PhCH 2CHCOOHNH 2Tol refiux,2hN OOCHCOOH CH 2PhC 原子上的酰化反应P113 Friedel-Crafts 反应(芳烃取代成芳酮)S+H 3COOO CH 3H PO reflux,2hSOCH 3O O O+CH 3AlCl 390℃,3hCO 2HOCH 3NEtO 2CCO 2EtBF 20℃,15minNEtO 2COP116 Vilsmeier-Haack 反应(芳环引入醛基)N HDMF/POCl CH 2Cl 2H ON HCHOP122利用烯胺化进行的C-酰化反应ON HONOCOClEt 3NOO2P123习题 反应产物N Boc+HNDCC/CH Cl N BocN反应条件OHCH 3OOCOPhCH 3OOHOO OONP124H 3CO H 3CONHCOCH 3POCl 3,toluene△H 3CO H 3CON CH 3Ac O,py H 3CO H 3CON CH 2COCH 3P133 Robinson 环化法OCH 3+OO CH 3CH 3O OHCH 3O -H 2OCH 3Oα-羟烷基化(Aldol 缩合) P136 Reformatsky 反应 O+BrCF 2COOC 2H 5OHCF 2COC 2H 5OP138 Grignard 反应O1)BrMg PhOHPhα-卤烷基化(Blanc 反应) P139反应通式+H OH+HClZnCl Cl+H 2Oα-氨烷基化(Mannich 反应) P143 Pictet-Spengler 反应H323NH 2OCH 3N H 3CO3羰基烯化反应(Wittig 反应) P148反应机理148R (C 6H 5)3C R1R 2+(C 6H 5PCR1R 2CR 4R 3CR3R 4C R 1R 2(C 6H 5)3C C R 1R 2R 4R 3+(C 6H 5)3POP149 制备环外烯键化合物3Ph P=CH 3P150 制备共轭多烯化合物CHO+(C 6H 5)3PCOOC 2H 5COOC 2H 5LiAlH CH 2OHP165 习题 反应产物+NO 220℃NO 2C 到C 重排Wagner-Meerwein 重排P170 胺与亚硝酸作用生成碳正离子C CH 3H 3C CH 3CH 2NH 2HNO 2C CH 3H 3C CH 3CH 2N N2C CH 3H 3C CH 32P171CH 3NH 2HO 2C2HO 2CHHH 3C OHPinacol 重排P175制备环状酮(Tiffenfan 扩环) OH C Ph PhOH H SO /Et Or.t./3h2O Ph PhOH OH0.2molSnCl /HC(OMe)OWoff 重排(α-重氮酮生成烯酮) P182ON 22240min/-78℃/-N 2C Ohv,O /CH Cl -78℃~-10℃/20minOC 到杂重排Beckmann 重排(肟生成取代酰胺) P185立体专一性NH 2ONOHHNOSchmidt 反应 (叠氮酸) P191叠氮酸与羧酸生成伯胺HOOCCH 3CH 3COOH NaN /H SO /CHCl HOOCCH 3CH 3NH 2Baeyer-villiger 反应(酮与过氧酸重排成酯) P193HC OCH 333HO C OCH 3机理HC OCH 3HO C OCH 3HH C OHCH 33O C OPhC OH3-HCO O 2N33O 2NCO O机理CO O 2NCH 3CO 3H/AcOHO 2NCO OHCOH O 2N O 2C OH OC OCH 3C OOH O 2N-Hσ-键迁移重排P199 Claisen 重排(烯丙基芳基醚重排为邻烯丙基酚)O C C C ROH C C C R机理C RCO C HC C ROH C C C RP200脂肪族Claisen 重排OOOCO 2EtOCO 2EtP202 cope 重排Ph Ph150℃Ph PhCH 2CH2350℃习题 反应产物 P205OHHO CH 3COOH H 2SO 4OP207OCH 3CHOOOCH 3CHOOH(P199烯丙基重排到对位)醇类的氧化P220 氯铬酸吡啶鎓盐(PPC )氧化法OO CH 2OHCH 2Cl 2OO CHOP222 DMSO-DCC 氧化法OHON HNO CH 3OOAc 34r.t.ON HN OCH 3OOAcOHCP225 1,2-二醇的氧化HOOH4OO醛酮的氧化P226 Dakin 反应OH CHOC H COOHOH O C OHOH OH烯键化合物的氧化P229 不与羰基共轭的烯键的环氧化t-BuOOH 6OP232顺式羟基化OOsO OHHOH OH习题 反应条件 P248CH 33.2CH 3O (p218 Collins 试剂 烯丙酮的制备)3333(P229 过氧酸环烯烃环氧化)羰基的还原P263 Clemmensen 反应(酸性锌汞齐还原醛酮为甲基亚甲基) Ph C OCH 2CH 2COOHZn-Hg/HCl/TolCH 2CH 2CH 2COOHPhC H C HPh COOEtZn-Hg/HCl PhCH 2CH 2COOEtP264 Wolff-kishner-黄鸣龙还原反应OR R'H NNH NNH 2R R'R CH 2R'+N 2P265 腙还原为烃CO H NNH CN NH 2DMSOC HHP272 Leuckart-Wallach 反应O NCH 3CH 3HCON(CH )OHN(CH 3)2CHO HCOOHOHNH(CH 3)22N(CH 3)2HCOOH 中间体羧酸及衍生物的还原 P278 金属复氢化物的还原CNNO 325℃NO 3CH 2NH 2含氮化合物的还原P281 Benoxaprofen 中间体制备 O 2NHC CN CH 34H 2NHC CH 3CNP282 HOO 2N NO 224HOH 2N NO 2习题 反应产物 P290FCHO +NHFHC NFH 2C N2Zn(BH )反应条件 P291COClNO 2O 2NCHONO 2O 2NLiAlH[OC(CH )](三叔丁氧基氢化铝锂/甘醇二甲醚) H 3COC NH 3COCHODIBAL-H /H 2SO 4(氢化二异丁基铝/硫酸)4hv,refluxN HMeOBr /DMFN HMeOBrNOMe3NBrH 3C CHCOOHH 3CP,Br 100℃(CH 3)2CHCOBrCH 3NHCOCH 3Br,CH COOH 50-55℃CH 3NHCOCH 3BrHNCS,(C 6H 5)3PHCOOHAgNO /KOHr.t.CO 2AgBr /CCl heat,1hBrBr NH 21)NaNO ,HCl,H O Br F2)HPF 6Br N 2PF 6△(168℃)OHO O OHOMeMeI/NaOHOMeO O OHOMeNNHORHN HHOArNH O N O OK RX/DMFN O ORNH 23N CHMeH /Raney NiNHCH 2CHCF 3NH 2+ClCOOH无水K 23105-110℃F 3C NHHO 2C N H+O CH 3NCH 3KNOO+O DMFNO O PhHNOOPhH NNH.2+OOBrOMeSnCl 0℃OOMeO2OLiN CHON CHO3+NO 2CO 2HDEAD/Ph 3r.t.,1h2NCO 22NNHO OHOOHNS S N/PPh 3PhH/r.t.HOOHH 3C NCH 3OH1)(CH 3CH 2CO)2O/Py2)HClH 3C NCH 3OCOCH 2CH 3.HCl(Anadol)NNNO OHNClClONNCH 3.HClpy/CH 2Cl 2NNNO N ClONN OCH 3(Zopiclone)O O O+PhCH 2CHCOOHNH 2Tol refiux,2hN OOCHCOOH CH 2PhS+H 3COO O CH 3H PO reflux,2hSO CH 3O O O+CH 3AlCl 390℃,3hCO 2HOCH 3NEtO 2CCO 2EtBF 320℃,15minNEtO 2CON HDMF/POCl CH 2Cl 2H 2ON HCHOON HONOCOClEt 3NOO2N Boc+HNDCC/CH Cl N BocNOHCH3 O ClCOPhOCOPhCH3OOHO ONH3COH3CONHCOCH3POCl3,toluene△H3COH3CONCH3OCH3+O OCH3CH3OAldol缩合OHCH3OO+BrCF2COOC2H5OHCF2COC2H5OO1)BrMg PhOHPh+HOH+HClZnCl Cl+H2OH32CHO3 NH2OCH3NH3COCH3148R(C6H5)3P CR1R2(C6H5)P CR1R2CR4R3R3R4CR1R2(C6H5)3CCR1R2R4R3+3Ph3P=CH23CHO+(C6H5)3P COOC2H5COOC2H5LiAlH4+NO220℃NO2CCH3H3CCH3CH2NH2HNO2CCH3H3CCH3CH N2CCH3H3CCH32CH3NH2HO2C2HO2CHHH3C OHOH C Ph PhOH H SO /Et Or.t./3h2O Ph PhOH OH0.2molSnCl /HC(OMe)-20℃/5minOON 22240min/-78℃/-N 2C Ohv,O /CH Cl -78℃~-10℃/20minONH 2ONOHHOOCCH 3CH 3COOH NaN /H SO /CHCl r.t.,25hHOOCCH 3CH 3NH 2HC OCH 333HO C OCH 3HC OCH 3HO C OCH 3HHC OHCH 33O C OPhC OH3-HCO O2N CH3CO3H/AcOHO2NCOOCOO2N33O2N C O OHCOHO2NO2COOHO2N-HO C C CRheatOHC C C RO OOCO2EtOCO2EtPhPh150℃PhPhCH2CH2350℃1hOHHO 3H 2SO 4OOCH 3CHOOOCH 3CHOOHOO CH 2OHCH 2Cl 2OOCHOOHON HNO CH 3OOAc34r.t.ON HN OCH 3OOAcOHCHOOH4(60%)OOOH CHOC H COOHOHO C OHOH OHt-BuOOH 6OOOsO4OHHOHOHCH3CrO(Py)CH3OOH333OH3Ph COCH2CH2COOHZn-Hg/HCl/TolCH2CH2CH2COOHPhCHCHPh COOEtZn-Hg/HClheatPhCH2CH2COOEtORR'H NNHNNH2RR'RCH2R'+N2 CO H NNHCNNH2DMSO ON3CH3HCON(CH)OHN(CH3)2CHOHCOOHOHNH(CH3)2 2N(CH3)2HCOOHCNNO 3B H /THF25℃NO 3CH 2NH 2O 2NHC CN CH 3495℃,1.5hH 2NHC CH 3CNHOO 2N NO 22480~85℃HOH 2N NO 2FCHO +NHFHCNF2Zn(BH )COClNO 2O 2NCHONO 2O 2NGlymeLiAlH[OC(CH )]H 3COC NH 3COCHODIBAL-H /H 2SO 4。
(完整word版)药物合成反应(闻韧_第三版)课后翻译(word文档良心出品)

1、About 216 -224 g. (1.62 —.68 moles) of powdered an hydrous alumi numchloride is added to a 1Lthree-necked flask. 在1L 的三口烧瓶中加入大约216-224g(1.62 —.68 moles) 的无水三氯化铝。
While the free-flowi ng catalyst isstirred (Note 3), 81 g. (0.67 mole) of acetophenone is added from the droppingfunnel in a slow stream over a period of 20 -30 min utes. 自由流动的催化剂边搅拌边用滴液漏斗缓慢滴加81g 苯乙酰。
Considerable heat is evolved, and, if the drops of ketoneare not dispersed, darke ning or charri ng occurs. 放热反应,假如滴加的酮不能被分散,就会变黑或是碳化。
When about on e-third of the acetophe none has bee n added, themixture becomes a viscous ball-like mass that is difficult to stir. 当三分之一的乙酰苯被滴加,反应混合物变成一个很难搅拌的粘性的球状团块。
Turning of the stirrer by hand ormore rapid additi on of ket one is n ecessary at this point. 在这时,改用手动搅拌或快速滴加酮是非常必要的。
The additi on of ket one, however, should not be so rapid as toproduce a temperature above 180 .然而,速度不能太快,当反应温度超过180 C时。
