大同市2017-2018学年高一3月月考化学试题 含答案
2017-2018学年度高一语文第二学期期末试卷 含答案

2017-2018学年度第二学期第二次月考(全二册)高一年级语文试卷命题人:校对:考试时长:150 分钟分值:150 分I 卷(选择题,共44分)一基础知识单项选择题(本大题共10小题,每小题2分,共20分。
在下列各小题的备选答案中,选择一个正确的答案)1.下列加点的字注音,错误最多的一项是()A.憎.恶(zèng)岑.寂(cán)流涎.(yán)锱.铢必较(zhī)B.目眦.(zì)攻讦.(jiān)拉纤.(qiàn)一蹴.而就(cù)C.瞋.目(chēng)绮.丽(yǐ)得逞.(chěng)昙.花一现(tán)D.折腾.(teng)帷.幕(weí)露.穷(lù)清沁.肺腑(qìng)2.下列词语中,错别字最多的一项是()A.不及不离挥豁无度珍羞美味源源不断B.抱残守却诩诩如生转瞬即逝迫在眉睫C.相形见拙烟熏火燎宠然大物屈指可数D.莫名其妙震耳欲聋猝不及防冠冕堂煌3.下列词语中,加点字解释完全正确的一项是()A.待人接物.(物体)自鸣.得意(表示)无动于衷.(内心)B.疾.言厉色(急速)胡作非.为(不对)灭顶..之灾(水漫过头顶)C.自顾不暇.(时间)冥思苦.想(用心)一丝不苟.(苟且、马虎)D.小心..谨慎(留心)纵横交错.(叉开) 有史可稽.(考核、核查)4.依次填入下列句子横线处的关联词,最恰当的是()也有的播迁他邦,重振雄风;也有的昙花一现,未老而先亡。
————,————它们内容的深浅,作用的大小,时间的久暂,空间的广狭,————它们存在过,————都是传统文化。
A.不过如果只要便B.不过即使如果就C.但是不管只要便D.但是也许如果就5.下列句子中标点使用规范的一项()A.“你打碎了我的盘子”,她很低沉地说:“我的小儿子没有饭吃了。
”B. 做年夜饭不能拉风箱——呱嗒呱嗒的风箱声会破坏神秘感——因此要烧最好的草、棉花柴或者豆秸。
天津一中2017-2018学年高三第一次月考化学试题Word版含解析.pdf

2017-2018学年本试卷分为第I卷(选择题)、第II卷(非选择题)两部分,共100分,考试用时90分钟。
第I卷1 至2页,第II卷2 至4 页。
考生务必将答案涂写答题纸或答题卡的规定位置上,答在试卷最新试卷十年寒窗苦,踏上高考路,心态放平和,信心要十足,面对考试卷,下笔如有神,短信送祝福,愿你能高中,马到功自成,金榜定题名。
上的无效。
祝各位考生考试顺利!第Ⅰ卷(本卷共20 道题,每题2分,共40分)相对原子质量:H:1 C:12 N:14 O:16 S:32 Mg:24 Cu: 64 Fe: 56 一.选择题(每题只有一个正确选项)1.化学与环境、材料、信息、能源关系密切,下列说法正确的是( )A.绿色化学的核心是应用化学原理对环境污染进行治理B.开发高效氢能、太阳能等新型电动汽车,以解决城市机动车尾气排放问题C.PM2.5是指大气中直径接近 2.5×10-6m的颗粒物,分散在空气中形成胶体D.半导体行业中有一句话:“从沙滩到用户”,计算机芯片的材料是二氧化硅【答案】B【解析】【考点定位】考查常见的生活环境的污染及治理;硅和二氧化硅【名师点晴】本题考查化学与环境、材料、信息、能源关系密切相关的知识,为高频考点,侧重于基础知识的综合理解和运用的考查,注意能形成胶体的微粒直径在1-100nm之间,为易错点,注意绿色化学的核心高频考点。
若NA表示阿伏加德罗常数,下列说法中正确的是( )A.16 g CH4与18 g NH4+所含质子数相等B.常温下,5.6g 铁钉与足量浓硝酸反应,转移的电子数为0.3 NAL-1 Na2CO3溶液中,阴阳离子总数为1.5 NAC.1L 0.5 mol·D.常温常压下,11g CO2气体中所含的分子数为0.25NA【答案】D【解析】【考点定位】考查阿伏加德罗常数和阿伏加德罗定律【名师点晴】本题考查了阿伏伽德罗常的应用,主要考查质量换算物质的量计算微粒数,盐类水解的应用,关键常温下铁在浓硫酸、浓硝酸中发生钝化。
高中化学 2020-2021学年下学期高三3月月考卷 化学(A卷)学生版

0-2021学年下学期高三3月月考卷化 学(A )注意事项:1.答题前,先将自己的姓名、准考证号填写在试题卷和答题卡上,并将准考证号条形码粘贴在答题卡上的指定位置。
2.选择题的作答:每小题选出答案后,用2B 铅笔把答题卡上对应题目的答案标号涂黑,写在试题卷、草稿纸和答题卡上的非答题区域均无效。
3.非选择题的作答:用签字笔直接答在答题卡上对应的答题区域内。
写在试题卷、草稿纸和答题卡上的非答题区域均无效。
4.考试结束后,请将本试题卷和答题卡一并上交。
相对原子质量:H 1 C 12 N 14 O 16 Cl 35.5 Fe 56 Mn 55 Ba 137一、选择题(每小题6分,共42分,每小题只有一个选项符合题意)7.2019年,中国研发的“双曲线一号”火箭在酒泉发射升空;2020年,中国“奋斗者”号载人潜水器成功进行深海科考活动。
下列说法正确的是A .“双曲线一号”火箭中使用的碳纤维树脂复合材料可同时满足耐高温、化学稳定性高等特殊需求B .制造潜水器载人球舱的钛合金比纯金属钛具有更高的强度、韧性和熔点C .“奋斗者”号返回水面的浮力材料纳米级玻璃微珠可产生丁达尔效应D .“奋斗者”号使用的深海水下超高压光纤微缆属于新型有机高分子材料 8.设N A 为阿伏加德罗常数的值。
下列说法正确的是A .1mol 金刚石中含有2N A 个C —C 键,1mol SiO 2含有2N A 个Si —O 键B .标准状况下,将9.2g 甲苯加入足量的酸性高锰酸钾溶液中转移的电子数为0.6N AC .在含CO 2−3总数为N A 的Na 2CO 3溶液中,Na +总数为2N AD .标准状况下,22.4L 庚烷中所含的分子数约为N A9.某有机化合物(结构如图)是一种重要的材料中间体,下列有关该化合物的说法中不正确的是A .分子式为C 10H 10O 6B .能与CH 3COOH 、NaHCO 3、NaOH 、Na 反应C .分子中环上的碳原子不可能位于同一平面D .与该分子式相同的有机物可能是芳香族化合物10.如图所示为某同学设计的检验浓硫酸和碳反应所得气体产物的实验装置图。
专题2.1.1 简单分类法及其应用-学易试题君之K三关2018-2019学年高一化学人教版(必修1)

第二章 化学物质及其变化第一节 物质的分类第1课时 简单分类法及其应用一、常见的分类法1.分类及其意义把大量的事物按照事先设定的__________进行分类,是人们最熟悉,也是最方便的一种工作方法。
这样,当分类标准确定之后,__________中的事物在某些方面的相似性可以帮助我们做到举一反三;对__________事物的了解使我们有可能做到由此及彼。
2.常见分类法交叉 分类法 含义 根据________的分类标准,对同一事物进行多种分类的一种分类方法举例树状 分类法 含义 对________事物按照某种属性进行________的分类法举例二、分类法的应用分类可以帮助我们更好地认识物质的性质,找出各类物质之间的关系。
如:Ca −−→①CaO −−→②Ca(OH)2 −−→③CaCO 3 C −−→④CO 2−−→⑤H 2CO 3−−→⑥CaCO 3 化学方程式分别为:①___________________________________; ②___________________________________; ③___________________________________; ④___________________________________; ⑤___________________________________;_____盐(根据阳离子)Na 2CO 3_____盐(根据阴离子) _____盐(根据溶解性)单质 _______物质纯净物_______⑥___________________________________。
【答案】一、1.标准同类不同类2.不同钠碳酸易溶同类再分类化合物混合物二、①2Ca+O22CaO②CaO+ H2O Ca(OH)2③Ca(OH)2+CO2CaCO3↓ +H2O④C+O2点燃CO2⑤CO2 + H2O H2CO3⑥Ca(OH)2 + H2CO3CaCO3↓ +2H2O一、根据纯净物的组成与性质对其进行分类【总结归纳】二、单质、酸、碱、盐、氧化物之间的转化关系有关化学方程式举例:①Mg+Cl2MgCl2②Fe+CuSO4FeSO4+Cu③Zn+H2SO4ZnSO4+H2↑④CaO+SiO2CaSiO3⑤CO2+Ca(OH)2CaCO3↓+H2O⑥CuO+H2SO4CuSO4+H2O⑦NaOH+HCl NaCl+H2O⑧3NaOH+FeCl 3Fe(OH)3↓+3NaCl⑨AgNO 3+HClAgCl↓+HNO 3 ⑩Na 2SO 4+BaCl 2BaSO 4↓+2NaCl典例1 (浙江省温州市十五校联合体2017−2018学年高一下学期期中联考)下列物质属于碱性氧化物的是 A .Na 2O B .SO 2 C .KOH D .H 2SO 4 【答案】A【解析】碱性氧化物是指溶于水而成碱或与酸反应而成盐的氧化物。
【精品】2017-2018年度九年级化学第1次月考试卷及答案

(1)氮气是无色无味的气体
;
(2)煤气燃烧
;
(3)水沸腾变成水蒸气
;
( 4)铁丝能在氧气中剧烈燃烧
。
24、造成空气污染的物质是
和
两大类。
ቤተ መጻሕፍቲ ባይዱ
25、某气体既能用排水法收集,又能用向上排空气法收集,该气体应具备的物理性质是
( 1) ___ ____
___
( 2) _
26、实验室制取氧气与工业制取氧气的本质区别是
,
再
。
(4)如果用 D 收集氧气,检验氧气是否收集满的方法是:
。
第4页
9、下列物质属于纯净物的是
A .食用醋
B .洁净的空气
C .含碘盐
D .蒸馏水
第1页
10、某集气瓶里盛有空气,采用燃烧法除去氧气而得到较纯净的氮气,最好采用的试剂是
A.铁丝
B .红磷
C .木炭
D .硫
11、学校运动会上,发令抢响后产生一缕白烟,你认为白烟的主要成份是
A. CO2
B
. P2O5
C
. SO2
2、在取用液体药品时,如果没有说明用量,一般应取用的最少量是
A . 0.5mL
B . 1mL~ 2mL
C . 3mL~ 4mL
D . 5mL~ 6mL
3、 实验室中,不小心将酒精灯碰倒在桌子上燃烧起来,合理简单的灭火方法是
A . 用水冲灭
B. 用书本扑打扑灭
C .用嘴吹灭
D . 用湿抹布盖灭
4、 1 元硬币的外观有银白色的金属光泽,一些同学认为它可能是铁制成的。在讨论时,有同学提出: “我们可以先拿磁铁来吸一下 ”。就 “拿磁铁来吸一下 ”这一过程而言,属于科学探究中的
山西省大同一中2017-2018学年高一上学期10月月考试题 化学 Word版含答案

大同一中2017-2018学年高一年级第一学期阶段考试(10月)化学可能用到的原子量:Cl--35.5 N--14 C--12 O--16 Al--27 S--32一、选择题(本题包括15小题,每小题3分,共45分。
每题只有一个选项符合题意)1.下列仪器中,可用酒精灯直接加热的是A.烧杯B.烧瓶C.锥形瓶D.蒸发皿2. 下列实验操作中,正确的是A.向试管中滴加试剂时,将滴管下端紧靠试管内壁B.不能用燃着的酒精灯去点燃另一酒精灯C.使用试纸检验溶液的性质时,将试纸浸入溶液中D. 加完药品后应将滴管洗净后再放回原瓶3.下列常用的混合物分离或提纯操作中,需使用分液漏斗的是A.过滤B.蒸发C.蒸馏D.分液4.在1g O2和1g O3中()A.所含原子数不相同B.所含分子数相同C.物质的量相同D.所含质子数相同5.下列叙述正确的是()A.NaCl的摩尔质量是58.5gB.64g氧气中含有2mol氧C.58.5g NaCl中含有1mol NaCl分子D.0.1mol二氧化碳含有6.02×1022个CO2分子6.用N A表示阿伏加德罗常数的值,下列叙述正确的是A.含有N A个氦原子的氦气的物质的量为2摩尔。
B.2摩尔水的摩尔质量是1摩尔水的摩尔质量的2倍。
C.25℃,1.01×105Pa,64g的SO2中含有的原子数为3N AD.1摩尔任何物质所含的分子数均为N A7.如果1g水中含有n个氢原子,则阿伏加德罗常数是()A.n/1 mol-1 B.9n mol-1 C.2n mol-1 D.n mol-1 8.下列有关化学实验安全问题的叙述中不正确的是A.少量的浓硫酸沾到皮肤上时,必须迅速用大量水冲洗B.取用化学药品时,应特别注意观察药品包装容器上的安全警示标记C.凡是给玻璃仪器加热,都要加垫石棉网,以防仪器炸裂D.闻任何化学药品的气味都不能使鼻子凑近药品9.在实验室从自来水制取蒸馏水的实验中,下列说法错误的是A.烧瓶中要放入碎瓷片防止暴沸B.不用温度计C.冷凝水应该是下进上出,与蒸汽的流向相反D.开始蒸馏时,应该先加热,再开冷凝水;蒸馏完毕,应该先关冷凝水再撤酒精灯10.将碘水中的碘萃取出来的实验中,下列说法错误的是A.分液漏斗使用前要检验它是否漏水B.萃取剂要求不溶于水,且比水更容易使碘溶解C.注入碘水和萃取剂,倒转分液漏斗反复用力震荡后立即分液D.分液时,打开旋塞,使下层液体流出,上层液体从上口倒出11.下列说法正确的是()A.物质的摩尔质量等于其相对分子(原子)质量B.“物质的量”是国际单位制中的一个基本单位C.0.012kg 12C中所含的碳原子数为N AD.1 mol任何物质都含有约6.02×1023个原子12、相同质量的下列气体中电子数最多的是:A.O2 B. Cl2 C. N2 D. CO213、下列叙述正确的是:A.阿伏加德罗常数个硫酸分子里含有4mol O B.CH4的摩尔质量为16g C.1mol Fe的质量为56g/mol D.1mol NH3 为18克14.对于相同物质的量的SO 2和SO 3,下列说法中正确的是A .硫元素的质量比为5:4B .分子数之比为1:1C .原子总数之比为2:3D .质量之比为1:1 15.某硫酸铝溶液中,含 Al 3+a g ,则溶液中SO24的物质的量为 ( )A .23a mol B .18a mol C .27amol D .96amol 二、填空题16.19g 某二价金属的氯化物ACl 2中含有0.4mol Cl -离子,ACl 2的摩尔质量是 ,相对分子质量是 ,A 的相对原子质量是 。
山西省大同市第一中学2017-2018学年高一12月月考化学试题 Word版含答案

2017-2018学年可能用到的相对原子质量:Na -23 H-1 O-16 Zn-65 Fe-56 Cu-64 Mg-24 Al-27一、(每小题只有一个正确选项,每小题3分,共45分)1、等质量的钠进行下列实验,其中生成氢气最多的是A.将钠投入到足量水中B.将钠用铝箔包好并刺一些小孔,再放入足量的水中C.将钠放入足量稀硫酸中D.将钠放入足量稀盐酸中2、下列反应中,氧化剂与还原剂物质的量之比为1∶2的是A. 3S + 6NaOH=2Na2S + Na2SO3 + 3H2OB. 2CH3COOH + Ca(ClO)2 = 2HC1O + Ca(CH3COO)2C. l2 + 2NaC1O3= 2NaIO3 + Cl2D. 4HC1(浓)+ MnO2△MnCl2十C12↑+ 2H2O3、氧化还原反应中,水的作用可以是氧化剂、还原剂、既是氧化剂又是还原剂、既非氧化剂又非还原剂等。
下列反应与Br2+ SO2+ 2H2O = H2SO4+ 2HBr相比较,水的作用不相同的是A. 2Al + 2NaOH + 2H2O = 2NaA1O2 + 3H2↑B. 4Fe(OH)2 +O2 + 2H2O = 4Fe(OH)3C. BrCl+ H2O = HCl + HBrOD. 2Na2O2 +2H2O = 4NaOH + O2↑4、已知下列分子或离子在酸性条件下都能氧化KI,自身发生如下变化:H2O2→H2O ,IO3-→I2,MnO4-→Mn2+,HNO3→NO。
如果分别用等物质的量的这些物质氧化足量的KI,得到I2最多的是A. H2O2B. IO3-C. MnO4-D. HNO35、下列各组物质中,第一种是含氧酸,第二种是强电解质,第三种是混合物的是A.水、纯碱、空气B. H2SO4、NaCl、烟C. HNO3、盐酸、碱石灰D.Fe2O3、BaSO4、饱和食盐水6、ClO2是一种消毒杀菌效率高、二次污染小的水处理剂,实验室可通过以下反应制得:2KClO3+H2C2O4+H2SO4△2ClO2↑+ K2SO4+2CO2↑+ 2H2O据此,下列说法不正确的是A. KClO3发生还原反应B. H2C2O4在反应中被氧化C. H2C2O4的氧化性强于ClO2的氧化性D.1mol ClO2生成,该反应转移的电子数约为6.02×10237、在强酸性溶液中,下列离子组能大量共存且溶液为无色透明的是A. Na+、K+、Cl-、CH3COO-B. Na+、MnO4-、SO42-、NO3-C. Mg2+、NH4+、SO42-、Cl-D. Ba2+、CO32-、NO3-、K+8、下列各项中,两种物质在溶液中的反应可用同一离子方程式表示的是A.醋酸与烧碱、硝酸与澄清石灰水B.氯化钡与硫酸钠、硫酸与硝酸钡C.碳酸铵与氢氧化钠、碳酸铵与石灰乳D.纯碱与硫酸、碳酸氢钾与盐酸9、下列离子方程式正确的是A.硝酸银溶液与铜:Cu + Ag+=Cu2++AgB.氧化铜与盐酸反应:O2-+2H+=H2OC.硫酸氢钠与氢氧化钠溶液混合:OH-+H+=H2OD.向澄清石灰水中加入盐酸:2H++Ca(OH)2 = Ca2+ +2H2O10、已知在碱性溶液中可发生如下反应:2R(OH)3+3ClO-+4OH-=2RO4n-+3Cl- +5H2O。
山西省大同市第一中学2017-2018学年高一5月月考化学试题 Word版含答案

一、单选题(每题3分,共48分)1. 下表是部分短周期元素的原了半径及主要化合价,根据表中信息,下叙述正确的是A. L2+与R2-B. M与T形成的化合物既能与酸反应又能与强碱反应C.氢化物的稳定性为H2T<H2RD.单质与浓度相等的稀盐酸反应的速率为Q>L2.已知33As、35Br位于同一周期。
下列关系正确的是A.原子半径:As>Cl>PB.热稳定性:HCl>AsH3>HBrC. 还原性:As3->S2->Cl-D.酸性:H3AsO4>H2SO4>H3PO43.某元素的一个原子形成的离子可表示为a b X n-,下列说法正确的是A. X n-含有的中子数为a+bB. X n-含有的电子数为a-nC. X原子的质量数为a+b+nD. X原子的质量约为b/(6.02×1023)4.下列关于热化学反应的描述中正确的是A. HCl 和NaOH反应的中和热△H=-57.3kJ/mol,则H2SO4和Ca(OH)2反应的中和热△H=2×(-57.3)kJ/molB. CO(g)的燃烧热是283.0kJ/mol,则2CO2(g)=2CO(g)+O2(g) △H=+2×283.0kJ/molC. 需要加热才能发生的反应一定是吸热反应D.1mol 甲烷完全燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热5. 少量铁粉与100mL 0.01mol/L的稀盐酸反应,反应速率太慢。
为了加快此反应速率而不改变H2的产量,可以使用如下方法中的①加H2O ②加NaOH固体③滴入几滴浓盐酸④加CH3COONa固体⑤加NaCl溶液⑥滴入几滴硫酸铜溶液⑦升高温度(不考虑盐酸挥发)⑧改用10mL 0.1mol/L盐酸A.③⑦⑧B.①⑥⑦C. ③⑤⑧D.⑤⑦⑧6.一定温度下,10mL0.40 mol/L H2O2溶液发生催化分解。
不同时刻测得生成O2的体积(已折算为标准状况)如下表。
【化学】山西省大同市第一中学2017-2018学年高一3月月考试题(解析版)

山西省大同市第一中学2017-2018学年高一3月月考试题1. 元素符号、反应方程式、结构示意图、电子式、结构式等通常叫做化学用语。
下列有关化学用语的表示方法中错误的是()A. 次氯酸的电子式为B. S2-的结构示意图为C. O-18的原子符号188OD. CO2分子的结构式:O=C=O【答案】A【解析】试题分析:次氯酸电子式中O原子在中间,A错,选A;S2-是18电子体,结构示意图正确,B对;不选;元素符号左上角表示的是质量数,左下角是质子数,C对,不选;CO2分子中C、O原子间以双键结合,结构式正确,D不选。
2. 下列各组物质中,化学键类型完全相同的是()A. HI 和NalB. H2S和CO2C. Cl2和CCl2D. NaOH和NaBr【答案】B【解析】HI为共价化合物,含有共价键,NaI离子化合物,含有离子键,A错误;H2S为共价化合物,含有极性共价键,而为极性共价键,所以化学键类型完全相同,B正确;含有非极性共价键,含有极性共价键,C错误;NaBr只含有离子键的离子化合物,NaOH含有离子键、极性共价键的离子化合物,化学键类型不完全相同,D错误;正确选项B。
3. 下列说法正确的是()A. 含有金属元素的离子—定是阳离子B. 含有离子键和共价键的化合物一定是离子化合物C. 目前使用的元素周期表中,最长的周期含有36种元素D. 第ⅦA族元素的阴离子还原性越强,其最高价氧化物的水化物的酸性越强【答案】B4. 镭是元素周期表中第七周期第ⅡA族元素,关于其叙述不正确的是()A. 镭在化合物中呈+2价B. 单质能与水反应生成H2C. 镭的属性比钙弱D. 碳酸镭难溶于水【答案】C【解析】镭最外层有两个电子,且失电子能力强,所以在化合物中呈价,A正确;镭的金属性强于钙,所以镭单质也能和水反应生成氢气,B正确;同主族元素,元素序数越大,金属性越强,所以镭的金属性比钙强,C错误;第IIA族元素与碳酸根生成的碳酸盐都难溶于水,D正确;正确选项C。
2017-2018学年度第一学期高一第一次月考成绩统计表
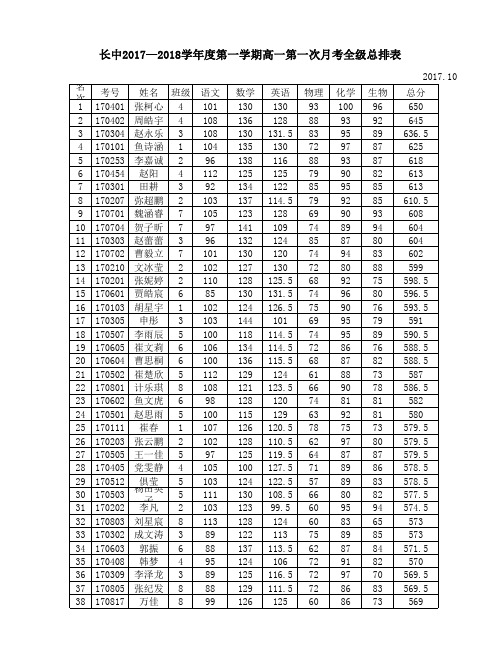
长中2017—018学年度第一学期高一第一次月考全级总排表
2017.10 名次 77 78 79 80 81 82 83 84 85 86 87 88 89 90 91 92 93 94 95 96 97 98 99 100 101 102 103 104 105 106 107 108 109 110 111 112 113 114 考号 170614 170104 170822 170712 170107 170834 170114 170115 170311 170708 171055 170318 170417 170815 170333 170519 170624 170217 170215 170308 170729 170514 170516 170617 170809 170811 170225 170711 170411 170610 170223 170406 170234 170108 170618 170211 170508 170616 姓名 班级 司梦晨 6 惠嘉康 1 胡叶叶 8 周逸飞 7 鱼朝阳 1 弥田 8 高金枝 1 尚甜甜 1 陈宝玲 3 李阳 7 杨广 10 杨扬 3 宇文雅 4 郭钾 8 黎佳昊 3 于莹莹 5 全宝婷 6 张晨 2 洪亦璇 2 李昭伟 3 解欣 7 陈雪彤 5 景凡 5 李一杰 6 党佳杰 8 尚国梁 8 罗睿青 2 剡心怡 7 梁娜 4 高星 6 曹亚鹏 2 曹锐洋 4 申岩 2 司帅 1 王帅 6 李煜 2 贾文丽 5 尚丁 6 语文 98 96 89 82 102 103 93 97 90 88 100 88 95 94 87 98 101 95 108 93 102 101 99 94 89 87 91 84 84 107 83 100 92 94 92 90 102 91 数学 117 126 117 119 101 126 112 109 107 120 118 101 103 119 113 115 124 92 97 108 120 116 111 113 138 118 114 123 118 125 123 98 111 102 133 113 112 110 英语 114 100 123.5 89.5 109 105.5 101.5 123 113 98.5 76 113 114.5 81.5 86.5 104 114.5 105.5 106.5 101.5 108 113 78 90.5 87 111.5 99 105 72 79.5 84.5 108.5 73 95.5 109.5 67.5 117 76 物理 57 60 67 67 70 48 66 50 58 65 64 61 63 62 80 59 42 69 47 45 56 42 62 55 44 57 65 56 74 50 62 69 80 68 56 70 52 67 化学 73 85 83 90 73 76 86 82 92 87 82 82 87 86 81 72 72 84 84 89 62 70 86 89 88 80 76 76 95 86 78 76 84 86 80 90 55 95 生物 77 68 54 86 78 74 74 71 71 72 89 83 64 84 79 78 72 79 79 85 72 78 84 78 73 65 72 73 73 68 84 62 73 67 42 82 74 73 总分 536 535 533.5 533.5 533 532.5 532.5 532 531 530.5 529 528 526.5 526.5 526.5 526 525.5 524.5 521.5 521.5 520 520 520 519.5 519 518.5 517 517 516 515.5 514.5 513.5 513 512.5 512.5 512.5 512 512
2017-2018 学年.七中.高一下.第一次月考化学试卷及答案

2.能作为 Cl、Br、I 元素非金属性递变规律的判断依据的是( )
①Cl2、Br2、I2 的熔点
②Cl2、Br2、I2 的氧化性
③HCl、HBr、HI 的热稳定性
④HCl、HBr、HI 的酸性
A.①②③
B.②③
C.②③④
D.①②③④
器 3.下列各组物质中化学键的类型完全相同的是( )
A.NaCl MgCl2 Na2O
2017-2018 学年.七中.高一下.第一次月考.试卷及答案
一、选择题(共 16 小题,每小题 4 分,共 64 分)
1.中国科Lv
的名称为鉝。关于
293 116
Lv
的叙述错误的是
()
A.原子序数 116
B.中子数 177
C.核外电子数 116
D.质 子 数 177
B.H2O
辑 C.Na2S NaOH H2SO4
D.NH4Cl
MgO CO2 NaNO3 NH3
4.下列分子的电子式书写正确的是( )
编 A.氨气
C.氮气
B.四氯化碳 D.二氧化碳
捷PDF 5.下列反应过程中的能量变化与如图一致的是( )
迅A. 2Al + Fe2O3 高温 2Fe + Al2O3 C. C + H2O 高温 CO + H2
B. CaCO3 高温 CaO + CO2 ↑ D. C + CO2 ∆ 2CO
6.关于碱金属元素的说法中正确的是( ) A.ⅠA 族元素都是碱金属元素 B.碱金属单质可将铜从其盐溶液中置换出来 C.金属钾具有强还原性,K+具有强氧化性 D.Cs 常温下与水反应会发生爆炸
7.反应 3A(g) + B(g)=2C(g) + 2D(g) ,在不同条件下,用不同物质表示其反应速率,分别为 ①v(A) = 0.6mol ⋅ L−1 ⋅ min−1 ②v(B) = 0.45mol ⋅ L−1 ⋅ min−1 ③v(C) = 0.02mol ⋅ L−1 ⋅ min−1 ④v(D) = 0.45mol ⋅ L−1 ⋅ min−1
大同市2017-2018学年高二5月月考化学试题含答案

可能用到的相对原子质量:H-1 B-11 C-12 N-14 O-16 F -19 Ca-40 Cu-64 ―、选择题(16个小题,每题2分,共32分,每小题只有一个选项符合题意。
)1、下列说法或有关化学用语的表达正确的是A.在基态多电子原子中,p轨道电子能量一定高于s轨边电子能量B.基态Fe原子的外围电子排布图为C.因氧元素电负性比氮元素大,故氧原子第一电离能比氮原子第一电离能大D.根据原子核外电子排布的特点,Cu在元素周期表中位于s区23、现有三种元素的基态原子的电子排布式:①1s22s22p63s23p4;②1s22s22p63s23p3;③1s22s22p5。
则下列有关比较中正确的是A.第一电离能:③>②>①B.原子半径:③>②>①C.电负性:③>②>①D.最高正化合价:③>②>①4、下列各组微粒的空间构型相同的是①NH3和H2O ②NH4+和H3O+ ③NH3和H3O+ ④O3和SO2 ⑤CO2和BeCl2 ⑥SiO44- 和SO42- ⑦BF3和A12C16A.全部B.除④⑥⑦以外C.③④⑤⑥D. ②⑤⑥5、关于化学式[TiCl(H2O)5]Cl2·H2O的配合物的下列说法中正确的是A.配位体是Cl-和H2O,配位数是9B.中心离子是Ti4+,配离子是[TiCl(H2O)5]2+C.内界和外界中的Cl的数目比是1∶2D.加入足量AgNO3溶液,所有Cl-均被完全沉淀6、最近发现一种由钛(Ti)原子和碳原子构成的气态团簇分子,分子模型如图所示,其中圆圈表示钛原子,黑点表示碳原子,则它的化学式为A. TiCB. Ti13C14C. Ti4C7D. Ti14C137、下列叙述错误的是①离子键没有方向性和饱和性,而共价键有方向性和饱和性;②配位键在形成时,是由成键双方各提供一个电子形成共用电子对;③金属键的实质是金属中的“自由电子”与金属阳离子形成的一种强烈的相互作用;④在冰晶体中,既有极性键、非极性键,又有氢键;;⑤化合物NH4Cl和CuSO4.5H2O都存在配位键;⑥NaCl、HF、CH3CH2OH、SO2都易溶于水,但原因不完全相同A. ①③B. ②④C. ②⑤D. ④⑥8、下列关于晶体的说法中,不正确的是①晶体中原子呈周期性有序排列,有自范性;而非晶体中原子排列相对无序,无自范性;②含有金属阳离子的晶体一定是离子晶体;③共价键可决定分子晶体的熔、沸点;④MgO的晶格能远比NaCl大,这是因为前者离子所带的电荷数多,离子半径小;⑤晶胞是晶体结构的基本单元,晶体内部的微粒按一定规律作周期性重复排列;⑥晶体尽可能采取紧密堆积方式,以使其变得比较稳定;⑦干冰晶体中,一个CO2分子周围有12个CO2分子紧邻;CsCl和NaCl晶体中阴、阳离子的配位数都为6A. ①②③B. ②③④C. ④⑤⑥D. ②③⑦9、除去下列物质中所含少量杂质(括号内为杂质),所选用的试剂和分离方法能达到实验目10、某烃结构式用键线表示为,该烃与Br2按物质的量之比为1 : 1加成时,所得产物有A. 3种B. 6种C. 5种D. 4种11、有关分子结构的下列叙述中正确的是①除苯环外的其余碳原子有可能都在一条直线上②除苯环外的其余碳原子不可能都在一条直线上③12个碳原子不可能都在同一平面上④12个碳原子有可能都在同一平面上A. ①②B. ②③C. ①③D. ②④12、金刚烷(C10H16)是一种重要的脂肪烷烃,其结构高度对称,如右图所示。
化学-山西省大同市第三中学2017-2018学年高一4月月考试题

山西省大同市第三中学2017-2018学年高一4月月考试题可能用到的相对原子质量:Zn-65 Fe-56 S-32 C-12 N-14 H-1 O-16 Mg-24 Cl-35.5 Na -23 Al-27 Si-28 Ca-40一、选择题(本题包括25小题,每题2分。
每小题只有1个选项符合题意。
50分)1、下面是元素周期表的一部分(表中数字和X代表原子序数),其中x为53的是()A. B.C. D.2、X 元素最高价氧化物对应的水化物为H3XO4,则它对应的气态氢化物为()A.HXB.H2XC.XH4D.XH33、下列含有非极性键的共价化合物是()A.HC1B.Na2O2C.H2O2D.H2R n+,则元素R的原子序数是()4、已知某粒子AZA.ZB.A-ZC.Z-nD.Z+n5、元素的性质随着元素原子序数的递增而呈周期性变化的原因是()A.元素原子的核外电子排布呈周期性变化B.元素的原子半径呈周期性变化C.元素的化合价呈周期性变化D.元素的金属性、非金属性呈周期性变化6、已知周期表中短周期的一部分如图所示,若a原子最外层电子数比次外层电子数少3,下列说法中不正确的是()A.原子半径大小顺序是c>b>d>aB.d的氢化物比a的氢化物稳定C.a和d的原子结合可以形成带3个负电荷的阴离子D.a、b、c最高价氧化物对应水化物的酸性强弱关系是c>b>a7、X、Y均为短周期元素,X位于IA族,X、Y能形成X2Y化合物,下列说法正确的是()A.X与Y形成的化合物中原子个数比可能为1: 1B.X2Y不可能是共价化合物C. X和Y分别形成的简单离子不可能具有相同电子层结构D.根据周期表递变规律判断X原子半径一定大于Y原子半径8、已知X+、Y2+、Z-、W2-四种离子均具有相同的电子层结构。
下列关于X、Y、Z、W四种元素的描述,不正确的是()A.原子序数:Y>X>Z>WB.离子半径:X+>Y2+>Z->W2-C.原子最外层电子数:Z>W>Y>XD.还原性:X>Y,W2->Z-9、下列有关元素周期律的叙述中,正确的是()A.氧化性强弱:F2<C12B.金属性强弱:K<NaC.酸性强弱:H3PO4<H2SO4D.碱性强弱:NaOH<Mg(OH)210、下列关于元素周期表的说法正确的是()A.能生成碱的金属元素都在ⅠA族B.原子序数为14的元素位于元素周期表的第3周期ⅣA族C.稀有气体元素原子的最外层电子数均为8D.第二周期ⅣA族元素的原子核电荷数和中子数一定为611、已知同周期X、Y、Z三种元素的最高价氧化物对应水化物酸性由强到弱的顺序为HXO4>H2YO4>H3ZO4,则下列判断中正确的是()A.元素非金属性技X、Y、Z的顺序减弱B.阴离子的还原性按X、Y、Z的顺序减弱C.气态氢化物的稳定性按X、Y、Z的顺序增强D.单质的氧化性按X、Y、Z的顺序增强12、下列电子式书写正确的是()A. B. C. D.13、下列关于ⅦA族元素的叙述正确的是()A.ⅦA族元素是同周期中原子半径最大的元素(惰性气体元素除外)B.ⅦA族元素是同周期中非金属性最弱的元素C.ⅦA族元素的最高正价都是+7价D.ⅦA族元素其简单阴离子的核外电子层数等于该元素所在的周期数14、下列各组元素性质递变情况错误的是()A. Li、Be、B原子最外层电子数逐渐增多B.N、O、F原子半径依次增大C.P、S、C1最高正价依次升高D.Li、Na、K、Rb的金属性依次增强15、含硒(Se)的保健品已开始进入市场。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
可能用到的相对原子质量H—1 Li—7 O—16 Na—23 K—39
一、选择题(每题4分,共48分)
1.YBa2Cu8O x(Y为元素钇)是磁悬浮列车中的重要超导材料,关于的说法正确的是()A.Y在周期表中的位置是第4周期IIIB族B.属于非金属元素
C.核素的质子数与中子数之差为50 D.和是两种不同的核素
2.下列叙述正确的是()
A.碱金属元素是指IA族的所有元素
B.副族元素没有非金属元素
C.同周期第ⅡA族和第IIIA族的元素,原子序数之差只能是1或25
D.部分卤族元素的某种性质A随核电荷数的变化趋势如右上图所示, 则A可能表示单质的熔沸点
3.与NH4+质子总数和电子总数都相同的微粒是()
A.Al3+ B.H3O+ C.OH-D.H2O
4.我国在砷化镓太阳能电池研究方面处于国际领先地位。
砷(As)和镓(Ga)都是第四周期元素,分别属于第V A族和第IIIA族元素。
下列说法中不正确的是()
A.原子半径:Ga>As>P B.热稳定性:NH3>PH3 >AsH3
C.酸性:H3AsO4>H2SO4>H3PO4D.Ga(OH)3可能是两性氢氧化物
5.下列说法中不正确的是()
①质子数相同的粒子一定属于同种元素;
②同位素的性质几乎完全相同;
③质子数相同,电子数也相同的两种粒子,不可能是一种分子和一种离子;
④电子数相同的粒子不一定是同一种元素;
⑤一种元素只能有一种质量数;
⑥某种元素的相对原子质量取整数,就是其质量数
⑦元素周期表中从ⅢB族到ⅡB族10个纵行的元素都是金属元素
⑧核外电子排布相同的微粒化学性质不一定相同
⑨与得电子能力相同
A.①②④⑤B.③④⑤⑥C.②③⑤⑥D.①②⑤⑥6.几种短周期元素的原子半径及某些化合价见下表。
分析判断下列说法正确的是()
A.A的单质是一种常见的还原剂B.E的含氧酸酸性比D的含氧酸酸性强
C.A、I、J的商子半径由大到小顺序是A>J>I D.A的气态氢化物是强酸7.X、Y、Z均为短周期元素,X、Y处于同一周期,X、Z的最低价离子分别为X2-和Z-,Y+和Z-具有相同的电子层结构。
下列说法正确的是()
A.原子的最外层电子数:X>Y>Z B.阴离子还原性:X2-<Z-
C.离子半径:X2->Y+>Z-D.原子序数:X>Y>Z
8.A、B、C、D为原子序数依次增大的同周期的短周期元素,己知A、C、D三种元素原子的最外层共有11个电子,且这三种元素的最高价氧化物对应的水化物之间两两皆能反应,均生成盐和水。
下列判断正确的是()
A.C、D的最高价氧化物对应的水化物分別是强碱、强酸
B.A、C、D 三种元素有两种是金属,一种是非金属
C.D元素位于第3周期VIA族
D.A、B、C三种元素阳离子氧化性由强到弱为A>B>C
9.有X、Y两种元素,原子序数≤20,X的原子序数小于Y,且X、Y原子的最外层电子数
相同(选项中m、n均为正整数)。
下列说法正确的是()
A.若X的最高价含氧酸为强酸,则X的氢化物溶于水一定显酸性
B.若Y的最高正价为+m,则X的最高正价一定为+m
C.若X元素形成的单质是X2,则Y形成的单质一定是Y2
D.若X(OH)n为强碱,则Y(OH)n也一定为强碱
10.X、Y、Z、W、M均为短周期主族元素,原子序数依次增大,X 质子总数与电子层数相同,Y元素的一种同位素可用于考古时测定一些文物的年代,z的气态氢化物可以与Cl2反应产生白烟,用来检验氯气管道是否泄漏。
Y、Z、W位于同一周期,且最外层电子数之和为15,M的质子数是X、Y、Z、W四种元素质子数之和的1/2,下列说法正确的是()
A.原子半径M>W>Y>Z>X
B.1molM2W2溶于足量的水中完全反应,共转移2mol电子
C.X、Z两种元素只能组成化学式为ZX3的化合物
D.最简单气态氢化物的稳定性:W>Z>Y
11.四种主族元素的离子a X m+、b Y n+、c Z n-和d R m-(a、b、c、d为元素的原子序数),它们具有相同的电子层结构,若m>n,则下列叙述正确的是()
①a-b=n-m ②元素的原子序数:a>b>c>d
③元素非金属性:Z>R ④最高价氧化物对应的水化物的碱性:X>Y
A.只有③B.①②③④C.①②③D.②③
12.有a X n-和b Y m+两种简单离子,且X、Y均为短周期元素,已知X n-比Y m+多2个电子层,下列关系和说法正确的是()
A.Y可能是第二周期元素B.a-b+n+m的和只可能等于10
C.b大于5 D.X只能是第三周期元素
二、非选择题(共52分)
13.(18分)己知H元素有多种同位素。
(1)有H、D()、T()三种原子,各自可形成双原子分子H2、D2、T2。
①标准状况下,它们的密度之比为。
②相同物质的量的三种单质中,质子数之比为。
③同温同压下,1L各单质气体中所含电子数之比为。
(2)36gH2O与80gD2O的物质的量之比是,它们分別与Na反应时,所放出气体体积之比(同条件)是,质量之比是。
14.(19分)X、Y、Z、W、T是原子序数依次増大的五种短周期元素,且X、Y、Z、W的原子序数之和为32。
其中X是元素周期表中原子半径最小的元素,Y、Z左右相邻,Z、W位于同一主族。
T的单质常用于自来水的杀菌消毒。
请回答下列问题:
(1)W元素在周期表中的位置为:
(2)由X、Y、Z、W四种元素中的三种组成一种强酸,该强酸的稀溶液能与金属铜反应,该反应的离子方程式为。
(3)Y元素的气态氢化物与其最高价氧化物的水化物可以相互反应,写出其离子方程式:
(4)Y和T两元素的非金属性强弱为Y T (填“>”“<”或者“=”)。
可以验证该结论的方法是A.比较这两种元素的气态氢化物的沸点
B.比较这两种元素所形成含氧酸的酸性
C.比较这两种元素的气态氢化物的稳定性D.比较这两种元素与氢气化合的难易程度
E.比较这两种元素气态氢化物的还原性
(5)某化学兴趣小组欲通过实验探究元素N、C、Si 非金属性强弱。
实验装置如下:
①溶液a和溶液b分别为溶液、溶液(填溶质化学式)
②经验证,N、C、Si的非金属性由强到弱为:
15.(14分)利用元素周期表,我们可以认识更多元素的性质
(1)元素周期表位于对角线的两种元素其性质相似称之为对角线规则。
根据周期表对角线规律,金属Be单质及其化合物的性质与铝单质及其化合物的性质相似。
则鉴别说Be(OH)2和Mg(OH)2可选用的试剂为溶液。
(2)铅(Pb)、锡(Sn)、锗(Ge)与元素(C)、硅(Si)同主族,常温下其单质在空气中,锡、锗不反应而铅表面生成一层氧化铅;锗与盐酸不反应,而锡与盐酸反应。
由此可得出以下结论:
①锗的原子序数为;
②铅(Pb)、锡(Sn)、锗(Ge)的+4价氢氧化物的碱性由强到弱的顺序为
(填化学式)。
(3)最近,德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来最重大突破。
己知铷(Rb)是37号元素,质量数是85,与钠同主族。
回答下列问题:
①铷在周期表中的位置为
②同主族元素的同类化合物的性质相似,请写出:
AlCl3与过量的RbOH反应的离子方程式:
③现有铷和另一种碱金属形成的混合金属50g,当它与足量水反应时,放出标准状况下的氢气22.4L,这种碱金属可能是
A.Li B.Na C.K D.Cs
一、选择题(每题4分,共48分)
1-5 DBBCD 6-10 CDBDD 11.D 12.A
二、非选择題(共52分)
13.(每空3分,共18分)
(1)① 1∶2∶3 ② 1∶1∶1 ③ 1∶1∶1
(2)1∶2 1∶2 1∶4
14.(共20分)
(1)第三周期第VIA族(2 分)
(2)3Cu + 8H+ +2NO3- = 3Cu2+ +2N O↑ +4H2O (3 分)(3)NH3 + H+=NH4+(3 分)
(4)<(2 分)CDE(3 分)
(5)①HNO3(2 分)NaHCO3(2 分)
②N>C>Si (3 分)
15.(共14分)
(1)NaOH (2 分)
(2)32 (2 分)Pb(OH)4>Sn(OH)4>Ge(OH)4(3 分)
(3)①第五周期第ⅠA族(2 分)
②Al3+ + 4OH- = A1O2-+2H2O (3分)
③AB (2 分)。
