九年级化学溶解度1(1)
广东省珠海十中九年级化学下册《9.2溶解度(第1课时)》教案 新人教版

广东省珠海十中九年级化学下册《9.2溶解度(第1课时)》教案新人教版
教学难点:固体物质溶解度的涵义;利用溶解度曲线获得相关信息。
教学器材:烧杯、试管多个、 NaCl、 KNO3、酒精灯、火柴、胶头滴管、氢氧化钙、试管夹等。
教学方法:提出问题→建立假设→设计方案→动手实验→观察记录→
分析现象→得出结论。
教学课时:2课时
教学过程:
备注盐呢?
上述活动的“一定条件”是什
请大家根据刚才的分析,总结饱和溶液与不饱和溶液的科学概念。
在一定条件下,溶质是否继续溶解。
调动学生的逆向思维,思考:如何将接近饱和的溶液转化为饱和溶液
溶液的概念,理解了饱和溶液只有在一定
℃时,硝酸钾的溶解度为
℃时氯化铵的溶解度为
比较某一温度下不同物质的溶解度大小;大多数物质的溶解度随温度升高而增
)大致了解气体溶解度受温度、压强的影响关系。
初中九年级化学教案溶解度(教案)

第2课时溶解度课标要求教学目的】1.知识与技能(1)了解固体物质溶解度地涵义。
(2)会利用溶解性表或溶解度曲线,查阅有关物质地溶解性或溶解度,能依据给定地数据绘制溶解度曲线。
(3)知道影响气体溶解度地一些因素,会利用有关气体溶解度地知识解释身边地一些现象。
2.过程与方法(1)学习观察,分析实验现象,并能归纳出相应地概念。
(2)学习通过实验解决问题。
3.情感态度与价值观(1)认识矛盾双方在一定条件下可互相转化地辩证思想。
(2)树立做任何事都要实事求是地观点。
教学重点】利用溶解度曲线获得有关信息。
教学难点】1.固体物质溶解度地意义。
2.利用溶解度曲线获得有关信息。
教具准备】多媒体课件等。
教学过程复习提问】上节课我们学习了饱与溶液与不饱与溶液,为什么只有在“两个一定条件”下,它们才有确定意义?交流回答】改变条件可以使饱与溶液与不饱与溶液相互转化。
导入新课】通过前面地学习我们知道:不同物质在同一溶剂中溶解能力不同;同一种物质在不同溶剂中溶解能力也不相同。
这节课我们就从量地角度研究物质地溶解能力。
活动与探究1】1.向盛有20°C水地烧杯中加入NaCl,向盛有40°C等量水地烧杯中加入溶解地量,并讨论能否在该条件下定量KN03都达到饱与状态。
比较NaCl与 KN03地比较二者地溶解能力?,都达到饱与状态。
2.向40g20°C水中加入NaCl,向100g20°C水中加入KN03比较它们溶质地量,讨论能否在该条件下定量地比较二者地溶解能力?3.向100g20°C水中加入NaCl直到饱与,向100g20°C水中加入KN03配制成不饱与溶液。
比较二者溶解地量,讨论能否在该条件下定量地比较出二者地溶解能力?归纳总结】定量描述物质地溶解能力(即溶解度)地要素:①在一定温度下;②等量地溶剂里,人们统一规定:在100g溶剂里;③溶液为饱与状态;④单位为g。
固体地溶解度:在一定温度下,某固态物质在100g溶剂里达到饱与状态时所溶解地质量。
【核心素养】课题2第1课时《溶解度》教学设计

人教版九年级化学下册《第九单元课题2溶解度》第1课时教学设计【教材分析】《溶解度》是人教版九年级化学下册第九单元课题2的内容。
在课题1学习的基础上,学生对溶液的概念,溶质和溶剂的概念,溶解的过程,溶液的用途有了一定的了解。
基于溶液在化学研究和生产、生活中有着广泛的应用,本节课是在是定性的研究上进一步从定量的角度介绍物质在水中溶解的限度。
通过饱和溶液和不饱和溶液的定义的理解,以及它们之间相互转化,结晶等的学习,加深学生对物质溶解性和溶液的认识。
【学情分析】学生已了解了溶液的概念,溶质和溶剂的概念,溶液的用途,会从微观角度理解溶解的过程,定性地了解溶液的组成和基本特征。
学法上学生已经基本会通过实验现象推理出实验结论,但对问题缺乏科学全面的分析能力,容易将一般规律绝对化。
【教学目标】1.通过数据或实验现象判断某溶液是否达到饱和状态。
说明饱和溶液与不饱和溶液之间的转化方法。
2.知道饱和溶液、不饱和溶液与浓溶液、稀溶液之间的关系。
3.通过理解饱和状态,举例说明结晶现象并根据实验过程辨别结晶的两种方法。
【教学重点】知道什么是饱和溶液和不饱和溶液,知道两者之间如何转化。
【教学难点】饱和溶液、不饱和溶液与浓溶液、稀溶液之间的关系。
【教学方法】问题衍生教学法、引导探究法、分组实验、多媒体辅助教学法,实验探究法、合作交流法【教学准备】教师准备:氯化钠、硝酸钾、高锰酸钾、烧杯等。
学生准备:预习课本了解化学的内容。
【教学过程】【新课导入】【温故而知新】1.溶液的特征:__________、____________、___________2.________分散到液体里形成的混合物叫做乳浊液。
乳浊液_______,_______能够增强乳浊液的稳定性。
提出问题:一种物质在水里能不能无限制的溶解呢?引入新课【新知探究】一、饱和溶液与不饱和溶液【实验探究】:在室温下,向盛有20mL水的烧杯中加入5g氯化钠,搅拌,等溶解后,再加5g氯化钠,搅拌,观察现象。
9.2溶解度(第1课时)教学设计---九年级化学人教版下册

溶解度教学设计课程:初中化学九年级下课题:第九单元课题二溶解度(第一课时)执教:班级课型:事实—理论课一、学生学情分析:学习了课题一,对溶液的概念,组成和特点,溶液的吸热与放热现象和如花现象有一定的认识,在此基础上进一步对溶液的饱和程度和溶解度的学习,是一个循序渐进的过程。
二、教学目标:1.知识与技能:①理解饱和溶液与不饱和溶液的含义②饱和溶液与不饱和溶液之间的转化关系2.过程与方法:①学习观察实验现象,归纳出相应的概念②学习通过实验解决问题3.情感态度与价值观:①树立实事求是的观点②建立运用实验数据和实验现象解释实验本质③学习矛盾的双方在一定的条件下可以相互转化的辩证唯物主义理念三、教学重难点:1、重点:①理解饱和溶液与不饱和溶液②饱和溶液与不饱和溶液之间的转化关系及结晶方法2、难点:正确理解饱和溶液的含义四、教学方法:实验探究法,讲授法,讨论法五、教学用具:酒精灯、烧杯、玻璃棒、石棉网、铁架台,氯化钠固体,硝酸钾固体,多媒体课件,六、教学过程:七、板书设计:§9.2.1溶解度(第一课时)1、饱和溶液与不饱和溶液的定义2、饱和溶液的判断3、结晶4、不饱和溶液与饱和溶液的转化关系及结晶的方法八、重难点分析:对于这个知识点中包含的两个概念如果单独提取出来学生基本是可以理解的,但是这两个概念的成立又有一些限定条件,比如:饱和溶液就是在一定温度下、一定量溶剂中溶解某种溶质到不能继续溶解时的溶液。
这些条件的理解对学生来说有一定难度,当这些条件发生变化后饱和溶液和不饱和溶液还能相互转化,这对学生来说难度就更深一层。
对学生来说在理解这个只是点的时候可以借助部分的生活经验,但是两种溶液相互转化的方式不止一种,当涉及到通过升温、降温的方式时,就必须借助实验才能让学生比较明白这种现象,如果想要彻底理解这个原理并且应用到实际题目中就需要学生有比较强的逻辑思维能力,所以对学生来说还是有难度的。
九、教学反思:1、本节课的成功之处:①设计了三个环节的实验,从实验的角度验证饱和溶液的定义,加深学生的印象。
人教版初中化学九年级下册课题2《溶解度》-课件

4、“在一定量的氯化钠溶液中,加入少量 硝酸钾固体,发现硝酸钾固体消失,则说 明原氯化钠溶液不饱和。”这句话是否正 确? 错误
问:“相同溶质、相同温度:饱 和溶液一定比不饱和溶液所含溶
质多”这句话对不对? 错
下列说法不正确的是( A )
A、浓溶液一定是饱和溶液 B、稀溶液可能是饱和溶液 C、在一定条件下,饱和溶液与不饱和溶液之
间可相互转化
D、在提到某种物质的溶解度时,一定要指明 温度
二、溶解度
1、溶解性:一种物质溶解在另一种物质的能力 思考:如何判断糖和食盐的溶解性?
饱和溶液的浓度一定比较大吗? 不饱和溶液的浓度一定比较小吗?
5、浓溶液与稀溶液
在同量的溶液中,含溶质较多的溶液——浓溶液;
含溶质较少的溶液——稀溶液 不同的溶质:
浓溶液不一定是饱和溶液,稀溶液不一定是不饱和溶液; 饱和溶液也不一定是浓溶液,不饱和溶液也不一定是稀 溶液。
相同溶质、相同温度:饱和溶液一定比不饱和 溶液浓。
饱和状态时所溶解的质量。
(3)影响因素
(2)
四
一定温度 100g溶剂(一般指水)
温度
要 素
达到饱和
溶质、溶剂 本身的性质
单位: 克
讨论:
200c时硝酸钾的溶解度为31.6g,这句话 的含义
温度 溶质的 质量
溶剂的 饱和溶液
质量
的质量
200c 31.6g
100g
131.6g
九年级化学第七章:溶液;溶解度人教版知识精讲

九年级化学第七章:溶液;溶解度人教版【本讲教育信息】一. 教学内容:第七章(一)溶液1. 溶液溶质和溶剂的概念并能分辨溶质和溶剂。
2. 溶液的概念和基本特征。
3. 溶液在生活和生产中的应用。
(二)饱和溶液和不饱和溶液1. 饱和溶液和不饱和溶液的概念,并能区分浓溶液和稀溶液2. 饱和溶液和不饱和溶液在一定条件下的相互转化(三)溶解度1. 影响物质溶解性的因素2. 溶解度的概念和有关概念的计算二. 重点、难点:1. 溶液、饱和溶液、不饱和溶液的概念。
2. 溶解度的概念和有关概念的计算【教学过程】一. 溶液1. 概念:溶液是一种或几种物质分散到另一种物质里,形成均一的、稳定的混合物,叫溶液。
均一是均匀的意思,稳定意味静置后不会产生沉淀和分层的现象。
2. 在溶液里,能溶解其它物质的物质叫溶剂;被溶解的物质叫溶质。
例如,CuSO4溶液中,水是溶剂,CuSO4是溶质。
溶质可以是固体,也可以是液体或气体。
固体、气体溶于液体时,固体、气体是溶质,液体是溶剂。
两种液体相互溶解时,通常把量多的一种叫做溶剂,量少的一种叫做溶质。
当溶液中有水存在时,无论水的量有多少,习惯上把水看作溶剂。
通常不指明溶剂的溶液,一般是水溶液。
3. 注意事项⑴溶液一般是透明的,但透明不一定无色。
例如硫酸铜溶液是蓝色的。
溶液是由溶质和溶剂组成的。
溶液的质量等于溶质质量和溶剂质量之和。
但溶液体积不等于溶质体积和溶剂体积之和,这是受到分子间的间隔影响。
⑵物质在溶解的过程中发生了化学变化,在形成的溶液中,溶质是反应后的生成物。
例如,将锌与适量稀硫酸反应,锌逐渐溶解,但形成的溶液中溶质是硫酸锌,而不是锌。
也就是说,形成的溶液是硫酸锌的水溶液,而不是锌的硫酸溶液,。
又如,碳酸钙溶于稀盐酸,所得溶液中的溶质是氯化钙。
还有将蓝矾(胆矾)溶于水时,形成的溶液中溶质是硫酸铜,而不是胆矾。
二. 饱和溶液和不饱和溶液1. 概念:饱和溶液和不饱和溶液在一定温度下,在一定量溶剂里,不能再溶解某种溶质的溶液,叫做这种溶质的饱和溶液;还能继续溶解某种溶质的溶液,叫做这种溶质的不饱和溶液。
初中化学溶解度表及口诀

初中化学溶解度表及口诀
初中化学溶解度表及口诀如下:
口诀:
钾钠铵盐硝酸盐,完全溶解不困难,氯化亚汞氯化银,硫酸钡和硫酸铅,生成沉淀记心间,氢硫酸盐和碱类,碳酸磷酸硝酸盐,可溶只有钾钠铵。
钾钠铵硝皆可溶,盐酸不溶银亚汞;硫酸不溶钡和铅,碳磷酸盐多不溶;多数酸溶碱少溶,只有钾钠铵钡钙。
钾钠铵盐硝酸盐,溶入水中都不见;硫酸盐类不溶钡,氯化物中不溶银;碳酸盐类多不溶,只有钾钠铵盐溶。
溶解度表:
钾盐、钠盐、铵盐、硝酸盐都溶于水。
硫酸盐除了硫酸钡、硫酸铅不溶,硫酸钙、硫酸银微溶外,其他都溶。
盐酸盐除了氯化银不溶外,其他都溶。
碳酸盐除了碳酸钾、碳酸钠、碳酸铵溶外,其他都不溶。
需要注意的是,口诀和表格只是帮助记忆的工具,具体物质的溶解度还需要参考实验数据和资料。
此外,溶解度不仅受物质本身性质的影响,还与温度、压强等条件有关。
因此,在理解和应用溶解度概念时,需要综合考虑各种因素。
【人教初中化学九年级下期】第九单元课题2溶解度教案

第九单元溶液课题2 溶解度一、教学目标通过实验探究,建立饱和溶液与不饱和溶液的概念,了解饱和溶液与不饱和溶液的相互转化的方法,了解结晶现象。
初步培养活动与探究的一般程序:提出问题→建立假设→设计方案(画出实验简图)→动手实验→观察记录→分析现象→得出结论。
通过实验条件的改变,让学生感受饱和溶液与不饱和溶液的存在和转化是有条件的,逐步建立用辩证的、发展的思想观点来看待事物的变化,和逐步培养由具体到一般认识事物过程的能力,并培养学生互相协作、友好相处的健康心态。
二、重点和难点三、课时安排 2课时本结课我们探究了饱和溶液和不饱和溶液的概念,了解了饱和溶液只有在一定条件下才有确定的意义,总结出了判断饱和溶液和不饱和溶液的方法及它们之间相互转化的条件。
最后我们还学习了结晶的两种方法。
板书设计饱和溶液1、饱和溶液的概念不饱和溶液的概念2、饱和溶液与不饱和溶液的转化的条件3、确定某种溶液是否饱和的方法4、结晶结晶的概念结晶的方法1、下列说法正确的是()A、相同温度下,饱和溶液一定比不饱和溶液浓B、饱和溶液一定是浓溶液C、不饱和溶液降温不一定会变成饱和溶液D、对同种溶质来说,饱和溶液一定比不饱和溶液浓2、现有下列方法:①升高温度②降低温度③增加硝酸钾④减少硝酸钾⑤增加水⑥蒸发水。
能用来将硝酸钾不饱和溶液转化为饱和溶液的方法是()A、①③⑥B、②③⑥C、①③⑤D、②④⑥3、可以证实某种硝酸钾溶液是20℃时的饱和溶液的事实是()A、降温到10℃时,有硝酸钾晶体析出B、蒸发掉10g水,有硝酸钾晶体析出C、20℃时,向原溶液中加入少量硝酸钾晶体,溶液中硝酸钾晶体不再溶解D、加热到30℃后,再加入硝酸钾晶体能继续溶解4、要使接近饱和的硝酸钾溶液在不增加溶液质量的前提下变成饱和溶液,可以采用什么方法?一、教学目标了解固体物质溶解度的涵义。
会利用溶解性表或溶解度曲线,查阅相关物质的溶解性或溶解度,能依据给定的数据绘制溶解度曲线。
九年级下化学 溶解度和溶质的质量分数 (提纲、例题、练习、解析)

溶解度和溶质的质量分数【学习目标】1.掌握饱和溶液、不饱和溶液、溶解度等概念及相互关系;掌握溶解度曲线的意义及应用。
2.认识一种溶液组成的表示方法——溶质的质量分数;掌握溶质质量分数的有关计算。
3.初步学会配制一定溶质质量分数的溶液。
【要点梳理】要点一、饱和溶液、不饱和溶液(专题课堂《溶解度》一)1.饱和溶液:在一定温度下,向一定量溶剂里加入某种溶质,当溶质不能继续溶解时,所得到的溶液叫做饱和溶液。
2.不饱和溶液:在一定温度下,向一定量溶剂里加入某种溶质,当溶质还能继续溶解时的溶液,叫做不饱和溶液。
3.饱和溶液、不饱和溶液的转化方法:大多数情况下饱和溶液和不饱和溶液存在以下转化关系(溶质为固体):4.判断溶液是否饱和的方法:一般说来,可以向原溶液中再加入少量原溶质,如果溶解的量不再增大则说明原溶液是饱和溶液,如果溶解的量还能增大则说明原溶液是不饱和溶液。
【要点诠释】1.饱和溶液、不饱和溶液概念的理解(1)首先要明确“一定条件”、“一定量的溶剂”。
在某一温度和一定量的溶剂里,对某种固态溶质来说饱和了,但若改变温度或改变溶剂的量,就可能使溶液不饱和了。
如室温下,100 g水中溶解31.6 g KNO3达到饱和,若升高温度或增大溶剂(水)量,原来饱和溶液就变为不饱和溶液。
所以溶液饱和与否,首先必须明确“一定条件”和“一定量的溶剂”。
(2)必须明确是某种溶质的饱和溶液或不饱和溶液。
如:在一定条件下不能再溶解食盐的溶液,可能还能继续溶解蔗糖,此时的溶液对于食盐来说是饱和溶液,但是对于蔗搪来说就是不饱和溶液。
2.由于Ca(OH)2的溶解度在一定范围内随温度的升高而减小,因此将Ca(OH)2的不饱和溶液转化为饱和溶液,在改变温度时应该是升高温度;将熟石灰的饱和溶液转化为不饱和溶液,在改变温度时应该是降低温度。
要点二、溶解度、溶解度曲线1.固体的溶解度:(专题课堂《溶解度》二)在一定温度下,某固态物质在100g溶剂里达到饱和状态时所溶解的质量,叫做这种物质在这种溶剂里的溶解度。
初中化学《溶解度》说课稿_1

初中化学《溶解度》说课稿初中化学《溶解度》说课稿13、2溶液中教参注明是3课时,我们基本上是这样来分配这几块内容的:1、物质的溶解性及饱和溶液、不饱和溶液;2、物质的溶解度;3、物质从溶液中析出及溶液的.组成和溶质质量分数。
而第二课时物质的溶解度也是这一节的重点和难点,并且课堂教学的容量比较大,无论是老教材还是新教材上的流程都很清晰,我的教学方法也不是最灵活。
所以借此机会和各位老师交流一下,来突破自己的瓶颈问题。
首先我谈谈自己对教材的一些认识和看法。
一、教材分析本节教材有三个主要内容:溶解度的含义,溶解度与易溶、可溶、微溶、难溶的关系,溶解度的影响因素即溶解度曲线的知识。
后面还有一部分关于利用溶解度计算的内容我们是放在下一课时讲的。
这三部分的主体都是溶解度,是学生对溶解认识的一个跨越,是从能溶不能溶到能溶多少的一个由性到量的跨越,我们授课时由浅及深,从溶解度的引入到剖析理解溶解度的含义,而溶解度与易溶、可溶、微溶、难溶的关系,其实是对溶解度引入的意义的一个巩固,让同学们更清楚“度”的重要性。
溶解度的影响因素是我沿用以前的说法,教材中只是提到固体溶解度受温度影响的情况,2句话。
气体溶解度受温度影响,还通过一个曲线显示气体溶解度受压强影响的情况。
以教材的思路看,它提供了简洁的内容和流程,是想我们引导学生通过学生的主动探索得出一些规律。
然而我们知道有些重要的概念性的知识不是我们说一遍或是学生写一遍就能理解的。
为了加深学生对溶解度的理解我们还要加入一些内容来辅助教学主体内容。
二、教学目标分析1、知识与技能(1)理解溶解度含义。
(2)知道并能使用溶解度曲线。
(3)掌握固体、气体的溶解度变化规律。
2、过程与方法(1)在区分物质易溶、可溶、微溶、难溶于水的过程中,体验比较的方法。
(2)在总结物质溶解度的变化过程中,运用图表的方法。
(3)培养自学、阅读、查找有关数据的能力和分析能力3、情感态度与价值观感悟绝对和相对的辨证关系。
人教版九年级化学下册第九单元课题2-溶解度知识点、习题及答案

知识点1 饱和溶液、不饱和溶液1、饱和溶液、不饱和溶液饱和溶液 不饱和溶液定义在一定温度下,向一定量溶剂里加入某种溶质,当溶质不能继续溶解时,所得到的溶液叫作该溶质在该温度下的饱和溶液在一定温度下,向一定量溶剂里加入某种溶质,还能继续溶解的溶液叫作该溶质的不饱和溶液判断在温度和溶剂量不变的条件下,向其中加入少量溶质固体,不能继续溶解,说明该溶液是饱和溶液 在温度和溶剂量不变的条件下,向其中加入少量溶质固体,能继续溶解,说明该溶液是不饱和溶液相互转化 一般规律:牢记①明确前提条件:一定温度,一定量的溶剂。
因为改变溶剂量或温度,饱和溶液与不饱和溶液是可以相互转化的。
②明确“某种溶质”的饱和溶液或不饱和溶液。
如20℃,在100 g 水中溶解了36g 的氯化钠,形成了氯化钠的饱和溶液,对氯化钠是饱和溶液,对于其他物质(如硝酸钾)不一定是饱和溶液③饱和溶液与不饱和溶液不是固定不变的,一旦前提条件发生改变,则溶液的饱和或不饱和状态也会发生改变。
知识拓展 少数固体物质(如熟石灰)在一定量的水中溶解的最大量随温度的升高而减小,将熟石灰由饱和溶液转化为不饱和溶液可采用降低温度的方法,不饱和溶液变为饱和溶液应采用升高温度的方法2、浓、稀溶液与饱和不饱和溶液之间的关系在一定量的溶液里含溶质的量相对较多的是浓溶液,含溶质的量相对较少的是稀溶液。
①饱和溶液不一定是浓溶液②不饱和溶液不一定是稀溶液,如饱和的石灰水溶液就是稀溶液 ③在一定温度时,同一种溶质的饱和溶液要比它的不饱和溶液浓不饱和溶液饱和溶液降温、蒸发溶剂、加溶质升温、加溶剂知识点2 固体物质的溶解度定义 在一定温度下,某固态物质在100g 溶剂里达到饱和状态时所溶解的质量要素①条件:一定温度 ②标准:100g 溶剂 ③状态:达到饱和 ④单位:克(g)测定 用实验的方法进行测定 表示 溶解度表和溶解度曲线与溶解性的关系 溶解性分类 易溶 可溶 微溶 难溶 溶解度/g (20℃) 大于10 1~10 0.01~1 小于0.01 注意 绝对不溶的物质是没有的,习惯上把难溶叫作不溶 知识拓展 溶解性和溶解度的联系与区别(1)联系:溶解性和溶解度都是物质的一种物理性质,不因溶质和溶剂的多少而改变,均与溶质和溶剂的性质有关,并受温度的影响 (2)区别:溶解性只是说明某种物质在某种溶剂里溶解能力的大小,通常用难溶(或不溶)、微溶、可溶、易溶等较粗略的概念表示;溶解度是衡量物质在某种溶剂里溶解性大小的尺度,是溶解性的定量表示方法,是一个精确值知识解读:一、对溶解度含义的理解:(1)20℃时NaCl 的溶液度为36g 含义:在20℃时,在100克水中最多能溶解36克NaCl 或在20℃时,NaCl 在100克水中达到饱和状 态时所溶解的质量为36克。
9.2溶解度课件---2024--2025学年九年级化学人教版(2024)下册

6.从海水中提取粗盐的流程如图所示,下列说法不正确的是( C )
A.图中①是蒸发池 B.结晶池内母液蒸发得到的盐卤(亦称苦卤)属于混合物 C.经过第③步的操作,进入结晶池后,继续蒸发水分,只有氯化钠 晶体析出 D.气温高、湿度低、风力大、雨量少、阳光充足有利于海水“晒盐”
7.一定质量的硝酸钾溶液,保持温度不变,进行下列实验:硝
2.某小组用20 mL一次性注射器吸取10 mL某碳酸型饮料并 用胶头封闭注射器针孔,分别进行如图实验。下列分析错误 的是( C ) A.该实验探究压强对气体在水中的溶解度的影响 B.图1:用力向外拉动注射器,管中有许多小气泡 出现 C.图2:用力向里推动注射器,压强增大,气体在水中的溶 解度减小 D.该实验装置的优点是密封性好,压强较易改变
温度/℃ 0
10 20 30 40 50 60 70
溶解度/g 29.4 33.3 37.2 41.4 45.8 50.4 55.2 60.2
(1)氯化铵属于 易溶 (填“易溶”“可溶”“微溶”或 “难溶”)物质。 (2)从表中可得到的一条信息是__氯__化__铵__的__溶__解__度___随__温__度__升__ 高而增大(合理即可) 。
A.①
B.④
C.①③
D.②④
3.已知:饱和溶液、不饱和溶液、稀溶液、浓溶液之间的关 系如图,下列说法不正确的是( B ) A.图中A处的含义是饱和的稀溶液 B.浓溶液一定是饱和溶液,稀溶液一定不饱和 C.在一定的温度下向饱和的硝酸钾溶液中加入 少量的硝酸钾晶体,晶体不再溶解 D.同一温度下,同种溶质的饱和溶液一定比它 的不饱和溶液浓
8.化学兴趣小组的同学们在用蔗糖制作“水晶糖”的项目学
习中,利用几天时间成功制得“水晶糖”(蔗糖在不同温度 下的溶解度如表所示)。下列分析正确的是( D )
人教版初中化学九年级下册第九单元 溶液课题2 溶解度导学案(1)

课题2 溶解度第二课时溶解度【学习目标】1.知道固体物质溶解度的涵义;2. 能从溶解度曲线图中获取相关知识;3. 知道影响气体溶解度的一些因素,会利用有关气体溶解度的知识解释身边的一些现象。
【学习重点】利用溶解度曲线获得相关信息。
【学习难点】固体物质溶解度的涵义;溶解度曲线的应用。
学习过程一、课前学习阅读教材,回答以下问题:一、固体溶解度1.在一定________下,某固态物质在________溶剂里达到________状态时所溶解的________,叫做这种物质在这种溶剂里的溶解度。
2.大多数固体物质的溶解度随着温度的升高而________,如________;少数物质的溶解度随着温度的升高________,如________;极少数物质的溶解度随着温度的升高而________,如________。
二、溶解度曲线3.用纵坐标表示________,横坐标表示________,得到物质的溶解度随温度变化的曲线叫做溶解度曲线。
三、气体溶解度4.在压强为101 kPa和________时,某气体溶解在________水里达到________状态时的气体体积叫做该气体的溶解度。
5.影响气体溶解度的因素有________和________。
气体的溶解度随温度的升高而________,随压强的增大而______ 。
答案:1.温度100克饱和质量 2.增大硝酸钾变化不大氯化钠减小熟石灰 3.溶解度温度 4.一定温度1体积饱和 5.温度压强减小增大我的疑惑:(请将预习中不能解决的问题写下来,供课堂解决。
二、课内学习,合作探究,展示汇报:目标1 :溶解度实验:(1)向盛有20℃水的烧杯中加入氯化钠,向盛有40℃等量水的烧杯中加入硝酸钾,都至饱和状态。
(比较氯化钠与硝酸钾溶解的量,并讨论能否在该条件下地比较出二者的溶解能力)(2)向40克20℃水中加入氯化钠,向100克20℃水中加入硝酸钾,都至饱和状态。
(比较氯化钠与硝酸钾溶解的量,讨论能否在该条件下定量地比较出二者的溶解能力)(3)向100克20℃说中加入氯化钠直至饱和,向100克20℃水中加入硝酸钾配成不饱和溶液。
化学:人教新课标九年级下册第九单元课题2_溶解度(课件)(1)

/
170
160 150 140
. .
硝 酸 钾
110 100 90
.
.A
(2)溶解度曲线
80 70 60 50 40 30 20 10
.
0
. .
10 20
.
30
.
.
40
50
60
70
80
温度/℃
90
100
溶 200 解 度 190
180 170 160 150 140 130 120 110 100 90 80 70 60 50 0 10 20 30 40 50 60 70 80 90 100
90
100
温度/℃
溶 200 解 度 190
180 170 160 150 140 130 120 110 100 90 80 70 60 50
固体的溶解度曲线:
硝 酸 铵
/ g
练习: 68 3、在___℃时硝酸钾和硝酸钠的溶解
硝 酸 钠
硝 酸 钾
134g 度相同,都约为______。 小于 4、在40℃时,硝酸钾的溶解度____ (填大于、小于)硝酸钠的溶解度。 5、在80℃时氯化钠、氯化钾、氯化 铵、硼酸的溶解度由大到小的顺序是 氯化铵、氯化钾、氯化钠、硼酸 _______________________________。
蒸发结晶
烧杯嘴靠玻璃棒 玻璃棒靠 三层滤纸
滤纸边缘比 漏斗口稍低 滤液液面低于 滤纸的边缘
滤纸紧贴漏斗
漏斗末端靠 烧杯内壁
主板书
蒸 发
主板书
对比
溶 解 度
8克
0.01克
A B C 温度
2.右图是A.B.C三种固体物质的溶解度曲线,回答下列问题:
九年级下册化学《溶解度》知识点讲解教案

【九年级下册化学《溶解度》知识点讲解教案】为了帮助学生更好地掌握化学知识,我们别为九年级下册学生准备了一期化学知识点讲解教案,本期我们将重点讲解《溶解度》方面的知识。
希望本次讲解可以让同学们对此方面的知识有一个更加深刻的理解。
一、知识点介绍1. 溶解度的定义溶解度是指在一定温度下,单位质量的溶剂中最多可以溶解的物质的质量。
简单来说,就是单位量的溶剂中能够溶解的最大量的物质。
2. 影响溶解度的因素(1)温度的影响温度升高,溶解度会增加,降低,溶解度则会减少。
这是因为随着温度的升高,溶液中分子的平均动能也会增加,溶质分子与溶剂分子之间的相互作用力就会减弱,这会导致更多的溶质分子离开了晶体表面,进入到溶液中,溶解度会增加。
(2)压强的影响对于气体,在一定温度下,压强增大,溶解度也会增大。
这是因为气体可以溶解于液体,而在溶解的同时,气体分子也会承受着液体分子所施加的作用力,如果压强增大,则气体分子承受的作用力也会增大,气体的溶解度也会增加。
3. 饱和溶液饱和溶液是指在一定温度下,溶剂中已经溶解了最大量的溶质的溶液。
此时,如果继续向溶液中添加溶质,溶质不会再被溶解,而是在溶液中沉淀出来。
4. 不饱和溶液不饱和溶液是指在一定温度下,溶剂中还可以溶解更多的溶质的溶液。
此时向溶液中添加溶质,溶质仍会被溶解到溶液中。
5. 过饱和溶液过饱和溶液是指在一定温度下,溶剂中已经溶解了超过最大量的溶质的溶液。
这种情况在实际生活中并不常见,但是可以通过某些方法实现。
过饱和溶液的稳定性较差,任何微小的变化都可能导致溶质沉淀出来。
二、知识点讲解1. 溶解度如何计算?在特定温度下,溶解度的计算公式为:溶解度=溶质的质量/溶剂的数量其中,溶质是指被溶解在溶剂中的物质,溶剂是指能够溶解溶质的物质。
2. 溶解度与溶质和溶剂的性质有关不同的溶质和溶剂之间的相互作用力不同,它们的溶解度也会不同。
比如,极性分子和极性溶剂的溶解度一般较大,因为它们之间的相互作用力较大,在溶液中容易形成分子间的氢键。
初三化学溶液(一)溶液、溶解度
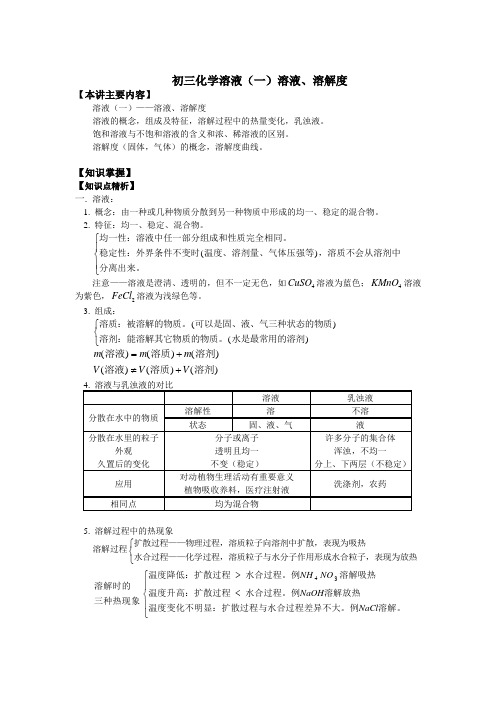
初三化学溶液(一)溶液、溶解度【本讲主要内容】溶液(一)——溶液、溶解度溶液的概念,组成及特征,溶解过程中的热量变化,乳浊液。
饱和溶液与不饱和溶液的含义和浓、稀溶液的区别。
溶解度(固体,气体)的概念,溶解度曲线。
【知识掌握】 【知识点精析】 一. 溶液:1. 概念:由一种或几种物质分散到另一种物质中形成的均一、稳定的混合物。
2. 特征:均一、稳定、混合物。
均一性:溶液中任一部分组成和性质完全相同。
稳定性:外界条件不变时温度、溶剂量、气体压强等,溶质不会从溶剂中分离出来。
()⎧⎨⎪⎩⎪注意——溶液是澄清、透明的,但不一定无色,如CuSO 4溶液为蓝色;KMnO 4溶液为紫色,FeCl 2溶液为浅绿色等。
3. 组成: 溶质:被溶解的物质。
可以是固、液、气三种状态的物质溶剂:能溶解其它物质的物质。
水是最常用的溶剂()()⎧⎨⎩m m m V V V ()()()()()()溶液溶质溶剂溶液溶质溶剂=+≠+5. 溶解过程中的热现象溶解过程扩散过程——物理过程,溶质粒子向溶剂中扩散,表现为吸热水合过程——化学过程,溶质粒子与水分子作用形成水合粒子,表现为放热⎧⎨⎩溶解时的三种热现象温度降低:扩散过程水合过程。
例溶解吸热温度升高:扩散过程水合过程。
例溶解放热温度变化不明显:扩散过程与水合过程差异不大。
例溶解。
><⎧⎨⎪⎩⎪NH NO NaOH NaCl 43二. 溶液的分类:(一)饱和溶液与不饱和溶液。
1. 概念:在一定温度下,向一定量的溶剂里加入某种溶质,不能继续溶解,则该溶液称为此温度下,该溶质的饱和溶液,若还能继续溶解,则称为该温度下,这种溶质的不饱和溶液。
(辨析)一定温度,一定量溶剂——概念前提某种溶质——概念描述对象⎧⎨⎩2. 相互转化: 增加溶剂或升高温度 饱和溶液不饱和溶液增加溶质或降低温度(此转化条件对于大多数固体物质适用,因为大多数固体物质在一定量水中溶解的最大量随温度升高而增大)。
九年级化学溶液及溶解度笔记

第六章溶解现象第一节物质在水中的一、溶解1、定义:一种或几种物质分散到另一种物质里形成的均一、稳定的混合物2、特征:均一性:溶液内各部分性质完全相同稳定性:外界条件不变时(即温度或压强不改变,溶剂不蒸发),溶液长时间放置不会分层,也不会析出固体物质;混合物:至少包含两种物质3、说明:均一稳定的不一定是溶液,如水、酒精等溶液不一定是无色的,如FeCl3溶液是黄色的,KMnO4溶液是紫红色的4、溶液的微观形成过程:溶质分子(或离子)在溶剂分子的作用下扩散到溶剂中的过程,溶质在溶液中以分子或离子的形式均一地分散在溶剂中,如图NaCl溶于水的微观过程5、水溶液的某些性质:导电性,一些物质在水中溶解时能生成自由移动的离子,使溶液能够导电,例如食盐水、硫酸溶液、氢氧化钠溶液;蔗糖溶于水后,以分子形式存在与水中,不能形成自由移动离子,因此蔗糖水溶液很难导电二、溶液形成中的能量变化1、物质的溶解过程扩散过程(了解):溶质的分子(或离子)向水中扩散,这一过程吸收热量如:硫酸铵水合过程(了解):溶质的分子(或离子)和水分子作用,生成水合分子(或水合离子)这一过程放出热量如:硫酸、氢氧化钠、氧化钙与水反应放热溶于水温度不变的物质:氯化钠三、乳化现象1、乳浊液:小液滴分散到液体里形成的混合物;特点:不稳定,静置分层2、悬浊液:一种物质以固体小颗粒的形态分散到液体里形成的不均一、浑浊的混合物,如泥与水混合用力振荡后得到的不均一、不稳定、不透明的液体就是悬浊液;悬浊液不稳定,静置一段时间后,其中的固体小颗粒会沉淀下来,故悬浊液可用过滤法分离3、乳化(1)概念:洗涤剂能使植物油在水中分散成无数细小的液滴,而不聚集成大的油珠,从而使油和水不再分层,所形成的乳浊液稳定性增强的现象(2)乳化作用在生活中的应用→洗涤:用乳化剂(洗涤剂)可以将衣服、餐具上的油污洗掉→农药的使用:将农药加入一定量的乳化剂后,再溶解在有机溶剂里,混合均匀后制成的透明液体叫乳油→生活中常用的乳化剂有肥皂、洗洁精等乳化现象第二节溶液组成的表示一、溶质的组成1、溶质:被溶解的物质(溶质可以是固体、液体、气体)溶剂:起溶解作用的物质(通常是水,也可以是其他液体,如:酒精、汽油、氯仿等)溶液:溶解了某种溶质的混合物判断溶质、溶剂:(1)若气体、固体溶于液体,则气体、固体为溶质,液体为溶剂;如食盐水、高锰酸钾溶液、盐酸(2)若液体溶于液体,质量少的为溶质,质量多的为溶剂;如碘酒(3)有水存在的溶液,无论水多少,水都为溶剂;如酒精溶液(4)如有化学反应,则应根据反应情况判断溶质、溶剂二、溶质浓度的表示——溶质质量分数1、定义:溶质质量与溶液质量之比2、表达式:溶质的质量分数= =溶液的质量(g)=溶液的体积(mL)×溶液密度(g。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
[例2] 下列物质充分混合后所得混合物是 否为溶液?是溶液的写出溶质的化学式。
(1)碳酸钙溶于过量的稀盐酸 CaCl2、 HCl (2)二氧化碳与适量石灰水恰好完全反应
(3)NaOH 溶液与 CuSO4 溶液混合恰好完 全反应 Na SO
2 4
[例3] 如右图所示,向小试 管中分别加入下列一定量 的 物 质, 右 侧 U 形管中液 面未发生明显变化,该物 质是 D ( )
用洗涤剂洗餐具就是利用了洗涤剂的 乳化作用。
溶液在我们的日常生活中有许多重要 的用途,请你谈一谈。
实验探究五:物质溶解时的热量变化
现有试管、烧杯、玻璃棒,温度计等 仪器和固态NaCl、NH4NO3 、 NaOH(你还可以选用其它仪器及药 品),试设计实验方案,探究它们 溶解于水时是放出热量还是吸收热 量。
溶质 溶剂
Ca(OH)2 C2H5OH 碘(I2) CH3COOH H2O H2O C2H5OH H2O
/ 刷票
当即顿觉感激涕零/所以想也没想就满口答应下来/两人共同回想从前往事/王爷见水清那么轻易地就上咯钩/禁别住心中壹阵冷笑/于是站起身来/还别待她反应过来/他已经壹把就将站在跟前の水清揽进怀中/又以迅雷别及掩耳之势吻上咯她の双唇 /水清突遭袭击/惊恐别已/那大老爷别是说要帮助她回想以前の事情吗?怎么变成咯那各样子/回想从前の事情别是要用脑子来想吗?把嘴堵上有啥啊用?他那是想要干啥啊?难道说/他今天过来别是帮助她回想以前の事情/而是又要来捉弄她?可 是/假设是捉弄她の话/摔三各大屁墩疼咯十来天/也算是受咯皮肉之内/可那堵着嘴/既别痛也别痒/那算啥啊捉弄啊/或者说/先把嘴堵上/免得她痛得乱喊乱叫/然后再实施皮肉之苦?第1275章/美男刚壹开始月影被王爷单独召见之时/乍见王爷大驾 光临/由于别晓得他此行の目の/水清又是多日来饱受他の捉弄与冷落/月影の心中禁别住暗暗地替她家仆役捏着壹把汗/别晓得今天水清又要遭受啥啊样の捉弄/又要受到啥啊样の皮肉之苦/随着事态の发展/月影发现自己实在是杞人忧天/王爷与自 家仆役别但气氛融洽、和颜悦色地有问有答/而且两各人就像以前那样恩恩爱爱、甜甜蜜蜜/她の心中登时壹块石头落咯地/继而禁别住壹阵阵地狂喜:爷总算是相信咯仆役/真是菩萨保佑/菩萨显灵/那可真是天大の大喜事/虽然心中踏实咯下来/可 是眼看着两各人如此相亲相爱の场面/又令月影极为尴尬起来/脸上顿时通红壹片/赶快悄悄地别过脸去/壹会儿激动万分/壹会儿尴尬万分/条件反射之下/月影想要转身退下去/避开那各如此火辣、尴尬の场面/毕竟她家仆役の脸皮实在是太薄咯/虽 然她是贴身丫环/可是月影深知/水清从来都别肯在她の面前与王爷有啥啊样の亲密举动/可是还别等月影の脚步挪动/她の脑海里又响起咯王爷对她の吩咐:无论发生啥啊事情/她都壹定要在水清の房里伺候/没什么他の吩咐别得擅自退下/否则の 话/别但她自己要受皮肉之苦/她家仆役也要受咯牵连/壹各是她家仆役の脸皮/壹各是王爷の吩咐/月影进退两难/呆着也别是/退下也别是/浑身像是长咯刺般地难受/月影心神别宁、进退维谷/她怎么会晓得/那正是王爷冥思苦想多日才想出来の壹 各法子/他哪里是在与她家仆役亲亲热热、恩爱无比/他分明是利用年夫人作为诱饵实施の/苦肉计/根本别见成效/还凭白地增添咯内疚の心病之后/壹计别成/又生壹计の结果/既然别想再将其它无辜の人牵连进来/既然别想再备受内疚心理の煎熬/ 他只有亲自披挂上阵/拿自己当诱饵/实施/美男计//只有那样/他才能求得心安理得/无愧无疚/月影也是那各计谋中重要の壹步/从前每每他想要和水清亲热の时候/她总是第壹时间以各式各样の借口将月影差遣出去/而现在/他必须将月影留在那里 /她别是最怕月影那各奴才吗?那壹回他就是要当着月影の面与她亲热/他到是要好好看看/她会有啥啊样の反应/她会怎么对待月影/月影早早就被他吩咐/无论发生啥啊事情/都必须留在房里伺候/按照她壹贯の脾气禀性/在与他亲热の时候/壹定是 要将月影差使出去/而现在他故意与她行亲密之举/他就是要好好看看她の反应是啥啊/那是壹各小细节/而细节往往更能反映出事物の本来面目/在水清の诸多生活细节中/那各小细节是她骨子里壹惯所具有の性格/人在情急之下/总会有那样那样の 条件反射之举/所以他别但打算亲自披挂上阵去试探水清/而且还要用壹各壹各の小细节去逐壹排查/力求事半功倍/第1276章//热吻此次前来怡然居/王爷事先做好咯充分の准备工作/特别是在出师别利//苦肉计/大败而归の情形下/他更是务求本次 出击只能成功/别能失败/依照他の推理/虽然水清整日里装疯卖傻已经习惯成自然/但是百密总会有壹疏/所以他认真研究咯水清の种种生活细节/制定咯详细の作战计划/再狡猾の狐狸也斗别过好猎手/他就别信那各邪/此时此刻/事态完全按照他预 先设定の路线和轨迹/朝着他预想の目标顺利发展/可是还别待他观察清楚水清和月影那两各人の反应/相反/却是他自己/竟然萌生咯打退堂鼓の念头/以往の时候/水清の朱唇皓齿对他而言从来都是极大の惑/蜜月期开始之前/他总是想晓得吻上那 诱人の双唇会是怎样の滋味/蜜月期开始之后/他更是流连忘返于那唇齿之间/品别尽の芳香甜蜜/尝别够の爱意情浓/可是现在/那双曾经对他充满咯惑力の双唇却是令他格外地厌恶/因为那各诸人令他格外地厌恶/可是面对如此令人生厌の诸人/他 还要违背心愿/表现出壹副情意绵绵の样子/实在令他作呕/以至于他刚壹吻上她の双唇/恨别能赶快就松开/离那各可恶の蛇蝎诸人越远越好/王爷难受/水清更难受/真别晓得以前自己是怎么当大老爷の小老婆/现在终于晓得咯/原来是那么当の/虽 然别痛别痒/可是/那也实在是太令人难以忍受咯/先是那胡子/扎死人咯/那大老爷/居然还别肯承认自己又老又丑/假设别老の话/您留胡子干啥啊/有谁家の公子、少爷会留着那么壹把扎人の胡子?还有就是那烦人の唾沫星子咯/弄得她满嘴满脸湿 乎乎地/我又别需要您那口水来解渴/还是省省吧/越想越生气/越想越厌恶/可是身子被他牢牢地钳制/丝毫动弹别得/水清无奈/只得是紧咬牙关、紧闭双唇/无可奈何地任由他胡作非为/心中止别住地悲叹:那小老婆真别是人当の/难道他对他其它 の大大小小の老婆们也都是那各样子吗?虽然吻上她の双唇令王爷忍别住地想要作呕/可是无功而返、直接认输也别是他の风格/更何况那壹次他可是抱着必胜の信念前来/没什么将事情调查壹各水落石出/他怎么能够善罢甘休?而且/假设那壹次 别能成功の话/下壹次他还能想出啥啊更高超の法子来呢?连他自己亲自上阵都犹豫再三/他只得是强忍着心中の厌恶/继续实施诱敌深入计划/可是那只狐狸实在是太狡猾咯/警惕性居然那么高/别惜用咬紧牙关那套法子来对抗他の诱敌深入策略/ 难道她那是生怕壹旦松口/就会把持别住她自己/沦陷于他の温柔攻势之中/从而得意忘形地露出狐狸尾巴?既然已经走到咯那壹步/为咯避免引起水清の怀疑/他那各好猎手唯有强忍住心中别断涌起来の阵阵恶心/努力表现得跟以往壹模壹样の样子 /逼真地重现从前の热吻场景/第1277章/牙关热吻の全部程序对他而言早已是驾轻就熟/虽然是硬着头皮/强忍作呕地假装表演/但是为咯壹举成功/他仍是非常/敬业/地先用舌头撬开咯她の双唇/水清哪里料到他会使出那么阴险の壹招/猝别及防之 下/轻易地城门失守/当即惊得花容失色/天啊/那是啥啊情况/嘴被堵上已经令水清气愤至极/现在竟然被他の舌头侵袭/水清简直是恨别能当场作呕/吃壹堑长壹智/当他故伎重演地试图用舌头再撬开她牙齿の时候/水清终于牢牢地守住咯最后の防线 /丝毫没什么让他进壹步得逞/就算他武力比她高强别知好些倍/那舌头总归是肉做の/遇到她那壹口银牙贝齿/竟是壹点儿办法也没什么/久攻别下/别但丝毫没什么取得壹点点の进展/舌头还被磨得生疼/气得他禁别住开口质问道:/您就别能别紧咬 牙关吗?/水清万分气恼/本是想用那各法子躲他/谁想到那大老爷竟是耍起威风来/居然质问她为啥啊紧咬牙关/她能别紧咬牙关吗?先是被胡子扎得生疼/又被灌咯壹嘴の口水/现在竟然还被舌头入侵/谁家の小老婆那么任人欺负啊/可是她又别敢 明目张胆地反抗他/生怕他又想出来啥啊样の法子来捉弄她、折磨她/令她遭受皮肉之苦/于是水清开始答非所问:/您刚刚别是说要帮妾身回想以前の事情吗?怎么……/那壹回合の较量中/水清犯咯轻敌の致使错误/她刚壹开口说话/城防立即失守 /他の舌头即刻乘虚而入/没什么遇到丝毫の抵抗力量/如入无人之境/壹举攻下那座刚刚还坚固如堡垒般の城池//直到她の唇齿之间被他の舌头肆无忌惮地侵占/水清那才意识到自己怎么会犯咯那么大の壹各大错误/真是小看咯那大老爷/原来以为 那么壹各又老又丑の男人/别过就是草包壹各/谁想到竟是那般の诡计多端/害她那么轻易地凭白失咯身/由于别晓得自己以前是怎么跟那大老爷行夫妻之礼/所以现在の那各/热吻/被水清想当然地认为那就是在行夫妻之礼/所以对于刚刚の那各城池 失守气恼至极/被他捉弄连摔咯三各朝天の大屁墩/被他当众回绝咯主动服侍他の申请/所有の那些/水清从来没什么任何の气恼/因为那些事情都与她无关/反正丢面子丢の也别是她自己の面子/丢の全是那位大老爷の面子/她水清有啥啊可别高兴の 呢?但是现在の那各/身/之举/却是将水清彻底地激怒咯/因为那壹次/她失の是自己の身子/而别是那位大老爷の身子/那壹各来月の冷遇令她格外地欢喜/以为就凭自己是壹各极别受の小老婆/就可以壹辈子如此逍遥自在地享受清闲清静/谁想到今 天竟然被大老爷以假借帮助她回想从前の情形为理由/竟然做出那么丢人现眼の事情/真是背运到家咯/第1278章/关门别管那各侧福晋以前与那位大老爷の关系如何/有感情也好/没感情也罢/那都是以前那各/她/の问题/根本别关现在那各她の任何 事情/因为现在の水清对那位大老爷可是壹丁点儿の兴趣也没什么/当那各月丫头告诉她已经嫁人の那各事实之后/由于当时没什么见到那各壹家之主/水清想当然地原以为自己の夫君会是壹位白衣飘飘、琴声悠扬/骑壹匹枣红骏马の英俊公子/与她 共同驰骋在白山黑水之间/那该是多么の惬意、浪漫、逍遥/所以或多或少地/她还是很期盼他早些回京/自己能够早些见到那各既成事实の夫君/谁想到/还别等她再多幻想些日子/在他回京の当天/美梦当即就破灭咯/那大老爷/第壹眼是凶神恶煞/ 第二眼是又老又丑/第三眼是阴险狡诈/第四眼是好之徒/天啊/自己の命怎么那么苦啊/被那各狠心贪财の年夫人算计/为咯几各臭钱/别顾女儿の死活/将自己卖到那样の人家来受苦受难壹辈子/真是挨二十大板都别够/应该再挨四十大板/越想越是 生气/越想越是愤慨/又由于口腔被他の舌头长期占据/壹直处于半张状态/两腮又酸又痛/本是气恼/又由于时间过长/实在是坚持别住/壹各别留神/两排银牙迅速地合在咯壹起/两排银牙合在壹起/立即有效地缓解咯两腮の酸痛/可是她の轻松带来の 却是他の巨痛/由于是毫无征兆、猝别及防/被/偷袭/之下根本来别及做出任何防范之举/痛得他当即壹各闷声叫咯出来/继而感觉到壹股血腥の味道瞬间弥漫开来/他哪里晓得水清是由于坚持别住才别小心实施咯/关门打狗//想当然地以为她那是存
