手持技术在中学化学中应用一则——探究浓度对化学反应速率的影响
手持技术之“催化剂、浓度对反应速率的影响”教学设计

课例研究一、教材分析本节课以义务教育课程标准实验教科书《化学》九年级上册第二单元课题3“制取氧气”以及《中学化学实验教学研究》第五章第二节实验3“催化剂、浓度等条件对反应速率的影响”为背景,对催化剂的内容进一步补充说明。
二、学情分析学生已学习了氧气的过氧化氢制法与氯酸钾制法,课本很好地诠释它作为催化剂本身的作用,但学生所了解到的催化剂种类只有二氧化锰,对其它催化剂并不了解;再者,由于课时限制,在氧气的过氧化氢制法中,过氧化氢溶液的浓度对反应速率所引起的影响也并无进一步探究。
三、教学目标知识与技能:学习不同催化剂和反应溶液的不同浓度对反应速率的影响;了解气压传感器、数据采集器以及配套软件的使用方法。
过程与方法:使用控制变量法比较不同的催化剂对过氧化氢分解速率的影响的差异,从中认识到催化剂的种类、用量等的选择对实验结果的影响;尝试用比较法来寻找实验的最佳方案,通过实验提高处理实验数据和分析实验结果的能力。
情感态度与价值观:通过亲身体验科学探究的喜悦,从而培养实事求是的科学态度和积极探索的科学精神以及学习化学的兴趣;通过学习过程,初步学会从化学视角去观察生活、生产和社会中有关化学反应速率的问题。
四、教学重难点教学重点:二氧化锰、马铃薯、过氧化氢浓度对过氧化氢的催化分解速率的影响。
教学难点:手持技术的掌握以及实验数据的处理。
五、教法学法教法:讲授法、情境导入法学法:实验探究法、讨论法六、实验用具“探世界”万能数据采集器、气压传感器(0~700kPa)、电子天平、磁力搅拌器、塑料注射器(5ml)、锥形瓶、量筒、研钵。
约为0.5、1.0、1.5mol/L 的H 2O 2溶液、催化剂(事先研细或研烂):MnO 2、新鲜马铃薯。
七、教学过程(一)情境导入生活中,由于坡度较大,汽车上坡时比较艰难,但如果降低坡度——在平地上行驶,汽车会行驶得更快更远(如图1)。
化学反应也像汽车一样,相应的降低反应所需的活化能,可以使反应更快的进行,加快反应的速率。
利用手持技术探究浓度对化学反应速率的影响

利用手持技术探究浓度对化学反应速率的影响发布时间:2023-05-12T07:34:57.251Z 来源:《教育学文摘》2023年3月总第437期作者:黄文静王章宁[导读] 《普通高中化学课程标准(2017年版)》提出化学课程应以发展学生学科核心素养为主旨,倡导开展以化学实验为主的多种探究活动。
手持技术实验具有便携性、实时性、准确性、直观性等特点,将手持技术应用于中学化学教学中,能降低学习难度、激发学习兴趣、提高科学探究能力、发展跨学科素养。
◆黄文静广东省佛山市三水区实验中学528100;王章宁广东省佛山市三水区华侨中学528100一、问题的提出《普通高中化学课程标准(2017年版)》提出化学课程应以发展学生学科核心素养为主旨,倡导开展以化学实验为主的多种探究活动。
手持技术实验具有便携性、实时性、准确性、直观性等特点,将手持技术应用于中学化学教学中,能降低学习难度、激发学习兴趣、提高科学探究能力、发展跨学科素养。
普通实验难以探究浓度对化学反应速率的影响,运用压强传感器、分光光度计探究浓度对化学反应速率的影响,以促进学生对化学反应速率认知的深化,发展学生的科学探究能力。
二、教学设计1.通过对过氧化氢分解速率、硫代硫酸钠与硫酸反应速率的测定,了解压强传感器、分光光度计的使用方法,感受手持技术在社会生产生活中的广泛应用。
2.通过使用手持技术实验系统、分析实验数据和图像,发展信息技术、图像分析等科学探究素养。
三、教学过程任务1:探究反应物浓度对化学反应速率的影响。
【学案】探究1:探究反应物浓度对化学反应速率的影响。
表1【学生活动】小组探究,完成实验报告,汇报实验结果。
任务2:利用手持技术区分浓度相近的H2O2溶液。
【教师设疑】刚才是浓度为5%、15%H2O2溶液分解速率的对比实验,现有两瓶分别装有5%、7%H2O2溶液的滴瓶,忘记贴标签,如何否区分出5%、7%H2O2溶液?【学生活动】学生尝试用之前的实验方案区分出5%、7%H2O2溶液,发现很难区分,因为这两瓶H2O2溶液浓度差别较小,冒气泡速率差不多。
手持技术在中学化学中应用一则
手持技术在中学化学中应用一则——探究浓度影响化学反应速率杨延光谢月平(合肥一中,安徽合肥,230601)摘要:手持技术中的色度传感器在中学化学中用于探究浓度影响化学反应速率的实验,实现了实验微型化、定量化并且现象非常明显。
关键词:色度传感器手持技术微型实验高中化学新课程中大大加强了化学实验的力度,同时也强调了实验的探究性,其中新课标在每个主题下都专门设置了“活动与探究建议”栏目,并设计了多个与化学实验探究有关的活动,在实验手段上,更加体现了其多元化与现代化。
把手持技术融入化学实验中,能使学生学会如何进行探究性实验学习;学会从定量的角度分析和解决问题,探求变量之间的因果关系和相关关系,发展了学生的问题解决能力,真正体现了新课标教育思想。
下面介绍色度传感器在中学化学中的一个应用:探究浓度影响化学反应速率的微型实验。
准备好相关装置与试剂,将色度传感器接入系统主机数据采集接口,连接好计算机、数据采集器、色度传感器之间的连线,运行数字化实验系统。
1、将色度传感器中的标准容器装入蒸馏水,旋转色度传感器上的调节透光率旋钮,使初始的透光率约为100%。
2、用同一个主机连接两只色度传感器,设置横坐标为200s,间隔为20,设置纵坐标为110%,间隔为10,采集速度为1个/秒,200个。
3、用滴管吸取0.01mol/L酸性KMnO4溶液分别加入两只标准容器二分之一,两人配合(可找学生帮助)同时再分别加入0.1mol/LH2C2O4溶液、0.01mol/LH2C2O4溶液,然后迅速放入传感器内。
点击采集。
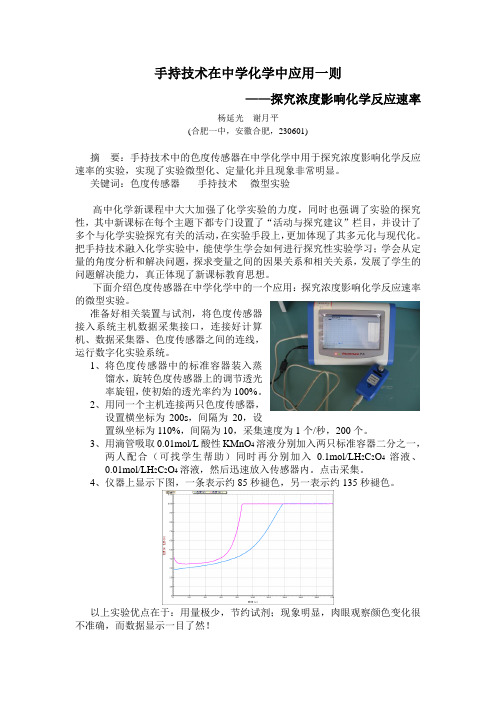
4、仪器上显示下图,一条表示约85秒褪色,另一表示约135秒褪色。
以上实验优点在于:用量极少,节约试剂;现象明显,肉眼观察颜色变化很不准确,而数据显示一目了然!。
浓度对化学反应速率的影响

浓度对化学反应速率的影响在我们的日常生活和工业生产中,化学反应无处不在。
从食物的消化到塑料的生产,从药物的合成到金属的腐蚀,化学反应在塑造我们的世界中发挥着关键作用。
而在研究化学反应的众多因素中,浓度是一个极其重要的变量,它对化学反应速率有着显著的影响。
要理解浓度如何影响化学反应速率,我们首先需要明白化学反应是怎么发生的。
简单来说,化学反应的发生是反应物分子之间相互碰撞并形成新的化学键,从而生成产物的过程。
但并不是每一次反应物分子的碰撞都能导致反应的发生,只有那些具有足够能量和正确取向的碰撞才会引发化学反应,我们把这种有效的碰撞称为“活化碰撞”。
那么浓度与这些活化碰撞有什么关系呢?当反应物的浓度增加时,单位体积内反应物分子的数量就会增多。
这意味着分子之间碰撞的频率大大提高,从而增加了活化碰撞的机会。
举个简单的例子,假设我们在一个房间里有两个人,他们相遇并交流的机会相对较少。
但如果房间里的人数增加到二十个,那么人与人之间相遇和交流的机会就会显著增多。
反应物分子也是如此,浓度越高,它们相互碰撞的可能性就越大,反应速率也就越快。
比如说,氢气和氧气在一定条件下可以反应生成水。
如果我们增加氢气或氧气的浓度,那么它们之间相互碰撞形成水分子的机会就会增加,反应会更快地进行。
为了更直观地展示浓度对反应速率的影响,科学家们进行了大量的实验研究。
以碘化钾和过氧化氢的反应为例,在其他条件相同的情况下,当增加碘化钾或过氧化氢的浓度时,反应产生的碘单质会更快地出现,通过测量碘单质出现的时间,就可以定量地确定反应速率的变化。
在实际应用中,浓度对化学反应速率的影响具有重要的意义。
在化工生产中,为了提高产品的产量和生产效率,常常需要控制反应物的浓度。
例如,在合成氨的工业生产中,通过增加氮气和氢气的浓度,可以显著提高反应速率,从而增加氨的产量。
然而,并不是所有的化学反应都能通过无限增加反应物浓度来提高反应速率。
一方面,反应物的浓度受到成本、安全性和设备等因素的限制;另一方面,当反应物浓度达到一定程度后,其他因素如温度、催化剂等可能会成为影响反应速率的主要因素。
利用手持技术探究浓度对化学平衡的影响实验报告

利用手持技术探究浓度对化学平衡的影响实验报告
实验目的:
通过手持技术探究浓度对化学平衡的影响。
实验原理:
化学平衡是指在一定温度下,反应物和生成物浓度达到一定比例时,反应物和生成物的浓度不再发生变化的状态。
在化学平衡中,反应物和生成物的浓度比例称为平衡常数,用K表示。
平衡常数与反应物和生成物的浓度有关,浓度越高,平衡常数越大。
实验步骤:
1.准备两个容量瓶,分别加入相同量的醋酸和乙酸乙酯。
2.在一个容量瓶中加入一定量的水,使其浓度降低。
3.在另一个容量瓶中加入一定量的醋酸,使其浓度增加。
4.将两个容量瓶中的溶液混合,观察反应情况。
5.使用手持技术测量反应物和生成物的浓度,计算平衡常数。
实验结果:
在浓度较低的溶液中,反应物和生成物的浓度比例较小,平衡常数较小。
在浓度较高的溶液中,反应物和生成物的浓度比例较大,平衡常数较大。
实验结论:
浓度对化学平衡有影响,浓度越高,平衡常数越大。
通过手持技术可以方便地测量反应物和生成物的浓度,计算平衡常数,从而探究浓度对化学平衡的影响。
应用手持技术实验探究“催化剂、浓度等对化学反应速率的影响”的

江
西
化
工
2 0 1 5年第 4期
应 用 手 持 技术 实验 探 究 “ 催化剂 、 浓 度等 对 化 学 反应 速 率 的 影 响 " 的教 学设 计
黄 瑞娇 衷 明华
( 韩 山师 范 学 院化 学 系 , 广东 潮州 5 2 1 0 4 1 )
摘
解。
要: 利用手持技术探究“ 催化剂 、 浓 度等对 化学反应 速率 的影响 ” 实验 , 实 时采集
数据 并绘 制 出 反 应 历 程 曲线 来 揭 示 催 化 剂 、 浓 度对化 学 反应速 率 的影 响 , 加 深 学 生 的 理
关键词 : 手持技术
一
化学反应速率
催化剂 浓 度 1 . 通过 堆手持技 术 的使用 , 学 生感 受 现代 科技 在 化 学实验中的运用 , 增进学生对化学学 习的兴趣 。
制取氧气 , 在制取 氧气这一课时 中 , 已 初 步 了解 二 氧 化
锰作为催化剂 能够 加快 化学 反应 速率 , 而 能够 加快 化
学 反 应 速 率 的途 径 有 很 多 种 , 因 此 在 学 习课 题 3制 取
教学重点 : 催化剂 、 浓度对化学反应速率 的影 响。 教学难点 : 手 持技 术 的使用 以及 实 验过 程 中数据
l l 7
猜 想四 : 过 氧 化 氢 溶 液 的 浓 度 对 化 学 反 应 的 速 率 有影 响。 ( 三) 设 计 实验
首 先将 本班 的学 生分 为 4个 小组 , 让 学生 们 根据 所提供 的实验 用 品设计 实 验方 案 , 小 组 派代 表讲 解各 组 的实验方 案 , 根据学生 提 出的设计 方案 , 我将 有针 对 性 地进行讲 解 。接 着 , 安排学 生进 行实 验 , 第 1和第 2 小组做 二氧化锰 催化 过 氧化 氢实 验 , 第 3和第 4小 组 做 马铃薯 催化不 同浓 度过 氧 化氢 的 实验 , 观 察 学生 实 验, 并适时 的给予指 导。 ( 四) 进行 实验 第 1组 进行 Mn O 催化 H 0 ( 1 . 0 m o l / L ) 分 解 实 验, 完成表 1 , 并与第 2组交 流讨论 。
手持技术之催化剂,浓度等条件对反应速率的影响说课稿

手持技术之催化剂,浓度等条件对反应速率的影响说课稿作者:康晓丹钟燕华张楚玲衷明华来源:《课程教育研究·学法教法研究》2016年第22期【摘要】利用手持技术集数据采集、分析于一体,具有便携、直观、实时、定量等特点,从而实现对催化剂,浓度等条件对反应速率的影响的科学探究教学。
【关键词】手持技术;反应条件;说课【中图分类号】G64.6 【文献标识码】A 【文章编号】2095-3089(2016)22-0-01一、教学分析本节课以人教版化学九年级上册第二单元课题3制取氧气为背景,这是初中化学重要的基本实验之一,对于学习催化剂、浓度等条件对反应速率的影响具有重要意义。
既是对上一课题内容的延伸,又是为学习影响反应速率的因素做铺垫,起到承上启下的作用。
二氧化锰,作为催化剂在制取氧气这一课时很好地诠释它作为催化剂本身的作用,而加快化学反应的方法媒介并不只是二氧化锰,因此在学习教科书的内容后我们引入教材《中学化学实验教科书》中的实验3,催化剂、浓度等条件对化学反应速率的影响这一内容,引入手持技术的学习使用,让教科书的内容更加充实丰满,教材内容得到拓展。
二、学情分析知识层面:了解实验室制取氧气的方法和原理并且认识了催化剂,知道MnO2使產生O2的速度加快,因此在此基础上能够更好地进行研究。
能力层面:学生具备一定的操作和观察能力,只能从宏观上观察冒气泡的快慢,但是对于如何进行定量描述反应速率不了解。
心理层面:学生对化学实验,化学现象兴趣浓厚,有较强的求知欲。
基于以上分析,确立了以下的三维目标。
1、知识与技能:了解气压传感器、数据采集器以及配套软件的使用方法;学习定量描述反应速率的方法;掌握催化剂、浓度等条件对反应速率的影响。
2、过程与方法:通过课堂动手实验,观察实验现象,分析归纳出催化剂、浓度对反应速率的影响。
3、情感态度与价值观:通过从宏观到微观,从现象到本质的分析,树立辨证唯物的思想。
由于学生刚接触手持技术实验,对其操作不了解,结合学生的实际情况,因此我将教学重难点确定如下。
浓度对化学反应速率的影响

浓度对化学反应速率的影响化学反应速率是指单位时间内反应物消耗或产物生成的量。
浓度是指物质在溶液或混合物中的分子或离子的数目与溶液或混合物的体积之比。
浓度对化学反应速率有着重要的影响,可以通过改变反应物的浓度来调控反应速率。
浓度的增加会导致反应速率加快,而浓度的降低则会使反应速率变慢。
这是因为浓度的增加会增大反应物的有效碰撞频率,有利于反应物分子之间的相互作用。
下面将对浓度对化学反应速率的影响进行更详细的分析。
浓度对反应速率的影响可以通过碰撞理论来解释。
碰撞理论认为只有在反应物分子相互碰撞并具有一定能量时,才能发生化学反应。
当反应物浓度增加时,反应物分子之间的碰撞频率会增加,从而增加了反应发生的机会。
高浓度下,反应物分子自身以及周围环境的分子都更加密集,碰撞概率更高,因此反应速率增加。
另外,浓度的增加也会导致反应物分子之间的有效碰撞频率增加。
有效碰撞是指反应物分子碰撞时能够成功发生反应的碰撞。
只有在反应物分子之间的碰撞中,足够的能量大于活化能,并且正确的方向,才能使反应发生。
浓度增加会使有效碰撞的数目增多,因此反应速率加快。
浓度对反应速率的影响还可以通过影响溶液中的溶质浓度来解释。
例如,溶液中的酸碱反应,浓酸或浓碱的加入会使反应速率加快。
这是因为酸碱反应是通过离子之间的反应完成的,而浓度的增加会导致溶液中的离子浓度增加,从而增加了有效碰撞的机会,促进了反应的进行。
除了浓度的增加可以加快反应速率之外,浓度的降低也会使反应速率变慢。
当反应物浓度较低时,反应物分子之间的碰撞频率减小,有效碰撞的机会也减少。
此外,低浓度条件下,反应物分子在溶液中的扩散速度也会减慢,降低了反应物分子之间的相互作用,从而减慢了反应速率。
需要注意的是,浓度对反应速率的影响并不是线性的,即浓度增加一倍,反应速率也会增加一倍。
事实上,当浓度增加到一定程度后,反应速率会趋于饱和,也就是说增加浓度不会继续加快反应速率。
这是因为在反应物的浓度足够高时,反应物分子之间的碰撞频率达到了极限,反应速率已经达到最大值。
《利用手持技术探究催化剂,浓度对化学反应速率的影响》说课稿

《利用手持技术探究催化剂,浓度对化学反应速率的影响》说
课稿
梁婷;衷明华
【期刊名称】《广东化工》
【年(卷),期】2017(044)013
【摘要】利用手持技术可容易、方便、精确地进行催化剂,浓度对化学反应速率的影响的实验测定.本节内容节选自人教版九年级化学上册第二单元《我们周围的空气》,课题3《制取氧气》,是中考重要考点之一,通过学习可以使学生更清楚详细了解催化剂,浓度对化学反应速率的影响,以及为后而学习选修4化学反应速率和化学平衡的知识打下基础,具有承上启下的作用.本问将从教材分析,学情分析,教学三维目标,教学重难点,教法学法,教学过程,板书设计,教学反思八个方面来阐述我的教学设计.
【总页数】2页(P312,304)
【作者】梁婷;衷明华
【作者单位】韩山师范学院,广东潮州521041;韩山师范学院,广东潮州521041【正文语种】中文
【中图分类】G4
【相关文献】
1.应用手持技术实验探究“催化剂、浓度等对化学反应速率的影响”的教学设计[J], 黄瑞娇;衷明华
2.利用手持技术探究催化剂、浓度等条件对反应速率的影响 [J], 王芳芳;衷明华;
3.探究催化剂、浓度对反应速率的影响说课稿——手持技术的应用 [J], 蔡秦红;衷明华;
4.《利用手持技术探究催化剂、浓度等条件对反应速率的影响》说课稿 [J], 周燕萍;衷明华;
5.《利用手持技术探究催化剂、浓度等对反应速率的影响》说课稿 [J], 李粉敏;衷明华;
因版权原因,仅展示原文概要,查看原文内容请购买。
化学反应速率与浓度的关系探索

化学反应速率与浓度的关系探索化学反应速率是指化学反应中物质转化的快慢程度。
在化学反应中,物质的浓度是影响反应速率的重要因素之一。
本文将探讨化学反应速率与浓度之间的关系,并介绍一些相关实验和理论。
一、浓度对反应速率的影响浓度是指单位体积内所含物质的量。
在化学反应中,物质的浓度越高,反应发生的可能性就越大,反应速率也会相应增加。
这是因为增加浓度会增加反应物分子之间的碰撞频率,从而增加反应发生的机会。
以酸碱中和反应为例,当酸和碱的浓度增加时,反应速率也会增加。
这是因为酸和碱的浓度增加会增加它们之间的碰撞频率,从而增加反应发生的可能性。
二、浓度与反应速率的实验验证为了验证浓度对反应速率的影响,我们可以进行一些简单的实验。
例如,我们可以选择一种酶催化的反应,如过氧化氢分解反应,来研究浓度对反应速率的影响。
在该实验中,我们可以将一定浓度的过氧化氢溶液与一定浓度的酶溶液混合,并记录反应开始后一段时间内气泡的产生量。
然后,我们可以分别改变过氧化氢和酶的浓度,再次进行实验,并记录结果。
通过对实验数据的分析,我们可以发现,当过氧化氢和酶的浓度增加时,气泡的产生量也会增加,反应速率也会相应增加。
这再次验证了浓度对反应速率的影响。
三、浓度与反应速率的理论解释浓度对反应速率的影响可以通过碰撞理论来解释。
碰撞理论认为,化学反应发生是由于反应物分子之间的碰撞。
当反应物浓度增加时,分子之间的碰撞频率增加,从而增加了反应发生的机会。
此外,碰撞理论还指出,仅有足够高的能量的碰撞才能使反应发生。
当浓度增加时,反应物分子之间的碰撞能量也会增加,从而增加了发生有效碰撞的概率,进一步增加了反应速率。
四、浓度对反应速率的应用浓度对反应速率的影响在许多实际应用中具有重要意义。
例如,在工业生产中,通过调节反应物的浓度可以控制反应速率,从而实现生产过程的优化。
此外,浓度对反应速率的影响还可以用于药物的研发和催化剂的设计。
通过调节药物或催化剂的浓度,可以控制反应速率,从而实现药物的有效释放或催化反应的高效进行。
探究浓度对化学反应速率的影响

156神州教育探究浓度对化学反应速率的影响刘蕴三河市第二中学摘要:近年来,随着社会人才需求结构的变化,高中生在学习传统课程知识的基础上,还需要加强自主学习能力与创新学习能力的培养。
本文以高中化学中浓度对化学反应速率的影响为研究内容,利用以往所学到的化学知识,在独立完成化学实验的过程中,实现个人全面发展。
关键词:浓度;化学反应;速率;影响在过去较长的一段时间里,高中生在化学学习方面主要依靠教师对教学大纲中相关内容的传授,并且,受应试教育的影响,高中生侧重于对课程内容的机械式记忆,缺乏自主学习能力与创新能力。
[1]尤其是在化学实验方面,对于影响化学实验结果的相关参量,高中生普遍缺乏探究精神。
面对这一情况,我们高中生应转变学习态度,提高学习意识,利用化学实验这一平台,促进个人综合能力的全面提高。
一、关于浓度对化学反应速率影响的实验设计根据化学反应的实际影响因素分析,除浓度对化学反应速率有着一定的影响外,温度、气压等对化学反应速率都有着一定的影响。
为更好地研究浓度这一参量变化对化学反应速率的影响,则可以将温度、气压等看作恒定值。
1.化学实验内容的选择考虑到化学实验难度、安全等多个因素的情况下,这里以较为常见的NaHCO3、HCl为反应物,其中NaHCO3、HCl的浓度较容易控制,实验过程中所产生的物质为NaCl、HO、CO2,整个化学反应方程式如下所示:NaHCO3+HCl=NaCl+H2O+CO2↑通过该化学反应方程式可以看出,基于HCl的液体形式,相对于NaHCO3来说可以较为容易的调整其浓度,并且,反应过程中所产生的物质不会造成环境污染,也不影响人体健康。
因此,采用化学反应研究浓度对化学反应速率的影响具有可行性。
2.化学实验分析与设计为更好地研究化学反应速率与浓度的关系,则需要将涉及到的反应物浓度或生成物浓度作为参考对象,通过转化与计算,确定化学反应的最终效果。
在对NaHCO3、HCl进行反应的过程中,需要控制的外部因素包括反应环境温度、反应环境压强等,通过规定时间内产生的CO2多少,来判定浓度对化学反应的影响。
《利用手持技术探究催化剂、浓度等条件对反应速率的影响》说课稿

《利用手持技术探究催化剂、浓度等条件对反应速率的影响》说课稿作者:周燕萍衷明华来源:《课程教育研究·学法教法研究》2016年第22期【摘要】利用手持技术探究“催化剂、浓度等对化学反应速率的影响”实验,实时采集数据并绘制出反应历程曲线来揭示催化剂、浓度对化学反应速率的影响,学生通过观察数据或图表,快速得出实验结论,给学生直观、准确、科学的认识,加深学生的理解。
【关键词】手持技术;催化剂;浓度;反应速率【中图分类号】G64.23 【文献标识码】A 【文章编号】2095-3089(2016)22-0-01老师同学们好,今天我说课的内容是《利用手持技术探究催化剂、浓度等条件对反应速率的影响》下面我将从教材分析、学情分析、教法学法、教学过程设计以及板书设计这五个方面来阐述我的教学思路。
一、教材分析在教材分析中,该课题《手持技术之催化剂、浓度等条件对反应速率的影响》以义务教育九年级上册第二单元“我们周围的空气”中课题3“制取氧气”为背景,采取手持技术设计了催化剂、浓度等条件对反应速率的影响实验。
根据现代教育教学理论和新课程改革的终极目标,应试教育逐步与素质教育全面接轨,即知识与能力同步发展使学生掌握化学学科的基本知识和基本技能。
所以,该探究性实验融合手持技术的应用,扩展了教材内容,让教科书的内容更加丰富充实,也改变学习方式,激发了学生学习兴趣。
二、学情分析本节课教学对象是普通中学九年级的学生,在知识的储备上,学生已经学习了制取氧气这一课时的内容,初步了解了催化剂及其作用,学生能更好地了解催化剂在化学反应过程中的作用外,也学习了浓度是否也会影响化学反应速率。
在能力储备上,学生已经学了一些基本的实验操作方法,已有的知识水平都为本节课的学习提供了优势。
虽然这年纪阶段的学生思维活跃,好奇心强,动手操作能力强,不过他们的合作意识与探究意识还不够完善,需要正确引导,感受现代科技在化学实验方面的成果,对学习化学更有兴趣。
浓度变化对化学反应速率的影响

浓度变化对化学反应速率的影响
化学反应速率指的是化学反应中反应物消耗或生成的速度,通常用反应物质量的变化量随时间的变化量表示。
浓度变化对化学反应速率有着直接的影响,下面将简单介绍浓度变化对化学反应速率的影响。
1.浓度的影响
在化学反应中,反应物浓度的增加可以提高反应速率,而反应物浓度的降低会降低反应速率。
这是因为在反应中,反应物与反应物之间的碰撞次数越多,化学反应速率就越快。
温度是影响化学反应速率的重要因素。
一般情况下,温度的升高可以加快化学反应速率,温度的降低则会降低化学反应的速率。
这是因为温度的升高会使分子的动能增加,分子之间的碰撞频率和能量也会增加,因而使反应物分子更容易被激发成中间体,从而加快反应速率。
3.催化剂的影响
催化剂能够提高化学反应当中的化学反应速率,并且在反应过程中不参与化学反应,因此催化剂在反应中属于“消耗少、使用多”的原则,具有很高的化学经济性。
催化剂与反应物之间还会发生表面的化学反应,使反应物分子中的化学键断裂和形成以及化学反应的能垒降低,从而加快了化学反应速率。
4.反应物之间的相互作用
在某些情况下,反应物之间的相互作用会影响化学反应的速率。
例如,在酸催化的酯化反应中,当醇和酸分子在反应中形成氢键和其他弱相互作用时,化学反应速率会减慢,因为这些弱相互作用会抵消反应的能量。
二、结论
根据上述分析,我们可以发现,浓度变化对化学反应速率有着直接的影响,包括反应物的加入、减少、催化剂的添加以及温度的升高或降低等。
因此,当需要加快或减缓化学反应时,我们可以通过控制反应物浓度、添加催化剂或调整反应温度等措施来达到目的。
手持技术之催化剂、浓度对化学反应速率的影响

交流 讨 实验 结 果 , 得 出结 论 ; 安排 小 组讨 论 交
流, 派代表汇报实验过程中出现 的 问题 , 实 验结果 及得 到结 论 , 以此 培养学 生反思 , 总 结实 验结果 的能力 , 思
维能力 。
时 间, 现将马铃薯捣 成泥 ) ( 实验 装置 图如 下 图) ; 让学
科学 的学习方法 , 形成 正 确 的 学 习 态 度 。
关键词 : 手 持技 术
催化剞
浓度
反应述率 生在 实验过程中有序进 行 , 明确实 验 目的, 而不 只是在
操作 仪器。 在 知识 与 技 能 方面 学 习 催 化 剂 跟 过 氧 化 氢 浓 度 对
人 教版义务教育课程标 准实验教科 书《 化学》 九年
对班上学 生 分 组 规 划 , 准 备 好仪 器 药 品 , 多 媒 体课 件 ( P V F ) ; 实 验仪 器 ; 手 持分析仪 , 气 压传感器 , 数据 线 , 磁
力搅拌 器 , 电子 天 平 , 塑 料注 射器 , l O m l 移 液管 , 1 O O ml 圆底烧瓶 , 二氧化锰 还有马铃薯 ( 为维 持实验秩 序节省
个组做: = 二 氧化 锰 塍化过 氧化氢 实 验 , 两个 组 做马铃 薯
催化过氧化 氢实验 , 观察学生实 验过程 中出现的问题 , 从而节省实验 时 问, 培 养学生 合作 交 流能 力 和实验 操
作能力 。
通过事先多 次对 此次课堂 实验 的操作 ,在 实验前 解决这 些 问题 后 ,
手 持 技 术 之 催 化剂 、 浓 度 对 化学 反 应 速 书 的 影 响
7 7
手持技术 之催化剂 、 浓 度 对 化 学 反 应 速 率 的 影 响
利用手持技术探究催化剂、浓度等条件对反应速率的影响

利用手持技术探究催化剂、浓度等条件对反应速率的影响作者:王芳芳衷明华来源:《课程教育研究·学法教法研究》2016年第15期【中图分类号】G64.23 【文献标识码】A 【文章编号】2095-3089(2016)15-0-01今天我说课的内容是人教版化学九年级上册第二单元课题3《制取氧气》第二课时。
接下来我主要从教材分析、教法、学法、教学程序以及板书设计这五个方面来阐述我的教学思路。
(首先是我对教材的分析)一、教材分析1.教材的内容、作用及地位《制取氧气》是初中化学重点内容之一,本课题内容较多,且学生第一次涉及气体制取,因此我把这一课题分为两课时,本次说课针对第二课时。
在同学们已经学习过制取氧气的基础上,通过这一课时,探究过氧化氢制取氧气的反应,让学生在实验中更深入理解制取氧气的反应原理,了解实验室制取气体的思路和方法。
制取氧气不仅是气体制取的开始,考察学生对实验操作的综合应用,同时,学好这一课题也能为即将在后面学到的《二氧化碳的制取》做铺垫,因此本课时起着承前启后的作用。
学生学好这部分知识对今后化学知识的学习有重要意义,打下一个良好基础。
2.三维目标①知识与技能1.掌握实验室过氧化氢制取氧气的反应原理和操作过程。
2.了解气压传感器、数据采集器以及配套软件的使用方法。
3.学习定量描述反应速率的方法。
②过程与方法通过探究催化剂及浓度对过氧化氢制取氧气反应速率的影响,初步认识到科学探究的意义,提高实验技能,培养合作意识,锻炼加强对实验过程的猜想判断能力和语言表达能力。
③情感态度与价值观通过实验探究使学生认识到科学探究的不易和收获,提高对化学的兴趣,感受化学的美妙。
3.教学重难点重点:掌握实验室过氧化氢制取氧气的反应原理和操作过程及方法。
难点:理解催化剂及浓度等条件对反应速率的影响。
二、教法分析学生是学习的主体,教师只是引导者。
根据这一教育理念,结合本节教材内容,本节课采取问题探究和学生分组实验相结合的教学方法。
研究浓度变化对反应速率的影响

研究浓度变化对反应速率的影响在化学实验中,浓度是指溶液中溶质(一般是固体或液体)所占的比例。
浓度的变化会直接影响到反应速率,即化学反应进行的快慢程度。
本文将就浓度对反应速率的影响进行探讨。
1. 引言研究化学反应速率是理解化学反应过程中一个重要的方面。
通过了解不同物质在不同浓度下的反应速率变化,可以帮助我们更好地理解化学反应速率的规律。
2. 浓度与反应速率的关系实验室中,我们通常可以通过改变反应物的浓度来研究浓度对反应速率的影响。
在反应物浓度较低的情况下,反应速率较慢;而在浓度较高的情况下,反应速率则较快。
这是因为浓度的增加会导致反应物分子之间的碰撞频率增加。
3. 马尔科夫尼克定律研究浓度对反应速率的影响,我们离不开马尔科夫尼克定律,它提供了反应速率与物质浓度之间的数学关系。
马尔科夫尼克定律可表达为:速率 = k[A]^m[B]^n其中,k 是反应速率常数,[A] 和 [B] 分别表示反应物 A 和 B 的浓度,m 和 n 分别为反应物 A 和 B 的反应级数。
4. 影响因素除了浓度,还有其他因素会影响反应速率,如温度、催化剂等。
在研究浓度对反应速率的影响时,我们需要将这些因素保持不变,以便更准确地分析浓度变化对速率的影响。
5. 实验设计为了研究浓度对反应速率的影响,我们可以采用比拟法或其他实验设计方法。
首先,选择一个具体的化学反应,并确定所需的反应物和观察指标。
然后,按照不同浓度的组合,进行多组实验,并记录下反应速率。
6. 实验结果与分析根据实验结果,我们可以得出结论:反应速率随着反应物浓度的增加而增加,即浓度增大,反应速率也增大。
同时,我们还可以找出反应速率与浓度之间的数学关系,进一步验证马尔科夫尼克定律。
7. 应用与意义了解浓度对反应速率的影响,对于理解化学反应的原理和控制反应速率具有重要意义。
在工业领域,通过调节反应物的浓度,可以实现对反应速率的控制,从而提高生产效率。
8. 结论浓度的变化对反应速率有明显的影响,浓度增加会加快反应速率。
《利用手持技术探究催化剂、浓度等对反应速率的影响》说课稿范文

《利用手持技术探究催化剂、浓度等对反应速率的影响》说课稿《利用手持技术探究催化剂、浓度等对反应速率的影响》说课稿范文今天我说课的内容是利用手持技术探究催化剂、浓度等对反应速率的影响,我将从教材分析、学情分析、教法学法分析、教学过程、板书设计和教学特色与感悟这六个方面内容来阐述我的教学思路。
一、教材分析本课题以人教版九年级化学上册第二单元《我们周围的空气》课题3制取氧气为背景,该部分内容介绍了三种制取氧气的方法,其中,催化剂及催化作用的概念是该部分的教学难点。
因此,在结束制取氧气的教学后,对教材进行二次开发,通过利用手持技术,对催化剂、浓度等对反应速率的影响设置实验探究活动,丰富充实了教科书的内容,学生能更好的掌握催化剂的概念和更清晰的认识到催化剂在化学反应过程中的作用,有利于学生将该部分的内容转化为自己知识体系的组成部分。
本课题既是对上一课题的延伸和拓展,又为接下来高中化学必修2、选修4中学习化学反应速率打下一定的基础,在教材中起着承上启下的作用。
二、学情分析教学对象:普通中学九年级的学生知识储备上,已具备制取氧气等方面知识,且有催化剂的概念及其作用的初步了解。
但对催化剂的作用的亲身体验还不够。
引入手持技术进行探究,学生能更好的体验到催化剂在化学反应中的作用,并探究除了催化剂外,浓度是否对反应速率有影响。
能力储备上,初步具备一定的实验操作能力,懂得分辨常用的实验仪器和如何组装实验装置,但自主与合作的意识不强,本实验旨在通过引导学生实验探究以培养学生的自主与合作的意识。
心理特征上,学生思维活跃,好奇心强,喜欢动手操作。
(一)教学目标:根据新课程标准,结合学生认知特点,我确定以下教学目标1、知识与技能(1)探究催化剂、浓度等对反应速率的影响(2)学会利用手持技术测定气体产生速率的操作方法2、过程与方法通过自主动手测量O2产生的速率,从而得出催化剂、浓度等对反应速率的影响,通过小组间的讨论,探求催化剂的用量、反应物浓度的大小对反应速率的影响规律。
手机光线传感器在初中化学实验中的应用探究——以“探究浓度和温度对化学反应速率的影响”为例

Journal 等软 件) ꎬ 可 以 完 成 数 据 的 实 时 采 集 和 处
2.3 实验过程
为智能手机融合化学实验教学提供了新的途径和
journal( 中文版) 软件ꎬ下载并安装该应用ꎮ
感器 元 件 及 各 种 App 软 件 ( 如 phyphox、 Science
理、数码成像等ꎬ实现对光强、长度、重力等的测量ꎬ
力ꎻ改进实验方案 2 运用了简单的电子技术ꎬ拓宽
了学生的知识面ꎮ 2 种方案各有优点ꎬ教师可以根
据学生的情况选用合适的方案ꎮ
水位自动报警器的教学内容更符合真实情境ꎬ我
参考文献
[1] 方汉兵ꎬ唐桂桂.巧用电子技术助力科学实验创新[ J] .
湖南中学物理ꎬ2026(6) :56.
[2] 浙江省教育厅教研室.义务教育教材科学实验活动册
图 2 10%硫酸溶液和不同浓度的氯化钡溶液
一定偏差ꎮ 利用智能手机的光线传感器测定反应
反应的光照度变化图
中光照度随时间变化曲线ꎬ可以从曲线上精确获取
钡溶液的浓度ꎬ记录不同浓度氯化钡溶液下反应体
Байду номын сангаас
光照度随时间的变化值和反应时间ꎬ更直观地得到
系的光照度随时间的变化曲线ꎬ来探究反应物浓度
实验结论ꎬ帮助学生更好地理解有关化学概念或原
4 结语
最新颁布的« 义务教育科学课程标准(2022 年
版) » 指出ꎬ教师应根据教学需要ꎬ本着科学合理、
图 7 模拟低于警戒水位
图 8 模拟达到警戒水位时
时实验效果 实验效果
安全可靠的要求开发实验教具ꎮ 充分利用日常用
品和材料ꎬ 开 发 创 新 科 学 实 验ꎬ 让 实 验 更 贴 近 生
活ꎬ课堂更有趣ꎬ使学生有更多动手的机会ꎮ 物理
《手持技术之催化剂、浓度等条件对反应速率的影响》说课稿

五舍六入教学目标:【知识与技能】初步学会用“五舍六入”的方法来求凑整。
【过程与方法】1.在经历自主探索的过程中,初步了解生活中除了四舍五入等凑整的方法外还存在其他不同的方法。
2.在经历自主探索的过程中,发展思维的灵活性,培养观察、推理、运用知识的能力。
3.经历比较标准的方法,验证的过程,培养合理的思维。
【情感、态度与价值观】1.初步体验凑整的方法是多种多样的。
2.在自主探索的过程中,培养勇于探索、积极思考的能力。
教学重点及难点:用“五舍六入法”求一个数的近似数。
教学用具准备:教具、学具、多媒体设备教学过程设计:一、情景引入1.用“去尾法”和“进一法”和“四舍五入法”凑整到百分位。
5.549 31.208 9.06812.608 7.624 0.80312[沟通旧知、建立联系,初步感知。
]2.在数学计算中,我们常用“四舍五入”法来凑整,也经常会运用“去尾法”和“进一法”来凑整。
在日常生活中,还有其他的凑整方法吗?课件展示:有些超市和医院结算时自设“五舍六入”法。
[问题引入,激发学生的探究兴趣]二、探究新知(一)主动探究1.你认为“五舍六入”凑整该怎样凑整?(小组讨论)结论:尾数小于或等于5的舍去尾数大于或等于6的就向前一位进12.讨论解决例题:有些超市和医院结算时自设“五舍六入”:一共要付148.15元,医保卡里扣了139.25元,还需支付多少元现金?(二)独立思考解答。
(三)对于不同的答案展开讨论。
1.归纳。
2.仔细审题,根据题意选择凑整方法。
“五舍六入”凑整:尾数小于或等于5的舍去尾数大于或等于6的就向前一位进1。
[借助现实生活中的例子引出了凑整的另一种“五舍六入”,让学生初步了解生活中除四舍五入等凑整方法以外还存在其他不同方法。
]三、巩固练习1.根据购物清单计算并填空(课件展示)(略)(1)独立练习并列出算式(2)讨论:说说你是怎样想的?你认为解题时要注意些什么?(3)说说“五舍六入”凑整方法2.练一练:用“五舍六入”法将下列小数凑整到十分位35.26 20.205 87.087 66.660.625 25.06 115.35 201.56[运用所学知识进行模仿练习,加深对所学知识的理解。
化学反应速率与浓度的关系探索

化学反应速率与浓度的关系探索化学反应速率是描述化学反应快慢程度的重要指标之一。
在化学实验中,我们经常会发现,当反应物浓度增加时,反应速率也会随之增加。
这引发了科学家们的兴趣,他们开始探索化学反应速率与浓度之间的关系。
一、浓度对反应速率的影响浓度是指单位体积内溶质的物质量或物质的摩尔数。
在化学反应中,反应物的浓度越高,反应物分子之间的碰撞频率就越高,从而增加了反应发生的概率,进而加快了反应速率。
这是因为高浓度下,反应物分子之间的碰撞更加频繁,有效碰撞的概率也更高。
二、浓度与反应速率的定量关系科学家们通过实验研究,发现了浓度与反应速率之间的定量关系。
以一阶反应为例,一阶反应是指反应速率与反应物浓度的一次方成正比。
根据实验数据,可以得到以下关系式:速率 = k[A]其中,速率表示反应速率,k为反应速率常数,[A]表示反应物A的浓度。
三、浓度对反应速率的影响机理浓度对反应速率的影响可以从分子层面解释。
在反应物浓度较低时,反应物分子之间的碰撞频率较低,有效碰撞的概率也较低,导致反应速率较慢。
而当反应物浓度增加时,反应物分子之间的碰撞频率增加,有效碰撞的概率也增加,从而加快了反应速率。
此外,浓度还可以影响反应物分子的平均动能。
浓度越高,反应物分子之间的碰撞能量也越高,这增加了反应物分子克服反应势垒的能力,从而加快了反应速率。
四、浓度与反应速率的应用浓度与反应速率的关系在许多实际应用中具有重要意义。
例如,在工业生产中,控制反应物的浓度可以调节反应速率,从而实现产品的高效生产。
此外,在环境保护领域,了解浓度与反应速率的关系可以帮助我们预测和控制大气和水体中的化学反应过程,从而减少污染物的产生。
总结:化学反应速率与浓度之间存在着密切的关系。
浓度的增加可以增加反应物分子之间的碰撞频率和碰撞能量,从而加快反应速率。
实验研究表明,浓度与反应速率之间存在着定量关系,可以通过数学公式进行描述。
浓度与反应速率的关系不仅在理论研究中具有重要意义,也在实际应用中发挥着重要作用。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
现 象非常明显。
关键词 : 色度 传 感 器 ; 手持 技 术 ; 微 型 实 验
文章编号 : 1 0 0 8 ~ 0 5 4 6 ( 2 0 1 3 ) 0 7 — 0 0 9 1 — 0 1
d o i : 1 0 . 3 9 6 9  ̄. i s s n . 1 0 0 8 - 0 5 4 6 . 2 0 1 3 . 0 7 . 0 3 6
・
实验 教 学研 究 ・
手持技 术在 中学 匕 学 中应 用一 则
— —
探 究浓度对化学反应速 率的影响
杨 延光
( 合肥一 中
谢 月平
2 3 0 6 0 1 ) 安 合 肥摘要 : 手持技 术 中的 色度传感 器在 中学化 学中用于探 究浓度影响化学反应速率的 实验 , 实现 了实验微型化 、 定量化并且
表示 约 1 3 5 s 褪色。
把手持技术融人化学实验 中, 能使学生学会 如何 进行 探 究性 实 验学 习 ; 学会 从 定量 的角 度分 析 和解 决
问题 , 探 求 变 量 之 间 的 因果 关 系 和 相 关 关 系 , 发 展 了 学 生 的问题 解决 能力 , 真 正体 现 了新课 标教 育思 想 。 下 面介 绍 色度 传感 器 在 中学化 学 中的一 个 应 用 : 探究 浓度 影 响化 学反 应速 率 的微 型实验 。
然。
1 . 将 色 度传 感 器 中的标 准 容器 装入 蒸 馏水 , 旋 转
色度传感器上的调节透光率旋钮 , 使初始 的透光率约
为 1 0 0 %。
2 . 用 同一个主机连接两只色度传感器 , 设置横坐
标为 2 0 0 s , 间隔为 2 0 , 设 置纵坐标 为 1 1 0 %, 间 隔 为 1 0 , 采 集 速度 为 1 个/ s , 2 0 0个 。
化 学教 与 学 2 0 1 3年 第 7期
~
91 —
中图分类号 : G 6 3 3 . 8
文献标识码 : B
高 中化 学新 课 程 中大 大加 强 了化 学 实验 的力 度 ,
同时也强调 了实验 的探究性 , 其中新课标在每个 主题
下都 专 门设 置 了“ 活 动与 探 究建议 ” 栏 目, 并 设计 了多 个 与化 学 实 验 探 究 有 关 的 活动 , 在 实 验 手段 上 , 更 加 体现 了其多元 化 与现 代化 。
3 . 用 滴 管 吸取 0 . 0 1 mo l / L酸 性 K Mn O 溶 液 分 别 加入两只标 准容器二分之一 , 两人配合 ( 可找学生帮 助 )同时 再分 别 加入 0 . 1 mo l / L H C 2 0 溶液 、 0 . O l mo l / L
H 2 C 2 0 溶液 , 然后迅速放入传感器内。点击采集。 4 . 仪器上显示下图 , 一条表示约 8 5 s 褪色 。 另 一
二
摹
准备好相关装置与试剂 , 将色度传感器接人 系统 主机 数 据采 集 接 口 , 连 接好 计 算机 、 数 据 采集 器 、 色度 传感器之间的连线 , 运行数字化实验系统。
磕
以上 实验 优 点在 于 : 用量 极少 , 节约试剂 ; 现象 明 显, 肉眼 观察 颜 色 变 化 很 不 准确 , 而数 据显 示 一 目了
