自然界中的硫ppt 鲁科版优质课件
合集下载
鲁科版高中化学必修一 3.3 硫的转化(共18张ppt)(共18张PPT)

分析硫单质化合价
-2
低价
还原剂
0
S
氧化剂
+4 +6
高价
中间价态
气态氢化物
氧化物
硫矿石
含氧酸
解释为什么硫既可以与金
属反应,又可以与非金属 含氧酸盐
反应
硫在生活中的用处
1.制造硫酸、化肥、火柴、杀虫剂等
硫在生活中的用处
2.制造火药,烟花爆竹
点燃
S + 2KNO3 + 3C
K2S + 3CO2 + N2
反应放出的热能使反应继续进行
硫和氯气都能分别与铜、铁反应, 试比较反应有何异同。
点燃 +2
Cu + Cl2 = CuCl2
△ +3
2Fe + 3Cl2 = 2FeCl3
△ +1
2Cu + S = Cu2S
△ +2
Fe + S = FeS
氯气是氧化剂
硫是氧化剂
化合反应
化合反应
生成高价的金属氯化物
生成低价的金属硫化物
2、2Cu+S =Cu2S
3、2Na+S=Na2S
4、Hg+S=HgS
5、2Al+3S
△
=ห้องสมุดไป่ตู้Al2S3
实验
将铁粉与硫 粉的混合物平铺 在一石棉网上, 用一根加热后的 玻璃棒去引燃药 品的一端。
硫与铁的反应
0△
-2
Fe + S = FeS
氧化剂
现象:剧烈燃烧,发光
发热,生成黑色固体。
注意: 生成 硫化亚铁 FeS 不生成 硫化铁 Fe2S3
石膏(CaSO4·2H2O)
《自然界中的硫》课件

天然硫资源
硫矿的种类和分布
了解不同类型硫矿的产地和分 布情况。
硫酸盐岩和硫化物
深入研究硫酸盐岩和硫化物等 硫矿资源。
天然氧化铁硫矿
探索天然氧化铁硫矿的形成和 特点。生 Nhomakorabea体中的硫
硫的来源
了解生物体中硫的不同来源和进入方式。
蛋白质中的硫元素
研究蛋白质中的硫元素的作用和功能。
活性硫代谢
探索生物体中活性硫代谢的重要性和机制。
• 研究硫在不同行业中的具体应用案例。 • 了解硫对产业发展的重要性。
硫的污染与环保
1 硫化物和硫酸盐对人体的影响
深入了解硫化物和硫酸盐对人体健康的潜在风险。
2 硫化氢的毒性及其防护
探索硫化氢的毒性特点和相应的防护措施。
3 硫磺的安全操作和储存要求
研究硫磺的安全操作和储存标准和要求。
环境中的硫
大气硫的来源和污染
深入了解大气中硫的来源和相关的环境污染问题。
水中硫的循环与控制
研究水体中硫的循环过程和相关的环境控制策略。
土壤中硫的形态和生物作用
探索土壤中硫的不同形态和其对生物的影响。
硫的工业应用
硫的生产与加工工艺
• 了解硫的工业生产过程和加工技术。 • 探索硫的应用范围和用途。
硫在肥料、化学品、制药、矿冶等领 域的应用
《自然界中的硫》PPT课 件
自然界中的硫有着丰富的特性和多样的应用。让我们一起探索硫的概念与性 质,硫的分类和形式,以及硫在地球化学循环中的作用。
硫的地球化学循环
1
循环过程
了解硫在自然界中的循环过程和相互作用。
2
生物转化
探索生物体如何参与硫的转化和循环过程。
3
水体和土壤
【化学】鲁科版必修1课件:第3章3节(第1课时)自然界中的硫

还原性,含+6价硫元素的物质具有氧化性,含0价和+4
价硫元素的物质既有氧化性,又有还原性。
自主探究
精要解读
实验探究
1. 了解含硫元素的物质在自然界的存在及其主要来源。 2. 应用氧化还原反应理论,探究含硫元素物质间的相互转
化。 掌握硫和二氧化硫的主要性质和用途。 3.
4. 了解硫及其化合物在生产、生活中的应用。 5. 了解酸雨的危害,能够提出减少向大气中排放二氧化硫的
还原性 1.
当硫与氧化性较强的物质反应时, 通常失电子, 化合价升高, 点燃 表 现 一 定 的 还 原 性 , 如 S + O2 ===== SO2 , S + △ 2H2SO4(浓)=====3SO2↑+2H2O。
自主探究 精要解读 实验探究
2.氧化性 (1)当硫与 H2、部分金属等还原性较强的物质反应时,通常 △ 得电子,化合价降低,表现氧化性,如 S+ H2=====H2S, S △ △ + 2Cu=====Cu2S, S+ Hg===HgS,Fe+S=====FeS。 (2)在黑火药爆炸的反应中,硫化合价降低,表现氧化性, 点燃 化学方程式为:S+ 2KNO3+ 3C=====K2S+ 3CO2↑+N2↑。
还原性 。 _______
自主探究 精要解读 实验探究
(2)与金属的反应 一定条件下,S能与Fe等金属反应,化学方程式为
△ Fe+S=====FeS ;产物中硫的化合价为______ -2价 ,体现了硫 ______________
氧化性 。 的_______
自主探究
精要解读
实验探究
笃学三
用途
硫酸 、 _____ 化肥 、 _____ 火柴 及杀虫剂等,还用于 主要用于制造_____ 火药 、 _____ 烟花 、 _____ 爆竹 等。 制造_____
鲁科版高中化学必修一《硫的转化》物质的性质与转化PPT(第一课时自然界中的硫二氧化硫)

鲁科版高中化学必修一 《硫的转化》物质的性质与转化PPT(第一课时自然 界中的硫二氧化硫)
科 目:化学
适用版本:鲁科版
适用范围:【教师教学】
第2节 硫的转化
第一课时 自然界中的硫 二氧化硫
第一页,共五十二页。
[新教材内容有哪些]
第二页,共五十二页。
[新课程标准是什么] 1.了解硫、二氧化硫的主要性质。 2.认识硫、二氧化硫在生产中的应用和对生态环境的影响。
(2)由硫元素组成的单质有多种,如正交硫和单斜硫,它们 是硫元素的__同__素__异__形__体_____。
(3)晋人葛洪《抱朴子·金丹篇》说:“凡草木烧之即烬,
而丹砂炼之成水银,积变又还成丹砂,其去草木亦远矣。”
丹 砂 即 HgS , 上 述 变 化 过 程 的 化 学 方 程 式 为 __H__g_S_=_=△_=_=_=_H__g_+__S_、__H_g_+__S_=_=_=__H_g_S_____。
第七页,共五十二页。
(4)我国古代的炼丹家在长期的炼制丹药过程中,发现硝酸钾、 硫黄和木炭的混合物能够燃烧爆炸,由此诞生了中国古代四 大发明之一的火药。请查阅资料,用化学方程式表示其反应 原理:_2_K__N_O__3_+__S_+__3_C_=_=_=_K__2_S_+__N_2_↑__+__3_C_O__2↑_________。 (5)硫单质中硫元素的化合价为 0,具有___升__高__和__降__低____的趋 势,可能表现的性质为__还__原__性__和__氧__化__性_________________。
点燃 S+O2=====SO2
S表现的 性质
氧化性
还原性
第九页,共五十二页。
[落实新知能] 1.自然界中的硫
科 目:化学
适用版本:鲁科版
适用范围:【教师教学】
第2节 硫的转化
第一课时 自然界中的硫 二氧化硫
第一页,共五十二页。
[新教材内容有哪些]
第二页,共五十二页。
[新课程标准是什么] 1.了解硫、二氧化硫的主要性质。 2.认识硫、二氧化硫在生产中的应用和对生态环境的影响。
(2)由硫元素组成的单质有多种,如正交硫和单斜硫,它们 是硫元素的__同__素__异__形__体_____。
(3)晋人葛洪《抱朴子·金丹篇》说:“凡草木烧之即烬,
而丹砂炼之成水银,积变又还成丹砂,其去草木亦远矣。”
丹 砂 即 HgS , 上 述 变 化 过 程 的 化 学 方 程 式 为 __H__g_S_=_=△_=_=_=_H__g_+__S_、__H_g_+__S_=_=_=__H_g_S_____。
第七页,共五十二页。
(4)我国古代的炼丹家在长期的炼制丹药过程中,发现硝酸钾、 硫黄和木炭的混合物能够燃烧爆炸,由此诞生了中国古代四 大发明之一的火药。请查阅资料,用化学方程式表示其反应 原理:_2_K__N_O__3_+__S_+__3_C_=_=_=_K__2_S_+__N_2_↑__+__3_C_O__2↑_________。 (5)硫单质中硫元素的化合价为 0,具有___升__高__和__降__低____的趋 势,可能表现的性质为__还__原__性__和__氧__化__性_________________。
点燃 S+O2=====SO2
S表现的 性质
氧化性
还原性
第九页,共五十二页。
[落实新知能] 1.自然界中的硫
鲁科版高中化学必修一课件3.3.1自然界中的硫
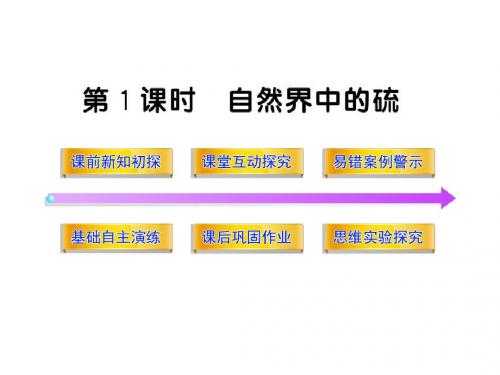
FeS+2HCl====FeCl2+H2S↑ Fe+2HCl====FeCl2+H2↑
分析以上两个方程式可知不论Fe与S反应是谁过量,生成气 体的物质的量与原混合物中Fe的物质的量相等。已知生成
标准状况下2.24 L气体,则一定有0.1 mol Fe(5.6 g)存
在,C正确。当5.6 g铁粉恰好与3.2 g硫粉反应,生成 8.8 g FeS;若硫粉过量,则硫粉的质量大于3.2 g,混合物
==== FeS
88 4.4 g
△
2.8 g 1.6 g
即5.6 g 铁和1.6 g S反应时铁过量,反应后得到混合物。
【典例】下列各选项中的杂质,欲用括号内物质除去,其中 能达到目的的是 A.CO中混有少量CO2(澄清石灰水)
B.CO2中混有少量氯化氢气体 (NaOH溶液)
C.氯化氢气体中混有少量水蒸气(碱石灰) D.N2中混有少量O2 (灼热的氧化铜) 【思路点拨】解答本题要注意以下两点:
【解析】单质硫俗称硫黄,硫蒸气的相对分子质量为
22.4×11.42=256,分子式为S8。硫与钠反应生成硫化钠。
答案:(1)硫黄 (3)S+2Na====Na2S (2)S8
某学校实验小组欲探究硫粉与铁粉的反应,并验证反应后 的产物中铁元素的化合价,如图是铁粉和硫粉反应的装置图
。
(1)将硫粉和铁粉按物质的量之比1∶1充分混合。 (2)按装置图将仪器连接好。 (3)_______________________________________。
【解析】选B。A项,硫在空气中燃烧生成SO2而不是SO3。B
项,分离黑火药中的三组分可利用它们溶解性的差异,先 用CS2处理,使硫黄溶解,滤渣再用水处理,溶解硝酸钾,
分析以上两个方程式可知不论Fe与S反应是谁过量,生成气 体的物质的量与原混合物中Fe的物质的量相等。已知生成
标准状况下2.24 L气体,则一定有0.1 mol Fe(5.6 g)存
在,C正确。当5.6 g铁粉恰好与3.2 g硫粉反应,生成 8.8 g FeS;若硫粉过量,则硫粉的质量大于3.2 g,混合物
==== FeS
88 4.4 g
△
2.8 g 1.6 g
即5.6 g 铁和1.6 g S反应时铁过量,反应后得到混合物。
【典例】下列各选项中的杂质,欲用括号内物质除去,其中 能达到目的的是 A.CO中混有少量CO2(澄清石灰水)
B.CO2中混有少量氯化氢气体 (NaOH溶液)
C.氯化氢气体中混有少量水蒸气(碱石灰) D.N2中混有少量O2 (灼热的氧化铜) 【思路点拨】解答本题要注意以下两点:
【解析】单质硫俗称硫黄,硫蒸气的相对分子质量为
22.4×11.42=256,分子式为S8。硫与钠反应生成硫化钠。
答案:(1)硫黄 (3)S+2Na====Na2S (2)S8
某学校实验小组欲探究硫粉与铁粉的反应,并验证反应后 的产物中铁元素的化合价,如图是铁粉和硫粉反应的装置图
。
(1)将硫粉和铁粉按物质的量之比1∶1充分混合。 (2)按装置图将仪器连接好。 (3)_______________________________________。
【解析】选B。A项,硫在空气中燃烧生成SO2而不是SO3。B
项,分离黑火药中的三组分可利用它们溶解性的差异,先 用CS2处理,使硫黄溶解,滤渣再用水处理,溶解硝酸钾,
鲁科版高中化学必修一课件3.3.1自然界中的硫
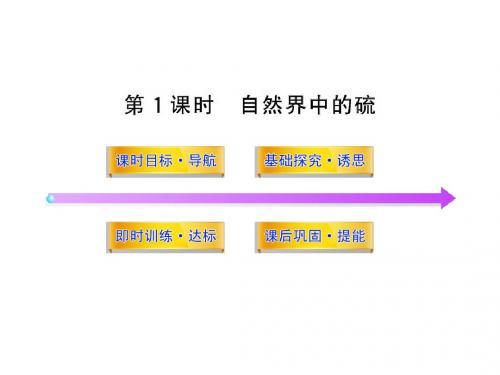
3.根据反应条件判断 当不同的氧化剂作用于同一还原剂时,若氧化产物价态相 同,可根据反应条件的难易来判断。
二、非选择题(本题包括2小题,共 26 分)
7.(12分)为了证明铁和硫反应产物中铁的化合价,下面是 某同学设计的实验过程的一部分:
请回答以下问题: (1)为什么反应在“惰性气体环境”中进行________。 (2)操作②的作用是______,热的KOH溶液还可以改用
B.汞洒落在地上,可用硫粉处理 C.硫与金属或非金属反应均作为氧化剂 D.1.6 g硫与6.4 g铜反应能得到8.0 g纯净硫化物
【规范解答】选B、D。 元素在自然界中的存在形式虽与化 学活泼性有关,但不能以非金属性强弱作为依据,如 O、
N、S的非金属性并不弱,但在自然界仍存在游离态的单质
O2、N2、S。所以A不正确。汞易与硫粉反应,生成不挥发的 无毒的HgS。所以B正确。硫单质为0价,是中间价态,与金
1.结合硫的物理性质,思考如何洗涤试管壁上附着的硫? 提示:硫不溶于水,微溶于酒精,易溶于 CS2,所以应用CS2
洗涤。
2.比较Fe、Cu分别与Cl2、S的反应,找出规律并思考: (1)Cl2和S的氧化性谁的更强? (2)能否由单质直接化合得到FeCl2、CuS? 提示:(1)2Fe+3Cl2 ==== 2FeCl3 Fe+SFeS ==== 2Cu+S
(2)硫与变价金属反应一般生成低价化合物,如:Fe+S FeS ,2Cu+S ==== ==== HgS。 2.洗涤试管壁上残存的硫除了可以用CS2外,也可以用热的
△ NaOH溶液,发生反应6NaOH+3S ==== 2Na2S+Na2SO3+3H2O。 △
自然界中的硫ppt 鲁科版2

3.洗涤试管内壁上附着的硫黄,可选用的方法( D )
A.加水洗涤 B.通入氢气加热 C.加热试管使硫熔化 D.用CS2洗涤
4.下列化合物能由两种单质直接化合而生成的是
( D )
A.Fe2S3
C.FeCl2
B.CuS
D.FeCl3
【提醒】氧化性:Cl>S,Cl2与变价金属反应时 生成高价金属化合物,S与变价金属反应时生成低 价金属化合物,故A项应为FeS,B项应为Cu2S。
第3节硫的转化
第1课时自然界中的硫
火山喷发是一种奇特的 地质现象,是岩浆等喷出物 在短时间内从火山口向地表
的释放。
你知道火山喷发产生的
气体的主要成分吗?在火山
口附近经常有一些黄色物质, 你知道是什么吗?
1.了解硫元素在自然及含硫物质的主要来源。 2.掌握硫单质的物理性质和化学性质。(重点)
广东从化温泉
当硫与强还原剂(金属、氢气、碳等)反应时,
表现氧化性。(硫元素化合价降低)
当硫与氧气等强氧化剂反应时,表现还原性。
(硫元素化合价升高)
硫是一种比较活泼的非金属单质,既可表现氧
化性,又可表现还原性。
1.(双选)下列说法不正确的是( AD ) A.硫是一种淡黄色的能溶于水的晶体 B.硫的化合物常存在于火山喷出的气体中和矿 泉水里
一、自然界中的硫
火 山 口 的 硫
火 山 爆 发
【想一想】
1.火山喷发时,产生的许多含有硫元素的气体是
什么?
2.自然界中含硫化合物有哪些?
1.自然界中不同价态硫元素间的转化
大 气 H2S
部分硫
SO2 SO3
阳光、H2O、 O2 氧化
H2SO3
H2SO4
化学课件《自然界中的硫》优秀ppt 鲁科版3

3、向第二支试管中加等量的酒精,了解硫在酒精中的 溶解情况,观察发生的现象 ; 4、向第三支试管中加等量的二硫化碳 ,了解硫在二硫 化碳中的溶解情况,观察发生的现象 ; 5、取少量硫粉放在试管中,在酒精灯上将其加热至熔 化,观察发生的现象。
总结:硫的物理性质
1、一种黄色或淡黄色的固体 2、不溶于水 微溶于酒
3、小磁铁落下
交流 研讨
1、通过什么现象说明铁粉与硫粉反 应了?
2、移开玻璃棒后仍能剧烈反应说明 什么?
S具有弱的氧化性,只能将变价金属氧化为低价
知识·整合
还原剂
-2
0
低价
S
中
间
H2S FeS等
价 态
氧化剂
+4 +6
高价
SO2、SO3 H2SO3、H2SO4 Na2SO4 等
畅所 欲言
你能说出硫在生产、生活中的应用吗?
[答案]A。
巩固练习
2.下列实验现象的描述错误的是( ) (A)氢气在氯气中燃烧生成绿色烟雾 (B)红热的铁丝在氧气中燃烧,火星四射,生成黑色 固体颗粒 (C)点燃的硫在氧气中剧烈燃烧,发出蓝紫色火焰 (D)钠在空气中燃烧,发出黄色的火焰,生成淡黄色 固体 [答案]A。
巩固练习
3.有关物质燃烧时火焰颜色描述错误的是( ) (A)氢气在氯气中燃烧 — 苍白色 (B)钠在空气中燃烧 — 黄色 (C)乙醇在空气中燃烧 — 淡蓝色 (D)硫在氧气中燃烧 — 绿色 [答案]D。
1、“硫磺”温泉可以医治皮肤病
惠州龙门铁泉
惠州龙门天然温泉
2、制造火药,烟花爆竹
点燃
S + 2KNO3 + 3C == K2S + 3CO2↑+ N2↑
总结:硫的物理性质
1、一种黄色或淡黄色的固体 2、不溶于水 微溶于酒
3、小磁铁落下
交流 研讨
1、通过什么现象说明铁粉与硫粉反 应了?
2、移开玻璃棒后仍能剧烈反应说明 什么?
S具有弱的氧化性,只能将变价金属氧化为低价
知识·整合
还原剂
-2
0
低价
S
中
间
H2S FeS等
价 态
氧化剂
+4 +6
高价
SO2、SO3 H2SO3、H2SO4 Na2SO4 等
畅所 欲言
你能说出硫在生产、生活中的应用吗?
[答案]A。
巩固练习
2.下列实验现象的描述错误的是( ) (A)氢气在氯气中燃烧生成绿色烟雾 (B)红热的铁丝在氧气中燃烧,火星四射,生成黑色 固体颗粒 (C)点燃的硫在氧气中剧烈燃烧,发出蓝紫色火焰 (D)钠在空气中燃烧,发出黄色的火焰,生成淡黄色 固体 [答案]A。
巩固练习
3.有关物质燃烧时火焰颜色描述错误的是( ) (A)氢气在氯气中燃烧 — 苍白色 (B)钠在空气中燃烧 — 黄色 (C)乙醇在空气中燃烧 — 淡蓝色 (D)硫在氧气中燃烧 — 绿色 [答案]D。
1、“硫磺”温泉可以医治皮肤病
惠州龙门铁泉
惠州龙门天然温泉
2、制造火药,烟花爆竹
点燃
S + 2KNO3 + 3C == K2S + 3CO2↑+ N2↑
自然界中的硫ppt 鲁科版

【典题训练】(2015·宿州高一检测)在如图所
示的转化关系中,已知B、D都是淡黄色固体,D
与G的浓溶液在一定条件下反应生成E,回答下列问题:
(1)写出下列物质的化学式:
A
;F
;H
。
(2)D与热的C溶液反应时氧化产物与还原产物的物质的量之比为1∶2,
试写出其离子方程式:
。
【解题指南】解答本题需注意以下3点: (1)中学阶段淡黄色固体为Na2O2、单质硫和AgBr; (2)B为A与氧气反应的产物,则B为含氧化合物; (3)D与NaOH溶液反应时化合价升降应保持一致。
答案:(1)Na SO3 Na2SO4
(2)3S+6OH-
==△== 2S2-+
S
O
2- 3
+3H2O
【补偿训练】1.下列关于硫的说法正确的是 ( ) A.硫在空气中的燃烧产物是三氧化硫 B.铜丝擦亮后伸入硫蒸气中产物是CuS C.硫与非金属反应均作还原剂 D.1.6 g硫与5.6 g铁反应不能得到7.2 g纯净硫化物
2.表现氧化性:硫与还原性较强的物质(如金属、氢气等)反应时,得电
子,化合价降低,被还原,表现氧化性。
(1)金属单质:S+Fe
△
====
FeS,S+2Cu
△
====
Cu2S,
硫与变价金属反应时生成低价态金属硫化物。
(2)氢气:S+H2
△
====
H2S。
(3)在黑火药爆炸的反应中,硫的化合价降低,表现氧化性,化学方程式
【解析】选A。硫是一种淡黄色固体,不溶于水,微溶于酒精,易溶于二 硫化碳。雄黄、辰砂、石膏都是含硫物质。自然界中硫元素广泛存在 于海洋、大气和地壳中,也存在于动植物体内,火山喷发时,地壳中的 硫元素会随之进入大气和水中。
自然界中的硫ppt3

高价
SO2、SO3 H2SO3、H2SO4 Na2SO4 等
畅所 欲言
你能说出硫在生产、生活中的应用吗?
1、“硫磺”温泉可以医治皮肤病
惠州龙门铁泉
惠州龙门天然温泉
2、制造火药,烟花爆竹
S + 2KNO3 + 3C == K2S + 3CO2↑+ N2↑
点燃
3.轮胎、胶管等橡胶制品
4、制造硫酸、化肥、火柴、杀虫剂等
鲁科版(必修一)
节硫的转化
课时:自然界中的硫
你知 道吗
在哥伦比亚东部的普莱斯火山地区,有一条河,全 长580多公里,河里鱼虾绝迹,两岸寸草不生。要是哪个 不知天高地厚的人喝一口那河里的水,便会高热眩晕, 口舌溃烂,五脏俱损甚至死亡。如果有人想到河里去游 泳,过不了多久,就会皮开肉绽,一命呜呼,甚至连块 骨头也留不下。这条河就是堪称世界五大奇河之一的“ 雷欧维拉力河”,当地人称它为“谋杀河” !!!
观察· 思考1
探究硫与氧气的反应
取少量的硫粉放入燃烧匙中,将燃烧 匙放在酒精灯上加热至硫粉呈熔化状态后, 迅速伸入底部有少量水的盛满氧气的集气 瓶中。请同学们仔细观察实验现象
实验现象:
1、产生明亮的蓝紫色火焰
2、生成一种有刺激性气味的气体
观察· 思考2
探究硫粉和铁粉的反应
玻璃棒
把研细的硫粉和铁 粉按照一定比例均匀混 合,并按照右图放在铜 片上,用灼热的玻璃棒 触及一端。请同学们仔 细观察现象并作记录。
含硫物质的产生
SO3 H2S
O2
H2O
H2SO4 H2SO3
微生物
S H 2S
SO2
地表
石膏(CaSO4· 2H2O) 芒硝(Na2SO4· 10H2O)
自然界中的硫ppt 鲁科版3

总结:硫的物理性质
1、一种黄色或淡黄色的固体 2、不溶于水 微溶于酒 精,易溶于二硫化碳 3、熔点和沸点都不高 4、很脆,易研成粉末 硫有多种同素异形体 如:斜方硫、单斜硫等
单斜硫
探究二:硫的化学性质
交流 研讨
1、从元素化合价的角度,预测硫
单质可能具有什么化学性质?
2、从物质类别的角度,预测硫单 质可能与哪几类物质反应?
含硫物质的产生
SO3 H2S
O2
H2O
H2SO4 H2SO3
微生物
S H) 芒硝(Na2SO4· 10H2O)
雌 黄 黄 铁 矿 雄 黄 辰 砂
地下
探究一:硫的物理性质
实验啦
1、分别取少量硫粉装在四支小试管中,观察试管中硫 粉的颜色和状态; 2、向第一支试管中加水,了解硫在水中的溶解情况; 3、向第二支试管中加等量的酒精,了解硫在酒精中的 溶解情况,观察发生的现象 ; 4、向第三支试管中加等量的二硫化碳 ,了解硫在二硫 化碳中的溶解情况,观察发生的现象 ; 5、取少量硫粉放在试管中,在酒精灯上将其加热至熔 化,观察发生的现象。
观察· 思考1
探究硫与氧气的反应
取少量的硫粉放入燃烧匙中,将燃烧匙 放在酒精灯上加热至硫粉呈熔化状态后,迅 速伸入底部有少量水的盛满氧气的集气瓶中。 请同学们仔细观察实验现象
实验现象:
1、产生明亮的蓝紫色火焰
2、生成一种有刺激性气味的气体
观察· 思考2
探究硫粉和铁粉的反应
玻璃棒
把研细的硫粉和铁 粉按照一定比例均匀混 合,并按照右图放在铜 片上,用灼热的玻璃棒 触及一端。请同学们仔 细观察现象并作记录。
41、从现在开始,不要未语泪先流。 42、造物之前,必先造人。 43、富人靠资本赚钱,穷人靠知识致富。 44、顾客后还有顾客,服务的开始才是销售的开始。 45、生活犹如万花筒,喜怒哀乐,酸甜苦辣,相依相随,无须过于在意,人生如梦看淡一切,看淡曾经的伤痛,好好珍惜自己、善待自己。 46、有志者自有千计万计,无志者只感千难万难。 47、苟利国家生死以,岂因祸福避趋之。 48、不要等待机会,而要创造机会。 49、如梦醒来,暮色已降,豁然开朗,欣然归家。痴幻也好,感悟也罢,在这青春的飞扬的年华,亦是一份收获。犹思“花开不是为了花落,而是为了更加灿烂。 50、人活着要呼吸。呼者,出一口气;吸者,争一口气。 51、如果我不坚强,那就等着别人来嘲笑。 52、若不给自己设限,则人生中就没有限制你发挥的藩篱。 53、希望是厄运的忠实的姐妹。 54、辛勤的蜜蜂永没有时间悲哀。 55、领导的速度决定团队的效率。 56、成功与不成功之间有时距离很短只要后者再向前几步。 57、任何的限制,都是从自己的内心开始的。 58、伟人所达到并保持着的高处,并不是一飞就到的,而是他们在同伴誉就很难挽回。 59、不要说你不会做!你是个人你就会做! 60、生活本没有导演,但我们每个人都像演员一样,为了合乎剧情而认真地表演着。 61、所谓英雄,其实是指那些无论在什么环境下都能够生存下去的人。 62、一切的一切,都是自己咎由自取。原来爱的太深,心有坠落的感觉。 63、命运不是一个机遇的问题,而是一个选择问题;它不是我们要等待的东西,而是我们要实现的东西。 64、每一个发奋努力的背后,必有加倍的赏赐。 65、再冷的石头,坐上三年也会暖。 66、淡了,散了,累了,原来的那个你呢? 67、我们的目的是什么?是胜利!不惜一切代价争取胜利! 68、一遇挫折就灰心丧气的人,永远是个失败者。而一向努力奋斗,坚韧不拔的人会走向成功。 69、在真实的生命里,每桩伟业都由信心开始,并由信心跨出第一步。 70、平凡的脚步也可以走完伟大的行程。 71、胜利,是属于最坚韧的人。 72、因害怕失败而不敢放手一搏,永远不会成功。 73、只要路是对的,就不怕路远。 74、驾驭命运的舵是奋斗。不抱有一丝幻想,不放弃一点机会,不停止一日努力。 75、自己选择的路,跪着也要走完。 76、当你的希望一个个落空,你也要坚定,要沉着! 77、蚁穴虽小,溃之千里。 78、我成功因为我志在成功! 79、凡真心尝试助人者,没有不帮到自己的。 80、相信自己,你能作茧自缚,就能破茧成蝶。 81、偶尔,只需要一个鼓励的微笑,就可以说服自己继续坚强下去。 82、年轻是本钱,但不努力就不值钱。 83、一时的忍耐是为了更广阔的自由,一时的纪律约束是为了更大的成功。 84、在你不害怕的时间去斗牛,这不算什么;在你害怕时不去斗牛,也没有什么了不起;只有在你害怕时还去斗牛才是真正了不起。 85、能把在面前行走的机会抓住的人,十有八九都会成功。 86、天赐我一双翅膀,就应该展翅翱翔,满天乌云又能怎样,穿越过就是阳光。 87、活鱼会逆流而上,死鱼才会随波逐流。 88、钕人总是把男人的谎言当作誓言去信守。 89、任何业绩的质变都来自于量变的积累。 90、要战胜恐惧,而不是退缩。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第3节 硫的转化 第1课时 自然界中的硫
一、自然界中的硫 1.硫的存在:
存在形态
游离态
_化__合__态
如_硫__黄__
ቤተ መጻሕፍቲ ባይዱ
如硫酸钠
存在范围 海洋、大气、地壳、
动植物体内
2.自然界中不同价态的硫之间的转化。 请在下边的横线上填上相应的物质的化学式。
H2SO3
SO3
H2SO4
FeS2 HgS
As4S4 As2S3
结论 硫表 现_氧__ _化__性
硫表 现_还__ _原__性
【微点拨】硫在空气、氧气中燃烧火焰颜色不同,但产物相同。
4.用途:主要用于制造硫酸、化肥、火柴、杀虫剂等,还用于制造火药 (如以_硫__黄__、__硝__石__和__木__炭__为主要成分的黑火药)、烟花爆竹等。
【自我小测】 1.思考辨析: (1)硫黄是一种硬度很大的淡黄色固体。 ( ) 分析:×。硫黄是一种很脆的淡黄色固体。 (2)硫是黑火药的主要成分之一。 ( ) 分析:√。黑火药的主要成分是硫、木炭和硝酸钾。
铜丝在硫蒸气中燃烧, 生成黑色固体
混合即发生反应,生成 硫化汞
反应方程式
结论
△
_F_e_+_S__=_=_=_=__F_e_S_
△
2Cu+S ==== Cu2S
Hg+S====HgS
硫表现 _氧__化__性
【微点拨】(1)硫与汞常温下即可化合生成高价汞硫化物。 (2)硫与铁、铜等变价金属反应生成低价态金属硫化物,而不是高价态 金属硫化物。
【微点拨】除去试管内壁附着硫黄的方法是用CS2溶解或用热的碱液
清洗(3S+6NaOH
△
====
2Na2S+Na2SO3+3H2O)。
3.化学性质:
(1)与金属的反应。
反应物 与铁
与铜 与汞
实验现象
混合物用灼热的玻璃棒加 热后保持_红__热__状态,移开 玻璃棒后仍呈_红__热__状态, 生成_黑__色固体
B.硫在氧气中燃烧 D.硫与钠反应
【解析】选B。硫溶于CS2属于物理变化;硫与铁、钠的反应中硫作氧 化剂。
硫单质的氧化性和还原性 思考探究: 自然界中的含硫物质种类很多,天然矿物有硫黄、黄铁矿、雄黄、石 膏,还有氢化物、氧化物等气体。 (1)上述含硫物质中硫元素的化合价是多少? (2)从化合价的角度分析,硫单质应该具有怎样的性质?
CaSO4·2H2O Na2SO4·10H2O
二、硫单质 1.硫元素的同素异形体:常见同素异形体有_斜__方__硫和_单__斜__硫。
2.物理性质:
俗称 颜色 状态 硬度 水
_黄__色__或__
硫黄
固体 脆
_淡__黄__色__
_不__溶__
溶解度 酒精
_微__溶__
CS2 _易__溶__
熔沸点 较低
(3)硫在化学反应中只能作氧化剂。 ( ) 分析:×。硫与氧气反应时表现还原性。 (4)铜丝在硫蒸气中燃烧生成CuS。 ( ) 分析:×。硫与铜反应生成Cu2S。
2.洗涤试管上附着的硫黄,可以选用的方法是 ( )
A.加水洗涤
B.通氧气加热
C.加热试管使硫熔化
D.用CS2洗涤
【解析】选D。由于硫易溶于CS2,所以可以用CS2洗涤。
【解析】选A。硫是一种淡黄色固体,不溶于水,微溶于酒精,易溶于二 硫化碳。雄黄、辰砂、石膏都是含硫物质。自然界中硫元素广泛存在 于海洋、大气和地壳中,也存在于动植物体内,火山喷发时,地壳中的 硫元素会随之进入大气和水中。
5.(LK必修1·P93改编)下列各过程中硫表现出还原性的是( )
A.硫溶于CS2 C.硫粉与铁粉混合加热
【归纳总结】 硫单质的氧化性和还原性 硫元素的常见化合价有-2、0、+2、+4、+6,硫单质中硫元素化合价 为0,在氧化还原反应中化合价既能降低又能升高,硫单质既有氧化性 又有还原性。 1.表现还原性:当硫与氧化性较强的物质(如氧气等)反应时,失电子,
化合价升高,被氧化,表现一定的还原性,如S+O2 =点=燃== SO2。
2.表现氧化性:硫与还原性较强的物质(如金属、氢气等)反应时,得电
子,化合价降低,被还原,表现氧化性。
(1)金属单质:S+Fe
△
====
FeS,S+2Cu
△
====
Cu2S,
硫与变价金属反应时生成低价态金属硫化物。
(2)氢气:S+H2
△
====
H2S。
(3)在黑火药爆炸的反应中,硫的化合价降低,表现氧化性,化学方程式
3.在自然界中只以化合态形式存在的元素是 ( )
A.氯
B.碳
C.氮
D.硫
【解析】选A。氯是非常活泼的元素,在自然界中只以化合态形式存在。
4.下列说法不正确的是 ( ) A.硫是一种淡黄色能溶于水的固体 B.硫的化合物常存在于火山喷出的气体中和矿泉水里 C.雄黄、辰砂、石膏中均含有硫元素 D.一些动植物体内也含有硫元素
【典题训练】(2015·宿州高一检测)在如图所
示的转化关系中,已知B、D都是淡黄色固体,D
与G的浓溶液在一定条件下反应生成E,回答下列问题:
(1)写出下列物质的化学式:
A
;F
;H
。
(2)D与热的C溶液反应时氧化产物与还原产物的物质的量之比为1∶2,
试写出其离子方程式:
。
【解题指南】解答本题需注意以下3点: (1)中学阶段淡黄色固体为Na2O2、单质硫和AgBr; (2)B为A与氧气反应的产物,则B为含氧化合物; (3)D与NaOH溶液反应时化合价升降应保持一致。
(2)与非金属的反应。
反应物
实验现象
加热条件下,硫可以与氢 与氢气
气化合生成H2S
与空气
硫在空气中燃烧,发出 微弱的淡_蓝__色火焰,有 无色_刺__激__性__气体生成
硫在氧气中剧烈燃烧,发 与氧气 出明亮的_蓝__紫__ 色火焰
反应方程式
_H_2+_S__=_=_△=_=__H_2_S_
_S_+_O_2_=点_=_燃=_=__S_O_2
为S+2KNO3+3C =点=燃== K2S+3CO2↑+N2↑。
3.既表现氧化性又表现还原性:硫与热的碱溶液反应时,既表现氧化性,
又表现还原性,如3S+6NaOH
△
====
2Na2S+Na2SO3+3H2O。
【点拨】硫单质的弱氧化性 (1)硫单质表现氧化性时,其氧化性较弱,所以与变价金属反应的时候, 通常生成的是低价态金属硫化物。 (2)与硫相比较,氯气具有较强氧化性,其在与变价金属发生反应时,生 成的是高价态金属氯化物。 (3)实验室中一旦有汞洒落,可在洒落的汞上面撒上硫粉,使汞与硫化 合生成硫化汞后再处理,此方法就是体现了硫的氧化性。
一、自然界中的硫 1.硫的存在:
存在形态
游离态
_化__合__态
如_硫__黄__
ቤተ መጻሕፍቲ ባይዱ
如硫酸钠
存在范围 海洋、大气、地壳、
动植物体内
2.自然界中不同价态的硫之间的转化。 请在下边的横线上填上相应的物质的化学式。
H2SO3
SO3
H2SO4
FeS2 HgS
As4S4 As2S3
结论 硫表 现_氧__ _化__性
硫表 现_还__ _原__性
【微点拨】硫在空气、氧气中燃烧火焰颜色不同,但产物相同。
4.用途:主要用于制造硫酸、化肥、火柴、杀虫剂等,还用于制造火药 (如以_硫__黄__、__硝__石__和__木__炭__为主要成分的黑火药)、烟花爆竹等。
【自我小测】 1.思考辨析: (1)硫黄是一种硬度很大的淡黄色固体。 ( ) 分析:×。硫黄是一种很脆的淡黄色固体。 (2)硫是黑火药的主要成分之一。 ( ) 分析:√。黑火药的主要成分是硫、木炭和硝酸钾。
铜丝在硫蒸气中燃烧, 生成黑色固体
混合即发生反应,生成 硫化汞
反应方程式
结论
△
_F_e_+_S__=_=_=_=__F_e_S_
△
2Cu+S ==== Cu2S
Hg+S====HgS
硫表现 _氧__化__性
【微点拨】(1)硫与汞常温下即可化合生成高价汞硫化物。 (2)硫与铁、铜等变价金属反应生成低价态金属硫化物,而不是高价态 金属硫化物。
【微点拨】除去试管内壁附着硫黄的方法是用CS2溶解或用热的碱液
清洗(3S+6NaOH
△
====
2Na2S+Na2SO3+3H2O)。
3.化学性质:
(1)与金属的反应。
反应物 与铁
与铜 与汞
实验现象
混合物用灼热的玻璃棒加 热后保持_红__热__状态,移开 玻璃棒后仍呈_红__热__状态, 生成_黑__色固体
B.硫在氧气中燃烧 D.硫与钠反应
【解析】选B。硫溶于CS2属于物理变化;硫与铁、钠的反应中硫作氧 化剂。
硫单质的氧化性和还原性 思考探究: 自然界中的含硫物质种类很多,天然矿物有硫黄、黄铁矿、雄黄、石 膏,还有氢化物、氧化物等气体。 (1)上述含硫物质中硫元素的化合价是多少? (2)从化合价的角度分析,硫单质应该具有怎样的性质?
CaSO4·2H2O Na2SO4·10H2O
二、硫单质 1.硫元素的同素异形体:常见同素异形体有_斜__方__硫和_单__斜__硫。
2.物理性质:
俗称 颜色 状态 硬度 水
_黄__色__或__
硫黄
固体 脆
_淡__黄__色__
_不__溶__
溶解度 酒精
_微__溶__
CS2 _易__溶__
熔沸点 较低
(3)硫在化学反应中只能作氧化剂。 ( ) 分析:×。硫与氧气反应时表现还原性。 (4)铜丝在硫蒸气中燃烧生成CuS。 ( ) 分析:×。硫与铜反应生成Cu2S。
2.洗涤试管上附着的硫黄,可以选用的方法是 ( )
A.加水洗涤
B.通氧气加热
C.加热试管使硫熔化
D.用CS2洗涤
【解析】选D。由于硫易溶于CS2,所以可以用CS2洗涤。
【解析】选A。硫是一种淡黄色固体,不溶于水,微溶于酒精,易溶于二 硫化碳。雄黄、辰砂、石膏都是含硫物质。自然界中硫元素广泛存在 于海洋、大气和地壳中,也存在于动植物体内,火山喷发时,地壳中的 硫元素会随之进入大气和水中。
5.(LK必修1·P93改编)下列各过程中硫表现出还原性的是( )
A.硫溶于CS2 C.硫粉与铁粉混合加热
【归纳总结】 硫单质的氧化性和还原性 硫元素的常见化合价有-2、0、+2、+4、+6,硫单质中硫元素化合价 为0,在氧化还原反应中化合价既能降低又能升高,硫单质既有氧化性 又有还原性。 1.表现还原性:当硫与氧化性较强的物质(如氧气等)反应时,失电子,
化合价升高,被氧化,表现一定的还原性,如S+O2 =点=燃== SO2。
2.表现氧化性:硫与还原性较强的物质(如金属、氢气等)反应时,得电
子,化合价降低,被还原,表现氧化性。
(1)金属单质:S+Fe
△
====
FeS,S+2Cu
△
====
Cu2S,
硫与变价金属反应时生成低价态金属硫化物。
(2)氢气:S+H2
△
====
H2S。
(3)在黑火药爆炸的反应中,硫的化合价降低,表现氧化性,化学方程式
3.在自然界中只以化合态形式存在的元素是 ( )
A.氯
B.碳
C.氮
D.硫
【解析】选A。氯是非常活泼的元素,在自然界中只以化合态形式存在。
4.下列说法不正确的是 ( ) A.硫是一种淡黄色能溶于水的固体 B.硫的化合物常存在于火山喷出的气体中和矿泉水里 C.雄黄、辰砂、石膏中均含有硫元素 D.一些动植物体内也含有硫元素
【典题训练】(2015·宿州高一检测)在如图所
示的转化关系中,已知B、D都是淡黄色固体,D
与G的浓溶液在一定条件下反应生成E,回答下列问题:
(1)写出下列物质的化学式:
A
;F
;H
。
(2)D与热的C溶液反应时氧化产物与还原产物的物质的量之比为1∶2,
试写出其离子方程式:
。
【解题指南】解答本题需注意以下3点: (1)中学阶段淡黄色固体为Na2O2、单质硫和AgBr; (2)B为A与氧气反应的产物,则B为含氧化合物; (3)D与NaOH溶液反应时化合价升降应保持一致。
(2)与非金属的反应。
反应物
实验现象
加热条件下,硫可以与氢 与氢气
气化合生成H2S
与空气
硫在空气中燃烧,发出 微弱的淡_蓝__色火焰,有 无色_刺__激__性__气体生成
硫在氧气中剧烈燃烧,发 与氧气 出明亮的_蓝__紫__ 色火焰
反应方程式
_H_2+_S__=_=_△=_=__H_2_S_
_S_+_O_2_=点_=_燃=_=__S_O_2
为S+2KNO3+3C =点=燃== K2S+3CO2↑+N2↑。
3.既表现氧化性又表现还原性:硫与热的碱溶液反应时,既表现氧化性,
又表现还原性,如3S+6NaOH
△
====
2Na2S+Na2SO3+3H2O。
【点拨】硫单质的弱氧化性 (1)硫单质表现氧化性时,其氧化性较弱,所以与变价金属反应的时候, 通常生成的是低价态金属硫化物。 (2)与硫相比较,氯气具有较强氧化性,其在与变价金属发生反应时,生 成的是高价态金属氯化物。 (3)实验室中一旦有汞洒落,可在洒落的汞上面撒上硫粉,使汞与硫化 合生成硫化汞后再处理,此方法就是体现了硫的氧化性。
