初中化学必背知识点:常见物质的化学式及俗名(表格版)
初中化学俗名(打印版)

初中化学俗名
1、食盐:主要成分:氯化钠,化学式NaCl
2、二氧化碳固体:化学式CO2,俗称干冰
3、氧化钙:化学式CaO,俗称生石灰
4、氢氧化钙:化学式Ca(OH)2,俗称熟石灰、消石灰
氢氧化钙溶液:俗称石灰水,主要成分Ca(OH)2
5、甲烷:化学式CH4,俗称天然气,瓦斯气、沼气的主要成分
6、乙醇:化学式C2H5OH ,俗称酒精
7、汞:化学式Hg,俗称水银
8、过氧化氢:化学式H2O2,俗称双氧水
9、硫酸铜晶体:化学式CuSO4•5H2O,俗称胆矾、蓝矾
10、氢氧化钠:化学式NaOH,俗称火碱、烧碱、苛性钠
11、大理石、石灰石的主要成分:CaCO3
12、氢氯酸(HCl):盐酸(氯化氢气体溶于水所得的溶液),学名:氢氯酸
13、天然气、沼气、瓦斯气的主要成分:甲烷(CH4)
14、碳酸钠:化学式:Na2CO3,俗称纯碱、苏打
15、碳酸氢钠:化学式:NaHCO3,俗称小苏打。
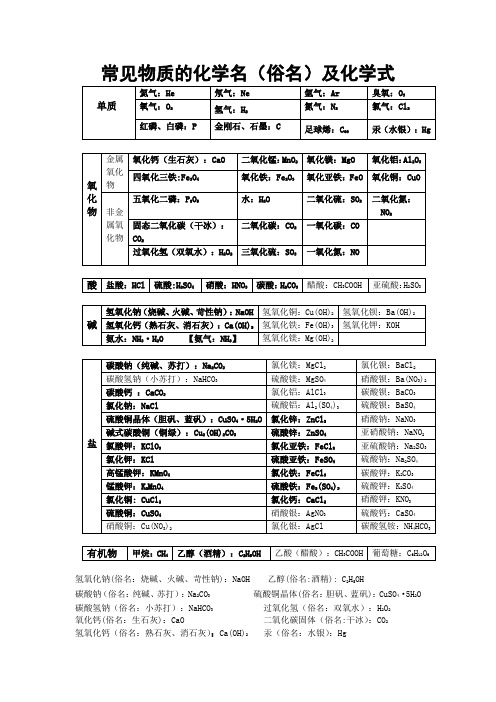
常见物质的化学名(俗名)及化学式
碱
氢氧化钠(烧碱、火碱、苛性钠):NaOH
氢氧化铜:Cu(OH)2
氢氧化钡:Ba(OH)2
氢氧化钙(熟石灰、消石灰):Ca(OH)2
氢氧化铁:Fe(OH)3
氢氧化钾:KOH
氨水:NH3·H2O【氨气:NH3】
氢氧化镁:Mg(OH)2
盐
碳酸钠(纯碱、苏打):Na2CO3
氯化镁:MgCl2
氧化亚铁:FeO
氧化铜:CuO
非金属氧化物
五氧化二磷:P化氮:NO2
固态二氧化碳(干冰):CO2
二氧化碳:CO2
一氧化碳:CO
过氧化氢(双氧水):H2O2
三氧化硫:SO3
一氧化氮:NO
酸
盐酸:HCl
硫酸:H2SO4
硝酸:HNO3
碳酸:H2CO3
醋酸:CH3COOH
硝酸钾:KNO3
硫酸铜:CuSO4
硝酸银:AgNO3
硫酸钙:CaSO4
硝酸铜:Cu(NO3)2
氯化银:AgCl
碳酸氢铵:NH4HCO3
有机物
甲烷:CH4
乙醇(酒精):C2H5OH
乙酸(醋酸):CH3COOH
葡萄糖:C6H12O6
氢氧化钠(俗名:烧碱、火碱、苛性钠):NaOH乙醇(俗名:酒精):C2H5OH
氯化钡:BaCl2
碳酸氢钠(小苏打):NaHCO3
硫酸镁:MgSO4
硝酸钡:Ba(NO3)2
碳酸钙:CaCO3
氯化铝:AlCl3
碳酸钡:BaCO3
氯化钠:NaCl
硫酸铝:Al2(SO4)3
硫酸钡:BaSO4
硫酸铜晶体(胆矾、蓝矾):CuSO4·5H2O
氯化锌:ZnCl2
初中化学物质俗称大全

初中化学物质俗称大全
小苏打、重曹
1.食盐是由氯化钠组成,化学式为NaCl。
二氧化碳固体
化学式为CO2,俗称干冰。
2.氧化钙的化学式为CaO,俗称生石灰。
3.氢氧化钙的化学式为Ca(OH)2,俗称熟石灰或消石灰。
它的溶液俗称石灰水,主要成分为Ca(OH)2.
4.甲烷的化学式为CH4,俗称天然气、瓦斯气或沼气。
5.乙醇的化学式为C2H5OH,俗称酒精。
6.汞的化学式为Hg,俗称水银。
7.过氧化氢的化学式为H2O2,俗称双氧水。
8.硫酸铜晶体的化学式为CuSO4·5H2O,俗称胆矾或蓝矾。
9.氢氧化钠的化学式为NaOH,俗称火碱、烧碱或苛性钠。
10.大理石和石灰石的主要成分为CaCO3.
11.氢氯酸(盐酸)是氯化氢气体溶于水所得的溶液,化
学式为HCl。
12.碳酸钠的化学式为Na2CO3,俗称纯碱或XXX。
13.碳酸氢钠的化学式为NaHCO3,俗称小苏打或重曹。
(完整版)初中化学必背知识点总结

初中化学知识总结一、物质的学名、俗名及化学式⑴金刚石、石墨:C⑵水银、汞:Hg (3)生石灰、氧化钙:CaO(4)干冰(固体二氧化碳):CO2(5)盐酸、氢氯酸:HCl(6)亚硫酸:H2SO3 (7)氢硫酸:H2S (8)熟石灰、消石灰:Ca(OH)2 (9)苛性钠、火碱、烧碱:NaOH (10)纯碱:Na2CO3碳酸钠晶体、纯碱晶体:Na2CO3·10H2O (11)碳酸氢钠、酸式碳酸钠:NaHCO3(也叫小苏打)(12)胆矾、蓝矾、硫酸铜晶体:CuSO4·5H2O (13)铜绿、孔雀石:Cu2(OH)2CO3(分解生成三种氧化物的物质)(14)甲醇:CH3OH 有毒、失明、死亡(15)酒精、乙醇:C2H5OH (16)醋酸、乙酸(16.6℃冰醋酸)CH3COOH(CH3COO-醋酸根离子)具有酸的通性(17)氨气:NH3(碱性气体)(18)氨水、一水合氨:NH3·H2O(为常见的碱,具有碱的通性,是一种不含金属离子的碱)(19)亚硝酸钠:NaNO2(工业用盐、有毒)二、常见物质的颜色的状态1、白色固体:MgO、P2O5、CaO、NaOH、Ca(OH)2、KClO3、KCl、Na2CO3、NaCl、无水CuSO4;铁、镁为银白色(汞为银白色液态)2、黑色固体:石墨、炭粉、铁粉、CuO、MnO2、Fe3O4▲KMnO4为紫黑色3、红色固体:Cu、Fe2O3、HgO、红磷▲硫:淡黄色▲Cu2(OH)2CO3为绿色4、溶液的颜色:凡含Cu2+的溶液呈蓝色;凡含Fe2+的溶液呈浅绿色;凡含Fe3+的溶液呈棕黄色,其余溶液一般不无色。
(高锰酸钾溶液为紫红色)5、沉淀(即不溶于水的盐和碱):①盐:白色↓:CaCO3、BaCO3(溶于酸)AgCl、BaSO4(也不溶于稀HNO3) 等②碱:蓝色↓:Cu(OH)2红褐色↓:Fe(OH)3白色↓:其余碱。
6、(1)具有刺激性气体的气体:NH3、SO2、HCl(皆为无色)(2)无色无味的气体:O2、H2、N2、CO2、CH4、CO(剧毒)▲注意:具有刺激性气味的液体:盐酸、硝酸、醋酸。
九年级上册化学必须记住的化学式和化学方程式

九年级上册化学必须记住的化学式一、单质的化学式:25个1、气态非金属单质:氧气O2、氮气N2、氢气H2、氯气Cl22、固态非金属单质:碳C 、磷P、硫S、硅Si3、稀有气体单质:氦He、氖Ne、氩Ar4、金属单质:铁Fe、铜Cu、锌Zn、铝Al、银Ag、镁Mg、钡Ba、铂Pt、金Au、汞Hg、钾K、钙Ca、锰Mn、钠Na 二、化合物的化学式:37个1、氧化物:水H2O、二氧化碳CO2、过氧化氢H2O2、二氧化锰MnO2、一氧化碳CO、二氧化硫SO2、二氧化氮NO2、氧化铜CuO、氧化铁Fe2O3、四氧化三铁Fe3O4、氧化镁MgO、氧化钙CaO、一氧化碳CO、五氧化二磷P2O5、氧化铝Al2O3、二氧化硅SiO2、氧化汞HgO、氧化亚铜Cu2O、氨气NH32、酸:硫酸H2SO4、碳酸H2CO3、盐酸HCl、硝酸HNO33、碱:氢氧化钠NaOH、氢氧化钙CaOH2、氢氧化钾KOH4、盐:氯化钠NaCl、氯化钾KCl、硫酸铜CuSO4、碳酸钠Na2CO3、氯酸钾KClO3、高锰酸钾KMnO4、锰酸钾K2MnO4、碳酸钙CaCO3、硫酸亚铁FeSO4、硫酸铁Fe2SO435、有机物:甲烷CH4、乙醇俗名酒精C2H5OH九年级上册化学必须记住的化学方程式34个1、镁燃烧:2Mg+O 2 2MgO2、铁燃烧:3Fe+2O 2Fe 3O 43、铝燃烧:4Al+3O 22Al 2O 34、氢气燃烧:2H 2+O 22H 2O 淡蓝色火焰5、红磷燃烧:4P+5O 22P 2O 56、硫粉燃烧: S+O 2SO 27、碳充分燃烧:C+O 2CO 2 8、碳不充分燃烧:2C+O 22CO9、二氧化碳通过灼热碳层: C+CO 22CO 10、一氧化碳燃烧:2CO+O 22CO 211、二氧化碳和水反应二氧化碳通入紫色石蕊试液:CO 2+H 2O==H 2CO 3溶液变红 12、生石灰溶于水:CaO+H 2O==CaOH 2 13、无水硫酸铜作干燥剂:CuSO 4+5H 2O==CuSO 4·5H 2O 14、实验室用双氧水制氧气:2H 2O 22H 2O+O 2↑15、加热高锰酸钾:2KMnO 4 K 2MnO 4+MnO 2+O 2↑ 16、水在直流电的作用下分解:2H 2O2H 2↑+O 2↑ 17、碳酸不稳定而分解:H 2CO 3==H 2O+CO 2↑ 18、高温煅烧石灰石二氧化碳工业制法:CaCO 3CaO+CO 2↑ 19、铁和硫酸铜溶液反应:Fe+CuSO 4==FeSO 4+Cu 湿法炼铜的反应原理 20、锌和稀硫酸反应实验室制氢气:Zn+H 2SO 4==ZnSO 4+H 2↑ 21、镁和稀盐酸反应:Mg+2HCl==MgCl 2+H 2↑ 22、氢气还原氧化铜:H 2+CuO Cu+H 2O 23、木炭还原氧化铜:C+2CuO2Cu+CO 2↑ 24、水蒸气通过灼热碳层:H 2O+CH 2+CO 水煤气 25、焦炭还原氧化铁:3C+2Fe 2O 34Fe+3CO 2↑26、氢氧化钠溶液与硫酸铜溶液反应:2NaOH+CuSO 4==CuOH 2↓+Na 2SO 4蓝色沉淀 27、甲烷在空气中燃烧:CH 4+2O 2CO 2+2H 2O 蓝色火焰 28、酒精在空气中燃烧:C 2H 5OH+3O 2 2CO 2+3H 2O 29、一氧化碳还原氧化铜:CO+CuOCu+CO 230、一氧化碳还原氧化铁:3CO+Fe 2O 3 2Fe+3CO 231、二氧化碳通过澄清石灰水检验二氧化碳:CaOH 2+CO 2==CaCO 3↓+H 2O 变浑浊 32、氢氧化钠和二氧化碳反应除去二氧化碳:2NaOH+CO 2==Na 2CO 3+H 2O 33、石灰石或大理石与稀盐酸反应二氧化碳的实验室制法:CaCO 3+2HCl==CaCl 2+H 2O+CO 2↑34、碳酸钠与浓盐酸反应泡沫灭火器的原理: Na 2CO 3+2HCl==2NaCl+H 2O+CO 2↑。
(2021年整理)初中化学常见物质化学式(表格)

初中化学常见物质化学式(表格)
编辑整理:
尊敬的读者朋友们:
这里是精品文档编辑中心,本文档内容是由我和我的同事精心编辑整理后发布的,发布之前我们对文中内容进行仔细校对,但是难免会有疏漏的地方,但是任然希望(初中化学常见物质化学式(表格))的内容能够给您的工作和学习带来便利。
同时也真诚的希望收到您的建议和反馈,这将是我们进步的源泉,前进的动力。
本文可编辑可修改,如果觉得对您有帮助请收藏以便随时查阅,最后祝您生活愉快业绩进步,以下为初中化学常见物质化学式(表格)的全部内容。
初中常见物质化学式一、常见单质化学式
2、其他化合物。
初中常见物质的化学式及其化学方程式(精编版)

初中常见物质的化学式一、化学式的含义:
化学式是用元素符号来表示物质组成的式子。
二、初中常见物质的化学式:
1、非金属单质
2、金属单质
3、常见氧化物
4、氯化物/盐酸盐
5、常见的酸
6、常见的盐
7、常见的碱
8、常见有机物
9、常见结晶水合物
10、常见化肥
11、沉淀
初中化学方程式汇总
一、氧气的性质:
1、单质与氧气的反应:(化合反应)
2、化合物与氧气的反应:
3、氧气的来源:
二、自然界中的水:
三、质量守恒定律:
四、碳和碳的氧化物:
1、碳的化学性质
2、煤炉中发生的三个反应:(几个化合反应)
3、二氧化碳的制法与性质:
4、一氧化碳的性质:
5、其它反应:
五、燃料及其利用:
六、金属
1、金属与氧气反应:
2、金属单质+ 酸=盐+ 氢气(置换反应)
3、金属单质+ 盐(溶液)=新金属+ 新盐
4、金属铁的治炼原理:3CO+ 2Fe2O3−
−高温4Fe + 3CO2↑
−→
七、酸、碱、盐
1、酸的化学性质
⑴酸+ 金属=盐+ 氢气(见上)
⑵酸+ 金属氧化物=盐+ 水
⑶酸+ 碱=盐+ 水(中和反应)
⑷酸+ 盐=另一种酸+ 另一种盐
2、碱的化学性质
⑴碱+ 非金属氧化物=盐+ 水
⑵碱+ 酸=盐+ 水(中和反应,方程式见上)
⑶碱+ 盐=另一种碱+ 另一种盐
3、盐的化学性质
⑴盐(溶液) + 金属单质=另一种金属+ 另一种盐
⑵盐+ 酸=另一种酸+ 另一种盐
⑶盐+ 碱=另一种碱+ 另一种盐
⑷盐+ 盐=两种新盐。
初中化学必背化学式大全

3.常见物质化学式与名称:单质:C:碳S:硫P:磷Fe:铁Mg:镁Al:铝Hg:汞Zn:锌Cu:铜Ag:银O2:氧气H2:氢气N2:氮气O3:臭氧氧化物:CO:一氧化碳CO2:二氧化碳SO2:二氧化硫MnO2:二氧化锰SO3:三氧化硫H2O2:过氧化氢CuO:氧化铜CaO:氧化钙MgO:氧化镁HgO:氧化汞Fe2O3:氧化铁Al2O3:氧化铝H2O:水P2O5:五氧化二磷Fe3O4:四氧化三铁HCl:盐酸H2SO4:硫酸NaCl:氯化钠KMnO4:高锰酸钾K2MnO4:锰酸钾KClO3:氯酸钾九年级化学方程式分类:1.碳充分燃烧:C+O 2点燃CO22.碳不充分燃烧: 2C+O2点燃2CO3.一氧化碳燃烧: 2CO+O2点燃2CO24.产生一氧化碳: C+CO2高温2CO5.硫燃烧:S+O2点燃SO26.红磷燃烧:4P+5O2点燃2P2O57.氢气燃烧:2H2+O2点燃2H2O8.铁燃烧:3Fe+2O2点燃Fe3O49.镁燃烧:2Mg+O2点燃2MgO10.铝燃烧:4Al+3O2点燃2Al2O311.甲烷燃烧:CH4+2O2点燃CO2+2H2O12.酒精燃烧:C2H5OH+3O2点燃2CO2+3H2O13.呼吸原理:C6H12O6+6O26CO2+6H2O14.高锰酸钾制氧气: 2KMnO4△K2MnO4+MnO2+O2↑15.氯酸钾制氧气:2KClO3MnO22KCl+3O2↑△16.过氧化氢制氧气: 2H2O2 MnO22H2O +O2↑17.水通电分解:2H2O2H2↑+O2↑18.氧化汞分解:2HgO△2Hg+O2↑19.实验室制氢气原理:Zn+H2SO4=ZnSO4+H2↑20.镁或硫酸性质:Mg+H2SO4=MgSO4+H2↑21.铁或硫酸性质:Fe+H2SO4=FeSO4+H2↑22.铝或硫酸性质:2Al+3H2SO4=Al2(SO4)3+H2↑23.镁或盐酸性质:Mg+2HCl=MgCl2+H2↑24.锌或盐酸性质:Zn+2HCl=ZnCl2+H2↑25.铁或盐酸性质:Fe+2HCl=FeCl2+H2↑26.铝或盐酸性质:2Al+6HCl=2AlCl3+3H2↑27.酸或碱性质:NaOH+HCl=NaCl+H2O28.酸或碱性质:Ca(OH)2+2HCl=CaCl2+H2O29.酸或碱性质:2NaOH+H2SO4=Na2SO4+2H2O30.酸或碱性质:Ca(OH)2+H2SO4=CaSO4+2H2O30.除铁锈原理或金属氧化物与酸性质:Fe2O3+6HCl=2FeCl3+3H2OFe2O3+3H2SO4=Fe2(SO4)3+3H2O31.制取CO2或CaCO3 作补钙药剂:CaCO3+2HCl=CaCl2+CO2↑+H2O32.碳酸盐或酸性质:Na2CO3+2HCl=2NaCl+CO2↑+H2O33.治疗胃酸过多症原理:NaHCO3 +HCl=NaCl+CO2↑+H2O34.氯化钠与硝酸银反应产生白色沉淀:NaCl+AgNO3=NaNO3+AgCl↓35.制取氢氧化钠原理:Ca(OH)2+Na2CO3=CaCO3↓+2NaOH36.氢氧化钠与硫酸铜反应产生蓝色沉淀:2NaOH+CuSO4=Na2SO4+Cu(OH)237.制取水煤气原理:C+H2O高温H2+CO38.氢气还原氧化铜:H2+CuO△Cu+H2O39.碳还原氧化铜:C+2CuO高温2Cu+CO2↑40.一氧化碳还原氧化铜:CO+CuO△Cu+CO241.氢气还原氧化铁:Fe2O3+3H2高温2Fe+3H2O42.碳还原氧化铁:2Fe2O3+3C高温4Fe+3CO2↑43.工业炼铁原理:Fe2O3+3CO高温2Fe+3CO244.铁置换硫酸铜中铜:Fe+CuSO4=Cu+FeSO445.铜置换硝酸银中银:Cu+2AgNO3=2Ag+Cu(NO3)246.铝置换硫酸铜中铜:2Al+3CuSO4=3Cu+Al2(SO4)347.生石灰制熟石灰:H2O+CaO=Ca(OH)248.碳酸不稳定:H2CO3=H2O+CO2↑49.工业制生石灰原理:CaCO高温CaO+CO2↑50.检验CO2或澄清石灰水变浑浊原理:CO2+Ca(OH)2=CaCO3↓+H2O51.烧碱变质原理:CO2+2NaOH=Na2CO3+H2O52.碱与非金属氧化物性质:SO2+2NaOH=Na2SO3+H2O SO3+2NaOH=Na2SO4+H2O 53.非金属氧化物性质:H2O+CO2 =H2CO3H2O+SO2 =H2SO3H2O+SO3 =H2SO4 1.书写元素符号:氢氦碳氮氧氟氖钠镁铝硅磷硫氯氩钾钙锰铁铜锌银钡铂金汞2.书写常见离子和化合物中元素化合价:氢离子钙离子镁离子钠离子钾离子铁离子银离子铜离子钡离子铝离子锌离子钾离子氢氧根离子硫酸根离子硝酸根离子氯离子碳酸根离子铵根离子亚铁离子3.用化学式表示下面常见物质:单质:碳硫磷铁镁铝汞锌铜银氧气氧气氮气臭氧氧化物:水一氧化碳二氧化碳二氧化硫二氧化锰三氧化硫过氧化氢氧化铜氧化钙氧化镁氧化汞氧化铁氧化铝五氧化二磷四氧化三铁酸:盐酸硫酸硝酸碳酸亚硫酸醋酸碱:氢氧化钠氢氧化钙氢氧化钾氢氧化镁氢氧化铜氢氧化铁氨水盐酸盐:氯化钾氯化钠氯化钾氯化银氯化铜氯化钙氯化镁氯化锌氯化钡氯化铝氯化铁氯化亚铁碳酸盐:碳酸钙碳酸钠碳酸氢钠碳酸钡碳酸钾碳酸氢铵硫酸盐:硫酸钠硫酸锌硫酸镁硫酸钙硫酸铜硫酸钡硫酸亚铁硫酸铁硫酸铝硫酸铵亚硫酸钠硝酸盐:硝酸银硝酸钠硝酸铜硝酸钾硝酸铵亚硝酸钠钾盐高锰酸钾锰酸钾氯酸钾有机化合物:乙醇葡萄糖甲烷书写化学方程式:1.碳充分燃烧:2.碳不充分燃烧:3.一氧化碳燃烧:4.碳和二氧化碳反应:5.硫燃烧:6.红磷燃烧:7.氢气燃烧:8.铁燃烧:9.镁燃烧:10.铝燃烧:11.甲烷燃烧:12.酒精燃烧:13.呼吸原理:14.高锰酸钾制氧气:15.氯酸钾制氧气:16.过氧化氢制氧气:17.水通电分解:18.氧化汞分解:19.实验室制氢气原理:20.镁和硫酸反应:21.铁和硫酸反应:22.铝和硫酸反应:23.镁和盐酸反应:24.锌和盐酸反应:25.铁和盐酸反应:26.铝和盐酸反应:27.盐酸和氢氧化钠反应:28.盐酸和氢氧化钙反应:29.硫酸和氢氧化钠反应:30.硫酸和氢氧化钙反应:30.盐酸或硫酸除铁锈原理:31.实验室制CO2或CaCO3 作补钙药剂:32.碳酸钠或盐酸酸反应:33.治疗胃酸过多症原理:34.氯化钠与硝酸银反应产生白色沉淀:35.制取氢氧化钠原理:36.氢氧化钠与硫酸铜反应产生蓝色沉淀:37.制取水煤气原理:38.氢气还原氧化铜:39.碳还原氧化铜:40.一氧化碳还原氧化铜:41.氢气还原氧化铁:42.碳还原氧化铁:43.工业炼铁原理:44.铁置换硫酸铜中铜:45.铜置换硝酸银中银:46.铝置换硫酸铜中铜:47.生石灰制熟石灰:48.碳酸不稳定:49.工业制生石灰原理:50.检验CO2或澄清石灰水变浑浊原理:51.烧碱变质原理:52.氢氧化钠与非金属氧化物(SO2、SO3)反应:53.水与非金属氧化物(CO2、SO2)反应:。
初中化学常见物质俗名、物质颜色

一、物质的学名、俗名及化学式⑴金刚石、石墨:C⑵水银、汞:Hg(3)生石灰、氧化钙:CaO(4)干冰(固体二氧化碳):CO2(5)盐酸、氢氯酸:HCl(8)熟石灰、消石灰:Ca(OH)2(9)苛性钠、火碱、烧碱:NaOH(10)纯碱:Na2CO3(11)碳酸氢钠:小苏打NaHCO3(12)胆矾、蓝矾、硫酸铜晶体:CuSO45H2O(13)铜绿、孔雀石:Cu2(OH)2CO3(分解生成三种氧化物的物质)(14)甲醇:CH3OH 有毒、失明、死亡(15)酒精、乙醇:C2H5OH(16)醋酸、乙酸CH3COOH 具有酸的通性(17)氨气:NH3(碱性气体)(18)氨水:NH3H2O(19)亚硝酸钠:NaNO2(工业用盐、有毒)二、常见物质的颜色的状态1、白色固体:MgO、P2O5、CaO、 NaOH、Ca(OH)2、KClO3、KCl、Na2CO3、NaCl、无水CuSO4;铁、镁为银白色(汞为银白色液态)2、黑色固体:石墨、炭粉、铁粉、CuO、MnO2、Fe3O4,KMnO4为紫黑色3、红色固体:Cu、Fe2O3、HgO、红磷。
硫:淡黄色,Cu2(OH)2CO3为绿色4、溶液的颜色:凡含Cu2+的溶液呈蓝色;凡含Fe2+的溶液呈浅绿色;凡含Fe3+ 的溶液呈棕黄色,高锰酸钾溶液为紫红色,其余溶液一般为无色。
5、沉淀(即不溶于水的盐和碱):①盐:白色↓:CaCO3、BaCO3(溶于酸) AgCl、BaSO4(也不溶于稀HNO3) 等②碱:蓝色↓:Cu(OH)2红褐色↓:Fe(OH)3白色↓:其余碱。
6、(1)具有刺激性气体的气体:NH3、SO2、HCl(皆为无色)(2)无色无味的气体:O2、H2、N2、CO2、CH4、CO(剧毒)▲注意:具有刺激性气味的液体:盐酸、硝酸、醋酸。
酒精为有特殊气体的液体。
7、有毒的,气体:CO 液体:CH3OH 固体:NaNO2 CuSO4(可作杀菌剂 ,与熟石灰混合配成天蓝色的粘稠状物质——波尔多液)三、物质的溶解性1、盐的溶解性含有钾、钠、硝酸根、铵根的物质都溶于水含Cl的化合物只有AgCl不溶于水,其他都溶于水;含SO42-的化合物只有BaSO4不溶于水,其他都溶于水。
初中化学必背化学式大全

3.常见物质的化学式与名称:单质:C:碳S:硫P:磷Fe:铁Mg :镁Al :铝Hg :汞Zn :锌Cu :铜Ag :银O 2:氧气H 2:氢气N 2 :氮气O 3 :臭氧氧化物:CO :一氧化碳CO2 :二氧化碳SO2:二氧化硫MnO 2:二氧化锰SO 3 :三氧化硫H 2O 2 :过氧化氢CuO :氧化铜CaO :氧化钙MgO :氧化镁HgO :氧化汞Fe2 O 3:氧化铁Al 2 O 3:氧化铝H 2 O :水P2 O5 :五氧化二磷Fe3 O 4:四氧化三铁HCl :盐酸H 2 SO4 :硫酸NaCl: 氯化钠KMnO 4 :高锰酸钾K2 MnO 4:锰酸钾KClO 3:氯酸钾九年级化学方程式分类:1. 碳充分燃烧 : C+O 2 点燃 CO22.碳不充分燃烧 : 2C+O 2 点燃 2CO3.一氧化碳燃烧 : 2CO+O 2 点燃 2CO 24.产生一氧化碳 : C+CO 2 高温 2CO5. 硫燃烧 : S+O 2 点燃 SO26.红磷燃烧 :4P+5O 2 点燃 2P2 O57.氢气燃烧 :2H 2+O 2 点燃 2H 2 O8. 铁燃烧 : 3Fe+2O 2 点燃 Fe3O 49. 镁燃烧 : 2Mg+O 2 点燃 2MgO10.铝燃烧 :4Al+3O 2 点燃 2Al 2 O311.甲烷燃烧 :CH4+2O 2 点燃 CO 2+2H 2 O12.酒精燃烧 :C2H5 OH+3O 2 点燃 2CO 2+3H 2O13. 呼吸原理 : C6H12O 6+6O 26CO 2 +6H 2O14. 高锰酸钾制氧气 : 2KMnO△+MnO 2+O 2↑4 K2MnO415.氯酸钾制氧气 : 2KClO 3 MnO△22KCl+3O 2↑16.过氧化氢制氧气 : 2H 2 O2 MnO2 2H 2O +O 2↑17. 水通电分解 : 2H 2O 2H 2 ↑+O2 ↑18. 氧化汞分解 : 2HgO △↑2Hg+O 219.实验室制氢气的原理 :Zn+H 2SO4=ZnSO 4 +H 2↑20.镁或硫酸性质 :Mg+H 2SO4=MgSO 4+H 2↑- 2 -22. 铝或硫酸性质 :2Al+3H2SO4=Al2(SO4)3+H2 ↑23.镁或盐酸性质 :Mg+2HCl=MgCl2+H2↑24.锌或盐酸性质 :Zn+2HCl=ZnCl2+H2 ↑25.铁或盐酸性质 :Fe+2HCl=FeCl2+H2 ↑26.铝或盐酸性质 :2Al+6HCl=2AlCl 3 +3H 2↑27.酸或碱的性质 :NaOH+HCl=NaCl+H 2 O28.酸或碱的性质 :Ca(OH) 2 +2HCl=CaCl 2 +H 2 O29.酸或碱的性质 :2NaOH+H 2SO4 =Na 2SO4 +2H 2O30.酸或碱的性质 :Ca(OH) 2 +H 2 SO4 =CaSO 4+2H 2 O30.除铁锈的原理或金属氧化物与酸的性质 : Fe2O3+6HCl=2FeCl 3 +3H 2 OFe2 O3+3H 2SO4 =Fe 2(SO 4 )3+3H 2O31.制取 CO 2 或 CaCO 3 作补钙药剂 :CaCO3 +2HCl=CaCl 2 +CO 2 ↑+H 2O32.碳酸盐或酸的性质 :Na 2 CO3 +2HCl=2NaCl+CO 2 ↑+H 2 O33.治疗胃酸过多症的原理 :NaHCO 3 +HCl=NaCl+CO 2 ↑+H 2 O34.氯化钠与硝酸银反应产生白色沉淀 :NaCl+AgNO 3=NaNO 3 +AgCl ↓35.制取氢氧化钠的原理 :Ca(OH) 2 +Na 2CO 3=CaCO 3↓+2NaOH36.氢氧化钠与硫酸铜反应产生蓝色沉淀:2NaOH+CuSO 4=Na 2SO4 +Cu(OH) 237.制取水煤气的原理 :C+H 2 O 高温 H2+CO氢气还原氧化铜+△38. :H2 CuO Cu+H 2 O39. 碳还原氧化铜 :C+2CuO 高温 2Cu+CO 2↑一氧化碳还原氧化铜△40. :CO+CuO Cu+CO 241.氢气还原氧化铁 :Fe2 O3 +3H 2 高温 2Fe+3H 2O42.碳还原氧化铁 :2Fe2O3 +3C 高温 4Fe+3CO 2 ↑43.工业炼铁的原理 :Fe2 O3 +3CO 高温 2Fe+3CO 244.铁置换硫酸铜中的铜 :Fe+CuSO 4=Cu+FeSO 445.铜置换硝酸银中的银 :Cu+2AgNO 3 =2Ag+Cu(NO 3 )246.铝置换硫酸铜中的铜 :2Al+3CuSO 4 =3Cu+Al 2 (SO4)347.生石灰制熟石灰 :H2O+CaO=Ca(OH) 248.碳酸不稳定 :H2CO 3=H 2 O+CO 2↑49.工业制生石灰的原理 :CaCO 3 高温 CaO+CO 2↑50.检验 CO 2 或澄清石灰水变浑浊原理 :CO 2+Ca(OH) 2=CaCO 3 ↓+H 2 O51.烧碱变质的原理 :CO2+2NaOH=Na 2 CO3 +H 2 O52.碱与非金属氧化物的性质 :SO+2NaOH=Na2 SO+H2O SO +2NaOH=Na SO +H2O2 3 3 2 453.非金属氧化物的性质:H2 O+CO 2 =H 2CO3 H2 O+SO 2 =H 2SO3 H2 O+SO 3 =H 2 SO41.书写元素符号:氢氦碳氮氧氟氖钠镁铝硅磷硫氯氩钾钙锰铁铜锌银钡铂金汞2.书写常见的离子和化合物中元素的化合价:氢离子钙离子镁离子钠离子钾离子铁离子银离子铜离子钡离子铝离子锌离子钾离子氢氧根离子硫酸根离子硝酸根离子氯离子碳酸根离子铵根离子亚铁离子3.用化学式表示下面常见的物质:单质:碳硫磷铁镁铝汞锌铜银氧气氧气氮气臭氧氧化物:水一氧化碳二氧化碳二氧化硫二氧化锰三氧化硫过氧化氢氧化铜氧化钙氧化镁氧化汞氧化铁氧化铝五氧化二磷四氧化三铁酸:盐酸硫酸硝酸碳酸亚硫酸醋酸碱:氢氧化钠氢氧化钙氢氧化钾氢氧化镁氢氧化铜氢氧化铁氨水盐酸盐:氯化钾氯化钠氯化钾氯化银氯化铜氯化钙氯化镁氯化锌氯化钡氯化铝氯化铁氯化亚铁碳酸盐:碳酸钙碳酸钠碳酸氢钠碳酸钡碳酸钾碳酸氢铵硫酸盐:硫酸钠硫酸锌硫酸镁硫酸钙硫酸铜硫酸钡硫酸亚铁硫酸铁硫酸铝硫酸铵亚硫酸钠硝酸盐:硝酸银硝酸钠硝酸铜硝酸钾硝酸铵亚硝酸钠钾盐高锰酸钾锰酸钾氯酸钾有机化合物:乙醇葡萄糖甲烷书写化学方程式:1.碳充分燃烧 :2.碳不充分燃烧 :3.一氧化碳燃烧 :4.碳和二氧化碳反应 :5.硫燃烧 :6.红磷燃烧 :7.氢气燃烧 :8.铁燃烧 :9.镁燃烧 :10.铝燃烧 :11.甲烷燃烧 :12.酒精燃烧 :13.呼吸原理 :14.高锰酸钾制氧气 :15.氯酸钾制氧气 :16.过氧化氢制氧气 :17.水通电分解 :18.氧化汞分解 :19.实验室制氢气的原理 :20.镁和硫酸反应 :21.铁和硫酸反应 :22.铝和硫酸反应 :23.镁和盐酸反应 :24.锌和盐酸反应 :25.铁和盐酸反应 :26.铝和盐酸反应 :27.盐酸和氢氧化钠反应 :28.盐酸和氢氧化钙反应 :29.硫酸和氢氧化钠反应 :30.硫酸和氢氧化钙反应 :30.盐酸或硫酸除铁锈的原理 :31.实验室制 CO2 或 CaCO 3 作补钙药剂 :32.碳酸钠或盐酸酸反应 :33.治疗胃酸过多症的原理 :34.氯化钠与硝酸银反应产生白色沉淀 :35.制取氢氧化钠的原理 :36.氢氧化钠与硫酸铜反应产生蓝色沉淀 :37.制取水煤气的原理 :38.氢气还原氧化铜 :39.碳还原氧化铜 :40.一氧化碳还原氧化铜 :41.氢气还原氧化铁 :42.碳还原氧化铁 :43.工业炼铁的原理 :44.铁置换硫酸铜中的铜 :45.铜置换硝酸银中的银 :46.铝置换硫酸铜中的铜 :47.生石灰制熟石灰 :48.碳酸不稳定 :49.工业制生石灰的原理 :50.检验 CO 2 或澄清石灰水变浑浊原理 :51.烧碱变质的原理 :52.氢氧化钠与非金属氧化物( SO2、SO3 )的反应 :53.水与非金属氧化物( CO2 、SO2)的反应:。
初中化学常见化学物质的化学式、名称和俗称

初中常见化学物质的化学式、名称、俗称1.Al(OH)3:氢氧化铝、胃舒平的主要成分;2.BaSO4:硫酸钡、钡餐、重晶石3.C:碳、金刚石、石墨、木炭、活性炭、焦炭、煤的主要成分;4.Ca(ClO)2和CaCl2:次氯酸钙和氯化钙混合物、漂白粉(有效成分为.Ca(ClO)2)5.CaO:氧化钙、生石灰;6.CaO、NaOH:氧化钙和氢氧化钠混合物、碱石灰;7.Ca(OH)2: 氢氧化钙、消石灰、熟石灰;石灰浆、石灰乳、石灰水的主要成分;8.CaCO3:碳酸钙、大理石、石灰石的主要成分;9.CaSO4.2H2O : 硫酸钙晶体、(生)石膏;10. (CaSO4)2.H2O:硫酸钙晶体、熟石膏;11.CH4:甲烷、天然气、瓦斯、沼气的主要成分;12.C2H5OH :乙醇、酒精;13.CH3COOH:乙酸、醋酸;14.C6H12O6:葡萄糖;15.CO2:二氧化碳、碳酸气、干冰;16.CO和H2混合气:水煤气;CO:煤气;17.CO(NH2)2:尿素;18.CuSO4•5H2O:硫酸铜晶体、胆矾、蓝矾;19. Cu2(OH)2CO3:碱式碳酸铜、铜绿、铜绿、孔雀石、铜锈;20. Cu SO4和Ca(OH)2:波尔多液21.FeSO4•7H2O:硫酸亚铁晶体、绿矾;22.Fe2O3:氧化铁、铁锈和赤铁矿主要成分;23.Fe3O4:四氧化三铁、磁铁矿、烤蓝、烤黑;24.Hg: 汞、水银;25.HCl:氢氯酸、盐酸、胃酸的主要成分;26.H2O2:过氧化氢、双氧水;27.H2和O2混合气:爆鸣气;28.KAl(SO4)2.12H2O:十二水硫酸铝钾、明矾;29.K2CO3:碳酸钾、草木灰主要成分;30.KOH:氢氧化钾、苛性钾;31.NaOH:氢氧化钠、苛性钠、烧碱,火碱;32.Na2CO3:碳酸钠、纯碱、苏打;33.NaHCO3:碳酸氢钠、小苏打34.Na2CO3.10H2O:纯碱晶体、石碱、口碱;35.Na2SiO3:硅酸钠、水玻璃;36.NaCl:氯化钠、食盐;37.Na2S2O3:硫代硫酸钠、大苏打、海波;38.NH4HCO3:碳酸氢铵、碳铵;39.(NH4)2SO4:硫酸铵、硫铵;40.NH4NO3:硝酸铵、硝铵;41.NH3•H2O:一水合氨、氨水;42.P:磷、白磷、红磷、黄磷;43.S :硫、硫磺;44.SiO2:二氧化硅、石英、石英砂、水晶;45. Fe:生铁、钢、不锈钢的主要成分。
初中化学-常见物质学名俗名化学式颜色总结!

初中化学-常见物质学名俗名化学式颜色总结!
一、物质的学名、俗名及化学式
⑴金刚石、石墨:C⑵水银、汞:Hg(3)生石灰、氧化钙:CaO(4)干冰(固体二氧化碳):CO2 (4)盐酸、氢氯酸:HCl(5)熟石灰、消石灰:Ca(OH)2 (6)苛性钠、火碱、烧碱:NaOH(7)纯碱:Na2CO3 (8)酒精、乙醇:C2H5OH (16)醋酸、乙酸CH3COOH(9)氨气:NH3(碱性气体)
二、常见物质的颜色的状态
1、白色固体:MgO、CaO、NaOH、Ca(OH)
2、铁、镁为银白色(汞为银白色液态)2、黑色固体:石墨、炭粉、铁粉、CuO、MnO2、Fe3O4
3、红色固体:Cu、Fe2O3、红磷
4、溶液的颜色:凡含Cu2+的溶液呈蓝色;凡含Fe2+的溶液呈浅绿色;凡含Fe3+的溶液呈棕黄色,其余溶液一般无色。
5、沉淀(即不溶于水的盐和碱):①盐:白色↓:CaCO3、BaCO3(溶于酸) AgCl、BaSO4(也不溶于稀HNO3) 等②碱:蓝色↓:Cu(OH)2红褐色↓:Fe(OH)3白色↓:其余碱。
6、具有刺激性气体的气体:NH3、SO2、HCl(皆为无色)无色无味的气体:O2、H2、N2、CO2、CH4、CO(剧毒)
中考化学二轮专题练习。
初中常见物质的学名俗名及化学式

初中常有物质的学名俗名及化学式
初中常有物质的学名、俗名及化学式
化学式 名称 俗称 化学式
名称 俗称
Hg
汞
水银
CaO
氧化钙
生石灰
气态:碳酸气
熟石灰、消
CO 2
Ca ( OH )2
氢氧化钙
二氧化碳
石灰
固态:干冰
NaOH
氢氧化钠
苛性钠、火
Ca CO 碳酸钙
石灰石、大
3
碱、烧碱
理石
Na 2CO
碳酸钠
纯碱、苏打
CuSO · 5H O
硫酸铜晶体
胆矾、蓝矾
3
4
2
碳酸氢钠、
NaHCO 3
小苏打
NaCl
氯化钠
食盐
酸式碳酸钠
C 2H 5OH
乙醇
酒精 CHCOOH
乙酸
醋酸
3
HCl
氢氯酸 盐酸
HO
过氧化氢
双氧水
2
2
Cu 2(OH)2CO 3
碱式碳酸铜
铜绿、孔雀
H 2O 氧化氢
水
石
4 甲烷
沼气、坑气
2 3
氧化铁 铁红
CH
FeO
CO
. 12HO
硫酸铝钾晶
一氧化碳 煤气
明矾
4
2
KAl(SO)
体。
