2018年全国高考III卷试题与参考答案
2018年高考全国卷新课标III卷(含答案)(Word精校版)

绝密★启用前2018年普通高等学校招生全国统一考试(新课标III卷)英语注意事项:1. 答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2. 回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。
如需改动,用橡皮擦干净后,再选涂其他答案标号。
回答非选择题时,将答案写在答题卡上,写在本试卷上无效。
3. 考试结束后,将本试卷和答题卡一并交回。
第一部分听力(共两节,满分30分)做题时,先将答案标在试卷上。
录音内容结束后,你将有两分钟的时间将试卷上的答案转涂到答题卡上。
第一节(共5小题;每小题1.5分,满分7.5分)听下面5段对话,每段对话后有一个小题,从题中所给的A、B、C三个选项中选出最佳答案。
听完每段对话后,你都有10秒钟的时间来回答有关小题和阅读下一小题。
每段对话仅读一遍。
例:How much is the shirt?A.£19.15.B.£9.18.C.£9.15.1.What does John find difficult in learning German?A .Pronunciation.B.V ocabulary.C. Grammar.2.What is the probable relationship between the speakers?A. Colleagues.B. Brother and sister.C. Teacher and student.3.Where does the conversation probably take place?A. In a bank.B. At a ticket office.C. On a train.4. What are the speakers talking about?A.A restaurant.B.A street.C.A dish.5.What does the woman think of her interview?A. It was tough.B. It was interesting.C. It was successful.第二节(共15小题;每小题1.5分,满分22.5分)听下面5段对话或独白,每段对话或独白后有几个小题,从题中所给的A、B、C三个选项中选出最佳选项。
2018年高考语文全国III卷答案及详解

5.请简要分析文中先行者的心理变化过程。( 6分)
【答案】 :
①先行者着陆之前,已经知道地球灾难的发生, 5. 【解析】:此题考鉴赏作品的文学形象,领 ( 1)希翼与期待。虽然先行者知道一切,但还是闭起 悟作品的艺术魅力的能力。题目要求分析鉴赏小说中 一方面心存侥幸,一方面又深知连侥幸也不过是 双眼默祷着,他希望睁开眼看到一个蓝色水晶球般的 人的心理变化过程,这过程可根据小说中的相关描述 地球。( 2)失望与悲伤。当小姑娘说出人类已经不存 幻想,心情复杂纠结; 进行分析得出。比如,“先行者没再关注别的行星, 在时,先行者的心如沉海底。( 3)激动与兴奋。当先 ②着陆后亲身感受到地球的荒凉,自认是宇宙间 径直飞回地球。啊,我的蓝色水晶球……先行者闭起 行者看到半球透明玻璃罩中的人类和文明时,看到了 最后一个人类,巨大的孤独感和绝望使他濒临崩 双眼默祷着”先行者没有看到任何迹,一切都熔化了, 希望。 溃; 文明已成过眼烟云”等语句,从中分析人物的心理特 ③意识到画面有可能并非虚拟,感到震撼,重新 征。
法是正确的,在文章中有体现,但“相应的动态发展 D 项表述是针对全文的,表述正确。 过程”则无明显依据。
X
3.根据原文内容,下列说法不正确的一项是(3分) 同 C项相关的内容在文本第四段,该段中“并能够使不同 D 项的干扰性较强,相关内容在文本第四段,“并能够使 A. 当一个城市体有更好的空间弹性和制度弹性时, 的意义与价值在总体上达到平衡与和谐,……当一体被某 不同的意义与价值在总体上达到平衡与和谐,当一个城市 其意义弹性也会相应变好。 一类型的意义体系固化时,这个城市体往往不具有综合吸 只允许一种 ……这个城市体可能繁荣一时,但必然会走向 B. 城市处在不同的发展阶段时会有不同危机,制度 纳力、发展潜力”的说法可印证此项表述的正确。正确不 衰落”,可见,城市的盛衰与不同的意义和价值在总体上 当选。 的主要功能也会因此不同。 和谐有关系,但并不是直接的。所以此项说法也是正确。 只有 A项说法在文本中找不到根据。 C. 要让一个城市体具有综合吸纳能力和发展潜力, 同B项相关的内容在第三段,原文中“正在兴起的城市,其 就应平衡各种主义的关系。 主要任务是聚集更多的发展资源、激活发展活力”,“已 经发展起来的城市,注重稳定功能”,对应该项表述中 D. 城市盛衰自有其规律,与不同的意义和价值在总 “不同的发展阶段”的说法,可见此项表述是正确的。 体上的和谐没有直接关系。
2018年高考理科数学全国卷3(含答案与解析)
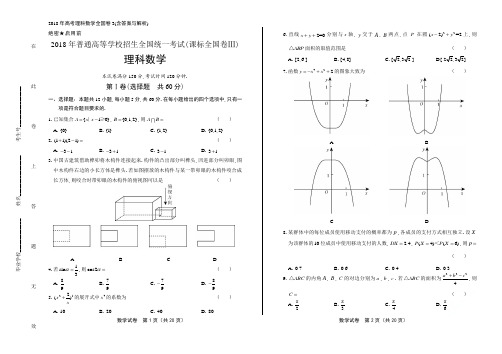
2018年高考理科数学全国卷3(含答案与解析) 数学试卷 第1页(共20页) 数学试卷 第2页(共20页)绝密★启用前2018年普通高等学校招生全国统一考试(课标全国卷Ⅲ)理科数学本试卷满分150分,考试时间120分钟.第Ⅰ卷(选择题 共60分)一、选择题:本题共12小题,每小题5分,共60分.在每小题给出的四个选项中,只有一项是符合题目要求的.1.已知集合{10}A x x =-∣≥,{0,1,2}B =,则A B = ( )A .{0}B .{1}C .{1,2}D .{0,1,2} 2.()(1i 2i)+-=( )A .3i --B .3i -+C .3i -D .3i +3.中国古建筑借助榫卯将木构件连接起来.构件的凸出部分叫榫头,凹进部分叫卯眼,图中木构件右边的小长方体是榫头.若如图摆放的木构件与某一带卯眼的木构件咬合成长方体,则咬合时带卯眼的木构件的俯视图可以是( )ABC D 4.若1sin 3α=,则cos2α=( )A .89B .79C .79-D .89-5.252()x x+的展开式中4x 的系数为( )A .10B .20C .40D .806.直线2=0x y ++分别与x 轴,y 交于A ,B 两点,点P 在圆22(2)=2x y -+上,则ABP △面积的取值范围是( )A .[2,6 ]B .[4,8]C .[2,3 2 ]D [ 22,32] 7.函数422y x x =-++的图象大致为( )ABCD8.某群体中的每位成员使用移动支付的概率都为p ,各成员的支付方式相互独立.设X为该群体的10位成员中使用移动支付的人数, 2.4DX =,()6(4)P X P X ==<,则p =( )A .0.7B .0.6C .0.4D .0.39.ABC △的内角A ,B ,C 的对边分别为a ,b ,c .若ABC △的面积为2224,则C = ( )A .π2B .π3C .π4D .π6毕业学校_____________ 姓名________________ 考生号________________ ________________ _____________-------------在--------------------此--------------------卷--------------------上--------------------答--------------------题--------------------无--------------------效----------------数学试卷 第3页(共20页) 数学试卷 第4页(共20页)10.设A ,B ,C ,D 是同一个半径为4的球的球面上四点,ABC △为等边三角形且其面积为93,则三棱锥D ABC -体积的最大值为( )A .123B .183C .243D .54311.设1F ,2F 是双曲线C :22221(0,0)x y a b a b-=>>的左、右焦点,O 是坐标原点.过2F 作C 的一条渐近线的垂线,垂足为P .若1||6||PF OP =,则C 的离心率为 ( )A .5B .2C .3D .2 12.设0.2log 0.3a =,2log 0.3b =,则( )A .0a b ab +<<B .ab a b +<<0C .0a b ab +<<D .0ab a b +<<第Ⅱ卷(非选择题 共90分)二、填空题:本题共4小题,每小题5分,共20分.13.已知向量2)(1,=a ,)2(2,=-b ,),(1λ=c .若2()+∥c a b ,则=λ . 14.曲线)e (1xy ax =+在点(0,1)处的切线的斜率为2-,则a = .15函数π()cos(3)6f x x =+在[0,π]的零点个数为 .16.已知点1()1,M -和抛物线C :²4y x =,过C 的焦点且斜率为k 的直线与C 交于A ,B 两点.若90AMB ∠=,则k = .三、解答题:共70分.解答应写出文字说明、证明过程或演算步骤.第17~21题为必考题,每个试题考生都必须作答.第22、23题为选考题,考生根据要求作答.) (一)必考题:共60分. 17.(12分)等比数列{}n a 中,11a =,534a a =. (1)求{}n a 的通项公式;(2)记n S 为{}n a 的前n 项和.若63m S =,求m .18.(12分)某工厂为提高生产效率,开展技术创新活动,提出了完成某项生产任务的两种新的生产方式.为比较两种生产方式的效率,选取40名工人,将他们随机分成两组,每组20人.第一组工人用第一种生产方式,第二组工人用第二种生产方式.根据工人完成生产任务的工作时间(单位:min )绘制了如下茎叶图:(1)根据茎叶图判断哪种生产方式的效率更高,并说明理由;(2)求40名工人完成生产任务所需时间的中位数m ,并将完成生产任务所需时间超过超过m不超过m第一种生产方式 第二种生产方式(3)根据(2)中的列联表,能否有99%的把握认为两种生产方式的效率有差异?附:22()(a b)(c d)(a c)(b d)n ad bc K -=++++,2()P K k ≥0.050 0.010 0.001k3.841 6.635 10.82819.(12分)-------------在--------------------此--------------------卷--------------------上--------------------答--------------------题--------------------无--------------------效----------------2018年高考理科数学全国卷3(含答案与解析)数学试卷 第5页(共20页) 数学试卷 第6页(共20页)如图,边长为2的正方形ABCD 所在的平面与半圆弧CD 所在平面垂直,M 是CD 上异于C ,D 的点.(1)证明:平面AMD ⊥平面BMC ;(2)当三棱锥M ABC -体积最大时,求面MAB 与面MCD 所成二面角的正弦值.20.(12分)已知斜率为k 的直线l 与椭圆C :22143x y +=交于A ,B 两点,线段AB 的中点为(1,)()M m m >0.(1)证明:12k <-;(2)设F 为C 的右焦点,P 为C 上一点,且0FP FA FB ++=.证明:FA ,FP ,FB成等差数列,并求该数列的公差. 21.(12分)已知函数22()()ln(1)2f x a x x x x +=-++.(1)若0a =,证明:当10x -<<时,()0f x <;当0x >时,()0f x >; (2)若=0x 是()f x 的极大值点,求a .(二)选考题:共10分.请考生在第22、23题中任选一题作答.如果多做,则按所做的第一题计分.22.[选修4—4:坐标系与参数方程](10分)在平面直角坐标系xOy 中,O 的参数方程为cos ,sin x y θθ=⎧⎨=⎩(θ为参数),过点(0,2)且倾斜角为α的直线l 与O 交于A ,B 两点. (1)求α的取值范围;(2)求AB 中点P 的轨迹的参数方程.23.[选修4—5:不等式选讲](10分) 设函数()211f x x x =++-. (1)画出() y f x =的图象;(2)当[ 0),x ∈+∞,()b x f ax +≤,求a b +的最小值.毕业学校_____________ 姓名________________ 考生号________________ ________________ _____________数学试卷 第7页(共20页) 数学试卷 第8页(共20页)2018年普通高等学校招生全国统一考试(课标全国卷Ⅲ)理科数学答案解析第Ⅰ卷一、选择题 1.【答案】C【解析】∵={1}A x x |≥,{0,1,2}B =,∴={1,2}A B ,故选C .2.【答案】D【解析】21i 2i)(2i 2i i 3i )(+-=-+-=+,故选D . 3.【答案】A【解析】两个木构件咬合成长方体时,小长方体(榫头)完全嵌入带卯眼的木构件,易知俯视图可以为A .故选A . 4.【答案】B 【解析】由1sin 3α=,得22127cos212sin 12()=1=399αα=-=-⨯-.故选B .5.【答案】C【解析】252()x x+的展开式的通项251103155()(2)2r r r r r r r T C x x C x ---+==,令1034r -=,得2r =,所以4x 的系数为225240C ⨯=.故选C . 6.【答案】A【解析】由圆22(2)=2x y -+可得圆心坐标(2,0),半径r =ABP △的面积记为S ,点P 到直线AB 的距离记为d ,则有12S AB d =.易知AB =maxd ==min d =所以26S ≤≤,故选A .7.【答案】D【解析】∵42()2f x x x =-++,∴3()42f x x x '=-+,令()0f x '>,解得x <或x 0<此时,()f x 递增;令()0f x '<,解得x <0或x ,此时,()f x 递减.由此可得()f x 的大致图象.故选D . 8.【答案】B【解析】由题知~1()0,X B p ,则(101 2.4)DX p p =⨯⨯-=,解得0.4p =或0.6.又∵()6(4)P X P X ==<,即446664221010(1)(1)(1)0.5C P p C P p p p p --⇒-⇒<<>,∴0.6p =,故选B .9.【答案】C【解析】根据余弦定理得2222cos a b c ab C +-=,因为2224ABCa Sbc +-=△,所以c 42os ABC ab C S =△,又1sin 2ABC S ab C =△,所以tan 1C =,因为π()0,C ∈,所以4C π=.故选C .10.【答案】B【解析】设ABC △的边长为a ,则1sin60=932ABC S a a =△,解得6a =(负值舍去).ABC △的外接圆半径r 满足62sin60r=,得r =球心到平面ABC 的距离为2=.所以点D 到平面ABC 的最大距离为246+=,所以三棱锥DABC -体积的最大值为163⨯=故选B .11.【答案】C【解析】点2(,0)F c 到渐近线b y x a =的距离2(0)PF b b ==>,而2OF c =,所以在2Rt OPF △中,由勾股定理可得OP a ,所以1PF ==.在2Rt OPF △中,222cos PF b PF O OF c∠==,在12F F P△中,2222222121221246cos 22PF F F PF b c a PF O PF F F b c+-+-∠==⋅⋅2,所以222222463464b b c a b c a c bc +-=⇒=-,则有22223()46c a c a -=-值舍去),即e =.故选C .2018年高考理科数学全国卷3(含答案与解析)数学试卷 第9页(共20页) 数学试卷 第10页(共20页)12.【答案】B【解析】解法一:∵0.20.2log 0.3log 1=0a =>,22log 0.3log 1=0b =<,∴0ab <,排除C . ∵0.20.20log 0.3log 0.2=1<<,22log 0.3log 0.5=1-<,即01a <<,1b <-,∴0a b +<,排除D .∵220.2log 0.3lg0.2log 0.2log 0.3lg 2b a ===,∴2223log 0.3log 0.2log 12b b a -=-=<,∴1bb ab a b a+⇒+<<,排除A .故选B . 解法二:易知01a <<,1b -<,∴0ab <,0a b +<, ∵0.30.30.311log 0.2log 2log 0.41a b +=+=<, 即1a bab+<,∴a b ab +>, ∴0ab a b +<<.故选B .第Ⅱ卷二、填空题13.【答案】12【解析】由已知得2(4,2)+=a b .又,()1c λ=,2()+∥c a b ,所以42=0λ-,解得12λ=. 14.【答案】3-【解析】设(e ))1(x f x ax =+,则()()1e x f x ax a '=++,所以曲线在点(0,1)处的切线的斜率(0)12k f a '==+=-,解得3a =-. 15.【答案】3【解析】令()0f x =,得πcos(3)6x +,解得ππ+()39k x k =∈Z .当0k =时,π9x =;当1k =时,4π9x =;当2k =时,7π9x =,又[ 0,π]x ∈,所以满足要求的零点有3个.16.【答案】2【解析】解法一:由题意可知C 的焦点坐标为(1,0),所以过焦点(1,0),斜率为k 的直线方程为1y x k =+,设111,y A y k ⎛⎫+ ⎪⎝⎭,221,y B y k ⎛⎫+ ⎪⎝⎭,将直线方程与抛物线方程联立得21,4,y x k y x ⎧=+⎪⎨⎪=⎩整理得2440y y k --=,从而得124y y k +=,124y y =-.∵1()1,M -,90AMB ∠=,∴0MA MB =,即1212(2)(2)(1)(1)0y yy y k k+++--=,即2440k k -+=,解得2k =.解法二:设11A(,)x y ,22(),B x y ,则2112224,4,y x y x ⎧=⎨=⎩①②②-①得2221214()y y x x -=-,从而2121124y y x x k y y --+==.设AB 的中点为M ',连接MM '.∵直线AB 过抛物线24y x =的焦点,∴以线段AB 为直径的M '⊙与准线:1l x =-相切.∵1()1,M -,90AMB ∠=,∴点M 在准线:1l x =-上,同时在M '⊙上,∴准线l 是M '⊙的切线,切点M ,且MM l '⊥,即MM '与x 轴平行,∴点M '的纵坐标为1,即1212221y y y y =⇒++=,故124422y y k =+==. 故答案为:2. 三、解答题17.【答案】(1)解:设{}n a 的公比为q ,由题设得1n n a q -=.由已知得424q q =,解得0q =(舍去)或2q =-或2q =. 故1(2)n n a -=-或12n n a -=. (2)若1(2)n n a -=-,则1(2)3nn S --=.数学试卷 第11页(共20页) 数学试卷 第12页(共20页)由63m S =得(2)188m -=-.此方程没有正整数解.若12n n a -=,则21n n S =-.由63m S =得264m =,解得6m =. 综上,6m =.【解析】(1)解:设{}n a 的公比为q ,由题设得1n n a q-=.由已知得424q q =,解得0q =(舍去)或2q =-或2q =. 故1(2)n n a -=-或12n n a -=.(2)若1(2)n n a -=-,则1(2)3n n S --=.由63m S =得(2)188m -=-。
2018年高考真题全国Ⅲ卷(含答案)

2018年普通高等学校招生全国统一考试3理科综合能力测试可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Mg 24 Al 27 S 32 Cr 52 Zn 65 I 127一、选择题:7.化学与生活密切相关。
下列说法错误的是A .泡沫灭火器可用于一般的起火,也适用于电器起火B .疫苗一般应冷藏存放,以避免蛋白质变性C .家庭装修时用水性漆替代传统的油性漆,有利于健康及环境D .电热水器用镁棒防止内胆腐蚀,原理是牺牲阳极的阴极保护法8.下列叙述正确的是A .24 g 镁与27 g 铝中,含有相同的质子数B .同等质量的氧气和臭氧中,电子数相同C .1 mol 重水与1 mol 水中,中子数比为2∶1D .1 mol 乙烷和1 mol 乙烯中,化学键数相同9.苯乙烯是重要的化工原料。
下列有关苯乙烯的说法错误的是A .与液溴混合后加入铁粉可发生取代反应B .能使酸性高锰酸钾溶液褪色C .与氯化氢反应可以生成氯代苯乙烯D .在催化剂存在下可以制得聚苯乙烯10.下列实验操作不当的是A .用稀硫酸和锌粒制取H 2时,加几滴CuSO 4溶液以加快反应速率B .用标准HCl 溶液滴定NaHCO 3溶液来测定其浓度,选择酚酞为指示剂C .用铂丝蘸取某碱金属的盐溶液灼烧,火焰呈黄色,证明其中含有Na +D .常压蒸馏时,加入液体的体积不超过圆底烧瓶容积的三分之二11.一种可充电锂-空气电池如图所示。
当电池放电时,O 2与Li +在多孔碳材料电极处生成Li 2O 2-x (x =0或1)。
下列说法正确的是A .放电时,多孔碳材料电极为负极B .放电时,外电路电子由多孔碳材料电极流向锂电极C .充电时,电解质溶液中Li +向多孔碳材料区迁移D .充电时,电池总反应为Li 2O 2-x =2Li+(1-2x)O 212.用0.100 mol·L-1 AgNO3滴定50.0 mL 0.0500 mol·L-1 Cl-溶液的滴定曲线如图所示。
2018年全国卷Ⅲ文综高考试题(有答案)

2 题。
1.与现代钢骨布面伞相比,油纸伞走俏国际市场依赖的主要优势是
A.携带方便
B.适用地广
C.文化蕴涵
D.经久耐用
2.下列地区中,宜作为油纸伞重点推销市场的是
A.欧洲西部
B.中亚
C.中东
D.撒哈拉以南非洲
大别山区某国家级贫国县农民可分为跨村种田大户农民、种植自家承包地农民、本地务工务农兼业农
民和常年外出务工农民等类型,该县以当地优势资源为基础的加工企业在县城活力较弱,但在中心集镇活
型农民
A.从事商业活动
B.留守子女上学
C.兼顾务工务农
D.扩大种田规模
5.为了实施乡村振兴战略,带领农民脱贫致富,该国家级贫困县可采取的有效措施是
①推广大规模机械化种植 ②鼓励外出务工农民回乡创业
③引导传统农民多种经营 ④推进中心集镇房地产开发
A.①② B.②③ C.③④ D.①④
贝加尔湖(图 2)是世界上最深的湖泊,监测表明湖水深度还在加大。贝加尔湖湖底沉积物巨厚,可达
A.世家大族影响巨大
B.社会阶层流动加强
C.宰相权力日益下降
D.科举制度功能弱化
26.我国第一部药学专书《神农本草经》大约成书于汉代,《唐本草》是世界上第一部由国家制定的药典, 宋代颁行了多部官修本草,明代李时珍撰成药物学集大成之作《本草纲目》,由朝廷颁行。这些史实说
明,我国古代药学的发展
A.源于大一统的政治体制
3.第Ⅱ卷必须用 0.5 毫米黑色签字笔作答,答案必须写在答题卡各题目指定区域内相应的位置;如 需改动,先划掉原来的答案,然后再写上新的答案;不能使用涂改液、胶带纸、修正带。不按以上要求作
答的答案无效。
一、选择题:本题共 35 小题,每小题 4 分,共 140 分。在每小题给出的四个选项中,只有一项是符合题目 要求的。
2018年高考语文(全国3卷)参考答案(附精准无遗漏译文)

2018年普通高等学校招生全国统一考试语文试题参考答案(包括精准无遗漏译文)一、现代文阅读(一)1. B 2. C 3. A(二)4. B5.①先行者着陆之前,已经知道地球灾难的发生,一方面心存侥幸,一方面又深知连侥幸也不过是幻想,心情复杂纠结;②着陆后亲身感受到地球的荒凉,自认是宇宙间最后一个人类,巨大的孤独感和绝望使他濒临崩溃;③意识到画面有可能并非虚拟,感到震撼,重新燃起了希望。
6.①科幻小说中的“科学”是“幻想”的基础,本文情节的基本框架,即地球灾难及文明重生,就是在宇宙科学基础上演绎的;而文中细节如宇宙飞船的星际航行、虚拟游戏、视频眼镜等,都已是或部分是科学事实。
②科幻小说中的“幻想”虽然立足于“科学”,但更要突破具体科技的限制,充分发挥想象力,将人文关怀与科学意识融汇在一起。
本文幻想出来的“宏纪元”与“微纪元”,有一定科学因素,主旨则是对人类文明的思考。
(三)7. D 8. A9 ①开始数字化转型,并与新兴媒体融合。
②营销模式多元化,赢利模式多样化。
③图书的传播速度加快,信息获取方式也发生转变,二、古代诗文阅读(一)10.D 11.C 12.D13.(1)正尽力去除先前的苛严,尚且担心做得不够,哪有宽松成为祸患的呢。
(2)愚人粗鲁无知,如果以叛逆定罪,恐怕会辜负陛下爱惜生灵的仁德。
(二)14. A15.观点一:同意。
①这两句诗是精卫坚韧不拔、前赴后继奋斗精神的自我抒发。
②意为即使自己在有生之年不能完成移山填海的事业,也希望子孙后代能够继承遗志,填海不止。
观点二:不同意。
①这两句诗是作者对精卫的同情与崇敬之情的表达。
②意为山填海的事业尚未完成,我愿牺牲生命来帮助精卫,以自己的生命来换精卫的生命。
(三) 16.(1)不如须臾之所学也不如登高之博见也(2)此先汉所以兴隆也此后汉所以倾颓也(3)小楼昨夜又东风恰似一江春水向东流三、语言文字运用17. B 18. B 19. C20.示例①“教书”改为“从教”。
2018年全国3卷高考英语真题及详细解答(解析版,学生版,精校版,新课标Ⅲ卷)

M: Isn't the chemistry homework due next Wednesday?
W: Yeah, but I have a full day of classes on Monday and a birthday party to attend on Tuesday.
M: All right, then. You go ahead, and I'll c while waiting.
【答案】10. C 11. A 12. B
【解析】Text 8
W: Welcome to our program, Dr Peterson. Let's see what questions we've got for you today. Here's one: Can cats see color?
B.To show off their hunting skills.
C.To make their owners happy.
12.How does the man sound at the end of the conversation?
A.Grateful.B.Humorous.C.Curious.
(完整版)2018年高考英语全国3卷试题及答案

2018年普通高等学校招生全国统一考试(课标全国卷Ⅲ)英语第一部分听力(共两节,满分30分)第二部分阅读理解(共两节,满分40分)第一节(共15小题;每小题2分,满分30分)阅读下列短文,从每题所给的A、B、C和D四个选项中,选出最佳选项。
AWelcome to Holker Hall & GardenVisitor InformationHow to Get to HolkerBy car: Follow brown signs on A590 from. J36, M6. Approximate travel times: Windermere—20 minutes, Kendal—25 minutes, Lancaster—45 minutes, Manchester—l hour 30minutesBy rail: the nearest station is Cark-in-Cartmel with trains to Carnforth. Lancaster and Preston for connections to major cities & airports.Opening timesSunday-Friday(closed on Saturday) 11:00 am-4;00pm, 30 March-2nd November.Admission ChargesHall & Gardens GardensAdults: £12.00 £8.00Gropes: £9.00Special EventsProducers Market 13th AprilJoin us to taste a variety of fresh local food and drinks. Meet the producers and get some excellent recipe ideas.Holker Garden Festival 30th MayThe event celebrates its 22nd anniversary with a great show of the very best of gardening, making it one of the most popular events in the gardening.National Garden Day 28th AugustHolker once again opens its gardens in aid of the disadvantaged. For just a small donation you can take a tour with our garden guide.Winter Market 8th NovemberThis is an event for all the family! Wander among a variety of shops selling gifts while enjoying a live music show and nice street entertainment.21. How long does it probably take a tourist to drive to Holker from Manchester?A.20 minutes.B. 25 minutes.C.45 minutes.D. 90 minutes.22. How much should a member of a tour group pay a visit to Hall & Gardens?A. £12.00.B. £9.00.C. £8.00D. £5.5023. Which event will you go to if you want to see a live music show?A. Producers Market.B. Holker Garden FestivalC. National Garden Day.D. Winter MarketBCities usually have a good reason for being where they are, like a nearby port on river. People settle in theseplaces because they are easy to get to and naturally suited to communications and trade. New York City, for example, is near a large harbour at the mouth of the Hudson River. Over 300 years its population grew gradually from 800 people to 8 million. But not all cities develop slowly over a long period of time. Boom towns grow from nothing almost overnight. In 1896 Dawson Canada was unmapped wilderness(荒野). But gold was discovered there in 1897 and two years later, it was one of the largest cities in the West, with a population of 30,000.Dawson did not have any of the natural conveniences of cities like London or Paris. People went there for gold. They travelled over snow-covered mountains and sailed hundreds of miles up icy rivers. The path to Dawson was covered with thirty feet of wet snow that could fall without warning. An avalanche (雪崩) once closed the path, killing 63 people. For many who made it to Dawson, however, the rewards were worth the difficult trip. Of the first 20,000 people who dug for gold, 4,000 got rich. About 100 of these stayed rich men for the rest of their lives.But no matter how rich they were, Dawson was never comfortable. Necessities like food and wood were very expensive. But soon, the gold that Dawson depended on had all been found. The city was crowded with disappointed people with no interest in settling down, and when they heard there were new gold discoveries in Alaska, they left Dawson City as quickly as they had come. Today, people still come and go to see where the Canadian gold rush happened. Tourism is now the chief industry of Dawson City - its present population is 762.24. What attracted the early settlers to New York City?A. Its business culture.B. Its small population.C. Its geographical position.D. Its favourable climate.25. What do we know about those who first dug for gold in Dawson?A. Two thirds of them stayed there.B. One out of five people got rich.C. Almost everyone gave up.D. Half of them died.26. What was the main reason for many people to leave Dawson?A. They found the city too crowded.B. They wanted to try their luck elsewhere.C. They were unable to stand the winter.D. They were short of food.27. What is the text mainly about?A. The rise and fall of a city.B. The gold rush in Canada.C. Journeys into the wilderness.D. Tourism in Dawson.CWhile famous foreign, architects are invited to lead the designs of landmark buildings in China such as the new CCTV tower and the National Center for the Performing Arts, many excellent Chinese architects are making great efforts to take the center stage.Their efforts have been proven fruitful. Wang Shu a 49-year-old Chinese architect, won the 2012 Pritzker Architecture Prize -which is often referred to as the Nobel Prize in architecture--on February 28. He is the first Chinese citizen to win this award.Wang serves as head of the Architecture Department at the China Department at the China Academy of Art(CAA). His office is located at the Xiangshan campus (校园)of the university in Hangzhou, Zhejiang Province. Many buildings on the campus are his original creations.The style of the campus is quite different from that of most Chinese universities. Many visitors were amazed by the complex architectural space and abundant building types. The curves (曲线)of the buildings perfectly match the rise and fall of hills, forming a unique view.Wang collected more than 7 million abandoned bricks of different ages. He asked the workers to use traditional techniques to make the bricks into walls, roofs and corridors. This creation attracted a lot of attention thanks to its mixture of modern and traditional Chinese elements.Wang’s works show a deep understanding of modern architecture and a good knowledge of traditions.Through such a balance, he had created a new type of Chinese architecture, said Tadao Ando, the winner of the1995 Pritzker Prize.Wang believes traditions should not be sealed in glass boxes at museums. “That is only evidence that traditions once existed, “ he said.“Many Chinese people have a misunderstanding of traditions. They think tradition means old things from the past. In fact, tradition also refers to the things that have been developing and that are still being created, “he said.“Today, many Chinese people are learning Western styles and theories rather than focusing on Chinese traditions. Many people tend to talk about traditions without knowing what they really are," said Wang.The study of traditions should be combined, with practice. Otherwise, the recreation of traditions would be artificial and empty, he said.28. Wang's winning of the prize means that Chinese architects areA. following the latest world trendB. getting international recognitionC. working harder than ever beforeD. relying on foreign architects29. What impressed visitors to the CAA Xiangshan campus most?A. Its hilly environment.B. Its large sizeC. Its unique style.D. Its diverse functions.30. What made Wang's architectural design a success?A. The mixture of different shapes.B. The balance of East and WestC. The use of popular techniquesD. The harmony of old and new.31. What should we do about Chinese traditions according to Wang?A. Spread them to the world.B. Preserve them at museums.C. Teach them in universities.D. Recreate them in practice.DAdults understand what if feels like to be flooded with objects. Why do we often assume that more is more when it comes to kids and their belongings? The good news is that I can help my own kids learn earlier than I did how to live more with less.I found the pre-holidays a good time to encourage young children to donate less-used things, and it worked. Because of our efforts, our daughter Georgia did decide to donate a large bag of toys to a little girl whose mother was unable to pay for her holiday due to illness. She chose to sell a few large objects that were less often used when we promised to put the money into her school fund (基金) (our kindergarten is serious about becoming a doctor).For weeks, I’ve been thinking of bigger, deeper questions. How do we make it a habit for them? And how do we train ourselves to help them live with, need and use less? Yesterday, I sat with my son, Shepherd, determined to test my own theory on this. I decided to play with him with only one toy for as long as it would keep his interest. I expected that one toy would keep his attention for about five minutes, ten minutes max. I chose a red rubber ball-simple, universally available. We passed it, he tried to put it in his mouth, he tried bouncing it, rolling it, sitting on it, throwing it. It was totally, completely enough for him. Before I knew it an hour had passed and it was time to move on to lunch.We both became absorbed in the simplicity of playing together. He had my full attention and I had his. My little experiment to find joy in a single object worked for both of us.32. What do the words “more is more” in paragraph 1 probably mean?A. The more, the better.B. Enough is enough.C. More money, more worries.D. Earn more and spend more.33. What made Georgia agree to sell some of her objects?A. Saving up for her holiday.B. Raising money for a poor girl.C. Adding the money to her fund.D. Giving the money to a sick mother.34. Why did the author play the ball with Shepherd?A. To try out an idea.B. To show a parent’s love.C. To train his attention.D. To help him start a hobby,.35. What can be a suitable title for the text?A. Take it or Leave it.B. A Lesson from Kids.C. Live More with Less.D. The Pleasure of Giving.第二节(共5小题;每小题2分,满分10分)根据短文内容,从短文后的选项中选出能填入空白处的最佳选项。
2018年全国卷Ⅲ英语高考试题(含答案)

2018年普通高等学校招生全国统一考试(新课标III卷)英语第一部分阅读理解(共两节,满分40分)第一节(共15小题;每小题2分,满分30分)阅读下列短文,从每题所给的A、B、C和D四个选项中,选出最佳选项。
AWelcome to Holker Ha ll & GardensVisitor InformationHow to Get to HolkerBy Car:Follow brown signs an A590 from JB6, M6.Approximale travel times: Windermere-20 minutes, Kendal-25 minutes, Lancaster-45 minutes, Manchester-I hour 30 minutes.z.x.xkBy Rail: The nearest stati on is Cark-in-Cartmel with trains to Carnforth, Lancaster Preston for connections to major cities & airports.Opening TimesSunday-Friday (closed on Saturday) 11:00 am-4:00pm, 30 March-2nd November.Admission ChargesHall & Gardens GardensAdults: £12.00 £8.00Groups £9 £5.5Producers: Market 13th AprilJoin us to taste a variety of fresh local food and drinks. Meet the producers and get some excellent recipe ideas.Holker Garden Festival 30th MayThe event celebrate its 22nd anniversary with a great show of the very best of gardening, making it one of the most popular events in gardening.National Garden Day 28th AugustHolker once again opens is gardens in aid of the disadvantaged. For just a small donation you can take a tour with our garden guide.Winter Market 8th NovemberThis is an event for all the family. Wander among a variety of shops selling gifs while enjoying a live music1show and nice street entertainment.1. How long does it probably take a tourist to drive to Holker from Manchester?A. 20minutes.B.25 minutes.C.45 minutes.D.90 minutes.2. How much should a member of a tour group pay to visit to Hall & Cardens?A.£l2.00.B. B.19.00.C.A8.0D.45.503. Which event will you go to if you want to see a live music show?A. Producers' Market.B. Holker Garden Festival.C. National Garden Day.D. Winter Market.BCities usually have a good reason for being where they are, like a nearby port or river. People settle in these places because they are easy to get to and naturally suited to communications and trade. New York City, for example, is near a large harbour at the mouth of the Hudson River. Over 300 years its population grew gradually from 800 people to 8 million. But not all cities develop slowly over a long period of time. Boom towns grow from nothing almost overnight. In 1896, Dawson, Canada, was unmapped wilderness(荒野). But gold was discovered there in 1897, and two years later, it was one of the largest cities in the West, with a population of 30,000.Dawson did not have any of the natural conveniences of cities like London or Paris. People went there for gold. They travelled over snow-covered mountains and sailed hundreds of miles up icy rivers. The path to Dawson was covered with thirty feet of wet snow that could fall without warming. An avalanche(雪崩) once closed the path, killing 63 people. For many who made it to Dawson, however, the rewards were worth the difficult trip. Of the first 20,000 people who dug for gold, 4,000 got rich. About 100 of these stayed rich men for the rest of their lives.But no matter how rich they were, Dawson was never comfortable. Necessities like food and wood were very expensive. But soon, the gold that Dawson depended on had all been found. The city was crowded with disappointed people with no interest in settling down, and when they heard there were new gold discoveries in Alaska, they left Dawson City as quickly as they had come. Today, people still come and go — to see where the Canadian gold rush happened. Tourism is now the chief industry of Dawson City — its present population is 762.4. What attracted the early settlers to New York City?A. Its business culture.B. Its small population.C. Its geographical position.D. Its favourable climate.25. What do we know about those who first dug for gold in Dawson?A. Two-thirds of them stayed there.B. One out of five people got rich.C. Almost everyone gave up.D. Half of them died.6. What was the main reason for many people to leave Dawson?A. They found the city too crowded.B. They wanted to try their luck elsewhere.C. They were unable to stand the winter.D. They were short of food.7. What is the text mainly about?A. The rise and fall of a city.B. The gold rush in Canada.C. Journeys into the wilderness.D. Tourism in Dawson.CWhile famous foreign architects are invited to lead the designs of landmark buildings in China such as the new CCTV tower and the National Center for the Performing Arts, many excellent Chinese architects are making great efforts to take the center stage.Their efforts have been proven fruitful. Wang Shu, a 49-year-old Chinese architect, won the 2012 Pritzker Architecture Prize — which is often referred to as the Nobel Prize in architecture — on February 28. He is the first Chinese citizen to win this award.Wang serves as head of the Architecture Department at the China Academy of Art (CAA). His office is located at the Xiangshan campus(校园) of the university in Hangzhou, Zhejiang Province. Many buildings on the campus are his original creations.The style of the campus is quite different from that of most Chinese universities. Many visitors were amazed by the complex architectural space and abundant building types. The curves(曲线) of the buildings perfectly match the rise and fall of hills, forming a unique view.Wang collected more than 7 million abandoned bricks of different ages. He asked the workers to usetraditional techniques to make the bricks into walls, roofs and corridors. This creation attracted a lot of attention3thanks to its mixture of modern and traditional Chinese elements(元素).Wang’s works show a deep understanding of modern architecture and a good knowledge of traditions. Through such a balance, he had created a new type of Chinese architecture, said Tadao Ando, the winner of the 1995 Pritzker Prize.Wang believes traditions should not be sealed in glass boxes at museums. "That is only evidence that traditions once existed," he said."Many Chinese people have a misunderstanding of traditions. They think tradition means old things from the past. In fact, tradition also refers to the things that have been developing and that are still being created, " he said."Today, many Chinese people are learning Western styles and theories rather than focusing on Chinese traditions. Many people tend to talk about traditions without knowing what they really are, " said Wang.The study of traditions should be combined with practice. Otherwise, the recreation of traditions would be artificial and empty, he said.8. Wang’s wi nning of the prize means that Chinese architects are ___________.A. following the latest world trendB. getting international recognitionC. working harder than ever beforeD. relying on foreign architects9. What impressed visitors to the CAA Xiangshan campus most?A. Its hilly environment.B. Its large size.C. Its unique style.D. Its diverse functions.10. What made Wang’s architectural design a success?A. The mixture of different shapes.B. The balance of East and West.C. The use of popular techniques.D. The harmony of old and new.11. What should we do about Chinese traditions according to Wang?A. Spread them to the world.B. Preserve them at museums.C. Teach them in universities.D. Recreate them in practice.DAdults understand what it feels like to be flooded with objects. Why do we often assume that more is more4when it comes to kids and their belongings? The good news is that I can help my own kids learn earlier than I did how to live more with less.z.x.xkI found the pre-holidays a good time to encourage young children to donate less-used things, and it worked. Because of our efforts, our daughter Georgia did decide to donate a large bag of toys to a little girl whose mother was unable to pay for her holiday due to illness. She chose to sell a few larger objects that were less often used when we promised to put the money into her school fund(基金)(our kindergarten daughter is serious about becoming a doctor)For weeks, I've been thinking of bigger, deeper questions: How do we make it a habit for them? And how do we train ourselves to help them live with, need, and use less? Yesterday, I sat with my son, Shepherd, determined to test my own theory on this. I decided to play with him with only one toy for as long as it would keep his interest. I expected that one toy would keep his attention for about five minutes, ten minutes, max. I chose a red rubber ball-simple, universally available. We passed it, he tried to put it in his mouth, he tried bouncing it, rolling it, sitting on it, throwing it. It was totally, completely enough for him. Before I knew it an hour had passed and it was time to move on to lunch.We both became absorbed in the simplicity of playing together. He had my full attention and I had his. My little experiment to find joy in a single object worked for both of us.12. What do the words “more is more” in paragraph 1 probably mean?A. The more, the better.B. Enough is enough.C. More money, more worries.D. Earn more and spend more.13.What made Georgia agree to sell some of her objects?A. Saving up for her holidayB. Raising money for a poor girlB. Adding the money to her fund D. Giving the money to a sick mother14. Why did the author play the ball with Shepherd?A. To try out an ideaB. To show a parent's loveC. To train his attentionD. To help him start a hobby15. What can be a suitable title for the text?A. Take It or Leave ItB. A Lesson from KidsC. Live More with LessD. The Pleasure of Giving5第二节(共5小题;每小题2分,满分10分)根据短文内容,从短文后的选项中选出能填入空白处的最佳选项。
2018年全国卷(III)高考语文试卷及答案

4.考试结束后,请将本试题卷和答题卡一并上交。
一、现代文阅读(36分)
(一)论述类文本阅读(本题共3小题,9分)
阅读下面的文字,完成1~3题。
对城市而言,文明弹性是一个城市体在生存、创新、适应、应变等方面的综合状态、综合能力,是公共性与私人性之间、多样性与共同性之间、稳定性与变迁性之间、柔性与刚性之间的动态和谐,过于绵柔、松散,或者过于刚硬、密集,都是弹性不足或丧失的表现,是城市体出现危机的表征。当代城市社会,尤其需要关注以下文明弹性问题。
其二,制度弹性,一种较为理想的、有弹性的城市制度,是能够在秩序与活力、生存与发展间取得相对平衡的制度。城市有其发展周期、发展阶段,对一个正在兴起的城市而言,其主要任务是聚集更多的发展资源、激活发展活力。而对一个已经发展起来的城市而言,人们会更为注重城市制度的稳定功能。但问题在于,即使是正在崛起的城市,也需要面对秩序与稳定的问题;即使是一个已经发展起来的城市,也需要面对新活力的激活问题。过于注重某种形式的城市制度,过于注重城市制度的某种目标,都是城市制度弹性不足、走向僵化的表现,都会妨害城市发展。
他看到了一个黑白相间的地球。
黑色的是熔化后又凝结的岩石,白色的是蒸发后又冻结的海洋。
飞船进入低轨道,从黑色的大陆和白色的海洋上空缓缓越过,先行者没有看到任何遗迹,一切都熔化了,文明已成过眼烟云。
这时,飞船收到了从地面发来的一束视频信号,显示在屏幕上。
先行者看到了一个城市的图像:先看到如林的细长的高楼群,镜头降下去,出现了一个广场,广场上一片人海,所有的人都在仰望天空。镜头最后停在广场正中的平台上,那儿站着一个漂亮姑娘,好像只有十几岁,她在屏幕上冲着先行者挥手,娇滴滴地喊:“喂,我们看到你了!你是先行者?”
2018年高考语文真题卷(全国Ⅲ卷)(含答案及过程详解)

绝密★启用前2018年普通高等学校招生全国统一考试(含听力音频)语文(全国Ⅲ卷)注意事项:1.答卷前,考生务必将自己的姓名、考生号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡对应题目的答案标号涂黑。
如需改动,用橡皮擦干净后,再选涂其他答案标号。
回答非选择题时,将答案写在答题卡上。
写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
一、现代文阅读(36分)(共3题;共36分)1.阅读下面的文字,完成小题对城市而言,文明弹性是一个城市体在生存。
创新、适应、应变等方面的综合状态、综合能力,是公共性与私人性之间,多样性与共同性之间,稳定性与变迁性之间、柔性与刚性之间的动态和谐,过于绵柔、松散,或者过于刚硬、密集,都是弹性不足或丧失的表现,是城市体出现危机的表征,当代城市社会,尤其需要关注以下文明弹性问题。
其一,空间弹性。
城市具有良好空间弹性的一个重要表现,是空间的私人性与公共性关系能够得到较为合理的处理。
任何城市空间都是私人性与公共性的统一,空间弹性的核心问题,就是如何实现空间的公共性与私人性的有机统一、具体转换。
片面地强调空间的公共性或成片面地强调空间的私人性,都会使城市发展失去基础,目前,人们更多地要求空间的私人性,注重把空间固化为永恒的私人所有物、占有物。
这种以私人化为核心的空间固化倾向,造成城市空间弹性不足,正在成为制约城市发展的一个重要原因。
其二,制度弹性,一种较为理想的、有弹性的城市制度,是能够在秩序与活力、生存与发展间取得相对平衡的制度。
城市有其发展周期、发展阶段,对一个正在兴起的城市而言,其主要任务是聚集更多的发展资源、激活发展活力,而对一个已经发展起来的城市而言,人们会更为注重城市制度的稳定功能。
但问题在于,即使是正在崛起的城市,也需要面对秩序与稳定的问题:即使是一个已经发展起来的城市,也需要面对新活力的激活问题。
过于注重某种形式的城市制度,过于注重城市制度的某种目标,都是城市制度弹性不足,走向僵化的表现,都会妨害城市发展。
2018高考语文全国III卷及答案

2018年普通高等学招生全国统一考试(三)语文注意事项:1、答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2、回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。
如需改动,用橡皮擦干净后,再选涂其他答案标或。
回答非选择题时,将答案写在大体看上。
写在本试卷上无效。
3、考试结束后,将本试卷和答题卡一并交回。
一、现代文阅读(36)(一)论述类文本阅读(本题共3小题,9分)对城市而言,文明弹性是一个城市体在生存、创新、适应、应变等方面的综合状态、综合能力,是公共性与私人性之间;多样性与共同性之间;稳定性与变迁性之间、柔性与刚性之间的动态和谐。
过于绵柔、松散,或者过于刚硬、密集,都是弹性不足或丧失的表现,是城市体出现危机的表征。
当代城市社会,尤其需要关注一下文明弹性问题。
其一,空间弹性。
城市具有良好空间弹性的一个重要表现,是空间的私人性与公共性关系能够得到较为合理的处理。
任何城市空间都是私人性与公共性的统一,空间弹性的核心问题,就是如何实现空间的公共性与私人性的有机统一、具体转换。
片面的强调空间公共性或片面的强调空间的私人性,都会使城市发展失去基础。
目前,人们更多地要求空间的私人性,注重把空间固化为永恒的私人所有物、占有物。
这种以私人化为核心的空间固化倾向,造成城市空间弹性不足,正在成为制约城市发展的一个重要原因。
其二,制度弹性。
一种较为理想的、有弹性的城市制度,是能够在秩序与活力、生存与发展间取得相对平衡的制度。
城市有其发展周期、发展阶段,对一个正在兴起的城市而言,其主要任务是聚集更多的发展资源、激活发展活力。
而对一个已经发展起来的城市而言,人们会更为注重城市制度的稳定功能。
但问题在于,即使是正在崛起的城市,也需要面对秩序与稳定的问题;即使是一个已经发展起来的城市,也需要面对新活力的激活问题。
过于注重某种形式的城市制度,过于注重城市制度的某种目标,都是城市制度弹性不足、走向僵化的表现,都会妨害城市发展。
2018年全国卷三文综高考试题高清版含答案

2018年高考全国卷三文科综合考前须知:1.答题前,考生务必用0.5毫米黑色签字笔将自己的姓名、座号、考生号、县区和科类写在答题卡和试卷规定的位置上。
2.第一卷每题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑;如需改动,用橡皮擦干净后,再选途其他答案标号。
写在试卷上无效。
3.第二卷必须用0.5毫米黑色签字笔作答,答案必须写在答题卡各题目指定区域内相应的位置;如需改动,先划掉原来的答案,然后再写上新的答案;不能使用涂改液、胶带纸、修正带。
不按以上要求作答的答案无效。
一、选择题:此题共35小题,每题4分,共140分。
在每题给出的四个选项中,只有一项为哪一项符合题目要求的。
油纸伞是我国非物质文化遗产,采用传统方法、全手工制作,油纸伞以竹为骨,以纸或丝绸为面、刷桐油以增强韧性并防水,但长期置于枯燥环境中易变脆、开裂,近年来,油纸伞走俏国际市场、据此完成1~2题。
1.与现代钢骨布面伞相比,油纸伞走俏国际市场依赖的主要优势是()A.携带方便B.适用地广C.文化蕴涵D.经久耐用2.以下地区中,宜作为油纸伞重点推销市场的是()A.欧洲西部B.中亚C.中东D.撒哈拉以南非洲大别山区*国家级贫国县农民可分为跨村种田大户农民、种植自家承包地农民、本地务工务农兼业农民和常年外出务工农民等类型。
该县以当地优势资源为根底的加工企业在县城活力较弱,但在中心集镇活力较强,图1示意该县居民点的等级构造。
据此完成3~5题。
3.与县城相比,中心集镇以当地优势资源为根底的加工企业活力较强的主要原因是A.根底设施较完善B.更接近消费市场C.资金供给较充裕D.更易招养劳动力4.面向*类型农民的需求,有专家建议在该县推进"村——中心集镇双栖〞居住模式。
这种模式旨在方便该类型农民A.从事商业活动B.留守子女上学C.兼顾务工务农D.扩大种田规模5.为了实施乡村振兴战略,带着农民脱贫政富,该国家级贫困县可采取的有效措施是①推广阔规模机械化种植②鼓励外出务工农民回乡创业③引导传统农民多种经营④推进中心集镇房地产开发A.①②B.②③C.③④D.①④贝加尔湖(图示)是世界上最深的湖泊,监测说明湖水深度还在加大。
2018年高考文科数学全国卷3(含答案与解析)

2018年高考文科数学全国卷3(含答案与解析)2018年普通高等学校招生全国统一考试课标全国卷III数学(文科)本试卷满分150分,考试时间120分钟。
第Ⅰ卷(选择题共60分)一、选择题:本题共12小题,每小题5分,共60分。
在每小题给出的四个选项中,只有一项是符合题目要求的。
1.已知集合$A=\{x|x-1\geq0\}$,$B=\{0,1,2\}$,则$AB=$A。
$\emptyset$ B。
$\{1\}$ C。
$\{1,2\}$ D。
$\{0,1,2\}$2.$(1+i)(2-i)=$A。
$-3-i$ B。
$-3+i$ C。
$3-i$ D。
$3+i$3.中国古建筑借助榫卯将木构件连接起来。
构件的凸出部分叫榫头,凹进部分叫卯眼,图中木构件右边的小长方体是榫头。
若如图摆放的木构件与某一带卯眼的木构件咬合成长方体,则咬合时带卯眼的木构件的俯视图可以是ABCD4.若$\sin\alpha=\frac{1}{3}$,则$\cos2\alpha=$A。
$\frac{8}{9}$ B。
$\frac{7}{99}$ C。
$-\frac{7}{9}$ D。
$-\frac{8}{9}$5.若某群体中的成员只用现金支付的概率为0.45,既用现金支付也用非现金支付的概率为0.15,则不用现金支付的概率为A。
0.3 B。
0.4 C。
0.6 D。
0.76.函数$f(x)=\frac{\tan x}{1+\tan^2x}$的最小正周期为A。
$\frac{\pi}{4}$ B。
$\frac{\pi}{2}$ C。
$\pi$ D。
$2\pi$7.下列函数中,其图象与函数$y=\ln x$的图象关于直线$x=1$对称的是A。
$y=\ln(1-x)$ B。
$y=\ln(2-x)$ C。
$y=\ln(1+x)$ D。
$y=\ln(2+x)$成任务的时间,得到以下数据:第一组:12.15.13.14.16.18.17.14.16.15.13.12.14.15.13.16.17.14.15.13第二组:16.17.14.18.15.16.13.14.15.16.17.15.14.16.15.17.15.16.18.141)分别计算两组工人完成任务的平均时间和标准差;2)根据以上数据,判断两种生产方式哪一种更有效,并说明理由.19.(12分)已知函数f(x)在区间[0,1]上连续,且f(0)=f(1)=0.证明:对于任意正整数n。
2018全国高考语文3卷(含答案解析)

(全国Ⅲ卷)2018年普通高等学校招生全国统一考试语文(含答案解析)注意事项:1.答卷前,考生务必将自己的姓名、淮考证号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。
如需改动,用橡皮擦干净后,再选涂其他答案标号。
回答非选择题时,将答案写在答题卡上。
写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
一、现代文阅读(36分)(一)论述类文本阅读(本题共3小题,9分)阅读下面的文字,完成1~3题。
对城市而言,文明弹性是一个城市体在生存。
创新、适应、应变等方面的综合状态、综合能力,是公共性与私人性之间,多样性与共同性之间,稳定性与变迁性之间、柔性与刚性之间的动态和谐,过于绵柔、松散,或者过于刚硬、密集,都是弹性不足或丧失的表现,是城市体出现危机的表征,当代城市社会,尤其需要关注以下文明弹性问题。
其一,空间弹性。
城市具有良好空间弹性的一个重要表现,是空间的私人性与公共性关系能够得到较为合理的处理。
任何城市空间都是私人性与公共性的统一,空间弹性的核心问题,就是如何实现空间的公共性与私人性的有机统一具体转换。
片面地强调空间的公共性成片面地强调空间的私人性,都会使城市发展失去基础,目前,人们更多地要求空间的私人性,注重把空间因化为永恒的私人所有物、占有物。
这种以私人化为核心的空间固化倾向,造成城市空间弹性不足,正在成为制约城市发展的一个重要原因,其二,制度弹性,一种较为理想的、有弹性的城市制度,是能够在秩序与活力、生存与发展间取得相对平衡的制度。
城市有其发展周期、发展阶段,对一个正在兴起的城市而言,其主要任务是聚集更多的发展资源、激活发展活力,而对一个已经发展起来的城市而言,人们会更为注重城市制度的稳定功能。
但问题在于,即使是正在崛起的城市,也需要面对秩序与稳定的问题:即使是一个已经发展起来的城市,也需要面对新活力的激活问题。
过于注重某种形式的城市制度,过于注重城市制度的某种目标,都是城市制度弹性不足,走向僵化的表现,都会妨害城市发展.其三,意义弹性。
2018年普通高等学校招生全国统一考试(全国Ⅲ卷)(附带答案及详细解析)

2018年高考语文真题试卷(全国Ⅲ卷)注意事项:1.答题前,考生务必将自己的姓名、准考证号填写在本试题相应的位置。
2.全部答案在答题卡上完成,答在本试题上无效。
3.回答选择题时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。
如需改动,用橡皮擦干净后,再选涂其他答案标号。
回答非选择题时,将答案用0.5mm黑色笔迹签字笔写在答题卡上。
4.考试结束后,将本试题和答题卡一并交回。
一、现代文阅读1.阅读下面的文字,完成小题对城市而言,文明弹性是一个城市体在生存。
创新、适应、应变等方面的综合状态、综合能力,是公共性与私人性之间,多样性与共同性之间,稳定性与变迁性之间、柔性与刚性之间的动态和谐,过于绵柔、松散,或者过于刚硬、密集,都是弹性不足或丧失的表现,是城市体出现危机的表征,当代城市社会,尤其需要关注以下文明弹性问题。
其一,空间弹性。
城市具有良好空间弹性的一个重要表现,是空间的私人性与公共性关系能够得到较为合理的处理。
任何城市空间都是私人性与公共性的统一,空间弹性的核心问题,就是如何实现空间的公共性与私人性的有机统一、具体转换。
片面地强调空间的公共性或成片面地强调空间的私人性,都会使城市发展失去基础,目前,人们更多地要求空间的私人性,注重把空间固化为永恒的私人所有物、占有物。
这种以私人化为核心的空间固化倾向,造成城市空间弹性不足,正在成为制约城市发展的一个重要原因。
其二,制度弹性,一种较为理想的、有弹性的城市制度,是能够在秩序与活力、生存与发展间取得相对平衡的制度。
城市有其发展周期、发展阶段,对一个正在兴起的城市而言,其主要任务是聚集更多的发展资源、激活发展活力,而对一个已经发展起来的城市而言,人们会更为注重城市制度的稳定功能。
但问题在于,即使是正在崛起的城市,也需要面对秩序与稳定的问题:即使是一个已经发展起来的城市,也需要面对新活力的激活问题。
过于注重某种形式的城市制度,过于注重城市制度的某种目标,都是城市制度弹性不足,走向僵化的表现,都会妨害城市发展。
2018年全国高考III卷试题与参考答案

绝密★启用前2018 年一般高等学校招生全国一致考试理科综合能力测试( III卷)可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Mg 24 Al 27 S 32 Cr 52 Zn 65 I 1277.化学与生活亲密有关。
以下说法错误的选项是A.泡沫灭火器可用于一般的起火,也合用于电器起火B.疫苗一般应冷藏寄存,以防止蛋白质变性C.家庭装饰时用水性漆代替传统的油性漆,有益于健康及环境D.电热水器用镁棒防备内胆腐化,原理是牺牲阳极的阴极保护法8.以下表达正确的选项是A.24 g镁与27 g铝中,含有同样的质子数B.同样质量的氧气和臭氧中,电子数同样C.1 mol 重水与 1 mol 水中,中子数比为2∶ 1D.1 mol 乙烷和 1 mol 乙烯中,化学键数同样9.苯乙烯是重要的化工原料。
以下有关苯乙烯的说法错误的选项是A.与液溴混淆后加入铁粉可发生代替反响B.能使酸性高锰酸钾溶液退色C.与氯化氢反响能够生成氯代苯乙烯D.在催化剂存在下能够制得聚苯乙烯10.以下实验操作不妥的是A.用稀硫酸和锌粒制取H2时,加几滴CuSO4溶液以加速反响速率B.用标准 HCl 溶液滴定NaHCO3溶液来测定其浓度,选择酚酞为指示剂C.用铂丝蘸取某碱金属的盐溶液灼烧,火焰呈黄色,证明此中含有Na+D.常压蒸馏时,加入液体的体积不超出圆底烧瓶容积的三分之二11.一种可充电锂 - 空气电池以下图。
当电池放电时,O2与Li+在多孔碳资料电极处生成Li 2O2- x(x=0 或 1)。
以下说法正确的选项是A.放电时,多孔碳资料电极为负极B.放电时,外电路电子由多孔碳资料电极流向锂电极C.充电时,电解质溶液中Li +向多孔碳资料区迁徙D.充电时,电池总反响为 Li O =2Li+ ( 1- x ) O2 2- x 2212.用 0.100 mol · L-1 AgNO3滴定 50.0 mL 0.0500 mol· L-1Cl-溶液的滴定曲线以下图。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
绝密★启用前2018年普通高等学校招生全国统一考试理科综合能力测试(in 卷)可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Mg 24 Al 27 S 32 Cr 52 Zn 65 I 1277•化学与生活密切相关。
下列说法错误的是A.泡沫灭火器可用于一般的起火,也适用于电器起火B.疫苗一般应冷藏存放,以避免蛋白质变性C.家庭装修时用水性漆替代传统的油性漆,有利于健康及环境D.电热水器用镁棒防止胆腐蚀,原理是牺牲阳极的阴极保护法8.下列叙述正确的是A.24 g镁与27 g铝中,含有相同的质子数B.同等质量的氧气和臭氧中,电子数相同C. 1 mol重水与1 mol水中,中子数比为 2 : 1D. 1 mol乙烷和1 mol乙烯中,化学键数相同9 .苯乙烯是重要的化工原料。
下列有关苯乙烯的说法错误的是A.与液溴混合后加入铁粉可发生取代反应B.能使酸性高锰酸钾溶液褪色C.与氯化氢反应可以生成氯代苯乙烯D.在催化剂存在下可以制得聚苯乙烯10.下列实验操作不当的是A.用稀硫酸和锌粒制取 H2时,加几滴CuSO溶液以加快反应速率B.用标准HCI溶液滴定NaHCO溶液来测定其浓度,选择酚酞为指示剂C.用铂丝蘸取某碱金属的盐溶液灼烧,火焰呈黄色,证明其中含有Na+D.常压蒸馏时,加入液体的体积不超过圆底烧瓶容积的三分之二211.一种可充电锂-空气电池如图所示。
当电池放电时,Q与Li +在多孔碳材料电极处生成 Li 2Q-X (x=0或1) o 下列说法正确的是A.放电时,多孔碳材料电极为负极B.放电时,外电路电子由多孔碳材料电极流向锂电极C.充电时,电解质溶液中 Li +向多孔碳材料区迁移D.充电时,电池总反应为 Li 2Q-x=2Li+ (1- - ) O非水电解质/高聚物隔鞭12.用0.100 mol • L AgNO滴定50.0 mL 0.0500 mol • L Cl-溶液的滴定曲线如图所示。
下列有关描述错误的是V(AgN()5ym],A.根据曲线数据计算可知K sp(AgCl)的数量级为10-10B.曲线上各点的溶液满足关系式c(Ag+)• c(Cl -)=K Sp(AgCl). ■ 1C.相同实验条件下,若改为0.0400 mol • L Cl ,反应终点c移到aD.相同实验条件下,若改为0.0500 mol • L-1 Br-,反应终点c向b方向移动13.W X、Y、Z均为短周期元素且原子序数依次增大,元素X和Z同族。
盐YZW与浓盐酸反应,有黄绿色气体产生,此气体同冷烧碱溶液作用,可得到YZW的溶液。
下列说法正确的是A.原子半径大小为W Xv Yv ZB. X的氢化物水溶液酸性强于Z的C.Y2W2与ZW均含有非极性共价键D.标准状况下W勺单质状态与X的相同26.(14分)硫代硫酸钠晶体(NstSQ・ 5H2Q M=248 g • mol-1)可用作定影剂、还原剂。
回答下列问题:(1)已知:K Sp(BaSQ4)=1.1 x 10- 10, K sp(BaS2Q)=4.1 x 10- 5。
市售硫代硫酸钠中常含有硫酸根杂质,选用下列试剂设计实验方案进行检验:试剂:稀盐酸、稀 HSQ、BaCl2溶液、NaaCQ溶液、H2Q溶液实验步骤现象①取少量样品,加入除氧蒸馏水②固体完全溶解得无色澄清溶液③④,有刺激性气体产生⑤静置,⑥(2)利用K2Cr2C7标准溶液定量测定硫代硫酸钠的纯度。
测定步骤如下:①溶液配制:称取 1.2000 g某硫代硫酸钠晶体样品,用新煮沸并冷却的蒸馏水在__________________ 中溶解,完全溶解后,全部转移至100 mL的__________ 中,加蒸馏水至_____________ 。
②滴定:取0.00950 mol •L- 1的K262Q标准溶液20.00 mL,硫酸酸化后加入过量KI,发生反应:C^O2- +6I- +14H f3l2+2Cr3++7H2 0。
然后用硫代硫酸钠样品溶液滴定至淡黄绿色,发生反应:I 2+2S2Q2-SC62-+21-。
加入淀粉溶液作为指示剂,继续滴定,当溶液__________________ ,即为终点。
平行滴定3次,样品溶液的平均用量为24.80 mL ,则样品纯度为__________ % (保留1位小数)。
27.(14分)KIO3是一种重要的无机化合物,可作为食盐中的补碘剂。
回答下列问题:(1)KIO3的化学名称是(2)利用“ KCI03氧化法”制备 KIO3工艺流程如下图所示:“酸化反应”所得产物有KH(IO3)2、Cl 2和KCI。
“逐CI2”采用的方法是溶质主要是 _______ 。
“调pH'中发生反应的化学方程式为______________(3)KCIO3也可采用“电解法”制备,装置如图所示。
①写出电解时阴极的电极反应式 _______ 。
②电解过程中通过阳离子交换膜的离子主要为__________ ,其迁移方向是______________ 。
③与“电解法”相比,“ KClO 3氧化法”的主要不足之。
“滤液”中的H3O hKCIthH2O处有_______________ (写出一点)。
28. (15分)三氯氢硅(SiHCl 3)是制备硅烷、多晶硅的重要原料。
回答下列问题:(1) SiHCl 3在常温常压下为易挥发的无色透明液体,遇潮气时发烟生成(HSiO )2O 等,写出该反应的化学方程式 ___________ 。
(2) SiHCl 3在催化剂作用下发生反应:2SiHCI 3(g )SiH 2Cl 2(g )+ SiCl 4(g ) △ H=48 kJ • mol -1-13SiH 2Cl 2(g )SiH 4(g )+2SiHCI 3 (g ) △ H 2=- 30 kJ • mol1则反应 4SiHCI 3(g )SiH 4(g )+ 3SiCl 4(g )的△ H= _____ kJ • mol -。
(3) 对于反应2SiHCl 3(g )SiH 2Cl 2(g )+SiCI 4(g ),采用大孔弱碱性阴离子交换树脂催化剂,在 323 K和 343 K 时SiHCl 3的转化率随时间变化的结果如图所示。
25 20 15 105① 343 K 时反应的平衡转化率a = _________ %平衡常数K M 3 K = _______________ (保留2位小数)。
② 在343 K 下:要提高 SiHCl 3转化率,可采取的措施是 _______________ ;要缩短反应达到平衡的时 间,可采取的措施有 ______________ 、 ___________ 。
③ 比较a 、b 处反应速率大小:v a___________________ V b (填“大于”“小于”或“等于”) 。
反应速率v=v 正-v 逆= k 正x 2SiH ci3 - k逆乂沁…乂眈打,k 正、k 逆分别为正、逆向反应速率常数, x 为物质的量分数,计算a 处竺= ______________ (保留1位小数)。
v 逆£菇芒主一「二一100 200 300 400tf'rnin35.[化学一一选修3:物质结构与性质](15分)锌在工业中有重要作用,也是人体必需的微量元素。
回答下列问题:(1)_______________________________________ Zn原子核外电子排布式为。
(2)黄铜是人类最早使用的合金之一,__________________ 主要由Zn和Cu组成。
第一电离能I i (Zn) I 1 (Cu)(填“大于”或“小于”)。
原因是 _________________ 。
(3)___________________________________________________ ZnF2具有较高的熔点(872 C ),其化学键类型是_____________________________________________________________; ZnF2不溶于有机溶剂而 ZnCI2、ZnBs Znl 2能够溶于乙醇、乙醚等有机溶剂,原因是____________________ 。
(4)《中华本草》等中医典籍中,记载了炉甘石(ZnCO)入药,可用于治疗皮肤炎症或表面创伤。
ZnCO中,阴离子空间构型为__________________ , C原子的杂化形式为 __________________ 。
(5)_____________________________________________________________________ 金属Zn晶体中的原子堆积方式如图所示,这种堆积方式称为_________________________________________________ 。
六棱柱底边边长为a cm,高为c cm,阿伏加德罗常数的值为N A, Zn的密度为_________________ g • cm 3 (列出计算式)。
36.[化学一一选修5:有机化学基础](15分)近来有报道,碘代化合物E与化合物H在Cr-Ni催化下可以发生偶联反应,合成一种多官能团的化合物Y,其合成路线如下:已知:RCHO+CH-CHO------------ RCH=CHCH t十H.-O回答下列问题:(1)A的化学名称是_________________ 。
C DEF・ I C X H EC?H,0NiOHHiO C J rlfUPJCLI ----- 1粼刑(2)B为单氯代烃,由 B生成C的化学方程式为____________________(3)____________________________________________________ 由A生成B、G生成H的反应类型分别是__________________________________________________________________ 、_(4) D的结构简式为 _______________ 。
(5) Y中含氧官能团的名称为 ________________ 。
(6) E与F在Cr-Ni催化下也可以发生偶联反应,产物的结构简式为_____________________ 。
(7) X与D互为同分异构体,且具有完全相同官能团。
X的核磁共振氢谱显示三种不同化学环境的氢,其峰面积之比为 3 : 3 : 2。
写出3种符合上述条件的 X的结构简式_____________________ 。
37.[生物——选修 1:生物技术实践]( 15 分)回答下列与酵母菌有关的问题:(1)分离培养酵母菌通常使用______________(填“牛肉膏蛋白胨”“ MS或“麦芽汁琼脂”)培养基, 该培养基应采用_________ 灭菌法灭菌。
