2020-2021中考化学化学溶解度(大题培优)及详细答案
2020-2021中考化学化学溶解度综合练习题含答案

下物质的溶解度。
10. t ℃时,向饱和溶液中加入一定量的水后,下列有关该溶液的叙述正确的是(
)
A.仍为饱和溶液
B.溶质的质量变小
C.溶质的溶解度不变 【答案】 C
D.溶质的质量分数不变
【解析】
【详解】
A 、 t℃时,向硝酸钠饱和溶液中加入一定量的水,溶液能继续溶解硝酸钠,溶液变为不饱 和溶液,故选项说法错误;
饱和,故 C 不正确; D、乙的溶解度随温度的升高变化不大,所以要从含有少量甲的乙溶液中得到较多的乙晶 体,应采用蒸发结晶的方法,故 D 不正确。故选 A。 【点睛】 乙的溶解度随温度的升高变化不大,从含有少量甲的乙溶液中得到较多的乙晶体,采用蒸 发结晶的方法。
8. 关于如图两种物质的溶解度曲线说法正确的是
A.氯化钠的溶解度减小了 B.溶液中溶质的质量分数减小了 C.溶剂质量减小了 D.溶液变成不饱和溶液了 【答案】 C 【解析】
A、温度不变溶质的溶解度不变,错误; B、析出溶质后溶液仍为这一温度下的饱和溶液,
溶质质量分数不变,错误; C、 饱和食盐水露置在干燥的空气中,水分会不断蒸发减小,正
确; D、析出溶质的溶液所剩溶液一定饱和,错误。故选
C.要从甲物质的饱和溶液中获得晶体甲,可采用降温结晶的方法
D.将丙物质的饱和溶液转化为不饱和溶液可以采用加水或降温的方法 【答案】 B
【解析】
【详解】
A、根据饱和时质量分数的计算式
溶解度 溶解度 +100g × 100%,即溶解度相等则质量分数也相
等, t1℃时甲、丙的溶解度相等,所以要配制溶质质量分数相等的饱和溶液,应该在此温 度,正确;
C. 向烧杯中加入 NH4NO3 固体后,试管 2 中一定有晶体析出
2020-2021年 中考化学溶液 溶解度20篇(附带答案解析)(word)

2020-2021年中考化学溶液溶解度20篇(附带答案解析)(word)一、溶液选择题1.K2CO3和KNO3在不同温度时的溶解度及其溶解度曲线如下。
下列说法错误的是A.t℃在60℃到80℃之间B.t℃时,两种溶液的溶质质量分数不一定相等C.两种饱和液从80℃降温到20℃,析出晶体的质量(不含结晶水)无法比较D.把60℃时的105g KNO3饱和液降温至20℃,能析出晶体73.4g【答案】D【解析】【分析】【详解】A、t℃时K2CO3和KNO3的溶解度相同,由表格中的数据可知,在60℃到80℃之间溶解度都包括126-139间的数值,所以t℃在60℃到80℃之间,故A正确;B、t℃时,两种物质只有是饱和溶液时,溶质质量分数一定相等,则溶质质量分数不一定相等,故B正确;C、等质量的两种饱和液从80℃降温到20℃,析出晶体(不含结晶水)的质量硝酸钾比碳酸钾多,如质量不等,则无法比较,故C正确;D、把60℃时硝酸钾的溶解度为110g,则105g KNO3饱和液中溶剂是50g,溶质是55g,20℃,硝酸钾的溶解度为31.6g,50g水中最多能溶15.8g,所以降温后能析出晶体39.2g,故D不正确。
故选D。
2.盐场晒盐后得到的卤水中含有MgCl2、KCl和MgSO4等物质,它们的溶解度曲线如下图所示。
下列说法正确的是A.MgSO4的溶解度始终随温度的升高而减小B.t1℃时,KCl和MgSO4两溶液所含溶质质量一定相等C.t2℃时,100gMgCl2的饱和溶液中含有agMgCl2D.将t1℃时的KCl饱和溶液升温到t2℃,溶液由饱和变为不饱和【答案】D【解析】【分析】【详解】A、由溶解度曲线可知,MgSO4的溶解度不是始终随温度的升高而减小,故A错误;B、t1℃时,氯化钾和硫酸镁的溶解度相等,如果两种溶液是饱和溶液,并且溶液质量相等,则溶质质量一定相等,但题目未告知两溶液质量是否相等,故B错误;C、t2℃时,溶解度的含义是100g水中最多能溶解ag氯化镁,因此100gMgCl2的饱和溶液中含有氯化镁的质量小于ag,故C错误;D、氯化钾的溶解度随着温度的升高而增大,将t1℃时的KCl饱和溶液升温到t2℃,溶液由饱和溶液变成不饱和溶液,故D正确。
2020-2021中考化学培优 易错 难题(含解析)之化学溶解度及详细答案

2020-2021中考化学培优易错难题(含解析)之化学溶解度及详细答案一、初中化学溶解度1.甲、乙、丙三种固体物质的溶解度曲线如图所示。
下列说法不正确的是( )A.T2℃时,取等质量的甲、乙分别配制成饱和溶液,所需水的质量:甲>乙B.将T1℃时等质量的甲、乙、丙饱和溶液升温到T2℃,所得溶液中溶剂的质量为丙<甲=乙C.若甲中混有少量的丙,可采用降温结晶的方法提纯甲D.T1℃时,100g甲溶液中含甲物质的质量小于30克【答案】A【解析】【分析】【详解】A、T2℃时,甲物质的溶解度大于乙物质的溶解度,所以取等质量的甲、乙分别配制成饱和溶液,所需水的质量:甲<乙,故A错误;B、T1℃时等质量的甲、乙、丙饱和溶液中,丙物质的溶解度最大则溶剂最少,甲、乙物质的溶剂质量相等,所以升温到 T2℃,所得溶液中溶剂的质量为丙<甲=乙,故B正确;C、甲物质的溶解度受温度变化影响较大,所以若甲中混有少量的丙,可采用降温结晶的方法提纯甲,故C正确;D、T1℃时,甲物质的溶解度是30g,所以100g 甲溶液中含甲物质的质量小于30克,故D 正确。
故选A。
2.如图是甲、乙两种固体物质的溶解度曲线,下列说法正确的是()A.甲和乙的溶解度相等B.乙的溶解度受温度影响比甲大C.降低温度可使接近饱和的甲或乙溶液变为饱和D.10℃时,甲、乙的饱和溶液中所含溶质质量一定相等【答案】C【解析】试题分析:A、没有温度限制不能比较溶解度的大小,故A错;B、由图示可知甲的溶解度曲线较陡,所以乙的溶解度受温度影响比甲小,故B错;C、降温后甲和乙的溶解度都变小,所以由不饱和变为饱和溶液,故C正确;D、不知道溶液的质量,没法比较含溶质质量的大小.故D错.故选C.考点:固体溶解度曲线及其作用;饱和溶液和不饱和溶液相互转变的方法.点评:溶解度曲线能定量地表示出溶解度变化的规律,从溶解度曲线可以看出:同一溶质在不同温度下的溶解度;同一温度下,不同溶质的溶解度;温度对不同物质的溶解度影响不同.3.如图是X、Y、Z三种固体物质的溶解度曲线图,以下说法错误的是A.要配制相同浓度的Y、Z饱和溶液,需要把温度控制在t2℃B.t1℃时,将X、Y、Z的饱和溶液都升温到t3℃,仍然是饱和溶液C.t3℃时,将X、Y、Z的饱和溶液都降温到t1℃,溶液中溶质质量分数由大到小的顺序为Y>Z>XD.若0℃时,Y的溶解度为20g,此温度下Y饱和溶液的质量分数是16.7%【答案】B【分析】【详解】A、要配制相同浓度的Y、Z饱和溶液,需要把温度控制在t2℃正确,因为此温度下两物质的溶解度相等,正确但不符合题意,故选项错误;B、t1℃时,将X、Y、Z的饱和溶液都升温到t3℃,仍然是饱和溶液错误,X、Y的溶解的都随温度升高而增大,属于不饱和溶液,Z的溶解度随温度升高而减小,是饱和溶液,错误符合题意,故选项正确;C、根据溶解度曲线可知,t3℃时,将X、Y、Z的饱和溶液都降温到t1℃,溶液中溶质质量分数由大到小的顺序为Y>Z>X正确,正确但不符合题意,故选项错误;D、若0℃时,Y的溶解度为20g,此温度下Y饱和溶液的质量分数=20g120g×100%≈16.7%,正确但不符合题意,故选项错误;故选B。
2020-2021中考化学综合题专练∶化学溶解度附详细答案

2020-2021中考化学综合题专练∶化学溶解度附详细答案一、初中化学溶解度1.如图是a、b、c三种物质的溶解度曲线,下列说法错误的是A.t2℃时a、b、c三种物质的溶解度由大到小的顺序是a>b>cB.P点表示t1℃时,a、c两种物质的溶解度相等C.将c的饱和溶液变为不饱和溶液,可采用降温的方法D.t2℃时,将30g a物质加入到50g水中充分搅拌,得到80g a的饱和溶液【答案】D【解析】试题分析:依据图形,A、B、C正确; t2℃时,a的溶解度为50g,则t2℃时,将30g a物质加入到50g水中充分搅拌时只能溶解25ga物质,则75ga的饱和溶液,D错误。
考点:溶解度曲线。
2.甲、乙两种固体物质(均不含结晶水)的溶解度曲线如图所示,下列说法错误的是()A.t1℃时,甲、乙的溶解度相等B.t2℃时,甲的溶解度为50C.甲中混有少量的乙时,可用降温结晶的方法提纯甲D.t1℃时,甲、乙两种饱和溶液恒温蒸发等质量的水,析出晶体的质量相等【答案】B【解析】【详解】A、通过分析溶解度曲线可知,t1℃时,甲、乙的溶解度相等,故A正确,不符合题意;B、t2℃时,甲的溶解度为50g,题中未加单位,故B错误,符合题意;C、甲物质的溶解度受温度变化影响较大,所以甲中混有少量的乙时,可用降温结晶的方法提纯甲,故C正确,不符合题意;D、t1℃时,甲、乙的溶解度相等,所以甲、乙两种饱和溶液恒温蒸发等质量的水,析出晶体的质量相等,故D正确,不符合题意。
故选B。
3.如图为甲、乙两种固体物质(不含结晶水)的溶解度曲线。
下列说法错误的是A.t2℃时,甲的溶解度大于乙B.t1℃时,甲、乙各25g加到50g水中,均得70g溶液C.t1℃时,甲、乙两种物质的溶液中溶质质量分数相等D.t2℃时,将溶剂均为100g的甲、乙的饱和溶液分别降温到t1℃时,析出晶体的质量甲>乙【答案】C【解析】【分析】【详解】A.由图像可知,t2℃时,甲的溶解度大于乙,正确;B、t1℃时,甲、乙两种物质的溶解度是40g,所以各25g分别加入到50g水中,充分溶解,得到的溶液质量都是70g,故B正确;C、t1℃时,溶液的饱和状态不确定,所以甲溶液的溶质质量分数不一定等于乙溶液的溶质质量分数,故C错误;D. t2℃时,甲的溶解度大于乙,将溶剂均为100g的甲、乙的饱和溶液分别降温到t1℃时,析出晶体的质量甲>乙,正确;故选C。
2020-2021中考化学压轴题之化学溶解度(中考题型整理,突破提升)附详细答案

2020-2021中考化学压轴题之化学溶解度(中考题型整理,突破提升)附详细答案一、初中化学溶解度1.下图是A、B、C三种物质的溶解度曲线,下列说法错误的是( )A.将t2℃时A、B、C的饱和溶液同时降温至t1℃后,所得溶液中溶质的质量分数由大到小的顺序是C>B>AB.当A中含有少量B时,可以通过降温结晶的方法提纯AC.升高温度可使接近饱和的C溶液变为饱和D.t1℃时,A、B、C三种物质的溶解度由大到小的顺序是C>B>A【答案】A【解析】A、由溶解度曲线可知,AB两种物质的溶解度随温度的升高而升高,C物质的溶解度随温度的升高和降低,将t2℃时A、B、C的饱和溶液同时降温至t1℃后AB两种物质仍然为饱和溶液,C为不饱和溶液,C溶液中溶质的质量分数不变,t1℃时B的溶解度大于A的溶解度,故B 的质量分数大于A 的质量分数,C 的质量分数小于B的质量分数,故错误;B、A的溶解度随温度的变化较大,B 的溶解度随温度的变化不大,故当A中含有少量B 时,可以通过降温结晶的方法提纯A,正确;C、由图可知,C物质的溶解度随温度的升高而降低,故升高温度可使接近饱和的C溶液变为饱和,正确;D、由图可知,t1℃时,A、B、C三种物质的溶解度由大到小的顺序是C>B>A,正确。
故选A。
2.如图为甲、乙两种固体物质(不含结晶水)的溶解度曲线。
下列说法错误的是A.t2℃时,甲的溶解度大于乙B.t1℃时,甲、乙各25g加到50g水中,均得70g溶液C.t1℃时,甲、乙两种物质的溶液中溶质质量分数相等D.t2℃时,将溶剂均为100g的甲、乙的饱和溶液分别降温到t1℃时,析出晶体的质量甲>乙【答案】C【解析】【分析】【详解】A.由图像可知,t2℃时,甲的溶解度大于乙,正确;B、t1℃时,甲、乙两种物质的溶解度是40g,所以各25g分别加入到50g水中,充分溶解,得到的溶液质量都是70g,故B正确;C、t1℃时,溶液的饱和状态不确定,所以甲溶液的溶质质量分数不一定等于乙溶液的溶质质量分数,故C错误;D. t2℃时,甲的溶解度大于乙,将溶剂均为100g的甲、乙的饱和溶液分别降温到t1℃时,析出晶体的质量甲>乙,正确;故选C。
2020-2021初三培优化学溶解度辅导专题训练及答案

C、 t1℃时, 100g a、 c 两物质的溶液中,溶液状态不能确定,所以含 定,故 C 不正确;
a、 c 的质量不能确
D、 t 2℃时, a 物质的溶解度最大, c 物质的溶解度最小,所以等质量 a、 b、 c 三种物质的
饱和溶液中, c 溶液中的溶剂质量最大,所以温度降低到
0℃时,溶剂质量不变,还是 t 2℃
t 1℃时,甲、乙析出
饱和溶液溶质质量分数 = 溶解度
100%
100g+ 溶解度
6. 如图是甲、乙、丙三种固体物质的溶解度曲线。下列有关说法错误的是(
)
A.丙物质的溶解度随温度的升高而降低
B. T1℃时三种物质的饱和溶液,乙的溶质质量分数最大
C. P 点表示 T2℃时甲、乙两物质的溶解度相等,均为 50%
D. t 2℃时,等质量 a、 b、 c 三种物质的饱和溶液,温度降低到 量最多的是 c
0℃时,所得溶液中溶剂质
【答案】 D
【解析】
【分析】
根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解
性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的
大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶
数大,而 T1℃三种物质的溶解度的大小关系是乙>甲=丙,溶解度最大的是乙,所以三种 物质的饱和溶液中,溶质的质量分数最大的是乙,说法正确;故不符合题意;
C、溶解度曲线的交点表示同一温度下物质的溶解度相等, 溶解度相等,均为 50 g,说法错误;故符合题意;
P 点表示 T2℃时甲、乙两物质的
D、甲的溶解度随温度的升高而增大, Q 点是甲的不饱和溶液,所以保持溶质质量分数不变 的情况下,使处于 Q 点的甲溶液达到饱和状态应采取降温的方法,说法正确;故不符合题
2020-2021备战中考化学培优专题复习化学溶解度练习题含答案

一、初中化学溶解度
1. 饱和溶液用水稀释变成不饱和溶液的过程中,保持不变的是(
)
A.溶质的质量
B.溶剂的质量
C.溶液的质量
D.溶质与溶剂的质量比
【答案】 A
【解析】
【详解】
A 项,饱和溶液用水稀释变成不饱和溶液的过程中,溶质的质量不变,正确;
分析上表中的数据不能得出的结论是(
)
A. KNO3 在水中的溶解度随温度的升高而增大
B. NaCl 在水中的溶解度受温度变化影响不大
C.固体物质在水中溶解度的大小与溶质的种类有关
D.固体物质在水中溶解度的大小与溶剂的种类有关 【答案】 D
【解析】
【详解】
A、由表中的数据可知, KNO3 在水中的溶解度随温度的升高而增大,选项正确;
13. 甲、乙两种固体的溶解度曲线如图所示。下列说法中,正确的是
A.20℃ 时,甲、乙溶液中溶质的质量一定相等 B. 40℃ 时,分别在 100 g 水中加入 45 g 甲、乙,所得甲、乙溶液的溶质的质量分数相等 C. 40℃ 时,将 10%的甲溶液降温至 20℃ ,溶液中溶质的质量分数不变 D. 40℃ 时,将甲、乙的饱和溶液降温至 20℃ ,析出晶体的质量甲大于乙 【答案】 C 【解析】 【分析】 【详解】
8. 图 1 可表示 “M与 N 的并列关系 ”,图 2 可表示 “M属于 N 的从属关系 ”。下列概念间的
关系符合图 3 所示关系的是(
)
选项 A B C D
X 溶质 悬浊液 氧化物 饱和溶液
Y 溶液 乳浊液 单质 不饱和溶液
Z 溶液 溶液 化合物 浓溶液
A. A 【答案】 A
2020-2021九年级培优化学溶解度辅导专题训练及详细答案

2020-2021九年级培优化学溶解度辅导专题训练及详细答案一、初中化学溶解度1.根据如图的溶解度曲线判断,下列说法正确的是A.50℃时,A 物质的溶解度为 80B.20℃时,B 的溶解度大于 A 的溶解度C.升温可使 C 物质的饱和溶液变成不饱和溶液D.将 50℃三种物质的饱和溶液分别降温到 20℃时,A 析出固体最多【答案】B【解析】【详解】A、50℃时,A物质的溶解度为80g,此选项错误;B、通过分析溶解度曲线可知,20℃时,B的溶解度大于A的溶解度,此选项正确;.C、 C物质的溶解度随温度的降低而增大,所以降温可使C物质的饱和溶液变成不饱和溶液,此选项错误;D、将 50℃三种物质的饱和溶液分别降温到20℃时,饱和溶液的质量不能确定,析出晶体的质量也不能确定,此选项错误。
故选B。
2.KNO3和NaNO3的溶解度曲线如图所示。
下列说法正确的是()A.KNO3的溶解度大于NaNO3的溶解度B.t1℃时,在50g水里加入5gKNO3充分溶解,所得溶液中溶质与溶液的质量比为1:6 C.从硝酸钾溶液中获得硝酸钾晶体时,必须采用蒸发溶剂的方法D.分别将t1℃时KNO3、NaNO3饱和溶液加热至t2℃时,KNO3溶液溶质的质量分数小于NaNO3溶液【答案】D【解析】【详解】A. 没有指明温度范围,KNO3的溶解度大于NaNO3的溶解度,说法错误;B. t1℃时,硝酸钾的溶剂给杜是20g,在50g水里加入5gKNO3充分溶解,所得溶液中溶质与溶液的质量比为5g:50g=1:10,故错误;C. KNO3的溶解度受温度影响较大,从硝酸钾溶液中获得硝酸钾晶体时,采用降温结晶的方法,故错误;D. t1℃时,硝酸钾的溶解度小于硝酸钠的溶解度,此时硝酸钾饱和溶液的质量分数小于硝酸钠饱和溶液的质量分数,加热至t2℃时,溶液质量分数不变,KNO3溶液溶质的质量分数仍然小于NaNO3溶液,故正确;故选D。
3.图是A、B、C三种物质的溶解度曲线,当等质量的A、B、C三种物质的饱和溶液同时从t=2℃降温到t=1℃时,其中溶质质量分数没有发生改变的是A.AB.BC.CD.AB【答案】C【解析】试题分析:由题中所给的坐标曲线可知,A、B两物质的溶解度随温度升高而升高,C物质随温度的升高而降低,所以当等质量的A、B、C三种物质的饱和溶液同时从t=2℃降温到t=1℃时,C物质的溶解度增大,没有物质析出,所以溶质质量分数不变,A、B均有溶质析出,所以溶质质量分数减小。
2020-2021九年级化学化学溶解度的专项培优易错难题练习题及答案
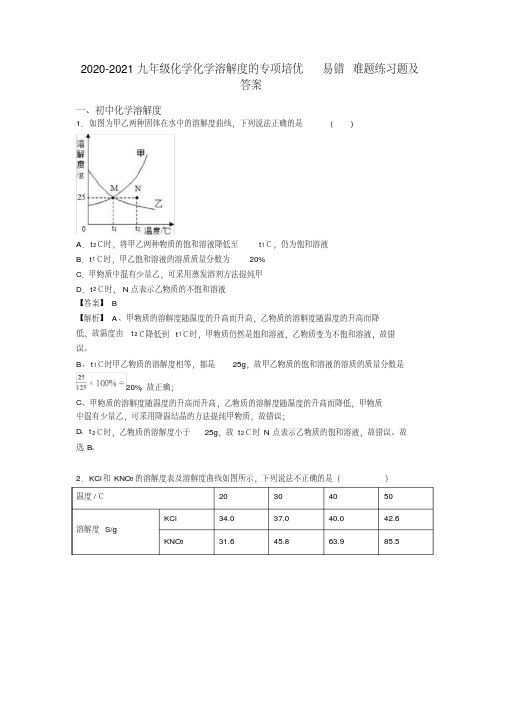
A、 t 1℃时,丙的溶解度为 40g,故丙的饱和溶液中溶质的质量分数为
40g 100% 40%,故选项错误;
40g+100g
B、 t2℃时,甲和乙的溶解度相等,故甲、乙两饱和溶液的溶质质量分数相等,但因为溶液 的质量不确定,故溶质质量不一定相等,故选项错误;
C、甲的溶解度随温度的升高变化明显,故欲从含有少量乙的甲溶液中提纯甲,可采用降温 结晶法,故选项正确;
3. 下图是甲、乙两种固体物质 (不含结晶水 )的溶解度曲线,下列有关说法正确的是 ()
A. t 2℃ 时,在两个各盛有 100g 水的烧杯中,分别加入 50g 的甲、乙两种固体,充分搅 拌,所得甲、乙溶液中溶质的质量不等
B. t1℃ 时,等质量甲、乙溶液中所含溶剂的质量甲等于乙
C.乙中含有少量甲,可以用冷却热饱和溶液的方法提纯甲
【解析】 【详解】
A 项,固体物质的溶解度只受一个外界因素的影响 也就没有意义,错误;
——温度,因此没有说明温度,溶解度
B 项,由两物质的溶解度曲线不难看出,甲的溶解度受温度的影响大,正确;
C 项,由于在 t 2℃ 时,乙的溶解度是 50 g,即在 100 g 水中最多溶解 50 g 乙,错误;
D 项,由于甲的溶解度受温度的影响大,因此相同质量的甲、乙的饱和溶液由
低,故温度由 t 2℃降低到 t 1℃时,甲物质仍然是饱和溶液,乙物质变为不饱和溶液,故错 误。
B、 t 1℃时甲乙物质的溶解度相等,都是 25g,故甲乙物质的饱和溶液的溶质的质量分数是
20%,故正确; C、甲物质的溶解度随温度的升高而升高,乙物质的溶解度随温度的升高而降低,甲物质 中混有少量乙,可采用降温结晶的方法提纯甲物质,故错误; D、 t 2℃时,乙物质的溶解度小于 25g,故 t 2℃时 N 点表示乙物质的饱和溶液,故错误。故 选 B。
2020-2021备战中考化学化学溶解度(大题培优)及答案
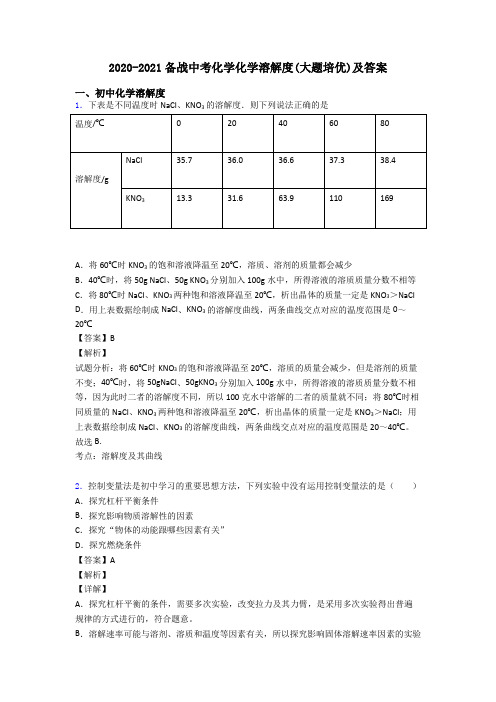
2020-2021备战中考化学化学溶解度(大题培优)及答案一、初中化学溶解度1.下表是不同温度时NaCl、KNO3的溶解度.则下列说法正确的是A.将60℃时KNO3的饱和溶液降温至20℃,溶质、溶剂的质量都会减少B.40℃时,将50g NaCl、50g KNO3分别加入100g水中,所得溶液的溶质质量分数不相等C.将80℃时NaCl、KNO3两种饱和溶液降温至20℃,析出晶体的质量一定是KNO3>NaCl D.用上表数据绘制成NaCl、KNO3的溶解度曲线,两条曲线交点对应的温度范围是0~20℃【答案】B【解析】试题分析:将60℃时KNO3的饱和溶液降温至20℃,溶质的质量会减少,但是溶剂的质量不变;40℃时,将50gNaCl、50gKNO3分别加入100g水中,所得溶液的溶质质量分数不相等,因为此时二者的溶解度不同,所以100克水中溶解的二者的质量就不同;将80℃时相同质量的NaCl、KNO3两种饱和溶液降温至20℃,析出晶体的质量一定是KNO3>NaCl;用上表数据绘制成NaCl、KNO3的溶解度曲线,两条曲线交点对应的温度范围是20~40℃。
故选B.考点:溶解度及其曲线2.控制变量法是初中学习的重要思想方法,下列实验中没有运用控制变量法的是()A.探究杠杆平衡条件B.探究影响物质溶解性的因素C.探究“物体的动能跟哪些因素有关”D.探究燃烧条件【答案】A【解析】【详解】A.探究杠杆平衡的条件,需要多次实验,改变拉力及其力臂,是采用多次实验得出普遍规律的方式进行的,符合题意。
B.溶解速率可能与溶剂、溶质和温度等因素有关,所以探究影响固体溶解速率因素的实验应使用控制变量法,不合题意;C.在速度一定时,质量越大,动能越大;在质量一定时,速度越大,动能越大,采用的是控制变量法,不合题意;D.燃料的燃烧与温度、可燃物种类及氧气浓度都有关系,探究燃烧的条件,需要保持其中两个物理量一定,改变一个物理量,采用的是控制变量法,不合题意。
2020-2021全国中考化学化学溶解度的综合中考真题分类汇总附答案

2020-2021全国中考化学化学溶解度的综合中考真题分类汇总附答案一、初中化学溶解度1.甲、乙两种固体的溶解度曲线如图所示。
下列说法中,正确的是A.20℃时,甲、乙溶液中溶质的质量一定相等B.40℃时,分别在100 g水中加入45 g甲、乙,所得甲、乙溶液的溶质的质量分数相等C.40℃时,将10%的甲溶液降温至20℃,溶液中溶质的质量分数不变D.40℃时,将甲、乙的饱和溶液降温至20℃,析出晶体的质量甲大于乙【答案】C【解析】【分析】【详解】A.没有指明溶液质量,无法确定,故A错误;B.40℃时甲和乙的溶解度分别为50g和40g,故甲全溶,溶液溶质为45g,乙只溶解40g,故两溶液的溶质质量分数不相等,故B错误;C.利用20℃时甲的溶解度为30g和饱和溶液的溶质质量分数的计算公式可得:30g100%23.0% 30g+100g 10%⨯≈>,故C正确;D.没有指明溶液质量,不能比较析出晶体的质量,故D错误。
2.下列有关溶液的说法中,错误的是A.外界条件不改变,溶质不会从溶液中分离出来B.餐具上的油污可利用洗涤剂的乳化功能将其洗去C.相同质量的同一溶质的饱和溶液一定比它的不饱和溶液所含的溶质多D.对于同一溶质的溶液,在同一温度时,其饱和溶液一定比其不饱和溶液浓【答案】C【解析】【分析】【详解】A、溶液是均一的,稳定的混合物,只要外界条件不改变,溶质就不会从溶液中分离出来,说法正确;故不符合题意;B、洗涤剂具有乳化作用,因此餐具上的油污可利用洗涤剂的乳化功能将其洗去,说法正确;故不符合题意;C、同种物质在不同温度下溶解度不同,因此相同质量的同一溶质的饱和溶液不一定比它的不饱和溶液所含的溶质多,说法错误,故不符合题意;D、由于温度一定,溶剂一定,根据溶解度可知,饱和溶液一定比不饱和溶液的质量分数更大;因此对于同一溶质的溶液,在同一温度时,其饱和溶液一定比其不饱和溶液浓,说法正确;故不符合题意;故选C【点睛】溶液是均一的、稳定的混合物,物质的溶解度随温度的变化而变化,若温度不变,则溶解度不改变。
2020-2021年 中考化学溶液 溶解度20篇(附带答案解析)经典

2020-2021年 中考化学溶液 溶解度20篇(附带答案解析)经典一、溶液选择题1.下图是甲、乙、丙三种固体物质的溶解度曲线,下列说法错误的是( )A .将等量甲、乙的饱和溶液从t3℃降到t2℃,析出甲的质量大大B .t2℃时,甲和乙的饱和溶液各100 g ,其溶质的质量一定相等C .分别将t3℃时甲、乙、丙的饱和溶液降温至t1℃,则所得的三种溶液中溶质的质量分数大小关系是乙>甲>丙D .t1℃时,丙的饱和溶液中溶质的质量分数为40%【答案】D【解析】A 、将相同质量甲、乙的饱和溶液从t 3℃降到t 2℃,可通过比较甲、乙两物质在t 2℃和t 3℃时溶解度的差的大小作出判断,差值大析出晶体多。
由溶解度曲线可知,t 2℃时两物质的溶解度相等,而t 3℃时甲物质的溶解度大于乙,故析出甲的质量大,正确;B 、据溶解度曲线知,t 2℃时,甲和乙两种溶液的溶解度相同,故t 2℃时,甲和乙的饱和溶液各100g ,其溶质的质量一定相等,正确;C 、甲、乙的溶解度随温度的升高而增大,丙的溶解度随温度的升高而减小,t 3℃时甲、乙、丙的溶解度大小关系是甲>乙>丙,由于饱和溶液中饱和时质量分数的计算式: =?100%+100溶解度溶质的质量分数溶解度,即溶解度越大质量分数也就越大,故t 3℃时甲、乙、丙的溶质质量分数大小关系是甲>乙>丙;降温至t 1℃,甲、乙析出晶体,依然是饱和溶液,此时溶解度大小关系是乙>甲,丙降温后变为不饱和溶液,溶质的质量分数与t 3℃时相等,而t 3℃时丙的溶解度小于t 1℃时甲的溶解度,则所得的三种溶液中溶质的质量分数大小关系是乙>甲>丙,正确;D 、饱和溶液中=?100%+100溶解度溶质的质量分数溶解度知。
t 1℃时,丙的饱和溶液中40g =?100%40g+100g溶质的质量分数<40%,错误。
故选D 。
2.下图是甲、乙两种固体物质在水中的溶解度曲线。
下列说法不正确的是A.10℃时,甲、乙两种物质的饱和溶液浓度相同B.保持20℃,蒸发溶剂可使接近饱和的乙溶液变成饱和溶液C.30℃时,将40g甲物质加入50g水中,充分溶解后溶液的质量为80gD.10℃时,将两种饱和溶液升温至30℃,溶液中溶质的质量分数都增大【答案】D【解析】【分析】【详解】A、根据溶解度曲线,10℃时,甲、乙的溶解度都是20g,故甲、乙两种物质的饱和溶液浓度相同,选项A正确;B、保持20℃,蒸发溶剂可使接近饱和的乙溶液变成饱和溶液,选项B正确;C、根据溶解度曲线,30℃时,甲物质的溶解度为60g,故将40g甲物质加入到50g水中并充分搅拌,只能溶解30g,故充分溶解后溶液的质量为80g,选项C正确;D、根据溶解度曲线,物质甲、乙的溶解度都随温度的升高而增大,故10℃时,将两种饱和溶液升温至30℃,都成为30℃时的不饱和溶液,但溶液中的溶质、溶剂质量都不变,故溶质质量分数也不变,选项D错误。
2020-2021中考化学化学溶解度培优易错试卷练习(含答案)及答案

2020-2021中考化学化学溶解度培优易错试卷练习(含答案)及答案一、初中化学溶解度1.下图是甲、乙两种固体物质的溶解度曲线。
下列说法中错误的是( )A .20℃时,甲、乙饱和溶液中溶质质量分数相等B .40℃时,甲的溶解度大于乙的溶解度C .40℃时,乙的饱和溶液中溶质的质量分数为40%D .将40℃甲的饱和溶液降温到20℃,会有晶体析出【答案】C 【解析】A 、由溶解度曲线可知,20 ℃时,甲、乙两种物质的溶解度相等,根据饱和溶液的溶质质量分数=100100g溶解度%溶解度,故20 ℃时,甲、乙饱和溶液中溶质质量分数相等,正确;B 、由溶解度曲线可知,40 ℃时,甲的溶解度大于乙的溶解度,正确;C 、由图可知,40 ℃时,乙的溶解度为40 g ,故40 ℃时,乙的饱和溶液中溶质的质量分数为40g 100100g40g%=28.6%,故错误;D 、甲物质的溶解度随温度的升高而升高,故将40 ℃甲的饱和溶液降温到20 ℃,会有晶体析出,正确。
故选C 。
2.如图是X 、Y 、Z 三种固体的溶解度曲线,下列有关说法中不正确的是()A .Z 的溶解度随温度的升高而降低B .t 1℃时,Y 的溶解度大于Z 的溶解度C .t 3℃时,X 的饱和溶液中溶质的质量分数为40%D .t 2℃时,X 的溶解度和Y 的溶解度相等【答案】C【解析】根据溶解度曲线,可以看出物质的溶解度随着温度的变化而变化的情况;还可以判断或比较某一物质在不同温度下的溶解度大小;饱和溶液中溶质的质量分数=×100%。
观察溶解度曲线,可以看出Z的溶解度随温度的升高而降低,A正确;观察溶解度曲线,可以看出t1℃时,Y的溶解度大于Z的溶解度,B正确;观察溶解度曲线,可以看出t3℃时,X的溶解度是100g,所以其饱和溶液溶质的质量分数是:×100%=50%,故C错误;观察溶解度曲线,可以看出t2℃时,X的溶解度和Y的溶解度相交于一点,说明二者的溶解度在此温度下相等, D正确。
2020-2021全国中考化学化学溶解度的综合中考真题分类汇总附详细答案

2020-2021全国中考化学化学溶解度的综合中考真题分类汇总附详细答案一、初中化学溶解度1.根据如图的溶解度曲线,判断下列说法中不正确的是( )A .t 1℃时,甲物质的溶解度小于乙物质的溶解度B .t 2℃时,甲、乙两物质的饱和溶液中含甲、乙两物质的质量相等C .将t 3℃的甲、乙两物质的饱和溶液降温至t 2℃时,都会析出晶体D .当甲物质中混有少量乙物质时,可采用冷却热饱和溶液的方法提纯甲 【答案】B 【解析】A 、t 1℃时,甲物质的溶解度小于乙物质的溶解度,正确;B 、t 2℃时,等质量的甲、乙两物质的饱和溶液中含甲、乙两物质的质量相等,错误;C 、甲和乙的溶解度都随温度的升高而增大,故将t 3℃的甲、乙两物质的饱和溶液降温至t 2℃时,都会析出晶体,正确;D 、甲的溶解度受温度影响变化大,故当甲物质中混有少量乙物质时,可采用冷却热饱和溶液的方法提纯甲,正确; 故选B .【点评】解答本题的关键是知道溶解度曲线表示的意义,交点表示的意义,物质从溶液中结晶析出的方法等知识,考查了学生分析、解决问题的能力.2.现有30℃时的氯化钾饱和溶液,在下列情况下溶液中溶质的质量分数不变的是( )A .温度不变,向溶液中加入氯化钾晶体B .温度不变,向溶液中加入水C .降低温度至10℃D .升高温度蒸发掉一部分水,温度保持在40℃ 【答案】A 【解析】 【分析】=100% 溶质质量溶质的质量分数溶液质量【详解】A 、因温度不变,虽向溶液中加入氯化钾晶体,但溶质及溶液的质量未变,溶质的质量分数也不变,故A正确;B、因溶液的质量变了,所以溶质的质量分数也相应发生变化,故B不正确;C、降低温度有晶体析出,溶剂质量不变,其溶质的质量分数变小,故C不正确;D、因溶液中溶剂质量减小,所以溶质的质量分数将增大,故D不正确。
故选A。
3.几种固体物质在水中的溶解度如下表所示:温度/℃2030405060溶解度/g NaCl36.036.336.637.037.3 KNO331.645.863.985.5110 Ca(OH)20.170.150.130.120.11分析上表中的数据不能得出的结论是()A.KNO3在水中的溶解度随温度的升高而增大B.NaCl在水中的溶解度受温度变化影响不大C.固体物质在水中溶解度的大小与溶质的种类有关D.固体物质在水中溶解度的大小与溶剂的种类有关【答案】D【解析】【详解】A、由表中的数据可知,KNO3在水中的溶解度随温度的升高而增大,选项正确;B、由表中的数据可知,NaCl在水中的溶解度受温度变化影响不大,选项正确;C、由表中的数据可知,不同溶质的溶解度在同一温度的溶解度不同,可以得出固体物质在水中溶解度的大小与溶质的种类有关,选项正确;D、由题意可知,表中的数据是不同物质在水中的不同温度时的溶解度,溶剂相同,得不出固体物质在水中溶解度的大小与溶剂的关系,选项错误,故选D。
2020-2021中考化学化学溶解度(大题培优 易错 难题)含答案

2020-2021中考化学化学溶解度(大题培优易错难题)含答案一、初中化学溶解度1.固体硝酸钾的溶解度曲线如图所示,下列说法正确的是()A.70℃时,硝酸钾的溶解度为114B.70℃时,C点为硝酸钾的不饱和溶液C.70℃时,B点为硝酸钾的饱和溶液D.A、C两点对应溶液的溶质质量分数相同【答案】D【解析】A、由溶解度曲线可知,70℃时,硝酸钾的溶解度为144g,故A错误;B、由溶解度曲线可知,70℃时,C点在溶解度曲线的上面,应为硝酸钾的饱和溶液,故B 错误;C、由溶解度曲线可知,70℃时,B点在溶解度曲线的下面,应为硝酸钾的不饱和溶液,故C错误;D、由溶解度曲线可知,A、C两点对应溶液的都是同一温度下同一种溶质的饱和溶液,溶液中溶质的质量分数是一定值,所以,A、C两点对应溶液的溶质质量分数相同.故D正确.故选D.2.下列有关溶液的说法中,错误的是A.外界条件不改变,溶质不会从溶液中分离出来B.餐具上的油污可利用洗涤剂的乳化功能将其洗去C.相同质量的同一溶质的饱和溶液一定比它的不饱和溶液所含的溶质多D.对于同一溶质的溶液,在同一温度时,其饱和溶液一定比其不饱和溶液浓【答案】C【解析】【分析】【详解】A、溶液是均一的,稳定的混合物,只要外界条件不改变,溶质就不会从溶液中分离出来,说法正确;故不符合题意;B、洗涤剂具有乳化作用,因此餐具上的油污可利用洗涤剂的乳化功能将其洗去,说法正确;故不符合题意;C、同种物质在不同温度下溶解度不同,因此相同质量的同一溶质的饱和溶液不一定比它的不饱和溶液所含的溶质多,说法错误,故不符合题意;D、由于温度一定,溶剂一定,根据溶解度可知,饱和溶液一定比不饱和溶液的质量分数更大;因此对于同一溶质的溶液,在同一温度时,其饱和溶液一定比其不饱和溶液浓,说法正确;故不符合题意;故选C【点睛】溶液是均一的、稳定的混合物,物质的溶解度随温度的变化而变化,若温度不变,则溶解度不改变。
3.下图是甲、乙两种固体物质(不含结晶水)的溶解度曲线,下列有关说法正确的是()A.t2℃时,在两个各盛有100g水的烧杯中,分别加入50g的甲、乙两种固体,充分搅拌,所得甲、乙溶液中溶质的质量不等B.t1℃时,等质量甲、乙溶液中所含溶剂的质量甲等于乙C.乙中含有少量甲,可以用冷却热饱和溶液的方法提纯甲D.t2℃时,将甲、乙的饱和溶液降温至t1℃,甲溶液析出晶体的质量大于乙【答案】A【解析】试题分析:A、从溶解度曲线可看出,t2℃时,甲的溶解度=50g,而乙的溶解度<50g,故在两个各盛有l00g水的烧杯中,分别加入50g的甲、乙两种固体,充分搅拌,甲能全部溶解,而乙有剩余,故所得甲、乙溶液中溶质的质量不等,正确,B、t1℃时,甲、乙物质的溶解度相等,但没有指明是饱和溶液,故等质量甲、乙溶液中所含溶剂的质量甲不一定等于乙,错误, C、从溶解度曲线可看出,甲的溶解度随温度的升高变化较大,而乙的溶解度随温度的升高而变化较小,故乙中含有少量甲,可以用冷却热饱和溶液的方法提纯乙,错误,D、没有指明高温时的溶液是否是等质量,故无法判断析出晶体量的多少,错误,故选A考点:溶解度曲线的意义4.下图是M、N两种物质的溶解度曲线,由溶解度曲线得出以下几条信息,你认为错误的是()A.t1℃时,M、N两物质溶液的溶质质量分数相等B.N物质的溶解度随温度的升高而降低C.t2℃时,M物质的溶解度大于N物质的溶解度D.由t1℃升温到t2℃时,N物质溶液的溶质质量分数可能改变【答案】A【解析】试题分析:有溶解度曲线图可知A.t1℃时,M、N两物质溶液溶质质量分数相等是错误的叙述,没有说明溶液是否饱和;B选项N物质的溶解度随温度的升高而降低是正确的叙述;C选项t2℃时,M物质的溶解度大于N物质的溶解度D选项由t1℃升温到t2℃时,N 物质溶液溶质质量分数可能改变是正确的叙述,看是否加入溶质;故选A考点:溶解度曲线5.如图是甲、乙、丙三种固体物质的溶解度曲线,下列说法正确的是()A.t1℃时,丙的饱和溶液中溶质的质量分数为40%B.t2℃时,甲、乙两饱和溶液的溶质质量相等C.欲从含有少量乙的甲溶液中提纯甲,可采用降温结晶法D.分别将t3℃时甲、乙、丙的饱和溶液降温至t1℃,则所得三种溶液中溶质的质量分数大小关系是乙>丙>甲【答案】C【解析】【详解】A、t1℃时,丙的溶解度为40g,故丙的饱和溶液中溶质的质量分数为40g⨯≠40%,故选项错误;100%40g+100gB、t2℃时,甲和乙的溶解度相等,故甲、乙两饱和溶液的溶质质量分数相等,但因为溶液的质量不确定,故溶质质量不一定相等,故选项错误;C、甲的溶解度随温度的升高变化明显,故欲从含有少量乙的甲溶液中提纯甲,可采用降温结晶法,故选项正确;D、分别将t3℃时甲、乙、丙的饱和溶液降温至t1℃,甲和乙的溶解度减小,且甲变化明显,故甲、乙均有晶体析出,而丙的溶解度增大,溶液的组成不变,故则所得三种溶液中溶质的质量分数大小关系是乙>甲>丙,故选项错误。
2020-2021中考化学二轮 化学溶解度 专项培优附详细答案

2020-2021中考化学二轮化学溶解度专项培优附详细答案一、初中化学溶解度1.常温下,将盛有KNO3饱和溶液的试管插入盛有冰水混合物的烧杯中,如图所示.下列说法正确的是()A.试管内溶液中溶质的质量不变B.试管内溶液总质量不变C.硝酸钾的溶解度不变D.试管内水的质量不变【答案】D【解析】【详解】A.硝酸钾的溶解度随着温度的降低而减小,将盛有KNO3饱和溶液的试管插入盛有冰水混合物的烧杯中,温度降低,硝酸钾的溶解度减小,有硝酸钾晶体析出,试管内溶液中溶质的质量减小,故选项说法错误。
B.由A选项的分析,试管内溶液中溶质的质量减小,溶剂的质量不变,则试管内溶液总质量减小,故选项说法错误。
C.硝酸钾的溶解度随着温度的降低而减小,将盛有KNO3饱和溶液的试管插入盛有冰水混合物的烧杯中,温度降低,硝酸钾的溶解度减小,故选项说法错误。
D.硝酸钾的溶解度随着温度的降低而减小,将盛有KNO3饱和溶液的试管插入盛有冰水混合物的烧杯中,温度降低,硝酸钾的溶解度减小,有硝酸钾晶体析出,溶液中溶剂的质量不变,故选项说法正确。
故选:D。
【点睛】本题难度不大,掌握硝酸钾的溶解度受温度影响的变化趋势、温度改变后溶液组成的变化是正确解答本题的关键.2.如图是A、B、C三种固体物质的溶解度曲线。
下列分析正确的是()A.t1℃时,A、C两种物质的饱和溶液中溶质的质量相等B.t2℃时,把50gA放入50g水中能得到A的饱和溶液,其中溶质和溶液的质量比为1:3 C.将t2℃时A、B、C三种物质的饱和溶液降温到t1℃,所得溶液的溶质质量分数的大小关系是B=C>AD.将t1℃时C的饱和溶液变为不饱和溶液,可采用的方法是升高温度【答案】B【解析】【详解】A、t1℃时,A、C两种物质的溶解度相等,但是饱和溶液的质量不能确定,所以饱和溶液中溶质的质量也不能确定,选项错误;B、t2℃时,A物质的溶解度是50g,所以把50gA放入50g水中能得到A的饱和溶液,其中溶质和溶液的质量比为25g:75g=1:3,选项正确;C、t1℃时,B物质的溶解度最大,A、C物质的溶解度相等,降低温度,A、B物质的溶解度减小,C物质的溶解度增大,应该按照t2℃时的溶解度计算,所以将t2℃时A、B、C三种物质的饱和溶液降温到t1℃,所得溶液的溶质质量分数的大小关系是B>A>C,选项错误;D、C物质的溶解度随温度的升高而减小,所以将t1℃时C的饱和溶液变为不饱和溶液,可采用的方法是降低温度,选项错误,故选B。
2020-2021中考化学化学溶解度综合经典题含答案
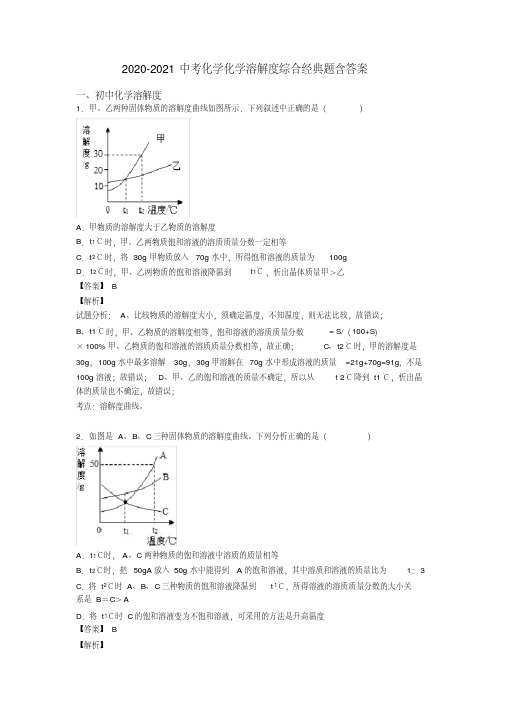
D、 t2℃ 时,甲的溶解度为 110g,用 210 g 甲的饱和溶液加水可以配制成 500g 溶质质量分
110g
数为:
× 100% =22 %的甲溶液,错误。故选 A。
500g
11. 如图是甲、乙、丙三种物质的溶解度曲线,下列说法错误的是(
)
A.要配制相同质量分数的甲、丙两种物质的饱和溶液,应该将温度控制在
)
A. t 1℃时, A、C 两种物质的饱和溶液中溶质的质量相等 B. t2℃时,把 50gA 放入 50g 水中能得到 A 的饱和溶液,其中溶质和溶液的质量比为
1: 3
C.将 t2℃时 A、B、 C 三种物质的饱和溶液降温到 系是 B=C> A
t 1℃,所得溶液的溶质质量分数的大小关
D.将 t1℃时 C 的饱和溶液变为不饱和溶液,可采用的方法是升高温度 【答案】 B
C、 t1℃时, B 物质的溶解度最大, A、 C 物质的溶解度相等,降低温度, 度减小, C 物质的溶解度增大,应该按照 t2℃时的溶解度计算,所以将 种物质的饱和溶液降温到 t 1℃,所得溶液的溶质质量分数的大小关系是 误;
A、 B 物质的溶解 t2℃时 A、 B、 C 三 B> A> C,选项错
500 g 20%的甲溶液
【详解】
A 、 t2℃ 时,甲、乙两种溶液降温至 t l℃ 均有固体析出时,都属于饱和溶液, 物质的溶解度相等,故所得甲、乙溶液溶质质量分数相等,正确;
t l℃ 时甲、乙两
B、甲物质溶解度受温度影响变化较大,所以甲中混有少量乙,可用降温结晶的方法提纯 乙,错误;
C、 tl℃ 时,甲、乙两种饱和溶液的质量不能确定,所以饱和溶液的溶质质量不能确定,错 误;
【解析】
【详解】
2020-2021中考化学 化学溶解度 综合题含答案

2020-2021中考化学化学溶解度综合题含答案一、初中化学溶解度1.下图为甲、乙、丙三种固体物质在水中的溶解度曲线,下列说法正确的是A.50℃时,分别将等质量的甲和乙溶于适量的水恰好配成饱和溶液,所得溶液的质量前者比后者大B.若甲中混有少量的乙,最好采用蒸发结晶的方法提纯甲C.将50℃甲、乙、丙三种物质的饱和溶液降温到10℃,析出晶体最多的是甲D.向100g 50℃的水中加入65g甲固体,发现全部溶解,一段时间后又有部分甲的晶体析出,可能是因为甲物质溶于水显著放热【答案】D【解析】A、50℃时,甲的溶解度大于乙的溶解度,分别将等质量的甲和乙溶于适量的水恰好配成饱和溶液,所需要的水甲比乙少,所得溶液的质量前者比后者小,错误;B、甲的溶解度随温度升高变化明显,当甲溶液中混有少量的乙时,可采用降温结晶提纯甲,错误;C、50℃,甲、乙、丙三种物质的饱和溶液降温到10℃时,不知三种溶液质量大小,故无法判断析出晶体质量多少,错误;D、向100g50℃的水中加入65g甲固体,发现全部溶解,一段时间后又有部分甲的晶体析出,由于甲的溶解度随温度升高而增大,先溶解则说明温度升高了,后析出则说明温度降低了,甲溶于水会放出显著热量,正确。
故选D。
2.图是A、B、C三种物质的溶解度曲线,当等质量的A、B、C三种物质的饱和溶液同时从t=2℃降温到t=1℃时,其中溶质质量分数没有发生改变的是A.AB.BC.CD.AB【答案】C【解析】试题分析:由题中所给的坐标曲线可知,A、B两物质的溶解度随温度升高而升高,C物质随温度的升高而降低,所以当等质量的A、B、C三种物质的饱和溶液同时从t=2℃降温到t=1℃时,C物质的溶解度增大,没有物质析出,所以溶质质量分数不变,A、B均有溶质析出,所以溶质质量分数减小。
考点:溶解度曲线的意义点评:关于溶解度曲线的题目属于中考必考的题型,通常在选择题较为靠后的位置出现,有一定的难度,考生应熟知基础知识点,仔细审题,理解其曲线的含义。
2020-2021九年级中考化学化学溶解度解答题压轴题提高专题练习附详细答案

2020-2021九年级中考化学化学溶解度解答题压轴题提高专题练习附详细答案一、初中化学溶解度1.甲、乙、丙三种固体的溶解度曲线如图所示,下列说法不正确的是A.t2℃时,三种物质的溶解度:甲>乙=丙B.t1℃时,饱和溶液溶质的质量:甲=乙C.t1℃时,甲、乙、丙的饱和溶液升温到t2℃,所得溶质的质量分数:丙>甲=乙D.甲中混有少量乙时,可通过溶解、加热浓缩、冷却结晶的方法提纯【答案】B【解析】【分析】甲乙的溶解度随温度的升高而增大,丙的溶解度随温度升高而减小,甲的溶解度比乙的溶解度受温度影响大;t1℃时,甲、乙溶解度相等,t2℃时,乙丙溶解度相等。
【详解】A、 t2℃时,甲的溶解度最大,乙丙相等,三种物质的溶解度:甲>乙=丙,说法正确,不符合题意;B、 t1℃时,等质量的甲乙饱和溶液中溶质的质量才相等,说法错误,符合题意;C、t1℃时,甲、乙、丙的饱和溶液中溶质质量分数是甲乙相等小于丙,升温到t2℃,甲乙溶质质量分数不变,丙减小,但仍然大于甲乙的溶质质量分数。
所得溶质的质量分数:丙>甲=乙,说法正确,不符合题意;D、甲的溶解度比乙的溶解度受温度影响大。
甲中混有少量乙时,可通过溶解、加热浓缩、冷却结晶的方法提纯甲,说法正确,不符合题意。
故选B。
2.甲、乙两种固体物质(均不含结晶水)的溶解度曲线如图所示,下列说法错误的是()A.t1℃时,甲、乙的溶解度相等B.t2℃时,甲的溶解度为50C.甲中混有少量的乙时,可用降温结晶的方法提纯甲D.t1℃时,甲、乙两种饱和溶液恒温蒸发等质量的水,析出晶体的质量相等【答案】B【解析】【详解】A、通过分析溶解度曲线可知,t1℃时,甲、乙的溶解度相等,故A正确,不符合题意;B、t2℃时,甲的溶解度为50g,题中未加单位,故B错误,符合题意;C、甲物质的溶解度受温度变化影响较大,所以甲中混有少量的乙时,可用降温结晶的方法提纯甲,故C正确,不符合题意;D、t1℃时,甲、乙的溶解度相等,所以甲、乙两种饱和溶液恒温蒸发等质量的水,析出晶体的质量相等,故D正确,不符合题意。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
A.甲溶液中溶质的质量分数随温度升高不断增大 B.t ℃时,甲、乙两物质的溶解度一定相等 C.通过升温可以将甲的饱和溶液变为不饱和溶液 D.乙物质的溶解度随温度升高而增大 【答案】D 【解析】 【详解】 随温度升高,甲的溶解度减低,甲的固体析出,A 错误;起始时甲和乙均为饱和溶液,但
故选 C。
7.几种固体物质在水中的溶解度如下表所示:
温度/℃
20
30
NaCl
36.0
36.3
溶解度/g
KNO3
31.6
45.8
Ca(OH)2
0.17
0.15
40
50
60
36.6
37.0
37.3
63.9
85.5
110
0.13
0.12
0.11
分析上表中的数据不能得出的结论是( ) A.KNO3 在水中的溶解度随温度的升高而增大 B.NaCl 在水中的溶解度受温度变化影响不大 C.固体物质在水中溶解度的大小与溶质的种类有关 D.固体物质在水中溶解度的大小与溶剂的种类有关 【答案】D 【解析】 【详解】 A、由表中的数据可知,KNO3 在水中的溶解度随温度的升高而增大,选项正确; B、由表中的数据可知,NaCl 在水中的溶解度受温度变化影响不大,选项正确; C、由表中的数据可知,不同溶质的溶解度在同一温度的溶解度不同,可以得出固体物质在 水中溶解度的大小与溶质的种类有关,选项正确; D、由题意可知,表中的数据是不同物质在水中的不同温度时的溶解度,溶剂相同,得不 出固体物质在水中溶解度的大小与溶剂的关系,选项错误,故选 D。
5.图是 A、B、C 三种物质的溶解度曲线,当等质量的 A、B、C 三种物质的饱和溶液同时 从 t=2℃降温到 t=1℃时,其中溶质质量分数没有发生改变的是
A.A B.B C.C D.AB 【答案】C 【解析】
试题分析:由题中所给的坐标曲线可知,A、B 两物质的溶解度随温度升高而升高,C 物质 随温度的升高而降低,所以当等质量的 A、B、C 三种物质的饱和溶液同时从 t=2℃降温到 t=1℃时,C 物质的溶解度增大,没有物质析出,所以溶质质量分数不变,A、B 均有溶质析 出,所以溶质质量分数减小。 考点:溶解度曲线的意义 点评:关于溶解度曲线的题目属于中考必考的题型,通常在选择题较为靠后的位置出现, 有一定的难度,考生应熟知基础知识点,仔细审题,理解其曲线的含义。
溶解度 A、根据饱和时质量分数的计算式 溶解度+100g ×100%,即溶解度相等则质量分数也相
等,t1℃时甲、丙的溶解度相等,所以要配制溶质质量分数相等的饱和溶液,应该在此温 度,正确; B、t1℃时甲的溶解度是 20g,即 100g 水中最多溶解 20g 的甲,所以 50g 水中最多溶解
10g
10g,溶质的质量分数是 ×100%≈16.7%,故错误;
C.t3℃时,X 的饱和溶液中溶质的质量分数为 40% D.t2℃时,X 的溶解度和 Y 的溶解度相等 【答案】C 【解析】 根据溶解度曲线,可以看出物质的溶解度随着温度的变化而变化的情况;还可以判断或比 较某一物质在不同温度下的溶解度大小;饱和溶液中溶质的质量分数
=
×100%。观察溶解度曲线,可以看出 Z 的溶解度随温度的升高而降低,A 正
ห้องสมุดไป่ตู้
确;观察溶解度曲线,可以看出 t1℃时,Y 的溶解度大于 Z 的溶解度,B 正确;观察溶解度 曲线,可以看出 t3℃时,X 的溶解度是 100g,所以其饱和溶液溶质的质量分数是:
×100%=50%,故 C 错误;观察溶解度曲线,可以看出 t2℃时,X 的溶解度和 Y 的溶解 度相交于一点,说明二者的溶解度在此温度下相等, D 正确。
6.20℃时,将等质量的 a、b 两种不含结晶水的固体物质,分别加入到盛有 100g 水的烧杯 中,充分搅拌后,现象如图 1;然后升温到 50℃时,现象如图 2;a、b 两种物质的溶解度 曲线如图 3.由这一过程可知( )
A.30℃时 a、b 溶液溶质质量分数不相等 B.40℃时 a、b 溶液溶质质量分数大小无法比较 C.从 20℃到 50℃,b 溶液质量分数不变 D.图 3 中表示 a 的溶解度曲线是 N 【答案】C 【解析】 【分析】 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解 性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的 大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶 的方法达到提纯物质的目的. 【详解】 图 1 中,溶剂质量相等,甲中物质溶解的质量小于乙中物质,所以 M 表示的是 a 物质的溶 解度曲线,N 表示的是 b 物质的溶解度曲线; A、30℃时,甲、乙溶液是否达到饱和状态不能确定,所以甲、乙溶液溶质质量分数也不 能确定,错误; B、40℃时,a 的溶解度大于 b,故二者都是全部溶解,a、b 溶液溶质质量分数大小相等, 错误; C、从 20℃到 50℃,b 溶液质量分数不变,正确; D、M 表示的是 a 物质的溶解度曲线,错误。
2020-2021 中考化学化学溶解度(大题培优)及详细答案
一、初中化学溶解度
1.如图是甲、乙、丙三种物质的溶解度曲线,下列说法错误的是( )
A.要配制相同质量分数的甲、丙两种物质的饱和溶液,应该将温度控制在 t1℃ B.t1℃时,将 30g 甲物质加入到 50g 水中不断搅拌,形成的溶液中溶质的质量分数是 37.5% C.要从甲物质的饱和溶液中获得晶体甲,可采用降温结晶的方法 D.将丙物质的饱和溶液转化为不饱和溶液可以采用加水或降温的方法 【答案】B 【解析】 【详解】
D、将 30℃时甲、乙、丙三种物质的饱和溶液降温至 20℃,甲乙溶解度减小,均析出晶
体,溶质的质量减小,溶质的质量分数减小,丙溶解度增大,溶液中溶质、溶剂的质量不
溶解度
变,溶质的质量分数与降温前相等;饱和溶液中溶质质量分数=
溶解度+100g
×100%,
即溶解度越大质量分数也就越大,20℃时乙的溶解度大于甲的溶解度大于 30℃时丙的溶解
4.如图是 A、B、C 三种固体物质的溶解度曲线。下列分析正确的是( )
A.t1℃时,A、C 两种物质的饱和溶液中溶质的质量相等 B.t2℃时,把 50gA 放入 50g 水中能得到 A 的饱和溶液,其中溶质和溶液的质量比为 1:3 C.将 t2℃时 A、B、C 三种物质的饱和溶液降温到 t1℃,所得溶液的溶质质量分数的大小关 系是 B=C>A D.将 t1℃时 C 的饱和溶液变为不饱和溶液,可采用的方法是升高温度 【答案】B 【解析】 【详解】 A、t1℃时,A、C 两种物质的溶解度相等,但是饱和溶液的质量不能确定,所以饱和溶液 中溶质的质量也不能确定,选项错误; B、t2℃时,A 物质的溶解度是 50g,所以把 50gA 放入 50g 水中能得到 A 的饱和溶液,其中 溶质和溶液的质量比为 25g:75g=1:3,选项正确; C、t1℃时,B 物质的溶解度最大,A、C 物质的溶解度相等,降低温度,A、B 物质的溶解 度减小,C 物质的溶解度增大,应该按照 t2℃时的溶解度计算,所以将 t2℃时 A、B、C 三 种物质的饱和溶液降温到 t1℃,所得溶液的溶质质量分数的大小关系是 B>A>C,选项错 误; D、C 物质的溶解度随温度的升高而减小,所以将 t1℃时 C 的饱和溶液变为不饱和溶液,可 采用的方法是降低温度,选项错误,故选 B。
度,故所得溶液中溶质的质量分数的大小关系是乙>甲>丙,故 D 正确。
故选 B。
【点睛】
硝酸铵溶液水吸收热量,温度降低,影响其他物质的溶解度。
10.如图是甲、乙两种物质(不含结晶水)的溶解度曲线,根据图象及相关知识判断,下列 说法中正确的是( )
A.t2℃时,甲溶液溶质质量分数一定大于乙溶液溶质质量分数 B.甲物质的溶解度一定大于乙物质的溶解度
60g
C、甲的溶解度随温度升高而增大,所以要从甲物质的饱和溶液中获得晶体甲,可采用降温 结晶的方法,正确; D、丙的溶解度随温度升高而减小,所以要使其饱和溶液变为不饱和溶液可采用加溶剂或 降温的方法,正确; 故选 B。
2.如图是 X、Y、Z 三种固体的溶解度曲线,下列有关说法中不正确的是( )
A.Z 的溶解度随温度的升高而降低 B.t1℃时,Y 的溶解度大于 Z 的溶解度
溶解度一定不同,在 t℃时,甲乙的固体质量一样,表示溶解的质量分数不同,故溶解度不 相等,B 错误;甲物质温度升高,溶解度降低,则升温时甲物质的饱和溶液仍然为饱和溶 液,C 错误;由图可知,乙物质随温度升高溶解度增大。D 正确。故选 D。
9.图 1 是甲、乙、丙三种固体物质的溶解度曲线,图 2 是 30℃时,取其中两种固体各 1g 分别放进盛有 10g 水的两支试管中,充分振荡后的溶解情况,下列说法正确的是( )
A.甲物质的溶解度比乙物质的溶解度大
B.加入试管 1 的固体是丙
C.向烧杯中加入 NH4NO3 固体后,试管 2 中一定有晶体析出 D.将 30℃时甲、乙、丙三种物质的饱和溶液各 100g 降温至 20℃,所得溶液中溶质的质
量分数的大小关系是乙>甲>丙
【答案】B
【解析】
【详解】
A、在比较物质的溶解度时,需要指明温度,故 A 错误;
A、t2℃时,甲、乙溶液的状态不能确定,所以溶液中的溶质质量分数不能确定,故 A 不正 确;
B、在比较物质的溶解度时,需要指明温度,故 B 不正确;
C、t1℃时,甲、乙物质的溶解度相等,所以甲、乙两种物质的饱和溶液的溶质质量分数相
等,升温到 t2℃时,溶剂质量不变,溶质质量不变,所得溶液溶质质量分数仍然相等,故 C 正确;
3.如图为甲、乙两种固体物质(不含结晶水)的溶解度曲线。下列说法错误的是
