弱电解质的电离知识点总结
高中化学电离平衡九大知识点

高中化学电离平衡九大知识点一、弱电解质的电离1、定义:电解质:在水溶液中或熔化状态下能导电的化合物,叫电解质。
非电解质:在水溶液中或熔化状态下都不能导电的化合物。
强电解质:在水溶液里全部电离成离子的电解质。
弱电解质:在水溶液里只有一部分分子电离成离子的电解质。
2、电解质与非电解质本质区别:电解质——离子化合物或共价化合物非电解质——共价化合物注意:①电解质、非电解质都是化合物②SO2、NH3、CO2等属于非电解质③强电解质不等于易溶于水的化合物(如BaSO4不溶于水,但溶于水的BaSO4全部电离,故BaSO4 为强电解质)——电解质的强弱与导电性、溶解性无关。
3、电离平衡:在一定的条件下,当电解质分子电离成离子的速率和离子结合成时,电离过程就达到了平衡状态,这叫电离平衡。
4、影响电离平衡的因素:A、温度:电离一般吸热,升温有利于电离。
B、浓度:浓度越大,电离程度越小;溶液稀释时,电离平衡向着电离的方向移动。
C、同离子效应:在弱电解质溶液里加入与弱电解质具有相同离子的电解质,会减弱电离。
D、其他外加试剂:加入能与弱电解质的电离产生的某种离子反应的物质时,有利于电离。
5、电离方程式的书写:用可逆符号弱酸的电离要分布写(第一步为主)6、电离常数:在一定条件下,弱电解质在达到电离平衡时,溶液中电离所生成的各种离子浓度的乘积,跟溶液中未电离的分子浓度的比是一个常数。
叫做电离平衡常数,(一般用Ka表示酸,Kb表示碱。
)表示方法:ABA++B- Ki=[ A+][B-]/[AB]7、影响因素:a、电离常数的大小主要由物质的本性决定。
b、电离常数受温度变化影响,不受浓度变化影响,在室温下一般变化不大。
C、同一温度下,不同弱酸,电离常数越大,其电离程度越大,酸性越强。
如:H2SO3>H3PO4>HF>CH3COOH>H2CO3>H2S>HClO二、水的电离和溶液的酸碱性1、水电离平衡:水的离子积:KW= c[H+]·c[OH-]25℃时,[H+]=[OH-] =10-7 mol/L ; KW= [H+]·[OH-] = 1*10-14注意:KW只与温度有关,温度一定,则KW值一定KW不仅适用于纯水,适用于任何溶液(酸、碱、盐)2、水电离特点:(1)可逆(2)吸热(3)极弱3、影响水电离平衡的外界因素:①酸、碱:抑制水的电离 KW〈1*10-14②温度:促进水的电离(水的电离是吸热的)③易水解的盐:促进水的电离 KW 〉1*10-144、溶液的酸碱性和pH:(1)pH=-lgc[H+](2)pH的测定方法:酸碱指示剂——甲基橙、石蕊、酚酞。
弱电解质的电离平衡考点归纳

弱电解质的电离平衡考点归纳弱电解质电离平衡是电解质理论的基础,也是中学化学基本理论中的重要组成部分,近几年高考命题中反复考查。
在学生已经学过化学平衡理论并了解电解质在水溶液中发生电离和离子间发生反应等知识的基础上,进一步学习弱电解质的电离平衡。
高考命题的热点主要有影响弱电解质电离平衡因素,通过图象分析弱电解质和强电解质,电离常数和电离度等,为了更好的学习这一部分内容,本文做了详细的总结和归纳,希望对同学们的学习有所启发,达到触类旁通的效果。
一、弱电解质电离平衡1.电离平衡概念一定条件(温度、浓度)下,分子电离成离子的速率和离子结合成分子的速率相等,溶液中各分子和离子的浓度都保持不变的状态叫电离平衡状态,简称电离平衡。
任何弱电解质在水溶液中都存在电离平衡,达到平衡时,弱电解质在该条件下的电离程度最大。
2.电离平衡的特征电解质的电离平衡属于化学平衡中的一种形式,具有以下一些特征:“逆”——弱电解质的电离是可逆的,存在电离平衡“动”——电离平衡是动态平衡“等”——v(=v(分子化)≠0离子化)“定”——达到电离平衡状态时,溶液中分子和离子的浓度保持不变,是一个定值“变”——电离平衡是相对的,外界条件改变时,平衡被破坏,发生移动形成新的平衡。
二、影响弱电解质电离平衡的因素(符合勒?夏特列原理)1.内因:弱电解质本身的性质,是决定性因素。
2.外因①温度: 升高温度,由于电离过程吸热,平衡向电离方向移动,电离程度增大。
②浓度: 加水稀释,使弱电解质的浓度减小,电离平衡向电离的方向移动,电离程度增大。
因为溶液浓度越小,离子相互碰撞结合成分子的机会越小,弱电解质的电离程度就越大;所以,稀释溶液会促进弱电解质的电离。
例如:在醋酸的电离平衡CH3COOH CH3COO-+H+A 加水稀释,平衡向正向移动,电离程度变大,但c(CH3COOH)、c(H+)、c(CH3COO-)变小;B 加入少量冰醋酸,平衡向正向移动,c(CH3COOH)、c(H+)、c(CH3COO-)均增大但电离程度小;③外加相关物质(同离子效应)例如:0.1 mol/L的CH 3COOH溶液CH3COOH CH3COO-+ H+向其中加入CH3COONa固体,溶液中c(CH3COO-)增大,CH3COOH的电离平衡向左移动,电离程度减小,c(H+)减小,pH增大。
(完整版)弱电解质的电离知识点总结精品,推荐文档

【选修四】弱电解质的电离知识要点与方法指导【知识要点】一、电解质有强弱之分(不同的电解质在水溶液中的电离程度是不一样的)1、知识回顾:电解质:在水溶液中或熔化状态下能够导电的化合物 例:酸、碱、盐、H2O等 非电解质:在水溶液和熔化状态下都不能导电的化合物 例:大多数有机物、SO3、CO2等2、强、弱电解质: ⑴观察试验3-1:得出强电解质与弱电解质的概念 实验3-1:体积相同、浓度相同的盐酸和醋酸与等量镁条(Mg条使用前应用砂纸除去表面的氧化膜)反应,并测量溶液的pH值。
实验表明浓度相同的盐酸和醋酸溶液的pH值不同,并且1mol/L HCl与镁条反应剧烈,而1 mol/L CH3COOH与镁条反应较慢。
说明两种溶液中的H+浓度是不同的。
1 mol/L HCl溶液中氢离子浓度大,氢离子浓度为1 mol/L,说明HCl完全电离;1mol/LCH3COOH溶液中氢离子浓度较盐酸小,小于1 mol/L,说明醋酸在水中部分电离。
所以不同电解质在水中的电离程度不一定相同。
注:反应速率快慢与Mg条的表面积大小及H+浓度有关⑵强、弱电解质的概念 根据电解质在水溶液中离解成离子的程度大小分为强电解质和弱电解质: ①强电解质:在水分子作用下,能完全电离为离子的电解质。
包括大多数盐类、强酸、强碱、部分碱性氧化物等 例:NaCl电离方程式 NaCl = Na++Cl- ②弱电解质:在水分子作用下,只有部分分子电离的电解质。
包括弱酸(如HAc、H2S)、弱碱(如NH3·H2O) 、Al(OH)3、H2O等例:CH 3COOH电离方程式 CH3COOH CH3COO-+H+ 小结:二、弱电解质的电离过程是可逆的(属于化学平衡的一种,符合平衡移动原理) 弱电解质溶于水时,在水分子的作用下,弱电解质分子电离出离子,而离子又可以重新结合成分子。
因此,弱电解质的电离过程是可逆的。
分析CH3COOH的电离过程:CH3COOH 的水溶液中,既有CH3COOH分子,又有CH3COOH电离出的H+和CH3COO-,H+和CH3COO-又可重新结合成CH3COOH分子,因此CH3COOH分子电离成离子的趋向和离子重新碰撞结合成CH3COOH分子的趋向并存,电离过程是可逆的,同可逆反应一样,最终也能达到平衡。
弱电解质的电离
大多数有机物,SO3、CO2 等 说明:溶液导电与否是由内外因共同作用的结果,内因为必须有 电解质,外因在水的作用下两者缺一不可,可用下列图示表示: 电解质 电离 导电
溶液导电性强弱是由溶液中自由移Fra bibliotek离子浓度决定。
讨论以下几种说法是否正确,并说明原因。 讨论以下几种说法是否正确,并说明原因。 1.石墨能导电,所以是电解质。 石墨能导电,所以是电解质。 由于BaSO 不溶于水,所以不是电解质。 2.由于BaSO4不溶于水,所以不是电解质。 盐酸能导电,所以盐酸是电解质。 3.盐酸能导电,所以盐酸是电解质。 4.SO2、NH3、Na2O溶于水可导电,所以均为电 溶于水可导电, 解质。 解质。 实验3 体积相同, 实验3-1:体积相同,氢离子浓度相同的盐酸和醋 酸与等量镁条反应,并测量溶液的pH pH值 酸与等量镁条反应,并测量溶液的pH值
H2PO4 2HPO
4
H+ + H+ +
HPO4 PO4
3-
2-
一(2) 一(3)
就电离本身而言, 就电离本身而言,你推测每一步的电离程 度如何变化,为什么? 度如何变化,为什么?
对于多元酸: 对于多元酸:
多元弱酸是分步电离的, 多元弱酸是分步电离的,K1》K2(一般要 相差10 相差 5)。 多元弱酸的酸性由第一步电离决定。 多元弱酸的酸性由第一步电离决定。 试根据课本中“一些弱酸和弱碱的电离平衡 试根据课本中“ 常数”比较它们的相对强弱。 常数”比较它们的相对强弱。
什么叫强电解质?什么叫弱电解质? 什么叫强电解质?什么叫弱电解质? 在水溶液里全部电离成离子的电解质叫强电 解质;如强酸、强碱、绝大多数盐。 解质;如强酸、强碱、绝大多数盐。 只有一部分分子电离成离子的电解质叫弱电 解质。如弱酸、弱减、 解质。如弱酸、弱减、水。
【知识解析】弱电解质的电离平衡
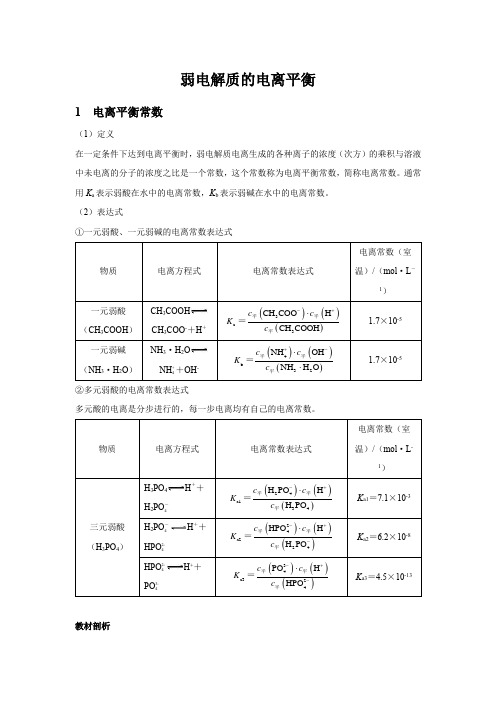
弱电解质的电离平衡1 电离平衡常数(1)定义在一定条件下达到电离平衡时,弱电解质电离生成的各种离子的浓度(次方)的乘积与溶液中未电离的分子的浓度之比是一个常数,这个常数称为电离平衡常数,简称电离常数。
通常用K a表示弱酸在水中的电离常数,K b表示弱碱在水中的电离常数。
(2)表达式①一元弱酸、一元弱碱的电离常数表达式CH3COOHCH3COO-+H+NH3·H2ONH ++OH-4②多元弱酸的电离常数表达式多元酸的电离是分步进行的,每一步电离均有自己的电离常数。
H3PO4H++H2PO-4H2PO-H++4HPO2-4H++HPO2-4PO3-4教材剖析【教材P98】 “多元弱酸的各级电离常数逐级减小。
对于各级电离常数相差很大的多元弱酸,其水溶液中的H +主要是由第一步电离产生的。
”【教材剖析】 多元弱酸第一步电离出H +后,剩余的酸根离子带负电荷,对H +的吸引力增强,使其电离出H +更困难,故一般K a1>>K a2>>K a3……。
因此计算多元弱酸溶液中的c (H+)或比较弱酸酸性的相对强弱时,通常只考虑第一步电离。
(3)意义电离常数表征了弱电解质的电离能力,根据相同温度下电离常数的大小可以判断弱电解质电离能力的相对强弱。
弱酸的电离常数越大,弱酸电离出H +的能力就越强,酸性也就越强;反之,酸性越弱。
如:名师提醒(1)电离常数服从化学平衡常数的一般规律,只受温度的影响。
(2)电离常数相对较大、电离能力较强的弱电解质,其溶液的导电能力不一定强。
这是因为溶液的导电能力与溶液中的离子浓度和离子所带电荷数有关。
(3)相同温度下,等浓度的多种一元弱酸溶液,弱酸的电离常数越大,溶液中c (H +)越大,溶液的导电能力也就越强。
2 电离度(1)定义弱电解质在水中的电离达到平衡状态时,已电离的溶质的分子数占原有溶质分子总数(包括已电离的和未电离的)的百分率称为电离度,通常用α表示。
【知识解析】弱电解质的电离

弱电解质的电离1 电离方程式(1)相关概念电解质在水溶液中或熔融状态下产生自由移动的离子的过程叫做电离。
表示电解质在水溶液中或熔融状态下电离成能够自由移动的离子的式子叫做电离方程式。
(2)电离方程式的书写①强电解质:完全电离,用“===”。
如: HCl===H ++Cl -NaOH===Na ++OH -NaNO 3===Na ++NO - 3 ②弱电解质:部分电离,用“”。
如:CH 3COOH CH 3COO -+H +NH 3·H 2ONH + 4+OH -③多元弱酸的电离分步进行,以第一步电离为主。
如: H 2CO 3H ++HCO - 3(主要) HCO 3-H ++CO 2- 3(次要)④多元弱碱的电离也分步进行,但是一般用一步电离表示。
如: Cu (OH )2Cu 2++2OH -深化理解(1)酸式盐:强酸的酸式盐完全电离,一步完成。
如:NaHSO 4===Na ++H ++SO 2- 4(水溶液),NaHSO 4===Na ++HSO - 4(熔融状态)。
弱酸的酸式盐强中有弱,分步完成。
如:NaHCO 3===Na ++HCO - 3,HCO 3-H ++CO 2- 3。
(2)两性化合物:双向电离。
如:。
2 电离平衡(1)概念电离平衡:一定条件(如一定温度、浓度)下,当弱电解质分子电离成离子的速率和离子重新结合成弱电解质分子的速率相等时,电离过程就达到了平衡状态,这叫做电离平衡。
图3-1-1(2)特征弱电解质电离平衡的特征可概括为六个字——“弱”“逆”“等”“动”“定”“变”。
具体特征为3 弱电解质电离平衡的影响因素注意弱电解质的电离是吸热过程,即ΔH>0。
但也有极少数弱电解质,其电离是放热过程.如HF(aq)H+(aq)+F-(aq)ΔH<0。
(1)内因:电解质本身的性质决定了弱电解质在水中达到电离平衡时电离程度的大小。
(2)外因①温度:一般情况下,由于弱电解质的电离过程吸热,因此升高温度,电离平衡向电离方向移动,电离程度增大。
化学:弱电解质的电离平衡归纳总结

弱电解质得电离平衡考查方式:本章为历年高考考试中考点分布得重点区之一,主要得题型为选择题,偶有简答题,尚未出现过综合性得大题,涉及此内容得考点将基本不变,热点将常考常新,跨学科得综合性大题将有可能出现。
从近几年高考命题规律来瞧,今后得高考试题中这部分内容出来得概率仍然很高,这就是这部分内容在教材中得地位决定得,有关PH值得计算、离子共存、离子浓度大小得比较将仍就是必考点。
命题规律:1.弱电解质得电离平衡电离平衡就是化学平衡理论应用得范例,在化学中占有重要得地位在历年高考均受到重视,近五年得高考题也承继了这个传统。
考查得主要内容集中点比较某些物质导电性强弱;外界条件对弱电解质电离平衡得影响;依据电离平衡移动理论,解释某些问题。
同浓度(或PH)强弱电解质得比较,如氢离子浓度大小,起始反应速率,中与碱得能力、稀释后得PH得变化等。
2.水得电离与溶液得PH以水得电离与溶液pH 计算为考查内容得试题能有效地测试考生得判断、推理、运算等思维能力,仍将就是将来考试得热点。
考试内容包括:(1).已知pH 得强酸、强碱混合,或已知浓度得强酸、强碱混合,计算溶液得pH(2).已知pH或c得强弱酸碱混合,分析溶液得酸碱性。
(3).已知混合溶液得pH,推断混合前得酸碱得各种可能,或已知溶液得pH及强酸、强碱得pH,求混合比例。
(4).中与滴定接近终点时,溶液pH计算。
(5).在新情景下,考查水电离平衡及K w。
3、盐类水解考查得内容有:1.盐对水得电离程度得影响做定性判断或定量计算2.盐溶液蒸干灼烧后产物得判断;3.pH大小得比较;4.离子浓度大小得比较等。
另外,判断离子共存、配制溶液、试剂贮存、化肥得混用、物质鉴别推断、某些盐得分离除杂等内容在高考中也涉及到盐得水解。
其中命题得热点就是离子浓度大小得比较。
在高考试题中,特别就是选择题,常常将盐类水解与弱电解质得电离、酸碱中与滴定、pH等知识融合在一起,具有一定得综合性。
弱电解质的电离(1)

电离平衡是一种 化学平衡 特征:逆、等、动、定、变
反 应 速 率
V(电离) V(结合)
V(电离)
=
V(结合) 电离平衡状态
时间 弱电解质电离平衡状态建立示意图
1、请写出下列物质在水溶液
NH3· H2O
H2CO3
Fe(OH)3
H2SO4
Ba(OH)2
2、下列物质
能导电的是 属于强电解质的是 属于弱电解质的是 属于非电解质的是 ①铜 ④熔融氯化钠 ⑦氯化钾 ②稀硫酸 ⑤氢氧化铝 ⑧氯气 , , , 。 ③氯化氢 ⑥二氧化碳 ⑨胆矾晶体
二、强电解质和弱电解质
1、定义 强电解质:在水溶液中能全部电离成离子的电 解质。 弱电解质:在水溶液中只部分电离成离子的 电解质。 注意: 强弱电解质的区分依据:溶于水的部分是否完全 电离。 (与该物质溶解度的大小,和其水溶液导电能力 的强弱无关 )
2、常见强、弱电解质 常见的强电解质: 强酸、强碱、大部分盐、 活泼金属氧化物、活泼金属过氧化物 常见的弱电解质: 水、弱酸:CH3COOH、H2CO3、H2SO3、 H3PO4、HClO、HF、H2S等 弱碱:NH3· H2O Fe(OH)3 Cu(OH)2 等
第三章 水溶液中的离子平衡
第一节 弱电解质的电离
一、电解质和非电解质
电解质: 在水溶液中或熔融状态时能够导电 的化合物。 (如:酸、碱、盐、水、活泼金属氧化物、活 泼金属过氧化物)
非电解质: 在水溶液中和熔融状态时都不能 导电的化合物。
(如:多数有机物、某些非金属氧化物如SO2、 某些非金属氢化物如 CH4、NH3 等 )
弱电解质的电离平衡知识点

弱电解质的电离平衡知识点集团文件版本号:(M928-T898-M248-WU2669-I2896-DQ586-M1988)一、弱电解质的电离1、定义:电解质:在水溶液中或熔化状态下自身能够电离出自由移动离子的化合物,叫电解质。
非电解质:在水溶液中且熔化状态下自身都不能电离出自由移动离子的化合物。
概念理解:①电解质、非电解质都是化合物,能导电的物质可能是溶液(混合物)、金属(单质),但他们不属于电解质非电解质的研究对象,因此他们既不是电解质也不是非电解质;②自身电离:SO2、NH3、CO2、等化合物能和水反应形成酸或碱,但发生电离的并不是他们本身吗,因此属于非电解质;③只能在水中发生电离的电解质有酸或者某些易溶于水高温下易分解的盐,如液态氯化氢是化合物,只存在分子,没有发生电离,因此不能导电,又如NaHCO3在高温时即分解,不能通过熔融态证明其为电解质;只能在熔融状态下电离的电解质是活泼金属氧化物,如Na2O、CaO,他们在溶液中便不存在,要立刻反应生成键,因此不能通过溶液中产生离子证明;既能在水溶液中又能在溶液中发生电离的物质是某些高温难分解盐,绝大多数盐溶解在水中都能发生完全电离,某些盐熔融时也发生电离,如BaSO4。
④电离不需要通电等外界条件,在熔融或者水溶液中即能够产生离子;⑤是电解质,但是要产生离子也要在溶液状态或者熔融状态,否则即便存在离子也无法导电,比如NaCl ,晶体状态不能导电。
⑥电解质的强弱与导电性、溶解性无关。
如如BaSO 4不溶于水,但溶于水的BaSO 4全部电离,故BaSO 4为强电解质。
导电性与自由移动离子的浓度和带电荷数等有关。
强电解质 :在水溶液里全部电离成离子的电解质。
弱电解质:在水溶液里只有一部分电离成离子的电解质 。
2.常见的电解质为酸碱盐、活泼金属氧化物、水,其中强电解质与偌电解质常见分类:3、电离方程式的书写——“强等号,弱可逆,多元弱酸分步离”①强电解质:如H 2SO 4:H 2SO 4===2H ++SO 2-4 。
高中化学总复习 弱电解质电离的核心知识
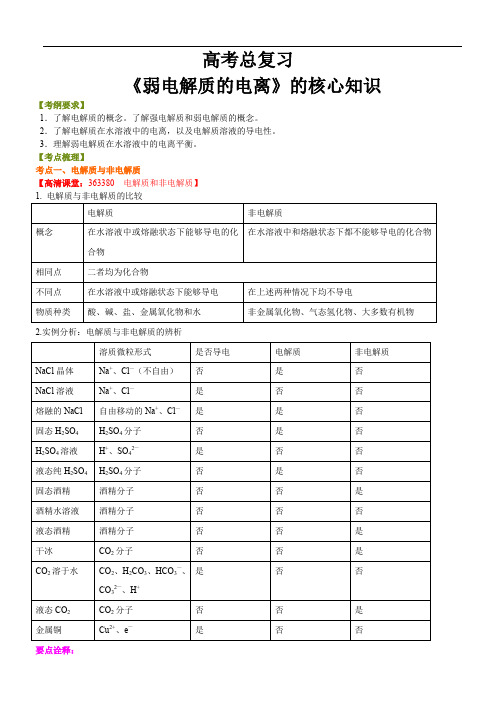
高考总复习《弱电解质的电离》的核心知识【考纲要求】1.了解电解质的概念。
了解强电解质和弱电解质的概念。
2.了解电解质在水溶液中的电离,以及电解质溶液的导电性。
3.理解弱电解质在水溶液中的电离平衡。
【考点梳理】考点一、电解质与非电解质【高清课堂:363380 电解质和非电解质】2.实例分析:电解质与非电解质的辨析要点诠释:(1)溶液导电与否是由内外因共同作用的结果,内因必须有电解质,外因是电解质在水的作用下或加热熔融下,电解质电离出自由移动的离子,自由移动离子浓度越大,导电性越强。
可用下列图示表示:(2)离子型的电解质在水溶液中或熔融状态下都可以导电,如:NaCl、NaOH等,而共价型的电解质只有在水溶液中才能导电,如:H Cl、H2SO4等。
(3).电解质与非电解质均为化合物,金属属于单质,故既不是电解质,也不是非电解质。
考点二、强电解质与弱电解质【高清课堂:363380 强电解质和弱电解质】1、强电解质与弱电解质的比较要点诠释:(1)、CaCO3、Fe(OH)3的溶解度都很小,但二者溶解的部分,CaCO3完全电离,故CaCO3属于强电解质,而Fe(OH)3部分电离,故Fe(OH)3属于弱电解质。
CH3COOH、HCl的溶解度都很大,HCl完全电离,属于强电解质;而CH3COOH部分电离,属于弱电解质。
因此,电解质的强弱与其溶解性大小无必然联系,区分强弱电解质,就看溶解的部分是否完全电离。
(2)电解质的强弱与溶液导电性的强弱也无必然联系。
溶液导电性的强弱取决于溶液中离子浓度大小,浓的弱电解质可能比稀的强电解质导电能力强,只有在相同条件(浓度、温度)下,强电解质才比弱电解质导电能力强。
如:同温、同浓度下盐酸比醋酸导电能力强。
2.电离方程式的书写(1)强电解质用“==”,弱电解质用“”。
如:H2SO4==2H++SO42-;NaHSO4==Na++H++SO42—;Ca(HCO3)2==Ca2++2HCO3—CH3COOH CH3COO- + H+;NH3·H2O NH4+ +OH- ;H2O H++ OH-(2)多元弱酸分步电离,且第一步电离程度远远大于第二步,如碳酸电离方程式:H2CO3H++HCO3―;HCO3―H++CO32―(3)多元弱碱电离方程式一步写出,如氢氧化铁电离方程式:Fe(OH)3Fe3++3OH―(4)两性氢氧化物双向电离,如:H++AlO2―+H2O Al(OH)3Al3++3OH-(5)弱酸的酸式盐强中有弱,如:NaHCO3==Na++HCO3-、HCO3-H++CO32-考点三、弱电解质的电离平衡⒈电离平衡的概念:在一定条件(如温度、浓度)下,当弱电解质分子电离成离子的速率和离子重新结合成分子的速率相等时,电离过程就达到了平衡状态。
高中化学分步搞定“弱电解质的电离平衡”!
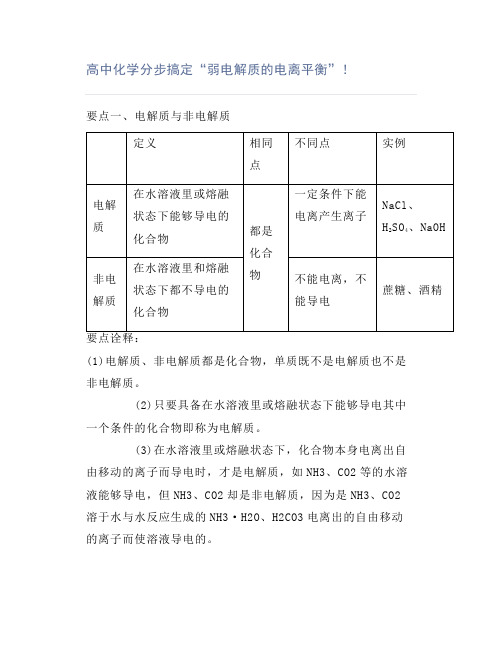
高中化学分步搞定“弱电解质的电离平衡”!要点一、电解质与非电解质(1)电解质、非电解质都是化合物,单质既不是电解质也不是非电解质。
(2)只要具备在水溶液里或熔融状态下能够导电其中一个条件的化合物即称为电解质。
(3)在水溶液里或熔融状态下,化合物本身电离出自由移动的离子而导电时,才是电解质,如NH3、CO2等的水溶液能够导电,但NH3、CO2却是非电解质,因为是NH3、CO2溶于水与水反应生成的NH3·H2O、H2CO3电离出的自由移动的离子而使溶液导电的。
(4)电解质不一定导电(如固态NaCl),导电物质不一定是电解质(如Cu);非电解质不导电,但不导电的物质不一定是非电解质。
(5)某些离子型氧化物,如Na2O、CaO、Na2O2等,它们虽然溶于水后电离出来的自由离子不是自身的,但在熔融状态时自身却可完全电离,故属于电解质。
(6)电解质溶液里的导电能力由自由移动的离子浓度与离子所带的电荷数决定。
要点二、强电解质与弱电解质强电解质弱电解质电离程度完全电离部分电离化学键离子键或强极性共价键极性共价键电离特点无电离平衡,不可逆存在电离平衡,过程可逆书写用“=”号用“”号溶液中微粒只有离子(水合离子)离子(水合离子)和分子示例HCl、H2SO4、NaOH、Ba(OH)2、K2SO4等CH3COOH、NH3·H2O、HClO、H2CO3、H2O等(1)强电解质、弱电解质与其溶解性无关。
某些难溶或微溶于水的盐,由于其溶解度很小,如果测其溶液的导电能力,往往是很弱的。
但是其溶于水的部分,却是完全电离的,所以它们仍然属于强电解质,例如:CaCO3、BaSO4等。
相反,少数盐尽管能溶于水,但只有部分电离,仍属于弱电解质。
(2)强电解质、弱电解质的电离与有无外电场无关。
划分电解质和非电解质的标准是在水溶液里或熔融状态下能否导电。
划分强电解质和弱电解质的标准是在水溶液里是否完全电离。
(3)导电能力强不一定是强电解质,强电解质不一定导电能力强。
弱电解质的电离

弱电解质的电离一、电解质1电解质和非电解质电解质:在水溶液里或熔融状态下能导电的化合物。
非电解质:在水溶液里或熔融状态下不能导电的化合物。
【注意】(1)电解质和非电解质的范畴都是化合物,所以单质既不是电解质也不是非电解质。
(2)化合物为电解质,其本质是自身能电离出离子,有些物质溶于水时所得溶液也能导电,但这些物质自身不电离,而是生成了一些电解质,则这些物质不属于电解质。
如:SO2、SO3、CO2、NO2等。
(3)常见电解质的范围:酸、碱、盐、离子型氧化物。
(4)溶剂化作用:电解质溶于水后形成的离子或分子并不是单独存在的,而是与水分子相互吸引、相互结合,以“水合离子”或“水合分子”的形态存在,这种溶质分子或离子与溶剂相互吸引的作用叫做溶剂作用。
2强电解质和弱电解质NH3·H2O NH+4+OH-H2S H++HS-HS- H++S2-【注意】(1)强、弱电解质与溶解性的关系:电解质的强弱取决于电解质在水溶液中是否完全电离,与溶解度的大小无关。
一些难溶的电解质,但溶解的部分能全部电离,则仍属强电解质。
如:BaSO4、BaCO3等。
(2)强、弱电解质与溶液导电性的关系:溶液的导电性强弱与溶液中的离子浓度大小有关。
强电解质溶液的导电性不一定强,如很稀的强电解质溶液,其离子浓度很小,导电性很弱。
而弱电解质溶液的导电性不一定弱,如较浓的弱电解质溶液,其电离出的离子浓度可以较大,导电性可以较强。
(3)强、弱电解质与物质结构的关系:强电解质一般为离子化合物和一些含强极性键的共价化合物,弱电解质一般为含弱极性键的化合物。
(4)强、弱电解质在熔融态的导电性:离子型的强电解质由离子构成,在熔融态时产生自由移动的离子,可以导电。
而共价型的强电解质以及弱电解质由分子构成,熔融态时仍以分子形式存在,所以不导电。
例1. 下列物质的水溶液都能导电,但属于非电解质的是A、CH3COOH B、Cl2C、NH4HCO3D、SO2例2. 下列说法下列正确的是A、强电解质的水溶液中不存在溶质分子,弱电解质的水溶液中存在溶质分子和离子B、强电解质的水溶液导电性强于弱电解质的水溶液C、强电解质都是离子化合物,弱电解质都是共价化合物D、强电解质易溶于水,弱电解质难溶于水二、弱电解质的电离平衡:强电解质在溶液中完全电离,不存在电离平衡。
弱电解质的电离知识点总结

弱电解质的电离一、电解质、非电解质、1、电解质:在水溶液里或熔融状态下能导电的化合物。
2、非电解质:在水溶液里和熔融状态下都不能导电的化合物。
①电解质和非电解质均指化合物,单质和混合物既不属于电解质也不属于非电解质。
②电解质必须是自身能直接电离出自由移动的离子的化合物。
SO2、CO2③条件:水溶液或融化状态对于电解质来说,只须满足一个条件即可,而对非电解质则必须同时满足两个条件。
④难溶性化合物不一定就是弱电解质。
例如:BaSO4、AgCl 难溶于水,导电性差,但由于它们的溶解度太小,测不出(或难测)其水溶液的导电性,但它们溶解的部分是完全电离的,所以他们是电解质。
⑤酸、碱、盐、金属氧化物和水都是电解质(特殊:盐酸是电解质溶液);蔗糖、酒精为非电解质。
二、强电解质与弱电解质1、强电解质:溶于水或熔融状态下几乎完全电离的电解质。
2、弱电解质:溶于水或熔融状态下只有部分电离的电解质。
①电解质的强弱与化学键有关,但不由化学键类型决定。
强电解质含有离子键或强极性键,但含有强极性键的不一定都是强电解质,如H2O、HF等都是弱电解质。
②电解质的强弱与溶解度无关。
如BaSO4、CaCO3等③电解质的强弱与溶液的导电能力没有必然联系。
说明离子化合物在熔融或溶于水时离子键被破坏,电离产生了自由移动的离子而导电;共价化合物只有在溶于水时才能导电.因此,可通过使一个化合物处于熔融状态时能否导电的实验来判定该化合物是共价化合物还是离子化合物。
3、电解质溶液的导电性和导电能力① 电解质不一定导电(如NaCl 晶体、无水醋酸),导电物质不一定是电解质(如石墨),非电解质不导电,但不导电的物质不一定是非电解质;② 电解质溶液的导电性强弱决定于溶液离子浓度大小,浓度越大,导电性越强。
离子电荷数越高,导电能力越强。
③ 强电解质溶液导电性不一定比弱电解质强(浓度可不同);饱和强电解质溶液导电性不一定比弱电解质强④ 电解质的导电条件是水溶液或高温熔融液(熔液)。
高中化学选修四第三章弱电解质的电离知识点

第一节弱电解质的电离一、电解质1、定义:○1电解质:在水溶液中或熔化状态下能导电的化合物;○2非电解质:在水溶液中或熔化状态下都不能导电的化合物;(非金属氧化物、大多数有机物。
如)○3强电解质:在水溶液里全部电离成离子的电解质;(强酸、强碱、大多数盐。
如)○4弱电解质:在水溶液里只有一部分分子电离成离子的电解质。
(弱酸、弱碱,极少数盐,水。
如HClO、)2、电解质与非电解质的本质区别:电解质——离子化合物或共价化合物非电解质——共价化合物注意:○1电解质、非电解质都是化合物○2强电解质不等于易溶于水的化合物(如不溶于水,但溶于水的全部电离,故为强电解质)○3电解质的强弱与导电性、溶解性无关【习题一】(2017秋•邢台期末)下列事实不能证明H2C2O4(乙二酸)是弱电解质的是()A.草酸能使酸性KMnO4溶液褪色B.常温下,0.1mol/L的H2C2O4溶液的PH=2C.浓度均为1mol/L=l的H2C2O4溶液的导电能力比硫酸的导电能力弱D.常温下,pH=4的H2C2O4溶液稀释100倍,pH约为5【考点】弱电解质的判断.【专题】电离平衡与溶液的pH专题.【分析】强弱电解质的根本区别是电离程度,部分电离的电解质是弱电解质,只要说明乙二酸部分电离就能证明乙二酸是弱电解质,据此分析解答。
【解答】解:A.草酸能使酸性KMnO4溶液褪色,是草酸的还原性,不能证明为弱酸,故A符合;B.常温下,0.1mol/L的H2C2O4溶液的PH=2,说明溶液中存在电离平衡,草酸为弱电解质,故B不符合;C.浓度均为1mol/L的H2C2O4溶液的导电能力比硫酸的导电能力弱,说明草酸部分电离,为弱电解质,故C不符合;D.常温下,pH=4的H2C2O4溶液稀释100倍,若为强电解质PH变化为6,pH 约为5,说明稀过程中草酸又电离出氢离子,存在电离平衡,说明为弱电解质,故D不符合;故选:A。
【习题二】(2017秋•平罗县校级期末)下列说法中,正确的是()A.强电解质的水溶液一定比弱电解质溶液的导电能力强B.强电解质都是离子化合物,弱电解质都是共价化合物C.强电解质的水溶液中不存在溶质分子D.不溶性盐都是弱电解质,可溶性酸和具有极性键的化合物都是强电解质【考点】强电解质和弱电解质的概念.【专题】电离平衡与溶液的pH专题.【分析】A.溶液导电能力取决于溶液中离子浓度大小,与电解强弱无关;B.某些共价化合物是强电解质;C.强电解质完全电离成离子;D.某些不溶性盐是强电解质;某些可溶性酸是弱电解质;某些具有极性键的化合物是弱强电解.【解答】解:A.溶液的导电能力与溶液中离子浓度成正比,与电解质的强弱无关,强电解质溶液的导电能力不一定比弱电解质溶液强,故A错误;B.强电解质不一定都是离子化合物,如氯化氢;弱电解质都是共价化合物,故B错误;C.强电解质的特征水溶液中完全电离,所以不存在溶质分子,故C正确;D.不溶性盐不一定是弱电解质,如硫酸钡;可溶性酸不一定是强电解质如醋酸;具有极性键的化合物不一定是强电解,如甲烷,故D错误,故选:C。
弱电解质的电离平衡-知识点

弱电解质的电离平衡考点一:弱电解质的电离平衡一、弱电解质的电离平衡 1.电离平衡的建立在一定条件(如温度、浓度等)下,当弱电解质分子电离成离子的速率和离子结合成弱电解质分子的速率相等时,电离过程就达到平衡。
平衡建立过程如图所示。
2.电离平衡的特征二、影响电离平衡的外界条件1.温度:温度升高,电离平衡向右移动,电离程度增大。
2.浓度:稀释溶液,电离平衡向右移动,电离程度增大。
3.同离子效应:加入与弱电解质具有相同离子的强电解质,电离平衡向左移动,电离程度减小。
4.加入能反应的物质:电离平衡向右移动,电离程度增大。
三、实例分析以CH 3COOH CH 3COO -+H +ΔH >0为例:名师点拨(1)电离平衡右移,电解质分子的浓度不一定减小,离子的浓度也不一定增大。
例如:对于CH 3COOHCH 3COO -+H +平衡后,加入冰醋酸,c (CH 3COOH)增大,平衡右移,根据勒夏特列原理,再次平衡时,c (CH 3COOH)比原平衡时大;加水稀释或加少量NaOH 固体,都会引起平衡右移,但c (CH 3COOH)、c (H +)都比原平衡时要小。
(2)稀释弱电解质溶液时,并非所有粒子浓度都减小。
例如:HA 溶液稀释时,c (HA)、c (H +)、c (A -)均减小(参与平衡建立的微粒),但c (OH -)会增大。
考 点 二 电离平衡常数一、表达式1.对于一元弱酸HA :HAH ++A -,电离平衡常数K =c (H +)·c (A -)c (HA )。
2.对于一元弱碱BOH :BOHB ++OH -,电离平衡常数K =c (B +)·c (OH -)c (BOH )。
二、特点1.电离平衡常数只与温度有关,因电离是吸热过程,所以升温,K 值增大。
2.多元弱酸的各级电离平衡常数的大小关系是K 1≫K 2≫K 3≫…,故其酸性取决于第一步。
三、意义K 越大―→越易电离―→酸(碱)性越强名师点拨(1)电离平衡常数与化学平衡常数一样,只与温度有关,与其他条件无关。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
弱电解质的电离一、电解质、非电解质、1、电解质:在水溶液里或熔融状态下能导电的化合物。
2、非电解质:在水溶液里和熔融状态下都不能导电的化合物。
①电解质和非电解质均指化合物,单质和混合物既不属于电解质也不属于非电解质。
②电解质必须是自身能直接电离出自由移动的离子的化合物。
SO2、CO2③条件:水溶液或融化状态对于电解质来说,只须满足一个条件即可,而对非电解质则必须同时满足两个条件。
④难溶性化合物不一定就是弱电解质。
例如:BaSO4、AgCl 难溶于水,导电性差,但由于它们的溶解度太小,测不出(或难测)其水溶液的导电性,但它们溶解的部分是完全电离的,所以他们是电解质。
⑤酸、碱、盐、金属氧化物和水都是电解质(特殊:盐酸是电解质溶液);蔗糖、酒精为非电解质。
二、强电解质与弱电解质1、强电解质:溶于水或熔融状态下几乎完全电离的电解质。
2、弱电解质:溶于水或熔融状态下只有部分电离的电解质。
强弱电解质与结构的关系①电解质的强弱与化学键有关,但不由化学键类型决定。
强电解质含有离子键或强极性键,但含有强极性键的不一定都是强电解质,如H 2O 、HF 等都是弱电解质。
②电解质的强弱与溶解度无关。
如BaSO 4、CaCO 3等 ③电解质的强弱与溶液的导电能力没有必然联系。
说明 离子化合物在熔融或溶于水时离子键被破坏,电离产生了自由移动的离子而导电;共价化合物只有在溶于水时才能导电.因此,可通过使一个化合物处于熔融状态时能否导电的实验来判定该化合物是共价化合物还是离子化合物。
3、电解质溶液的导电性和导电能力① 电解质不一定导电(如NaCl 晶体、无水醋酸),导电物质不一定是电解质(如石墨),非电解质不导电,但不导电的物质不一定是非电解质;② 电解质溶液的导电性强弱决定于溶液离子浓度大小,浓度越大,导电性越强。
离子电荷数越高,导电能力越强。
③ 强电解质溶液导电性不一定比弱电解质强(浓度可不同);饱和强电解质溶液导电性不一定比弱电解质强④ 电解质的导电条件是水溶液或高温熔融液(熔液)。
共价化合物只能在溶液中导电,离子化合物在熔液和溶液均可导电。
(区别离子与共价化合物)三、弱电解质的电离平衡 1、电离平衡概念一定条件(温度、浓度)下,分子电离成离子的速率和离子结合成分子的速率相等,溶液中各分子和离子的浓度都保持不变的状态叫电离平衡状态(属于化学平衡)。
导电性离子浓离子所带溶液浓电离程任何弱电解质在水溶液中都存在电离平衡,达到平衡时,弱电解质具有该条件下的最大电离程度。
2、电离平衡的特征①逆:弱电解质的电离过程是可逆的,存在电离平衡。
②等:弱电解质电离成离子的速率和离子结合成分子的速率相等。
③动:弱电解质电离成离子和离子结合成分子的速率相等,不等于零,是动态平衡。
④定:弱电解质在溶液中达到电离平衡时,溶液里离子的浓度、分子的浓度都不再改变。
⑤变:外界条件改变时,平衡被破坏,电离平衡发生移动。
3、影响电离平衡的因素(符合勒沙特列原理)(1)内因—电解质本身的性质,是决定性因素。
(2)外因①温度—由于弱电解质电离过程均要吸热,因此温度升高,电离度增大。
②浓度—同一弱电解质,浓度越大,电离度越小。
在一定温度下,浓度越大,电离程度越小。
因为溶液浓度越大,离子相互碰撞结合成分子的机会越大,弱电解质的电离程度就越小。
因此,稀释溶液会促进弱电解质的电离。
例如:在醋酸的电离平衡CH3COOH CH3COO-+H+A 加水稀释,平衡向右移动,电离程度变大,但c(CH3COOH)、c(H+)、c(CH3COO-)变小;B 加入少量冰醋酸,平衡向右移动,c(CH3COOH)、c(H+)、c(CH3COO-)增大但电离程度小;③外加物质若加入的物质电离出一种与原电解质所含离子相同的离子,则会抑制原电解质的电离,使电离平衡向生成分子的方向移动;若加入的物质能与弱电解质电离出的离子反应,则会促进原电解质的电离,使电离平衡向着电离的方向移动。
以电离平衡CH3COOH CH3COO-+H+为例,各种因素对平衡的影响可归纳为下表:项目平衡移动方向c(H+)n(H+)c(Ac-)c(OH-)c(H+)/c(HAc)导电能力电离程度加水稀释向右减小增多减小增多增多减弱增大加冰醋酸向右增大增多增多减小减小增强减小升高温度向右增大增多增多增多增多增强增大加NaOH(s)向右减小减少增多增多增多增强增大H2SO4(浓)向左增大增多减少减少增多增强减小加醋酸铵(s)向左减小减少增多增多减小增强减小加金属Mg 向右减小减少增多增多增多增强增大加CaCO3(s)向右减小减少增多增多增多增强增大四、电离方程式的书写(1)强电解质用=,弱电解质用(2)多元弱酸分步电离,多元弱碱一步到位。
H2CO3H++HCO3-,HCO3-H++CO32-,以第一步电离为主。
NH3·H2O NH4+ + OH-Fe(OH)3Fe3+ + 3OH-(3)弱酸的酸式盐完全电离成阳离子和酸根阴离子,但酸根是部分电离。
NaHCO3=Na++HCO3-,HCO3-H++CO32-(4)强酸的酸式盐如NaHSO4完全电离,但在熔融状态和水溶液里的电离是不相同的。
熔融状态时:NaHSO 4=Na ++HSO 4- 溶于水时:NaHSO 4=Na ++H ++SO 42-五、电离平衡常数(相当化学平衡常数)在一定温度下,当弱电解质的电离达到平衡状态时,溶液中电离产生的各种离子浓度的乘积与溶液中未电离的弱电解质分子浓度的比值是一个常数,这个常数叫做电离平衡常数,简称电离常数,通常用K a 表示弱酸的电离常数。
AB)()-B ()A (c c c K ⋅=+电离 AB⇋A ++B-(1)K 的意义:K 值越大,则电离程度越大,电解质(即酸碱性)越强;K 值越小,电离程度越小,离子结合成分子就越容易,电解质(即酸碱性)越弱。
表达式中各组分的浓度均为平衡浓度。
(2)K 的影响因素:K 的大小与溶液的浓度无关,只随温度的变化而变化.温度不变,K 值不变;温度不同,K 值也不同。
(3)多元弱酸的K :多元弱酸的电离是分步电离的,每步电离平衡常数,通常用K 1、K 2、 K 3 分别表示,但第一步电离是主要的。
如:磷酸的三个K 值,K 1>K 2>K 3 ,磷酸的电离只写第一步。
说明:①一元弱酸、一元弱碱的电离常数表达式: CH 33COO -+ H +一定温度下CH 3COOH 的电离常数为: NH 3·H 24++ OH -一定温度下NH 3·H 2O 的电离常数为:②多元弱酸的电离特点及电离常数表达式:A 分步电离:是几元酸就分几步电离.每步电离只能产生一个H +,每一步电离都有其相应的电离常数。
B 电离程度逐渐减小,且K 1>K 2>K 3,故多元弱酸溶液中平衡时的H +主要来源于第一步。
所以,在比较多元弱酸的酸性强弱时,只需比较其K1即可。
例如25℃时,H 3PO 4的电离;)()()(33COOH CH c COO CH c H c Ka -+⋅=)()()(234O H NH c OH c NH c Kb ⋅⋅=-+H 3PO 42PO 4- + H +343421105.7)()()(-+-⨯=⋅=PO H c H c PO H c KH 2PO 4-42- + H +842242102.6)()()(--+-⨯=⋅=PO H c H c HPO c KHPO 42-43- + H +132********.2)()()(--+-⨯=⋅=HPO c H c PO c K多元弱酸溶液中的c(H +)是各步电离产生的c(H +)的总和,在每步的电离常数表达式中的c(H +)是指溶液中H +的总浓度而不是该步电离产生的c(H +)。
六、电离度电离度(α)(相当转化率,与温度、浓度均有关) 电离度(α)=%100⨯分子数溶液中原有电解质的总数己电离的电解质的分子A 内因:电解质的本性。
B 外因:温度和溶液的浓度等。
(1)浓度的影响:醋酸稀释时电离度变化的数据:浓度(mol/L) 0.2 0.1 0.001 电离度(%) 0.948 1.32 12.4可见,电离度随浓度的降低而增大。
(因浓度越稀,离子互相碰撞而结合成分子的机会越少,电离度就越大。
)章节知识结构图。
