《第三章自然界中的元素》基础知识总结
鲁科版化学必修1课件:第三章第一节

第三章
自然界中的元素
3.近年来科学家在氦的气氛中给石墨电极通 电,石墨挥发,在其挥发产生的黑烟中发现了 C60。C60 的金属渗入物具有可贵的超导性质。 北京大学首先将 C60 渗锡,获得超导转变温度 为 37 K 的好成果。 这种 C60 是________元素的 一种________,其摩尔质量为________;若要 确证其元素的组成,可将它在足量的氧气中燃 烧,再用________试剂来检验生成的________ 气体,现象是__________________。
栏目 导引
第三章
自然界中的元素
新知初探自学导引
自主学习 一、多种多样的碳单质 1.同素异形体 由同一种元素组成的性质不同的几种单质,如 氧元素的同素异形体有 O2 和 O3,碳元素的同 素异形体有石墨、金刚石和 C60 等。 2.碳的同素异形体
栏目 导引
第三章
自然界中的元素
物 质 金刚石(C) 内容
栏目 导引
第三章
自然界中的元素
要点2
的吗?
【提示】
CO2与碱反应产物的确定
CO2与碱反应的产物是唯一 不唯一,少量CO2与碱液反应生
探究导引3
成碳酸盐,过量CO2与碱反应生成碳酸氢盐.
栏目 导引
第三章
自然界中的元素
探究导引4 的产物? 【提示】
如关键是熟
栏目 导引
第三章
自然界中的元素
物质 内容
碳酸钠
碳酸氢钠
NaHCO3+ ________________ NaOH===Na2CO ________________ 3+H2O ________________ 发酵粉、治疗胃病
与NaOH 不反应 溶液反应 用途 制玻璃、造纸
第三章 自然界中的元素第3节 硫的转化

第三章自然界中的元素第3节硫的转化【学习目标】1、用氧化还原反应的知识,探究-2价,0价,+4价,+6价硫元素的转化2、使学生了解二氧化硫对空气的污染、二氧化硫的漂白性等以及用途。
3、培养学生设计实验、实施实验、观察实验的能力,分析问题、解决问题的能力,以及探究意识和探究能力。
【学习重点】二氧化硫的主要性质【学习难点】通过探究不同价态硫元素之间的相互转化,使学生能够运用氧化还原反应寻找合适的氧化剂和还原剂。
【课堂讨论区】二、实验室里研究不同价态硫元素间的转化【问题组一】1、根据上节课介绍的及你们生活中所认识的,硫元素主要的化合价有哪些?你们讲讲生活中的含硫化合物有哪些?2、-2价,0价,+4价,+6价硫元素在氧化还原中会表现出有什么样的性质?以二氧化硫为例,如何证明+4价硫可能具有的性质?【问题组二】以二氧化硫为例,从氧化还原的角度分析:1、二氧化硫的硫元素要从从+4价转化成0价应加入氧化剂还是还原剂?你能从下面提供的试剂中找到吗?2、二氧化硫的硫元素要从从+4价转化成+6价应加入氧化剂还是还原剂?你能从下面提供的试剂中找到吗?试剂:H2S、酸性KMnO4溶液、氯水、硝酸、NaOH溶液。
【总结】预测二氧化硫的性质:(1) +4价→0价的硫在反应中应加入适当的(氧化剂还是还原剂)验证,可以用的还原剂有:;(2)+4价→+6价的硫在反应中应加入适当的(氧化剂还是还原剂)验证,可以用的的氧化剂有:。
设计实验证明二氧化硫的性质,完成硫元素从+4价→ 0价,+4价→+6价的转化。
试剂:亚硫酸钠(Na2SO3)固体、H2SO4、H2S(提示:可用Na2S+H2SO4= Na2SO4+ H2S↑制的)、酸性KMnO4溶液、氯水、NaOH溶液,实验仪器任选。
首先以小组为单位,设计实验方案,填入下列表格中,并画出装置图。
思考:1、通过实验现象结合氧化还原的知识,写出反应的化学方程式,总结二氧化硫的化学性质。
2、在实验过程中,你遇到了哪些问题?是如何解决的?【整理归纳】1、二氧化硫的性质,用方程式来表示。
2022化学第3章自然界中的元素第3节硫的转化教案

第3节硫的转化考纲定位要点网络1.掌握O3和H2O2的主要性质及其应用。
2。
掌握硫元素单质及其重要化合物的主要性质及应用。
3。
了解硫、氧及其重要化合物的制备方法。
4.了解硫元素单质及其重要化合物对环境的影响.绿色氧化剂-—O3和H2O2知识梳理1.臭氧——氧元素的一种单质(1)组成与物理性质臭氧的分子式为O3,与O2互为同素异形体,是一种有特殊臭味的淡蓝色气体.O3在空气中含量很少,使人们感到清爽,但超过一定浓度,则会影响人体的健康。
(2)化学性质①不稳定性:O3不稳定,容易分解,反应的化学方程式为2O3===3O2。
②强氧化性a.能氧化具有还原性的物质,如KI、FeCl2等。
O3+2KI+H2O===I2+2KOH+O2b.漂白性:因O3有强氧化性,所以它能使有色物质退色,并被用来杀菌消毒.(3)用途①可用作漂白剂、脱色剂和消毒剂.②臭氧层可以吸收来自太阳的紫外线,是人类和其他生物的保护伞。
(4)生成在放电条件下空气中的O2可以转化为O3,3O2错误!2O3.2.过氧化氢--其水溶液俗称双氧水(1)结构:H错误!错误!错误!错误!错误!H,结构式为H—O—O—H,含有的共价键有极性键、非极性键,为共价化合物,为无色液体。
(2)化学性质及应用①不稳定性:加热、加催化剂都能使其分解速率加快.2H2O2错误!2H2O+O2↑(实验室制O2)。
常见H2O2的催化剂有MnO2、Fe3+和Cu2+等。
②弱酸性:相当于二元弱酸。
H2O2H++HO错误!,HO错误!H++O错误!。
③强氧化性a.用10%的双氧水漂白羽毛及丝织品(漂白剂)。
b.氧化Fe2+等还原性粒子,其离子方程式为H2O2+2Fe2++2H+===2Fe3++2H2O。
c.使湿润的淀粉。
KI试纸变蓝,其离子方程式为H2O2+2I-+2H+===I2+2H2O。
d.杀菌、消毒.④弱还原性:遇强氧化剂时作还原剂。
2KMnO4+5H2O2+3H2SO4===K2SO4+2MnSO4+5O2↑+8H2O。
化学第三章物质构成的奥秘知识点总结

第三章知识点第1节构成物质的基本微粒一、微粒的性质实验一:氨分子扩散(无色酚酞遇碱变红)1、向水中加酚酞,酚酞不变色。
结论:水不能使酚酞变红。
2、再向烧杯中加几滴浓氨水,酚酞变红。
结论:浓氨水能使酚酞变红。
3、把装有浓氨水的一个烧杯,和另一个装酚酞试液的烧杯用一大烧杯罩在一起,一段时间后,酚酞试液变红。
结论:①(主要)微粒在不段运动。
②(其它)浓氨水有挥发性。
氨水显碱性。
注:温度越高,微粒运动速率越快。
实验二:半管水和半管酒精混合,总体积小于一管。
气体易被压缩,固体液体不易被压缩。
结论:微粒间有空隙。
气体微粒间空隙大,固体液体微粒间空隙小。
注:温度越高,微粒间空隙越大。
总结:微粒的性质:1、物质是由极小的,肉眼看不见的微粒构成的。
2、微粒是在不断的动运。
温度越高,微粒运动速率越快。
3、微粒间有空隙。
温度越高,微粒间空隙越大。
能直接构成物质的微粒有三种:分子(气体、水、碘单质)、原子(金属、稀有气体、碳、硅)、离子(盐)二、分子1、不同物质由不同种分子构成。
同种分子性质相同,不同种分子性质不同。
2、同种分子构成的物质是纯净物,反之为混合物。
3、分子是保持物质化学性质的一种微粒。
4、由分子构成的物质包括:气体(除稀有气体之外的气体)、水、碘(I2)5、所有分子都是由原子构成的。
6、H2O由H元素和O元素组成,由水分子构成。
水分子由H原子和O原子构成,一个水分子由2个H原子和一个O原子构成。
注:只有氧气中才含有氧分子,只有水中才有水分子,只有氢气中才有氢分子,以此类推。
三、原子1、化学变化的实质:分子分解成原子,原子再重新结合成新分子。
2、化学变化中分子可分,原子不可分,原子是化学变化中的最小微粒。
3、化学变化前后,分子种类一定改变,原子种类一定不变。
4、分子的质量不一定比原子的质量大。
5、原子构成的物质包括:金属、稀有气体、碳单质、硅单质6、提出原子学说:道尔顿发现电子:汤姆生发现原子核:卢瑟福原子核质子(+)(+)中子(不带电)原子(正电=负电)电子(-)H原子的原子核中没有中子。
元素的结构知识点总结

元素的结构知识点总结
1. 元素是物质世界的基本构成单位,它由原子构成。
原子是构成元素的最小单位,由质子、中子和电子组成。
2. 元素的质子数决定了元素的化学性质,被称为元素的原子序数。
原子序数不同的元素具
有不同的化学性质。
3. 元素的电子分布决定了元素的化学反应性。
具有相似电子分布的元素具有相似的化学性质,被归为同一族。
4. 元素的核子数等于质子数加上中子数,决定了元素的原子量。
原子量是一个相对的数值,以碳-12的原子质量为基准。
5. 元素可以通过周期表来进行分类。
周期表是将元素按照原子序数的大小排列在一起的表格,它反映了元素的周期性规律。
6. 元素的结构可以通过原子核结构和电子云结构来描述。
原子核结构主要描述元素的核子
组成,而电子云结构描述了电子在原子周围的分布情况。
7. 元素的稳定性跟其原子结构有关。
原子核内质子和中子的相互作用力决定了核子的稳定性,而电子的排布决定了原子的化学稳定性。
8. 元素的化学性质主要由其电子组织和元素的原子结构决定。
电子的数量和排布决定了元
素的离子化倾向和共价化倾向,而核子的排布则决定了元素的同位素特性。
9. 元素的物理性质也受其原子结构的影响。
原子核结构决定了元素的密度、熔点和沸点,
而电子云结构则决定了元素的导电性、热导性和光学性质。
化学必修一第三章第1节 碳的多样性(共20张PPT)

碳“三角”
C
2、木炭燃烧
CO
CO2
【概括·整合】
碳的同素异形体和碳的化合物
碳元素
碳单质
含碳化合物
金刚石
C60
石墨
无机化合物 有机化合物
一氧化碳 二氧化碳
碳酸
碳酸盐
C
CO2
Na2CO3
NaHCO3
CO CaCO3
Ca(HCO3)2
1、只要有坚强的意志力,就自然而然地会有能耐、机灵和知识。2、你们应该培养对自己,对自己的力量的信心,百这种信心是靠克服障碍,培养意志和锻炼意志而获得的。 3、坚强的信念能赢得强者的心,并使他们变得更坚强。4、天行健,君子以自强不息。5、有百折不挠的信念的所支持的人的意志,比那些似乎是无敌的物质力量有更强大 的威力。6、永远没有人力可以击退一个坚决强毅的希望。7、意大利有一句谚语:对一个歌手的要求,首先是嗓子、嗓子和嗓子……我现在按照这一公式拙劣地摹仿为:对 一个要成为不负于高尔基所声称的那种“人”的要求,首先是意志、意志和意志。8、执着追求并从中得到最大快乐的人,才是成功者。9、三军可夺帅也,匹夫不可夺志也。 10、发现者,尤其是一个初出茅庐的年轻发现者,需要勇气才能无视他人的冷漠和怀疑,才能坚持自己发现的意志,并把研究继续下去。11、我的本质不是我的意志的结果, 相反,我的意志是我的本质的结果,因为我先有存在,后有意志,存在可以没有意志,但是没有存在就没有意志。12、公共的利益,人类的福利,可以使可憎的工作变为可 贵,只有开明人士才能知道克服困难所需要的热忱。13、立志用功如种树然,方其根芽,犹未有干;及其有干,尚未有枝;枝而后叶,叶而后花。14、意志的出现不是对愿 望的否定,而是把愿望合并和提升到一个更高的意识水平上。15、无论是美女的歌声,还是鬓狗的狂吠,无论是鳄鱼的眼泪,还是恶狼的嚎叫,都不会使我动摇。16、即使 遇到了不幸的灾难,已经开始了的事情决不放弃。17、最可怕的敌人,就是没有坚强的信念。18、既然我已经踏上这条道路,那么,任何东西都不应妨碍我沿着这条路走下 去。19、意志若是屈从,不论程度如何,它都帮助了暴力。20、有了坚定的意志,就等于给双脚添了一对翅膀。21、意志坚强,就会战胜恶运。22、只有刚强的人,才有神 圣的意志,凡是战斗的人,才能取得胜利。23、卓越的人的一大优点是:在不利和艰难的遭遇里百折不挠。24、疼痛的强度,同自然赋于人类的意志和刚度成正比。25、能 够岿然不动,坚持正见,度过难关的人是不多的。26、钢是在烈火和急剧冷却里锻炼出来的,所以才能坚硬和什么也不怕。我们的一代也是这样的在斗争中和可怕的考验中 锻炼出来的,学习了不在生活面前屈服。27、只要持续地努力,不懈地奋斗,就没有征服不了的东西。28、立志不坚,终不济事。29、功崇惟志,业广惟勤。30、一个崇高 的目标,只要不渝地追求,就会居为壮举;在它纯洁的目光里,一切美德必将胜利。31、书不记,熟读可记;义不精,细思可精;惟有志不立,直是无着力处。32、您得相 信,有志者事竟成。古人告诫说:“天国是努力进入的”。只有当勉为其难地一步步向它走去的时候,才必须勉为其难地一步步走下去,才必须勉为其难地去达到它。33、 告诉你使我达到目标的奥秘吧,我唯一的力量就是我的坚持精神。34、成大事不在于力量的大小,而在于能坚持多久。35、一个人所能做的就是做出好榜样,要有勇气在风 言风语的社会中坚定地高举伦理的信念。36、即使在把眼睛盯着大地的时候,那超群的目光仍然保持着凝视太阳的能力。37、你既然期望辉煌伟大的一生,那么就应该从今 天起,以毫不动摇的决心和坚定不移的信念,凭自己的智慧和毅力,去创造你和人类的快乐。38、一个有决心的人,将会找到他的道路。39、在希望与失望的决斗中,如果 你用勇气与坚决的双手紧握着,胜利必属于希望。40、富贵不能淫,贫贱不能移,威武不能屈。41、生活的道路一旦选定,就要勇敢地走到底,决不回头。42、生命里最重 要的事情是要有个远大的目标,并借助才能与坚持来完成它。43、事业常成于坚忍,毁于急躁。我在沙漠中曾亲眼看见,匆忙的旅人落在从容的后边;疾驰的骏马落在后头, 缓步的骆驼继续向前。44、有志者事竟成。45、穷且益坚,不坠青云之志。46、意志目标不在自然中存在,而在生命中蕴藏。47、坚持意志伟大的事业需要始终不渝的精神。 48、思想的形成,首先是意志的形成。49、谁有历经千辛万苦的意志,谁就能达到任何目的。50、不作什么决定的意志
自然界中的元素硫

*
C+2H2SO4 (浓) CO2↑+2SO2↑+2H2O
【综合实践】 1.合理组装实验仪器,分别检验产物的成分。 2.类比---《新课堂》109页 2题
6
【了解】硫酸的工业制法——接触法制硫酸
4FeS2 +11 O2 2Fe2O3 + 8SO2
高 温
SO3 + H2O H2SO4
SO2+H2O H2SO3
SO2+Na2O=Na2SO3
SO2+ Ca(OH)2=CaSO3↓+H2O CaSO3+SO2+H2O=Ca(HSO3)2
化学性质
*
⑵还原性 ①与O2:SO2+O2 2SO3 ②与氯水: SO2+Cl2+2H2O= H2SO4+2HCl ⑶氧化性 2H2S+SO2=3S↓+2H2O ⑷漂白性----课本89页 图3-3-7 将SO2通入品红溶液,品红溶液褪色,加热,又恢复红色。 原理:有机色质化合生成无色物质。该物质受热易分解,又恢复原色。
Na2SO3+H2SO4=Na2SO4+SO2↑+H2O SO2的物理性质: 无色、刺激性、气体;易溶于水;有毒。
H2S的制取:FeS、稀盐酸或稀硫酸
FeS+2H+=Fe2++H2S↑
H2S物理性质: 无色,臭鸡蛋味,气体;能溶于水;剧毒。
*
S S S S
+4
+6
S→S
化学性质
1)强酸:酸的通性—指示剂 金属
*
【概括整合】
H2S H2SO3 H2SO4 BaSO4 FeS S SO2 SO3 CuSO4
人教版化学九年级上册第三单元课题3《元素》知识点

课题3 元素
一、元素
1.概念:具有相同质子数(即核电荷数)的一类原子的总称。
2.自然界中元素的分布
(1)地壳中含量较高的元素依次是氧、硅、铝、铁,含量最高的金属元素是铝;含量最高的非金属元素是氧。
(2)生物细胞中的元素组成(元素种类和质量分数)均相近,含量较多的元素依次是氧、碳、氢。
3.元素的分类
元素
4.元素和原子的比较
思维拓展
物质、元素、分子、原子、离子间的关系
二、元素符号
1.书写原则
(1)由一个字母表示的元素符号要大写。
(2)由两个字母表示的元素符号,第一个字母大写,第二个字母小写。
2.元素符号的意义
(1)宏观上表示一种元素。
(2)微观上表示该元素的一个原子。
特别提醒:(1)在元素符号前面加上计量数后,就只具有微观意义,表示若干个原子,不再表示某元素。
(2)由原子直接构成的物质,元素符号还可表示这种物质。
如“Fe”可以表示铁元素、一个铁原子,还可以表示铁这种物质。
三、元素周期表
1.概述
(1)周期:每一个横行叫做一个周期,共有7个周期。
(2)族:每一个纵行叫做一个族(其中8、9、10三个纵行共同组成一个族),共有16个族。
(3)元素周期表的起始(第一周期除外):金属元素→非金属元素→稀有气体元素。
2.元素周期表中元素所在单元格包含的信息
3.规律
(1)原子序数=核电荷数=质子数=核外电子数。
(2)同一周期:从左至右,电子层数相同,最外层电子数依次增加。
(3)同一族:从上到下,电子层数依次增加,最外层电子数相同。
地球的物质组成
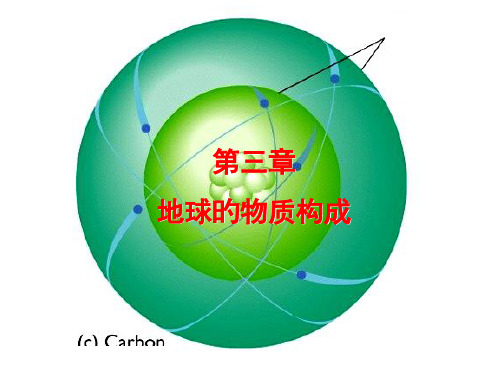
7. 石英
指甲
8. 黄玉
3. 方解石
9. 刚玉
铜币
10.金刚石
4. 萤石
5. 磷灰石
刀刃/玻璃
• 滑石硬度最小 (硬度为1)、
金刚石硬度最大(硬度为10)
应用举例:
将欲测定旳矿物与萤石相 刻划,若彼此无损伤,则硬 度相等,即所测矿物旳硬度 为4;若此矿物能刻划萤石, 但不能刻划磷灰石,相反却 为磷灰石所刻划,则其硬度 应在4-5之间,所以可定为 4.5。
第三章 地球旳物质构成
本章主要内容:
地球中旳元素 自然界中旳矿物
一、地球中旳元素 • 构成地球旳物质(按质量计)主要为铁、氧、硅、镁 等92种元素 • 地壳旳元素构成以氧、硅、铝、铁、镁为主(占92%)
整个地球
地壳
• 生物圈以氧、碳、氢为主 • 水圈主要由氧、氢构成
据 Press et al., 2023
颜色
(Color)
条痕
(Streak)
光泽
(Luster)
硬度
(Hardness)
解理
(Cleavage)
二、自然界中旳矿物
3、矿物旳物理性质
晶体形态 • 矿物一般都有自己固有旳形态, 但在自然界产出时多不完整 • 少数矿物易以其特征旳形态产出
金刚石
石英
石榴石 黄铁矿
二、自然界中旳矿物
3、矿物旳物理性质
经切割旳黄玉
(硬度=8)
经切割旳钻石
(金刚石,硬度=10)
红宝石(刚玉,硬度=9)
二、自然界中旳矿物
3、矿物旳物理性质
解理 • 矿物趋于沿一定方向产生破裂面旳性质 • 受晶体构造中旳单薄面控制
云母-片状
鲁科版高中化学必修一学案:第三章自然界中的元素第2节氮的循环

第3章第3节硫的转化【本讲教育信息】一. 教学内容:第3章第2节氮的循环二. 教学目的1. 能简要说明氮循环的基本过程,知道固氮的本质以及生物固氮和人工固氮这两种固氮形式。
2. 了解氮循环过程中的重要物质以及人类活动对氮循环和环境的影响(知道酸雨、光化学烟雾和富营养化等环境问题)3. 能列举含氮元素的单质及其化合物了解氮气、氨气、铵盐及硝酸的主要物理性质和化学性质,的检验方法和氨气的实验室制法,能书写相关反应的化学方程式。
知道NH4三. 教学重点、难点氮气、氨、铵盐和硝酸的性质四. 知识分析空气中的主要物质?植物生长需要的主要元素?(一)氮在自然界中的循环和存在形式1. 氮元素在自然界中的存在形式自然界中氮元素存在的形式一种是游离态,如N2,一种是化合态,如铵盐、硝酸盐、氨、蛋白质等。
2. 氮在自然界中的循环(1)氮在自然界中的循环的基本过程自然界里,空气的氮气转化为植物可以直接吸收含氮化合物的两种主要形式,豆科植物的根瘤菌把N2转化为硝酸盐;闪电使少量N2与O2化合生成NO,随之变为硝酸随降水进入土壤和水体。
植物的根从土壤中吸收铵盐、硝酸盐,经过复杂的生物转化,形成了各种氨基酸,氨基酸最后变成蛋白质。
动物以植物为食而获得植物蛋白,并将其转化为动物蛋白,动物遗体中的蛋白质被微生物分子分解成铵离子、硝酸根和氨,又回到了土壤和水体中,被植物再次吸收利用。
(2)氮循环的重要意义由于存在着氮元素的循环,其他生命元素的循环,以及水的循环,地球的生命才生生不息,生机勃勃。
(二)氮循环的重要物质及其变化1. 氮气(1)物理性质无色无味的难溶于水的气体;密度比空气小,在空气中约占总体积的78%,占其它质量的75%。
(2)分子结构两个氮原子之间的强烈作用,要破坏这种牢固的结合,需要很高的能量。
常温下,N2的化学性质很不活泼,但在高温、放电、点燃等条件下能与O2、Mg、H2等反应。
(3)化学性质①与O2反应:N2+O2=2NO ②与H2反应:N2+3H2=2NH3③与Mg的反应:N2+3Mg=Mg3N2温馨提示:●由于N2的化学性质不活泼,所以N2与其它物质的反应,需特别注意标明条件。
★★必修1第三章第三节硫的转化

△ △
+1 +2
2Cu + S = Cu2S Fe + S = FeS(黑色) (黑色)
2、硫与氧气反应
0 点燃
S + O2 = SO2(蓝色) 蓝色)
+4
当堂检测
1.下列说法中不正确的是( AB ) 下列说法中不正确的是( 下列说法中不正确的是 A. 硫是一种淡黄色的能溶于水的固体 B. 硫在自然界中仅以化合态存在 C. 硫与铁反应生成硫化亚铁 D. 硫在空气中的燃烧产物是二氧化硫
0 点燃 +4
实验现象
S + O2 = SO2
硫作为还原剂
学以致用 一位同学做实验时不小心将温度计打碎了, 一位同学做实验时不小心将温度计打碎了, 水银剧毒,他应该怎么处理干净? 水银剧毒,他应该怎么处理干净? 他先将大个汞珠收集,碎珠撒上一层硫粉,过 一会儿再处理掉。这就是我们紧急处理洒 落水银的方法。请问他利用了硫的什么性 质?
1.硫与铁的反应 硫与铁的反应
实验现象: 实验现象:
剧烈燃烧,发光发热, 剧烈燃烧,发光发热,生成黑色 固体。 固体。 反应放出的热能使反应继续进行
写出化学反应方程式,并指出 写出化学反应方程式, 氧化剂还原剂。 氧化剂还原剂。
0 -2 △
Fe + S = FeS(黑色) (黑色)
氧化剂
交流讨论
写出氯气与铁反应的化学方程式, 写出氯气与铁反应的化学方程式,比较 与硫和铁的反应有何异同。 与硫和铁的反应有何异同。
色 态 溶解性 溶沸点 同素异 形体
黄色或淡黄色 固体、 固体、很脆
不溶于水 微溶于酒精 易溶于CS 易溶于 2
不高
斜方硫、 斜方硫、单斜硫 等多种
高一化学必修一第三章知识点总结归纳

高一化学必修一第三章知识点总结归纳高一化学必修一(一)金属的化学性质一金属的通性1.金属的存在(1)金属元素的存在绝大多数金属以化合态的形式存在于自然界中,如Al、Fe等,极少数化学性质不活泼的金属以游离态的形式存在于自然界中,如Au。
在地壳中的含量较多的为O、Si、Al、Fe、Ca。
2.金属单质的物理通性①状态:常温下,大部分为固体,唯一呈液态的是汞。
②色泽:除Cu、Au外,大多数金属为银白色,有金属光泽。
③三性:良好的导电性、导热性、延展性。
3.单质的化学性质(1)与非金属的反应常温下,镁在空气中跟氧气反应,生成一层致密的氧化物薄膜,能够阻止内部金属继续被氧化。
镁在空气中燃烧,产生耀眼的白光,生成白色固体,反应的化学方程式为:2Mg+O2点燃=====2MgO。
镁还可以和氮气点燃,反应方程式为:3Mg+N2点燃=====Mg3N2。
(2)与酸的反应Fe与稀H2SO4反应的离子方程式:Fe+2H+===Fe2++H2↑。
(3)与盐溶液的反应Cu与AgNO3溶液反应的离子方程式:Cu+2Ag+===Cu2++2Ag。
归纳金属的通性(1)金属化学性质特点(2)金属还原性的强弱取决于其失去电子的难易程度,而不是失去电子个数的多少。
【活学活用】1.判断下列说法是否正确,正确的划“√”,错误的划“×”(1)金属具有良好的导热、导电性()(2)金属单质在氧化还原反应中总是作还原剂()(3)钠原子在氧化还原反应中失去1个电子,而铝原子失去3个电子,所以铝比钠活泼()(4)金属在加热条件下均易与O2反应()答案(1)√(2)√(3)×(4)×解析(3)错误,金属的活泼性与原子失去电子个数无关,与失电子能力有关,钠比铝易失电子,钠比铝活泼;(4)错误,Au、Pt等金属不与O2反应。
二钠与氧气的反应按表中要求完成实验,并将观察到的实验现象及其原因解释填入表中。
[归纳总结]钠与氧气的反应(1)钠的性质及其保存钠是一种硬度小、熔点低的银白色的金属,具有金属光泽。
自然界中的元素

第三章自然界中的元素基础知识总结第一节碳的多样性1. 由同一种元素组成的性质不同的几种单质,互称为同素异形体。
金刚石、石墨和C60是碳元素的同素异形体。
2. 金刚石是无色透明的片状固体。
其中,每个碳原子均与相邻的4个碳原子相连,形成正四面体结构。
在自然界中硬度最大,不导电。
3. 石墨是深灰色、有金属光泽、不透明的片状固体。
质软、有滑腻感。
碳原子呈层状排列,每一层的碳原子形成平面正六边形。
4. C6o是灰黑色固体,形成球状结构,表面呈正六边形和正五边形。
5. Na t CG和NaHCO的性质比较6. Na t CG和NaHCO如何鉴别?(1)加热比较:分解产生气体并通入澄清石灰水变浑浊的是碳酸氢钠,无现象的是碳酸钠(2)加酸反应比较:比较剧烈是碳酸氢钠(3)滴加CaCl2、E aCl2溶液:产生白色沉淀的是碳酸钠,无现象的是碳酸氢钠。
7. 温室效应:由于人类的活动,特别是生产和生活中化石燃料大幅度增加,使大气中二氧化碳的含量猛增,破坏了自然界中原有平衡,导致全球气候变暖。
7. 高炉炼铁中碳的转化:过程是将 铁矿石还原成金属铁的过程,原料是 焦炭和铁矿石(主要成分是F e 2Q )。
但起还原作用的主要是一氧化碳。
焦炭在炼铁过程中的两个作用: ①燃烧提供热量;②用于制还原剂 CO8. 在生活中,水壶中常常有水垢,它的主要成分是碳酸钙。
自来水中存在 Ca(HCO) 2,受热分解生成CaCO,积聚在壶底,便形成水垢。
相关化学方程式:_____________________第二节氮的循环1. 氮气的物理性质:在通常状况下,氮气是一种无色无味、难溶于水的气体。
在空气中约占其体积的78%2. 化学性质:在通常情况下,氮气的化学性质不活泼,很难与其他物质发生反应。
但在一定 条件下,氮气能与 氧气、氢气 等物质发生反应。
反应方程式:啟电° (?)3. 使空气中游离态的氮转化为含氮化合物的方法叫氮的固定,简称固氮。
九年级化学上册 第三章 物质构成的奥秘知识点归纳 (新版)沪教版
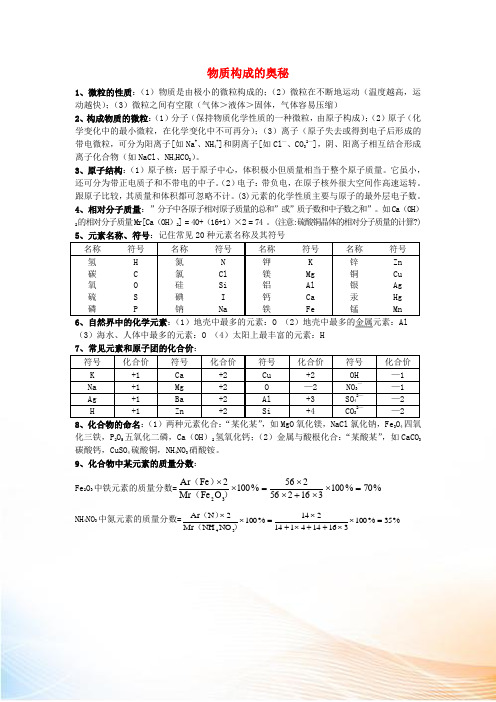
物质构成的奥秘1、微粒的性质:(1)物质是由极小的微粒构成的;(2)微粒在不断地运动(温度越高,运动越快);(3)微粒之间有空隙(气体>液体>固体,气体容易压缩)2、构成物质的微粒:(1)分子(保持物质化学性质的一种微粒,由原子构成);(2)原子(化学变化中的最小微粒,在化学变化中不可再分);(3)离子(原子失去或得到电子后形成的带电微粒,可分为阳离子[如Na +、NH 4+]和阴离子[如Cl —、CO 32—],阴、阳离子相互结合形成离子化合物(如NaCl 、NH 4HCO 3)。
3、原子结构:(1)原子核:居于原子中心,体积极小但质量相当于整个原子质量。
它虽小,还可分为带正电质子和不带电的中子。
(2)电子:带负电,在原子核外很大空间作高速运转。
跟原子比较,其质量和体积都可忽略不计。
(3)元素的化学性质主要与原子的最外层电子数。
4、相对分子质量:”分子中各原子相对原子质量的总和”或”质子数和中子数之和”。
如Ca (OH )2的相对分子质量Mr[Ca (OH )2] = 40+(16+1)×2 = 74 。
(注意:硫酸铜晶体的相对分子质量的计算?) 5、元素名称、符号:记住常见20种元素名称及其符号名称 符号 名称 符号 名称 符号 名称 符号 氢 H 氮 N 钾 K 锌 Zn 碳 C 氯 Cl 镁 Mg 铜 Cu 氧 O 硅 Si 铝 Al 银 Ag 硫 S 碘 I 钙 Ca 汞 Hg 磷 P 钠 Na 铁 Fe 锰 Mn 6、自然界中的化学元素:(1)地壳中最多的元素:O (2)地壳中最多的金属元素:Al (3)海水、人体中最多的元素:O (4)太阳上最丰富的元素:H 7、常见元素和原子团的化合价: 符号 化合价 符号 化合价 符号 化合价 符号 化合价 K +1 Ca +2 Cu +2 OH —1 Na +1 Mg +2 O —2 NO 3— —1 Ag +1 Ba +2 Al +3 SO 42— —2 H+1Zn+2Si+4CO 32——28、化合物的命名:(1)两种元素化合:“某化某”,如MgO 氧化镁,NaCl 氯化钠,Fe 3O 4四氧化三铁,P 2O 5五氧化二磷,Ca (OH )2氢氧化钙;(2)金属与酸根化合:“某酸某”,如CaCO 3碳酸钙,CuSO 4硫酸铜,NH 4NO 3硝酸铵。
第三章 自然界中的元素(第二课时3)

+氧化剂
SO2
+还原剂
H2SO4
+6
+强氧化剂
含有不同价态硫元素的物质间的转化 属于氧化还原反应。
归纳· 整理
2.根据实验,总结二氧化硫的化学性质。
SO2既有还原性,又有氧化性。
SO2+2H2S = 3S↓+ 2H2O 2 SO2+O2
催化剂
2 SO3
归纳· 整理 3. 你还能实现其他含有不
同价态硫元素的物质间的转
H2SO4的转化呢?
2. 如何证明反应后有SO2生成?如何证明 产物中有SO42-?
3. 反应中产生的SO2能否直接排放到 大气中?应如何处理?
H2SO4
+Cu
SO2 SO2
+碘水
H2SO4
模拟实验演示
铜与浓 硫酸的 混合物
滴有酚酞的 NaOH溶液
碘水
NaOH溶液
实验报告1
预期 转化 H2SO4 所选 物质 实验 现象 结论
SO2 SO2 H2SO4
铜片 碘水
滴有酚酞 的NaOH 溶液退色
碘水退色;取 反应后溶液 加BaCl2溶 液,有白色沉 淀生成
产物中有 SO2生成
2 生 有 SO4 成,体现了 SO2的还原性
实验探究2
实验室常用FeS和 硫酸来制备。 实验室常用1、要实现SO2 到硫单质的
Na2SO 转化,应选择什么物质? 3和硫 酸来制备。
硫黄 或黄 铁矿 矿石
用98%的硫酸吸收三氧化硫 :
SO3+H2O
H2SO4
根据 需要 稀释 浓硫 酸
知识小结:
二氧化硫既有氧化性又有还 原性。
2018-2019版高中化学 第3章 自然界中的元素 3.2.2 氨气与铵盐课件 鲁科版必修1

K12课件
从能否电离的角度分析下列物质是电解质还是非电解质:氨 气是_非__电__解__质__,NH3·H2O是_电__解__质__,氨水是_混__合__物__,__既__不_ _是__电__解__质__也__不__是__非__电__解__质__; NH3·H2O为可溶性一元弱碱(具有碱的通性),写出AlCl3 与氨水反应的离子方程式: _A_l_3+_+_3_N_H_3_·__H_2O_______3_N_H__4__+_A_l_(_O_H_)_3_↓__。
取少量样品与碱混合于试管中然后加热将湿润的红色石蕊试纸靠近管口试纸变蓝说明样品中含有也可将蘸有浓盐酸的玻璃棒靠近管口若有白烟产生说明样品中含有对点训练2判断正误
K12课件
第2课时 氨气与铵盐
1
K12课件
一、氨气 (一)物理性质 _无__色__ _有__刺__激__性__气味_气__体,标准状况下,密度比空气_小__,_易__ 溶于水,常温、常压下1体积水能溶解约_7_0_0_体积氨气,易 液化。
29
K12课件
检验氨气的方法:_①__用__湿__润__的__红__色__石__蕊__试__纸__靠__近__瓶__口__,__若__试__ _纸__变__蓝__,__证__明__是__氨__气__;__②__用__玻__璃__棒__一__端__蘸__取__浓__盐__酸__靠__近__瓶__ _口__,__若__产__生__白__烟__,__证__明__是__氨__气__。
22
K12课件
【对点训练1-1】下列关于氨水的说法中,不正确的是( C )
A.氨水和液氨不同,氨水是混合物,液氨是纯净物
B.氨水中物质的量浓度最大的粒子是NH3·H2O(除了水) C.氨水显弱碱性,故通常保存在金属容器中
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第三章自然界中的元素基础知识总结
第一节碳的多样性
1.由同一种元素组成的性质不同的几种单质,互称为同素异形体。
金刚石、石墨和C60
是碳元素的同素异形体。
2.金刚石是无色透明的片状固体。
其中,每个碳原子均与相邻的4个碳原子相连,形成正
四面体结构。
在自然界中硬度最大,不导电。
3.石墨是深灰色、有金属光泽、不透明的片状固体。
质软、有滑腻感。
碳原子呈层状排列,
每一层的碳原子形成平面正六边形。
4.C60是灰黑色固体,形成球状结构,表面呈正六边形和正五边形。
5.Na2CO3和NaHCO3的性质比较
性质Na2CO3NaHCO3
俗称纯碱或苏打小苏打
色态白色粉末白色固体
溶解度Na2CO3> NaHCO3
NaHCO3+HCl=NaCl+CO2↑+H2O 与盐酸反应Na2CO3+2HCl=2NaCl+CO2↑
+H20
NaHCO3与酸反应比较剧烈
与NaOH反应不反应NaOH+ NaHCO3= Na2CO3+ H2O 与BaCl2溶液反应不反应
稳定性(加热)稳定不稳定,加热分解
相互转化
6.Na2CO3和NaHCO3如何鉴别?
(1)加热比较:分解产生气体并通入澄清石灰水变浑浊的是碳酸氢钠,无现象的是碳酸钠(2)加酸反应比较:比较剧烈是碳酸氢钠
(3)滴加CaCl2、BaCl2溶液:产生白色沉淀的是碳酸钠,无现象的是碳酸氢钠。
7.温室效应:由于人类的活动,特别是生产和生活中化石燃料大幅度增加,使大气中二氧
化碳的含量猛增,破坏了自然界中原有平衡,导致全球气候变暖。
8.高炉炼铁中碳的转化:过程是将铁矿石还原成金属铁的过程,原料是焦炭和铁矿石(主
要成分是Fe2O3)。
但起还原作用的主要是一氧化碳。
焦炭在炼铁过程中的两个作用:
①燃烧提供热量;②用于制还原剂CO
9.在生活中,水壶中常常有水垢,它的主要成分是碳酸钙。
自来水中存在Ca(HCO3)2,受
热分解生成CaCO3,积聚在壶底,便形成水垢。
相关化学方程式:____________________
第二节氮的循环
1.氮气的物理性质:在通常状况下,氮气是一种无色无味、难溶于水的气体。
在空气中约
占其体积的78%
2.化学性质:在通常情况下,氮气的化学性质不活泼,很难与其他物质发生反应。
但在一
定条件下,氮气能与氧气、氢气等物质发生反应。
反应方程式:○1_____________
○2
3.使空气中游离态的氮转化为含氮化合物的方法叫氮的固定,简称固氮。
分为自然固氮和
人工固氮。
4.氮的氧化物有六种:N2O、NO、N2O3、NO2、N2O4、N2O5 。
NO是无色、难溶于水的
气体,易被空气中的氧气氧化为NO2:______________;NO2是红棕色、有刺激性气味有毒的气体,易溶于水,重要的反应有:__________________________
5.氨是没有颜色、有刺激性气味的气体,比空气轻,极易溶于水而且能快速溶解,在常温
下1体积水大约能溶700体积的氨气。
易液化,常作制冷剂。
6.氨的喷泉实验要成功,需保证烧瓶和烧杯液体之间有足够大的压强差,为此需注意三方
面:○1氨气要收集满○2氨和烧瓶都要干燥○3气密性要良好
7.氨的化学性质:
(1)能水反应___________________,溶液显碱性。
(2)与酸反应NH3+HCl==NH4Cl 将分别蘸有浓盐酸和浓氨水的两根玻璃棒靠近(不要接触),会有白烟产生,原因是挥发出来的HCl和NH3两气体相遇,生
成了NH4Cl固体小颗粒。
这也是检验氨气的方法之一。
(3)有还原性
8.氨的实验室制法原理:
装置:固——固反应加热装置(与制取O2装置相同)收集方法:只能用向下排空气法干燥方法:用碱石灰、固体NaOH等
检验方法:○1用湿润的红色石蕊试纸(变蓝)○2蘸有浓盐酸的玻璃棒接近瓶口(产生白烟)
棉花团的作用:防止NH3与空气形成对流,提高了收集NH3的纯度。
9.铵盐都是白色晶体,都溶于水。
不稳定,受热易分解:
与碱反应都能生成氨气,离子方程式为:,产生的气体能使红色石蕊试纸变蓝,故一般用这个原理来检验铵盐。
10.纯净的硝酸是无色、易挥发、有刺激性气味的液体。
质量分数在95%以上的浓硝酸在空
气中由于挥发出硝酸蒸气会产生“发烟”现象,通常叫做发烟硝酸。
11.硝酸的化学性质
(1):酸性:稀硝酸使石蕊试液变红,浓硝酸使石蕊试液先变红后褪色。
(2)不稳定性:浓硝酸受热或见光易分解产生红棕色的NO2, 二氧化氮又溶在浓硝酸中
而使溶液呈黄色。
其方程式为:,一般保存在棕
色试剂瓶中并放置在阴凉处。
(3)强氧化性
○1与金属反应:能与除金、铂、钛以外的大多数金属反应,产物与硝酸的浓度有关。
通常浓硝酸与金属反应生成二氧化氮,稀硝酸与金属反应生成一氧化氮,不会产生氢气。
在反应中硝酸既表现酸性又表现氧化性。
如:
○2与非金属反应,只表现氧化性。
12.氮的氧化物(NO2和NO)是产生光化学烟雾和酸雨的主要原因。
水体中含有过量的氮会使
水体富营养化,造成污染。
第三节硫的转化
1.硫以游离态和化合态广泛存在于自然界中,并且能相互转化。
2.硫单质俗称硫磺,它是一种黄色或淡黄色固体;很脆,易研成粉末;不溶于水,
微溶于酒精,易溶于二硫化碳,熔点和沸点都不高。
硫有多种同素异形体,常见
的有斜方硫和单斜硫。
3.单质硫化合价处于中间价态,既有氧化性又有还原性:
(1)氧化性:(剧烈反应,能保持红热,生成黑色固体)
注意:S与变价金属Fe、Cu反应时,化合价显低价,说明硫的氧化性比氯气的氧化性弱。
(2)还原性:硫在空气中点燃,火焰为淡蓝色,在纯氧中则为蓝紫色,生成二氧化
硫气体。
其方程式为:
4.通常状况下,二氧化硫是无色、有刺激性气味、有毒气体,1体积水大约能溶40体积。
总结:(1)常见气体溶解性NH3>HCl>SO2>Cl2>CO2>O2
(2)常见有刺激性气体Cl2、HCl 、NH3、SO2 、NO2
5.SO2的化学性质
(1)是酸性氧化物,是亚硫酸的酸酐,具有酸性氧化物的通性。
与水反应:
(2)与碱反应:
将SO2通入澄清的石灰水中变浑浊,继续通入又变澄清。
和CO2的性质相似
(4)还原性:
(5)氧化性:
(6)漂白性:SO2能跟某些有色物质反应而生成不稳定的无色物质,该物质受热分解会恢复原状,如品红溶液。
HClO是因为有氧化性而具有漂白性,不能恢复原状。
6. 纯硫酸是无色粘稠油状液体,沸点高,难挥发。
易溶于水,放出大量的热。
稀释时应将浓硫酸慢慢加入水中,并用玻璃棒不断搅拌。
7. 浓硫酸具有吸水性、脱水性、强氧化性。
能够与很多物质发生氧化还原反应。
第四节海水中的元素
1.海水中的元素分常量元素和微量元素。
其中常量元素大部分以盐的形式存在,在这些盐
类物质中,NaC l占80%以上。
2.从海水中提镁的基本方法是往海水里加碱,得到Mg(OH)2沉淀,将沉淀分离出来后加
入盐酸,把它变成氯化镁,然后经过结晶、过滤、干燥、电解,就可以得到金属镁。
3.镁是一种密度较小、熔点较低、硬度很软的有金属光泽的银白色固体,有良好的导电、
导热和延展性。
4.镁是一种比较活泼的金属,具有较强的还原性。
(1)与非金属反应
(2)与水反应
(3)在点燃条件下,能与二氧化碳反应
(Mg燃烧不能用灭火器来扑灭)
5.卤族元素包括氟、氯、溴、碘等,其中溴称为海洋元素。
都具有较强的氧化性,其单质
氧化性强弱顺序为F2>Cl2>Br2>I2
6.溴和碘的物理性质
物理性质溴单质碘单质
颜色红棕色紫黑色
状态液态固体
溶解性和溶液颜色水橙黄色褐(深黄色)酒精橙红褐色
CCl2 橙红紫红
物理特性易挥发易升华
7.溴有毒,微溶液水,易溶于酒精、四氯化碳等有机溶剂。
在实验室中溴单质盛放在磨砂、
细口的玻璃瓶中,且常用水封,防止溴的挥发。
8.碘单质是易升华的固体,故碘保存在广口玻璃瓶,置于低温避光处。
9.利用混合物中一种溶质在互不相溶的溶剂里溶解性的不同,用一种溶剂从它与另一溶剂
所组成的溶液中提取出来的方法叫萃取。
10.溴单质的氧化性介于氯气和液溴单质之间,因此在海水提溴的化工生产中可以选用氯气
做氧化剂。
从海水中,一般要经历浓缩、氧化和提取三个步骤。
11.Cl-、Br-、I-的检验:
加入AgNO3溶液,有白色沉淀(AgCl),则含有Cl-;若有淡黄色沉淀(AgBr),则有Br-;若产生黄色沉淀(AgI),则含有I-。
