界面化学试题
环境化学试题
一、填空1、造成环境污染的因素有物理、化学和生物的三方面,其中化学物质引起的约占______。
2、污染物的性质和环境化学行为取决于它们的和在环境中的。
3、环境中污染物的迁移主要有、和三种方式。
4、人为污染源可分为___________、___________、___________、和____________。
二、选择题1、属于环境化学效应的是。
A热岛效应B温室效应C土壤的盐碱化D噪声2、五十年代日本出现的痛痛病是由______污染水体后引起的。
A CdB HgC PbD As3、五十年代日本出现的水俣病是由______污染水体后引起的。
A CdB HgC PbD As三、名词解释环境污染、环境化学、环境效应、环境污染物环境污染:由于人为因素使环境的构成或状态发生变化,导致环境素质下降,从而扰乱或破坏生态系统和人们正常的生活与生产条件的现象。
环境化学:环境化学是在化学科学的传统理论和方法基础上发展起来的,以化学物质在环境中出现而引起的环境问题为研究对象,以解决环境问题为目标的一门新兴学科。
环境化学主要研究有害化学物质在环境介质中的存在、化学特性、行为和效应及其控制的化学原理和方法。
环境效应:自然过程或人类的生产和生活活动会对环境造成污染和破坏,从而导致环境系统的结构和功能发生变化,称为环境效应。
环境污染物:指进入环境后使环境的正常组分和性质发生直接或间接的有害于人类的变化的物质。
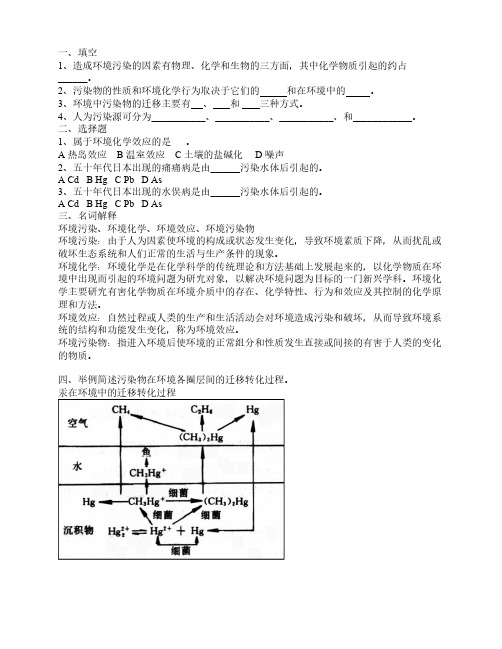
四、举例简述污染物在环境各圈层间的迁移转化过程。
汞在环境中的迁移转化过程环境化学第二章练习题参考答案一、填空题1、造成环境污染的因素有物理、化学和生物的三方面,其中化学物质引起的约占80%-90%。
2、污染物在环境中的迁移主要有机械迁移、物理-化学迁移和生物迁移三种方式。
3、污染物的性质和环境化学行为取决于它们的化学结构和在环境中的存在状态。
4、当今世界上最引人瞩目的几个环境问题臭氧空洞、温室效应、酸雨等是由大气污染所引起的。
物化考研试题

A卷一、单项选择题(共30 题, 75 分)1.反应A(g)+B(g)?D(g)在固体催化剂下进行,在等温下达到吸附平衡时,覆盖度:q A= k A P A/( 1+k A P A+k B P B)q A= k A P A/ (1+k A P A+k B P B)当 A 是弱吸附,而 B 是强吸附时,反应速率为A. r=KPA B. r=KP BC. r=K(P B/P A)D. r=K(P A/P B)2.对于化学吸附,下列说法不正确的是A.吸附是单分子层B.吸附力来源于化学键力C.吸附热接近反应热D.吸附速度快,升高温度能降低吸附速度3.晶体颗粒大小与其溶解度关系是,微小晶体的溶解度A.大于大块、大粒晶体C.等于大块、大粒晶体B. 小于小块、小粒晶体D.与大块、大粒晶体溶解度的关系不好确定4.固体吸附剂在溶液中的吸附量A. 总是随浓度的增加而增加B.随溶解度的增加而增加C.随溶质极性的增加而增加D.能使固液表面自由能降低最多的溶质被吸附的量是最多5.液体在毛细管中上升的高度与下列哪一个因素无关A.温度B. 液体密度C.附加压力D. 大气压力6.一分散体系,在温度 T 每当高度升高-2m时,体系浓度降低一半,则粒子在分散介质中的重量为4′10A. 0.02272 kTB. 17.33 kTC. 39.9 1 kTD. 0.02272/kT7.下列有关冷光描述中, 正确的是A.原子或分子吸收外界光变为激发分子,发出与原光源不同的光B.化学反应过程中产生的激发分子回到基态时发出的光C.切断电源后继续发出的光D.由物体反射回来的光8.将含有表面活性剂的水溶液形成下列四种半径为R的液滴或气泡,受到附加压力最大的是A.在空气中形成的液滴B.在空气中吹成的气泡C.在溶液中吹出的气泡D.将此溶液滴入石蜡中形成液滴9.将浓度为-3-3的 AgNO溶液等体积混合后制的得AgI 溶胶,下列三0.5 mol×dm的 KI 溶液和 0.1 mol×dm3种电解质,其聚沉值由大到小的顺序为A. FeCl >MgSO>K Fe(CN)B. K Fe(CN) >MgSO>FeCl精选文库C. MgSO4>FeCl3 >K3Fe(CN) 6D. K 3 Fe(CN)6 >FeCl3 >MgSO410.Donnan 平衡的现象是:在有大分子电解质存在的条件下,小离子在膜两边浓度不相等的现象,产生此现象的原因是A.溶液粘度大,大离子迁移速度小B.小离子浓度大,影响大离子通过半透摸膜C.大离子不能透过半透膜,因静电作用妨碍小离子的均匀分布D.大离子浓度大,妨碍小离子通过半透膜11.有两种蛋白质,第一种的分子量为100000,第二种为60000,在相同介质相同温度下形成密度相近的溶液,其扩散系数之比D1/D 2A. 1.67B. 0.60C. 0.84D. 1.1812.洗涤时,用表面活性剂能除去油脂油垢A. 完全是由于润湿作用B.完全是由于加溶作用C. 完全是由于乳化作用D.是由于上述三种作用的综合13.竖直玻璃毛细管内有一小段润湿液柱,在液柱下端处涂一点表面活性剂,则管内液柱A.向上移动B.向下滑落C.不动D.液柱不动,但液面的曲率半径变大14.吉布斯吸附等温式中,表面吸附量G 的意义A.溶液表面层的浓度B.溶液表面的浓度与溶液本体的浓度差C.溶质超过体相的物质相D.单位表面上溶质超过体相内同量溶剂中所含溶质的物质量15.在相同条件下,同一物质的微小晶体比之普通晶体具有A. 较小的蒸气压B.较高的熔点C.较大的化学势D.较小的溶解度16.溶胶在外加直流电场作用下,向某一电极方向运动的只是A.胶核B.胶粒C.胶团D.紧密层17.溶胶和大分子溶液的本质区别在于A.粒子大小不同B.渗透压差别很大C.热力学稳定性不同D.丁达尔效应的强弱不同18.在 Fe(OH)3、 As2 S3、 Al(OH) 3和 AgI (含过量AgNO3)四种溶液中有一种不能和其它溶胶相互混合,否则会引起聚沉,这种溶胶是A. Fe(OH) 3B. As 2 S3C. Al(OH) 3D. AgI19. 298 K 时,某溶胶在介质粘度-122-1h=0.001 Pa ×S时,其扩散系数 D=2.18 ′ 10m×S,同温度下该溶精选文库胶在介质粘度h=0.01 Pa ×S时,扩散系数-122-1则该溶胶在上述两种情况下的胶粒半D=4.36 ′ 10m×S ,径之比 r 1 /r 2为A. 1:10B. 2:1C. 20:1D. 1:2020. HLB值是表示表面活性剂的A.效率B.酸碱平衡常数C.亲水性、亲油性强弱D.溶解度21.关于溶胶的某些特征,正确的说法是A.多相系分散介质不能透过半透膜,分散相可透过半透膜B.分散相和分散介质之间存在某种界面,分散相可透过滤纸,但透不过半透膜C.多相体系分散介质透不过半透膜,分散相可透过滤纸D.多相系分散相和介质均可透过滤纸和半透膜22.根据 DLVO理论,以下说法正确的是A.溶胶是否稳定取决于双电层斥力、范德华力和化学作用力B.聚沉值与起聚沉作用的离子价数的六次方成反比C.由于溶剂化壳层的作用,当胶粒不带电时也可能稳定D.当胶粒间的距离趋向无限大时,双电层斥力势能和范德华力能不为零,大小相等,符号相同23.在两个充有 0.001mol ×dm -3KCl 溶液的容器之间是一个AgCl 多孔塞,塞中充满了KCl 溶液,在多孔塞两侧放两个电极,接通直流电源,则液体向A.正极移动B. 负极移动C.一部分向正极,另一部分向负极D. 不移动24.在一水平毛细管中装有润湿液体( 如水 ) ,若在右端加热,则液体A.不移动B. 向左移动C.向右移动 D .无法判断25.当表面活性剂入加入到溶剂后,所产生的结果是A. dr/dC > 0,负吸附B. dr/dC > 0,正吸附C. dr/dC < 0,负吸附 D . dr/dC < 0,正吸附26.对于物理吸附,哪一点是不正确的A. 吸附力来源于范德华力B.吸附速率较小C.吸附热较小,一般无选择性 D .吸附层可以是单层也可为多层27.一肥皂泡的站半径为R,表面张力为r ,则肥皂泡的内外压力差DP为A.0B.r/RC.2r/R D .4r/R28.下列有关 x 电势的描述,正确的是A.x 电势只有当固 - 液两相相对运动时,都能被测定B.x 电势与胶粒在电场中的电势梯度成正比C.x 电势是胶粒表面的双电层的热力学电势D.介质粘度越大,胶粒在电场中运动速率越慢,x 电势就越大29.溶胶与大分子溶液的主要区别A.粒子大小不同B.相状态和热力学稳定性不同C.渗透压不同 D .丁达尔效应强弱不同30.在选用乳化剂时,表面活性剂的HLB值是一个重要参数。
表面化学试题及答案

表面化学试题及答案表面化学是研究物质表面性质和表面现象的科学。
以下是一套表面化学的试题及答案,供参考。
一、选择题(每题2分,共20分)1. 表面张力的单位是什么?A. 牛顿(N)B. 帕斯卡(Pa)C. 焦耳(J)D. 米(m)答案:B2. 表面活性剂的分子结构通常具有什么特点?A. 非极性分子B. 极性分子C. 两亲分子D. 离子分子答案:C3. 以下哪个不是表面化学中常见的界面?A. 气-液界面B. 固-液界面C. 液-液界面D. 真空界面答案:D4. 表面能是指什么?A. 表面张力与表面面积的乘积B. 表面张力与体积的乘积C. 表面张力与质量的乘积D. 表面张力与密度的乘积答案:A5. Langmuir吸附等温线描述的是:A. 吸附量与压力的关系B. 吸附量与温度的关系C. 吸附量与时间的关系D. 吸附量与浓度的关系答案:A二、填空题(每空2分,共20分)6. 表面化学中的吸附现象可以分为________和________两种基本类型。
答案:物理吸附;化学吸附7. 在Langmuir吸附等温线中,当吸附分子覆盖率为1时,表示吸附分子已经________了整个表面。
答案:饱和8. 表面张力是由于液体表面的分子受到不均匀的________作用而产生的。
答案:力9. 表面活性剂在降低表面张力方面的作用是由于其分子结构中具有________和________两端。
答案:亲水;亲油10. 在Kelvin方程中,气体的吸附量与温度、压力和________有关。
答案:孔径三、简答题(每题15分,共30分)11. 简述表面化学在工业生产中的应用。
答案:表面化学在工业生产中的应用非常广泛,例如在石油工业中,表面活性剂用于提高石油的采收率;在化妆品工业中,表面活性剂用于稳定乳液;在制药工业中,表面活性剂用于制备药物的分散体系等。
12. 解释什么是表面活性剂,并举例说明其在日常生活中的应用。
答案:表面活性剂是一种能够显著降低液体表面张力的化合物,通常具有两亲分子结构。
2000-2010中科院《环境化学》考研真题

中国科学院生态环境中心环境化学历年试题2000年环境化学一、基本概念与常识1、常压下25°C的水中能有多少溶解氧?如果用{CH2O}来表示有机物的话,降解多少有机物就可以消耗完这些溶解氧?(8分)2、水的硬度(2分)3、水的总碱度(2分)4、水中二氧化碳的主要来源是什么?(2分)5、土壤的组成(2分)6、大多数土壤中氮的形态、其最终形态为何。
(2分)7、地球温暖化有什么危害?如何控制?(2分)8、大气分为几层?臭氧层位于那一层?主要臭氧层破坏物质;最近一次有关臭氧层保护的国际大会于何时在哪国召开?(5分)二、计算题1、在碱性条件下向7.9×10-5mol/L的铜离子溶液中加入EDTA 并使之过量200mg/L,请计算溶液中铜离子的平衡浓度。
EDTA络合物的稳定常数为6.3×1018,EDTA的分子量为372.1。
(15分)2、CaF2溶解度积为3.5×10-11,请计算要想使氟离子浓度达到8mg/L以下,至少需要多大的钙离子浓度。
(氟离子的分子量为19、钙离子的分子量为40)(10分)三.论述题1.何谓硝酸化作用、其在自然界中的意义何在?写出其反映方程式;何谓反硝化作用,硝酸化、反硝化在水处理上有何重要应用?(15分)2.主要点源水污染有那些,主要面源水污染有那些,面源和点源的主要控制或治理方法。
(15分)3.什么是富营养化、它有什么危害。
(10分)4.什么是二恶英、其危害及来源。
(10分)2001年环境化学一、试述环境化学的学科特点,对象和主要研究内容(20分)二、试解释以下名次(20分)1、天然水的酸度和碱度2、电子活度3、双电层理论4、光量子产率5、共代谢6、专属吸附7、多氯联苯(PCB)8、毒性(Toxicity)9、无观察效应浓度(NOEC)10、生态效应三、问答题(20分)1、氮的自然循环过程在废水中的有机、无机氮化物的去除过程得到了有效地应用。
表面化学试题及答案

表面化学试题及答案一、选择题(每题2分,共10分)1. 表面化学主要研究物质的哪个区域的化学性质?A. 内部B. 表面C. 界面D. 外部答案:B2. 表面张力是指液体表面分子之间相互吸引的力,其单位是?A. 牛顿B. 焦耳C. 帕斯卡D. 牛顿·米答案:C3. 表面活性剂在水溶液中降低表面张力的机理是什么?A. 表面活性剂分子的疏水部分朝向空气B. 表面活性剂分子的亲水部分朝向空气C. 表面活性剂分子的疏水部分朝向水D. 表面活性剂分子的亲水部分朝向水答案:A4. 固体表面的吸附作用主要分为哪两种类型?A. 物理吸附和化学吸附B. 静态吸附和动态吸附C. 单层吸附和多层吸附D. 可逆吸附和不可逆吸附答案:A5. 表面能是指单位面积表面所具有的能量,通常用哪个符号表示?A. ΔHB. ΔGC. γD. Q答案:C二、填空题(每题2分,共10分)1. 表面化学中的吸附作用是指分子、原子或离子在固体或液体表面的________现象。
答案:积累2. 表面化学中的润湿现象可以通过接触角的大小来描述,接触角越小,润湿性越________。
答案:强3. 在表面化学中,表面活性剂的临界胶束浓度(CMC)是指表面活性剂分子开始形成胶束的最低浓度,其值越低,表面活性剂的________越强。
答案:表面活性4. 表面化学中的Langmuir吸附等温线描述了在一定温度下,吸附量与吸附质的平衡压力之间的关系,当吸附达到饱和时,吸附量与压力的关系呈________。
答案:线性5. 表面化学中的Zisman方程用于描述固体表面的临界表面张力,该方程的斜率与固体表面的________有关。
答案:极性三、简答题(每题5分,共20分)1. 简述表面化学在工业生产中的应用。
答案:表面化学在工业生产中的应用非常广泛,例如在涂料工业中,通过控制表面张力来改善涂料的流平性和附着力;在石油工业中,通过降低油水界面的表面张力来提高原油的采收率;在纺织工业中,利用表面活性剂改善纤维的润湿性和染色均匀性;在医药领域,通过控制药物的表面性质来提高其生物利用度等。
材料化学专业试题及答案

材料化学专业试题及答案一、选择题(每题2分,共20分)1. 下列哪种物质不属于材料化学的研究范畴?A. 金属材料B. 陶瓷材料C. 生物高分子D. 塑料制品答案:D2. 材料的微观结构对其宏观性能有重要影响,以下哪项不是微观结构的描述?A. 晶格结构B. 缺陷C. 相界面D. 颜色答案:D3. 下列哪种材料具有铁磁性?A. 铜B. 铝C. 镍D. 铅答案:C4. 材料的热处理过程中,淬火的目的是什么?A. 提高硬度B. 增加韧性C. 减少成本D. 提高导电性答案:A5. 下列哪种现象不属于材料的老化?A. 氧化B. 腐蚀C. 磨损D. 熔化答案:D6. 材料的断裂韧性通常用来描述材料的哪项性能?A. 硬度B. 韧性C. 强度D. 塑性答案:B7. 下列哪种材料具有最高的热导率?A. 石墨烯B. 硅C. 橡胶D. 玻璃答案:A8. 材料的疲劳寿命与加载频率的关系是什么?A. 正比B. 反比C. 无关D. 先增加后减少答案:B9. 下列哪种合金具有形状记忆效应?A. 铝合金B. 铜合金C. 镍钛合金D. 铁合金答案:C10. 在材料科学中,霍尔效应常用于测量材料的哪种性质?A. 电阻率B. 热导率C. 磁导率D. 载流子浓度答案:D二、填空题(每题2分,共20分)11. 材料的硬度是指材料抵抗塑性变形的能力。
12. 材料的断裂强度是指材料在断裂前能承受的最大应力。
13. 陶瓷材料通常具有高熔点、硬度大和良好的化学稳定性等特点。
14. 金属材料的腐蚀可以通过涂层、阴极保护或使用耐腐蚀合金等方法来减缓。
15. 材料的疲劳是指在循环应力下材料逐渐损伤直至断裂的过程。
16. 材料的导热性能可以通过测量其热导率来评估。
17. 材料的弹性是指在外力作用下材料发生形变,去除外力后能恢复原状的性质。
18. 聚合物的玻璃化转变温度是指聚合物从玻璃态转变为高弹态的温度。
19. 纳米材料的特殊性质包括光学性质、磁学性质和催化性质等。
(完整版)固态相变原理考试试题+答案

固态相变原理考试试题一、(20分)1、试对固态相变地相变阻力进行分析固态相变阻力包括界面能和应变能,这是由于发生相变时形成新界面,比容不同都需要消耗能量.(1)界面能:是指形成单位面积地界面时,系统地赫姆霍茨自由能地变化值.与大小和化学键地数目、强度有关.共格界面地化学键数目、强度没有发生大地变化,最小;半共格界面产生错配位错,化学键发生变化,次之;非共格界面化学键破坏最厉害,最大.(2)应变能①错配度引起地应变能(共格应变能):共格界面由错配度引起地应变能最大,半共格界面次之,非共格界面最小.②比容差引起地应变能(体积应变能):和新相地形状有关,,球状由于比容差引起地应变能最大,针状次之,片状最小.2、分析晶体缺陷对固态相变中新相形核地作用固相中存在各种晶体缺陷,如空位、位错、层错、晶界等,如果在晶体缺陷处形核,随着核地形成,缺陷将消失,缺陷地能量将给出一供形核需要,使临界形核功下降,故缺陷促进形核.(1)空位:过饱和空位聚集,崩塌形成位错,能量释放而促进形核,空位有利于扩散,有利于形核.(2)位错:①形成新相,位错线消失,会释放能量,促进形核②位错线不消失,依附在界面上,变成半共格界面,减少应变能.③位错线附近溶质原子易偏聚,形成浓度起伏,利于形核.④位错是快速扩散地通道.⑤位错分解为不全位错和层错,有利于形核.Aaromon总结:刃型位错比螺型位错更利于形核;较大柏氏矢量地位错更容易形核;位错可缠绕,割阶处形核;单独位错比亚晶界上位错易于形核;位错影响形核,易在某些惯习面上形成.(3)晶界:晶界上易形核,减小晶界面积,降低形核界面能二、(20分)已知调幅分解1、试分析发生调幅分解地条件只有当R(λ)>0,振幅才能随时间地增长而增加,即发生调幅分解,要使R(λ)>0,得且. 令R(λ)=0得λc—临界波长,则λ<λc时,偏聚团间距小,梯度项很大,R(λ)>0,不能发生;λ>λc时,随着波长增加,下降,易满足,可忽略梯度项,调幅分解能发生.2、说明调幅分解地化学拐点和共格拐点,并画出化学拐点、共格拐点和平衡成分点在温度——成分坐标中地变化轨迹化学拐点:当G”=0时.即为调幅分解地化学拐点;共格拐点:当G”+2η2Y=0时为共格拐点,与化学拐点相比共格拐点地浓度范围变窄了,温度范围也降低了.3、请说明调幅分解与形核长大型相变地区别1、阐明建立马氏体相变晶体学表象理论地实验基础和基本原理(1)实验基础1 / 32 /3 ① 在宏观范围内,惯习面是不应变面(不转变、不畸变);② 在宏观范围内,马氏体中地形状变形是一个不变平面应变;③ 惯习面位向有一定地分散度(指不同片、不同成分地马氏体);④ 在微观范围内,马氏体地变形不均匀,内部结构不均匀,有亚结构存在(片状马氏体为孪晶,板条马氏体为位错).(2)基本原理在实验基础上,提出了马氏体晶体学表象理论,指出马氏体相变时所发生地整个宏观应变应是下面三种应变地综合:① 发生点阵应变(Bain 应变),形成马氏体新相地点阵结构.但是Bain 应变不存在不变平面,不变长度地矢量是在圆锥上,所以要进行点阵不变切变.② 简单切边,点阵不变非均匀切变,在马氏体内发生微区域变形,不改变点阵类型,只改变形状,通过滑移、孪生形成无畸变面.③ 刚体转动,①②得到地无畸变地平面转回到原来地位置去,得到不畸变、不转动地平面.用W-R-L 理论来表示:P 1=RPB,P 1为不变平面应变地形状变形,B 为Bain 应变、用主轴应变来表示,R 为刚体转动、可以用矩阵来表示,P 为简单应变.2、阐明马氏体相变热力学地基本设想和表达式地意义答:基本设想:马氏体相变先在奥氏体中形成同成分地体心核胚,然后体心核胚再转变为马氏体M.所以马氏体相变自由能表达式为:M M G G G γγαα→→→∆=∆+∆,式中:① M G γ→∆表示奥氏体转变为马氏体地自由能差.,此时温度为Ms 温度.② G γα→∆表示母相中形成同成分地体心核胚时地自由能变化,定义为T 0温度γ与α地平衡温度,,为T<T 0时,产生核胚地温度.③ MG α→∆表示体心核胚转变为马氏体M 而引起地自由能变化.消耗于以下几个方面:切变能(进行不变平面切变、改变晶体结构和形状地能量);协作形变能(周围地奥氏体产生形变地能量);膨胀应变能(由于比容变化而致);存储能(形成位错地应变能、形成孪晶地界面能);其他(表面能、缺陷能、能量场地影响等).四、(20分)1、试解释沉淀相粒子地粗化机理由Gibbs-Thompson 定理知,在半径为r 地沉淀相周围界面处母相成分表达式: 2()()(1)m V C r C RTr αασ=∞-当沉淀相越小,其中每个原子分到地界面能越多,因此化学势越高,与它处于平衡地母相中地溶质原子浓度越高. 即:C (r 2)> C(r 1) .由此可见在大粒子r 1和小粒子r 2之间地基体中存在浓度梯度,因此必然有一个扩散流,在浓度梯度地作用下,大粒子通过吸收基体中地溶质而不断长大,小粒子则要不断溶解、收缩,放出溶质原子来维持这个扩散流.所以出现了大粒子长大、小粒子溶解地现象. 需要画图辅助说明!2、根据沉淀相粒子粗化公式:,分析粒子地生长规律(奥斯瓦尔德熟化)①当时,r=r ,rt ∂∂=0粒子不长大;②当时,r <r ,r t ∂∂<0小粒子溶解;③当时,r>r ,r t ∂∂>0粒子长大;④当时,r=2r ,r t ∂∂最大,长大最快;⑤长大过程中,小粒子溶解,大粒子长大,粒子总数减小,r 增加,更容易满足②,小粒子溶解更快;⑥温度T 升高,扩散系数D 增大,使rt ∂∂增大.所以当温度升高,大粒子长大更快, 小粒子溶解更快.五、(20分)已知新相地长大速度为:1、 试分析过冷度对长大速度地影响过冷度很小,∆gv 很小,∆gv 随过冷度地增加而增加,∆gv 越小长大速率越大,表明:长大速度u 与过冷度或者成正比,也就是当T 下降,过冷度增大,上升,长大速度u 增大.(1) 过冷度很很大,∆gv/kT 很大,exp(-∆gv/kT)→0,此时,温度越高长大速率越大,2、 求生长激活能过冷度很大时,exp(-∆gv/kT)→0,公式转化为0exp()Q kT μλν=-3 / 3 两边取对数,0exp()Q kT μλν=-则(ln )(1/)d Q K d T μ=-则为单个原子地扩散激活能,再乘以阿伏加德罗常数N 0,得生长激活能.。
结构化学试题及答案

结构化学试题及答案结构化学试题一、选择题(每小题只有一个最佳答案,共18小题,每题两分,共36分)1.下列性质属于化学性质的是A.沸点B.硬度C.稳定性D.溶解性2.下列变化过程中既有物理变化又有化学变化的是A. 活性炭吸附冰箱中的异味B.干冰汽化C.点燃蜡烛D.分离液态空气制取氧气3.下列物质的俗名与化学式一致的是A.水银Ag B碱石灰CaOH C.酒精CH4O D.烧碱NaOH4.吸烟有害健康,其原因是吸烟时会产生多种有害物质,污染环境,害人害己。
香烟燃烧产生的烟气中,最容易与人体血红蛋白结合的物质是A.一氧化碳B.尼古丁C.二氧化硫D.二氧化碳5.下列物质由离子构成的是A.铜B.氯化钠C.氧气D.金刚石6.下列混合物中不属于溶液的是A.食盐水B.泥水C.碘酒D.澄清石灰水7.右边结构示意图表示的微粒是A.原子B.分子C.阳离子D.阴离子8.人类只有一个地球,为了社会可持续发展,必须解决环境保护问题,化学在这方面可以发挥重要的作用。
下列处理不符合这一思想的是A.增加污水处理工厂B.向燃煤中加生石灰固硫C.大量使用含磷酸钠(Na3PO4)的洗衣粉D.垃圾的分类回收和处理9.下列实验操作中能达到实验目的的是A.检验氢气纯度时,没有听到任何响声,表明氢气已纯净B.用适量的水可以区分硝酸铵固体和氢氧化钠固体C.用100ml的量筒量取8.55ml的水D.用PH试纸测定溶液酸碱度时,先将PH试纸用水润湿,然后再测定10遵守实验室规则,学习基本的实验操作方法,是实验成功的重要保证。
下列实验操作不正确的是A.检查装置的气密性B.液体的量取C.液体的加热 D稀释浓硫酸11物质中的杂质(括号内物质为杂质),所选用试剂和操作方法都正确的是物质选用试剂(过量) 操作方法A CO2(CO) O2 点燃B Fe(Cu) 稀盐酸加入稀盐酸充分反应后过滤、洗涤C CuSO4溶液(H2SO4) 氧化铜加入氧化铜粉末充分反应后过滤D 盐酸(H2SO4) Fe 加入Fe粉充分反应后过滤12.家庭生活中一些常见物质的pH如下:物质食醋牛奶食盐水牙膏肥皂水pH 2~3 6~7 7 8~9 9~10当我们被蚊虫叮咬后,蚊虫能在人的皮肤内分泌蚁酸(具有酸的性质),从而使皮肤肿痛。
全国化学奥林匹克竞赛(初赛)模拟试题(4)

全国化学竞赛初赛模拟试卷(04)(时间:3小时满分:100分)第一题(12分)1.日本物理学家Katsuya Shimizu发现锂元素在极高的压力下,自身的电阻会消失,成为超导体。
因此,锂目前除了是最轻的金属之外,还是超导转变温度最高的元素。
请指出这个实验的困难之处。
2.正烷烃是指没有支链的烷烃。
请仔细研究正烷烃的二氯取代物的同分异构体的个数。
(1)请写出正烷烃的碳原子个数n与二氯代物同分异构体个数y之间的关系。
(2)请写出正三十八烷、四十七烷二氯代物的同分异构体的个数。
3.观察下面两个有机分子回答问题:OO OOOOOO OOOO(1)以习惯命名法命名这两个有机物。
(2)分析指出两者中何者熔点较高。
第二题(6分)某学生在实验中得到一白色粉末,经分析符合NH4SbCl5。
X射线衍射分析表明,该晶体中阴离子全部为一个Sb与6个Cl组成的原子团,磁性表明,该粉末为反磁性。
1.试画出NH4SbCl5的结构式。
2.有一种经验分子式为(NH4)2SbCl6的物质。
X射线衍射分析表明,该晶体中阴离子也全部为一个Sb与6个Cl组成的原子团,磁性表明,该粉末为反磁性。
请你推测该生得到的白色粉末可能是什么?第三题(15分)氯氧化合物是重要的化合物。
试回答下列问题:1.1797年Hoyle在用浓H2SO4和氯酸钾反应时得到一种具有爆炸性的黄色气体。
几十年后证实该气体为ClO2。
写出反应方程式。
2.1851年Davy使2体积上述黄色气体完全分解,产物为3体积气体,其中氧和氯体积比为2∶1。
为什么Davy未能由此导出黄色气体的分子式为ClO2呢?3.1882年,Pebal 测得黄色气体的密度后,确定其组成为ClO 2。
他是如何确定的?他得出结论的前提条件是什么?4.ClO 2和O 3反应可得到ClO 3,后者在强碱中将发生歧化反应。
写出反应方程式。
由此,可将ClO 3写成什么形式?5.近代研究表明:ClO 2分子中Cl —O 键长为147pm ,比计算单键键长短22pm 。
(完整word版)胶体与界面化学试题及答案

1.什么是气凝胶?有哪些主要特点和用途?当凝胶脱去大部分溶剂,使凝胶中液体含量比固体含量少得多,或凝胶的空间网状结构中充满的介质是气体,外表呈固体状,这即为干凝胶,也称为气凝胶。
气凝胶是一种固体物质形态,世界上密度最小的固体。
气凝胶貌似“弱不禁风”,其实非常坚固耐用。
它可以承受相当于自身质量几千倍的压力,在温度达到1200摄氏度时才会熔化。
此外它的导热性和折射率也很低,绝缘能力比最好的玻璃纤维还要强39倍。
用途:(1)制作火星探险宇航服(2)防弹不怕被炸(3)过滤与催化(4)隔音材料(5)日常生活用品2.试述凝胶形成的基本条件?①降低溶解度,使被分散的物质从溶液中以“胶体分散状态”析出。
②析出的质点即不沉降,也不能自由行动,而是构成骨架,在整个溶液中形成连续的网状结构。
3.简述光学白度法测定去污力的过程。
将人工制备的污布放在盛有洗涤剂硬水的玻璃瓶中,瓶内还放有橡皮弹子,在机械转动下,人工污布受到擦洗。
在规定温度下洗涤一定时间后,用白度计在一定波长下测定污染棉布试片洗涤前后的光谱反射率,并与空白对照。
4.试述洗涤剂的发展趋势。
液体洗涤剂近几年的新的发展趋势:(1)浓缩化(2)温和化、安全化(3)专业化(4)功能化(5)生态化: ①无磷化②表面活性剂生物降解③以氧代氯5.简述干洗的原理干洗是在有机溶剂中进行洗涤的方法,是利用溶剂的溶解力和表面活性剂的加溶能力去除织物表面的污垢。
6. 脂肪酶在洗涤剂中的主要作用是什么?脂肪酶,人的皮脂污垢如衣领污垢中因含有甘油三脂肪酸酯而很难去除,在食品污垢中也含有甘油三脂肪酸酯类的憎水物质,脂肪酶能将这些污垢分解成甘油和脂肪酸。
7.在洗涤剂中作为柔和剂的SAA主要是什么物质?用作柔和剂的表面活性剂主要是两性表面活性剂8.用防水剂处理过的纤维为什么能防水?织物防水原理:将纤维织物用防水剂进行处理,可使处理后的纤维不表面变为疏水性,防水织物由于表面的疏水性使织物与水之间的接触角θ>90°,在纤维与纤维间形成的“毛细管”中的液面成凸液面,凸液面的表面张力的合力产生的附加压力△P的方向指向液体内部因此有阻止水通过毛细管渗透下来的作用。
胶体及界面化学复习试题库

一、凝胶1.什么是凝胶?有何特征〔两个不同〕?外界条件(如温度、外力、电解质或化学反响)的变化使体系由溶液或溶胶转变为一种特殊的半固体状态,即凝胶。
〔又称冻胶〕其一,凝胶与溶胶(或溶液)有很大的不同。
溶胶或溶液中的胶体质点或大分子是独立的运动单位,可以自由行动,因而溶胶具有良好的流动性。
凝胶那么不然,分散相质点互相连接,在整个体系内形成构造,液体包在其中,随着凝胶的形成,体系不仅失去流动性,而且显示出固体的力学性质,如具有一定的弹性、强度、屈服值等。
其二,凝胶和真正的固体又不完全一样,它由固液两相组成,属于胶体分散体系,共构造强度往往有限,易于遭受变化。
改变条件,如改变温度、介质成分或外加作用力等,往往能使构造破坏,发生不可逆变形,结果产生流动。
由此可见,凝胶是分散体系的一种特殊形式,共性质介于固体和液体之间。
2.举例说明什么是弹性和非弹性凝胶?由柔性的线性大分子物质,如洋菜吸附水蒸气先为单分子层吸附,然后转变为多分子层吸附,硫化橡胶在苯蒸气中的吸附那么是从一开场即为多分子层吸附。
这类凝胶的干胶在水中加热溶解后,在冷却过程中便胶凝成凝胶。
如明胶、纤维素等,在水或水蒸气中都发生吸附。
不同的吸附体系,其吸附等温线的形状不同,弹性凝胶的吸附与解析通常会形成较窄的滞后圈。
由刚性质点〔如SiO2、TiO2,V2O5、Fe2O3等〕溶胶所形成的凝胶属于非弹性凝胶,亦称刚性凝胶。
大多数的无机凝胶,因质点本身和骨架具有刚性,活动性很小,故凝胶吸收或释出液体时自身体积变化很小,属于非膨胀型。
通常此类凝胶具有多孔性构造,液体只要能润湿,均能被其吸收,即吸收作用无选择。
这类凝胶脱水枯燥后再置水中加热一般不形成原来的凝胶,更不能形成产生此凝胶的溶胶,因此这类凝胶也称为不可逆凝胶。
3.试述凝胶形成的根本条件?①降低溶解度,使被分散的物质从溶液中以“胶体分散状态〞析出。
②析出的质点即不沉降,也不能自由行动,而是构成骨架,在整个溶液中形成连续的网状构造。
胶体与表面化学试卷

试卷(一)一、是非题(4×5=20分)1、一物体其比表面越大,表面能也越大。
2、对于液体,其液面为凸面时,表面张力的合力指向液体外部。
3、过饱和蒸气形成的原因是新生的微小液滴的蒸气压大于同温度下平面液体的蒸气压。
4、作布朗运动的粒子的平均位移与其质量无关。
5、固—液相界面存在双电层是电动现象产生的本质原因。
二、填空题(4×5=20分)1、F为亥氏自由能,A是面积,表面张力σ______。
2、在相同条件下,两液滴的饱和蒸气压P1>P2,则相应的液滴半径r1___r2。
3、根据溶液吸附的吉布斯方程,可知当___0,当(为溶质活度)时,溶液表面发生正吸附。
4、θ为接触角,当COSθ=____时(填数字),液体完全润湿固体。
5、H+和Li+对负溶胶聚沉能力比较,H+____Li+。
三、单选题(4×5=20分)1、液体的内压力和表面张力的联系与区别在于(A)产生的原因相同而力的作用点不同(B)产生的原因相同而力的作用方向不同(C)力作用点相同而方向不同(D)产生的原因不同2、防毒面具吸附毒气而基本上不吸附氧气是因为(A)毒气密度比氧气大(B)毒气是物理吸附,氧气是化学吸附(C)毒气吸附速度快,氧气吸附慢(D)毒气液化温度高,氧气液化温度低3、BET 吸附理论最基本的假定是(A)固体表面各处不均匀的,吸附能力不相同(B)同层被吸附分子间有作用(C)固体表面是多分子层吸附(D)固体表面只有物理吸附4、表面活性剂在结构上的特征是(A)一定具有亲水基和亲油基(B)一定具有脂肪酸基或氨基(C)一定具有磺酸基或高级脂肪烃基(D)一定具有羟基和高级脂肪酸基5、区别溶胶与真溶液及悬浮液最简单而灵敏的方法是:(A)超显微镜测定粒子大小(B)乳光计测定粒子浓度(C)观察丁达尔现象(D)自测试题(一)答案一、是非题(4×5=20 分)1.Yes 2.no 3.yes 4.yes 5 .yes二、填空题(4×5=20 分)1.= 2. < 3. < 4. 1 5. >三、单选题(4×5=20 分)1.B 2. D 3. C 4. A 5. C四、双选题(8×5=40 分)1.D,E 2. B,C 3. C,E 4. A,C 5. A,D试卷(二)一、是非题(4×5=20分)1、在等温等压下且组成不变时以可逆方式增加表面积做的功,量值等于表面能。
化学工程基础考试试题

4、决定流体内摩擦力大小的物理量称为
1、不可压缩流体在圆形管道中,任意截面的流速与管内径( A. C. 成反比 B.
) 。
D. 成正比 ) 。
2、 流体在圆管内作湍流流动时, 其平均流速 u 与管中心的最大流速 umax 的关系为 ( A. u≈1.5umax C. u≈0.5umax B. u≈0.8umax D. u≈umax
填空题 1、流体在圆形直管中作层流流动,如果流量等不变,只是将管径增大一倍,则阻力损失为 原来的________。 2、某流体在圆形直管中作滞流流动时,其速度分布是________ 曲线,其管中心最大流速 为平均流速的________倍,摩擦系数λ与 Re 的关系为________。 3、流体在流动过程中,其入口阻力损失系数= 。
(10 分) 2、 将高位槽内料液向塔内加料。 高位槽和塔内的压力均为大气压。 要求料液在管内以 0.5m/s 的速度流动。设料液在管内压头损失为 1.2m(不包括出口压头损失) ,试求高位槽液面比塔 入口处的高 x 为多少米?(10 分) 3、在图示装置中,水管直径为φ57×3.5mm。当阀门开启时,压力表读数为 2.03×104Pa, 设总压头损失为 0.5m。若水槽液面距水管管中心线的垂直距离为 3m ,求水的流量。水密 度ρ=1000kg/m3。 (10 分) 4、在图示装置中,管路用水泵从低位槽送往高位槽,高位槽压力表读数为 0.5KPa(表压) , 两液面高度差为 14 m,管路直径为φ57×3.5mm,管路总阻力损失为 5
4、在稳定多层壁导热过程中,当总温差一定时,传热速率的大小取决 于 。
5、 换热器根据冷、 热流体热量交换的原理和接触方式可分为: ________、 ________、 ________。 6、在稳定多层壁导热过程中,哪层热阻大,哪层温差就 7、导热系数在数值上等于单位温度梯度下的热通量, 强化传热来看,应选用 的材料。 ,减少热阻的最有效 。 越大 ,导热性能越 ;从
化学测试题

化学测试题1. 某温度下将氯气通入氢氧化钾溶液里,反应后得到KCl、KClO、KClO3的混合溶液,经测定ClO-和ClO3-的浓度之比为11:1,则氯气和氢氧化钾溶液反应时,被还原的氯元素和被氧化的氯元素的物质的量之比为A、1:3B、4:3C、2:1D、3:12.取相同体积的KI、Na2S和FeBr2溶液分别通入足量的Cl2,当反应恰好完成时,消耗Cl2的体积相同(同温同压下),则KI、Na2S、FeBr2溶液的物质的量浓度之比为A.1︰1︰2 B.2︰1︰3 C.6︰3︰2 D.3︰2︰13.实验室为监测空气中汞蒸气的含量,通常悬挂有CuI的滤纸,根据滤纸是否变色或颜色发生变化的时间来判断空气中汞的含量,其反应为:4CuI+Hg=Cu2HgI4+2Cu。
以下有关说法正确的是A.上述反应的产物Cu2HgI4中,Hg的化合价为+2B.上述反应中CuI既是氧化剂,又是还原剂C.上述反应中Hg与Cu均发生氧化反应D.上述反应中生成 64g Cu时,转移的电子数为2×6.02×10234.氯酸是一种强酸,浓度超过40%时会发生分解反应可表示为:a HClO3=b O2↑+c Cl2↑+d HClO4+e H2O,用湿润的淀粉碘化钾试纸检验气体产物时,试纸先变蓝后褪色。
下列说法不正确...的是A.该反应既是分解反应,又是氧化还原反应B.变蓝的淀粉碘化钾试纸褪色可能发生的反应:5C12+I2+6H2O=12H++10Cl—+2IO3—C.若化学计量数a=8,b=3,则该反应转移电子数为20e—D.氯酸分解所得O2和Cl2的物质的量之比是确定不变的5. 已知常温下氯酸钾与浓盐酸反应放出氯气,现按下图进行卤素的性质实验。
玻璃管内装有分别滴有不同溶液的白色棉球,反应一段时间后,对图中指定部位颜色描述正确的是6.密度为0.910g/cm氨水,质量分数为25.0%,该氨水用等体积的水稀释后,所得溶液的质量分数为A.等于13.5% B.大于12.5% C.小于12.5% D.无法确定7.反应①是自海藻灰中提取碘的主要反应,反应②是自智利硝石中提取碘的主要反应:①2NaI+MnO2+3H2SO4 =2NaHSO4+MnSO4+2H2O+I2②2NaIO3+5NaHSO3 =2Na2SO4+3NaHSO4+H2O+I2已知NaIO3的氧化性与MnO2相近,下列有关说法正确的是A.I2 在反应①中是还原产物,在反应②中是氧化产物B.两个反应中生成等量的I2 时转移的电子数相等C.NaI和NaIO3 在一定条件下能反应生成I2D.NaIO3在化学反应中只能做氧化剂不能做还原剂8.已知KOCN中碳为+4价,在KOCN + KOH + Cl2→ CO2 + N2 + KCl + H2O 反应中,如果有6 mol Cl2完全反应,则被氧化的KOCN的物质的量是A.2 mol B.3 mol C.4 mol D.6 mol9. 将NaCl和NaBr的混和物mg溶于足量的水配成500mL的溶液A,再向其中通入足量的氯气,充分反应后蒸发至干,得干燥晶体(m-2)g,则A溶液中Na+、Br-、Cl-的物质的量浓度之比不可能为A.3︰2︰1 B.3︰1︰2 C.4︰3︰1 D.3︰1︰410. 已知氧化还原反应:2Cu(IO3)2+24KI+12H2SO4=2CuI↓+13I2+12K2SO4+12H2O则有关该反应的说法正确的是A.当1 mol Cu(IO3)2发生反应共转移的电子为10mol B.反应中KI被氧化C.I2是氧化产物CuI是还原产物D.当1 mol Cu(IO3)2发生反应被Cu2+氧化的I—为2 mol11. 在KIO3、KHSO3的酸性混合溶液中加入少量KI和淀粉,不停地搅拌,有下列反应发生:① IO3-+ 5I—+ 6H+→3I2 + 3H2O ② I2 + 2HSO3-+ H2O →2I-+ 2SO42-+ 4H+当反应进行到15min时,溶液突然变为蓝色,随之又很快消失。
2024年江苏省常州市中考化学试题(含答案解析)

常州市2024年初中学业水平考试化学试题注意事项:本试卷满分100分,考试时间100分钟。
可能用到的相对原子质量:Ar(H)=l Ar(Li)=7 Ar(C)=12 Ar(N)=14 Ar(O)=16 Ar(Na)=23Ar(S)=32 Ar(Cl)=35.5 Ar(Ca)=40一、选择题:共20题,每题2分,共40分。
每题只有一个选项符合题意。
1.下列变化属于化学变化的是A.酒精挥发B.冶炼钢铁C.品红扩散D.石油分馄2.下列物质属于纯净物的是A.海水B.食醋C.干冰D.碘酒3.历史上第一次明确提出空气是由氧气和氮气组成的科学家是A.拉瓦锡B.居里夫人诺贝尔 D.门捷列夫4.下列一般标识在矿泉水瓶上的标志是C.物品回收A.有害垃圾 B.D.当心火灾当心爆炸/ \5.将紫色石蕊试液滴入下列溶液能变蓝色的是A 纯碱溶液B.蔗糖水C.柠檬汁D.食盐水6.香肠中的下列成分中不能为人类提供能量的是A.脂肪B.糖类C.蛋白质D.无机盐7.锢在元素周期表中的部分信息如图所示,下列说法正确的是A.锢原子核外电子数为49B. 一个锢原子的质量为114.8gC.锢元素属于非金属元素D.锢原子中质子数等于中子数8.高层建筑建造时常使用铝合金材料。
下列说法正确的是A.铝合金材料属于复合材料B.铝土矿是主要含铝矿物之一C.铝合金的硬度小于单质铝D.铝材致密氧化膜要及时除去9.下列用高镒酸钾固体制取氧气的系列操作中正确的是A.取用药品C.收集氧气带火星 木条D.氧气验满10.下列关于化石燃料说法正确的是A.化石燃料都属于可再生能源B.煤完全燃烧时不会产生污染C.石油为原料能制造合成纤维D.天然气主要成分为一氧化碳11.科学家用淀粉和改性材料制成生物降解塑料,该塑料在自然界条件下最终能完全降解成CO 2. H2O 等物质。
下列说法不正确的是A.该技术可以减少“白色污染〃B.淀粉与碘单质作用呈现红色C.该塑料的降解参与“碳循环”D.生物降解塑料也需合理使用12. 《本草纲目》记载食肉桂能,面生光华” o 肉桂mc 9H 8o 2)^肉桂的主要有效成分,下列说法正确的是A.肉桂酸由碳、氢、氧三种原子构成B.肉桂酸中碳与氢元素质量比为9: 8C.肉桂酸中氧元素的质量分数为21.6%D. 一个肉桂酸分子中含有一个氧分子13. 氮肥为解决人类面临的粮食危机做出了重大贡献。
电化学试题

电化学练习题1判断正误1. 由于离子迁移数与离子的迁移速率成正比,因此,一种离子的迁移速率一定时,其迁移数也一定,凡是能够改变离子迁移速率的因素都能改变离子迁移数。
( )2. 摩尔电导率c m /κ=Λ,对于弱电解质溶液,式中的c 表示已经解离部分的浓度。
( )3. 在一定温度下稀释电解质溶液,摩尔电导率Λm 一定增大,而电导率κ 的值的变化方向则不一定。
( )4. 任何可溶性的强电解质溶液都可以作为盐桥使用。
( )5. 以两种不同浓度的电解质溶液间的相界面处由于离子迁移速率不同而产生的电位差称为液接电势,用盐桥可以完全消除液接电势。
( )6. 对于给定的电极反应,标准电极电势ϕ为常数,其数值不随温度而变。
( )7. 只要电极反应为可逆反应的电极就能作为参考电极。
( )8. 化学电池的电动势决定于电池内的氧化还原反应,因此,对应于一定的电池总反应必有确定的电动势数值。
( )9. 不论是原电池还是电解池,极化的结果都是使阳极电势升高,阴极电势降低。
( ) 10. 电解时在电极上首先发生反应的离子总是承担了大部分的电量迁移任务。
( )参考答案1. ( × )离子迁移数与离子的迁移速率成正比,但是一种离子的迁移速率一定时,其迁移数并不总是一定,这是因为离子的迁移数不但决定于离子的本性,而且与共存的离子有关。
能够改变离子迁移速率可能改变离子迁移数,但是不一定。
例如改变外加电压,可影响离子的运动速度,但是因为正、负离子处于相同的电场强度下,其迁移速率会成比例地改变,因此外压电压的大小一般不影响离子的迁移数。
2. ( × )摩尔电导率是指相距1m 的两个平行电极之间含有1mol 电解质所具有的电导。
此处的1mol 电解质可能全部解离,也可能只解离一部分。
需要把摩尔电导率和无限稀释的摩尔电导率区分开来。
3. (√)强酸、强碱溶液的电导率与其浓度的关系曲线(κ-c )上存在极大点。
当浓度较小时,随浓度增加,导电离子数目增多;因此电导率κ 的值增大。
表面与界面化学试卷(a)2008

Fig.1Figure 1 shows an adsorbed structure on an fcc surface. How might this adsorbate structure on the surface be described武汉理工大学教务处试题标准答案及评分标准用纸课程名称—表面与界面化学——(A 卷)1. chemisorption: a chemical bond, involving substantial rearrangement of electron density, is formed between the adsorbate and substrate.Physisorption : the only bonding is by weak Van der Waals - type forces. There is no significant redistribution of electron density in either the molecule or at the substrate surface.2. the surface energies determined are not equal. in air<under argon<and in a vacuum. When the mica is prepared in air, chemisorptions will occur on the mica surface and release heat. Under argon, there is only physisorption occur, the released energy is lower. In a vacuum, no adsorption occurs, the real surface energy is determined.3. The first raindrop sliding down the window glass, the contact angle of the water and glass is the advancing contact angle, which gives a large force to prevent the sliding of raindrop. The first raindrop leaves a water film on the glass. The later raindrop will show a spreading wetting on the window and give a quick sliding rate.4. (1) M=WRT/ A=(2) sodium dodecylsulfate is an ionic surfactant。
结构化学试题及答案

兰州化学化学化工学院结构化学试卷及参考答案2002级试卷A——————————————————————————————————————说明:1.试卷页号P.1-5,答题前请核对.[]3.Y(θ,φ)图A.即电子云角度分布图,反映电子云的角度部分随空间方位θ,φ的变化B. 即波函数角度分布图,反映原子轨道的角度部分随空间方位θ,φ的变化C.即原子轨道的界面图,代表原子轨道的形状和位相[]4.为了写出原子光谱项,必须首先区分电子组态是由等价电子还是非等价电子形成的。
试判断下列哪种组态是等价组态:A.2s12p1 B.1s12s1 C.2p2[]5.对于O2,O2-,O22-,何者具有最大的顺磁性?A.O2B.O2-C.O22-[]6.苯胺虽然不是平面型分子,但-NH2与苯环之间仍有一定程度的共轭。
据此判断A.苯胺的碱性比氨弱B.苯胺的碱性比氨强C.苯胺的碱性与氨相同[]7.利用以下哪一原理,可以判定CO、CN-的分子轨道与N2相似:A.轨道对称性守恒原理B.Franck-Condon原理C.等电子原理[]8.下列分子中,哪种分子有两个不成对电子?A.BB[]9.[]10.[]11.,它们[]12.[]13.A.D3B.D3h→D3→D3dC.C3h→C3→C3V[]14.S在室温下稳定存在的形式为正交硫,其中的分子是S8环,分子点群为A.C4vB.D4dC.D8h[]15.Cl原子基态的光谱项为2P,其能量最低的光谱支项为A.2P3/2B.2P1/2C.2P3/2或2P1/2,二者能量相同[]16.下列哪种物质最不可能是晶体A.金刚石B.琥珀C.食盐粉末[]17.晶系和晶体学点群各有多少种?A.7种晶系,32种晶体学点群B.14种晶系,32种晶体学点群C.7种晶系,14种晶体学点群[]18.下列哪一式是晶体结构的代数表示——平移群:A.T mnpB.r=xaC.Δ[]19.A.[]20.A.([]22.[]23.为了区分素格子与复格子,空间格子中的每个顶点、棱心、面心只分别算作A.1,1,1B.1/8,1/4,1/2C.1,1/2,1/4[]24.CuZn合金(即β黄铜)中两种金属原子的分数坐标分别为0,0,0和1/2,1/2,1/2。
视觉界面设计师试题含答案

视觉界面设计师试题含答案1、压力蒸汽灭菌的监测中哪一种监测不需要每天开展()。
A、B-D试验B、工艺监测C、生物监测D、化学监测答案:C2、关于过氧化氢等离子低温灭菌说法不正确的是()。
A、灭菌前物品应充分干燥B、灭菌物品应使用专用包装材料和容器C、灭菌物品和包装材料不应含有植物纤维材质D、灭菌腔壁温度为45℃-60℃答案:D3、清洗不合格的器械应返回去污区重新清洗或者()。
A、消毒B、监测C、去污处理D、预处理答案:C4、下列说法正确的是()。
A、回收工具每周清洗消毒一次,干燥备用B、回收工具每次使用后清洗消毒干燥备用C、耐湿耐热器械器具和物品应首选化学消毒灭菌方法D、可以在诊疗场所对污染的器械、工具和物品进行清点答案:B5、压力蒸汽灭菌用化学指示物()A、暴露于干热140摄氏度,30分钟下,应变色或变色不完全B、饱和蒸汽,121摄氏度完全变色时间不少于3分钟C、饱和蒸汽下,121摄氏度完全变色时间不超过10分钟D、饱和蒸汽下,134摄氏度完全变色时间不超过2分钟E、都正确答案:E6、微生物对消毒因子的敏感性从高到低的顺序是什么?A、亲脂病毒、细菌繁殖体、亲水病毒、真菌、细菌芽孢、朊毒B、亲脂病毒、细菌繁殖体、真菌、亲水病毒、朊毒C、亲脂病毒、细菌繁殖体、真菌、亲水病毒、朊毒、细菌芽孢D、细菌繁殖体、亲脂病毒、真菌、亲水病毒、细菌芽孢、朊毒E、亲脂病毒、细菌繁殖体、真菌、亲水病毒、朊毒、亲水病毒答案:B7、根据结构分类装载:需要拆卸后清洗的复杂器械,放置在()清洗篮筐中,利于器械配套组装的操作,避免器械装配时发生混乱;组合成套的手术器械量过多时,分开装载。
A、一个B、两个C、三个D、四个E、多个答案:A8、用下排气式压力蒸汽灭菌器的物品体积不得超过()A、30㎝×30㎝×20㎝B、30㎝×30㎝×50㎝C、30㎝×30㎝×25㎝D、30㎝×30㎝×30㎝答案:C9、压力仪表的压力范围()A、0—200kpaB、0—300kpaC、0—400kpaD、0—500kpaE、0—600kpa答案:C10、目前常用的压力蒸汽灭菌器为()。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
(3) ⎜⎛ ∂G (σ ) ⎟⎞
⎜ ⎝
∂As
⎟ ⎠T , p,nj
(6) ⎜⎛ ∂A(σ ) ⎟⎞
⎜ ⎝
∂As
⎟ ⎠ S ,U ,nj
二、按照 Gibbs 界面模型,界面相的热力学基本方程 dG (σ ) =?
恒温下,在一带有活塞的汽缸里,半径为 r 的纯物质微小液滴与其蒸气达到气液平衡。试按照 Gibbs
3. 在 热 力 学 上 , 通 常 用 模 型 的 方 法 将 界 面 层 处 理 为 ____________ 相 。 吉 布 斯 的 处 理 方 法 是 _________________________________________________________________________。按照吉布斯模 型 , 两 相 平 衡 系 统 的 体 积 V=_____________ , 物 质 的 量 n =___________ , 亥 氏 函 数 A=______________ 。界面过剩量 ni(σ ) = _____________________ 。
《物理化学》下册练习-5
第 15 章 界面化学
基本概念
1. 两相的界面为什么存在收缩张力______________________________________________。表面张力的定 义是______________________________ 。
2. 表面张力随温度的升高而_________ 。当液体的温度升高到临界温度时,表面张力等于__________ 。 这是因为__________________________________ 。
物理吸附
化学吸附
吸附力
吸附热
选择性
吸附分子层
吸附速度
吸附可逆性
19.多相催化反应的基本步骤是
。
20.气体 A 在某催化剂表面发生分解反应 A (g) → 2B (g) 。若产物 B 在催化剂表面与 A 竞争吸附,则 A 和
B 的兰缪尔等温方程分别为:θ A =
,θ B =
。
《物理化学》下册练习-7
的单位界面吸附量
Γ
(1) 2
=
3×10-10
molxcm-2。已知
25℃时纯水的表面张力为
72.0×10-3 Nxm-1
,试计
算该溶液的表面张力。
6. 存在弯曲界面的多相系统的平衡条件为:热平衡_____________ ;力平衡____________ ;相平衡 ________________ 。
7. 试写出 Laplace 方程:___________________ 。对于半径为 r 的球形液滴,上式可写成
______________ 。对于半径为 r 的液体中的气泡,上式可写成_________________ 。
界面模型,写出界面相的热力学基本方程 dA(σ ) = ?
三、下图表示四根毛细管插入某种液体后所引起的液面升高或降低,试指出何者是正确的?
四、在一个锥形容器中,放入一滴液体,若液面微微呈凸形,如下图所示 。试画出接触角,并判断其是 润湿还是不润湿。(θ < 90o )
五、若将一表面积为 AS 的固体在某液体中浸湿。试表示该过程的吉氏函数变化,并用杨氏方程证明,该 固体一定能被该液体所润湿。
六、已知水能润湿玻璃。今将三根半径不同的玻璃毛细管放在空气中,试简要描述,当空气的湿度逐渐增 大时,三根毛细管中所发生的变化。
七、从热力学角度分析,吸附应是吸热的还是放热的?为什么?请用热力学关系式 ΔG =ΔH-TΔS 分析说明之。
八、有一表面活性剂浓度很稀的水溶液,在 25℃时用快速移动的刀片刮取该溶液的表面,测得表面活性剂
计算题 一、试指出下列哪些偏导数是表面张力?
(1) ⎜⎛ ∂A(σ ) ⎟⎞
⎜ ⎝
∂As
⎟ ⎠T, p,nj
(2) ⎜⎛ ∂H (σ ) ⎟⎞
⎜ ⎝
∂A s
⎟ ⎠S, p,nj
(4) ⎜⎛ ∂H (σ ) ⎟⎞
⎜ ⎝
∂As
⎟ ⎠T , p,nj
(5) ⎜⎛ ∂U (σ ) ⎟⎞
⎜ ⎝
∂As
⎟ ⎠T , p,nj
4. 若有一个二元系,两相达到平衡。试用 Gibbs 界面模型在下图中标出 n2( σ ) = ?是正吸附还是负吸附?
5. 试写出界面相的一个热力学基本方程, dG (σ ) = _______________________________。根据这个基本方 程,可得表面张力的热力学表示式σ = _________________________。
10.试写出 Kelvin 方程____________________ 。试指出微小液滴的饱和蒸汽压为什
么要比平面液体的大
。
11.试分析液体过热的原因,并指出为避免过热而采取的一些方法
______________________________________________________________________ ___________________________________________________________ 。
8. 如图所示,在一玻璃管两端分别有一个肥皂泡。今打开考克使它们接通, 其结果是大泡变大、小泡变小,还是大泡变小、小泡变大?二者最终能 否达到平衡状态?
9. 将玻璃毛细管插入水中(如右图),经验告诉我们,毛细管中的液面升高 了,这是因为
______________________________bs 吸附等温式_______________________________________________ 。 何谓正吸附?_____________ ,哪些物质加入水中呈正吸附______________________ 。 何谓负吸附?_____________ ,哪些物质加入水中呈负吸附_____________________ 。
15.如何判断液体在固体表面是否润湿_________________________ ,试写出杨氏方程
__________________________ 。对于下列三种情况选填符号>、=、<,指出何者铺展、何者润湿?
ϕ ______ 0
ϕ ______ 0 cosθ ____ 0
ϕ ______ 0 cosθ ____ 0
《物理化学》下册练习-6
13.有一表面活性剂加入水中,在浓度很低时,表面
Γ
(1) 2
张力与浓度间服从公式
c2
=
σ∗ −σ b
,在浓度较高
时,服从公式 c2 =Ae (σ∗-σ)/B 试示意画出单位界
c2
面吸附量
Γ
(1)
2
随表面活性剂浓度
c2
的变化曲线。式中σ∗为纯水的表面张力,b、A
和
B
为常数。
14.如何判断一液滴在固体表面上是否铺展_____________________ ,铺展系数的表示式是 ϕ = __________________________ ,它的物理意义是_____________________ 。
16. 固体颗粒在液体中呈如下两种状态,试分别画出它们的接触角,并指出何者润湿,何者不润湿?
液体在毛细管中呈如下两种状态,试分别画出它们的接触角,并指出何者润湿,何者不润湿?
17.何谓临界胶束浓度?
,当表面活性物
质的浓度超过临界胶束浓度后,溶液内将生成不同形式的胶束,它们
是
。
18.试在下表所列指标中填写物理吸附与化学吸附的特征或区别:
