有机溶剂极性表
有机溶剂极性表

有机溶剂极性表极性与非极性是针对分子说的。
首先化学共价键分为极性键与非极性键。
非极性键就是共用电子对没有偏移,出现在单质中比如O2;极性键就是共用电子对有偏移比如HCl。
而当偏移的非常厉害之后,看上去一边完全失电子另一边得到了电子,就会变成离子键了,如NaCl再说极性分子与与非极性分子。
由于极性键的出现,所以就使某些分子出现了电极性,但是并不是说所有有极性键的分子都是极性分子。
比如CH4,虽然含有4个极性的C-H键,但是因为其空间上成对称的正四面体结构,所以键的极性相消,整个分子没有极性对与H2O,虽然与CO2有相同类型的分子式,也同样有极性共价键,但二者分子的极性却不同。
CO2是空间对称的直线型,所以分子是非极性分子,H2O是折线型,不对称,所以是极性分子,作为溶剂称为极性溶剂非极性溶剂由非极性分子组成,是指分子中各原子的化学键的合力为零,如CCl4分子为正四面体,四个C-Cl键的合力为零,CCl4分子无极性,CCl4就是非极性溶剂非极性溶剂"脂肪油(fattyoils) "液状石蜡(1iquidparaffin) "醋酸乙酯(ethyloleate) "肉豆蔻酸异丙酯(isopropylmyristate)非极性溶剂是由非性分子溶液组成的溶剂,非极性分子多由共价键构成,无或电子活性很小.最简单准确的说就是偶极矩为零的溶剂。
知道什么是偶极矩吗?非极性溶剂是由非性分子溶液组成的溶剂,非极性分子多由共价键构成,无或电子活性很小。
偶极矩小的溶剂溶剂英文名称solvent又称溶媒。
能溶解气体、固体、液体而成为均匀混合物的一种液体。
习惯上把气体和固体叫溶质,液体叫溶剂。
对于两种液体所组成的溶液,通常把含量较多的组分叫溶剂,少者叫溶质。
分为无机溶剂和有机溶剂两大类。
水是应用最广泛的无机溶剂,酒精、汽油、氯仿及丙酮等是常用的有机溶剂。
溶剂是一种可以溶化固体,液体或气体溶质的液体,继而成为溶液.在日常生活中最普遍的溶剂是水. 而所谓有机溶剂即是包含碳原子的有机化合物. 溶剂通常拥有比较低的沸点和容易挥发.或是可以由蒸馏来去除, 从而留下被溶物. 因此,溶剂不可以对溶质产生化学反应 . - 它们必须为惰性. 溶剂可从混合物萃取可溶化合物, 最普遍的例子是以热水冲泡咖啡或茶溶剂通常是透明,无色的液体,他们大多都有独特的气味.溶液的浓度取决于溶解在溶剂内的物质的多少.溶解度则是溶剂在特定温度下,可以溶解最多多少物质.有机溶剂主要用于干洗(例如四氯乙烯), 作涂料稀释剂(例如甲苯, 松节油), 作洗甲水或去除胶水(例如丙酮, 醋酸甲酯, 醋酸乙酯), 除锈(例如己烷), 作洗洁精(柠檬精), 用于香水(酒精)跟用于化学合成(Chemical synthesis).溶剂和溶质大致上可分为极性基(亲水的) 和非极性基(疏水的). 极性可以透过量度物质的介电常数或偶极距得知。
常见的溶剂极性表有机溶剂表
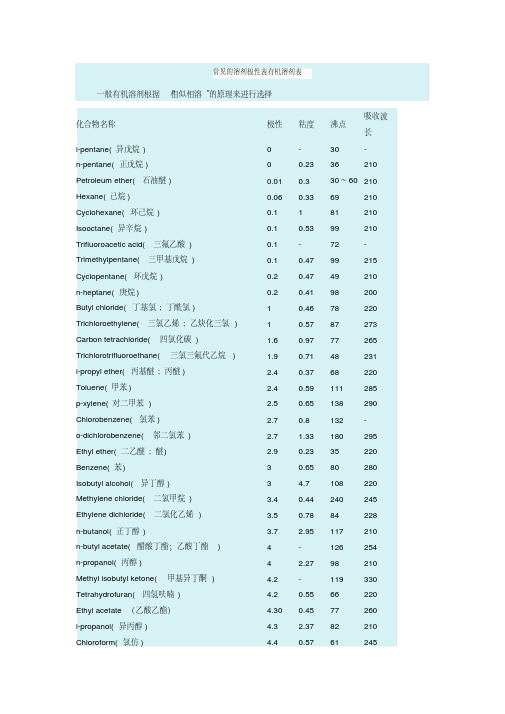
常见的溶剂极性表有机溶剂表一般有机溶剂根据“相似相溶”的原理来进行选择化合物名称极性粘度沸点吸收波长i-pentane(异戊烷) 0 - 30 -n-pentane(正戊烷) 0 0.23 36 210 Petroleum ether(石油醚) 0.01 0.3 30~60 210 Hexane(己烷) 0.06 0.33 69 210 Cyclohexane(环己烷) 0.1 1 81 210 Isooctane(异辛烷) 0.1 0.53 99 210 Trifluoroacetic acid(三氟乙酸) 0.1 - 72 - Trimethylpentane(三甲基戊烷) 0.1 0.47 99 215 Cyclopentane(环戊烷) 0.2 0.47 49 210 n-heptane(庚烷) 0.2 0.41 98 200 Butyl chloride(丁基氯; 丁酰氯) 1 0.46 78 220 Trichloroethylene(三氯乙烯; 乙炔化三氯) 1 0.57 87 273 Carbon tetrachloride(四氯化碳) 1.6 0.97 77 265 Trichlorotrifluoroethane(三氯三氟代乙烷) 1.9 0.71 48 231 i-propyl ether(丙基醚; 丙醚) 2.4 0.37 68 220 Toluene(甲苯) 2.4 0.59 111 285 p-xylene(对二甲苯) 2.5 0.65 138 290 Chlorobenzene(氯苯) 2.7 0.8 132 -o-dichlorobenzene(邻二氯苯) 2.7 1.33 180 295 Ethyl ether(二乙醚; 醚) 2.9 0.23 35 220 Benzene(苯) 3 0.65 80 280 Isobutyl alcohol(异丁醇) 3 4.7 108 220 Methylene chloride(二氯甲烷) 3.4 0.44 240 245 Ethylene dichloride(二氯化乙烯) 3.5 0.78 84 228 n-butanol(正丁醇) 3.7 2.95 117 210 n-butyl acetate(醋酸丁酯;乙酸丁酯) 4 - 126 254 n-propanol(丙醇) 4 2.27 98 210 Methyl isobutyl ketone(甲基异丁酮) 4.2 - 119 330 Tetrahydrofuran(四氢呋喃) 4.2 0.55 66 220 Ethyl acetate(乙酸乙酯) 4.30 0.45 77 260 i-propanol(异丙醇) 4.3 2.37 82 210 Chloroform(氯仿) 4.4 0.57 61 245。
溶剂极性列表

有机溶剂极性表化合物名称极性粘度沸点吸收波长i-pentane(异戊烷) 0 - 30 -n-pentane(正戊烷) 0 0.23 36 210 Petroleum ether(石油醚) 0.01 0.3 30~60 210 Hexane(己烷) 0.06 0.33 69 210 Cyclohexane(环己烷) 0.1 1 81 210 Isooctane(异辛烷) 0.1 0.53 99 210 Trifluoroacetic acid(三氟乙酸) 0.1 - 72 - Trimethylpentane(三甲基戊烷) 0.1 0.47 99 215 Cyclopentane(环戊烷) 0.2 0.47 49 210n-heptane(庚烷) 0.2 0.41 98 200 Butyl chloride(丁基氯; 丁酰氯) 1 0.46 78 220 Trichloroethylene(三氯乙烯; 乙炔化三氯) 1 0.57 87 273 Carbon tetrachloride(四氯化碳) 1.6 0.97 77 265 Trichlorotrifluoroethane(三氯三氟代乙烷) 1.9 0.71 48 231i-propyl ether(丙基醚; 丙醚) 2.4 0.37 68 220 Toluene(甲苯) 2.4 0.59 111 285p-xylene(对二甲苯) 2.5 0.65 138 290 Chlorobenzene(氯苯) 2.7 0.8 132 -o-dichlorobenzene(邻二氯苯) 2.7 1.33 180 295 Ethyl ether(二乙醚; 醚) 2.9 0.23 35 220 Benzene(苯) 3 0.65 80 280 Isobutyl alcohol(异丁醇) 3 4.7 108 220 Methylene chloride(二氯甲烷) 3.4 0.44 240 245 Ethylene dichloride(二氯化乙烯) 3.5 0.78 84 228n-butanol(正丁醇) 3.7 2.95 117 210n-butyl acetate(醋酸丁酯;乙酸丁酯) 4 - 126 254n-propanol(丙醇) 4 2.27 98 210 Methyl isobutyl ketone(甲基异丁酮) 4.2 - 119 330 Tetrahydrofuran(四氢呋喃) 4.2 0.55 66 220 Ethanol (乙醇) 4.3 1.2 79 210 Ethyl acetate(乙酸乙酯) 4.30 0.45 77 260i-propanol(异丙醇) 4.3 2.37 82 210 Chloroform(氯仿) 4.4 0.57 61 245 Methyl ethyl ketone(甲基乙基酮) 4.5 0.43 80 330Dioxane(二恶烷;二氧六环; 二氧杂环己烷) 4.8 1.54 102 220Pyridine(吡啶) 5.3 0.97 115 305Acetone(丙酮) 5.4 0.32 57 330 Nitromethane(硝基甲烷) 6 0.67 101 330Acetic acid(乙酸) 6.2 1.28 118 230 Acetonitrile(乙腈) 6.2 0.37 82 210Aniline(苯胺) 6.3 4.4 184 -Dimethyl formamide(二甲基甲酰胺) 6.4 0.92 153 270Methanol(甲醇) 6.6 0.6 65 210Ethylene glycol(乙二醇) 6.9 19.9 197 210Dimethyl sulfoxide(二甲亚砜DMSO) 7.2 2.24 189 268Water(水)10.2 1 100 268强极性溶剂:甲醇〉乙醇〉异丙醇中等极性溶剂:乙氰〉乙酸乙酯〉氯仿〉二氯甲烷〉乙醚〉甲苯非极性溶剂:环己烷,石油醚,己烷,戊烷常用混合溶剂:乙酸乙酯/己烷:常用浓度0-30%。
常用有机溶剂极性表
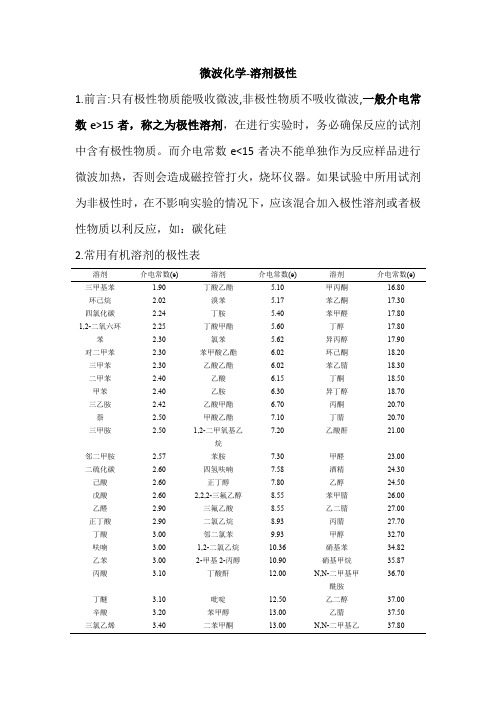
微波化学-溶剂极性1.前言:只有极性物质能吸收微波,非极性物质不吸收微波,一般介电常数e>15者,称之为极性溶剂,在进行实验时,务必确保反应的试剂中含有极性物质。
而介电常数e<15者决不能单独作为反应样品进行微波加热,否则会造成磁控管打火,烧坏仪器。
如果试验中所用试剂为非极性时,在不影响实验的情况下,应该混合加入极性溶剂或者极性物质以利反应,如:碳化硅2.常用有机溶剂的极性表溶剂介电常数(e) 溶剂介电常数(e) 溶剂介电常数(e) 三甲基苯 1.90 丁酸乙酯 5.10 甲丙酮16.80 环己烷 2.02 溴苯 5.17 苯乙酮17.30 四氯化碳 2.24 丁胺 5.40 苯甲醛17.801,2-二氧六环 2.25 丁酸甲酯 5.60 丁醇17.80 苯 2.30 氯苯 5.62 异丙醇17.90 对二甲苯 2.30 苯甲酸乙酯 6.02 环己酮18.20 三甲苯 2.30 乙酸乙酯 6.02 苯乙腈18.30 二甲苯 2.40 乙酸 6.15 丁酮18.50 甲苯 2.40 乙胺 6.30 异丁醇18.70 三乙胺 2.42 乙酸甲酯 6.70 丙酮20.70 萘 2.50 甲酸乙酯7.10 丁腈20.707.20 乙酸酐21.00三甲胺 2.50 1,2-二甲氧基乙烷邻二甲胺 2.57 苯胺7.30 甲醛23.00 二硫化碳 2.60 四氢呋喃7.58 酒精24.30 己酸 2.60 正丁醇7.80 乙醇24.50 戊酸 2.60 2,2,2-三氟乙醇8.55 苯甲腈26.00 乙醛 2.90 三氟乙酸8.55 乙二腈27.00 正丁酸 2.90 二氯乙烷8.93 丙腈27.70 丁酸 3.00 邻二氯苯9.93 甲醇32.70 呋喃 3.00 1,2-二氯乙烷10.36 硝基苯34.82 乙苯 3.00 2-甲基2-丙醇10.90 硝基甲烷35.8736.70丙酸 3.10 丁酸酐12.00 N,N-二甲基甲酰胺丁醚 3.10 吡啶12.50 乙二醇37.00 辛酸 3.20 苯甲醇13.00 乙腈37.50 三氯乙烯 3.40 二苯甲酮13.00 N,N-二甲基乙37.80酰胺脲 3.50 丁醛13.40 乙酰胺41.00 二乙胺 3.60 戊酮13.90 二甲基亚砜46.70 苯甲醚 4.33 环氧乙烷14.00 丙二睛47.00 乙醚 4.33 环己醇15.00 甲酸58.00 苯乙醚 4.50 戊醇15.80 水80.40 氯仿 4.81 乙二胺16.00 甲酰胺111.00。
有机试剂极性一览表

有机试剂极性大小下面这份溶剂极性表列出了常用有机溶剂极性顺序,并有常见溶剂的粘度、沸点、吸收波长等物理参数,在进行薄层色谱柱(TLC)洗脱的时候时很有帮助。
可能有不准确的,希望在留言处给予更正。
化合物名称极性粘度沸点吸收波长i-pentane(异戊烷)0-30-n-pentane(正戊烷)036210 Petroleum ether(石油醚)30~60210 Hexane(己烷)69210 Cyclohexane(环己烷)181210 Isooctane(异辛烷)99210 Trifluoroacetic acid(三氟乙酸)-72-Trimethylpentane(三甲基戊烷)99215 Cyclopentane(环戊烷)49210 n-heptane(庚烷)98200 Butyl chloride(丁基氯; 丁酰氯)178220 Trichloroethylene(三氯乙烯; 乙炔化三氯)187273 Carbon tetrachloride(四氯化碳)77265 Trichlorotrifluoroethane(三氯三氟代乙烷)48231 i-propyl ether(丙基醚; 丙醚)68220 Toluene(甲苯)111285 p-xylene(对二甲苯)138290 Chlorobenzene(氯苯)132-o-dichlorobenzene(邻二氯苯)180295 Ethyl ether(二乙醚; 醚)35220 Benzene(苯)380280 Isobutyl alcohol(异丁醇)3108220 Methylene chloride(二氯甲烷)240245 Ethylene dichloride(二氯化乙烯)84228 n-butanol(正丁醇)117210 n-butyl acetate(醋酸丁酯;乙酸丁酯)4-126254 n-propanol(丙醇)498210 Methyl isobutyl ketone(甲基异丁酮)-119330 Tetrahydrofuran(四氢呋喃)66220 Ethyl acetate(乙酸乙酯)77260 i-propanol(异丙醇)82210 Chloroform(氯仿)61245Methyl ethyl ketone(甲基乙基酮)80330 Dioxane(二恶烷; 二氧六环; 二氧杂环己烷)????102220 Pyridine(吡啶)115305 Acetone(丙酮)57330 Nitromethane(硝基甲烷)??6101330 Acetic acid(乙酸)??118230 Acetonitrile(乙腈)??82210 Aniline(苯胺)184-Dimethyl formamide(二甲基甲酰胺)153270 Methanol(甲醇)??65210 Ethylene glycol(乙二醇 )??197210 Dimethyl sulfoxide(二甲亚砜 DMSO)189268 Water(水)1100268下图是混合有机溶剂极性顺序(由小到大,括号内表示的是混合比例)一:溶剂极性参数表,方便以下比较展开剂。
常见有机溶剂极性表

常见有机溶剂极性表 Prepared on 22 November 2020有机溶剂是能溶解一些不溶于水的物质的一类有机化合物,其特点是在常温常压下呈液态,具有较大的挥发性,在溶解过程中,溶质与溶剂的性质均无改变。
有机溶剂的种类较多,按其化学结构可分为10大类:①芳香烃类:苯、甲苯、二甲苯等;②脂肪烃类:戊烷、己烷、辛烷等;③脂环烃类:环己烷、环己酮、甲苯环己酮等;④卤化烃类:氯苯、二氯苯、二氯甲烷等;⑤醇类:甲醇、乙醇、异丙醇等;⑥醚类:乙醚、环氧丙烷等;⑦酯类:醋酸甲酯、醋酸乙酯、醋酸丙酯等;⑧酮类:丙酮、甲基丁酮、甲基异丁酮等;⑨二醇衍生物:乙二醇单甲醚、乙二醇单乙醚、乙二醇单丁醚等;⑩其他:乙腈、吡啶、苯酚等。
有机溶剂具有脂溶性,因此除经呼吸道和消化道进入机体内外,尚可经完整的皮肤迅速吸收,有机溶剂吸收入人体后,将作用于富含脂类物质的神经、血液系统,以及肝肾等实质脏器,同时对皮肤和粘膜也有一定的刺激性。
不同有机溶剂其作用的主要靶器官和作用的强弱也不同,这决定于每一种有机溶剂的化学结构、溶解度、接触浓度和时间,以及机体的敏感性。
常用溶剂的极性顺序:水(极性最大)>甲酰胺>乙腈>甲醇>乙醇>丙醇>丙酮>二氧六环>四氢呋喃>甲乙酮>正丁醇>醋酸乙酯>乙醚>异丙醚>二氯甲烷>氯仿>溴乙烷>苯>氯丙烷>甲苯>四氯化碳>二硫化碳>环己烷>己烷>庚烷>煤油(极性最小)有机溶剂的极性根据官能团和对称性可初步判断,具体的需参照极性参数,如下表示有机溶剂的极性,关系到其物理化学性质、如介电常数、偶极矩或折射率。
这种表示方法把所有的溶剂看作是连续作用的介质,而不是看作由各个分子组成的非连续统一体,并且未考虑到溶剂和溶质之间的特殊的相互作用。
有机试剂极性一览表

有机试剂极性大小下面这份溶剂极性表列出了常用有机溶剂极性顺序,并有常见溶剂的粘度、沸点、吸收波长等物理参数,在进行薄层色谱柱(TLC)洗脱的时候时很有帮助。
可能有不准确的,希望在留言处给予更正。
下图是混合有机溶剂极性顺序(由小到大,括号内表示的是混合比例)一:溶剂极性参数表,方便以下比较展开剂。
环已烷 :-0.2、石油醚(Ⅰ类,30~60℃)、石油醚(Ⅱ类,60~90℃)、正已烷:0.0、甲苯:2.4、二甲苯:2.5、苯:2.7、二氯甲烷:3.1、异丙醇:3.9、正丁醇:3.9、四氢呋喃:4.0、氯仿:4.1、乙醇:4.3、乙酸乙酯:4.4、甲醇:5.1、丙酮:5.1、乙腈:5.8、乙酸:6.0、水:10.2 数值越大,极性越大二:常用溶剂的沸点、溶解性和毒性溶剂名称沸点(101.3kPa)溶解性毒性液氨-33.35℃特殊溶解性:能溶解碱金属和碱土金属剧毒性、腐蚀性液态二氧化硫-10.08 溶解胺、醚、醇苯酚、有机酸、芳香烃、溴、二硫化碳,多数饱和烃不溶剧毒甲胺-6.3 是多数有机物和无机物的优良溶剂,液态甲胺与水、醚、苯、丙酮、低级醇混溶,其盐酸盐易溶于水,不溶于醇、醚、酮、氯仿、乙酸乙酯中等毒性,易燃二甲胺7.4 是有机物和无机物的优良溶剂,溶于水、低级醇、醚、低极性溶剂强烈刺激性石油醚不溶于水,与丙酮、乙醚、乙酸乙酯、苯、氯仿及甲醇以上高级醇混溶与低级烷相似乙醚34.6 微溶于水,易溶与盐酸.与醇、醚、石油醚、苯、氯仿等多数有机溶剂混溶麻醉性戊烷36.1 与乙醇、乙醚等多数有机溶剂混溶低毒性二氯甲烷39.75 与醇、醚、氯仿、苯、二硫化碳等有机溶剂混溶低毒,麻醉性强二硫化碳46.23 微溶与水,与多种有机溶剂混溶麻醉性,强刺激性溶剂石油脑与乙醇、丙酮、戊醇混溶较其他石油系溶剂大丙酮56.12 与水、醇、醚、烃混溶低毒,类乙醇,但较大1,1-二氯乙烷57.28 与醇、醚等大多数有机溶剂混溶低毒、局部刺激性氯仿61.15 与乙醇、乙醚、石油醚、卤代烃、四氯化碳、二硫化碳等混溶中等毒性,强麻醉性甲醇64.5 与水、乙醚、醇、酯、卤代烃、苯、酮混溶中等毒性,麻醉性,四氢呋喃66 优良溶剂,与水混溶,很好的溶解乙醇、乙醚、脂肪烃、芳香烃、氯化烃吸入微毒,经口低毒己烷68.7 甲醇部分溶解,比乙醇高的醇、醚丙酮、氯仿混溶低毒。
常见有机溶剂极性表

有机溶剂是能溶解一些不溶于水的物质的一类有机化合物,其特点是在常温常压下呈液态,具有较大的挥发性,在溶解过程中,溶质与溶剂的性质均无改变。
有机溶剂的种类较多,按其化学结构可分为10大类:①芳香烃类:苯、甲苯、二甲苯等;②脂肪烃类:戊烷、己烷、辛烷等;③脂环烃类:环己烷、环己酮、甲苯环己酮等;④卤化烃类:氯苯、二氯苯、二氯甲烷等;⑤醇类:甲醇、乙醇、异丙醇等;⑥醚类:乙醚、环氧丙烷等;⑦酯类:醋酸甲酯、醋酸乙酯、醋酸丙酯等;⑧酮类:丙酮、甲基丁酮、甲基异丁酮等;⑨二醇衍生物:乙二醇单甲醚、乙二醇单乙醚、乙二醇单丁醚等;⑩其他:乙腈、吡啶、苯酚等。
有机溶剂具有脂溶性,因此除经呼吸道和消化道进入机体内外,尚可经完整的皮肤迅速吸收,有机溶剂吸收入人体后,将作用于富含脂类物质的神经、血液系统,以及肝肾等实质脏器,同时对皮肤和粘膜也有一定的刺激性。
不同有机溶剂其作用的主要靶器官和作用的强弱也不同,这决定于每一种有机溶剂的化学结构、溶解度、接触浓度和时间,以及机体的敏感性。
常用溶剂的极性顺序: 水(极性最大) > 甲酰胺 > 乙腈 > 甲醇 >乙醇 > 丙醇 > 丙酮 > 二氧六环 > 四氢呋喃 > 甲乙酮 > 正丁醇 > 醋酸乙酯 > 乙醚 > 异丙醚 > 二氯甲烷 > 氯仿 > 溴乙烷 > 苯 > 氯丙烷 > 甲苯 > 四氯化碳 > 二硫化碳 > 环己烷 > 己烷 > 庚烷 > 煤油(极性最小)有机溶剂的极性根据官能团和对称性可初步判断,具体的需参照极性参数,如下表示有机溶剂的极性,关系到其物理化学性质、如介电常数、偶极矩或折射率。
这种表示方法把所有的溶剂看作是连续作用的介质,而不是看作由各个分子组成的非连续统一体,并且未考虑到溶剂和溶质之间的特殊的相互作用。
常用溶剂极性顺序表

常用有机溶剂的极性排列顺序石油醚V汽油V庚烷V己烷V二硫化碳V二甲苯V甲苯V氯丙烷V苯V溴乙烷V溴化苯V二氯乙烷V三氯甲烷V异丙醚V硝基甲烷V乙酸丁酯V乙醚V乙酸乙酯V正戊烷V正丁醇V苯酚V 甲乙醇V叔丁醇V四氢呋喃V二氧六环V丙酮V乙醇V乙腈V甲醇V氮氮二甲基甲酰胺V水常用有机溶剂极性表化合物名称极性粘度沸点吸收波长i-pentane(异戊烷)0 - 30n-pentane(正戊烷)0 0.23 36 210 Petroleum ether(石油醚)0.01 0.3 30〜6 0 210 Hexa ne(己烷)0.06 0.33 69 210 Cyclohexane(环己烷)0.1 1 81 210 Isooctane(异辛烷)0.1 0.53 99 210 Trifluoroacetic acid(三氟乙酸)0.1 - 72 - Trimethylpentane(三甲基戊烷)0.1 0.47 99 215 Cyclopentane(环戊烷)0.2 0.47 49 210n-heptane(庚烷)0.2 0.41 98 200 Butyl chloride(丁基氯 ; 丁酰氯) 1 0.46 78 220 Trichloroethylene(三氯乙烯; 乙炔化三氯) 1 0.57 87 273 Carbon tetrachloride(四氯化碳) 1.6 0.97 77 265 Trichlorotrifluoroethane(三氯三氟代乙烷) 1.9 0.71 48 231i-propyl ether(丙基醚 ; 丙醚) 2.4 0.37 68 220 Toluene(甲苯) 2.4 0.59 111 285p-xylene(对二甲苯) 2.5 0.65 138 290 Chlorobenzene(氯苯) 2.7 0.8 132 -o-dichlorobenzene(邻二氯苯) 2.7 1.33 180 295 Ethyl ether(二乙醚; 醚) 2.9 0.23 35 220 Benzene(苯) 3 0.65 80 280 Isobutyl alcohol(异丁醇) 3 4.7 108 220 Methylene chloride(二氯甲烷) 3.4 0.44 240 245 Ethylene dichloride(二氯化乙烯) 3.5 0.78 84 228n-butanol(正丁醇) 3.7 2.95 117 210n-butyl acetate(醋酸丁酯;乙酸丁酯) 4 - 126 254n-propanol(丙醇) 4 2.27 98 210 Methyl isobutyl ketone(甲基异丁酮) 4.2 - 119 330 Tetrahydrofuran(四氢呋喃) 4.2 0.55 66 220Ethyl acetate (乙酸乙酯) 4.30 0.45 77 260 i-propanol(异丙醇) 4.3 2.37 82 210 Chloroform(氯仿) 4.4 0.57 61 245 Methyl ethyl ketone(甲基乙基酮) 4.5 0.43 80 330Dioxane(二恶烷; 二氧六环 ; 二氧杂环己烷) 4.8 1.54 102 220 Pyridine(吡啶) 5.3 0.97 115 305 Acetone(丙酮) 5.4 0.32 57 330 Nitromethane(硝基甲烷) 6 0.67 101 330 Acetic acid(乙酸) 6.2 1.28 118 230 Acetonitrile(乙腈) 6.2 0.37 82 210 Aniline(苯胺) 6.3 4.4 184 - Dimethyl formamide(二甲基甲酰胺) 6.4 0.92 153 270 Methanol(甲醇) 6.6 0.6 65 210 Ethylene glycol(乙二醇) 6.9 19.9 197 210 Dimethyl sulfoxide(二甲亚砜 DMSO)7.2 2.24 189 268 Water (水)10.2 1 100 268柱子的极性取决于固定相的极性我们常用柱子的极性如下 :一、非极性1、100%Dimethyl polysiloxane ,100%聚二甲基硅氧烷,商品名: AC1,OV-101,OV-1,DB-1,SE-30,HP-1,RTX-1,BP-1二、弱极性2、5%Phenyl dimethyl polysiloxane, 5%二苯基 (95%)二甲基聚硅氧烷,商品名: AC5,SE-52,3、5% Phenyl 1%vinyl dimethyl polysiloxane ,5%二苯基 1%乙烯基 (94%)二甲基聚硅氧烷,商品名: OV-5,DB-5,SE-54,HP-5,RTX-5,BP-5注:2、3 常无严格区分,通常混称。
常见有机溶剂极性表

有机溶剂是能溶解一些不溶于水的物质的一类有机化合物,其特点是在常温常压下呈液态,具有较大的挥发性,在溶解过程中,溶质与溶剂的性质均无改变。
有机溶剂的种类较多,按其化学结构可分为10大类:①芳香烃类:苯、甲苯、二甲苯等;②脂肪烃类:戊烷、己烷、辛烷等;③脂环烃类:环己烷、环己酮、甲苯环己酮等;④卤化烃类:氯苯、二氯苯、二氯甲烷等;⑤醇类:甲醇、乙醇、异丙醇等;⑥醚类:乙醚、环氧丙烷等;⑦酯类:醋酸甲酯、醋酸乙酯、醋酸丙酯等;⑧酮类:丙酮、甲基丁酮、甲基异丁酮等;⑨二醇衍生物:乙二醇单甲醚、乙二醇单乙醚、乙二醇单丁醚等;⑩其他:乙腈、吡啶、苯酚等。
有机溶剂具有脂溶性,因此除经呼吸道和消化道进入机体内外,尚可经完整的皮肤迅速吸收,有机溶剂吸收入人体后,将作用于富含脂类物质的神经、血液系统,以及肝肾等实质脏器,同时对皮肤和粘膜也有一定的刺激性。
不同有机溶剂其作用的主要靶器官和作用的强弱也不同,这决定于每一种有机溶剂的化学结构、溶解度、接触浓度和时间,以及机体的敏感性。
常用溶剂的极性顺序: 水(极性最大) > 甲酰胺> 乙腈> 甲醇> 乙醇> 丙醇> 丙酮>二氧六环> 四氢呋喃> 甲乙酮> 正丁醇> 醋酸乙酯> 乙醚> 异丙醚> 二氯甲烷> 氯仿> 溴乙烷> 苯> 氯丙烷> 甲苯> 四氯化碳> 二硫化碳> 环己烷> 己烷> 庚烷> 煤油(极性最小)有机溶剂的极性根据官能团和对称性可初步判断,具体的需参照极性参数,如下表示有机溶剂的极性,关系到其物理化学性质、如介电常数、偶极矩或折射率。
这种表示方法把所有的溶剂看作是连续作用的介质,而不是看作由各个分子组成的非连续统一体,并且未考虑到溶剂和溶质之间的特殊的相互作用。
常见有机溶剂极性表

有机溶剂是能溶解一些没有溶于火的物量的一类有机化合物,其特性是正在常温常压下呈液态,具备较大的挥收性,正在溶解历程中,溶量取溶剂的本量均无改变.之阳早格格创做有机溶剂的种类较多,按其化教结构可分为10大类:①芳香烃类:苯、甲苯、两甲苯等;②脂肪烃类:戊烷、己烷、辛烷等;③脂环烃类:环己烷、环己酮、甲苯环己酮等;④卤化烃类:氯苯、两氯苯、两氯甲烷等;⑤醇类:甲醇、乙醇、同丙醇等;⑥醚类:乙醚、环氧丙烷等;⑦酯类:醋酸甲酯、醋酸乙酯、醋酸丙酯等;⑧酮类:丙酮、甲基丁酮、甲基同丁酮等;⑨两醇衍死物:乙两醇单甲醚、乙两醇单乙醚、乙两醇单丁醚等;⑩其余:乙腈、吡啶、苯酚等.有机溶剂具备脂溶性,果此除经呼吸讲战消化讲加进肌体内中,尚可经完备的皮肤赶快吸支,有机溶剂吸支进人体后,将效率于富含脂类物量的神经、血液系统,以及肝肾等真量净器,共时对于皮肤战粘膜也有一定的刺激性.分歧有机溶剂其效率的主要靶器官战效率的强强也分歧,那决断于每一种有机溶剂的化教结构、溶解度、交触浓度战时间,以及肌体的敏感性.时常使用溶剂的极性程序: 火(极性最大) > 甲酰胺> 乙腈> 甲醇> 乙醇> 丙醇> 丙酮> 两氧六环> 四氢呋喃> 甲乙酮> 正丁醇> 醋酸乙酯> 乙醚> 同丙醚> 两氯甲烷> 氯仿> 溴乙烷> 苯> 氯丙烷> 甲苯> 四氯化碳> 两硫化碳> 环己烷> 己烷> 庚烷> 煤油(极性最小)有机溶剂的极性根据官能团战对于称性可收端推断,简直的需参照极性参数,如下表示有机溶剂的极性,闭系到其物理化教本量、如介电常数、奇极矩或者合射率.那种表示要领把所有的溶剂瞅做是连绝效率的介量,而没有是瞅做由各个分子组成的非连绝统一体,而且已思量到溶剂战溶量之间的特殊的相互效率.。
常见有机溶剂极性表

常见有机溶剂极性表 Document number:NOCG-YUNOO-BUYTT-UU986-1986UT有机溶剂是能溶解一些不溶于水的物质的一类有机化合物,其特点是在常温常压下呈液态,具有较大的挥发性,在溶解过程中,溶质与溶剂的性质均无改变。
有机溶剂的种类较多,按其化学结构可分为10大类:①芳香烃类:苯、甲苯、二甲苯等;②脂肪烃类:戊烷、己烷、辛烷等;③脂环烃类:环己烷、环己酮、甲苯环己酮等;④卤化烃类:氯苯、二氯苯、二氯甲烷等;⑤醇类:甲醇、乙醇、异丙醇等;⑥醚类:乙醚、环氧丙烷等;⑦酯类:醋酸甲酯、醋酸乙酯、醋酸丙酯等;⑧酮类:丙酮、甲基丁酮、甲基异丁酮等;⑨二醇衍生物:乙二醇单甲醚、乙二醇单乙醚、乙二醇单丁醚等;⑩其他:乙腈、吡啶、苯酚等。
有机溶剂具有脂溶性,因此除经呼吸道和消化道进入机体内外,尚可经完整的皮肤迅速吸收,有机溶剂吸收入人体后,将作用于富含脂类物质的神经、血液系统,以及肝肾等实质脏器,同时对皮肤和粘膜也有一定的刺激性。
不同有机溶剂其作用的主要靶器官和作用的强弱也不同,这决定于每一种有机溶剂的化学结构、溶解度、接触浓度和时间,以及机体的敏感性。
常用溶剂的极性顺序:水(极性最大)>甲酰胺>乙腈>甲醇>乙醇>丙醇>丙酮>二氧六环>四氢呋喃>甲乙酮>正丁醇>醋酸乙酯>乙醚>异丙醚>二氯甲烷>氯仿>溴乙烷>苯>氯丙烷>甲苯>四氯化碳>二硫化碳>环己烷>己烷>庚烷>煤油(极性最小)有机溶剂的极性根据官能团和对称性可初步判断,具体的需参照极性参数,如下表示有机溶剂的极性,关系到其物理化学性质、如介电常数、偶极矩或折射率。
这种表示方法把所有的溶剂看作是连续作用的介质,而不是看作由各个分子组成的非连续统一体,并且未考虑到溶剂和溶质之间的特殊的相互作用。
有机试剂极性一览表

有机试剂极性大小下面这份溶剂极性表列出了常用有机溶剂极性顺序,并有常见溶剂的粘度、沸点、吸收波长等物理参数,在进行薄层色谱柱(TLC洗脱的时候时很有帮助可能有不准确的,希望在留言处给予更正。
吸收波化合物名称极性粘度沸点长i-pentane(异戊烷)0- 30-n-pentane(正戊烷)036210 Petroleum ether(石油醚)30 〜60210 Hexa ne(己烷)69210 Cyclohexane(环己烷) 1 81210 Isooctane(异辛烷)99210 Trifluoroacetic acid(二氟乙酸)- 72-Trimethylpentane(三甲基戊烷)99215 Cyclopentane(环戊烷)49210n-heptane(庚烷)98200 Butyl chloride(丁基氯;丁酰氯)178220 Trichloroethylene(三氯乙烯;乙炔化三氯)187273 Carbon tetrachloride(四氯化碳)77265 Trichlorotrifluoroethane(三氯三氟代乙烷)48231i-propyl ether(丙基醚;丙醚)68220 Toluene(甲苯)111285p-xylene(对一甲苯)138290 Chlorobenzene(氯苯)132-o-dichlorobenzene(令B二氯苯)180295Ethyl ether(二乙醚; 醚)35220Benzene(苯)380280 Isobutyl alcohol(异丁醇)3108220Methylene chloride(二氯甲烷)240245Ethylene dichloride(二氯化乙烯)84228 n-butanol(正丁醇)117210n-butyl acetate(醋酸丁酯;乙酸丁酯)4-126254n-propanol(丙醇)498210Methyl isobutyl ketone(甲基异丁酮)-119330Tetrahydrofuran(四氢呋喃)66220Ethyl acetate (乙酸乙酯)77260i-propanol(异丙醇)82210 Chloroform(氯仿)61245Methyl ethyl ketone(甲基乙基酮)80330 Dioxane(二恶烷; 二氧六环; 二氧杂环己102220烷)Pyridine(吡啶)115305Acetone(丙酮)57330Nitromethane(硝基甲烷)6101330Acetic acid(乙酸)118230Acetonitrile(乙腈)82210-Aniline(苯胺)184Dimethyl formamide(二甲基甲酰胺)153270Methanol(甲醇)65210Ethylene glycol(乙二醇)197210Dimethyl sulfoxide(二甲亚砜DMSO)189268100 268Water (水)下图是混合有机溶剂极性顺序(由小到大,括号内表示的是混合比例)鶯用混台溶剂极性顺序-环己烷-乙酸乙醋隅十”氯仿丙酮3十k苯炳酮巴十1L苯-乙厳乙际3+可亠氧仿-乙徹钊尸莓-甲醇少巧尸苯-乙瞇卩坤-环己烷-乙舉巴龍(1+1)-^®仿N 题构f氯仿-甲廉3十1)+奉甲醇少氯仿炳ffl(Sd+15)十命乙醋(4杓一苯一邑酸乙酷(1+1尸氯仿一甲萝3+5>^1仿一丙酮(74刃-奉乙酸乙◎弐苯-乙鹼1杓~乙醛-甲醇(9田尸乙酸乙陽龜袖SHL■苯炳酮。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
有机溶剂极性表极性与非极性是针对分子说的。
首先化学共价键分为极性键与非极性键。
非极性键就是共用电子对没有偏移,出
现在单质中比如02极性键就是共用电子对有偏移比如HCI。
而当偏移的非常厉害之后,看上去一边完全失电子另一边得到了电子,就会变成离子键了,如NaCI 再说极性分子与与非极性分子。
由于极性键的出现,所以就使某些分子出现了电极性,但是并不是说所有有极性键的分子都是极性分子。
比如CH4虽然含有4
个极性的C-H键,但是因为其空间上成对称的正四面体结构,所以键的极性相消,整个分子没有极性
对与H20虽然与C02有相同类型的分子式,也同样有极性共价键,但二者分子的极性却不同。
C02是空间对称的直线型,所以分子是非极性分子,H20是折线型,不对称,所以是极性分子,作为溶剂称为极性溶剂
非极性溶剂由非极性分子组成,是指分子中各原子的化学键的合力为零,如CCI4 分子为正四面体,四个C-CI键的合力为零,CCI4分子无极性,CCI4就是非极性溶剂
非极性溶剂"脂肪油(fattyoils)" 液状石蜡(liquidparaffin)" 醋酸乙酯(ethyloleate)" 肉豆蔻酸异丙酯(isopropylmyristate)
非极性溶剂是由非性分子溶液组成的溶剂,非极性分子多由共价键构成,无或电
子活性很小.
最简单准确的说就是偶极矩为零的溶剂。
知道什么是偶极矩吗?
非极性溶剂是由非性分子溶液组成的溶剂,非极性分子多由共价键构成,无或电子活性很小。
偶极矩小的溶剂
溶剂英文名称solve nt
又称溶媒。
能溶解气体、固体、液体而成为均匀混合物的一种液体。
习惯上把气体和固体叫溶质,液体叫溶剂。
对于两种液体所组成的溶液,通常把含量较多的组分叫溶剂,少者叫溶质。
分为无机溶剂和有机溶剂两大类。
水是应用最广泛的无机溶剂,酒精、汽油、氯仿及丙酮等是常用的有机溶剂。
溶剂是一种可以溶化固体,液体或气体溶质的液体,继而成为溶液.在日常生活中最普遍的溶剂是水.而所谓有机溶剂即是包含碳原子的有机化合物•溶剂通常拥有比较低的沸点和容易挥发.或是可以由蒸馏来去除,从而留下被溶物• 因此,溶剂不可以对溶质产生化学反应•- 它们必须为惰性•溶剂可从混合物萃取可溶化合物,最普遍的例子是以热水冲泡咖啡或茶溶剂通常是透明,无色的液体, 他们大多都有独特的气味.
溶液的浓度取决于溶解在溶剂内的物质的多少.溶解度则是溶剂在特定温度下,可以溶解最多多少物质.有机溶剂主要用于干洗(例如四氯乙烯), 作涂料稀释剂(例如
甲苯, 松节油), 作洗甲水或去除胶水(例如丙酮, 醋酸甲酯, 醋酸乙酯), 除锈(例如己烷), 作洗洁精(柠檬精), 用于香水(酒精)跟用于化学合成(Chemical synthesis).
溶剂和溶质大致上可分为极性基(亲水的)和非极性基(疏水的). 极性可以透过量度物质的介电常数或偶极距得知。
非极性溶剂由非极性分子组成,是指分子中各原子的化学键的合力为零,如
CCI4分子为正四面体,四个C-CI键的合力为零,CCI4分子无极性,CCI4就是非极性溶剂. 非极性溶剂" 脂肪油(fattyoils) " 液状石蜡(1iquidparaffin) " 醋酸乙酯(ethyIoIeate) " 肉豆蔻酸异丙酯(isopropyImyristate) . 非极性溶剂
是由非性分子溶液组成的溶剂, 非极性分子多由共价键构成,无或电子活性很小. 最简单准确的说就是偶极矩为零的溶剂。
知道什么是偶极矩吗?非极性溶剂是由非性分子溶液组成的溶剂, 非极性分子多由共价键构成,无或电子活性很小。
偶极矩小的溶剂通过理解非极性溶剂的意义来明白什么叫极性溶剂
一、相似相溶原理1.极性溶剂(如水)易溶解极性物质(离子晶体、分子晶体中的极性物质如强酸等);2.非极性溶剂(如苯、汽油、四氯化碳、酒精等)能溶解非极性物质(大多数有机物、Br2、I2 等);
3•含有相同官能团的物质互溶,如水中含羟基(一0H能溶解含有羟基的醇、酚、羧酸。
二、有机物的溶解性与官能团的溶解性1.官能团的溶解性:
(1)易溶于水的官能团(即亲水基团)有—OH、—CHO、—COO、H—NH2。
(2)难溶于水的官能团(即憎水基团)有:所有的烃基(—CnH2n+1、—CH=CH、2 —C6H5等)、卤原子(一X)、硝基(一N02 等。
2.分子中亲水基团与憎水基团的比例影响物质的溶解性:
(1)当官能团的个数相同时,随着烃基(憎水基团)碳原子数目的增大,溶解性逐渐降低;
例如,溶解性:CH3OH>C2H5OH>C3H7OH> —般地,碳原子个数大于5的醇难溶于水。
(2)当烃基中碳原子数相同时,亲水基团的个数越多,物质的溶解性越大;
例如,溶解性:CH3CH2CH2OH
(3)当亲水基团与憎水基团对溶解性的影响大致相同时,物质微溶于水;
例如,常见的微溶于水的物质有:苯酚C6H5—OH苯胺C6H5-NH2苯甲酸
C6H5- COOH正戊醇CH3CH2CH2CH2CHO H(上述物质的结构简式中“一”左边的为憎水基团,右边的为亲水基团);乙酸乙酯CH3COOCH2CH其中一CH3和—
CH2CH为憎水基团,一CO—为亲水基团)。
(4)由两种憎水基团组成的物质,一定难溶于水。
例如,卤代烃R-X、硝基化合物R-NO2,由于其中的烃基F—、卤原子一X和硝基一
N02均为憎水基团,故均难溶于水。
三、液态有机物的密度
1. 难溶于水,且密度小于水的有机物
例如,液态烃(乙烷、乙烯、苯、苯的同系物……),液态酯(乙酸乙酯、硬脂酸甘油酯……),一氯卤代烷烃(1-氯乙烷……),石油产品(汽油、煤油、油脂……)注:汽油产品分为直馏汽油和裂化汽油(含不饱和烃)。
2. 难溶于水,且密度大于水的有机物
例如:四氯化碳、氯仿、溴苯、二硫化碳
参考资料:
一些溶剂的极性
水(极性最大)>甲酰胺〉乙腈〉甲醇〉乙醇〉丙醇〉丙酮〉二氧六环〉四氢呋喃〉甲乙酮〉正丁醇〉醋酸乙酯〉乙醚〉异丙醚〉二氯甲烷〉氯仿〉溴乙烷>苯>氯丙烷〉甲苯〉四
氯化碳〉二硫化碳〉环己烷〉己烷〉庚烷〉煤油(极性最小),k; q3 J" |1 E0 11 Z4 e (1)极性相似原则
非极性溶质能溶于非极性或弱极性溶剂中,而极性溶质溶于极性溶剂中。
各
种溶剂在20°C下偶极矩如表所示。
各种溶剂在20下的偶极矩
偶极矩为时是非极性溶剂,偶极矩低于5的为弱极性溶剂,大于5的为极性溶剂,大于10的为强极性溶剂。
各种树脂的偶极矩是由组成聚合物分子的共价键的键矩之和(矢量之和)组成的。
表为某些共价键的键矩。
组成聚合物的某些共价键键矩(键矩单位为德拜用D表示),i( b6 F; {' b/
HO e& ?0 Z
聚合物的偶极矩,不仅与单体键节的偶极矩有关,还同分子的凝集态和分子之间的相互作用有关。
聚合物的偶极矩是一个统计性的量,它反映了聚合物分子极化的总和,而聚合物分子的极化有三类:变形极化(诱导极化)、取向极化(偶极极化)和界面极化。
作为非极性的聚合物有PE PS PTFE等没有固有偶极矩
的聚合物,而PMMAPVC PC酚醛等是有固有偶极极矩的极性聚合物。
/ v7 n3 14 h! V ( I! D2 F9 R H' m
(2)溶解度参数相近原则0 t/ C4 ?( J9 L1 V$ g. W {0 p+ |8 ]
溶解度参数相近的溶质和溶剂可以互相溶解,溶剂和树脂的溶解质参数的差值小于〜的,可以溶解,>的不能溶解。
混合溶剂的溶解度参数是混合溶剂中各种单一溶剂的溶解度参数同该溶剂在混合溶剂中的重量%的乘积之和。
树脂和溶
剂的溶解度参数可参看“热溶胶及其在复合包装中的应用”表为各类溶剂的溶解参数范围。
8 i. J$ p. A6 ~7 a" n9 T, A
表各类溶剂的溶解度参数范围
聚合物分子和溶剂接触,如果溶剂对聚合物表面分子的作用力大于树脂内聚力,则树脂可溶解,这种作用就是溶剂化作用。
它主要是高分子的酸性基团(或碱性基团)能与溶剂中的碱性基团(或酸性基团)起溶化作用而溶解。
酸(H+ 是亲电子体(电子接受体),而碱(OHJ是亲核体(电子给予体)。
亲电子基团的强弱排布如下:
—S020IH —COOH —C6H4OIH = CHCIN = CHNdCH2CI> = CHCI 亲核基团的强弱排布如下一CH2NH2 —C6H4NH2C0N(CH3)2 —CON— > 三PO>—CH2COCH2>— CH2OCOC—>—CH2- O- CH2- / |! [# V5 f: 1( _
判断溶剂溶解能力应当把上述三个原则结合起来考虑。
例如:聚碳酸酯的溶
解度参数为,PVC的3=,按溶解度参数相近相溶原则,氯仿(3=)、二氯甲烷
(3=)、环已酮(3=)都与PC PVC相近,能溶解,但实际上PC不溶于环已酮,只溶于氯仿和二氯甲烷,而PVC只溶于环已酮,不溶于氯仿和二氯甲烷。
这是由于PC是给电子性的,PVC是弱亲电子性的,而二氯甲烷是亲电子性的,环已酮是给电子性的,PVC同环已酮发生了溶剂化作用,而PC同二氯甲烷发生了溶剂化作用的缘故。
