2020高考化学双向细目表
2020年山东卷高考题双向细目表分析

2020年山东高考试题分析
2020年山东高考试题分析
电梯下楼,s-t图像判断运动情况、超重失重。 β衰变形成电流判断衰变的粒子个数 光通过玻璃片计算时间差 有振动图像判断波动图像 判断变压器副线圈滑动变阻器电阻
通过P-v图像判断做功、吸热、放热情况 火星探测器减速的制动力大小 斜面上板块+滑轮
有光线射出的面积、全反射的影响因素 电势能、电势比较分析
考点 运动学规律+牛顿运动定律
β衰变+电流定义式 双缝干涉+光的折射 机械波+机械振动 变压器+闭合电路欧姆定律
理想气体 万有引力与航天+匀减速运动
共点力平衡 全反射 电场 功能关系 电磁感应
测重力加速度 测电源的电动势和内阻
理想气体 斜抛运动 组合场 动量守恒定律、机械能守恒定律
基础题44分 中档题36分 难题20分
序号 题型 分值 1 单选 3 2 单选 3 3 单选 3 4 单选 3 5 单选 3 6 单选 3 7 单选 3 8 单选 3 9 多选题 4 10 多选题 4 11 多选题 4 12 多选题 4 13 题 8 17 计算题 14 18 计算题 16
滑轮、弹簧、物块、绳子分析功与能 线圈切割磁场、判断电流与受力 物块沿斜面下滑计算加速度 电流变内接测电源电动势和内阻
火罐与抽气罐比较、计算抽出气体比例 运动的分解计算两个方向的位移大小 质谱仪电场加速、磁场竖直偏转、电场匀加速
滑块反复碰撞、多过程问题分析
四翼 基础性 基础性 基础性 基础性 基础性 综合性 基础性 基础性 基础性 创新性 综合性 综合性、创新性 基础性、创新性 基础性 基础性、应用性 基础性、创新性 综合性、创新性 综合性、创新性
2023届高考化学知识点双向细目表——物质结构与性质模块
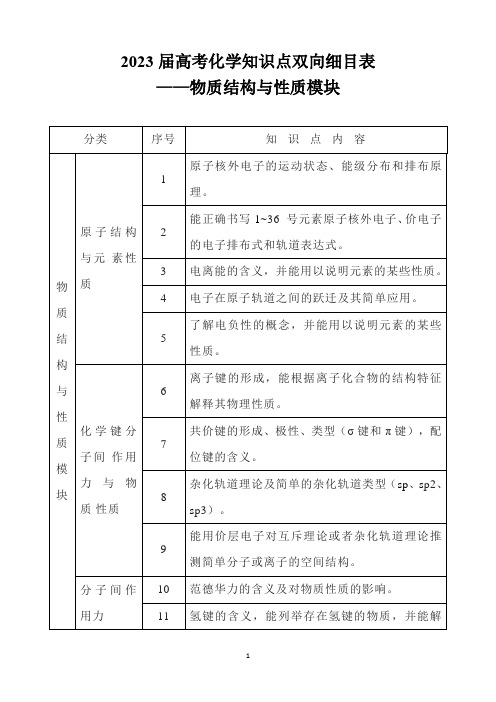
与物质的性质
10
范德华力的含义及对物质性质的影响。
11
氢键的含义,能列举存在氢键的物质,并能解释氢键对物质性质的影响。
5
了解电负性的概念,并能用以说明元素的某些性质。
化学键分子间作用力与物质性质
6
离子键的形成,能根据离子化合物的结构特征解释其物理性质。
7
共价键的形成、极性、类型(σ键和π键),配位键的含义。
8
杂化轨道理论及简单的杂化轨道类型(sp、sp2、sp3)。
9
能用价层电子对互斥理论或者杂化轨道理论推测简单分子构与性质模块
分类
序号
知识点内容
物
质
结
构
与
性
质
模
块
原子结构与元素性质
1
原子核外电子的运动状态、能级分布和排布原理。
2
能正确书写1~36号元素原子核外电子、价电子的电子排布式和轨道表达式。
3
电离能的含义,并能用以说明元素的某些性质。
4
电子在原子轨道之间的跃迁及其简单应用。
高中化学必修和必修双向细目表

高中化学必修1双向细目表
高中化学必修2双向细目表
高一历史人教版必修二知识细目表
中国史(一、三、四、五单元)
第一单元古代中国经济的基本结构与特点
第三单元近代中国经济结构的变动与资本主义的曲折发展
第四单元中国特色社会主义建设的道路
第五单元中国近现代社会生活的变迁
世界史(二、六、七、八单元)
第二单元资本主义世界市场的形成和发展
第六单元世界资本主义经济政策的调整
第七单元苏联的社会主义建设
第八单元世界经济的全球化趋势
高一历史必修二教学进度表
2021-----2021学年第二学期高一化学教学进度表。
2020高考化学双向细目表

了解化学反应中的能量变化,吸热反应、放热反应、反应热、燃烧热和中和热及新能源的开发等概念。
26,热方程,反应热7分
11热化学书写反应热,中等
7热化学书写反应热,中等
溶液
20
了解溶液的含义
8涉及
21
了解溶液的组成,理解溶液中溶质的质量分数的概念。
22
了解饱和溶液、不饱和溶液的概念。了解溶解度的概念。了解温度对溶解度的影响及溶解度曲线。
8,涉及离子反应量变关系
10题涉及29题15分多半,综合元素化合物知识
6,方程式书写,中下9综合反应速率图象29电解综合运用15分,涉及实验方案
37
理解离子反应的概念。
38
理解电解质的电离平衡概念。
39
了解水的电离、溶液pH等概念。
7,选择,6分,中等
10综合电离,
8涉及,
40
了解强酸强碱中和滴定的原理。
30题有机结构简式确定
30涉及
化
学
实
验
78
了解常见化学仪器的主要用途、使用方法
历年均在有机无机综合题中涉及
79
能绘制和识别典型的实验仪器装置图
80
常见试剂的化学性质及其保存方法
81
化学实验的基本操作(药品取用,天平使用,仪器连接,气密性检查,物质的加热、过滤、蒸发,试纸的使用,容量瓶使用,萃取、分液、蒸馏等),了解实验室一般事故的预防和处理方法。
化
合
物
常
见
金
属
元
素
的
性
质
44
了解金属钠的物理性质,掌握钠和镁化学性质。
45
从原子的核外电子排布,理解ⅠA 、ⅡA族元素(单质、化合物)的相似性和递变性。
高考化学试题双向细目表

6
7 一般
全部
常见无机物及其应用-卤素及其化合物-氯及其化合物-氯气
6
7 较难
全部
化学反应原理-化学反应原理综合考查
6
7 一般
全部
物质结构与性质-元素周期表 元素周期律-元素周期律-元素周 6
期律的应用-微粒半径大小的比较方法
7 一般
全部
化学反应原理-化学能与电能-原电池-原电池原理-原电池电极反 6
11 困难
全部
化学反应原理-化学能与热能-化学反应中能量变化-盖斯定律及 14
11 较难
全部
五、有机推断题
12 较难
全部
其有关计算-盖斯定律与热化学方程式
物质结构与性质-原子结构与性质-基态原子核外电子排布的表 15
示-核外电子排布规律
共 15
分
有机化学基础-烃的衍生物-卤代烃-卤代烃的性质-卤代烃的消去 15
反应
应式书写
7 较难
全部
化学反应原理-水溶液中的离子平衡-水的电离及溶液的酸碱性6
酸碱中和滴定
二、工业流程题
共 14 分
8 一般
全部
认识化学科学-氧化还原反应-氧化还原反应综合分析-氧化还原 14
反应方程式的配平
பைடு நூலகம்
三、实验题
共 14 分
9 一般
全部
常见无机物及其应用-铁及其化合物-铁盐
14
四、原理综合题
共 29 分
2020 年高考化学试题双向细目表
考查范围:常见无机物及其应用、有机化学基础、化学反应原理、物质结构与性质、认识化
学科学
题号 难度 考查范围
知识点
分值
一、单选题
2023届高考化学知识点双向细目表——有机化学基础模块
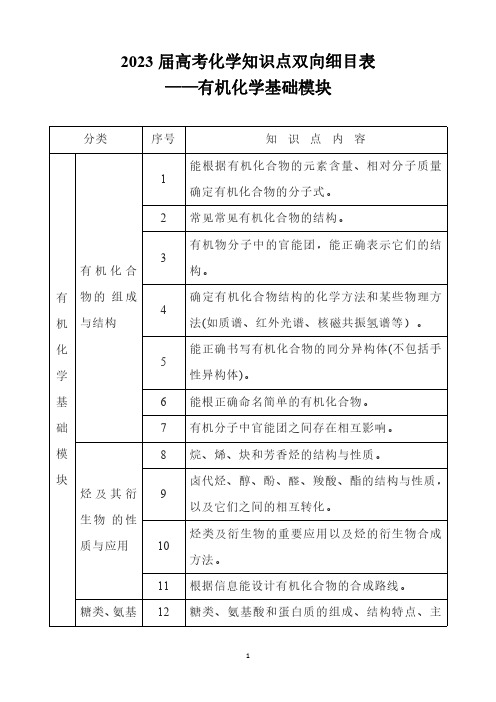
质与应用 10
方法。
11 根据信息能设计有机化合物的合成路线。
糖类、氨基 12 糖类、氨基酸和蛋白质的组成、结构特点、主
1
酸
要化学性质及应用。
和蛋白质 13 糖类、氨基酸和蛋白质在生命过程中的作用。
合成高分子的组成与结构特点。能依据简单合
14 成高分子的结构分析其链节和单体。
合成高分 15 加聚反应和缩聚反应的含义。
2023 届高考化学知识点双向细目表 ——有机化学基础模块
分类
序号
知识点内容
能根据有机化合物的元素含量、相对分子质量
1 确定有机化合物的分子式。
2 常见常见有机化合物的结构。
有机物分子中的官能团,能正确表示它们的结
3
有机化合
构。
有 物的 组成
确定有机化合物结构的化学方法和某些物理方
4
机 与结构
法(如质谱、红外光谱、核磁共振氢谱等)。
化
能正确书写有机化合物Байду номын сангаас同分异构体(不包括手
5
学
性异构体)。
基
6 能根正确命名简单的有机化合物。
础
7 有机分子中官能团之间存在相互影响。
模
8 烷、烯、炔和芳香烃的结构与性质。
块
卤代烃、醇、酚、醛、羧酸、酯的结构与性质,
烃及其衍 9
以及它们之间的相互转化。
生物 的性
烃类及衍生物的重要应用以及烃的衍生物合成
子
合成高分子在高新技术领域的应用以及在发展 16
经济、提高生活质量方面中的贡献。
2
山东高考+2020模拟高考化学知识点双向细目表
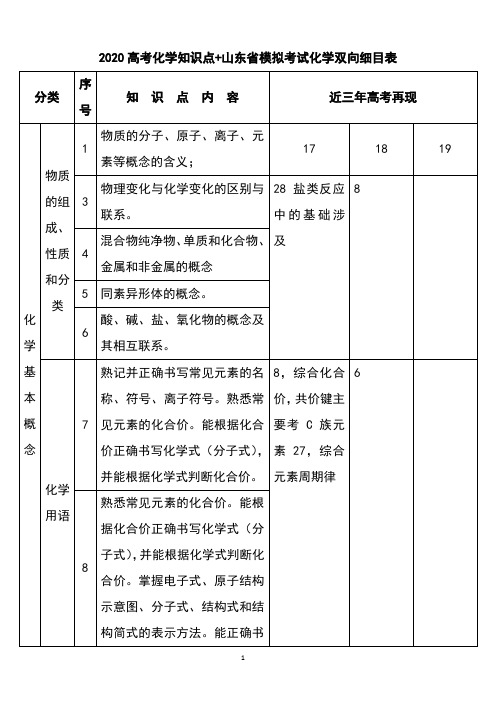
71
了解石油化工、农副产品化工、资源综合利用及污染和环保的概念。
72
了解在生活和生产中常见有机物的性质和用途。
73
以葡萄糖为例,了解糖类的基本组成和结构,主要性质和用途。
74
了解蛋白质的基本组成和结构、主要性质和用途。
11综合同位素,物质的量计算,中等
9题,综合元素周期表,中等
27
以第1,2,3周期的元素为例,了解原子核外电子排布规律。
28
理解离子键、共价键的含义。理解极性键和非极性键。了解极性分子和非极性分子。了解分子间作用力。初步了解氢键。
29
了解几种晶体类型(离子晶体、原子晶体、分子晶体、金属晶体)及其性质。
47
了解金属的通性,金属冶炼的一般原理。初步了解金属的回收和资源保护。
48
掌握Fe和Al的化学性质。
49
掌握常见金属的活动顺序。
50
以Fe(Ⅱ)Fe(Ⅲ)的相互转化为例,了解变价金属元素的氧化还原性。
51
了解铝的重要化合物。
52
初步了解合金的概念。
常
见
非
金
属
元
素
的
性
质
53
以氯为例,了解卤族元素的物理性质和化学性质。
54
从原子的核外电子排布,理解卤族元素(单质、化合物)的相似性和递变性。
55
掌握氯气的化学性质,了解几种重要的含卤素化合物的性质和用途。
56
了解这些元素(如:H,O,S,N,P,C,Si)的单质及某些氧化物、氢化物的性质。
57
以Na2O2为例,了解过氧化物的性质。
高考化学双向细目表

71
了解石油化工、农副产品化工、资源综合利用及污染和环保的概念。
72
了解在生活和生产中常见有机物的性质和用途。
73
以葡萄糖为例,了解糖类的基本组成和结构,主要性质和用途。
74
了解蛋白质的基本组成和结构、主要性质和用途。
88
掌握有关物质的量的计算。
89
掌握有关气体摩尔体积的计算。
90
掌握有关溶液浓度(溶液中溶质的质量分数和物质的量浓度)的计算。
91
掌握利用化学反应方程式的计算。
92
掌握有关溶液pH与氢离子浓度、氢氧根离子浓度的简单计算。
93
掌握有关燃烧热的简单计算。
94
以上各类化学计算的综合应用。
注:上表项目为高考化学考点总表,元素化合物知识部份的分析考虑到此知识点为学生记忆内容,为必掌握内容,是学习基础,复习和平时训练均不断重复,故并未对期分值和难度进行细分。
84
根据实验现象,观察、记录、分析或处理数据,得出正确结论。
85
根据实验试题要求,设计或评价实验方案。
86
综合运用化学知识和实验基本技能分析和解决实验中出现的各种问题
化
学
计
算
87
掌握有关相对原子质量、相对分子质量及确定分子式的计算。
备注:若当年高考卷中未出现纯粹的计算题,单项分析中均已涉及计化学计算及实验、实验方案设计,限于篇幅,不再重复罗列,高考复习中将专题复习化学综合计算和实验方案设计
39
了解水的电离、溶液pH等概念。
7,选择,6分,中等
10综合电离,
8涉及,
40
2020湖北省重点高中协作体高二期中高二化学双向细目表
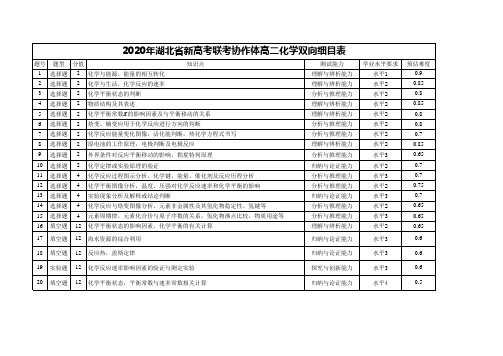
归纳与论证能力
水平3
0.6
19 实验题 12 化学反应速率影响因素的验证与测定实验
探究与创新能力
水平3
0.6
20 填空题 12 化学平衡状态,平衡常数与速率常数相关计算
归纳与论证能力
水平4
0.5
k
7 选择题 2 化学反应能量变化图像,活化能判断,热化学方程式书写
8 选择题 2 原电池的工作原理,电极判断及电极反应
9 选择题 2 外界条件对反应平衡移动的影响,勒夏特列原理
10 选择题 2 化学定律或实验原理的验证
11 选择题 4 化学反应过程图示分析,化学键、能量、催化剂及反应历程分析
12 选择题 4 化学平衡图像分析,温度、压强对化学反应速率和化学平衡的影响
2020年湖北省新高考联考协作体高二化学双向细目表
题号 题型 分值
知识点
1 选择题 2 化学与能源,能量的相互转化
2 选择题 2 化学与生活,化学反应的速率
3 选择题 2 化学平衡状态的判断
4 选择题 2 物质结构及其表述
5 选择题 2 化学平衡常数K 的影响因素及与平衡移动的关系
6 选择题 2 焓变、熵变应用于化学反应进行方向的判断
13 选择题 4 实验现象分析及解释或结论判断
14 选择题 4 化学反应与焓变图像分析,元素非金属性及其氢化物稳定性、氢键等
15 选择题 4 元素周期律,元素化合价与原子序数的关系,氢化物沸点比较,物质用途等
16 填空题 12 化学平衡状态的影响因素,化学平衡的有关计算
测试能力 理解与辨析能力 理解与辨析能力 分析与推理能力 理解与辨析能力 理解与辨析能力 分析与推理能力 分析与推理能力 理解与辨析能力 分析与推理能力 归纳与论证能力 分析与推理能力 分析与推理能力 归纳与论证能力 分析与推理能力 分析与推理能力 理解与辨析能力
高考化学双向细目表

16
物质的量的单位——摩尔(mol)、摩尔质量、气体摩尔体积、物质的量浓度、阿伏加德罗常数的含义
了解
17
根据物质的量与微粒(原子、分子、离子等)数目、气体体积(标准状况下)之间的相互关系进行有关计算
综合应用
三、溶液
18
溶液的含义
了解
19
溶解度、饱和溶液的概念
了解
20
溶液的组成;溶液中溶质的质量分数的概念,并能进行有关计算
了解
3
物质的组成、结构和性质的关系;化学反应的本质、基本原理以及能量变化等规律
了解、了解
4
定量研究的方法是化学发展为一门科学的重要标志;摩尔(mol)是物质的量的基本单位,可用于进行简单的化学计算
了解、理解
5
科学、技术、社会的相互关系(如化学与生活、材料、能源、环境、生命过程、信息技术的关系等);在化工生产中遵循“绿色化学”思想的重要性
了解
14
氨基酸的组成、结构特点和主要化学性质;氨基酸与人体健康的关系
了解、了解
15
蛋白质的组成、结构和性质
了解
16
化学Байду номын сангаас学在生命科学发展中所起的重要作用
了解
四、合成高分子化合物
17
合成高分子的组成与结构特点;依据简单合成高分子的结构分析其链节和单体
了解、理解
18
加聚反应和缩聚反应的特点
了解
20
新型高分子材料的性能及其在高新技术领域中的应用
综合应用
常见无机物及其应用
一、常见金属元素(如Na、Al、Mg、Fe、Cu等)
55
常见金属的活动顺序
了解
56
常见金属及其重要化合物的主要性质及其应用
高考化学双向细目表

30
掌握元素周期律的实质,了解元素周期表(长式)的结构(周期、族)及其应用。
27.
9题涉及
12题综合周期律、表
31
以第3周期为例,掌握同一周期内元素性质(如:原子半径、化合价、单质及化合物性质)的递变规律与原子结构的关系;以I A 和ⅦA 族为例,掌握同一主族内元素性质递变规律与原子结构的关系。
43
理解电解原理。了解铜的电解精练、镀铜、氯碱工业等反应原理。
10,选择,6分,
元
素
及
其
化
合
物
常
见
金
属
元
素
的
性
质
44
了解金属钠的物理性质,掌握钠和镁化学性质。
45
从原子的核外电子排布,理解ⅠA 、ⅡA族元素(单质、化合物)的相似性和递变性。
46
以氢氧化钠为例,了解重要的碱的性质和用途。了解钠的重要化合物。
13有机综合迁移能力,烯烃复分解30题综合推断,增加了未知知识点推导未知知识点的给规律题型
71
了解石油化工、农副产品化工、资源综合利用及污染和环保的概念。
72
了解在生活和生产中常见有机物的性质和用途。
73
以葡萄糖为例,了解糖类的基本组成和结构,主要性质和用途。
74
了解蛋白质的基本组成和结构、主要性质和用途。
88
掌握有关物质的量的计算。
89
掌握有关气体摩尔体积的计算。
90
掌握有关溶液浓度(溶液中溶质的质量分数和物质的量浓度)的计算。
91
掌握利用化学反应方程式的计算。
92
掌握有关溶液pH与氢离子浓度、氢氧根离子浓度的简单计算。
93
高中化学双向细目表

序号
内容
知道
了解
理
解
应
用
第一
章
物质结构儿糸周期
律
第一节
元素周期表
1、元素周期表的结构以及
周期、族等概念
V
2、原子结构与元素在周期
表中位置间的关系
V
3、通过对碱金属、卤族元素性质的探究,理解元素性质与原子结构以及元素在周期表中的位置的相互关系,掌握碱金属和卤族元糸的相似性和递变性
1、乙醇的物理性质,乙酸和乙酸乙脂的物理性质
2、乙醇的生理作用和工业制法
3、理解乙醇的结构,通过分析乙醇的结构式掌握乙醇在发生化学反应时的断键位置,从而推断乙醇所具有的化学性质
V
4、乙酸的物理性质以及它
与人们生活的关系
5、通过分析乙醇和乙酸的结构式,掌握它们发生脂化反应的原理以及实验的操作方法,分析实验现象,会熟练地书写该化学方程式
V
第二节
化学能与电能
1、火力发电中的能量转化
V
2、原电池的原理
V
3、氧化还原反应是使化学
能转换为电能的关键
V
4、通过对原电池装置的分析,掌握原电池正、负极判断方法
V
5、通过原电池装置来判断
金属的活动性顺序
V
6、几种发展中的化学电源
V
7、学会自己设计原电池
V
第三节
化学反应的速率和限度
1、化学反应速率的涵义及
V
4、掌握蛋白质的基本性质,认识蛋白质是生命现象最基本的物质基础
V
第四
章
化学与可持续发展
第一节
开发利用金属矿物和海水
资源
1、了解金属冶炼的一般原理,理解金属冶炼方法的选择同金属活动性的关系,了解常见金属的冶炼方法
高考化学双向细目表

9题涉及
12题综合周期律、表
31
以第3周期为例,掌握同一周期内元素性质(如:原子半径、化合价、单质及化合物性质)的递变规律与原子结构的关系;以I A 和ⅦA 族为例,掌握同一主族内元素性质递变规律与原子结构的关系。
8,选择,6分,,简单27,综合元素化合物15分
28元素周期律和元素化合物知识共15分难度中等及中上
29题综合卤代烃、酯类、烯烃类,醛类主要官能团反应
12酚、酯考查,官能团计算30题共15分有机推断
13有机综合迁移能力,烯烃复分解30题综合推断,增加了未知知识点推导未知知识点的给规律题型
71
了解石油化工、农副产品化工、资源综合利用及污染和环保的概念。
72
了解在生活和生产中常见有机物的性质和用途。
73
9,选择,6分,
13离子反应量变关系
41
理解盐类水解的原理。了解盐溶液的酸碱性。
10综合电离水解
中上难度
8涉及
42
理解原电池原理。初步了解化学电源。了解化学腐蚀与电化学腐蚀及一般防腐蚀方法。
10主要电解综合原电池
43
理解电解原理。了解铜的电解精练、镀铜、氯碱工业等反应原理。
10,选择,6分,
元
素
及
其
化
合
物
常
见
金
属
元
素
的
性
质
44
了解金属钠的物理性质,掌握钠和镁化学性质。
45
从原子的核外电子排布,理解ⅠA 、ⅡA族元素(单质、化合物)的相似性和递变性。
46
以氢氧化钠为例,了解重要的碱的性质和用途。了解钠的重要化合物。
47
了解金属的通性,金属冶炼的一般原理。初步了解金属的回收和资源保护。
2020全国卷双向细目表

了解选择题15查复数的运算√25考查集合的交集运算√35考查棱锥的几何性质45考查抛物线性质的应用55考查回归方程,考查学生的读图视图能力65考查利用导数研究过曲线上某点处的切线方程75考查三角函数的图象和性质,主要是函数的周期的求法85考查二项式定理的应用95考查三角函数的化简求值,考查同角三角函数基本关系式与二倍角公式的应用105考查球的内接体问题,球的表面积的求法115考查直线与圆位置关系的应用,考查圆的切线方程,考查过圆两切点的直线方程的求法125主要考查指数函数以及对数函数性质的应用填空题135考查了简单的线性规划,以及利用几何意义求最值145考查向量的模的求法,数量积的应用155考查双曲线的简单性质的应用,离心率的求法165考查三棱锥展开图,涉及余弦定理的应用,数形结合思想解答题1712考查等比数列的通项公式和求和公式的运用,以及等差数列的中项性质,考查数列的错位相减法求和,主要考查方程思想和化简运算能力1812本题考查线面垂直的判定以及利用空间向量求解二面角,考查推理能力及计算能力1912考查概率的求法,考查相互独立事件概率计算公式和互斥事件概率加法公式等基础知识,考查运算求解能力2012查了求椭圆的方程问题,考查直线和椭圆的关系以及直线方程问题2112考查导数的运用:求单调性和最值,考查构造函数法,主要考查分类讨论思想和化简运算能力、推理能力选做题2210考查简单曲线的极坐标方程,考查参数方程化普通方程,考查计算能力2310考查了绝对值函数的解法题型题号分值知识内容知识要求理解掌握空间想象能力抽象概念能力推理论证能力运算求解能力数据处理能力应用与创新意识√易√易√√√易√√易√√易√√易√√√中√√中√√√中√√√中√√√中√√√中√√易√√中√√√√中√√√√中√√√√中√√√中√√√√中√√√较难√√√√√难√√中√√中难度要求能力目标。
2020高考化学双向细目表

题
号分数知识目标
能力目标难度要求
考纲要求的核心考点
接受、吸收、整合信息能力分析和解决问题的能力化学实验与探究的能力
选择题
76化学与生活、材料、能源、生命、信息技术等的关系;化学变化和物理变化;环境污染问题等
√√易86常见元素的主要性质、应用与化学实验的基本操作的结合
√√√
易96元素周期表及周期律,化学键
√√中难106有机物的同分异构体及醇、酯的性质
√√难116小流程:化学实验基础知识,元素的性质,反应原理分析√√√中难126电化学的综合运用√√中13
6
水溶液中的离子平衡,
√
√
√
难
非选择题
2614 1.化学实验常用仪器的主要用途和使用方法2.化学实验的基本操作3.有机物的分离和提纯4.有机化合物的主要性质5.酸碱中和滴定及计算
√√√中难
2714物质制备类化工流程 1.方程式的书写2.流程图分析
3.化学实验仪器及常用的提纯与分离方法
4.电极反应方程式的书写
5.电化学中离子交换膜的考察。
√√√中难
2815 1.能量转化,盖斯定理,碰撞理论,活化能2.识图整合知识,速率平衡移动,K 的计算。
√√√中难选做题
3515电子排布图,价层电子对互斥理论,分子的性质,空间结构,杂化,化学键,均摊法,有关晶胞密度的计算,晶胞投影
√√中36
15
流程推断,反应类型判断,共线共面问题,官能团,核磁共振氢谱,同分异构体,有机物主要性质。
√
√
中。
(原创2023)化学高考双向细目表

(原创2023)化学高考双向细目表一、无机化学1. 元素和化合物- 1.1 元素周期表- 1.2 常见元素的性质和应用- 1.3 水和溶液中的离子反应- 1.4 化合物的命名和化学式2. 化学反应- 2.1 燃烧反应- 2.2 氧化还原反应- 2.3 酸碱中和反应- 2.4 沉淀反应- 2.5 气体生成和反应3. 化学原理- 3.1 序列化反应和电位差- 3.2 动态平衡和平衡常数- 3.3 反应速率和速率常数- 3.4 催化剂和化学反应速率二、有机化学1. 有机化合物- 1.1 碳的特性和共价键- 1.2 烃类化合物- 1.3 醇、酚、醚类化合物- 1.4 醛、酮、羧酸类化合物- 1.5 氨基酸和蛋白质2. 有机反应- 2.1 烃类的燃烧反应- 2.2 单官能团化合物的反应- 2.3 多官能团化合物的反应- 2.4 聚合反应和聚合物的合成- 2.5 脂肪酸和酯的反应3. 有机化学原理- 3.1 反应机理和反应路径- 3.2 功能团和化学性质- 3.3 离子和自由基反应- 3.4 共轭系统和共轭反应三、化学实验1. 基本实验操作- 1.1 实验室安全和实验室常识- 1.2 仪器使用和实验操作技巧- 1.3 实验记录和数据处理2. 实验现象和解释- 2.1 气体生成与气体收集- 2.2 溶液中的颜色变化- 2.3 岩石和矿石的检验- 2.4 酸碱中和和中和滴定- 2.5 电解质的电导性实验3. 实验设计和控制变量- 3.1 实验变量和实验因素- 3.2 实验设计和实验步骤- 3.3 实验结果的误差和精度- 3.4 实验报告的撰写和结论以上为高考化学学科的双向细目表,其中包含了无机化学、有机化学和化学实验三个部分的细分内容。
学生可以根据这份细目表来进行有针对性的学习和复习,以便在高考中取得好成绩。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
8
4
混合物纯净物、单质和化合物、金属和非金属的概念
5
同素异形体的概念。
6
酸、碱、盐、氧化物的概念及其相互联系。
化学
用语
7
熟记并正确书写常见元素的名称、符号、离子符号。熟悉常见元素的化合价。能根据化合价正确书写化学式(分子式),并能根据化学式判断化合价。
8,综合化合价,共价键主要考C族元素27,综合元素周期律
化学反应速率
化学平衡
32
了解化学反应速率的概念,反应速率的表示方法,理解外界条件(浓度、温度、压强、催化剂等)对反应速率的影响。
13,综合考化学速率及平衡6分,中等以上难度
26,第三问速率及平衡,中上4分
27综合整块知识,有图象分值,转化率计算,方向15分,中等及中上难度
8涉及27题15分综合化学平衡及速率,难度中上
化
合
物
常
见
金
属
元
素
的
性
质
44
了解金属钠的物理性质,掌握钠和镁化学性质。
45
从原子的核外电子排布,理解ⅠA 、ⅡA族元素(单质、化合物)的相似性和递变性。
46
以氢氧化钠为例,了解重要的碱的性质和用途。了解钠的重要化合物。
47
了解金属的通性,金属冶炼的一般原理。初步了解金属的回收和资源保护。
48
掌握Fe和Al的化学性质。
33
了解化学反应的可逆性。理解化学平衡的含义及其与反应速率之间的联系。
34
理解勒沙特列原理的含义。理解浓度、温度、压强等条件对化学平衡移动的影响。
35
以合成氨工业生产为例,用化学反应速率和化学平衡的观点理解工业生产的条件。
电
解
质
溶
液
36
了解电解质和非电解质、强电解质和弱电解质的概念。
28题,共13分,综合离子反应,盐类反应,实验方案,离子检验
8,涉及离子反应量变关系
10题涉及29题15分多半,综合元素化合物知识
6,方程式书写,中下9综合反应速率图象29电解综合运用15分,涉及实验方案
37
理解离子反应的概念。
38
理解电解质的电离平衡概念。
39
了解水的电离、溶液pH等概念。
7,选择,6分,中等
10综合电离,
8涉及,
40
了解强酸强碱中和滴定的原理。
49
掌握常见金属的活动顺序。
50
以Fe(Ⅱ)Fe(Ⅲ)的相互转化为例,了解变价金属元素的氧化还原性。
51
了解铝的重要化合物。
52
初步了解合金的概念。
常
见
非
金
属
元
素
的
性
质
53
以氯为例,了解卤族元素的物理性质和化学性质。
54
从原子的核外电子排布,理解卤族元素(单质、化合物)的相似性和递变性。
55
掌握氯气的化学性质,了解几种重要的含卤素化合物的性质和用途。
19
了解化学反应中的能量变化,吸热反应、放热反应、反应热、燃烧热和中和热及新能源的开发等概念。
26,热方程,反应热7分
11热化学书写反应热,中等
7热化学书写反应热,中等
溶液
20
了解溶液的含义
8涉及
21
了解溶液的组成,理解溶液中溶质的质量分数的概念。
22
了解饱和溶液、不饱和溶液的概念。了解溶解度的概念。了解温度对溶解度的影响及溶解度曲线。
9,选择,6分,
13离子反应量变关系
41
理解盐类水解的原理。了解盐溶液的酸碱性。
10综合电离水解
中上难度
8涉及
42
理解原电池原理。初步了解化学电源。了解化学腐蚀与电化学腐蚀及一般防腐蚀方法。
10主要电解综合原电池
43
理解电解原理。了解铜的电解精练、镀铜、氯碱工业等反应原理。
10,选择,6分,
元
素
及
其
6
8
熟悉常见元素的化合价。能根据化合价正确书写化学式(分子式),并能根据化学式判断化合价。掌握电子式、原子结构示意图、分子式、结构式和结构简式的表示方法。能正确书写化学方程式、离子方程式、电离方程式、电极反应式。
化学
中常
用计
量
12
了解相对原子质量、相对分子质量的含义。
11,综合原子结构
中等
6,氧化还原涉及
简单
13
物质的量的单位--摩尔(mol),摩尔质量、气体摩尔体积(相应单位为g·mol-1、L·mol-1)。
14
物质的量浓度(mol·L-1)、阿伏加德罗常数。
15
掌握物质的量与微粒(原子、分子、离子等)数目、气体体积(标准状况下)之间的相互关系。
化学反应与能量
16
掌握化学反应的四种基本类型:化合、分解、置换、复分解。
12氧化还原、物质的量、化学计算
中等26题一问
6,综合部份物质的量计算,主要得失电子守恒、部份氧化还原,中上13题氧化与离子综合
10,得失电子守恒,方程式配平
17
理解氧化还应反应,了解氧化剂和还原剂等概念。掌握重要氧化剂、还原剂之间的常见反应。
18
能判断氧化还原反应中电子转移的方向和数目,并能配平反应方程式。
9题,综合元素周期表,中等
27
以第1,2,3周期的元素为例,了解原子核外电子排布规律。
28
理解离子键、共价键的含义。理解极性键和非极性键。了解极性分子和非极性分子。了解分子间作用力。初步了解氢键。
29
了解几种晶体类型(离子晶体、原子晶体、分子晶体、金属晶体)及其性质。
元素周期律和周期表
30
掌握元素周期律的实质,了解元素周期表(长式)的结构(周期、族)及其应用。
27.
9题涉及
12题综合周期律、表
31
以第3周期为例,掌握同一周期内元素性质(如:原子半径、化合价、单质及化合物性质)的递变规律与原子结构的关系;以I A 和ⅦA 族为例,掌握同一主族内元素性质递变规律与原子结构的关系。
8,选择,6分,,简单27,综合元素化合物15分
28元素周期律和元素化合物知识共15分难度中等及中上
56
了解这些元素(如:H,O,S,N,P,C,Si)的单质及某些氧化物、氢化物的性质。
57
以Na2O2为例,了解过氧化物的性质。
58
掌握硫酸、硝酸的化学性质。
23
初步了解结晶、结晶水、结晶水合物、风化、潮解的概念。
24
了解胶体的概念及其重要性质和应用。
7,综合胶体性质及应用,中等
化
学
基
本
理
论
物
质
结
构
25
了解原子的组成及同位素,以及质量数与质子数、中子数之间的相互关系
11综合同位素,物质的量计算,中等
本文从网络收集而来,上传到平台为了帮到更多的人,如果您需要使用本文档,请点击下载,另外祝您生活愉快,工作顺利,万事如意!
2020高考化学双向细目表
分类
序号
知 识 点 内 容
近三年高考再现
化
学
基
本
概
念
物质的组成、性质和分类
1
物质的分子、原子、离子、元素等概念的含义;
17
18
19
3
物理变化与化学变化的区别与联系。
