重庆大学有机化学习题答案
《有机化学》章节习题答案.docx
第一章习题1.何为共价键的饱和性和方向性?2.下列分子中哪些具有极性键?哪些是极性分子?(1)CH4 (2) CH2C12 (3) CH3Br (4) CH3OH (5) CH30CH3 (6) HC=CH3.按碳架形状分类,下列化合物各属哪一类化合物?第二章习题1.用系统命名法命名下列化合物:(1) (CH3CH2)2CHCH3C2H5 (2) CH3CCH2CH3CH2CH2CH3CH3CH2 CH2CH3(3)\ c // \(CH3)3C CH(CH3)2(4) (C2H5)2CHCH(C2H5)CH2CH(CH3)2CH(CH3)2(5)CH3—CH—CH2—CH—CH—CH3CH2CH3 CH3CH2CH34.指出下列每个分子中存在的官能团类型:⑺ H3C ----- < C(CH3)3 (8)2. 写出下列化合物的构造式:(1) 由一个叔丁基和异丙基组成的烷炷; (2) 含一侧链甲基,分子量为98的环烷炫(3) 分子量为114,同时含有1°、2°、3。
、4。
碳的烷炷。
3.写出下列化合物的结构式,如其名称与系统命名原则不符,请予以改正。
(1)3, 3-二甲基丁烷 (2)2, 3-二甲基-2-乙基丁烷 (3) 4 -异丙基庚烷(4) 3> 4-二甲基-3 -乙基戊烷(5)3, 4, 5-三甲基-4-正丙基庚烷 ⑹2 -叔丁基-4, 5 -二甲基己烷4. 相对分子质量为72的烷任进行高温氯化反应,根据氯化产物的不同,推测各种烷炷的结构式。
(1)只生成一种一氯代产物(2)可生成三种不同的一氯代产物(3) 生成四种不同的一氯代产物 (4)只生成二种二氯代产物 5.不查表将下列烷炷的沸点由高至低排列成序: (1)2, 3-二甲基戊烷 (2) 2-甲基己烷 (3)正庚烷 (4) 正戊烷(5)环戊烷6. 写出下列化合物的优势构象—( 「CH2CH3 (1) BrCH 2CH 2Cl (2) CH 3CH 2CH 2CH 2CH 3 (3) '、'、—/(4)反-1-甲基-4-叔丁基环己烷7. 写出1, 3-二甲基环已烷和1-甲基-4-异丙基环已烷的顺、反异构体优势构象,并比较每组中哪个稳定。
重庆大学大学化学习题答案

习题答案11.△f H m(298.15K)=44.01 kJ·mol-12mol时,△H(298.15K)=88.02kJ吸热Q p=△H=88.02kJ做功W=83.06 kJ2.νA= -3,νB= -1,νc= 2,△ξ(1)=0.5mol3.(1)△ξ(1)=4mol△r H m(298.15K)= -92.30kJ·mol-1△r H(298.15K)= -369.2kJ(2)△ξ(2)=2mol△r m(298.15K)= -184.6kJ·mol-1△r H (298.15K)= -369.2kJ4.△f m(298.15K)= -157kJ·mol-15.A.△r m(298.15K)分别为-2599kJ·mol-1,-890.3kJ·mol-1,-566.0kJ·mol-1B.△c H 分别为-1299.5kJ·mol-1,-890.3kJ·mol-1,-283.0kJ·mol-1 C.发热量排队C2H2>CH4>CO D.发热量排队CH4>C2H2>CO 6.(1)C,(2)B 7.(1)31.7kJ,(2)1.91×103kJ·mol-1 8.△= -626.6kJ·mol-110.△r m(298.15K)=173.14kJ·mol-1,有11. △f m(298.15K)= -1015kJ·mol-1 12.B13.T<1.24×103K,建议不可行,因为任何温度下,△r G(T)>0 14.D<A<C<B<E15.(1)△r m(298.15K)=689.94kJ·mol-1△r S m(298.15K)=0.360kJ·K-1·mol-1(2)△r m(298.15K)=582.2·mol-1,否(3)△r(1 000K)=329.0kJ·mol-1,否(4)T>1912K16.T<463.7K21. νA=0.5mol·dm-3·s-1,νB=0.5mol·dm-3·s-1,νC=0.5mol·dm-3·s-1,3. ν=kc2A c B三级反应4.9.36 5,75kJ·mol-1 6.k=3×1012s–17.Ea=1.0×105J·mol-1,A=1.1×1013s-18. k=1.2×10-2s–1 9.20% 10.4.69×106倍11. k=4.9×10-4s–112.k1(平均值)=2.15×10-4s–1,t1/2=3223.9s13.(1)v0(蔗糖)=6.43×10-5 mol·dm-3·s-1(2)n(葡萄糖)=n(果糖)=0.128mol(3)α(蔗糖)=0.3214.1.8×10-11 mol·dm-3·s-1 15.4600年31.p总=3.9×104pa2.n(O2)=2.0×10-2mol3.p(N2)=4.6×105pa,P(O2)=105pa5.K =2.0×10-106.K =2.3×10-29,K p=8.9×10-32pa7.(1)△r G(298K)=173.1kJ·mol-1,K =5.01×10-31(2)△r m(298K)=208.4kJ·mol-1,K =3.16×10-37(3)△r G m(298K)= -33.0kJ·mol-1,K =6.03×1058.(1)△r G(298K.15K)=37kJ·mol-1,K =3.3×10-7(2)K (800K)≈1.4×1039. K (500K)=1.47×101010.K2×104,△r G m(292K)= -27.2kJ·mol-111.△r m(298K)=86.55kJ·mol-1,K(298K)=6.8×10-16△r(1 573K)≈70.7kJ·mol-1,K(1 573K)≈4.5×10-312.(1)pH=5.15(2)pH=3.8814. pH= 4.7515. pH=9.25,α=9.0×10-516.(1)1.3×10-5mol·dm-3(2)1.8×10-10mol·dm-317.(1)无沉淀生成(2)c(Cl-)=8.9×10-3mol·dm-3(3)2.2%45.(Ni2+/Ni)= -0.257V6.(1)E,△r G m= -98.4kJ·mol-1,反应能自发。
重庆大学大学化学习题答案

成绩重庆大学大学化学(Ⅱ)期末考试试卷(B)学院___________ 专业___________姓名___________ 学号___________(请考生注意:本试卷共5页)大题一二三四成绩一、对的在题末括号内填“+”、错的填“-”。
(本大题分9小题, 每小题1分, 共9分)1、金属元素与非金属元素之间形成的化学键不一定都是离子键。
答()2、所有电子的电子云都有方向性。
答()3、微细的铝粉、麦面粉、煤粉等与乙醚、丙酮、苯等类似,也属于有火灾爆炸危险性的危险品。
答()4、 r H大,并不预示其反应速率快。
答:()5、由于共价键十分牢固,因而共价化合物的熔点均较高。
答()6、稀有气体固态时,在晶格结点上排列着原子,所以它们的晶体属于原子晶体。
答()7、同一元素的离子半径小于其原子半径。
答()8、碳原子只有两个未成对电子,故只能形成2 个共价键。
答()9、过渡元素在高氧化态时一般均可与活泼非金属形成离子化合物。
答()二、将一个或两个正确答案的代码填入题末的括号内。
若正确答案只有一个,多选时,该题为0分;若正确答案有两个,只选一个且正确,给1分,选两个且都正确给2分,但只要选错一个,该小题就为0分。
(本大题分11小题, 每小题2分, 共22分)1、下列各系统中,具有最大摩尔熵值的是答:()(1) 20 K 时的冰(2) 273.15 K 时的冰(3) 373.15 K 时的水蒸气(4) 400 K 时的水蒸气2、H2分子之间的作用力有答()(1) 氢键(2) 取向力(3) 诱导力(4) 色散力3、在一定条件下,由蔗糖水溶液、冰、水蒸气、氧气、氮气组成的系统中有答()(1) 三个相(2) 四个相(3) 三种组分(4) 四种组分(5) 五种组分4、确定多电子原子中,轨道的能量的是答()(1)n (2)n和l(3)n,l和m (4)n,l,m和m s5氢作为一种很有发展前途的能源,下列各项中尚需研究解决的有答()(1) H2是一种没有污染的能源(2) 用水制氢资源丰富(3) H2的运输方便、安全(4) H2的燃烧热值大(5) 价廉的制氢方法和技术6、下列有机高聚物中电绝缘性最好的是答:()(1) 酚醛树脂(2) 聚氯乙烯(3) 聚四氟乙烯(4) 聚酰胺7、下列有机高聚物中,最适宜作粘结剂,且使用范围最广的粘结剂是答:()(1) 聚碳酸酯(2) 聚甲基丙烯酸甲酯(3) 环氧树脂(4) 酚醛树脂8、在由气体A 与B 组成的混合气体中,组分A 的分压力与总压力之比等于答:()(1) A 组分的摩尔分数(2) A 组分的分体积与总体积之比(3) B 组分的分压力与总压力之比 (4) A 组分与 B 组分的分体积之比9、在一定温度和压力下,已知有一气态化合物分解只产生两种气态物质:单质磷蒸气和氢气。
大学有机化学答案全
a
8
第四章 习题参考答案
1. (1) 1,1-二甲基-2-异丙基环丙烷 (2) 5-甲基螺[2,4]庚烷
2.
(3) 2-甲基-3-环丙基丁烷
(4) 1-甲基-3-乙基环己烷
3.
(5) 2-硝基苯磺酸
(6) 1,7-二甲基萘
4.
(7) 双环[3,2,1]辛烷
(8) 1-甲基-1,3-环戊二烯
5.
(9) 4-硝基-2-氯甲苯
11、12 略。 13. A 为:
有旋光活性。
B为:
a
27
14. A:
C: 15. I :
II :
B:
a
28
第八章 醇、酚、醚 习题参考答案
1. (1) 3,3-二甲基-1-丁醇
(2) E(顺)-3-甲基-3-戊烯-1-醇
2. (3) 1,5-己二烯-3,4-二醇 (4) 5-甲基-2-己醇
3. (5) 3 - (间) 羟基苯磺酸
反应式如下:
另一组答案为: A.
B.H 3 CC2H C2H C2 B Hr
C.
H 3CC2HCH C H 2 a
15
10.
氧化后得到的
对称二酮为:
11.
反应式如下:
12.
透视式
a
纽曼式
16
第五章 卤代烃习题参考答案
1. (1) 2-甲基-4-氯戊烷 (3) 4-溴-1-环己烯 (5) 2-氯-4-溴甲苯
(6) 8-甲基-1-萘酚
4. (7) 3 - (间) 甲基苯甲醚
CH3
C. H2C CH C CH2 D.
CH3
H3C
a
22
12.
1.
大学有机化学课后答案
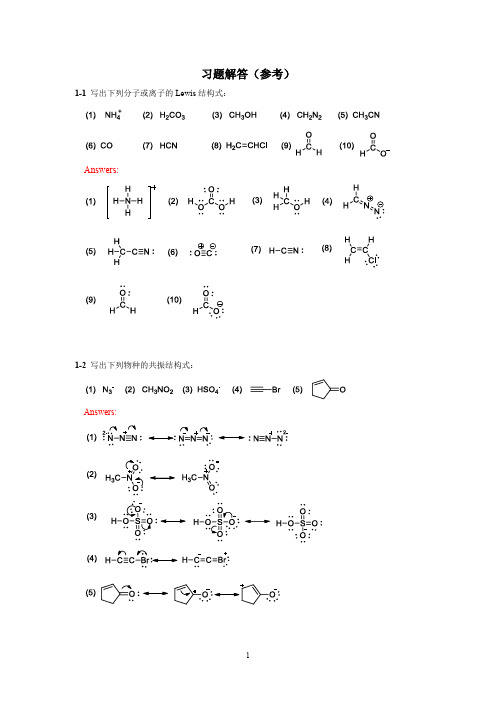
习题解答(参考)1-1 写出下列分子或离子的Lewis结构式:Answers:1-2 写出下列物种的共振结构式:Answers:1-3 下列各组共振结构中哪一个对共振杂化体贡献最大?Answers:(1)a对共振杂化体贡献最大。
因为共振式a所含有的共价键最多,且所有原子均为电中性,能量最低,最稳定。
(2)a对共振杂化体贡献最大。
因为共振式a中含有八隅体结构的原子多,含有的共价键也多,且每个原子均为电中性,因此共振式a结构最稳定。
(3)b对共振杂化体贡献最大。
因为共振式b中含有的共价键多,且碳原子和氧原子均为八隅体结构,更加稳定。
(4)a对共振杂化体贡献最大。
因为共振式a中除了氢原子以外的原子都符合八隅体结构,并且都是电中性,结构稳定。
1-4指出下列各组共振结构中不正确的共振式:Answers:(1)b、c为不正确的共振式。
不同电负性原子形成的双键,其π电子流向电负性较大的原子,因此碳氧双键中的π电子应该流向氧原子。
正确的共振式应该为(2)b、c为不正确的共振式。
由相同电负性原子形成的双键,其 电子流向正电荷。
因此正确的共振式应该为:(3)c为不正确的共振式。
因为所有的共振式结构中未成对的电子数应该相同,但是共振式c中有两个未成对电子,而共振式a、b中没有未成对电子,因此共振式c为错误结构。
(4)d为不正确的共振式。
因为中间的碳原子不符合价键理论,已经超过了四价。
习题解答(参考)2-1 写出分子式为C7H16的所有异构体,并用系统命名法命名。
Answers:正庚烷2-甲基己烷3-甲基己烷2,4-二甲基戊烷2,3-二甲基戊烷3,3-二甲基戊烷2,2-二甲基戊烷3-乙基戊烷2,2,3-三甲基丁烷2-2 用系统命名法命名下列化合物(双键和取代环烷烃的构型用顺/反或Z/E标记):Answers:(1)(E)-3-异丙基-2-辛烯-5-炔(E)-3-isopropyloct-2-en-5-yne(2)(E)-1-氘-3,3-二甲基-2-乙基-1-丁烯(E)-1-D-2-ethyl-3,3-dimethyl-1-butene(3)(Z)-7-甲基-6-乙基-3-辛烯(Z)-6-ethyl-7-methyloct-3-ene(4) 3-甲基环己烯3-methylcyclohex-1-ene(5) 顺-1-甲基-3-乙基环戊烷cis-1-ethyl-3-methylcyclopentane(6) 10,10-二甲基-7-溴-二环[4,3,2]-十一-3-烯7-bromo-10,10-dimethylbicyclo[4.3.2]undec-3-ene(7) 6-甲基-螺[4,5]-癸烷6-methylspiro[4.5]decane(8) 8-溴-螺[2,5]-辛-5-烯8-bromospiro[2.5]oct-5-ene(9) 7-甲基-二环[2,2,1]-庚烷7-methylbicyclo[2.2.1]heptane2-3 写出下列化合物的结构式:(1)反-1-甲基-4-叔丁基环己烷 (2)(2E,4Z)-2,4-庚二烯 (3)3,3-二甲基戊烷 (4)1-庚烯-4-炔(5)2,6-二甲基螺[3.4]辛-5-烯 (6)3,4-二甲基-5-(2-甲基丁基)十二-1-烯(1)(2)(3)(4)(5)(6)3)32-4 将下列化合物的结构式改写出为纽缦投影式,并用纽缦投影式表示每个化合物的优势构象。
大学有机化学总结习题及答案-最全

有机化学总结一.有机化合物的命名1. 能够用系统命名法命名各种类型化合物:包括烷烃,烯烃,炔烃,烯炔,脂环烃(单环脂环烃和多环置换脂环烃中的螺环烃和桥环烃),芳烃,醇,酚,醚,醛,酮,羧酸,羧酸衍生物(酰卤,酸酐,酯,酰胺),多官能团化合物(官能团优先顺序:-COOH >-SO3H >-COOR >-COX >-CN >-CHO >>C =O >-OH(醇)>-OH(酚)>-SH >-NH2>-OR >C =C >-C ≡C ->(-R >-X >-NO2),并能够判断出Z/E 构型和R/S 构型。
2. 根据化合物的系统命名,写出相应的结构式或立体结构式(伞形式,锯架式,纽曼投影式,Fischer 投影式)。
立体结构的表示方法:1)伞形式:CCOOHOHH 3CH2)锯架式:CH 3OHHHOH C 2H 53) 纽曼投影式:HH H HHHHH H HHH 4)菲舍尔投影式:COOH CH 3OHH5)构象(conformation)(1) 乙烷构象:最稳定构象是交叉式,最不稳定构象是重叠式。
(2) 正丁烷构象:最稳定构象是对位交叉式,最不稳定构象是全重叠式。
(3) 环己烷构象:最稳定构象是椅式构象。
一取代环己烷最稳定构象是e 取代的椅 式构象。
多取代环己烷最稳定构象是e 取代最多或大基团处于e 键上的椅式构象。
立体结构的标记方法1.Z/E标记法:在表示烯烃的构型时,如果在次序规则中两个优先的基团在同一侧,为Z构型,在相反侧,为E构型。
CH3C C H ClC2H5CH3C CHC2H5Cl(Z)-3-氯-2-戊烯(E)-3-氯-2-戊烯2、顺/反标记法:在标记烯烃和脂环烃的构型时,如果两个相同的基团在同一侧,则为顺式;在相反侧,则为反式。
CH3C C H CH3HCH3C CHHCH3顺-2-丁烯反-2-丁烯CH3HCH3HCH3HHCH3顺-1,4-二甲基环己烷反-1,4-二甲基环己烷3、R/S标记法:在标记手性分子时,先把与手性碳相连的四个基团按次序规则排序。
大学《有机化学》课后习题答案
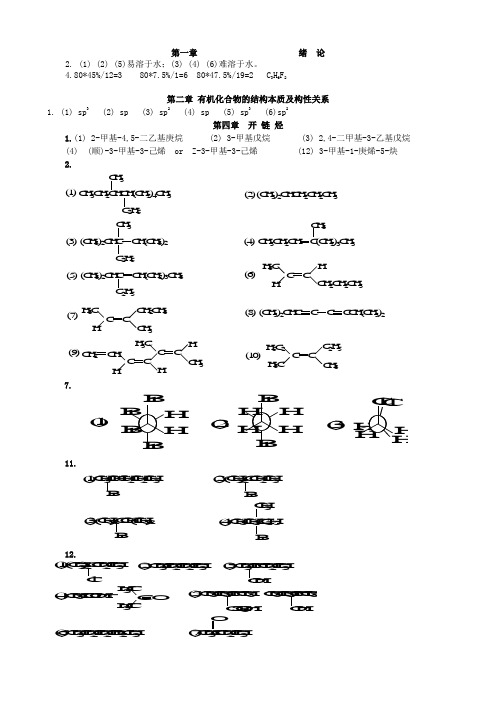
第一章绪论2. (1) (2) (5)易溶于水;(3) (4) (6)难溶于水。
4.80*45%/12=3 80*7.5%/1=6 80*47.5%/19=2 C3H6F2第二章有机化合物的结构本质及构性关系1.(1) sp3 (2) sp (3) sp2 (4) sp (5) sp3 (6)sp2第四章开链烃1.(1) 2-甲基-4,5-二乙基庚烷 (2) 3-甲基戊烷 (3) 2,4-二甲基-3-乙基戊烷(4) (顺)-3-甲基-3-己烯 or Z-3-甲基-3-己烯 (12) 3-甲基-1-庚烯-5-炔2.7.11.12.14. (5) > (3) > (2) > (1) > (4) 即: CH2=CHC +HCH 3 >(CH3)3C + >CH 3CH 2C +HCH 3 >CH 3CH 2CH 2C +H 2> (CH 3)2CHC +H 216. (1)(2)(3)17.21AB.10.(1)CH 3-CH=CH 2−−−−−→−+H /KMnO 4CH 3COOH(2)CH 3-C≡CH+HBr(2mol ) CH 3CBr 2CH 3(3)CH 3-3-C=CH 2−−→−2Br CH 3CBr 2CH 2Br 第四章 环 烃 2.1-戊烯 1-戊炔 戊 烷Br 2/CCl 4室温,避光√ 溴褪色√ 溴褪色× × √灰白色1-丁炔 2-丁炔 丁 烷Br 2/CCl 4 室温,避光√溴褪色 × Ag(NH 3)2+√灰白色↓ × ×1,3-丁二烯 1-己炔 2,3-二甲基丁烷Br 2/CCl 4√ 溴褪色 √ 溴褪色 × Ag(NH 3)2+×√ 灰白色↓C(CH 3)3CH 3(1)(2)(3)3.(1)反式CH 3Br(3)顺式4.C H 3B rC lC l +C l C lC O O HH 3CO 2N (C H 3)3C C O O H(1)(2)(3)(4)(5)(6)(7) B rC 2H 5C 2H 5B r +C H 3C O C H 3(C H 3)2C C H (C H 3)2B r(8) 1molCl 2 / h, 苯/无水AlCl 3N H C O C H 3N O 2C H 3C H 3S O 3H(9) (10)7. (2)有芳香性 10.第六章 旋光异构6-32. (1)× (2)× (3)× (4)√ (5)√ (6)√7.2.66120678.58.18][20+=⨯÷+=⨯=l c Dαα第七章 卤 代 烃2、C l C lC l (2)4、第八章 醇、酚、醚1. (1) 3-甲基-3-戊烯-1-醇 (2) 2-甲基苯酚 (3) 2,5-庚二醇 (4) 4-苯基-2-戊醇 (5) 2-溴-1-丙醇 (6) 1-苯基乙醇(7) 2-硝基-1-萘酚 (8) 3-甲氧基苯甲 (9) 1,2-二乙氧基乙烷(乙二醇二乙醚)(1)(2)3、4. (1) 甲醇 分子间氢键 (6) 邻硝基苯酚 分子内氢键、分子间氢键 5、(1)CH 2IH 3COOH(5)(6)HOOCH 3H(7)6、AgNO 3/乙醇,室温白↓× ×AgNO 3/乙醇,加热白↓×OH+OHBrBr(1)(2)10、OH O ClA B C D第九章醛、酮、醌一、命名下列化合物。
重庆大学大学化学习题答案10和11

第10章习题1.为什么钛被人们称为“空间金属”?钛及钛合金具有哪些重要性质?2.简述稀土元素的基本性质,工业上为什么常用混合稀土?稀土金属应怎样保存?列举稀土金属的用途2~3种。
3.解释下列名词:(1)金属陶瓷(2)硬质合金(3)功能陶瓷(4)超导电性(5)光导纤维(6)纳米材料4.氮化硅可作高温结构陶瓷,请回答氮化硅如何制备,写出反应方程式。
5.采用化学气相沉积法在钢铁表面涂覆碳化钛的反应可简单表示如下:TiCl4(g)+2H2(g)+C(s) = TiC(s)+4HCl(g)已知该反应的△r m(298.15K) < 0,试问单从从热力学角度考虑,欲沉积TiC 时的温度采用高温还是低温有利?为什么?6.从化学结构分析,影响高分子链顺性的因素是哪些?7.排出下列两组高聚物刚性依次增大的顺序,并简要说明其理由。
a. —[CH2—]n—[CH2—CH2—]n—[CH2—CH—]nCH2b. —[CH2—CH—]n—[CH2—CH—]n—[CH2—CH—]nCN CH2 Cl8.作为塑料,其使用的上限温度以什么作为衡量标准?作为橡胶,其使用的下限温度又以什么为衡量的标准?作为合成纤维,其使用的上限温度是多少?9.写出下列物质电绝缘性的大小次序,并扼要说明其理由。
聚四氟乙烯聚氯乙烯聚乙炔10.试计算下列高聚物的平均聚合度n:(1)[NH—(CH2)5CO]n105(2)[OCH2—CH2O—CO]n的平均相对分子质量为10511.排出下列高聚物的T g大小次序,并扼要说明其理由。
CH3CH3 CH3(Si—O—Si—O)n(CH2—CH2)n (O C O—C)n CH3CH3 CH3 O 12.环氧树指胶粘剂为什么要采用固化剂?其固化剂的主要种类有哪些?试举列说明固化反应机理。
13.试述α-氰基丙烯酸酯、厌氧胶、丙烯酸脂乳液胶粘剂的特点和用途。
14.写出下列高聚物的结构式,简述它们的主要性能和用途:(1)ABS (2)聚甲醛(3)丁苯橡胶(4)硅橡胶鞋(5)环氧树酯15.什么是复合材料?复合材料中的基本材料和增强材料分别在其中起什么作用?试以玻璃钢为例说明复合材料的组成及特点。
大学有机化学试题及答案pdf

大学有机化学试题及答案pdf一、选择题(每题2分,共20分)1. 下列哪个化合物不是芳香化合物?A. 苯B. 甲苯C. 环己烷D. 萘2. 碳正离子的稳定性顺序是?A. 3° > 2° > 1°B. 1° > 2° > 3°C. 2° > 3° > 1°D. 3° = 2° = 1°3. 以下哪个反应是亲电加成反应?A. 卤代烃的水解B. 烯烃与溴水反应C. 醇的脱水D. 羧酸与醇的酯化4. 哪个反应是消除反应?A. 醇的氧化B. 醇的脱水C. 醛的还原D. 酯的水解5. 以下哪个是立体异构体?A. 1-丁醇和2-丁醇B. 1,2-二氯乙烷C. 1,1,2-三氯乙烷D. 1,1,1-三氯乙烷...(此处省略其他选择题)二、简答题(每题10分,共20分)1. 简述SN1和SN2反应的区别。
2. 解释什么是共振结构,并给出一个例子。
三、计算题(每题15分,共30分)1. 某化合物的分子式为C3H6O,已知其红外光谱显示有羰基吸收峰,请写出可能的结构式,并计算其分子量。
2. 给定一个醇的分子式C2H6O,如果它发生脱水反应生成一个烯烃,请计算该烯烃的分子式。
四、合成题(每题15分,共15分)1. 给出从苯合成硝基苯的合成路径,并说明每一步反应的条件和机理。
五、实验题(每题15分,共15分)1. 描述如何通过实验鉴别1-丁醇和2-丁醇。
结束语本试题涵盖了大学有机化学的基础知识和应用,旨在检验学生对有机化学概念、反应机理、合成策略以及实验技能的掌握程度。
希望同学们能够通过本试题,加深对有机化学的理解,提高解决实际问题的能力。
答案一、选择题1. C2. A3. B4. B5. D二、简答题1. SN1反应是单分子亲核取代反应,反应速率只与底物浓度有关,而SN2反应是双分子亲核取代反应,反应速率与底物和亲核试剂的浓度都有关。
重庆大学大学化学习题答案
B07003T卷(答案)注:各主观题答案中每步得分是标准得分,实际得分应按下式换算:第步实际得分本题实际得分解答第步标准得分解答总标准得分N=N ⨯一、对的在题末括号内填“+”、错的填“-”。
(本大题分9小题, 每小题1分, 共9分)1、+2、-3、+4、+5、-6、-7、-8、-9、 1 分二、将一个或两个正确答案的代码填入题末的括号内。
若正确答案只有一个,多选时,该题为0分;若正确答案有两个,只选一个且正确,给1分,选两个且都正确给2分,但只要选错一个,该小题就为0分。
(本大题分11小题, 每小题2分, 共22分)1、(4)2、(4)3、(1),(4)4、(2)5、(3)(5)6、(3)7、(3) 8、(1),(2) 9、(4) 10、(3)(4)11、(1)(3)三、填空题。
1、N(氮) 1 分2、小于 1 分3、-1.89×1032分4、Sn Pb Sb Bi 各0.5 分5、太阳光中的大部分紫外线皮肤癌6、C≡C C-C7、I A HCl VII A NaH 0.5 分/ 空8、IV、V、VI 高熔点高硬度 1 分9、(-)Pt|FeCl2(aq),FeCl3(aq)|Cl2(g)|Pt(+) 2 分10、k c(Cl)•c(CH4) 1分二 1 分11、2:1 1 分阳极:H2O12O2↑+2H++2e-(或2OH-12O2↑+H2O+2e-)阴极:2H2O+2e-H2↑+2OH-(或2H++2e-H2↑) 1 分12、苯乙烯或C H2C H丁二烯或CH2=CH-CH=CH2丙烯腈或CH2=CH-CN 加聚13、c(Cu2+)/mol⋅dm-3c(Zn2+)/mol⋅dm-3(1) Zn(s),Cu(s) 均存在~1⨯10-38~0.2(2) 只存在Zn(s),无Cu(s)~1⨯10-38~0.2(3) 只存在Cu(s),无Zn(s)0.1 0.1(4) Zn(s),Cu(s) 不存在0.1 0.10.5 分 / 空 14、(1)MgO>CaO>BaO>NaBr>NaI 2 分(2)Cl>As>Ni>Ca>K 2 分 四、根据题目要求,通过计算解答下列各题。
大一下有机化学课后习题参考答案

第一章绪论习题参考答案1.什么是有机化合物?它有那些特性?有机化合物是指碳氢化合物及其衍生物。
有机化合物的特性:1、数目众多、结构复杂;2、易燃;3、熔沸点较低3、难溶于水,易溶于有机溶剂;4.反应慢、副反应多。
2.什么是σ键和π键?沿着轨道对称轴方向重叠形成的键叫σ键。
其特点为电子云可以达到最大程度的重叠,所以比较牢固。
另外σ键旋转时不会破坏电子云的重叠,所以σ键可以沿对称轴自由旋转。
P轨道“肩并肩”平行重叠形成的共价键叫π键,其特点为电子云重叠程度小,键能低;电子云分布呈块状分布于σ键所在平面的上下,受核的束缚小,易受极化;成键的两个原子不能沿键轴自由旋转。
3.指出下列化合物所含的官能团名称:(1) (2) (3) (4) (5)NO2CH3CH3H3C CCH3CH3CH2ClOH苯环、硝基苯环卤代烃酚环烯 (6) (7) (8) (9)O CHO NH2OH环酮环醛苯环、胺环、醇4.根据键能的数据,当乙烷分子受热裂解时,那一个共价键首先破裂?为什么?这个过程是吸热还是放热?乙烷分子受热裂解时,分子中的碳碳首先破裂,因为C—C键能为376 KJ·mol-1,而C —H键能为439 KJ·mol-1。
这个过程是吸热。
5.指出下列各化合物分子中碳原子的杂化状态:(1)(2)(3)H3C CH CHCHO sp3sp2sp2sp2CH3sp3CH CH2sp2sp2苯环上的碳原子是sp2 杂化环己烷上的碳原子是sp3杂化(4)(5)(6)HC CCH2CH CH2sp3sp sp sp2sp2H2C C CHCH3sp2sp sp2sp3H3C COOHsp3sp2第二章烷烃习题参考答案1.解:(1)CH3CH2CHCH2CH2CH2CH3CH2CH3(2)CH3CCH2CHCH3CH3CH3CH3(3)CH3CH2CH2CHCHCH2CH2CH3CH3CH2CH3(4)CH3CH2CCHCHCH2CH2CH3CH2CH3CH(CH3)2H3CCH2CH2CH32.解:(1) 2,3-二甲基辛烷(2) 2,7-二甲基-4-乙基壬烷 (3) 3,6-二甲基壬烷 3.解:(1)C CH 3CH 3H 3C CH 3(2) CH 3CHCH 2CH 3CH 3(3)CH 3CH 2CH 2CH 2CH 34.解:(1)CH 3CH 2CH 2CH 2CH(CH 3)2,(CH 3)2CHCH 2CH(CH 3)2,CH 3CH 2CHCHCH 3CH 3CH 3,H 3C C HC CH 3H 3H 3CCH 3(2)CH 3CH 2CH 2CHCH 3CH 3,CH 3CH 2CHCH 2CH 3CH 3(3)H 3C C HC CH 3H 3C H 3CCH 35.解:(1)CH 2CH 2CH 3,CH 2CH 2CH 3( 正戊烷绕C 1-C 2σ键旋转产生的交叉式和重叠式构象)(2)C 2H 5H 3C ,C 2H 5CH 3,C 2H 5CH3,C 2H 5CH 3(正戊烷绕C 2-C 3σ键旋转产生的全重叠式、邻位交叉式、部分重叠式、对位交叉式构象)(3)CH 3C 2H 5,CH 3C 2H 5(异戊烷绕C 1-C 2σ键旋转产生的交叉式和重叠式构象) (4)H 3CCH 3CH 3H 3C CH 3CH 3H 3C CH 3H 3CH 3CCH 3CH 3(异戊烷绕C 2-C 3σ键旋转产生的全重叠式、邻位交叉式、部分重叠式、对位交叉式构象) (5)CH(CH 3)2CH(CH 3)2(异戊烷绕C 3-C 4σ键旋转产生的交叉式和重叠式构象)(6)H 3CCH 3H 3CCH 3CH 3H 3C(新戊烷绕C 1-C 2σ键旋转产生的交叉式和重叠式构象) 6.解:(3)>(2)>(4)>(1) 7.解:1°H =12;2°H =0;3°H =0 8.解:FF FF9.解:CH 310.解: 链引发:Cl 2hvCl ·+Cl ·链增长:Cl ·+CH 3CHCH 3CH 2·+HCl Cl 2+CH 3CH 2Cl ·+CH 3CH 2Cl 链终止:Cl ·+Cl Cl 2 Cl ·+CH 3CH 2·CH 3CH 2Cl CH 3CH 2·+CH 3CH 2·CH 3CH 2CH 2CH 3第三章 烯烃 炔烃 二烯烃习题参考答案1. (1)5–甲基–1–己烯 (2)3–甲基–1–丁炔 (3)4–甲基–1,3–戊二烯(4)2,7–二甲基–2,7–壬二烯 (5)3–乙基–4–己烯–1–炔(6)5–甲基–1,3–环己二烯 (7)( Z )–3–甲基 –3–庚烯 (8)顺,反–2,4–庚二烯(或(2Z,4E )–2,4–庚二烯) 2.CH 3C H CCH(CH 3)2HH 3CH C3)CH 2CH 3CH 3CCl Br C CH 2CH 2CH 3HClHC C C(CH 3)2CH 2CH 2CH 3CH CHH 2C C 2H 5C CH(1)(2)(3)(4)(5)(6)3.(1)(2)(3)(4)(5)(6)(7)(8)CH 3CH 3CH 2CH 2COOH + CO 2CH 3CCH 2CH 2CH 3CH 3BrCH 2ClCH 2CF 3CH 3CH CH 3SO 3HCH 3CH CH 3OH COOC 2H 5COOC 2H 5CH 3CH 2CH 2CH 2BrCH 3CH 2CHCCH 3OCuCCCH 34.答案不唯一,只要方法可行都可以。
2024年重庆市高考化学有机题答案解析

2024年重庆市高考化学有机题答案解析高考化学中的有机题,一直以来都是许多考生感到棘手的部分。
2024 年重庆市高考化学的有机题,更是对考生们的知识掌握、思维能力和解题技巧进行了全面的考查。
下面我们就来对这些题目进行详细的答案解析。
首先来看第一题,题目给出了一种有机化合物的结构简式,要求判断其可能的化学性质。
从给出的结构可以看出,存在着多个官能团,比如羟基、羧基等。
羟基具有一定的还原性,可以被氧化剂氧化;羧基则具有酸性,能够与碱发生中和反应。
同时,由于分子中存在不饱和键,还可能发生加成反应。
所以,这道题的答案应该是综合考虑这些官能团的性质得出的。
接下来的第二题,是关于有机反应类型的判断。
题目描述了一个有机反应的过程,让考生判断属于哪种反应类型。
这就需要考生对常见的有机反应类型,如取代反应、加成反应、消去反应、氧化反应等有清晰的认识。
比如说,如果反应中是一个原子或基团被另一个原子或基团所替代,那就是取代反应;如果是双键或三键打开,与其他物质结合,就是加成反应。
通过仔细分析题目中反应物和生成物的结构变化,就能准确判断出反应类型。
再看第三题,是关于有机物同分异构体的书写。
这道题的难度相对较大,需要考生充分理解同分异构体的概念,即具有相同分子式但结构不同的化合物。
在书写时,要注意按照一定的顺序和规律,比如先考虑碳链异构,再考虑官能团的位置异构和类别异构。
同时,要注意避免重复和遗漏。
第四题是关于有机合成路线的设计。
这不仅考查了考生对有机反应的掌握,还考查了他们的创新思维和综合运用知识的能力。
在设计合成路线时,要从最终的目标产物出发,逆向推导,选择合适的起始原料和反应步骤。
每一步反应都要符合有机化学的基本原理和反应条件。
比如说,要合成一种含有特定官能团的有机物,可以先分析该官能团可以通过哪些反应引入,然后再根据题目给出的条件和原料,选择最优的合成路线。
同时,还要考虑反应的可行性、产率等实际问题。
第五题考查了有机物的分离和提纯方法。
重庆大学大学化学习题答案12

第12章习题
1.简要说明气相色谱分析的分离原理。
2.气相色谱仪的基本设备包括哪几部分?各有什么作用?
3.原子发射光谱定性分析、定量分析的基本原理是什么?
4.原子吸收光谱仪的主要组成部分有哪些?简要说明原子吸收光谱产生的原理。
5.在分子光谱中电子跃迁有哪几种类型?哪些类型的跃迁能在紫外及可见光区吸收光谱中反映出来?
6.举例说明紫外吸收光谱在分析上有哪些应用?
7.红外光谱定性分析的基本依据是什么?
8.何谓化学位移?它有什么重要性?
9.在CH3—CH2—COOH的核磁共振谱图中可观察到其中有四重峰及三重峰各一组:
(1)说明这些峰产生的原因;
(2)哪一组峰处于较低场?
10.有机化合物在离子源中有可能形成哪些类型的离子?从这些离子的质谱峰中可以得到一些什么信息?。
重庆大学大学化学习题答案2

第2章 习 题1.设反应A+3B →3C在某瞬间时c (C )=3mol ·dm -3,经过2s 时c (C )=6mol ·dm -3,问在2s 内,分别以A ,B 和C 表示的反应速率υA ,υB ,υC 各为多少?2.下列反应为基元反应(1)I+H →HI (2)I 2→2I (3)Cl+CH 4→CH 3+HCl写出上述各反应的质量作用定律表达式。
它们的反应级数各为多少?3.设反应aA+bB →C恒温下,当c A 恒定时,若将c B 增大的原来的二倍,测得其反应速率亦增大为原来的二倍;当c B 恒定时,若将c A 增大为原来的二倍,测得其反应速率原来的四倍。
试写出此反应的速率方程式,它是几级反应?4.根据实验结果,在高温时焦炭与二氧化碳的反应为:C(s)+CO 2(g)═2CO(g)其活化能为167360J ·mol -1,计算自900K 升高到1000K 时,反应速率之比。
5.在301K 时鲜牛奶大约4.0h 变酸,但在278K 的冰箱中可保持48h 。
假定反应速率与变酸时间成反比,求牛奶变酸反应的活化能。
6.已知反应N 2O 4(g)→2NO 2(g )的指数前因子A=1×1022s -1,活化能E a =5.44×104J ·mol -1,求此反应在298K 时的k 值是多少?7. 反应252421N O ()N O ()O ()2g g g →+在298K 时k 1=3.4×10-5s -1,在328K 时k 2=1.5×10-3s -1,求此反应的活化能E a 和指数前因子A 。
8. 对下列反应2524C H Cl()C H ()HCl()g g g →+已知其活化能E a =246.9kJ ·mol -1,700K 时的速率常数k 1=5.9×10-5s -1,求800K 时的速率常数k 2是多少?9. 人体中某种酶的催化反应的活化能为50kJ ·mol -1,正常人的体温为310K (37︒C)。
《有机化学》习题答案

第一章 习题参考答案 1-1 略 1-2C O H H H C OH H H (1)(2)H(3)sp 3sp 3 sp 2C NH H H C C H H H ⋯⋯N (4)(5)C C HHH ⋯⋯N O sp 3 sp 3sp sp 3 sp1-3 C 18H 11NO 21-4 (A): c < b < a; (B): c < b < a; (C): b < a < c1-5有机化合物氧原子具有未共享电子对,表现为碱,与质子结合,从而溶于冷的浓硫酸。
加水稀释后,释放出硫酸,又得到原来的化合物。
以乙醚为例:+ H 2SO 4O + HSO 4H+ HSO 4HO+ H 2SO 41-6 (1) CH 3CH 2OH (2) CH 3CH 2O - (3) CH 3CH 2S - (4) HCOO -(5)H 2PO 4-(6) I -(7) (CH 3)2N -(8) HO -(9) H 2O (10) NH 31-7 写出下列碱的共轭酸。
(1) O H(2) HF (3) C 2H 5OH(4) H 3O + (5) (CH 3)2NH 2+1-8 Lewis 酸BF 3,ZnCl 2,AlCl 3; Lewis 碱CH 3CH 2OH ,CH 3CH 2OCH 2CH 3,NH 3,H-C ≡C -,C 2H 5O -,CH 3SCH 3,H 2C =CH 2 1-9 A: CHCl 3 > CH 2Cl 2 > CH 3Cl > CCl 4HCl H HHCl Cl H HCl HCl B:<<1-10N ON OOS OS ON OON OON OO第二章 习题参考答案 2-1(1)3-甲基-4-乙基庚烷;(2)2-甲基-4-异丙基己烷;(3)新壬烷;(4)2-甲基-5-乙基庚烷 (5)4-异丙基庚烷;(6)4-叔丁基辛烷;2-2 (1)(2)CH 3CHCHCH 3H 3CCH 3C CH 2CH 3CH 3CH 3H 3C (3)CH 3CHCH2CH 2CH 3CH32-3(1)庚烷(2)2-甲基己烷(3)(4)(5)(6)(7)(8)(9)3-甲基己烷2, 2-二甲基戊烷3, 3-二甲基戊烷2, 3-二甲基戊烷2, 4-二甲基戊烷3-乙基戊烷2, 2, 3-三甲基丁烷2-4CH 3—C —CH 2—CH —CH 2—CH 3CH 3CH 3CH 31°2°3°2°4°1°1°1°1°2-5 该化合物分子式为C 8H 18,结构式 命名为:2,2,3,3-四甲基丁烷 2-6 化合物沸点依次降低顺序:(4)>(2)>(3)>(5)>(1)H 3CH 3CC C CH 3CH 3H3CCH 3(7) (CH 3)2CHCH 2CH 3(8) (CH 3)2CHCHCH 2CH 2 CCH 2CH 3CH 2CH 3CH 3CH 2CH 3(9)(10)2-7 熔点:(1)>(2);沸点:(1)<(2) 2-8 稳定性大小:(1)>(3)>(2)>(4)2-9 1,2-二溴乙烷的四种典型构象式(从左到右稳定性依次降低)H HBr H H BrH H Br H HBrH H H HHHBr HBrH BrBr对位交叉式邻位交叉式 部分重叠式 全重叠式3, 4-二甲基己烷的优势构象为:2-10链引发:Cl 22Cl ∙链增长:Cl ∙+Cl∙+ HCl∙+ Cl 2Cl ∙+链终止:Cl ∙Cl ∙+Cl 2∙Cl ∙+Cl∙+∙2-11 主要的原因是:甲基环己烷分子结构中有1个3º H ,10个2º H ,3个1º H ,进行溴代CH 3Br25反应时,不同类型氢原子的反应活性大小是3º H ∶2º H ∶1º H = 1600∶82∶1,可以初步计算出3º H 被溴取代后的产物所占百分比例大约是66%,因此反应主要得到 2-13 该化合物为: Cl 2++ HClC C H 3C H 3C H 3C CH 3CH 3CH 3C C H 3C H 3C H 3C CH 3CH 3CH 2Cl第三章 习题参考答案 3-1(1)甲基环戊烷 (2)1-甲基-4-乙基环己烷 (3)2-甲基-3-环丙基-6-环丁基辛烷 (4)反-1-甲基-2-异丙基环丁烷 (5)1-甲基-3-环戊基环己烷 (6)2-甲基-8-乙基螺[4.5]癸烷 (7)2, 7, 7-三甲基二环[4.1.0]庚烷 (8)二环[3.3.3]十一烷(9)1-甲基二环[2.2.2]辛烷(10) (11) (12) (13)3-2 该烃分子可能为下列化合物之一:甲基环己烷 乙基环戊烷 丙基环丁烷 丁基环丙烷 3-3(1)2) H 2OBrBr CH 2BrOHC C H 3C H 3C H 3C CH 3CH 3CH 3(2)HBrBr3-4顺-1-甲基-4-丙基环己烷的椅式构象式 反-1-甲基-4-丙基环己烷的椅式构象式CH 3C(CH 3)3H 3CC(CH 3)3CH 3C(CH 3)3C(CH 3)3CH 3最优势构象 3-5(1)CH 3H 3CC(CH 3)3(2) CH 32H 5CH 3(3)CH 3(4) C(CH 3)3C 2H 5(5)C 2H 5C 2H 5H 5C 23-6 3, 4-二溴-1-叔丁基环己烷可能的构象异构体如下:C(CH 3)3C(CH 3)3Br BrC(CH 3)3BrBr C(CH 3)3BrBrC(CH 3)3Br BrBrBr C(CH 3)3BrBrC(CH 3)3BrBrC(CH 3)3BrBr3-7 化合物A 是: 化合物B 是: Br反应式:溴水褪色BrCH2BrBr3-8褪 色褪 色无变化KMnO 溶液无变化褪 色3-9 反-1,2-二甲基环己烷采用ee 构象时,亚甲基和甲基是处在对位交叉式,分子内能较小;而在aa 构象中,亚甲基和甲基是处在邻位交叉式,分子扭转张力相对比较大,同时由于1,3-竖键作用,空间张力大。
有机化学课后习题参考答案(全)

第一章绪论 (1)第二章饱和烃 (3)第三章不饱和烃 (7)第四章环烃 (14)第五章旋光异构 (22)第六章卤代烃 (27)第七章波谱分析 (33)第八章醇酚醚 (34)第九章醛、酮、醌 (41)第十章羧酸及其衍生物 (50)第十一章取代酸 (58)第十二种含氮化合物 (65)第十三章含硫和含磷有机化合物 (72)第十四章碳水化合物 (74)第十五章氨基酸、多肽与蛋白质 (78)第十六章类脂化合物 (82)第十七章杂环化合物 (88)第一章绪论1.1 扼要归纳典型的以离子键形成的化合物与以共价键形成的化合物的物理性质。
1.2是否相同?如将CH4 及CCl4各1mol混在一起,与CHCl3及CH3Cl各1mol的混合物是否相同?为什么?答案:NaCl与KBr各1mol与NaBr及KCl各1mol溶于水中所得溶液相同。
因为两者溶液中均为Na+ , K+ , Br-, Cl-离子各1mol。
由于CH4 与CCl4及CHCl3与CH3Cl在水中是以分子状态存在,所以是两组不同的混合物。
1.3 碳原子核外及氢原子核外各有几个电子?它们是怎样分布的?画出它们的轨道形状。
当四个氢原子与一个碳原子结合成甲烷(CH4)时,碳原子核外有几个电子是用来与氢成键的?画出它们的轨道形状及甲烷分子的形状。
答案:C+624HCCH 4中C 中有4个电子与氢成键为SP 3杂化轨道,正四面体结构CH 4SP 3杂化2p y2p z2p x2sH1.4 写出下列化合物的Lewis 电子式。
a. C 2H 4b. CH 3Clc. NH 3d. H 2Se. HNO 3f. HCHOg. H 3PO 4h. C 2H 6i. C 2H 2j. H 2SO 4答案:a.C C H H H HCC HH HH或 b.H C H c.H N HHd.H S He.H O NO f.O C H Hg.O P O O H H Hh.H C C HHH H HO P O O H HH或i.H C C Hj.O S O HH OO H H或1.5 下列各化合物哪个有偶极矩?画出其方向。
重庆大学食品专业大一《有机化学》考试A卷及答案
有机化学试卷A适用专业 考试日期:试卷所需时间:120分钟 闭卷 试卷总分 :100分一、 命名下列化合物或根据名称写出结构式(每题1.5分,共15分)1.COOH2.CH 3CH 2CHCHCH 2CH 3CH 3CH 33. CH 3CH 2CH 2CH 2Cl4.5.CH 3CH 2OHCH 3H6.N(CH 3)27. CCCH 2CH 2CH 3CH 3CH 28. 苦味酸9. α-呋喃甲醛 10. 反-1-甲基-2-异丙基环己烷的优势构象二、 单项选择题(每题2分,共24分)1、按“次序规则” ,最优先的基团是:( )A .-CNB .-COOHC .-BrD .-NO 2 2、最难发生醇解反应的是:( )A. 乙酰胺B. 乙酸酐C. 乙酰氯D. 乙酸乙酯 3、下列化合物中存在顺反异构体的是:( ) A .2-甲基-1-丁烯 B .2-甲基-2-丁烯C .2-甲基-2-戊烯D .3-甲基-3-己烯 4、下列化合物能使溴水褪色的是:( )A .B .C .D .CH 35、下列化合物加入 Ag(NH 3)2+ 有白色沉淀的是:( )A .CH 3C≡CCH 3B .CH 2=CH -CH =CH 2C .(CH 3)2CHC≡CHD .6、下列关于S N 2 反应的特点说法不正确的是( ) A 、反应经过过度态中间体 B 、反应产物构型转化C 、反应速率与Nu -及RX 浓度有关D 、反应分两步进行 7、下列化合物沸点最高的是:( )A .乙醛B .乙醇C .乙醚D .乙烷 8、下列化合物在水溶液中碱性最强的是:( )A .(CH 3CH 2)3NB .(CH 3CH 2)2NHC .CH 3CH 2NH 2D .NH 39、确定油脂不饱和度通常用:( )A .酸值B .皂化值C .碘值D .PI 值 10、下列化合物没有芳香性的是( )A 、B 、C 、ND 、11、能与 FeCl 3 溶液发生显色反应的是:( )院系: 专业班级: 姓名: 学号: 装 订 线A .苯甲酸B .苯酚C .丙酮D .环己醇 12、互为对映体的是:( )A .D -葡萄糖和L -葡萄糖B .D -葡萄糖和D -果糖C .甘油醛和甘油酮三、 完成下列反应方程式(每空2分,共20分)C H ≡CCH 2CH 3 + H 2O H 2SO 4Hg1.?NCONH 2Br 2/OH-2.??3.CH 2CH 3+Br 2?4.+CH 3CH=CH2ALCl 3KMnO 4+?5.OCH 3+HI(过量)?6.24200℃CH 3OH?7.CHO +HCHO浓 NaOH?8.+ONH 2(过量)CH 3CCl?9.CH 3CH 2COCH 3I 2?10.COOH COOH COOH△-CO 2四、 用化学方法鉴别下列化合物:(每题5分,共10分)1.CH 2CH 3CH=CH 2C ≡CH C(CH 3)32. 丙酮、乙醛、苯酚、异丙醇五、用指定的原料和必要的无机试剂合成下列化合物:(共17分)1.由苯合成1,3,5-三溴苯(10分)2.由乙烯合成正丁醇(7分)六、推断题:( 14分)1.某化合物A(C5H12O)经酸性KMnO4氧化后得到B(C5H10O),B能与苯肼反应,并与碘的碱溶液共热时有黄色沉淀产生。
重庆大学有机化学习题答案

习题答案第一章1.(1)有机化合物:含碳化合物(一氧化碳、二氧化碳、碳酸盐、金属碳化物等少数简单含碳化合物除外)或碳氢化合物及其衍生物的总称。
有机物是生命产生的物质基础。
(2)共价键:共价键(covalent bond)是化学键的一种,两个或多个原子共同使用它们的外层电子,在理想情况下达到电子饱和的状态,由此组成比较稳定的化学结构叫做共价键。
(3)同分异构:同分异构是一种有相同化学式,有同样的化学键而有不同的原子排列的化合物的现象。
(4)杂化:在形成多原子分子的过程中,中心原子的若干能量相近的原子轨道重新组合,形成一组新的轨道,这个过程叫做轨道的杂化。
(5)偶极矩:正、负电荷中心间的距离r和电荷中心所带电量q的乘积,叫做偶极矩μ=r×q。
它是一个矢量,方向规定为从负电荷中心指向正电荷中心。
(6)诱导效应:诱导效应是指在有机分子中引入一原子或基团后,使分子中成键电子云密度分布发生变化,从而使化学键发生极化的现象,称为诱导效应(Inductive Effects)。
(7)异裂:共价键断裂时,共用电子对完全转移给成键原子中的某个原子,形成了正、负离子,这种断键方式称为异裂。
(8)范德华力:在化学中通常指分子之间的作用力。
(9)键角:分子中和两个相邻化学键之间的夹角。
(10)Lewis酸:路易斯酸(Lewis Acid,LA)是指电子接受体,可看作形成配位键的中心体。
(11)疏水作用:非极性分子间或分子的非极性基团间的吸引力。
导致这些基团在水性环境中的缔合。
(12)官能团:决定有机物性质的原子或原子团称为官能团。
2.(1)(2)(3)(4)(5)(6)(7)(8)(9)3.具有偶极的分子:(1)两H原子中心指向O原子方向;(2)又H原子指向Br原子;(4)H原子指向三个Cl原子的中心方向;(5)乙基指向羟基方向4.(1)正庚烷;(2)异丁烷;(3)异己烷;(4)新戊烷5.(1)(2)(3)(4)6.酸:Cu2+ FeCl3 CH3CN碱:NH3 CH3NH2 C2H5OC2H5加合物:CH3COOH CH3OH7.(1)CH3COOH/CH3COO-H3O+/ H2O(2)H2SO4/HSO4-CH3OH2+/CH3OH(3)HNO3/NO3-(CH3)3NH+/(CH3)3N8.(3) CH3Cl > (2) CH3F >(4)CH3Br >(5)CH3I > (1) CH49. 单键最长,双键次之,叁键最短.单键中两个原子间的电子云密度小,叁键两个原子间的电子云密度最大,共同的电子把两个原子吸引得最近.所以说,叁键最短,单键最长,双键处于中间. 10.C5H12O11. C 8H 10N 4O 2第二章1. ⑶>⑵>⑴>⑸>⑷3. 2-甲基丁烷较稳定的构象是:3H 33CH3CH 3⑴⑵⑶其中⑴和⑵更稳定。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
习题答案第一章1.(1)有机化合物:含碳化合物(一氧化碳、二氧化碳、碳酸盐、金属碳化物等少数简单含碳化合物除外)或碳氢化合物及其衍生物的总称。
有机物是生命产生的物质基础。
(2)共价键:共价键(covalent bond)是化学键的一种,两个或多个原子共同使用它们的外层电子,在理想情况下达到电子饱和的状态,由此组成比较稳定的化学结构叫做共价键。
(3)同分异构:同分异构是一种有相同化学式,有同样的化学键而有不同的原子排列的化合物的现象。
(4)杂化:在形成多原子分子的过程中,中心原子的若干能量相近的原子轨道重新组合,形成一组新的轨道,这个过程叫做轨道的杂化。
(5)偶极矩:正、负电荷中心间的距离r和电荷中心所带电量q的乘积,叫做偶极矩μ=r×q。
它是一个矢量,方向规定为从负电荷中心指向正电荷中心。
(6)诱导效应:诱导效应是指在有机分子中引入一原子或基团后,使分子中成键电子云密度分布发生变化,从而使化学键发生极化的现象,称为诱导效应(Inductive Effects)。
(7)异裂:共价键断裂时,共用电子对完全转移给成键原子中的某个原子,形成了正、负离子,这种断键方式称为异裂。
(8)德华力:在化学常指分子之间的作用力。
(9)键角:分子中和两个相邻化学键之间的夹角。
(10)Lewis酸:路易斯酸(Lewis Acid,LA)是指电子接受体,可看作形成配位键的中心体。
(11)疏水作用:非极性分子间或分子的非极性基团间的吸引力。
导致这些基团在水性环境中的缔合。
(12)官能团:决定有机物性质的原子或原子团称为官能团。
2.(1)(2)(3)(4)(5)(6)(7)(8)(9)3.具有偶极的分子:(1)两H原子中心指向O原子方向;(2)又H原子指向Br原子;(4)H原子指向三个Cl原子的中心方向;(5)乙基指向羟基方向4.(1)正庚烷;(2)异丁烷;(3)异己烷;(4)新戊烷5.(1)(2)(3)(4)6.酸:Cu2+ FeCl3 CH3CN碱:NH3 CH3NH2 C2H5OC2H5加合物:CH3COOH CH3OH7.(1)CH3COOH/CH3COO-H3O+/ H2O(2)H2SO4/HSO4-CH3OH2+/CH3OH(3)HNO3/NO3-(CH3)3NH+/(CH3)3N8.(3) CH3Cl > (2) CH3F >(4)CH3Br >(5)CH3I > (1) CH49. 单键最长,双键次之,叁键最短.单键中两个原子间的电子云密度小,叁键两个原子间的电子云密度最大,共同的电子把两个原子吸引得最近.所以说,叁键最短,单键最长,双键处于中间.10.C5H12O11.C8H10N4O2第二章1. ⑶>⑵>⑴>⑸>⑷3. 2-甲基丁烷较稳定的构象是:3H 33CH3CH 3⑴⑵⑶其中⑴和⑵更稳定。
7.⑵>⑴>⑷>⑶8.⑴ 7,7-二甲基三环[2.2.1.02,6]庚烷 ⑵三环[3.3.1.13,7]癸烷11. 该烷烃的分子式为C8H18。
由于只能生成一种一氯产物,说明该烷烃中的18个氢原子是等性的,其结构式为:(CH3)3C—C(CH3)312. 2-甲基-1-溴丙烷的含量为0.6%,2-甲基-2-溴丙烷的含量为99.4%。
第三章2. ⑶、⑷为共轭化合物;⑴、⑶、⑷有顺反异构。
3.⑴E型⑵E型⑶Z型⑷E型4.⑴熔点:顺-2-丁烯>反-2-丁烯,因为顺式的偶极矩大;沸点:反式>顺式,因为反式的对称性好,分子排列紧密。
⑵熔点:2-丁炔>1-丁炔,因为2-丁炔对称性好,分子排列紧密。
沸点:2-丁炔>1-丁炔,因为末端炔烃具有较低的沸点。
5.7.生成的主要产物是4-甲基-3-溴环戊烯。
反应机理为自由基取代历程(略)。
10.⑴第一步用顺丁烯二酸酐检验,有沉淀生成者为1,3-丁二烯;第二步用溴水检验,不褪色者为丁烷;第三步用酸性高锰酸钾溶液检验,褪色者为1-丁烯;余者为甲基环丙烷。
⑵ 第一步用硝酸银的氨溶液或氯化亚铜的氨溶液检验,有沉淀者为1-戊炔;第二步用溴水检验,不褪色者为环戊烷;第三步用酸性高锰酸钾溶液检验,褪色者为环戊烯。
余者为乙基环丙烷。
11. ⑴ p-π共轭,σ-p 共轭 ⑵ p-π共轭,σ-π共轭⑶ p-π共轭 ⑷ π-π共轭,p-π共轭,σ-p 共轭13. ⑶>⑴>⑵+⑵2HO+-H +15. ⑴ 后一个式子是错误的,原子排列顺序发生改变。
⑵ 后一个式子是错误的,它的未成对电子数目不对。
⑶ 正确。
⑷ 两个式子间不是单纯的电子转移,原子位置发生了改变。
17. A.环丁烷 B.甲基环丙烷 C.1-丁烯 D.2-甲基丙烯 E、F为顺式和反式2-丁烯第四章⑴⑵⑶⑷⑸⑹CH 2Br CH 3HOBr Br BrC CH F1.CH 3Br ClCH 3BrClCH 3ClBrCH 3Cl BrCH 3ClBr2.CH 3ClCH 3BrClCH 3Cl BrCH 3BrClCH 3Cl BrBr3. ⑴ 对叔丁基甲苯 ⑵ 2-硝基-4-氯甲苯 ⑶ 对乙烯基苯甲酸 ⑷ 2,4,6-三硝基甲苯 ⑸ 2-甲基-3-苯基丁烷⑼⑺⑴⑵⑷⑸⑹CHClCH 3⑶⑻COCH 2CH 2CH 2ClCH 3CH(CH 3)2COCH 2CH 2COOH CH 2CH 3ClCH 2CH 3Cl+4.COOH5.CH 2+CH 2+CH 2+CH 2+6. ⑵和⑺322233⑴⑷⑹⑻7.CH 3H +H 3C CH 3Ph CH 3H 33CH 3H 3C PhCH 3+H +8.⑴+++⑵CH 3CH 2COClCH 2CH 2AlCl 3OCH3CH 3O CH 3OCH 2CH 3OH⑴⑵⑶⑷D >E >A >B >C B >D >E >A >C C >A >D >BC >D >B >A9.⑺⑴⑵⑷⑸⑹⑶⑻及其对映体10.11.⑴ 3,6-二甲基-2硝基萘 ⑵ 9,10-二溴菲CH 2C OCOCH 3⑹⑴⑵⑷⑸⑶NO 2OHC O NHNO 2CH 312.NO 2SO 3HBrBrNO 2SO 3H SO 3H +13. 四甲基苯的异构体有:⑴⑵⑶CH 3CH 3CH 3CH 3CH 3CH 3CH CH 3CH 3CH CH 3CH 3其中⑶的对称性最好,熔点最高。
A. B. C.14.CH 3CHCH 3CH 3HOOCCOOHHOOCCOOHNO 2反应式略。
15.⑴⑵CH 3⑶253HNO 3Cl 2NaOH醇浓 H 2SO 42H + / H 2O +2 H 2SO 4HNO 32416. ⑴ 有 ⑵ 无 ⑶ 无 ⑷ 无 ⑸有 ⑹有OH(Ⅰ)(Ⅱ)17.第五章1. (略)2.(1)正确。
(2)不正确。
R 、S 构型是人为规定的,而(+)、(-)是测定得到的,二者没有必然联系。
(3)不正确。
分子中没有对称面、对称轴与对称中心,也可以有旋光性如螺环化合物,有空间为阻的联苯类化合物、丙二烯型化合物等。
(4)不正确。
如2,3-二溴丁烷,含有2个不对称碳原子,只有一对对映异构体,一个消旋体。
只有3个立体异构体。
(5)不正确。
如消旋体,分子有手性碳,但因其有对称面并不具有光学活性。
(6)不正确。
如消旋体,分子虽具有不对称碳原子,但无旋光性。
(7)正确。
3. +2.3.0° 4. (4)(7)不同,其他相同。
(2)(3)(4)(5)(1)(CH 3)2CHCHClCH 2CH 3CH 3CHBrCH 2CHClCHOHCH 3H 2NCH 2CHBrCOOHH 3CClOH********5.6. 薄荷醇分子中有3手性碳原子,可能有8个异构体。
7. (1)(4)(6)有对称元素,没有手性。
(2)33D 3CH 3(5)3(3)38. 四个构型异构体,分别是H Cl CH 3HBr CH 3H Cl CH 3H BrCH 3Cl H CH 3HBr CH 3Cl H CH 3H BrCH 3(2S,3R)(2R,3S)(2R,3R)(2S,3S)9. 用R/S 标记下列化合物中不对称碳原子的构型。
(1)S (2)S (3)S (4)R (5)2R,3R (6)2S,3R (7)1S,2R (8)S (9)R (10)R(1)(2)(3)CH 3HHO ClH 2CH 310.H C 6H 5CH 2CH 3Cl BrCl COOH(4)Cl ClCH 3H H Cl H 3CH 3H Cl HBr (5)(6)(6)(5)H 3H CH 3ClHH 3HCH 2CH 32CH 2CH 3Br (2)(3)(1)11.H CH 2CH 3CH 2CH 2CH 3BrRS无对映异构体HCH 2CH 2Cl 2CH 3Cl RSH CH 2CH 2Cl CH 2CH 3Cl (4)RH C(CH 3)32CH(CH 3)2ClHC(CH 3)3CH 2CH(CH 3)2Cl(1)CH 3CH 2CH 32BrBr (2)Cl D 3H 7H H 3C CH 2CH 32BrBrRS(有旋光性)ClD C 3H 7H RS(有旋光性)(3)CH 3Br H OH H 3CH 3Br H HO H32R,3S2S,3R(有旋光性)CH 3H Br OH H 3CH 3H Br HO H32R,3R 2S,3S(有旋光性)C 6H 5CH 3H HH 3C 6H 5CH 3H 3C H H CH 332R,3R 2S,3S(有旋光性)(4)CH 3H CH 3H CH 332R,3S (无旋光性)内消旋体12.C 2H 5CH 3H H H 3C2H 53R,6R3S,6S(有旋光性)(5)3R,6S (无旋光性)内消旋体H H H H C 2H 5H 3C H H CH 32H 5H H H H C 2H 5H H 3C H H 3C2H 5H H H HCH 2OH HO H H OH 2OH(6)(7)(8)H HO 2R,4R2S,4S (有旋光性)CH 2OH HO H H OH 2OHH HO CH 2OH H OH H OH 2OHH HO CH 2OH HO H HO H2OHH HO 2S,4R (无旋光性)内消旋体2S,4R (无旋光性)内消旋体Cl ClCl Cl1R,2R1S,2S(有旋光性)1R,2S (无旋光性)内消旋体ClClCl分子具有对称面,无旋光性13. (3)相同,其它为对映体。
14. (1)(A )BrCH=CBrCH(CH 3)CH 2CH 3, (B) CH 2=CHCH(CH 3)CH 2CH 3,(C) CH 3COCH(CH 3)CH 2CH 3, (D) CH 2=CClCH(CH 3)CH 2CH 3,(2) 都是旋光体(3)都具有相同构型 (4)都不能预测15. (2)无,其它有。
