工程热力学思考题答案,第三章
工程热力学-第四版思考题答案(完整版)(沈维道)(高等教育出版社)

工程热力学-第四版思考题答案(完整版)(沈维道)(高等教育出版社)工程热力学第四版沈维道 思考题 完整版第1章 基本概念及定义1.闭口系与外界无物质交换,系统内质量将保持恒定,那么,系统内质量保持恒定的热力系一定是闭口系统吗?答:否。
当一个控制质量的质量入流率与质量出流率相等时(如稳态稳流系统),系统内的质量将保持恒定不变。
2.有人认为,开口系统中系统与外界有物质交换,而物质又与能量不可分割,所以开口系不可能是绝热系。
这种观点对不对,为什么? 答:不对。
“绝热系”指的是过程中与外界无热量交换的系统。
热量是指过程中系统与外界间以热的方式交换的能量,是过程量,过程一旦结束就无所谓“热量”。
物质并不“拥有”热量。
一个系统能否绝热与其边界是否对物质流开放无关。
⒊平衡状态与稳定状态有何区别和联系,平衡状态与均匀状态有何区别和联系? 答:“平衡状态”与“稳定状态”的概念均指系统的状态不随时间而变化,这是它们的共同点;但平衡状态要求的是在没有外界作用下保持不变;而平衡状态则一般指在外界作用下保持不变,这是它们的区别所在。
⒋倘使容器中气体的压力没有改变,试问安装在该容器上的压力表的读数会改变吗?在绝对压力计算公式中,当地大气压是否必定是环境大气压?答:可能会的。
因为压力表上的读数为表压力,是工质真实压力与环境介质压力之差。
环境介质压力,譬如大气压力,是地面以上空气柱的重量所造成的,它随着各地的纬度、高度和气候条件不同而有所变化,因此,即使工质的绝对压力不变,表压力和真空度仍有可能变化。
“当地大气压”并非就是环境大气压。
准确地说,计算式中的P b 应是“当地环境介质”的压力,而不是随便任何其它意义上的“大气压力”,或被视为不变的“环境大气压力”。
⒌温度计测温的基本原理是什么?答:温度计对温度的测量建立在热力学第零定律原理之上。
它利用了“温度是相互热平衡的系统所具有的一种同一热力性质”,这一性质就是“温度”的概念。
工程热力学课后思考题及答案

⼯程热⼒学课后思考题及答案第⼀章思考题1、如果容器中⽓体压⼒保持不变,那么压⼒表的读数⼀定也保持不变,对吗?答:不对。
因为压⼒表的读书取决于容器中⽓体的压⼒和压⼒表所处环境的⼤⽓压⼒两个因素。
因此即使容器中的⽓体压⼒保持不变,当⼤⽓压⼒变化时,压⼒表的读数也会随之变化,⽽不能保持不变。
2、“平衡”和“均匀”有什么区别和联系答:平衡(状态)值的是热⼒系在没有外界作⽤(意即热⼒、系与外界没有能、质交换,但不排除有恒定的外场如重⼒场作⽤)的情况下,宏观性质不随时间变化,即热⼒系在没有外界作⽤时的时间特征-与时间⽆关。
所以两者是不同的。
如对⽓-液两相平衡的状态,尽管⽓-液两相的温度,压⼒都相同,但两者的密度差别很⼤,是⾮均匀系。
反之,均匀系也不⼀定处于平衡态。
但是在某些特殊情况下,“平衡”与“均匀”⼜可能是统⼀的。
如对于处于平衡状态下的单相流体(⽓体或者液体)如果忽略重⼒的影响,⼜没有其他外场(电、磁场等)作⽤,那么内部各处的各种性质都是均匀⼀致的。
3、“平衡”和“过程”是⽭盾的还是统⼀的?答:“平衡”意味着宏观静⽌,⽆变化,⽽“过程”意味着变化运动,意味着平衡被破坏,所以⼆者是有⽭盾的。
对⼀个热⼒系来说,或是平衡,静⽌不动,或是运动,变化,⼆者必居其⼀。
但是⼆者也有结合点,内部平衡过程恰恰将这两个⽭盾的东西有条件地统⼀在⼀起了。
这个条件就是:在内部平衡过程中,当外界对热⼒系的作⽤缓慢得⾜以使热⼒系内部能量及时恢复不断被破坏的平衡。
4、“过程量”和“状态量”有什么不同?答:状态量是热⼒状态的单值函数,其数学特性是点函数,状态量的微分可以改成全微分,这个全微分的循环积分恒为零;⽽过程量不是热⼒状态的单值函数,即使在初、终态完全相同的情况下,过程量的⼤⼩与其中间经历的具体路径有关,过程量的微分不能写成全微分。
因此它的循环积分不是零⽽是⼀个确定的数值。
习题1-1 ⼀⽴⽅形刚性容器,每边长 1 m ,将其中⽓体的压⼒抽⾄ 1000 Pa ,问其真空度为多少毫⽶汞柱?容器每⾯受⼒多少⽜顿?已知⼤⽓压⼒为 0.1MPa 。
工程热力学课后作业答案(第三章)第五版

3-1 安静状态下的人对环境的散热量大约为400KJ/h,假设能容纳2000人的大礼堂的通风系统坏了:(1)在通风系统出现故障后的最初20min内礼堂中的空气内能增加多少?(2)把礼堂空气和所有的人考虑为一个系统,假设对外界没有传热,系统内能变化多少?如何解释空气温度的升高。
解:(1)热力系:礼堂中的空气。
闭口系统根据闭口系统能量方程Q+=∆UW因为没有作功故W=0;热量来源于人体散热;内能的增加等于人体散热。
⨯Q=2.67×105kJ2000⨯=2060/400(1)热力系:礼堂中的空气和人。
闭口系统根据闭口系统能量方程∆=Q+UW因为没有作功故W=0;对整个礼堂的空气和人来说没有外来热量,所以内能的增加为0。
空气温度的升高是人体的散热量由空气吸收,导致的空气内能增加。
3-5,有一闭口系统,从状态1经a变化到状态2,如图,又从状态2经b回到状态1;再从状态1经过c 变化到状态2。
在这个过程中,热量和功的某些值已知,如表,试确定未知量。
解:闭口系统。
使用闭口系统能量方程(1)对1-a-2和2-b-1组成一个闭口循环,有⎰⎰=WδQδ即10+(-7)=x1+(-4)x1=7 kJ(2)对1-c-2和2-b-1也组成一个闭口循环x2+(-7)=2+(-4)x2=5 kJ(3)对过程2-b-1,根据W U Q +∆==---=-=∆)4(7W Q U -3 kJ3-6 一闭口系统经历了一个由四个过程组成的循环,试填充表中所缺数据。
解:同上题3-7 解:热力系:1.5kg 质量气体闭口系统,状态方程:b av p +=)]85115.1()85225.1[(5.1---=∆v p v p U =90kJ由状态方程得1000=a*0.2+b200=a*1.2+b解上两式得:a=-800b=1160则功量为2.12.0221]1160)800(21[5.15.1v v pdv W --==⎰=900kJ 过程中传热量 WU Q +∆==990 kJ3-8 容积由隔板分成两部分,左边盛有压力为600kPa ,温度为27℃的空气,右边为真空,容积为左边5倍。
工程热力学 第三章答案

活塞距底面高度 h=10cm, 活塞及负载的总质量是 3-6 截面积 A = 100cm 的气缸内充有空气,
2
195kg(见图 3-11)。已知当地大气压力 p0 = 771mmHg ,环 气缸内空气恰与外界处于热力平衡状态, 境温度为 t0 = 27°C , 现将其负载取去 100kg,活塞将上升,最后与环境重新达到热 力平衡。设空气可以通过气缸壁充分与外界换热,达到热力平 衡时,空气的温度等于环境大气的温度。求活塞上升的距离,空气对外作出的功以及与环境的 换热量。 解:据题意,活塞上负载未取去前气缸内气体的初始状态 为: p1 = pb +
h1 = c p |
207° C 0° C
t1 = 1.0125kJ/(kg ⋅ K) × 207 o C = 209.6kJ/kg t2 = 1.0737kJ/(kg ⋅ K) × 827 o C = 887.9kJ/kg
h2 = c p |
827° C 0° C
∆h = h2 − h1 = 887.9kJ/kg − 209.6kJ/kg = 678.3kJ/kg
17
第三章 理想气体的性质
的热力性质表; (3)若上述过程为定压过程, 即 T1 = 480K,T2 = 1100K,p1 = p2 = 0.2MPa , 问这时的 u1、u2、∆u、h1、h2、∆h 有何改变?(4)对计算结果进行简单的讨论: 为什么由气体 性质表得出的 u,h 与平均质量热容表得出的 u, h 不同?两种方法得出的 ∆u,∆h 是否相同? 为什么? 解:由附表查得空气的气体常数 Rg = 0.287kJ/(kg ⋅ K)
t1 = T1 − 273 = 480 − 273 = 207°C , t2 = T2 − 273 = 1100 − 273 = 827°C
工程热力学第3章习题答案

可得
p1V1 p0V0
=
T1 T0
,
0.1×106 ×V1
1.01325×105 × 20000 ×10
=
273.15 +150 273.15
,得
V1
= 87.204m3/s
3600
由
π 4
D2
×c
= V1 ,可得烟囱出口处的内径
( ) 可得 p1 = T1 , ( ) p2 T2
0.1×106 − 60×103 0.1×106 − 90×T2
,得 T2
=
93.29K
需要将气体冷却到−179.86℃
3-5 某活塞式压气机向容积为 10m3 的储气箱中冲入压缩空气。压气机每分钟从压力为 p0=0.1MPa、温度 t0=20℃的大气中吸入 0.5m3 的空气。冲气前储气箱压力表的读数为 0.1MPa, 温度=20℃。问需要多长时间才能使储气箱压力表的读数提高到 0.5MPa,温度上升到 40℃?
T1
T1
根据题意,已知每分钟抽出空气的体积流量为 qV = 0.2m3/min
假设抽气时间为τ分钟,根据已知条件可得 p1V1 = p2 (V1 + qVτ )
质量流量为 qm
=
p2qV RgT1
=
0.1×106 × 5× 0.2
287 × 293.15× (5 + 0.2τ ) kg/min
∫ 因此需要抽气时间的计算为公式
或V = mv = 3× 0.0561 = 0.168m3
3-2 在煤气表上读得煤气的消耗量为 600m3。若在煤气消耗其间,煤气表压力平均值为 0.5 kPa,温度平均为 18℃,当地大气压力为=0.1MPa。设煤气可以按理想气体处理。试计算:
广大复习资料之工程热力学第三章思考题答案

第三章思考题3-1门窗紧闭的房间内有一台电冰箱正在运行,若敞开冰箱的大门就有一股凉气扑面,感到凉爽。
于是有人就想通过敞开冰箱大门达到降低室内温度的目的,你认为这种想法可行吗?解:按题意,以门窗禁闭的房间为分析对象,可看成绝热的闭口系统,与外界无热量交换,Q =0,如图3.1所示,当安置在系统内部的电冰箱运转时,将有电功输入系统,根据热力学规定:W <0,由热力学第一定律W U Q +∆=可知,0>∆U ,即系统的热力学能增加,也就是房间内空气的热力学能增加。
由于空气可视为理想气体,其热力学能是温度的单值函数。
热力学能增加温度也增加,可见此种想法不但不能达到降温目的,反而使室内温度有所升高。
3-2既然敞开冰箱大门不能降温,为什么在门窗紧闭的房间内安装空调器后却能使温度降低呢?解:仍以门窗紧闭的房间为对象。
由于空调器安置在窗上,通过边界向环境大气散热,这时闭口系统并不绝热,而且向外界放热,由于Q<0,虽然空调器工作时依旧有电功W 输入系统,仍然W<0,但按闭口系统能量方程:W Q U -=∆,此时虽然Q 与W 都是负的,但W Q >,所以∆U<0。
可见室内空气热力学能将减少,相应地空气温度将降低。
3-6 下列各式,适用于何种条件?(说明系统、工质、过程)1)δq=du+ δw ;适用于闭口系统、任何工质、任何过程2)δq=du+ pdv ;适用于闭口系统、任何工质、可逆过程3)δq=c v dT+ pdv ;适用于闭口系统、理想气体、任何过程4)δq=dh ;适用于开口系统、任何工质、稳态稳流定压过程5)δq=c p dT- vdp 适用于开口系统、理想气体、可逆过程3-8对工质加热,其温度反而降低,有否可能?答:有可能,如果工质是理想气体,则由热力学第一定律Q=ΔU+W 。
理想气体吸热,则Q>0,降温则ΔT<0,对于理想气体,热力学能是温度的单值函数,因此,ΔU <0。
工程热力学第三章课后答案

第三章 气体和蒸气的性质3−1 已知氮气的摩尔质量328.110 kg/mol M −=×,求: (1)2N 的气体常数g R ;(2)标准状态下2N 的比体积v 0和密度ρ0; (3)标准状态31m 2N 的质量m 0;(4)0.1MPa p =、500C t =D 时2N 的比体积v 和密度ρ; (5)上述状态下的摩尔体积m V 。
解:(1)通用气体常数8.3145J/(mol K)R =⋅,查附表23N 28.0110kg/mol M −=×。
22g,N 3N8.3145J/(mol K)0.297kJ/(kg K)28.0110kg/molR R M −⋅===⋅×(2)1mol 氮气标准状态时体积为22233m,N N N 22.410m /mol V M v −==×,故标准状态下2233m,N 3N 322.410m /mol 0.8m /kg28.0110kg/molV v M −−×===×223N 3N111.25kg/m 0.8m /kgv ρ===(3)标准状态下31m 气体的质量即为密度ρ,即0 1.25kg m =。
(4)由理想气体状态方程式g pv R T=g 36297J/(kg K)(500273)K2.296m /kg0.110Pa R T v p ⋅×+===×33110.4356kg/m 2.296m /kgv ρ===(5)2223333m,N N N 28.0110kg/mol 2.296m /kg 64.2910m /mol V M v −−==××=×3-2 压力表测得储气罐中丙烷38C H 的压力为4.4MPa ,丙烷的温度为120℃,问这时比体积多大?若要储气罐存1 000kg 这种状态的丙烷,问储气罐的体积需多大?解:由附表查得383C H 44.0910kg/mol M −=×3838g,C H 3C H8.3145J/(mol K)189J/(kg K)44.0910kg/molR R M −⋅===⋅×由理想气体状态方程式g pv R T=g 36189J/(kg K)(120273)K0.01688m /kg4.410PaR T v p⋅×+===×331000kg 0.01688m /kg 16.88m V mv ==×=或由理想气体状态方程g pV mR T=g 361000kg 189J/(kg K)(120273)K16.88m 4.410PamR T V p×⋅×+===×3−3 供热系统矩形风管的边长为100mm ×175mm ,40℃、102kPa 的空气在管内流动,其体积流量是0.018 5m 3/s ,求空气流速和质量流量。
工程热力学思考题答案,第三章

第三章 理想气体的性质1.怎样正确看待“理想气体”这个概念?在进行实际计算是如何决定是否可采用理想气体的一些公式?答:理想气体:分子为不占体积的弹性质点,除碰撞外分子间无作用力。
理想气体是实际气体在低压高温时的抽象,是一种实际并不存在的假想气体。
判断所使用气体是否为理想气体(1)依据气体所处的状态(如:气体的密度是否足够小)估计作为理想气体处理时可能引起的误差;(2)应考虑计算所要求的精度。
若为理想气体则可使用理想气体的公式。
2.气体的摩尔体积是否因气体的种类而异?是否因所处状态不同而异?任何气体在任意状态下摩尔体积是否都是 0.022414m 3 /mol? 答:气体的摩尔体积在同温同压下的情况下不会因气体的种类而异;但因所处状态不同而变化。
只有在标准状态下摩尔体积为 0.022414m 3 /mol3.摩尔气体常数 R 值是否随气体的种类不同或状态不同而异? 答:摩尔气体常数不因气体的种类及状态的不同而变化。
4.如果某种工质的状态方程式为pv =R g T ,那么这种工质的比热容、热力学能、焓都仅仅是温度的函数吗?答:一种气体满足理想气体状态方程则为理想气体,那么其比热容、热力学能、焓都仅仅是温度的函数。
5.对于一种确定的理想气体,()p v C C 是否等于定值?pv C C 是否为定值?在不同温度下()p v C C -、pv C C 是否总是同一定值?答:对于确定的理想气体在同一温度下()p v C C -为定值,pv C C 为定值。
在不同温度下()p v C C -为定值,pv C C 不是定值。
6.麦耶公式p v g C C R -=是否适用于理想气体混合物?是否适用于实际气体?答:迈耶公式的推导用到理想气体方程,因此适用于理想气体混合物不适合实际气体。
7.气体有两个独立的参数,u(或 h)可以表示为 p 和 v 的函数,即(,)u u f p v =。
但又曾得出结论,理想气体的热力学能、焓、熵只取决于温度,这两点是否矛盾?为什么?答:不矛盾。
大学工程热力学-思考题答案.docx

第一章基本概念与定义1.答:不一定。
稳定流动开口系统内质量也可以保持恒定2.答:这种说法是不对的。
工质在越过边界时,其热力学能也越过了边界。
但热力学能不是热量,只要系统和外界没有热量地交换就是绝热系。
3.答:只有在没冇外界影响的条件下,工质的状态不随时间变化,这种状态称Z为平衡状态。
稳定状态只要其丁质的状态不随时间变化,就称之为稳定状态,不考虑是否在外界的影响卜,这是他们的木质区别。
平衡状态并非稳定状态之必要条件。
物系内部各处的性质均匀一致的状态为均匀状态。
平衡状态不一定为均匀状态,均匀并非系统处于平衡状态之必要条件。
4.答:压力表的读数可能会改变,根据圧力仪表所处的环境压力的改变而改变。
当地大气压不一定是环境大气压。
环境大气圧是指压力仪表所处的环境的压力。
5.答:温度计随物体的冷热程度不同冇显苕的变化。
6.答:任何一种经验温标不能作为度量温度的标准。
山于经验温标依赖于测温物质的性质,当选用不同测温物质的温度计、采川不同的物理量作为温度的标志来测量温度时,除选定为基准点的温度,其他温度的测定值可能有微小的差异。
7.答:系统内部各部分之间的传热和位移或系统与外界之间的热量的交换与功的交换都是促使系统状态变化的原因。
8.答:(1)第一种情况如图IT (a),不作功(2)第二种情况如图IT (b),作功(3)第一种情况为不可逆过程不可以在p-v图上表示出来,第二种情况为可逆过程可以在p-v图上表示出来。
9.答:经历一个不可逆过程后系统可以恢复为原来状态。
系统和外界整个系统不能恢复原来状态。
10.答:系统经历一可逆正向循环及英逆向可逆循环后,系统恢复到原來状态,外界没冇变化; 若存在不可逆因索,系统恢复到原状态,外界产生变化。
11.答:不一定。
主要看输出功的主要作用是什么,排斥大气功是否冇用。
第二章热力学第一定律1.答:将隔板抽去,根据热力学第一定律9二A" + w其中q = O,w = O所以容器中空气的热力学能不变。
工程热力学思考题答案,第三章

第三章 理想气体的性质1.怎样正确看待“理想气体”这个概念在进行实际计算是如何决定是否可采用理想气体的一些公式答:理想气体:分子为不占体积的弹性质点,除碰撞外分子间无作用力。
理想气体是实际气体在低压高温时的抽象,是一种实际并不存在的假想气体。
判断所使用气体是否为理想气体(1)依据气体所处的状态(如:气体的密度是否足够小)估计作为理想气体处理时可能引起的误差;(2)应考虑计算所要求的精度。
若为理想气体则可使用理想气体的公式。
2.气体的摩尔体积是否因气体的种类而异是否因所处状态不同而异任何气体在任意状态下摩尔体积是否都是 0.022414m 3 /mol答:气体的摩尔体积在同温同压下的情况下不会因气体的种类而异;但因所处状态不同而变化。
只有在标准状态下摩尔体积为 0.022414m 3 /mol3.摩尔气体常数 R 值是否随气体的种类不同或状态不同而异 答:摩尔气体常数不因气体的种类及状态的不同而变化。
4.如果某种工质的状态方程式为pv =R g T ,那么这种工质的比热容、热力学能、焓都仅仅是温度的函数吗答:一种气体满足理想气体状态方程则为理想气体,那么其比热容、热力学能、焓都仅仅是温度的函数。
5.对于一种确定的理想气体,()p v C C 是否等于定值pv C C 是否为定值在不同温度下()p v C C -、pv C C 是否总是同一定值答:对于确定的理想气体在同一温度下()p v C C -为定值,pv C C 为定值。
在不同温度下()p v C C -为定值,pv C C 不是定值。
6.麦耶公式p v g C C R -=是否适用于理想气体混合物是否适用于实际气体答:迈耶公式的推导用到理想气体方程,因此适用于理想气体混合物不适合实际气体。
7.气体有两个独立的参数,u(或 h)可以表示为 p 和 v 的函数,即(,)u u f p v =。
但又曾得出结论,理想气体的热力学能、焓、熵只取决于温度,这两点是否矛盾为什么答:不矛盾。
工程热力学第三章课后答案

第三章 气体和蒸气的性质3−1 已知氮气的摩尔质量328.110 kg/mol M −=×,求: (1)2N 的气体常数g R ;(2)标准状态下2N 的比体积v 0和密度ρ0; (3)标准状态31m 2N 的质量m 0;(4)0.1MPa p =、500C t =D 时2N 的比体积v 和密度ρ; (5)上述状态下的摩尔体积m V 。
解:(1)通用气体常数8.3145J/(mol K)R =⋅,查附表23N 28.0110kg/mol M −=×。
22g,N 3N8.3145J/(mol K)0.297kJ/(kg K)28.0110kg/molR R M −⋅===⋅×(2)1mol 氮气标准状态时体积为22233m,N N N 22.410m /mol V M v −==×,故标准状态下2233m,N 3N 322.410m /mol 0.8m /kg28.0110kg/molV v M −−×===×223N 3N111.25kg/m 0.8m /kgv ρ===(3)标准状态下31m 气体的质量即为密度ρ,即0 1.25kg m =。
(4)由理想气体状态方程式g pv R T=g 36297J/(kg K)(500273)K2.296m /kg0.110Pa R T v p ⋅×+===×33110.4356kg/m 2.296m /kgv ρ===(5)2223333m,N N N 28.0110kg/mol 2.296m /kg 64.2910m /mol V M v −−==××=×3-2 压力表测得储气罐中丙烷38C H 的压力为4.4MPa ,丙烷的温度为120℃,问这时比体积多大?若要储气罐存1 000kg 这种状态的丙烷,问储气罐的体积需多大?解:由附表查得383C H 44.0910kg/mol M −=×3838g,C H 3C H8.3145J/(mol K)189J/(kg K)44.0910kg/molR R M −⋅===⋅×由理想气体状态方程式g pv R T=g 36189J/(kg K)(120273)K0.01688m /kg4.410PaR T v p⋅×+===×331000kg 0.01688m /kg 16.88m V mv ==×=或由理想气体状态方程g pV mR T=g 361000kg 189J/(kg K)(120273)K16.88m 4.410PamR T V p×⋅×+===×3−3 供热系统矩形风管的边长为100mm ×175mm ,40℃、102kPa 的空气在管内流动,其体积流量是0.018 5m 3/s ,求空气流速和质量流量。
工程热力学思考题及答案

工程热力学思考题及答案第一章基本概念1.闭口系与外界无物质交换,系统内质量保持恒定,那么系统内质量保持恒定的热力系一定是闭口系统吗?答:不一定。
稳定流动开口系统内质量也可以保持恒定。
2.有人认为,开口系统中系统与外界有物质交换,而物质又与能量不可分割,所以开口系统不可能是绝热系。
对不对,为什么?答:这种说法是不对的。
工质在越过边界时,其热力学能也越过了边界。
但热力学能不是热量,只要系统和外界没有热量的交换就是绝热系。
答:只有在没有外界影响的条件下,工质的状态不随时间变化,这种状态称之为平衡状态。
稳定状态只要其工质的状态不随时间变化,就称之为稳定状态,不考虑是否在外界的影响下,这是它们的本质区别。
平衡状态并非稳定状态之必要条件。
物系内部各处的性质均匀一致的状态为均匀状态。
平衡状态不一定为均匀状态,均匀并非系统处于平衡状态之必要条件。
4.假如容器中气体的压力没有改变,试问安装在该容器上的压力表的读数会改变吗?绝对压力计算公式p=pb+pe(p>pb),pv=pbp(pb 答:压力表的读数可能会改变,根据压力仪表所处的环境压力的改变而改变。
当地大气压不一定是环境大气压。
环境大气压是指压力仪表所处的环境的压力。
5.温度计测温的基本原理是什么?答:温度计随物体的冷热程度不同有显著的变化。
6.经验温标的缺点是什么?为什么?答:任何一种经验温标不能作为度量温度的标准。
由于经验温标依赖于测温物质的性质,当选用不同测温物质的温度计、采用不同的物理量作为温度的标志来测量温度时,除选定为基准点的温度,其他温度的测定值可能有微小的差异。
7.促使系统状态变化的原因是什么?答:系统内部各部分之间的传热和位移或系统与外界之间的热量的交换与功的交换都是促使系统状态变化。
8.(1)将容器分成两部分,一部分装气体,一部分抽成真空,中间是隔板。
若突然抽去隔板,气体(系统)是否做功?(2)设真空部分装有许多隔板,每抽去一块隔板让气体先恢复平衡再抽去一块,问气体(系统)是否做功?(3)上述两种情况从初态变化到终态,其过程是否都可在pv图上表示?答:(1)第一种情况不作功;(2)第二种情况作功;(3)第一种情况为不可逆过程不可以在p-v图上表示出来,第二种情况为可逆过程可以在p-v图上表示出来。
工程热力学思考题及答案

工程热力学思考题及答案第一章基本概念1.闭口系与外界无物质交换,系统内质量保持恒定,那么系统内质量保持恒定的热力系一定是闭口系统吗答:不一定;稳定流动开口系统内质量也可以保持恒定;2.有人认为,开口系统中系统与外界有物质交换,而物质又与能量不可分割,所以开口系统不可能是绝热系;对不对,为什么答:这种说法是不对的;工质在越过边界时,其热力学能也越过了边界;但热力学能不是热量,只要系统和外界没有热量的交换就是绝热系;3.平衡状态与稳定状态有何区别和联系,平衡状态与均匀状态有何区别和联系答:只有在没有外界影响的条件下,工质的状态不随时间变化,这种状态称之为平衡状态;稳定状态只要其工质的状态不随时间变化,就称之为稳定状态,不考虑是否在外界的影响下,这是它们的本质区别;平衡状态并非稳定状态之必要条件;物系内部各处的性质均匀一致的状态为均匀状态;平衡状态不一定为均匀状态,均匀并非系统处于平衡状态之必要条件;4.假如容器中气体的压力没有改变,试问安装在该容器上的压力表的读数会改变吗绝对压力计算公式p = pb +p e p >p b,p v=p bp p b <p中,当地大气压是否必定是环境大气压答:压力表的读数可能会改变,根据压力仪表所处的环境压力的改变而改变;当地大气压不一定是环境大气压;环境大气压是指压力仪表所处的环境的压力;5.温度计测温的基本原理是什么答:温度计随物体的冷热程度不同有显着的变化;6.经验温标的缺点是什么为什么答:任何一种经验温标不能作为度量温度的标准;由于经验温标依赖于测温物质的性质,当选用不同测温物质的温度计、采用不同的物理量作为温度的标志来测量温度时,除选定为基准点的温度,其他温度的测定值可能有微小的差异;7.促使系统状态变化的原因是什么答:系统内部各部分之间的传热和位移或系统与外界之间的热量的交换与功的交换都是促使系统状态变化;8.1将容器分成两部分,一部分装气体,一部分抽成真空,中间是隔板;若突然抽去隔板,气体系统是否做功2设真空部分装有许多隔板,每抽去一块隔板让气体先恢复平衡再抽去一块,问气体系统是否做功3上述两种情况从初态变化到终态,其过程是否都可在p v图上表示答:1第一种情况不作功;2第二种情况作功;3第一种情况为不可逆过程不可以在p-v 图上表示出来,第二种情况为可逆过程可以在p-v 图上表示出来;9.经历一个不可逆过程后,系统能否恢复原来状态包括系统和外界的整个系统能否恢复原来状态答:经历一个不可逆过程后系统可以恢复为原来状态;系统和外界整个系统不能恢复原来状态;10. 系统经历一可逆正向循环及其逆向可逆循环后,系统和外界有什么变化若上述正向及逆向循环环中有不可逆因素,则系统及外界有什么变化答:系统经历一可逆正向循环及其逆向可逆循环后,系统恢复到原来状态,外界没有变化;若存在不可逆因素,系统恢复到原状态,外界产生变化;11. 工质及气缸、活塞组成的系统经循环后,系统输出的功中是否要减去活塞排斥大气功才是有用功答:不一定;主要看输出功的主要作用是什么,排斥大气功是否有用;第二章 热力学第一定律1. 刚性绝热容器中间用隔板分为两部分,A 中存有高压空气,B 中保持真空;若将隔板抽去,分析容器中空气的热力学能如何变化若隔板上有一小孔,气体泄漏入B 中,分析A 、B 两部分压力相同时A 、B 两部分气体的热力学能如何变化答:将隔板抽去,根据热力学第一定律w u q +∆=其中0,0==w q 所以容器中空气的热力学能不变;若有一小孔,以B 为热力系进行分析只有流体的流入没有流出,0,0==i W Q δδ,忽略动能、势能B 部分气体的热力学能增量为U ∆,A 部分气体的热力学能减少量为U ∆2. 热力学第一定律能量方程式是否可以写成下列两种形式:()()121212w w u u q q -+-=-、 q = Δu + pv 的形式,为什么答: 热力学第一定律能量方程式不可以写成题中所述的形式;对于pv u q +∆=只有在特殊情况下,功w 可以写成pv ;热力学第一定律是一个针对任何情况的定律,不具有w =pv 这样一个必需条件;对于公式()()121212w w u u q q -+-=-,功和热量不是状态参数所以不能写成该式的形式;3. 热力学第一定律解析式有时写成下列两种形式:q = Δu + w⎰+∆=21pdVu q 分别讨论上述两式的适用范围.答:w u q +∆=适用于任何过程,任何工质⎰+∆=21pdVu q 可逆过程,任何工质4. 为什么流动功出现在开口系能量方程式中,而不出现在闭口系能量方程式中答:流动功是由流进出系统的工质传递而由工质后面的物质系统作出的;对于闭口系统,不存在工质的流进出所以不存在这样进行传递的功;5.稳定流动能量方程式是否可应用于活塞式压气机这种机械的稳定工况运行的能量分析为什么答:可以;稳定流动能量方程式可应用于任何稳定流动过程,对于连续工作的周期性动作的能量转换装置,只要在平均单位时间所作的轴功、吸热量以及工质的平均流量为常量,虽然它内部工质的状态及流动情况是变化的,但这种周期性的变化规律不随时间而变,所以仍然可以利用稳定流动能量方程式分析其能量转换关系;第三章热力学第二定律1.热力学第二定律能否表达为:“机械能可以全部变为热能,而热能不可能全部变为机械能;”这种说法有什么不妥当答:不能这样表述;表述不正确,对于可逆的定温过程,所吸收的热量可以全部转化为机械能,但是自身状态发生了变化;所以这种表述不正确;2.自发过程是不可逆过程,非自发过程必为可逆过程,这一说法是否正确答:不正确;自发过程是不可逆过程是正确的;非自发过程却不一定为可逆过程;3.请给“不可逆过程”一个恰当的定义;热力过程中有哪几种不可逆因素答:一切非准静态过程都是不可逆过程;不可逆因素有:摩擦、不等温传热和不等压做功; 4.试证明热力学第二定律各种说法的等效性:若克劳修斯说法不成立,则开尔文说也不成立;答:热力学第二定律的两种说法反映的是同一客观规律——自然过程的方向性−→−是一致的,只要一种表述可能,则另一种也可能;假设热量Q2能够从温度T2的低温热源自动传给温度为T1的高温热源;现有一循环热机在两热源间工作,并且它放给低温热源的热量恰好等于Q2;整个系统在完成一个循环时,所产生的唯一效果是热机从单一热源T1取得热量Q1-Q2,并全部转变为对外输出的功W;低温热源的自动传热Q2给高温热源,又从热机处接受Q2,故并未受任何影响;这就成了第二类永动机;⇒违反了克劳修斯说法,⇒必须违反了开尔文说法;反之,承认了开尔文说法,克劳修斯说法也就必然成立;5.1循环净功Wnet 愈大则循环效率愈高;× 2不可逆循环的热效率一定小于可逆循环的热效率;× 3可逆循环的热效率都相等;×6.循环热效率公式121 q qq t -=η121 T TT t -=η是否完全相同各适用于哪些场合答:这两个公式不相同;121 q qq t -=η适用于任何工质,任何循环;121 T TT t -=η适用于任何工质,卡诺循环7.与大气温度相同的压缩空气可以膨胀做功,此事实是否违反了热力学第二定律答:不违反热力学第二定律,对于理想气体的定温过程,从单一热源吸热并膨胀做功,工质的状态发生了变化,所以不违反热力学第二定律;8.下列说法是否正确:1熵增大的过程必定为吸热过程×;2熵减小的过程必为放热过程×;3定熵过程必为逆绝热过程×;9. 下列说法是否有错误:(1) 熵增大的过程必为不可逆过程×(2) 使系统熵增大的过程必为不可逆过程×(3) 熵产sg > 0 的过程必为不可逆过程√(4) 不可逆过程的熵变Δs 无法计算×(5) 如果从同一初始态到同一终态有两条途径,一为可逆,另一为不可逆,则可逆不可逆S S ∆>∆,可逆不可逆,,f f S S >,可逆不可逆,,g g S S >是否正确答:可逆不可逆S S ∆=∆、可逆不可逆,,f f S S <、可逆不可逆,,g g S S >(6) 不可逆绝热膨胀的终态熵大于初态熵,S 2>S 1,不可逆绝热压缩的终态熵小于初态熵S 2<S 1答:不可逆绝热膨胀的终态熵大于初态熵S>S 不可逆绝热压缩的终态熵也大于初态熵S>S;(7) 工质经过不可逆循环有⎰⎰<>0,0r T q ds δ 答:工质经过不可逆循环有⎰⎰<=0,0r T q ds δ10. 从点a 开始有两个可逆过程:定容过程a-b 和定压过程a-c,b 、c 两点在同一条绝热线上,问q a b 和q ac 哪个大并在T-s 上表示过程a-b 、a-c 及q ab 、q ac答:由图可知c a b a q q -->b a q -为1-a-b-2-1的面积;c a q -为1-a-c -2-1的面积11. 某种理想气体由同一初态经可逆绝热压缩和不可逆绝热压缩两种过程将气体压缩到相同的终压,在p-v 图和T-s 图上画出两过程,并在T-s 图上画出两过程的技术功及不可逆过程的用损失;答:由同一初态经可逆绝热压缩和不可逆绝热压缩两种过程到相同终压如图所示;由图可知,可逆绝热压缩过程的技术功为面积1-2T -j-m-1,不可逆绝热压缩过程的技术功为面积1-2’T -f-m-1,不可逆过程的用损失为面积1-g-n-m-112. 对于一个孤立系统,其内部若进行了可逆过程则孤立系统的总能不变,总熵不变总火用也不变答:若系统内进行的是不可逆过程则系统的总能不变,总熵增加,总火用减小;第四章 理想气体的性质1. 怎样正确看待“理想气体”这个概念在进行实际计算是如何决定是否可采用理想气体的一些公式答:理想气体:分子为不占体积的弹性质点,除碰撞外分子间无作用力;理想气体是实际气体在低压高温时的抽象,是一种实际并不存在的假想气体;判断所使用气体是否为理想气体1依据气体所处的状态如:气体的密度是否足够小估计作为理想气体处理时可能引起的误差;2应考虑计算所要求的精度;若为理想气体则可使用理想气体的公式;2. 气体的摩尔体积是否因气体的种类而异是否因所处状态不同而异任何气体在任意状态下摩尔体积是否都是mol答:气体的摩尔体积在同温同压下的情况下不会因气体的种类而异;但因所处状态不同而变化;只有在标准状态下摩尔体积为 m 3/mol3. 摩尔气体常数R 值是否随气体的种类不同或状态不同而异答:摩尔气体常数不因气体的种类及状态的不同而变化;4. 如果某种工质的状态方程式为pv = R g T ,那么这种工质的比热容、热力学能、焓都仅仅是温度的函数吗答:一种气体满足理想气体状态方程则为理想气体,那么其比热容、热力学能、焓都仅仅是温度的函数;5. 对于一种确定的理想气体,v p c c -是否等于定值 v pc c 是否为定值在不同温度下v p c c -、v p c c 是否总是同一定值答:对于确定的理想气体在同一温度下v p c c -为定值,v p c c 为定值;在不同温度下v p c c -为定值,v pc c 不是定值6. 迈耶公式是否适用于理想气体混合物是否适用于实际气体答:迈耶公式的推导用到理想气体方程,因此适用于理想气体混合物不适合实际气体;7. 试论证热力学能和焓是状态参数,理想气体热力学能和焓有何特点答:在工程热力学里,在无化学反应及原子核反应的过程中,化学能、原子核能都不变化,可以不考虑,因此热力学能包括内动能和内位能;内动能由温度决定,内位能由v 决定;这样热力学能由两个状态参数决定;所以热力学能是状态参数;由公式h = u + pv 可以看到,焓也是由状态参数决定,所以也是状态参数;对于理想气体热力学能和焓只是温度的函数;8. 气体有两个独立的参数,u 或 h 可以表示为p 和v 的函数,即u= f p, v;但又曾得出结论,理想气体的热力学能、焓、熵只取决于温度,这两点是否矛盾为什么答:不矛盾;实际气体有两个独立的参数;理想气体忽略了分子间的作用力,所以只取决于温度;9. 为什么工质的热力学能、焓、熵为零的基准可以任选理想气体的热力学能或焓的参照状态通常选定哪个或哪些个状态参数值对理想气体的熵又如何答:在工程热力学里需要的是过程中热力学能、焓、熵的变化量;热力学能、焓、熵都只是温度的单值函数,变化量的计算与基准的选取无关;热力学能或焓的参照状态通常取0K 或0℃时焓时为0,热力学能值为0;熵的基准状态取p 0 =101325Pa 、T 0 =0K 熵值为010. 气体热力性质表中的u 、h 及s0 的基准是什么状态答:气体热力性质表中的h u 、及0s 基准是态是()00,p T ,K T 00=,0p =101325Pa11. 在如图3-1 所示的T-s 图上任意可逆过程1-2 的热量如何表示理想气体在1 和2 状态间的热力学能变化量、焓变化量如何表示若在1-2 经过的是不可逆过程又如何 答:图3-2中阴影部分面积为多变过程1-2的热量;对于多变过程其热力学能变化量及焓变化量可由下面两式计算得到: 过初始状态点,做定容线2-2’,图3-3中阴影部分面积为多变过程1-2的热力学能变化量;过初始状态点,做定压线2-2’,图3-4中阴影部分面积为多变过程1-2的焓变化量 ;若为不可逆过程,热力学能、焓不变如上图;热量无法在图中表示出来;12. 理想气体熵变计算式是由可逆过程导出的,这些计算式是否可用于不可逆过程初、终态的熵变为什么答:可以;因为熵是状态参数,只与初终状态有关,与过程无关;13. 熵的数学定义式为 T q ds rev δ=,比热容的定义式为δq = cdT ,故Tds = cdT 理想气体的比热容是温度的单值函数,所以理想气体的熵也是温度的单值函数;这一结论是否正确若不正确,错在何处答: T q ds rev δ=中,rev q δ为一微元可逆变化过程中与热源交换的热量,而cdT q =δ中q δ为工质温度升高dT 所吸收的热量,它们是不能等同的所以这一结论是错误的;14. 1气体吸热后熵一定增大 ;2气体吸热后温度一定升高 ;3气体吸热后热力学能一定升高 ;4气体膨胀时一定对外做功 5气体压缩时一定耗功答:1× 2× 3× 4× 5√15. 道尔顿分压定律和亚美格分体积定律是否适用于实际气体混合物答:不适用;16. 混合气体中如果已知两种组分A 和B 摩尔分数x A >x B ,能否断定质量分数也是w A >w B 答:因为A A eqA w M M x =,B B eqB w M M x =,混合气体的折合摩尔质量相同,但是组分A 和B 摩尔的摩尔质量大小关系不能确定;所以不能断定B A w w >第五章 实际气体的性质及热力学一般关系式1. 实际气体性质与理想气体性质差异产生的原因是什么在什么条件下才可以把实际气体作为理想气体处理答:理想气体模型中忽略了气体分子间的作用力和气体分子所占据的体积;实际气体只有在高温低压状态下,其性质和理想气体相近;或者在常温常压下,那些不易液化的气体,如氧气、氦气、空气等的性质与理想气体相似,可以将它们看作理想气体,使研究的问题简化;2. 压缩因子Z 的物理意义怎么理解能否将Z 当作常数处理答:压缩因子为温度、压力相同时的实际气体比体积与理想气体比体积之比;压缩因子不仅随气体的种类而且随其状态而异,故每种气体应有不同的Z = f p ,T 曲线;因此不能取常数;3.范德瓦尔方程的精度不高,但在实际气体状态方程的研究中范德瓦尔方程的地位却很高,为什么答:范德瓦尔方程其计算精度虽然不高,但范德瓦尔方程式的价值在于能近似地反映实际气体性质方面的特征,并为实际气体状态方程式的研究开拓了道路,因此具有较高的地位;4.范德瓦尔方程中的物性常数a和b可以由试验数据拟合得到,也可以由物质的 Tcr 、pcr、vcr计算得到,需要较高的精度时应采用哪种方法,为什么答:当需要较高的精度时应采用实验数据拟和得到a、b;利用临界压力和临界温度计算得到的a、b 值是近似的;5.什么叫对应态原理为什么要引入对应态原理什么是对比参数答:在相同的压力与温度下,不同气体的比体积是不同的,但是只要它们的p r 和Tr 分别相同,它们的vr 必定相同,这就是对应态原理;对应态原理并不是十分精确,但大致是正确的;它可以使我们在缺乏详细资料的情况下,能借助某一资料充分的参考流体的热力性质来估算其他流体的性质;相对于临界参数的对比值叫做对比参数;6.什么是特性函数试说明 u = us, p是否是特性函数;答:对简单可压缩的系统,任意一个状态参数都可以表示成另外两个独立参数的函数;其中,某些状态参数若表示成特定的两个独立参数的函数时,只需一个状态函数就可以确定系统的其它参数,这样的函数就称为“特性函数”;但是对于比容无法用该函数表示出来,所以此函数不是特性函数;7.如何利用状态方程和热力学一般关系求取实际气体的Δu、Δh、Δs答:将状态方程进行求导,然后带入热力学能、焓或熵的一般关系式,在进行积分;8.本章导出的关于热力学能、焓、熵的一般关系式是否可用于不可逆过程答:热力学能、焓、熵都是状态参数,计算两个平衡状态之间的变量可任意选择其过程;所以同样适用于不可逆过程;9.水的相图和一般物质的相图区别在哪里为什么答:与水的相图比较,显着的差别是固液二相平衡线的倾斜方向不同,由于液态水凝固时容积增大,依据克拉贝隆-克劳修斯方程固液相平衡曲线的斜率为负;而其它物质则相反;第六章水蒸气与湿空气1.水的三相点的状态参数是不是唯一确定的三相点与临界点有什么差异答:水的三相点状态参数不是唯一的,其中温度、压力是定值而比体积不是定值;临界点是唯一的,其比体积、温度、压力都是确定的;三相点是三相共存的点,临界点是饱和水线与饱和蒸汽线的交点,在该点饱和水线与饱和蒸汽线不再有分别;2.刚性绝热的密闭容器内水的压力为4MPa,测得容器内温度为200℃,试问容器内的水是什么集态因意外事故容器上产生了一不大的裂缝,试分析其后果答:水的集态为高压水,若有裂缝则会产生爆裂事故;3.水的定压汽化过程中温度维持不变,因此有人认为过程中热量等于膨胀功,即q = w,对不对为什么答:这种说法是不对的;因为温度不变不表示热力学能不变;这里分析的是水,定压汽化有相变, 不能作为理想气体来处理,所以Δu ≠ 0;不能得到q = w这样的结果;4.为何阴雨天晒衣服不易干,而晴天则容易干答:阴雨天空气的湿度大,吸取水蒸气的能力差,所以晒衣服不易干;晴天则恰恰相反,所以容易干;5.为何冬季人在室外呼出的气是白色雾状冬季室内有供暖装置时,为什么会感到空气干燥用火炉取暖时,经常在火炉上放—壶水,目的何在答:人呼出的气体是未饱和湿空气;当进入外界环境时,外界环境的温度很低使得呼出的气体得到冷却;在冷却过程中,湿空气保持含湿量不变,温度降低;当低于露点温度时就有水蒸气不断凝结析出,这就形成了白色雾状气体;冬季室内有供暖装置时,温度较高,使空气含湿量减小;因此会觉得干燥;放一壶水的目的就是使水加热变成水蒸气散发到空气中增加空气的含湿量;6.何谓湿空气的露点温度解释降雾、结露、结霜现象,并说明它们发生的条件;答:露点:湿空气中水蒸气的分压力所对应的饱和温度称为湿空气的露点温度,或简称露点;a 雾是近地面空气中的水蒸气发生的凝结现象; 白天温度比较高,空气中可容纳较多的水汽;但是到了夜间,地面温度较低,空气把自身的热量传给地面,空气温度下降,这时湿空气随温度降低呈现出过饱和状态,就会发生凝结,当足够多的水分子与空气中微小的灰尘颗粒结合在一起,同时水分子本身也会相互粘结,就变成小水滴或冰晶,这就形成了雾;雾的形成基本条件,一是近地面空气中的水蒸气含量充沛,二是地面气温低;三是在凝结时必须有一个凝聚核,如尘埃等;b 露是水蒸气遇到冷的物体凝结成的水珠;露的形成有两个基本条件:一是水汽条件好,二是温度比较低的物体低,指与露点温度比较;,温度逐渐降低且保持含湿量不变,;当温度低于露点温度时就有水珠析出,这就形成露;c 霜是近地面空气中的水蒸气在物体上的凝华现象;霜的形成有两个基本条件,一是空气中含有较多的水蒸气,二是有冷O℃以下的物体;,湿空气与温度较低物体接触达到水汽过饱和的时候多余的水汽就会析出;如果温度在0°C 以下,则多余的水汽就在物体表面上凝华为冰晶,形成霜;7.对于未饱和空气,湿球温度、干球温度以及露点三者哪个大对于饱和空气,三者的大小又将如何答:对于未饱和空气,干球温度数值较大;对于饱和空气三者的大小相等;8.何谓湿空气的含湿量相对湿度愈大含湿量愈高,这样说对吗答:含湿量d:1 千克干空气所带有的的水蒸气的质量;相对湿度是湿空气中实际包含的水蒸气量与同温度下最多能包含的水蒸气量的百分比;相对湿度是一个比值,不能简单的地说相对湿度愈大含湿量愈高,他与同温度下最多能包含的水蒸气量是相关的;9.刚性容器内湿空气温度保持不变而充入干空气,问容器内湿空气的φ、 d 、 p v 如何变化答:φ减小, d 减小, p v 减小;10. 若封闭汽缸内的湿空气定压升温,问湿空气的 φ 、 d 、 h 如何变化答:φ 减小, d 不变, h 变大;第七章 理想气体的热力过程1. 分析气体的热力过程要解决哪些问题用什么方法解决试以理想气体的定温过程为例说明之;答:主答:主要解决的问题及方法:1.根据过程特点及状态方程−−→−确定过程方程 2.根据过程方程−−→−确定始、终状态参数之间的关系 3.由热力学第一定律等−−→−计算s h u q t ∆∆∆,,,,,ωω4.分析能量转换关系用P —V 图及T —S 图根据需要可以定性也可以定量例:1 过程方程式:常数=T 特征 常数=PV 方程2 初、终状态参数之间的关系:22111221V P V P V V P P ==或3计算各量: 1212ln lnP P R V V R s h u -==∆=∆=∆。
工程热力学与传热学第三章作业参考答案
“山水之乐”的具体化。3.第三段同样是写“乐”,但却是写的游人之乐,作者是如何写游人之乐的?明确:“滁人游”,前呼后应,扶老携幼,自由自在,热闹非凡;“太守宴”,溪深鱼肥,泉香酒洌,美味佳肴,应有尽有;“众宾欢”,投壶下棋,觥筹交错,说说笑笑,无拘无束。如此勾画了游人之乐。4.作者为什么要在第三段写游人之乐?明确:写滁人之游,
贯穿全篇,却有两个句子别出深意,不单单是在写乐,而是另有所指,表达出另外一种情绪,请你找出这两个句子,说说这种情绪是什么。明确:醉翁之意不在酒,在乎山水之间也。醉能同其乐,醒能述以文者,太守也。这种情绪是作者遭贬谪后的抑郁,作者并未在文中袒露胸怀,只含蓄地说:“醉能同其乐,醒能述以文者,太守也。”此句与醉翁亭的名称、“醉翁之
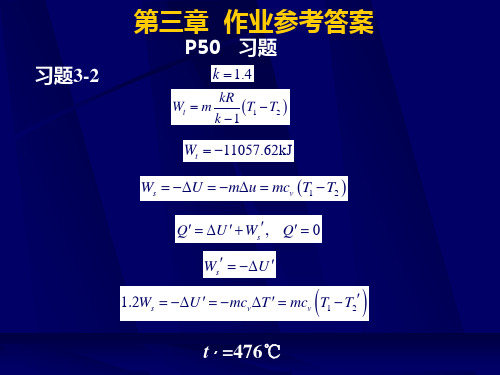
p50习题习题3214476p50习题习题33lnlnp50习题习题351331可逆绝热过程2自由膨胀lnln576kjkmcmr理想气体定值比热及比热比单原子双原子多原子摩尔定容比热ckjkmolk摩尔定压比热ckjkmolk比热比k16714129当计算精度要求不高或气体处于较低温度范围常采用定值比热忽略比热与温度的关系
Ws U mu mcv T1 T2 1746.3kJ
S 0
(2)自由膨胀
Ws 0 Q 0, U 0 T2 T1 340K
S
mcv
ln T2 T1
mR ln
v2 v1
5.76kJ/K
当计算精度要求不高,或气体处于较低温度 范围,常采用定值比热,忽略比热与温度的关系。 不同气体在标准状态下均为22.4m3,不同气体只 要其原子数相同则其摩尔定值比热相等。
江西)人,因吉州原属庐陵郡,因此他又以“庐陵欧阳修”自居。谥号文忠,世称欧阳文忠公。北宋政治家、文学家、史学家,与韩愈、柳宗元、王安石、苏洵、苏轼、苏辙、曾巩合称“唐宋八大家”。后人又将其与韩愈、柳宗元和苏轼合称“千古文章四大家”。
工程热力学第三章习题参考答案

第三章 热力学第一定律 习题参考答案思考题3-1门窗紧闭的房间……答:按题意,以房间(空气+冰箱)为对象,可看成绝热闭口系统,与外界无热量交换,Q=0电冰箱运转时,有电功输入,即W 为负值,按闭口系统能量方程:WU +Δ=0 或即热力学能增加,温度上升。
0>−=ΔW U 3-6 下列各式,适用于何种条件? 答:答案列于下表公式适用条件w du q δδ+= 闭口系统,任何工质,任何过程,不论可逆与不可逆 pdv du q +=δ 闭口系统,任何工质,可逆过程 pdv dT c q v +=δ闭口系统,理想气体,可逆过程dh q =δ 闭口系统,定压过程; 或开口系统与环境无技术功交换。
vdp dT c q v −=δ开口系统,理想气体,稳态稳流,可逆过程3-10 说明以下结论是否正确: (提示:采用推理原则,否定原则) ⑴ 气体吸热后一定膨胀,热力学能一定增加。
答:错误,如等容过程吸热后不膨胀;如不是等容过程吸热后热力学能也不一定增加,当对外净输出功量大于吸热量时,则热力学能不增加。
⑵ 气体膨胀一定对外作功。
答:错误,如气体向真空膨胀则不作功,另外气体膨胀对外作膨胀功的充要条件是:气体膨胀和要有功的传递和接受机构。
⑶ 气体压缩时,一定消耗外功。
答:错误,如处于冷却过程的简单可压缩系统,则会自发收缩(相当于被压缩),并不消耗外功。
⑷ 应设法利用烟气离开锅炉时带走的热量。
答:错误不应说设法利用烟气离开锅炉时带走的热量。
因为热量是过程量,不发生则不存在。
应该说设法利用烟气离开锅炉时带走的热能(或热焓)。
习 题3-1 已知:min 202000/400===time N hkJ q 人人求:?=ΔU 解:依题意可将礼堂看作绝热系统,思路:1、如何选取系统?2、如何建立能量方程? ⑴ 依题意,选取礼堂空气为系统,人看作环境,依热力学第一定律,建立能量方程:kJ time N q Q U W W Q U 51067.2602020004000×=××=⋅⋅==Δ∴=−=Δ人Q⑵ 如选“人+空气”作系统, 依据热力学第一定律:W Q U −=Δ0,0,0=Δ∴==U Q W Q如何解释空气温度升高:该系统包括“人+空气”两个子系统 ,人散热给空气,热力学能降低,空气吸热,能内升高,二者热力学能代数和为零。
工程热力学思考题及答案

⼯程热⼒学思考题及答案⼯程热⼒学思考题及答案第⼀章基本概念1.闭⼝系与外界⽆物质交换,系统内质量保持恒定,那么系统内质量保持恒定得热⼒系⼀定就是闭⼝系统吗?答:不⼀定。
稳定流动开⼝系统内质量也可以保持恒定。
2.有⼈认为,开⼝系统中系统与外界有物质交换,⽽物质⼜与能量不可分割,所以开⼝系统不可能就是绝热系。
对不对,为什么?答:这种说法就是不对得。
⼯质在越过边界时,其热⼒学能也越过了边界。
但热⼒学能不就是热量,只要系统与外界没有热量得交换就就是绝热系。
3.平衡状态与稳定状态有何区别与联系,平衡状态与均匀状态有何区别与联系?答:只有在没有外界影响得条件下,⼯质得状态不随时间变化,这种状态称之为平衡状态。
稳定状态只要其⼯质得状态不随时间变化,就称之为稳定状态,不考虑就是否在外界得影响下,这就是它们得本质区别。
平衡状态并⾮稳定状态之必要条件。
物系内部各处得性质均匀⼀致得状态为均匀状态。
平衡状态不⼀定为均匀状态,均匀并⾮系统处于平衡状态之必要条件。
4.假如容器中⽓体得压⼒没有改变,试问安装在该容器上得压⼒表得读数会改变吗?绝对压⼒计算公式p= p b+pe(p>p b),p v=p b?p (p b答:压⼒表得读数可能会改变,根据压⼒仪表所处得环境压⼒得改变⽽改变。
当地⼤⽓压不⼀定就是环境⼤⽓压。
环境⼤⽓压就是指压⼒仪表所处得环境得压⼒。
5.温度计测温得基本原理就是什么?答:温度计随物体得冷热程度不同有显著得变化。
6.经验温标得缺点就是什么?为什么?答:任何⼀种经验温标不能作为度量温度得标准。
由于经验温标依赖于测温物质得性质,当选⽤不同测温物质得温度计、采⽤不同得物理量作为温度得标志来测量温度时,除选定为基准点得温度,其她温度得测定值可能有微⼩得差异。
7.促使系统状态变化得原因就是什么?答:系统内部各部分之间得传热与位移或系统与外界之间得热量得交换与功得交换都就是促使系统状态变化。
8.(1)将容器分成两部分,⼀部分装⽓体,⼀部分抽成真空,中间就是隔板。
工程热力学思考题及答案

工程热力学思考题及答案第一章基本概念1.闭口系与外界无物质交换,系统内质量保持恒定,那么系统内质量保持恒定的热力系一定是闭口系统吗?答:不一定.稳定流动开口系统内质量也可以保持恒定。
2.有人认为,开口系统中系统与外界有物质交换,而物质又与能量不可分割,所以开口系统不可能是绝热系。
对不对,为什么?答:这种说法是不对的.工质在越过边界时,其热力学能也越过了边界。
但热力学能不是热量,只要系统和外界没有热量的交换就是绝热系。
3.平衡状态与稳定状态有何区别和联系,平衡状态与均匀状态有何区别和联系?答:只有在没有外界影响的条件下,工质的状态不随时间变化,这种状态称之为平衡状态。
稳定状态只要其工质的状态不随时间变化,就称之为稳定状态,不考虑是否在外界的影响下,这是它们的本质区别。
平衡状态并非稳定状态之必要条件。
物系内部各处的性质均匀一致的状态为均匀状态。
平衡状态不一定为均匀状态,均匀并非系统处于平衡状态之必要条件。
4.假如容器中气体的压力没有改变,试问安装在该容器上的压力表的读数会改变吗?绝对压力计算公式p = p b+p e(p >p b),p v=p b−p (p b〈p)中,当地大气压是否必定是环境大气压?答:压力表的读数可能会改变,根据压力仪表所处的环境压力的改变而改变。
当地大气压不一定是环境大气压。
环境大气压是指压力仪表所处的环境的压力.5.温度计测温的基本原理是什么?答:温度计随物体的冷热程度不同有显著的变化。
6.经验温标的缺点是什么?为什么?答:任何一种经验温标不能作为度量温度的标准。
由于经验温标依赖于测温物质的性质,当选用不同测温物质的温度计、采用不同的物理量作为温度的标志来测量温度时,除选定为基准点的温度,其他温度的测定值可能有微小的差异。
7.促使系统状态变化的原因是什么?答:系统内部各部分之间的传热和位移或系统与外界之间的热量的交换与功的交换都是促使系统状态变化。
8.(1)将容器分成两部分,一部分装气体,一部分抽成真空,中间是隔板。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
理想气体的性质
1.怎样正确看待理想气体”这个概念?在进行实际计算是如何决定是否可采用理想气体的一些公式?
答:理想气体:分子为不占体积的弹性质点,除碰撞外分子间无作用力。
理想气体是实际气体在低压咼温时的抽象,是一种实际并不存在的假想气体。
判断所使用气体是否为理想气体(1)依据气体所处的状态(如:气体的密度是否足够小)估计作为理想气体处理时可能引起的误差;(2)应考虑计算所要求的精度。
若为理想气体则可使用理想气体的公式。
2.气体的摩尔体积是否因气体的种类而异?是否因所处状态不同而
异?任何气体在任意状态下摩尔体积是否都是0.022414m3/mol?
答:气体的摩尔体积在同温同压下的情况下不会因气体的种类而异;
但因所处状态不同而变化。
只有在标准状态下摩尔体积为0.022414m 3/mol 3•摩尔气体常数R值是否随气体的种类不同或状态不同而异?
答:摩尔气体常数不因气体的种类及状态的不同而变化。
4•如果某种工质的状态方程式为pv二R g T,那么这种工质的比热容、热力学能、焓都仅仅是温度的函数吗?
答:一种气体满足理想气体状态方程则为理想气体,那么其比热容、热力学能、焓都仅仅是温度的函数。
C
5.对于一种确定的理想气体,(C p C v)是否等于定值?」是否为定
C v
值?在不同温度下(C P C v)、C P是否总是同一定值?
C
答:对于确定的理想气体在同一温度下(C p C v)为定值,—p为定值。
C v
C
在不同温度下(C p C v)为定值,—p不是定值。
C v
6.麦耶公式C p C v R g是否适用于理想气体混合物?是否适用于实际
气体?
答:迈耶公式的推导用到理想气体方程,因此适用于理想气体混合物不适合实际气体。
7.气体有两个独立的参数,u(或h)可以表示为P和V的函数,即
u f u(p,v)。
但又曾得出结论,理想气体的热力学能、焓、熵只取决
于温度,这两点是否矛盾?为什么?
答:不矛盾。
实际气体有两个独立的参数。
理想气体忽略了分子间的作用力,所以只取决于温度。
8•为什么工质的热力学能、焓、熵为零的基准可以任选?理想气体的热力学能或焓的参照状态通常选定哪个或哪些个状态参数值?对理想气体的熵又如何?
答:在工程热力学里需要的是过程中热力学能、焓、熵的变化量。
热力学能、焓、熵都只是温度的单值函数,变化量的计算与基准的选取无关。
热力学能或焓的参照状态通常取0K或0C时焓时为0,热力学能值为0。
熵的基准状态取
P b=101325Pa T o=OK熵值为0。
9•气体热力性质表中的h、u及s o的基准是什么状态?
答:气体热力性质表中的h、U及S0的基准是什么状态(T0,F0) T0 0K
P o 101325 Pa 。
示?理想气体在1和2状态间的热力学能变化量、焓变化量如何表
示?若在1-2经过的是不可逆过程又如何?
答:图3-2中阴影部分面积为多变过程 1-2的热量。
对于多变
过程其热力学能变化量及焓变化量可由下面两式计算得到:
1-2的热力学能变化量。
1-2的焓变化量。
10.在如图3-1所示的T-S 图上任意可逆过程
1-2的热量如何表
u C v (T 2 T 1) C/(T 2* T 1)
q v,1 2 h C p (T 2 TJ C p (T 2* TJ q p,12
过初始状态点,做定容线
2-2'图3-3中阴影部分面积为多变过程
过初始状态点,做定压线
2-2'图3-4中阴影部分面积为多变过程
q
8
S 圈3-
3
若为不可逆过程,热力学能、焓不变如上图。
热量无法在图中表示出来。
11•理想气体熵变计算式(3-39)、(3-41)、(3-43)等是由可逆过程导出的,这些计算式是否可用于不可逆过程初、终态的熵变?为什么?
答:可以。
因为熵是状态参数,只与初终状态有关,与过程无关。
12-熵的数学定义式为ds守,比热容的定义式为q妙,故dS竽理想气体的比热容是温度的单值函数’所以理想气体的熵也是温度的单值函数。
这一结论是否正确?若不正确,错在何处?答dS丰中, q rev为一微元可逆变化过程中与热源交换的热量'而
q cdT中q为工质温度升高dT所吸收的热量,他们是不能等同的,
所以这一结论是错误的。
13•是判断下列说法是否正确:(1)气体吸热后熵一定增大()。
(2)气体吸热后温度一定升高()。
(3)气体吸热后热力学能一定升高()。
(4)气体膨胀时一定对外做功()(5)气体压缩时一定耗功()答:(1) 3
14.氮、氧、氨这样的工质是否和水一样也有饱和状态的概念,也存在临界状态?
答:水的汽液饱和状态可以推广到所有的存物质,并且这种液相和气相动态平衡的概念也可以推广到固相和气相及固相和液相,他们的饱
和压力与饱和温度也是----- 对应的。
因此氮、氧、氨为存物质,也有饱和状态的概念,也存在临界状态。
15. 水的三相点的状态参数是不是唯一确定的?三相点与临界点有什 么差异? 答:水的三相点状态参数不是唯一的,其中温度、压力是定值而比体 积不是定值;临界点是唯一的,其比体积、温度、压力都是确定的;
三相点是三相共存的点,临界点是饱和水线与饱和蒸汽线的交点, 在 该点饱和水线与饱和蒸汽线不再有分别。
16. 水的汽化潜热是否为常数?有什么变化规律?
答:水的汽化潜热与压力有关,在一定的范围内压力增加,汽化潜热
减小,当压力达到临界点以上时,汽化潜热为 0
17. 水在定压过程中,温度维持不变,因此,根据 q u w 有人认为
过程中的热量等于膨胀功,即q w ,对不对?为什么?
答:这种说法是不对的。
因为温度不变不表示热力学能不变。
这里分 析的是水,定压汽化有相变,不能作为理想气体来处理,所以u 不能得到q w 这样的结果。
18.有人认为热力学第一定律解析式
q dh vdp 和比热容定义C — dT T2 T 是普遍适用于一切工质的。
进而推论得出水定 哪里?
答:h p C p T2
T 适用于理想气体,不能应用于水定压汽化过程,水 不能作为理想气体来处理。
所以认为
h p c p 压汽化时, 温度不变因此其焓变量
h p C p ; T 0。
这一结论错误在。
