化学计算题练习题基础、提高、难题_汇总(含答案)
【化学】 化学化学计算题专题练习(及答案)含解析

【化学】 化学化学计算题专题练习(及答案)含解析一、中考化学计算题1.实验室有一瓶标签模糊的烧碱溶液,小杰设计实验测定了其溶质质量分数。
请根据下图所示的实验过程和提供的数据进行分析和计算。
(注:滴入酚酞试液的质量忽略不计)(1)将稀盐酸逐滴滴入锥形瓶的过程中,应边滴加边摇动锥形瓶,当观察到溶液颜色恰好___________________时,停止滴加稀盐酸。
(2)通过计算确定该瓶烧碱溶液的溶质质量分数。
(写出计算步骤)___________。
【答案】无色 10% 【解析】 【分析】(1)根据酚酞溶液遇碱性溶液呈红色,遇中性溶液为无色解答;(2)根据化学方程式结合氢氧化钠的质量可以计算出稀盐酸的质量进而就算出其溶质的质量分数。
【详解】(1)在盛有烧碱溶液的锥形瓶中,滴加酚酞试液,溶液变红,逐滴滴入稀盐酸,稀盐酸会和氢氧化钠反应,当氢氧化钠被耗尽时,溶液变为无色。
故答案:无色(2)解:所取烧碱溶液的质量为:60g-20g=40g 设烧碱溶液的溶质质量为x ,2NaOH +HCl =NaCl+H O4036.5x 50g 7.3%⨯ 4036.5507.3%x g =⨯ 0.4x g =该瓶烧碱溶液的溶质质量分数0.4100%10%40gg⨯==答:该瓶烧碱溶液的溶质质量分数为10%。
2.请根据如图所示的实验过程和提供的数据计算。
(1)a 、b 的数值分别为_____、_____。
(2)合金中锌的质量分数为_____。
(3)第二次加入ag 14.6%的稀盐酸充分反应后所得溶液中溶质的质量分数。
_____(写出计算过程,计算结果精确至0.1%) 【答案】50 8.5 90% 24.2% 【解析】 【分析】 【详解】解:(1)由题意可知,第一次和第二次加入稀盐酸后锌有剩余,稀盐酸完全反应,即2ag14.6%的稀盐酸消耗锌粒15g ﹣2g =13g ;故b =15g ﹣13g2=8.5g ;由题意可知: 22+=+65736.514.6%Zn 2HCl ZnCl H g ag ↑⨯65 6.57314.6%g ag =⨯ a =50(2)合金中锌的质量分数为15 1.515g gg- ×100%=90%;(3)设第二次加入ag 14.6%的稀盐酸充分反应后所得溶液中溶质的质量为x ,生成氢气质量为y ,22+=Zn 2HCl Zn +6513621l 52C H g gxy↑-651362152g g x y==-x =27.2g y =0.4g第二次加入ag 14.6%的稀盐酸充分反应后所得溶液中溶质的质量分数:27.2(152)5020.4gg g g g-+⨯-×100%≈24.2%。
【化学】中考化学化学计算题及其解题技巧及练习题(含答案) (2)

【化学】中考化学化学计算题及其解题技巧及练习题(含答案)一、中考化学计算题1.马英同学取某地石灰石样品12g进行测定实验,现将100g稀盐酸分五次加入石灰石样品中(杂质不溶于水也不参与反应),充分反应后测得生成气体的总质量如表所示:第1次第2次第3次第4次第5次加入稀盐酸的质量/g2020202020生成气体的总质量/g 1.1 2.2m 4.4 4.4试求:(1)m的值为______g。
(2)12g石灰石样品中碳酸钙的质量是_____。
(3)所用稀盐酸溶液中溶质的质量分数是_____。
(4)反应完全后最终溶液中氯化钙的质量分数是____。
(结果保留小数点后一位小数)【答案】3.3g。
10g 9.1% 10.5%【解析】【详解】(1)分五次加入盐酸后,前两次,每次都增加1.1g二氧化碳,第四、五都生成4.4g二氧化碳,说明第三次没有完全反应,也增加1.1g,所以m值是3.3g;故填:3.3;(2)设参加反应的碳酸钙质量为x;第4次反应完全后用去稀盐酸的溶质的质量为y;第4次反应完全后生成氯化钙的质量为z,10073111==x y z解得x=10g,y=7.3g,z=11.1g,故填10g;(3)稀盐酸的溶质质量分数:7.3g×100%9.1%80g≈,故填9.1%;(4)反应完全后最终溶液中氯化钙的质量分数:11.1g100%10.5%10g+100g-4.4g≈⨯,故填10.5%;答:m的值为3.3g;12g石灰石样品中碳酸钙的质量是10g;所用稀盐酸溶液中溶质的质量分数9.1%;反应完全后最终溶液中氯化钙的质量分数10.5%。
2.某氢氧化钠样品中含有少量的碳酸钠杂质。
现取20g 样品于烧杯中,加入180g 水使其完全溶解,再向其中逐滴加入稀盐酸至过量,测得生成气体质量与所加稀盐酸质量关系如图所示,请回答下列问题:(1)下图中0—A 无气体产生,说明盐酸优先跟样品中的_____(填化学式)发生反应。
(化学)初中化学化学计算题解题技巧讲解及练习题(含答案)

(化学)初中化学化学计算题解题技巧讲解及练习题(含答案)一、中考化学计算题1.现将100 g溶质质量分数为9.8%的稀硫酸与一定质量的氯化钡溶液恰好完全反应后,过滤得到284.7 g滤液。
计算:(1)生成硫酸钡沉淀的质量。
(2)氯化钡溶液中溶质的质量分数。
【答案】(1)生成硫酸钡沉淀的质量为23.3 g。
(2)氯化钡溶液中溶质的质量分数为10%。
【解析】试题分析:解:设生成硫酸钡沉淀的质量为x,反应的氯化钡的质量为y。
H2SO4质量为:10 0g×9.8%=9.8 gBaCl2 + H2SO4 = BaSO4↓ + 2HCl208 98 233y9.8 g x233/98 =x/9.8x=23.3 g208/98 =y/9.8y=20.8 g(2)氯化钡溶液的质量为:284.7 g+23.3 g-100 g=208 g氯化钡溶液的溶质质量分数为:20.8 g/208 g×100%=10%考点:根据化学方程式的计算溶质的质量分数2.向13.6g碳酸钠和氯化钠的固体混合物滴加稀盐酸,所加稀盐酸质量与生成气体质量的关系如图所示。
计算:(1)固体混合物中碳酸钠的质量。
(2)该稀盐酸中溶质的质量分数。
(3)恰好完全反应时所得的溶液中溶质的质量分数。
(计算结果精确至0.1%)【答案】(1)10.6克(2)10%(3)17.9%【解析】试题分析:设固体混合物中Na2CO3的质量为x,稀盐酸中溶质的质量为y,反应生成NaCl 的质量为z。
Na2CO3+ 2HCl ="=" 2NaCl + H2O + CO2↑106 2×36.5 2×58.5 44x y z 4.4g得x=10.6克稀盐酸中溶质的质量分数为:恰好完全反应时所得的溶液溶质质量分数为:考点:根据化学方程式的计算 物质的质量分数3.将含有杂质(不溶于水)的氯化钡样品12.5g 放入39.6g 水中充分搅拌,完全溶解后过滤。
高中化学计算题学霸总结(含答案)

高中化学计算题学霸总结(含答案)高中化学计算题学霸总结(含答案)阳光老师:祝你学业有成一、计算题(本大题共30小题,共240.0分)1.把铁、铝混合物溶于盐酸中,反应后盐酸的浓度变为,溶液体积变化忽略不计。
求反应中消耗HCl的物质的量和该混合物中铝、铁的物质的量。
答案】消耗HCl的物质的量:设Al、Fe的物质的量分别为x、y。
2Al + 6HCl → 2AlCl3 + 3H2↑Fe + 2HCl → FeCl2 + H2↑根据反应方程式,消耗HCl的物质的量为2x + y。
该混合物中铝、铁的物质的量:根据题意,铝、铁混合物中铝、铁的质量比为2:3,设铝、铁的质量分别为m1、m2,则有:m1/m2 = 2/3m1 + m2 = 100g解得m1 = 40g,m2 = 60g铝、铁的相对原子质量分别为27和56,所以它们的物质的量分别为x = 1.48mol,y = 1.07mol。
解析】本题考查物质的量的计算,难度不大,解题的关键是对物质的量公式的熟练应用。
2.在由Na2CO3和NaHCO3组成的混合物中加入足量盐酸充分反应后,收集CO2的质量分数。
不考虑溶解,试计算原混合物中Na2CO3的质量分数。
答案】原混合物中Na2CO3的质量分数为。
设Na2CO3的物质的量为x,NaHCO3的物质的量为y。
Na2CO3 + 2HCl → 2NaCl + CO2↑ + H2ONaHCO3 + HCl → NaCl + CO2↑ + H2O根据反应方程式,CO2的物质的量为x + y。
CO2的质量分数为:答:原混合物中Na2CO3的质量分数为。
解析】本题考查质量分数的计算,掌握物质的性质和质量分数的计算方法是解答该题的关键,试题较容易。
3.计算质量比为51:32:34的C6H5OH、CH3OH、C2H5OH,其物质的量之比为______,它们所含氢原子数之比为______,所含质子数之比为______。
有含为,则C6H5OH 的摩尔质量为______,R的相对原子质量为______。
初中化学化学计算题及其解题技巧及练习题(含答案)及解析
初中化学化学计算题及其解题技巧及练习题(含答案)及解析一、中考化学计算题1.某石化厂有一种石油产品含有质量分数为4.9%的残余硫酸,过去他们都是用NaOH溶液来清洗这些硫酸。
请你计算:(1)若要清洗1000kg的这种石油产品,需要_____kg的NaOH。
(2)该石化厂进行了技术改造,采用Ca(OH)2中和这些残余硫酸。
每处理1000kg这种产品,他们可以节约多少经费_____?请你写出具体的计算过程。
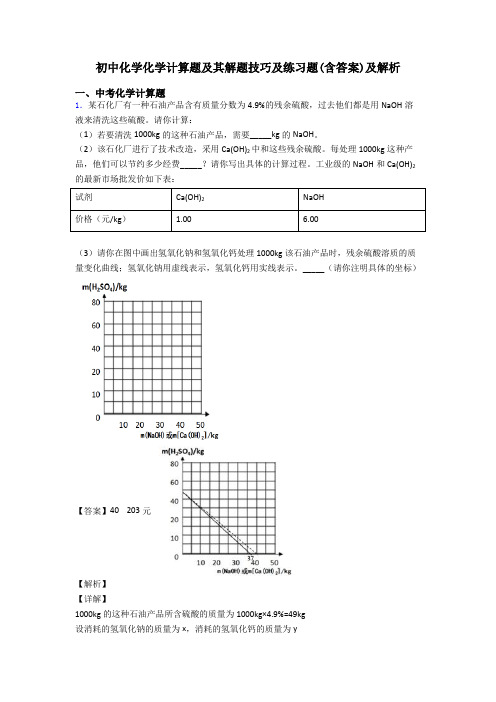
工业级的NaOH和Ca(OH)2的最新市场批发价如下表:试剂Ca(OH)2NaOH价格(元/kg) 1.00 6.00(3)请你在图中画出氢氧化钠和氢氧化钙处理1000kg该石油产品时,残余硫酸溶质的质量变化曲线;氢氧化钠用虚线表示,氢氧化钙用实线表示。
_____(请你注明具体的坐标)【答案】40 203元【解析】【详解】1000kg的这种石油产品所含硫酸的质量为1000kg×4.9%=49kg设消耗的氢氧化钠的质量为x,消耗的氢氧化钙的质量为y根据2NaOH+H2SO4=Na2SO4+2H2O和Ca(OH)2+H2SO4=CaSO4+2H2O可得关系式为242 2NaOH H SO Ca(OH)809874x49kg y::809874==x49kg yx=40kgy=37kg每处理1000kg这种产品,他们可以节约经费为6.00元/kg×40kg-1.00元/kg×37kg=203元图中画出用氢氧化钠和氢氧化钙处理1000kg该石油产品时,残余硫酸溶质的质量变化曲线;氢氧化钠用虚线“…”表示,氢氧化钙用实线“一”表示,答:(1)若要清洗1000kg的这种石油产品,需要 40kg的NaOH。
(2)该石化厂进行了技术改造,采用Ca(OH)2中和这些残余硫酸。
每处理1000kg这种产品,他们可以节约203元经费。
(3)残余硫酸溶质的质量变化曲线;氢氧化钠用虚线“…”表示,氢氧化钙用实线“一”表示,2.现有一份氧元素质量分数为 89.5%的过氧化氢溶液,加入 MnO2充分反应后,得到液体的质量为 90g(不考虑操作过程中液体的损失),则生成氧气的质量为________________g(精确到小数点后 1 位)。
初中化学计算题及答案

初中化学计算题及答案
计算题1:
题目:已知一瓶酒精溶液体积为200毫升,浓度为60%,求其中含有酒精的质量是多少?
解答:首先需要知道酒精溶液的浓度是指溶液中酒精的质量与溶液的总质量的比值,以百分比表示。
浓度等于酒精的质量除以溶液的体积。
所以,酒精的质量 = 浓度 * 溶液的体积。
= 60% * 200毫升
= 0.6 * 200毫升
= 120毫升
故其中含有酒精的质量为120毫升。
计算题2:
题目:已知一块铁块的体积为200立方厘米,密度为7.8克/立方厘米,求该铁块的质量是多少?
解答:密度是物质的质量与单位体积的比值,以克/立方厘米表示。
所以,质量等于密度乘以体积。
所以,铁块的质量 = 密度 * 体积
= 7.8克/立方厘米 * 200立方厘米
= 1560克
故该铁块的质量为1560克。
2020-2021中考化学压轴题之计算题(中考题型整理,突破提升)含答案

一、中考初中化学计算题1.工业生产的纯碱中常含有少量氯化钠杂质,现称取12 g 纯碱样品于烧杯中,加入水使其完全溶解,逐渐加入氯化钙溶液至过量,测得加入氯化钙溶液的质量与生成沉淀的关系如下图所示。
(反应的化学方程式:CaCl 2+Na 2CO 3=CaCO 3↓+2NaCl)(1)计算样品中碳酸钠的质量分数________(要求写出计算过程,精确到0.1%)。
(2)若要计算氯化钙溶液中溶质的质量分数,可使用上图中_____点的一组数据(填标号)。
【答案】(1)88.3%;(2)a (或 b ) 【解析】由图可以看出生成的碳酸钙的质量为10g ,设碳酸钠的质量为x2233CaCl +Na CO ==CaCO 2NaCl ↓+106 100 x 10g10610010x g = x =10.6g样品中碳酸钠的质量分数为10.6100%88.3%12.0gg⨯≈,当求算氯化钙溶液中质量分数时,由于50g 氯化钙溶液对应的沉淀为4g ,125g 氯化钙溶液对应的沉淀为10g 都是氯化钙完全反应,所以可以根据a 点或者b 点数据计算。
答:(1)计算样品中碳酸钠的质量分数约为88.3%;(2)若要计算氯化钙溶液中溶质的质量分数,可使用图中曲线上示出的点a 或者b 所对应的数据。
2.把2.4g 镁加入到一定质量的硫酸中,反应完毕后,向溶液中滴加质量分数为10%的NaOH 溶液,一段时间后有白色沉淀生成。
加入NaOH 溶液与生成沉淀质量的关系如图。
(1)计算与2.4g镁反应的H2SO4的质量是多少?________(请在答题卡上写出计算过程)(2)加入NaOH溶液____g时,开始生成沉淀;图中a的数值为____。
(3)利用上述计算结果,若将NaOH溶液改用Ba(OH)2溶液并逐滴加入上述镁与硫酸反应后的溶液中至不再产生沉淀为止,过滤、洗涤、烘干,得到沉淀的质量为____g。
【答案】9.8g8016052.4【解析】【分析】Mg+H SO==MgSO+H↑,根据反应的质量比即可计算出参(1)利用化学方程式:2442加反应的硫酸的质量;(2)镁与稀硫酸反应后的溶液中滴加氢氧化钠溶液,一段时间后才产生白色沉淀,说明与镁反应的稀硫酸是过量的,氢氧化钠先与稀硫酸反应,再与硫酸镁反应生成氢氧化镁沉淀。
(化学)初三化学化学计算题解题技巧及经典题型及练习题(含答案)含解析

(化学)初三化学化学计算题解题技巧及经典题型及练习题(含答案)含解析一、中考化学计算题1.现有l00g 8%的NaOH溶液,通过计算回答下列有关问题:(1)若用该溶液吸收CO2,最多可以生成Na2CO3多少克?____(写出详细计算过程)(2)当NaOH全部转化成为Na2CO3后,Na2CO3还会继续与CO2、H2O发生反应:Na2CO3+CO2+H2O=2NaHCO3,直至Na2CO3完全反应完。
请在如图画出利用l00g8%的NaOH 溶液吸收CO2与生成NaHCO3的曲线。
____(3)现有三种溶液:①100g8%NaOH溶液、②100g8%NaOH溶液吸收CO2转化为Na2CO3溶液、③100g8%NaOH溶液吸收过量CO2转化为NaHCO3溶液,分别用相同质量分数的硫酸与上述三种溶液恰好完全反应,需要的硫酸的质量_____(选填“相等”或“不相等”),原因是_____。
【答案】10.6g 相等三种溶液中所含的钠元素质量相等,与硫酸反应产生的Na2SO4质量相等,故消耗同种硫酸的质量相等【解析】【详解】(1)100g8%的NaOH溶液中含NaOH的质量=100g×8%=8g(2)设碳酸钠的质量为x,与氢氧化钠反应的二氧化碳的质量为y,碳酸氢钠的质量为z,和碳酸钠反应的二氧化碳的质量为a根据2NaOH+CO2=Na2CO3+H2O和 Na2CO3+CO2+H2O=2NaHCO3,可得关系式为:22323 2NaOH~CO~Na CO CO~2NaHCO8044106441688g y x a z804410644168====8g y x a zx=10.6gy=4.4gz =16.8ga=4.4g利用l00g8%的NaOH溶液吸收CO2与生成NaHCO3的曲线,起点4.4、拐点(8.8,16.8)。
如图:(3)三种溶液中所含的钠元素质量相等,根据钠元素守恒和硫元素守恒,可知与硫酸反应产生的Na2SO4质量相等,故消耗同种硫酸的质量相等。
中考化学初中化学题型强化提升:计算题(含答案)

中考化学初中化学题型强化提升:计算题学校:___________姓名:___________班级:___________考号:___________一、选择题1.某金属混合物样品由Mg 、Al 、Fe 、Cu 中的两种或三种组成。
2.8g 该样品与足量的稀盐酸反应生成0.2g 氢气,则该混合物的组成不可能是A .Mg 、AlB .Al 、CuC .Mg 、Fe 、CuD .Al 、Fe 、Cu2.将9.0g 氢氧化亚铁和氧化亚铁的混合物加入100g 稀硫酸中,二者恰好完全反应,则该稀硫酸中溶质的质量分数可能为A .B .C .D .3.一定量的木炭在盛有由氮气和氧气组成的混合气体的密闭容器中燃烧后生成和,测得反应后所得、、的混合气体中碳元素的质量分数为24%,则反应后氮气的质量分数可能为A .12%B .36%C .44%D .72%4.现有两种金属组成的混合物,在2.4g 该混合物中加入100g 一定溶质质量分数的稀盐酸,两者恰好完全反应,产生氢气的质量为m 。
下列说法正确的是A .若混合物为Mg 、Al ,m 可能是0.2gB .若混合物为Fe 、Zn ,m 可能是0.2gC .若混合物为Zn 、Al ,m 可能是0.2gD .若混合物为Fe 、Al ,则稀盐酸中溶质质量分数一定等于3.65%5.在100g 浓度为ω%的稀硫酸中加入4g 氧化铜粉末,待氧化铜全部溶解后,向所得蓝色溶液中加入10g 铁粉,充分反应后过滤,得滤液和5.2g 滤渣。
下列计算结果正确的是A .5.2g 滤渣是由3.2g 铜和2g 铁组成的B .滤液是25%的硫酸亚铁溶液C .反应过程中产生的氢气是0.286gD .ω=106.将2.0g 的两种物质的混合物与足量的稀盐酸反应,共生成0.2g 的氢气,混合物中一种是铁,另外一种物质可能是A .锌B .镁C .铜D .铝4.9%8.6%10.2%13.5%CO 2CO CO 2CO 2N7.某气体中可能含有CO2、O2、N2中的一种或几种,将该气体依次通过:①炽热的焦炭、②足量灼热的氧化铜、③足量碱石灰(氢氧化钠和氧化钙的混合物)。
初三化学计算题专题复习

计算题专题复习(提高篇)可能用到的相对原子质量:Mn—55;Mg—24;Fe—56;Zn—65;Al—27;Ca—40;Cl —35.5;K—39;Cu—64;H—1;O—16;C—12;Na—23;S—32;N—14;Si—28;Ba—137 一、平均值型计算选择题:例1:两种金属粉末的混合物30克,与足量的稀硫酸反应,只生成氢气1克,则这种混合物中的两种金属可能是()A.Mg Al B.Zn Fe C.Mg Fe D.Al Fe【同题链接】1、一种不纯的铁,已知它含有铜、钙、镁的一种或几种金属杂质,5.6g这样的铁跟足量的稀H2SO4反应时,生成H20.2g,则该铁样品中一定含有的金属杂质是()A.铜 B.镁 C.铝 D.钙2、把含有某一种氯化物杂质的氯化镁粉末95g溶于水后加入足量的AgNO3溶液,完全反应后生成白色沉淀300g,则氯化镁中的杂质可能是()A.NaCl B.AlCl3 C.KCl D.CaCl23、在某铁的样品中可能含有Zn、Mg、Al、Cu等杂质金属中的2种,取5.6g样品跟足量稀硫酸反应,得到0.20gH2,则此铁的样品中不可能含有的杂质金属组是()A. Cu和MgB. Zn和AlC. Mg和AlD. Zn和Cu4、某不纯的氯化铵样品中,测得其中氮元素的质量分数为28%,则混主的一种杂质可能是①NH4HCO3②(NH4)2SO4③NH4NO3④CO(NH2)2()A.只有① B.①③ C.②③ D.无法确定二、估算型选择题例2:20g20%的NaOH溶液与20g20%的H2SO4溶液充分反应后,滴入紫色石蕊试液是()A.蓝色 B.紫色 C.红 D.无色【同题链接】1、相同质量的下列的物质中,铁的质量分数最高的是()A.FeS B.FeCO3 C.Fe2O3 D.Fe3O42、由二氧化硫和三氧化硫组成的混合气体中,硫元素与氧元素的质量比可能是()A. 1∶1B. 1∶1.25C. 1∶1.5D. 1∶23、由碳和氧两种元素组成的气体,经测定碳与氧两种元素的质量比为3:5,该气体是()A.混合物B.纯净物C.化合物D.有机物三、特殊规律型选择题例3:某甲醛(HCHO)溶液中氢元素的质量分数为10%,则碳元素的质量分数正确的是()A.12% B.10% C.8% D.6%【同题链接】1、已知NaHS、MgSO4、和NaHSO3由组成的混合物中硫元素的质量分数为20%,则氧元素的质量分数为()A.35%B.25%C.65%D.无法计算2、将Na、Mg、Al分别放入盐酸溶液中,反应结束后,放出氢气质量相同,其原因是()A.放入Na、Mg、Al的质量相同B.放入Na、Mg、Al的质量比是23:12:9和足量盐酸反应C.放入过量的Na、Mg、Al,而盐酸为同质量分数、同体积、同质量。
初中化学计算题(带答案)

初中化学计算题一、根据化学式的计算1、计算相对分子质量相对分子质量=化学式中各原子的相对原子质量的总和。
点拨:①计算物质的相对分子质量时,同种元素的相对原子质量与其原子个数是相乘的关系,不同种元素相对质量是相加的关系。
②计算结晶水合物的相对分子质量时,化学式中的“·”表示相加,而不表示相乘。
③化学式中原子团(或根)右下角的数字表示的是原子团(或根)的个数。
计算时先求一个原子团或根的总相对原子质量,再乘以原子团(或根)的个数,即得出几个原子团的总相对原子质量。
2、计算物质中各元素的质量比组成化合物的各元素的质量比=化合物中各元素的相对原子质量总和(即相对原子质量与原子个数乘积)之比。
点拨:①计算时一定要写清楚各元素质量比顺序,因顺序不同,比值也不同。
②计算时的结果约成最简整数比。
3、计算物质中某元素的质量分数化合物中某元素的质量×100%4、已知某化合物的质量,求某元素的质量化合物里某元素的质量=化合物的质量×化合物中某元素的质量分数化合物的质量=化合物中已知元素的质量÷化合物中已知元素的质量分数5、求化学式点拨:求物质化学式的主要类型:①由元素的相对原子质量和化合物的相对分子质量,确定化学式。
②根据化合物中某元素质量分数确定化合物的化学式。
③已知化合物中元素的质量比和相对原子质量,确定化学式。
原子个数比=元素的质量比:相对原子质量比④根据质量守恒定律确定化学式。
6、计算不纯物中某元素(或某纯净物)的质量分数计算公式:①某纯净物的质量分数= ×100%②不纯物中某元素的质量分数=不纯物中纯净物的质量分数×该纯净物中某元素的质量分数。
③某纯净物的质量分数=实际上某元素的质量分数÷化学式中该元素的质量分数×100%二、根据化学方程式的计算根据化学方程式的计算就是从量的方面来研究物质变化的一种重要的方法,其计算步骤和方法,一般分为以下几步: ①设未知量,未知量不带单位,常用X 表示.②根据题意确定反应物与生成物,写出并配平反应的化学方程式. ③在有关物质化学式下面写出相对分子质量并代入已知量和所设未知量. ④列比例式求解,写出答案.在初中阶段,根据化学方程式的计算,主要有以下几种基本类型.(1)根据化学方程式计算反应物、生成物间的质量比反应物、生成物间的质量比,就是各反应物、生成物相对分子质量×计量数之比. (2)根据化学方程式计算反应物或生成物的质量反应物或生成物质量的计算,一般是根据化学方程式中各反应物、生成物间的质量比来求算的,对某些反应,可直接依据质量守恒定律进行计算.(3)根据化学方程式进行含有一定且杂质的反应物或生成物的计算根据化学方程式的计算,其反应物或生成物的质量必须是纯物质的质量.含有一定量杂质的反应物或生成物的质量,必须换算成纯物质的质量,才能按根据化学方程式的计算步骤和方法进行计算.纯物质质量=含有一定量杂质的物质质量×该物质质量分数三、有要溶液组成的计算1.用溶质所占溶液的质量分数表示溶液的组成,其关系如下:溶质的质量分数= 溶质质量溶质+溶剂 × 100%=溶液质量溶质质量 × 100%在饱和溶液中: 溶质的质量分数=+溶解度溶解度g 100 × 100%2、有关溶液加水稀释的计算在溶液加水稀释过程中,溶质的质量分数将随溶液的稀释而改变,溶质质量分数一定的溶液加水稀释,稀释前后溶质的总质量不会发生改变.溶液加水稀释的计算,根据的就是这个道理.M 浓溶液×浓溶液的溶质质量分数=M 稀溶液×稀溶液的溶质质量分数 =(M 浓溶液+M 水)×稀溶液的溶质质量分数 3、溶质的质量分数在化学方程式的应用反应后溶液的质量=反应物的总质量(包含溶液的质量)-生成气体或沉淀的质量四、综合计算题分类解析从近几年全国各地的中考化学试题来看,化学计算已经走出了“为计算而计算”的考查误区,考题所涉及的内容更加注重与日常生活、工农业生产的联系;更加注重对同学们图表、数据、信息、实验综合分析能力的考查。
初三化学考试 计算题25道(附答案)

25基础计算1.在一个实验室中发现一橡胶球可以漂浮在0.5mol/L的NaCl溶液表面,求该NaCl溶液的密度。
答案:1.018g/mL。
解析:根据阿威休斯定律得到:Fb=FgρVg=m*gρ=m/V=(Vg*g)/V=(Fg/Ag*g)/V=(4πr^3/3*g)/[(4/3)*π*r^3]=3/4*r*g=7.35*10^-5*g其中,Ag为橡胶球跟水接触的面积,r为橡胶球半径,g为重力加速度。
因此,NaCl溶液的密度为:ρNaCl=ρwater+ρball=1.000g/mL+7.35*10^-5*g/mL=1.018g/mL。
2.一种饱和食盐水的密度为1.20g/mL,问在哪个温度下它的浓度为26%。
答案:56.8°C。
解析:首先,要知道饱和食盐水在不同温度下的密度变化情况,参考表格得出如下数据:温度(°C)密度(g/mL)01.091101.078201.064301.049401.033501.015600.996700.975800.951900.9241000.895然后,根据浓度的定义可知:浓度=质量/总质量总质量=质量/浓度因为食盐水是饱和的,所以其浓度为100%。
设实验时食盐水的质量为m,则总质量为m/1.20,其中1.20为食盐水的密度。
根据题意,浓度为26%,所以食盐的质量为0.26*(m/1.20)。
由此0.26*(m/1.20)=m/(1.20+Δρ)其中Δρ为实验时食盐水的密度与需要求的密度的差值。
将参考表格中的数据代入上式计算,得到Δρ为0.325g/mL。
解方程得出:Δρ=0.325=0.26*m/(1.20+Δρ)m=68.45g因此,实验时食盐水的质量为68.45g。
而在哪个温度下其密度为1.20*0.26=0.312g/mL呢?查表可得,在56.8°C时,食盐水的密度约为0.312g/mL,因此答案为56.8°C。
初中化学九年级上计算题汇总(附参考答案与试题解析)

初中化学九年级上计算题汇总一.计算题(共50小题)1.用容积为45mL的试管给液体加热时,最多可盛液体的体积数是多少?若用容积为180mL的酒精灯给物质加热,则酒精灯内的酒精不超过多少毫升?2.甲同学用托盘天平称量10.2g食盐时(1g以下用游码),称后发现砝码放在左盘,食盐放在了右盘,所称食盐的实际质量是g。
3.甲学生用量筒量取液体,量筒摆放平稳,面对刻度,他先俯视读数为48mL,倾倒出部分液体后,又仰视读数为40mL,则该同学实际倒出的液体的体积是8mL(用“>”“<”“=”填空)。
4.小红同学用托盘天平称量物质的质量,砝码质量为25g,游码示数为2.8g。
(1)若称量时正确放置,则物质的质量为g。
(2)若称量后发现砝码的位置放反了,则物质的实际质量为g。
5.某同学用托盘天平称量固体物质时;把固体物质放在右盘,砝码放在左盘,称得固体物质的质量为10.8g(1克以下用游码),如果按正确的方法称量,这位同学所称固体的实际质量是多少克?6.小明做实验时要称8.3g的氯化钠固体,但他称时把药品和砝码放反了,他称药品时0.1g以下用游码,则他称到的氯化钠固体的实际质量为g;他量取水时先俯视读数为18mL,倒出一部分水后仰视读数为5mL,则他实倒出的水13mL,(填“大于”或“小于”或“等于”或“不确定”)。
7.某同学在称量46.5g(5g以下用游码)食盐时刚好将食盐与砝码放反了,其他操作完全正确,则所称量的食盐的实际质量是g。
8.体积50L的空气中含氧气的质量是多少g?(已知氧气的密度是1.43g/L.精确到0.1g)9.小明发现:收集的氧气占集气瓶容积的60%(空气占40%)时,能使带火星的木条复燃。
那么,使带火星的木条复燃的氧气的浓度最低值是多少呢?小明对此展开探究:第一组实验:取5支集气瓶,编号为①②③④⑤,分别装入其总容积10%、20%、30%、40%、50%的水。
用排水法收集氧气恰好把5只瓶子中的水排去,将带火星的木条依次插入①~⑤号瓶中,记录实验现象。
初中化学化学计算题常见题型及答题技巧及练习题(含答案)含解析

初中化学化学计算题常见题型及答题技巧及练习题(含答案)含解析一、中考化学计算题1.某化学兴趣小组的同学在实验室配制溶质质量分数为8%的氢氧化钠溶液,并用其测定某稀盐酸中溶质的质量分数。
下图表示用该氢氧化钠溶液与10g某稀盐酸发生反应时溶液温度的变化情况。
试计算稀盐酸中溶质的质量分数。
【答案】14.6%【解析】试题分析:由于中和反应放热,故随着反应的进行,溶液的温度逐渐升高,直至反应恰好完全,溶液温度达到最高,故根据图示可判断,当加入氢氧化钠那溶液的质量为20g时,反应恰好完全解:分析图知与10g稀盐酸恰好完全反应的氢氧化钠质量为:20g×8%=1.6g设稀盐酸中溶质的质量为xNaOH+HCl=NaCl+H2O40 36.51.6g x40:1.6g=36.5:xx=1.46g稀盐酸中溶质的质量分数为:1.46g/10g=14.6%答:稀盐酸中溶质的质量分数为14.6%考点:根据化学方程式计算2.BaCl2是一种重金属盐,其水溶液具有很强的毒性。
若误服了BaCl2溶液可立即服用MgSO4溶液解毒。
为测定某BaCl2溶液的溶质质量分数,现取100克BaCl2溶液,不断加入MgSO4溶液,反应过程中溶液总质量与加入MgSO4溶液的质量关系如图所示,请回答:(1)P 点时溶液中的溶质名称是_________________; (2)反应生成沉淀的最大质量为_________________克;(3)试计算原溶液中BaCl 2溶液的溶质质量分数为_________________。
【答案】MgCl 2 23.3g 20.8% 【解析】 【分析】 【详解】(1)当硫酸镁溶液的质量加到100g 时,溶液总质量出现拐点,此后随着硫酸镁溶液的增加,溶液总质量增加,不再产生新的变化。
故P 点时硫酸镁溶液与氯化钡溶液恰好完全反应生成硫酸钡沉淀和氯化镁。
因此P 点时溶液中的溶质名称是氯化镁; (2)由图可知,反应生成沉淀的最大质量为100g+100g-176.7g=23.3g ; (3)设原BaCl 2溶液的溶质质量分数为x2442BaCl +MgSO =BaSO +MgCl 208233100g x23.3g↓⨯ 208233=100g x 23.3g⨯x=20.8%答:原BaCl 2溶液的溶质质量分数为20.8%。
(化学)初中化学化学计算题及其解题技巧及练习题(含答案)含解析

(化学)初中化学化学计算题及其解题技巧及练习题(含答案)含解析一、中考化学计算题1.为测定某样品中锌的质量分数,取10g此样品,分五次向其中加入稀硫酸使之充分反应(假设锌的样品中杂质不与稀硫酸反应,且不溶于水),每次加入的稀硫酸质量及测定剩余固体的质量,记录数据如下表:第一次第二次第三次第四次第五次加入稀硫酸的质量/g1010101010剩余固体质量/g8.4 6.8 5.2 3.6 3.6请认真分析表中的数据,回答下列问题:(1)表示样品与稀硫酸恰好完全反应的是上表中第________次操作;(2)计算样品中锌的质量分数;(3)计算实验中所用稀硫酸的溶质质量分数。
【答案】(1)4(2)锌的质量分数(3)设恰好完全反应时消耗硫酸的质量为x【解析】本题考查的是实验数据处理的探究和根据化学反应方程式的计算。
(1)根据金属活动性,锌在活动性顺序中处于H之前,能与稀硫酸反应,而锌的样品中杂质不与稀硫酸反应,且不溶于水。
由记录数据表可知:第五次加入10g稀硫酸时,剩余固体质量不变仍为3.6g,说明混合物中的锌在第四次加酸后就已完全反应,剩余固体为不与硫酸反应的杂质。
另据上表可见,前三次中每加入10g的稀硫酸,都消耗1.6g的锌,二者结合分析故知第四次恰好完全反应。
(2)则样品中锌的质量分数m=(3)设恰好完全反应时消耗硫酸的质量为x65 98 (10﹣3.6) X 65/98=(10﹣3.6)/x X=9.6g∴所用稀硫酸的溶质质量分数==24℅2.现有一份氧元素质量分数为 89.5%的过氧化氢溶液,加入 MnO 2 充分反应后,得到液体的 质量为 90g(不考虑操作过程中液体的损失),则生成氧气的质量为________________g(精确到小 数点后 1 位)。
【答案】 5.2【解析】解法一:设生成氧气的质量为x ,过氧化氢溶液的质量为y ,根据反应前后氧元素的质量不变可得关系式:①y -90g=x ,②y 89.5%=x+90g100%,x=5.2g ,答:生成氧气的质量为5.2g 。
(化学)初三化学化学计算题常见题型及答题技巧及练习题(含答案)

(化学)初三化学化学计算题常见题型及答题技巧及练习题(含答案)(化学)初三化学化学计算题常见题型及答题技巧及练习题(含答案)⼀、中考化学计算题1.化学兴趣⼩组的同学⽤⼀瓶含有少量氯化钠和氯化钙的固体混合物进⾏下列实验:取样品14 g,放⼊烧杯中,加⼊96 g碳酸钠溶液恰好完全反应后过滤,称得滤液的总质量为100 g。
(1)根据质量守恒定律,可知⽣成沉淀的质量为___________________________。
(2)固体混合物中氯化钙的质量是___________?(3)所得滤液中溶质的质量分数是__________?【答案】10 g 2.9 g 14.6%【解析】(1) 、根据质量守恒定律可知,反应前物质质量总和=反应后物质质量总和,即反应前所有混合物的总质量=滤液的总质量+⽣成沉淀的质量;(2)、根据化学⽅程式中各物质之间的质量⽐,利⽤碳酸钙沉淀的质量,列出⽐例式,即可计算出固体混合物中氯化钙的质量。
(3) 、根据题意,反应完全后过滤,所得滤液为氯化钠溶液,滤液中的溶质NaCl包括混合物中原有的NaCl和反应⽣成的NaCl;根据上述⽅程式可以求出⽣成NaCl的质量,⽽混合物中原有的NaCl的质量=混合物总质量-氯化钙的质量,据此可以计算出滤液中溶质的质量,然后根据溶质质量分数= 溶质质量溶液质量×100%计算即可。
解:(1) 、根据质量守恒定律,⽣成沉淀的质量=14g+96g-100g=10g;(2)、设固体混合物中含氯化钙的质量为x,反应后⽣成氯化钠的质量为y。
Na2CO3+CaCl2=CaCO3↓+2NaCl111 100 117x 10g y111100117=10x g y=解得,x=11.1g y=11.7g(3) 、原混合物中含氯化钠的质量=14g-11.1g=2.9g则所得滤液中溶质的质量分数=2.911.7100g gg+×100%=14.6%答:(2)、原固体混合物中氯化钙的质量为11.1g;(3) 、所得滤液中溶质的质量分数为14.6%。
中考化学计算题(大题培优 易错 难题)含答案

一、中考初中化学计算题1.为测定石灰石样品中碳酸钙的含量,小明取25g 石灰石样品与一定质量的14.6%的稀盐酸恰好完全反应,将反应所得混合物蒸干得到固体27.2 g (不含结晶水,假设样品中的杂质既不与稀盐酸反应)。
试计算: (1)参加反应的盐酸的质量______。
(2)石灰石样品中碳酸钙的含量______。
【答案】100g 80% 【解析】 【分析】 【详解】设样品中杂质的质量为x ,反应消耗盐酸的为y3222CaCO +2HCl =CaCl +CO +H O1007311125g-x14.6%y 27.2g-x↑⨯ 10073111==25g-x 14.6%y 27.2g-x ⨯ x=5g y=100g石灰石样品中碳酸钙的质量分数为25g-5g100%=80%25g⨯ 答:样品中碳酸钙的含量为80%,反应消耗盐酸的为100g 考点:根据化学方程式的计算2.将Na 2CO 3和NaCl 固体混合物32.9g 放入烧杯中,此时总质量为202.9g ,加入326.9g 盐酸,恰好完全反应,待没有气泡逸出后再次称量,总质量为521.0g .计算所得溶液中溶质的质量分数______(CO 2的溶解忽略不计). 【答案】10 【解析】 【分析】首先根据质量守恒定律:化学反应前后,物质的质量不变,可先求出产生的气体二氧化碳的质量=202.9g+326.9g-521.0g=8.8g ,再根据化学反应方程式:Na 2CO 3+2HCl=2NaCl+H 2O+CO 2↑可知,反应后所得溶液中溶质是NaCl ,但NaCl 来自两部分,一是反应生成的,二是原固体混合物中含有的,生成的NaCl 可通过化学方程式来求解,原固体混合物中含有的NaCl 可通过混合物32.9g 减去Na 2CO 3的质量 【详解】解:根据质量守恒定律,反应生成的CO 2质量=202.9g+326.9g-521.0g=8.8g 设Na 2CO 3的质量为x ,生成的NaCl 的质量为y 。
九年级化学化学计算题常见题型及答题技巧及练习题(含答案)含解析

九年级化学化学计算题常见题型及答题技巧及练习题(含答案)含解析一、中考化学计算题1.某石化厂有一种石油产品含有质量分数为4.9%的残余硫酸,过去他们都是用NaOH溶液来清洗这些硫酸。
请你计算:(1)若要清洗1000kg的这种石油产品,需要_____kg的NaOH。
(2)该石化厂进行了技术改造,采用Ca(OH)2中和这些残余硫酸。
每处理1000kg这种产品,他们可以节约多少经费_____?请你写出具体的计算过程。
工业级的NaOH和Ca(OH)2的最新市场批发价如下表:试剂Ca(OH)2NaOH价格(元/kg) 1.00 6.00(3)请你在图中画出氢氧化钠和氢氧化钙处理1000kg该石油产品时,残余硫酸溶质的质量变化曲线;氢氧化钠用虚线表示,氢氧化钙用实线表示。
_____(请你注明具体的坐标)【答案】40 203元【解析】【详解】1000kg的这种石油产品所含硫酸的质量为1000kg×4.9%=49kg设消耗的氢氧化钠的质量为x,消耗的氢氧化钙的质量为y根据2NaOH+H2SO4=Na2SO4+2H2O和Ca(OH)2+H2SO4=CaSO4+2H2O可得关系式为242 2NaOH H SO Ca(OH)809874x49kg y::809874==x49kg yx=40kgy=37kg每处理1000kg这种产品,他们可以节约经费为6.00元/kg×40kg-1.00元/kg×37kg=203元图中画出用氢氧化钠和氢氧化钙处理1000kg该石油产品时,残余硫酸溶质的质量变化曲线;氢氧化钠用虚线“…”表示,氢氧化钙用实线“一”表示,答:(1)若要清洗1000kg的这种石油产品,需要 40kg的NaOH。
(2)该石化厂进行了技术改造,采用Ca(OH)2中和这些残余硫酸。
每处理1000kg这种产品,他们可以节约203元经费。
(3)残余硫酸溶质的质量变化曲线;氢氧化钠用虚线“…”表示,氢氧化钙用实线“一”表示,2.实验室现有氯化镁和硫酸钠的固体混合物样品,小明同学想测定样品中氯化镁的质量分数。
(化学)九年级化学化学计算题常见题型及答题技巧及练习题(含答案)

(化学)九年级化学化学计算题常见题型及答题技巧及练习题(含答案)一、中考化学计算题1.氧化亚铜(Cu 2O )可用于生产船底防污漆,防止海生物对船舶设备的污损。
现将Cu 2O 和Cu 的固体混合物20g 放入烧杯中,加入质量分数为24.5%的稀硫酸50g ,恰好完全反应。
已知:Cu 2O+H 2SO 4═CuSO 4+Cu+H 2O .计算:(1)所加稀硫酸中溶质的质量为_____g 。
(2)原混合物中Cu 2O 与Cu 的质量比_____(写出计算过程,结果用最简整数比表示) (3)在图中画出向20g Cu 2O 和Cu 的固体混合物中逐滴加入24.5%的稀硫酸至过量,铜的质量变化曲线_____。
【答案】12.25 9: 1 。
【解析】【分析】根据加入的硫酸中溶质的质量和对应的化学方程式求算氧化亚铜的质量,进而求算对应的比值以及画图。
【详解】(1)所加稀硫酸中溶质的质量为24.5%×50g =12.25g ;故填:12.25(2)设原混合物中Cu 2O 的质量为x ,生成的铜的质量为y 。
224421449864x 12.Cu O+H SO CuSO +C 2u +H 5O g y═ 1449864==x 12.25g y解得:x =18 g ;y =8g ; 原混合物中Cu 2O 与Cu 的质量比为18 g :(20 g ﹣18 g )=9:1;故填:9:1(3)没加入硫酸时,铜的质量为2g ,加入到50g 稀硫酸时铜的质量为2g+8g =10g 。
如下图所示;故填:【点睛】根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整。
2.取24g氢氧化钠和碳酸钠的固体混合物,加136g水完全溶解后,再缓慢加入石灰乳(氢氧化钙和水的混合物)至恰好完全反应,过滤得到4g沉淀和10%的氢氧化钠溶液.试计算反应中应加入石灰乳的质量是______________?【答案】73.6g【解析】【详解】设:24g样品中碳酸钠的质量为x,生成的氢氧化钠的质量为yCa(OH)2 + Na2CO3=CaCO3 + 2NaOH106 100 80x 4g yx= 4.24 g y = 3.2 g .得到的10%NaOH溶液的质量为(24 g – 4.24 g + 3.2 g) ÷10% = 229.6 g加入石灰乳的质量为 229.6 g + 4 g - 136 g -24 g = 73.6 g答:应加入石灰乳的质量是73.6 g。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
化学计算题练习题基础、提高、难题_汇总(含答案)一、中考化学计算题1.向盛有193.8g硫酸铜溶液的烧杯中,逐滴加入质量分数为8%的氧氧化钠溶液,反应过程中生成沉淀的质量与所用氧氧化钠溶液的质量关系如图所示。
(化学方程式为CuSO4+2NaOH=Cu(OH)2↓+Na2SO4),请计算:(1)恰好完全反应时生成沉淀的质量。
(2)恰好完全反应时溶液中溶质的质量分数。
【答案】9.8g 5%【解析】利用化学方程式,根据反应的质量比即可计算出生成的沉淀的质量和生成的硫酸钠的质量。
解:设生成氧氧化铜的质量为x,生成硫酸钠的质量为y。
CuSO4+ 2NaOH=Cu(OH)2↓+Na2SO480 98 142100g×8% x y=x=9.8g=y=14.2g溶液溶质质量分数为×100%=5%答:恰好完全反应时生成沉淀的质量为9.8g,所得溶液中溶质的质量分数为5%。
2.为了测定某硫酸铜溶液的质量分数,小杨同学取50.0g样品置于烧杯中,逐滴加入氢氧化钠溶液,加入氢氧化钠溶液质量和生成沉淀质量的关系如下图所示。
请计算:(1)NaOH 的化学式量为_________。
(2)硫酸铜刚好完全反应时,所得溶液的质量为_____g(保留一位小数)。
(3)硫酸铜溶液中溶质的质量分数是________?(写出计算过程) 【答案】40 65.1 16.0% 【解析】 【分析】(1)根据化学式量为化学式中的各原子的相对原子质量之和, (2)根据质量守恒定律分析所得溶液的质量;(3)根据氢氧化铜的质量结合化学方程式计算硫酸铜的质量,进一步计算硫酸铜溶液中溶质的质量分数。
【详解】(1)NaOH 的化学式量为23+16+1=40; (2)所得溶液的质量为50.0g +20.0g−4.9g =65.1g ; (3)设样品中硫酸铜的质量为x CuSO 4+2NaOH =Cu (OH )2↓+Na 2SO 4 160 98 x 4.9g160984.9x g= x =8 g硫酸铜溶液中溶质的质量分数为8100%16.0%50gg⨯= 答:硫酸铜溶液中溶质的质量分数为16.0%。
3.已知氯化钠和氯化钙的混合物中,钙元素的质量分数为20%.现取一定质量的该混合物放入烧杯中,与100g 溶质质量分数为10.6%的碳酸钠溶液恰好完全反应。
求: (1)原混合物中氯化钠的质量为多少克_____。
(2)反应后所得溶液的溶质质量分数_____。
【答案】8.9克 18.7% 【解析】 【详解】解:参加反应的碳酸钠的质量100g×10.6%=10.6g设氯化钙的质量为x,生成的氯化钠的质量为y,生成的碳酸钙的质量为z106:111=10.6g:x x=11.1g106:117=10.6g:y y=11.7g106:100=10.6g:z z=10g氯化钙中钙元素的质量为11.1g××100%=4g则氯化钠和氯化钙的混合物的质量为=20g氯化钠和氯化钙的混合物中氯化钠的质量为20g﹣11.1g=8.9g反应后所得溶液的溶质质量分数为×100%≈18.7%答:(1)原混合物中氯化钠的质量为8.9克。
(2)反应后所得溶液的溶质质量分数18.7%。
4.侯氏制碱法生产的碳酸钠中常含有少量的氯化钠。
某学习小组对其组成展开探究。
取碳酸钠和氯化钠的混合物样品24g,加入100g水使其完全溶解,再加入96g过量的氯化钙溶液,反应过程中生成沉淀的质量与氯化钙溶液的质量关系如图所示:(1)完全反应时,得到的沉淀质量是_____g。
(2)计算样品中Na2CO3的质量分数_____(写出计算过程,结果保留一位小数)。
(3)通过已知数据,可以求出的量有_____(写字母)。
A反应后溶液的总质量B参加反应的氯化钙质量C氯化钙溶液中溶质的质量分数D恰好完全反应时,溶液中氯化钠的溶质质量分数(4)取混合物样品12g,加入足量的稀盐酸,将生成的二氧化碳通入盛有8g炽热碳粉的密闭容器中充分反应,在下图中画出二氧化碳的质量与容器中固体质量变化的关系图。
_____【答案】20 88.3% ABCD【解析】【分析】【详解】(1)完全反应时,得到的沉淀质量是20g。
(2)设样品中Na2CO3的质量为x2233CaCl+Na CO=CaCO+2NaCl106100x20g106100=x20g↓x=21.2g样品中Na2CO3的质量分数为21.2g100%88.3%24g⨯≈。
(3)通过已知数据,可以求出的量有:A反应后溶液的总质量B参加反应的氯化钙质量C氯化钙溶液中溶质的质量分数D恰好完全反应时,溶液中氯化钠的溶质质量分数,故选ABCD。
(4)5.菱铁矿(主要成分是FeCO3)是炼铁的原料。
现取20.0g菱铁矿,向其中加入足量稀硫酸,充分反应,测得固体质量与所加稀硫酸的质量关系如下图所示。
已知:①FeCO3+H2SO4=FeSO4+CO2↑+H2O②菱铁矿中杂质不参加反应,且难溶于水。
请计算:(1)20.0g菱铁矿中FeCO3的质量为 g。
(2)列式计算所用稀硫酸的溶质质量分数(结果准确到0。
1%)【答案】(1)11.6 (2)19.6%【解析】根据所学知识和题中信息知,根据质量守恒定律知,(1)20.0g菱铁矿中FeCO3的质量为20g-8.4g=11.6g.(2)解∶设所用稀硫酸的溶质质量分数为xFeCO3+H2SO4=FeSO4+CO2↑+H2O116 9811.6g 50g×x116 11.6g =9850g x, x=19.6%.答∶(1)20.0g菱铁矿中FeCO3的质量为11.6g。
(2)所用稀硫酸的溶质质量分数是19.6%.。
点睛∶本题主要考查质量守恒定律的应用以及根据化学方程式进行计算。
6.在一烧杯中盛有24.3g Na2SO4和NaCl组成的固体混合物,加入100g水使Na2SO4和NaCl全部溶解。
向其中逐渐滴加溶质质分数为20%的氯化钡溶液,生成沉淀的总质量与所滴入氯化钡溶液的质量关系曲线如图所示。
(1)请分析当BaCl2溶液滴加到B点时,溶液中的溶质是。
(2)请计算当滴加BaCl2溶液至图中A点时,所得溶液的溶质质量分数(计算结果保留一位小数)。
【答案】(1)BaCl2NaCl (2)10.6%【解析】试题分析:(1)当沉淀的质量不再增加时,说明反应已经进行完毕,所以当BaCl2溶液滴加到B点时说明氯化钡溶液滴加过量,当BaCl2溶液滴加到B点时,溶液中的溶质有刚生成的氯化钠和原来的氯化钠以及过量的氯化钡。
(2)根据当滴加BaCl2溶液至图中A点时沉淀的质量不再增加说明氯化钡溶液和硫酸钠溶液恰好完全反应,利用氯化钡的质量求出生成氯化钠的质量以及沉淀的质量即可求出所得溶液的溶质质量分数。
解:设参加反应的硫酸钠的质量为x,生成的硫酸钡的质量为y,生成的氯化钠的质量为z BaCl2 + Na2SO4=2NaCl+BaSO4↓208 142 117 233104g×20% x z y=解得x=14.2g=解得y=23.3g=解得z=11.7g当滴加BaCl2溶液至图中A点时,所得溶液的溶质质量分数×100%=10.6%答:当滴加BaCl2溶液至图中A点时,所得溶液的溶质质量分数为10.6%考点:考查根据化学反应方程式的计算;有关溶质质量分数的简单计算7.某校化学兴趣小组在老师指导下探究孔雀石(一种铜矿石)的组成元素。
他们取50克孔雀石粉末,在密闭容器中加热,观察到孔雀石分解过程中有水和能使澄清石灰水变浑浊的气体产生,绿色的孔雀石逐渐变为黑色粉末(假设:孔雀石中的杂质不反应,生成的二氧化碳全部被石灰水吸收)。
在此过程中他们测定了五次,相关数据如下表:请分析数据,回答下列问题:(1)组成孔雀石的元素有。
(2)表中“X”的值为 g。
(3)实验最终生成二氧化碳的质量是多少克(写出计算过程)?【答案】(1)Cu C O H (2)15 (3)8.8【解析】(1)根据孔雀石分解过程中有水和能使澄清石灰水变浑浊的气体二氧化碳,以及孔雀石是一种铜矿石,根据质量守恒定律反应前后元素种类不会增减解答(2)由表可知生成5g沉淀同时生成0.9g水,第三次还是生成0.9g水,所以沉淀是生成5g,x=10g+5g=15g(3)由表可知第四次和第五次的沉淀物和水的质量一样,说明第四次孔雀石完全分解,可知生成水的质量,根据化学方程式列比例解答设最终生成二氧化碳的质量是x克, 由表可知最终生成水的质量是3.6gCu2(OH)2CO3 = 2CuO+H2O+CO2↑18 443.6g x18/3.6g=44/xx=8.8g8.工业生产的纯碱中常含有少量氯化钠杂质,现称取12 g 纯碱样品于烧杯中,加入水使其完全溶解,逐渐加入氯化钙溶液至过量,测得加入氯化钙溶液的质量与生成沉淀的关系如下图所示。
(反应的化学方程式:CaCl 2+Na 2CO 3=CaCO 3↓+2NaCl)(1)计算样品中碳酸钠的质量分数________(要求写出计算过程,精确到0.1%)。
(2)若要计算氯化钙溶液中溶质的质量分数,可使用上图中_____点的一组数据(填标号)。
【答案】(1)88.3%;(2)a (或 b ) 【解析】由图可以看出生成的碳酸钙的质量为10g ,设碳酸钠的质量为x2233CaCl +Na CO ==CaCO 2NaCl ↓+106 100 x 10g10610010x g = x =10.6g样品中碳酸钠的质量分数为10.6100%88.3%12.0gg⨯≈,当求算氯化钙溶液中质量分数时,由于50g 氯化钙溶液对应的沉淀为4g ,125g 氯化钙溶液对应的沉淀为10g 都是氯化钙完全反应,所以可以根据a 点或者b 点数据计算。
答:(1)计算样品中碳酸钠的质量分数约为88.3%;(2)若要计算氯化钙溶液中溶质的质量分数,可使用图中曲线上示出的点a 或者b 所对应的数据。
9.某研究小组欲检验草酸晶体样品分解产物并测定器质量分数(假设杂质不参与反应).草酸晶体(H 2C 2O 4•2H 2O )的理化性质见表.(1)加热分解草酸晶体最适宜的装置是 (填图1字母序号).(2)图2是验证热分解产物中含CO ,CO 2的装置 ①仪器a 和b 的名称分别是 和 .②证明存在CO2的现象是,证明存在CO的现象是,D 中反应的化学方程式是.③装置A的作用是,气囊的作用是.(3)为测定样品中草酸晶体的质量分数,设计两种如下方案.熔点沸点热稳定性与碱反应101°C~102°C150°C ~160°C升华100.1°C失去结晶水,175°C分解成CO2,CO,H2O与Ca(OH)2反应产生白色沉淀(CaC2O4)①称一定量样品用上图装置进行实验,测得装置D反应前后的质量差,由此计算出的实验结果比实际值偏低,排除仪器和操作的因素,其原因可能有:CO未完全反应、.②称取8.75g草酸晶体样品配制50.00g溶液,取10.00g溶液加适量的稀硫酸,然后滴加25.00g3.16%KMnO4溶液,恰好反应完全.(已知:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O)则KMnO4溶液显色,25.00g3.16%KMnO4溶液中KMnO4的质量 g.请计算样品中的质量分数.[写出计算过程,M2(H2C2O4)=90,M2(H2C2O4•2H2O)=126,M2(KMnO4)=158].【答案】(1)c(2)①烧杯、酒精灯②B中澄清的石灰水变浑浊;D中黑色固体变成红色 CO+CuO Cu+CO2③除去草酸蒸汽,防止对二氧化碳的检验产生干扰;收集一氧化碳,防止污染空气(3)①生成的铜又被氧化②紫红 0.79g 90%【解析】试题分析:(1)草酸的熔点较低,受热容易熔化,用c装置加热草酸时不容易下流,适宜用来加热草酸.故填:c.(2)①仪器a和b的名称分别是烧杯、酒精灯.故填:烧杯;酒精灯.②证明存在CO2的现象是:B中澄清的石灰水变浑浊;证明存在CO的现象是:D中黑色固体变成红色.故填:B中澄清的石灰水变浑浊;D中黑色固体变成红色.D中氧化铜和一氧化碳在加热时反应能生成铜和二氧化碳,反应的化学方程式是:CO+CuO Cu+CO2.故填:CO+CuO Cu+CO2.③装置A的作用是:除去草酸蒸汽,防止对二氧化碳的检验产生干扰;气囊的作用是:收集一氧化碳,防止污染空气.故填:除去草酸蒸汽,防止对二氧化碳的检验产生干扰;收集一氧化碳,防止污染空气.(3)①一氧化碳部分反应,生成的铜重新被氧化等因素都能够导致计算出的实验结果比实际值偏低.故填:生成的铜又被氧化.②高锰酸钾溶液是颜色紫红色的.故填:紫红.25.00g3.16%KMnO4溶液中KMnO4的质量为:25.00g×3.16%=0.79g.故填:0.79.设10.00g溶液中含草酸晶体的质量为X,由2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O可知,5H2C2O4•2H2O→5H2C2O4→2KMnO4,630 316X 0.79g=X=1.575g,50.00g溶液中含草酸晶体的质量为:1.575g×5=7.875g,草酸晶体的质量分数为:×100%=90%,答:样品中草酸晶体的质量分数为90%.考点:实验探究物质的组成成分以及含量;常见气体的检验与除杂方法.点评:本题涉及化学方程式的书写、实验现象的判断、根据化学方程式进行计算等方面的知识,是典型的综合题.10.(一)实验室有一瓶标签如图所示的浓盐酸,要配制200g7.3%的盐酸,需要用该盐酸多少毫升?(二)某校化学兴趣小组用所配制的稀盐酸,测定该某矿山上的石灰石样品中碳酸钙的质量分数,假设矿石中只含杂质二氧化硅(二氧化硅是一种极难溶于水也不与盐酸反应且耐高温的固体),他们取一块,将其粉碎后,称出11g放入烧杯内(烧杯的质量为20g), 然后加入100g所配制的稀盐酸,用玻璃棒搅拌至不再产生气泡为止,二者恰好完全反应,得到下列数据,请分析表格中的数据,回答下列问题。
