供应商审计报告模板
供应商审核报告

评鉴人员
Auditor
分 数
Score
评 鉴 评 分 标 准
Audit point Evaluation Scale
0´
供应商不熟悉必要的工作事项,且没有建立相关的文件(流程图、未来规划、计划、程序文件策略等)
Supplier is not familiar with the requirements of the element and has no relevant source documentation (flow charts, forecasts, plans, procedures, strategies, etc.) in the area.
Is the CAR writing notice sent out to supplier to reply for countermeasure?
5´
9
是否制定进料检验品质目标?如何执行、统计分析?
Has the quality aim of incoming inspection been brought out?How to perform and sat analysis?
2´
供应商熟悉必要的工作事情,有初步的来源文件但执行上不够完善.
Supplier is familiar with the requirements of the element and has preliminary source documentation with incomplete plans for implementation.
N/A
不适用。
Notapplicability.
1.0评鉴项目(Assessment checklist)
供应商审计报告

供应商审计报告
SMP-QA-00005R6-00
供应商名称
拟供应物料名称
种类
物料级别
质量负责人
联系电话
供应商资质
营业执照()生产、经营许可证()
原料药质量标准()GMP证书()
原料药生产批件()《药品注册证》()
□符合要求
□不符合要求
其他文件
经营授权书()业务员资料、样品检验报告()
□符合要求
□不符合要求
样品检测
(新增原辅料供应商)
检验结果
□符合要求
□不符合要求
与供应商提供的检验结果对比
物料小试
生产技术部小试结果:
签名:日期:
现场检查
时间
检查地址
检查
方式
现场范围
存在问题及风险评估:
整改建议:
跟踪检查结果:
检查人员签名:
质量管理部意见
再审计日期:年月日前签名:
质量受权人意见
签名:
供应商审核报告

2
1
0
1
品质手册、目的、方针明确
2
业务分担、责任、权限的明确度
3
确保有独立组织的品质保证部门及专门检查员
4
不良品的控制流程是否明确
5
质量记录的完整记录及保存
6
每年是否对质量管理体系进行内部审核
7
客户提供的文件、资料是否有效的保存、发放、管理
8
员工是否有入职培训、岗位培训并进行考核
9
是否有对供应商进行评估、考核、辅导
19
物料管理是否有先进先出管理
20
是否建立批次管理方法及实施
21
物料是否建立可追溯性管理及实施
22
生产设备是否定期点检、保养并记录
23
现场物料是否有区域划分
24
物料和成品是否有足够的保护措施,以防损坏
25
批量生产前是否有首件检验,OK后方可生产
2、
3、
4、
5、
总分数:
审核日期
品质部:研发部:采购部:其他部门:
10
是否有要求供应商提供出货报告、材质证明
11
是否有完善的生产计划管理和监控
12
是否有来料、生产、出货品质控制程序
13
来料、生产、出货的品质标准是否明确
14
全检、抽检标准是否明确Leabharlann 15检验员是否有培训上岗管理
16
是否有客户退货、客诉处理流程
17
是否有对不良品进行分析并作出改善措施
18
不合格品,合格品是否有独立放置区域并标识
供应商概要:初审□重审□年审□
公司名称:
地址:
成立时间:
电话:
法人代表:
传真:
003供应商审计报告
□
□
□
2厂区整体布局合理,与生活区、行政区分开
□
□
□
3厂区远离粉尘、烟雾、污浊气体等污染源
□
□
□
4厂房按工艺流程和洁净级别合理布局
□
□
□
5仓贮有足够空间,清洁卫生,通风良好
□
□
□
6有防鼠、防虫、防霉变、防污染和消防设施
□
□
□
设
备
1设备能满足生产规模与工艺要求
□
□
□
2设备档案齐全
□
□
□
物
料
管
理
1主要物料来源符合要求、符合国家质量标准
□
□
□
2物料是否按区存放,并有明显状态标识
□Байду номын сангаас
□
□
3不合格品是否严格管理
□
□
□
生
产
技
术
管
理
1工艺规程和岗位操作规程完善
□
□
□
2严格按质量标准、生产工艺规程和岗位操作规程组织生产
□
□
□
3是否按批次管理
□
□
□
4产品是否能有效防止污染和混淆
□
□
□
5废弃物是否及时处理
□
□
□
2药品摆放整齐、货架清洁卫生
□
□
□
设
备
1验收养护及设备齐全
□
□
□
2计量设备经过校验并在有效期内
□
□
□
3安装有药品经营监控及操作细统软件并有效可用
□
□
□
4设备档案齐全
医疗器械公司 供应商质量审计报告
供应商质量评估审计报告
供应商种类:生产[ ] 经营[ ] 编号:
供应商现场审计报告
供应商种类:生产[ ] 经营[ ] 编号:
供应商(单位)名称
详细地址
法人代表质量负责人
主要联系人联系方式
审计日期年月日至年月日
审计小组成员
姓名部门职务联系方式
审计小组负责人
姓名
职务
联系方式
审计报告总结
1、结论:
2、存在的问题及结论:
审计状态:□首次审计□日常审计□定期审计
目前审计次数:审计频率:
3、批准状态审计结论:□批准□整改后重新审计□不批准
结论批准人:批准时间:年月日.
4、审计信息 4.1拟提供物料种类:
4.2上次审计日期:年月日。
5、审计背景:5.1供应商简介:
5.2审计目的:
5.3审计范围:
审计内容:
5.4审计缺陷定义与分类:
5.5上次审计项目完成整改情况:
6、本次审计发
现的缺陷
存在的具体问题及合理化建议:
7、审计小组
成员签名
8、质量管理
部门意见签名或签章
年月日
供应商评估审计结果通知书
物资部:
公司依据《供应商评估和批准管理程序》相关要求及规定,质量部组织审计小组相关部门人员于年月日至月日期间,对供应商进行了审计。
经审计小组综合评定,该供应商能够满足我公司要求,现批准其成为我公司合格的物料供应商。
(批准供应物料名单见附表:供应商拟供货品种一览表)
特此通知!
批准人:
年月日
供应商拟供货品种一览表
物料名称包装规格批准文号(或
注册证号)执行相关(质
量)标准
公司用途(品种)资料有效期。
供应商审计报告范文

供应商审计报告范文一、引言供应商是企业发展的重要组成部分,对企业的稳定经营和持续发展起着关键作用。
因此,对供应商进行定期的审计是企业管理的一个重要环节。
本份报告旨在对供应商进行审计,为企业提供有关该供应商的综合评估和改进建议。
二、审计目标1.评估供应商的财务状况和经营绩效;2.评估供应商的质量管理体系及生产能力;3.评估供应商的配送能力和供货稳定性;4.评估供应商的合规性和风险管理。
三、审计方法1.收集相关资料,包括财务报表、合同及协议、供应商评价报告等;2.实地走访供应商,了解其生产设备和流程;3.面谈供应商的经营管理人员,了解其企业文化和内部控制;4.进行文件审核,核对财务报表的真实性和准确性。
四、审计结果及分析1.财务状况和经营绩效评估:根据审计资料和财务报表,供应商目前财务状况良好,营业额稳定增长,利润率保持在合理水平。
然而,其应收账款周转率较低,需要加强对客户信用的管理和风险控制。
2.质量管理体系及生产能力评估:供应商的质量管理体系初步完善,拥有ISO9001认证,并建立了质量管理团队。
然而,在一些关键工序上存在设备老化和生产效率低下的问题,应考虑对生产线进行更新和优化,以提高整体生产能力和质量水平。
3.供货稳定性和配送能力评估:供应商与多家物流公司建立了长期合作关系,具备较为稳定的供货渠道。
然而,对于一些订单,供应商在配送过程中存在一定的延误现象,需要进一步加强配送能力管理,以保证供货的及时性和稳定性。
4.合规性和风险管理评估:供应商合规经营,符合相关法规和规定,并拥有一定的风险管理体系。
然而,供应商在一些关键环节的风险控制还需进一步加强,如对原材料采购的风险管理和对员工行为的内部控制等。
五、改进建议1.加强客户信用管理,提高应收账款周转率;2.更新和优化生产线设备,提高生产效率和质量水平;3.加强配送能力管理,确保供货的及时性和稳定性;4.进一步完善风险管理体系,提高供应商的合规性和风险控制水平。
供应链审计报告模版

供应链审计报告模版1. 引言本报告是针对供应链的审计结果,旨在评估供应链的运作情况和存在的风险。
本报告介绍了审计目标、方法和结果,以及建议的改进措施。
2. 审计目标审计的目标是评估供应链的完整性、可靠性和合规性,包括物流运输、库存管理、供应商合规以及关键业务流程。
3. 审计方法审计采用了以下方法:- 文献分析:通过查阅文献了解供应链管理的最佳实践和规范。
- 数据收集:收集供应链相关数据,包括运输记录、库存数据、供应商信息等。
- 现场检查:对供应链关键环节进行实地考察和检查。
- 风险评估:评估供应链中存在的潜在风险和弱点。
4. 审计结果根据审计调查和分析,得出以下审计结果:- 供应链管理存在一定程度的不规范和风险。
- 物流运输环节存在延迟和损耗问题。
- 仓储管理不够高效,存在过多的库存积压。
- 供应商合规性不够严谨,存在一定的合规风险。
- 关键业务流程中存在一些漏洞和弱点。
5. 建议改进措施基于审计结果,提出以下改进措施建议:- 优化物流运输,提高运输效率和减少损耗。
- 优化仓储管理,减少库存积压,提高仓储效率。
- 加强供应商合规管理,确保供应商符合相关法规和合规要求。
- 完善关键业务流程,修复漏洞和强化内部控制措施。
6. 结论本报告对供应链的审计结果进行了综合评估,并提出了改进措施建议。
供应链管理方应根据报告内容,采取相应的措施改进供应链的运作,并持续监控和评估供应链的合规性和效率。
附录- 供应链相关数据和文献分析报告。
- 审计调查的详细数据和检查记录。
以上报告仅为供应链审计的模板,具体报告内容应根据实际情况进行调整和完善。
供应商现场审计报告

供应商现场审计报告一、审计目的本次对供应商进行现场审计的主要目的是评估其生产能力、质量管理体系、交货能力、服务水平等方面的情况,以确定其是否能够持续稳定地为我方提供符合要求的产品和服务,保障供应链的稳定和可靠。
二、审计范围本次审计涵盖了供应商的生产车间、仓库、质量管理部门、研发部门等主要场所,以及其相关的文件和记录。
三、审计时间和人员审计时间:具体日期审计人员:审计人员姓名四、供应商基本情况供应商名称:供应商名称供应商地址:详细地址主要产品:列举主要产品供应规模:说明供应的大致数量和规模五、生产能力审计1、生产设备现场查看了供应商的生产设备,包括列举主要设备名称和型号。
设备整体维护状况良好,有定期的保养和维修记录。
部分关键设备的先进程度能够满足当前生产需求,但对于未来可能的产能提升,部分设备可能需要更新或升级。
2、生产工艺供应商的生产工艺较为成熟,有明确的工艺流程文件和操作规范。
生产过程中的关键控制点得到了有效的监控和记录,但在一些细微环节上,工艺的稳定性还有待进一步提高。
3、产能情况根据现场观察和与供应商的沟通,目前的产能能够满足我方当前的订单需求。
然而,在旺季或订单量突然增加的情况下,其应急产能的扩充能力略显不足。
六、质量管理体系审计1、质量控制文件供应商具备完善的质量控制文件,包括质量手册、程序文件和作业指导书等。
但在文件的执行过程中,存在部分员工对文件内容理解不够准确,导致操作上的一些偏差。
2、原材料检验原材料的检验流程规范,检验记录完整。
但在原材料的供应商管理方面,还需要加强对供应商的评估和监督。
3、过程检验生产过程中的检验点设置合理,检验人员能够按照要求进行检验。
不过,在检验工具的校准和维护方面,存在一定的漏洞。
4、成品检验成品检验标准明确,检验报告齐全。
但对于不合格品的处理流程,还需要进一步优化,以确保不合格品不会流入市场。
七、交货能力审计1、交货及时性查阅了供应商的交货记录,大部分订单能够按时交付。
标准审计报告范文(10篇)

标准审计报告范文(10篇):审计质量审计报告审计计划审计准则审计流程采购公司财会供应商审核采购流程年度报告项目分析审计方法项目公司会计与审计审计目的注册会计师企业会计准则审计意见财务报表分析财务报表审计标准审计报告范文第一篇:总经理:根据20XX年度审计计划和审计委员会安排,自20XX年4月15日至20XX年5月10日,我们审计组对供应部20XX年度采购与付款情景进行了审计。
审计过程中得到了被审计部门的进取支持和配合,工作进展顺利。
审计工作已经结束,现将审计情景报告如下:一、基本情景为了加强对公司物资采购与付款业务的内部控制,规范采购与付款行为,防范采购与付款过程中的差错和舞弊,公司根据《企业内部控制规范》以及国家有关法律法规,结合公司的实际情景,制定了《采购与付款内部控制制度》。
物资采购流程分两大类,一类是生产物料采购,一类是五金物料采购。
生产物料的采购,每月11日前生产部根据营销中心销售预算情景编制需料计划,供应部在5个工作日内根据需料计划经过询价后编制订货计划,报物管部审核总经理批准后与客户签订采购合同;而五金物料的采购,则由使用部门自行填写申购单,仓库核实库存量及采购量后,由供应部询价,报物管部审核总经理批准后与客户签订采购合同,某些零散的五金备件直接采购。
允许的情景下采用不少于3家以上供应商以资质及询价筛选的方式,在合格供方中比价择优采购,而货比3家的先后依据是:质量、送货光(是否贴合我司生产需求)、付款方式、价格。
一般情景下,贴合资质的供方先将样板送来,待公司检验合格后,将其确认为可比可选的对象。
公司开发供应商的途径有多种,以上网查询搜索或由供应商同行介绍为多。
所选择的供应商必须按商品的类别供给相应的证照复印本,如原料(主料)需有营业执照、药品生产许可证、药品gmp证书、药品注册证;辅料需有营业执照、药品生产许可证、药品注册证;中药材需有营业执照、药品经营许可证、gsp证书,且购入的产地坚持相对的稳定;进口商品遵守《进品商品管理办法》供给进口商品注册证、进口药材批件、进品药品检验报告书。
原辅料、包装材料供应商审计报告

是否有相应的文件控制不合格品,抽查落实情况
8
不合格品是否及时销毁处理
9
溶剂或母液的回收是否建立了相应的质量标准
10
溶媒的套用是否影响产品质量
11
回收和套用是否有相应的记录
12
是否建立返工、再加工相关文件并严格执行
14
成品是否采用洁净包装并能有效防止污染
15
贴签和包装的管理是否符合要求
编号S024037-2
供应商审计报告Ⅰ
(原辅料、包装材料部分)
供应商名称:
审计方式:□现场审计□资料审计
报告日期:
一、企业基本情况
企业名称
企业性质
法人代表
生产地址
联系电话
资格证书
业务范围
审计物料名称
二、审计内容
类别
序号
审计内容说明
Y/N
状况评价
良好
一般
较差
人员机构
1
提供质量保证体系图
2
质量管理部门是否独立于其他的部门
4
实验室和生产区域是否分开
5
厂房的洁净级别是否符合产品用于制剂生产的要求
6
是否采取必要的防虫鼠措施
设备设施
1
提供关键生产设备及检验仪器一览表
2
是否为专用车间,若不是,列出其他产品名录
设备设施
3
对于多用途的设备是否记录设备的每次使用及清洗
4
企业的生产能力是否满足供货需求
5
是否对设施、设备按规定进行维护保养
7
包装、仓贮条件,物料的管理是否有效控制
8
仓库是否有不合格区,不合格区有无明显标识
卫生
1
是否有卫生清洁制度,现场执行情况如何
供应商审计报告范文

供应商审计报告范文标题:供应商审计报告摘要:本报告是对供应商进行审计的结果汇总和分析。
审计覆盖了供应商的财务状况、运营情况、管理制度、风险控制等方面。
通过对供应商的审计,可以帮助我方了解供应商的实际情况,评估其风险,并采取相应的措施进行风险管理。
审计结果发现供应商在财务报告的准确性和合规性方面存在一定的问题,但整体上仍具备合作的潜力。
在审计报告中,将详细阐述审计过程、审计结果、存在的问题以及相应的建议。
一、引言近年来,我方与供应商保持了良好的合作关系。
鉴于供应商的业务增长,为了进一步了解供应商的实际运营情况,我方决定对其进行审计。
本报告旨在总结和分析审计结果,为我方制定风险管理措施提供参考。
二、审计目标与范围本次审计的目标是评估供应商的财务状况、运营情况、管理制度和风险控制情况。
审计范围包括供应商的财务报告、资金运作、采购管理、供应链和合规性等方面。
三、审计方法与过程1.收集资料:我们要求供应商提供财务报告、资金流水、合同、采购记录和合规相关证明文件等。
2.风险评估:通过资料分析和财务指标计算等方法,评估供应商的偿债能力、盈利能力和运营风险。
3.内部控制评估:对供应商的管理制度、采购流程、仓储管理、风险控制体系等进行评估。
4.检查合规性:审查供应商的合同合规性、运作符合公司政策和法规要求等方面。
四、审计结果1.财务状况:-财务报表的准确性有待提高,存在一些账目不清晰和核算不规范的问题。
-资金状况良好,但资产负债表中呈现出供应商的负债结构风险,需要考虑合理的融资安排。
2.运营情况:-采购管理比较稳定,但在供应链管理中存在较高的运输风险,建议加强物流管理和运输合作伙伴的评估。
-存货管理存在亏损和库存周转率不佳的问题,需要优化库存管理和供应链配送。
3.管理制度:-内部控制制度相对完善,但在一些具体操作环节上仍存在欠缺,建议增强内部控制的执行力度。
-人力资源管理方面,员工激励机制有待完善,应加强培训和发展计划,提高员工的工作积极性。
供应商质量审计报告

6.6是否有物料和产品的留样管理规程并严格执行
6.7是否有产品的稳定性考察及记录
6.8是否有公用系统等的检测记录
6.9是否有检验结果超标的处理规程并严格执行
6.10是否有委托检验,如有,是否得到有效控制
6.11是否对杂质(有机/无机杂质和残留溶剂等)进行有效控制
4.4是否采取必要的防虫、鼠措施并检查记录
4.5厂房设施、设备是否按规定进行维护、保养
4.6现场标识是否齐全
4.7计量仪器仪表是否在有效期内
4.8是否为专用车间,如不是列出其他产品
5
生产管理
5.1是否有生产工艺流程图及关键控制点
5.2批的划分原则
5.3批的划分是否符合规定
5.4混批的控制是否符合要求
7.3是否有变更控制管理规程并严格执行,如有列出近三年变更情况
7.4是否有偏差控制规程并严格执行
7.5是否质量内审/自检,如有频次是
7.6是否有纠正及预防措施管理规程
7.7是否对物料供应商进行控制管理
7.8是否有产品的年度质量回顾
7.9是否有质量投诉处理规程并有相关处理记录
7.10是否建立退货产品处理规程并严格执行
5.5生产量和供应量是否匹配
5.6是否建立书面清场、清洁及消毒规程,执行是否有记录
5.7母液、溶剂或粗品的再利用是否符合要求
5.8人员操作及卫生是否符合要求
5.9生产记录是否符合要求
5.10是否有不合格品的处理规程并严格执行
5.11是否建立返工、再加工规程,并严格执行
5.12标签等印刷性包材的使用和管理是否符合要求
质量审计报告
一、审计对象及物料
企业名称(公章)
药品供应商审计模板

模版4:供应商审计
编写说明:
1. 本模板审计的范围是所有物料供应商的情况。
2. 建议企业至少每二年一次按照本模板现场考察其关键物料供应商情况。
基本信息
审计对象:
审计日期:
审计小组人员组成:
姓名:部门
审计结论:
经对上述内容进行审查,供应商管理方面………。
一、基本情况简介
二、主要问题及其风险评估
主要问题:
经过对上述问题的综合评估,本企业的质量部门在质量管理体系以及对产品的质量和安全方面存在风险如下:
三、整改建议和跟踪检查结果
包括对存在问题的整改建议、整改时限建议,跟踪检查等内容。
四、审计小组成员签字
附件:
关键物料供应商现场审计项目表。
原料药供应商审计报告样本
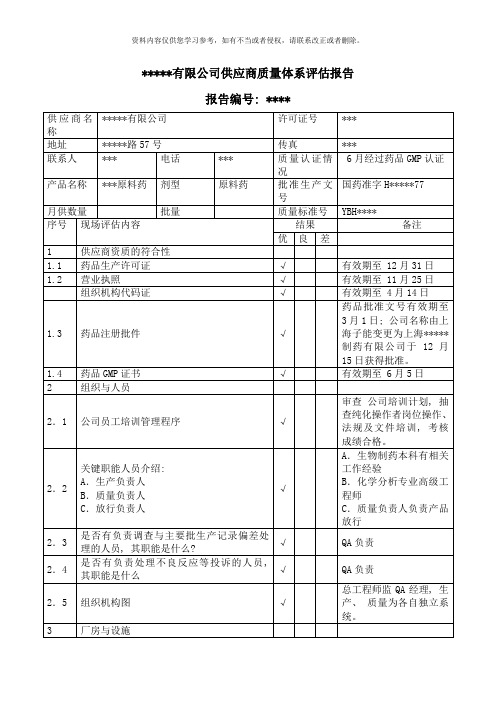
1、个别设备缺少必要标识。如精分用层析柱清洁后无清洁标识, 无法识别清洁状态;
2、称量用精密仪器天平缺少必要的防护, 未使用防震用操作台;
3、对冷链运输产品缺少文件支持;
11.12
标准品如何管理?
√
专人管理
12
稳定性数据的审计
12.1
稳定性试验的执行程序是? 请简要描述
√
12.2
是否使用成品进行稳定性试验?
√
12.3
是否所有的产品在有效期内是稳定的? 有没有关于如果不稳定该如何去做的SOP?
√
按偏差处理
12.4
与稳定性样品直接接触的包装材料是否上市品相同?
√
12.5
√
动物实验委托检验协议, 但公司名称变更后未重新签定, 还是3月1日以上海子能签定的。
11.10
请提供一份产品的检验报告单复印件? 检查其中项目, 与执行标准是否相符?
√
11.11
对有特殊要求的仪器、 仪表是否安放在专门的仪器室内, 有避免其它外界因素影响的设施。
√
天平与高效液相等在同一实验室, 天平使用实验台不具有防震功能。
5.10
标识管理
√
厂房、 设施设备标识清晰。但精分用层析柱处理后只标记为醋酸奥曲肽, 无其它状态标识。
5.11
不同洁净区之间压差
√
物流第一层缓冲与一般走廊之间压差为8Pa
6
包装及贴签控制
6.1
是否有包材和标签的接受和检验的SOP
√
标签为企业自制。
某胶塞生产企业的供应商审计报告

某胶塞生产企业的供应商审计报告产品质量方面:药品生产企业在选择药用胶塞时,进行相关试验时,发现存在析出物情况。
产品稳定性,导致药用胶塞实际使用时存在相容性问题。
客户抱怨胶塞存在外观不洁净,微粒多。
药用胶塞况。
在药品临床使用时,出现胶塞掉屑现象。
客户抱怨产品时有混淆情况出现。
产品质量一致性差,在药品罐装生产时,药用胶塞的外形尺寸公差、弹性等质量性能上存在批内、批间差异。
产品开发方面:目前药用胶塞企业研发力量不足。
研发部门工作缺乏系统的工作流程。
产品开发时缺乏对产品质量属性的分析,没有明白的设计标准。
产品开发时,缺乏系统的验证、技术评审工作流程和工作技术标准。
技术转移过程中信息不流畅,药用胶塞企业普遍缺乏技术转移管理体系,导致设计开发与生产管理脱节。
研发数据不足,某些技术资料不全。
产品再注册与注册变更缺乏系统管理。
原材料供应方面:关键生产物料除一部分是进口,国内生产的其余物料缺乏专业配套的生产供应商。
进口供应商处于技术保密、知识产权等原因商不愿配合提供一些原始资料。
例如:杜邦公司拒绝提供有关添加剂的成分。
国内生产原料生产企业普遍是手工作坊式生产企业,难以保证原料质量的稳定性、均一性。
例如陶土,国外是造粒的,国内原料有的是乡镇企业生产的,老工人凭经验生产,由于药用胶塞部分原料使用量小或者是海外生产,难以对大部分供应商进行供应商质量审计。
缺乏一套真正有效的原材料检控项目及标准。
生产管理方面:大部分企业目前存在产品规格编号不合理,可追溯性差。
大部分企业由于药品生产企业需求多种多样,统一标准产品,出现不同的质量要求,导致生产流程变化大,进而增加生产与质量管理难度。
药品生产企业需求多样性,只是药用胶塞企业生产组批困难,批量变化范围较大,从3万到500万不等;另外订单不稳定,生产计划性不强,经常发生插单生产的现象,导致生产管理难度加大,容易出现生产计划延误、质量均一性等诸多质量问题。
鉴于药用胶塞生产工艺特点和客户订货情况,药用胶塞生产采用多品种多批次生产管理模式,现场管理较为混乱。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
Ⅰ类内包材
审计内容:营业执照、生产许可证、经营许可证、药包材注册证(进口药包材注册证)、经营授权书、业务员资料。
合格标准:与原料同。
审计内容:机构与人员、厂房设施设备、物料管理、生产管理、质量保证与控制、检验手段、产品运输、变更控制、风险管理、售后服务。
1、供应商资质审核表
2、供应商样品质量检验、小试及稳定性试验审核表
编号:RE(M)-ZB-0001(1)-01
名称
供应商
种类
物料级别
阿普唑仑原料
某某某厂家
原料
A级
质量负责人
联系电话
供应商资质
药品生产许可证 □ 企业法人营业执照 □ 药品GMP证书 □ 税务登记证 □ 药品注册证 □ 组织机构代码证 □
备注:
时间
检查地址
存在问题及其风险评估:
整改建议:
检查人员签名:
现场审计时,如实填写《供应商现场审计表》。
现场审计人员签名:
7 定点供应商的批准
通过对阿普唑仑原料供应商的资质审核、样品检验及小试情况、现场审计情况等,各项审计指标符合方案要求,现给出综合分析意见,同意此供应商为我公司阿普唑仑定点供应商。定点周期为年
质量副总批准:
签字: 年 月 日
阿普唑仑原料供应商资质审核表
供应部成员签名: 年 月 日
质保部成员签名: 年 月 日
5 样品检验和报告比对:
根据供应商提供的样品及质量标准和检验报告书,由质控部进行比对,确认其报告真实性和检测水平符合程序规定。
质控部成员签名: 年 月 日
6 现场审计
对通过资质审核的供应商,质保部组织质量审计小组(两人以上)到供应商的生产现场按照预定方案进行客观公正质量审计。
范围:适用于本公司阿普唑仑原料供应商的审计和批准。
2 成立质量审计小组
质量审计小组成员及责任:
小组各成员保证在客观公正的立场上,认真履行自己的职责,对阿普唑仑原料供应商进行审计,得出正确的结论,并对其进行风险评估。
2.1 小组组长:
签名: 年 月 日
2.2 小组成员签名:
3 供应商的审计和评价流程图:
供应部索取资料,进行初步审查 未通过审查
通过,报质保部
质保部进行资质审查 未通过审查
通过,小样请验、检验
质控部进行检验、报告书比对 比对不合格
检验、比对通过
报质量副总批准,进行现场审计 未通过审计
通过
形成审计报告,报质量副总批准 未通过批准
通过批准
4 资质审核
供应部通过初步审核资料,质保部对供应商资质进行审查,各项资料符合程序规定,通过审查。(相信审核内容见审计方案)
质保部意见
再审计日期: 年 月 日前
签章:
年 料审计内容:营业执照、生产许可证、GMP证书、GSP证书、原料药生产批件、质量标准、经营授权书、业务员资料;进口物料的进口批件、样品检验报告书(包括生产企业的检验报告书和口岸药检所的检验报告书)、海关证明文件等。
合格标准:有以上资料并在有效期内,生产或经营的范围包括拟供货的物料。
辅料
审计内容:营业执照、生产许可证、具有药品批准文号的药用辅料的生产批件、质量标准、经营授权书、业务员资料、样品的检验报告书
3、物料供应商现场审计记录
4、供应商现场审计报告
5、聚氯乙烯固体药用硬片供应商质量审计详细信息
6、聚氯乙烯固体药用硬片Ⅰ类包装材料主要检测项目及检测设备
7、相关影像资料
阿普唑仑原料供应商审计报告
编号:
起草人:起草日期:
审核人:审核日期:
批准人:批准日期:
药业有限公司
1、目的
2、质量审计(质量评估)小组及责任
3、阿普唑仑原料供应商的选择和评价流程图:
4、阿普唑仑原料供应商的资质审核
5、与供应商签订的质量协议
6、样品检验数据和报告
7、阿普唑仑原料供应商的现场审核
8、审核的批准
9、产品稳定性考察
10、定期质量回顾分析
11、供应商变更审批
1 目的:为确保持续稳定地生产出符合预定用途和注册要求的阿普唑仑片,根据物料供应商质量审计管理规程,对阿普唑仑原料供应商的资质进行审计,并对其进行现场质量审计,以确定是否批准其为阿普唑仑原料定点供应商;通过现场审计与交流,确定签订质量协议内容;确定物料定点使用周期、审计周期等程序。
