《有机化学醇硫醇酚》PPT课件
合集下载
第七章醇硫醇酚3
Br 2,4,6-三溴苯酚 (tribromophenol)
反应非常灵敏,可用于部分酚类化合物的检验。
化学性质 2、芳环上的亲电取代反应 (1)卤代反应
OH
CS2
+ Br2 0℃
OH + HBr
Br 80~84%
H3C
OH + Br2
CHCl3 0℃
OH
+ HBr
H3C
Br
80 %
化学性质
2、芳环上的亲电取代反应
(2)硝化反应
OH
20% HNO3 25 ℃
OH
OH
+
NO2
O2N
(30~40%) 邻-硝基苯酚
(15%) 对-硝基苯酚
化学性质
2、芳环上的亲电取代反应
(3)磺化反应
25℃ OH
浓 H2SO4
100℃ HO
OH
o-羟基苯磺酸
SO3H
(49%)
浓 H2SO4, 100℃
SO3H p-羟基苯磺酸 (90%)
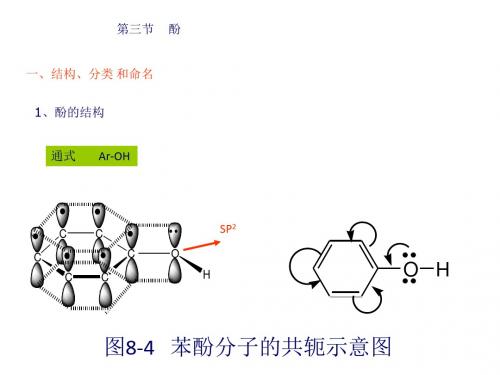
第三节 酚 一、结构、分类 和命名
1、酚的结构 通式 Ar-OH
C C
C
C C
C
SP2 O
H
OH
图8-4 苯酚分子的共轭示意图
一、结构、分类和命名 1、酚 的结构
①氧原子上电子云密度↓ O—H极 性↑ 酸性↑
P- 共轭 ②苯环内电子云密度↑ 环上亲电
的结果:
取代活性↑
③特殊的烯醇式结构 显色反应
蓝紫色 紫色 蓝色 绿色 暗绿色 红色
▲ :凡具有酚羟基结构的化合物均可与FeCl3显色。 应用:鉴别酚类化合物。
4、酚的自氧化与醌的结构
第七章 醇硫醇酚

上页 下页 返回 退出
1.3 醇的化学性质
醇的化学性质主要是由官能团羟基所决定, 同时也受到烃基的一些影响。从化学键来看C-O 和O-H都是极性键;因此,醇容易发生反应的部 位如虚线所示:
R C O H
酸碱性、醚的生成、酯的生成 卤化反应、脱水反应、氧化反应
上页 下页 返回 退出
H C O H
弱碱性
+
C H3
H2O
O H2
C H3 C H
C H C H3
+
重 排
C H3 C H3 C
+
2° 碳正离子
C H C H3 H
CH3 CH3 CH CH CH3 Br
Br-
3° 碳正离子
Br
CH3
仲醇与HX酸反应,
CH3 C Br
CH2 CH3
生成重排产物是SN1机理的重要特征
下页 退出
b. SN2:大多数伯醇,且没有重排反应。
第七章
醇 硫醇 酚
下页 返回 退出
基本内容和重点要求
醇、酚、醚的结构、分类和异构现象 醇、酚、醚的化学性质 环氧乙烷的开环反应 重点掌握醇、酚、醚的化学性质;醇 的氢键对其物理性质(沸点、水溶性)的影 响。
上页 下页 返回 退出
第一节 醇(Alcohols)
1.1 醇的结构、分类和命名
1.2 醇的物理性质
CH3 C CH2
2-甲基-2-乙基-1-己醇
H3C
CH2
CH2
CH2
CH2OH CH3
CH
CH CH3
CH3
OH
2-甲基-1-环己基-1-丙醇 上页 下页 返回 退出
如果为不饱和醇,应选择含有羟基并含有双键或 叁键的最长碳链作为主链,编号时应使羟基的位号最 小;在定名称时,表示主链碳原子数的“天干”或汉 字应写在“烯”字或“炔”字名称的前面。
有机化学- 醇、酚、醚、硫醇

OH
O
2-辛酮 (96%)
用于鉴别:常用K2Cr2O7和KMnO4催化。反应发生,
则KMnO4由紫红变为无色, K2Cr2O7由橙红变为绿色
人体内含羟基化合物在酶的作用下
发生生物氧化。
• 第一步,肝脏里的乙醇脱 氢酶(ADH)把酒精转变为 乙醛。
• 第二步,肝脏里的乙醛脱 氢酶(ALDH)把乙醛转变 为乙酸。
OH
Cl
仲丁醇
(3)g-氯丙醇
-CH2-OH 苯甲醇(苄醇)
2.系统命名法 • 选择含-OH的最长碳链作主链,按主链碳原子个数
称“某醇”,编号应使 –OH 所连的C有较小编号, 羟基的位次写在醇名之前。
CH3CH CHCH2OH CH3 CH3
2,3-二甲基-1-丁醇
CH3-CH2-CH2-CH-CH2-CH3 2-乙基-1-戊醇 CH2OH
OH OH 顺-1,2-环戊二醇
3.俗名
甲醇 乙醇 丙三醇 苯甲醇 环己六醇
木醇 酒精 甘油 苄醇 肌醇
具有视神经毒性,10毫升致盲 30毫升致死。
利用其可使蛋白质脱水变性凝 固的原理,用于杀菌。
含羟基多,具有吸湿性,用于 护肤产品、润滑剂、助溶剂。
具有微弱的麻醉功能和防腐性能
促进脂肪代谢,治疗脂肪肝。
(二) 醇与无机酸反应
1. 与氢卤酸反应
R-OH + H-X
+
RR--O-XH++HX2O-
H
不同的HX以及不同类型的醇反应速度不同:
HI > HBr > HCl (HF一般不反应)
叔醇 > 仲醇 > 伯醇 > CH3OH
常用无水氯化锌的浓盐酸溶液(Lucas 试剂) 鉴别伯、仲、叔三类醇:
7第七章醇硫醇酚1

△
⑤ 脱水(消除)反应
CH3CbH2CHCbH'3 OH
661£00H£2SCO4
CH3CH£CHCH3 £¨Saytzeff££ò £
2-££ £¨£÷££ú ££
CH2 CH CH2CH3 浓H2SO4 OH
CH CH CH2CH3
⑥1). KM氧n化O4反(H应+or OH-)、Na2Cr2O7-H2SO4 、HNO3
(一)酚的构造
.
sp2 H
O.
P–共轭 ··O—H
1.6D
①O–H键极性增强,–H比醇活泼 ②C–O键加强,–OH难取代 ③苯环被活化,环上易取代
(二)分类: 一元、多元酚 (三)命名
OH OH
邻-苯二酚
OH OH
OH 1,2,4-苯三酚
OH
α -萘酚
OH SO3H
间羟基苯磺酸
OH
CHO
对羟基苯甲醛
第七章 醇 硫醇 酚
醇 R-OH -OH(羟基)
酚 Ar-OH
OH -OH(羟基)
硫醇 R-SH -SH (巯基)
第一节 醇 一 醇的结构、分类和命名
H δ+
CO
H
1090
δ+
H
H
SP3
RO H
有较强的极性
1 醇的分类
饱 CH3–OH 甲醇 和 RCH2–OH 伯醇 醇 R2CH–OH 仲醇
按
R– 不饱 和醇
RSH + NaOH
RSNa + H2O
2 硫醇与重金属作用
RSH + Pb2+
R-S R-S Pb
3 氧化反应
[O]
2RSH
第八章醇、硫醇、酚

CH3—C︳H —CH2OH CH3
异丁醇(isobutylthanol)
C︳H3
CH3
—C —OH ︳
CH3
叔丁醇(tert-butylthanol)
(三)醇的命名 2. 醇的系统命名法
主链:含羟基最长C链 编号:靠近羟基端
432 1
例:
CH3—CH2
—CH
︳
—CH2OH
CH3
2-甲基-1-丁醇
OH CH3
邻-甲苯酚
OH
CH3
间-甲苯酚
结构、分类和命名
3. 命名
复杂酚:标明取代基位置,有时OH也作取代基
COOH OH
OH
O2N
NO2
邻-羟基苯甲酸 (水杨酸)
NO2
2,4,6-三硝基苯酚 (苦味酸)
二、物理性质
酚一般多为固体; 由于分子间形成氢键,所以有较高的沸点; 酚微溶于水,但加热时酚可无限溶解; 酚有较大的毒性。
一、结构与命名
CH3SH
甲硫醇 (methanethiol)
SH
CH3CH2CHCH2CH3
3-戊硫醇 3-pentanethiol
HSCH2CH2SH
1,2-乙二硫醇 1,2-ethanedithiol
HSCH2CH2OH
2-巯基乙醇 2-mercaptoethanol
二、化学性质 1. 弱酸性与成盐 RSH + HO -
第三节 酚 一、结构、分类 和命名 1. 酚的结构
通式 Ar-OH
C C
C
C C
C
SP2
O H
OH
图8-4 苯酚分子的共轭示意图
一、结构、分类和命名 1、酚 的结构
《醇硫醇酚》课件

将逐渐降低
应用领域:醇硫 醇酚的应用领域 将不断扩大,如 医药、化工、食
品等领域
市场竞争:随着 市场竞争的加剧, 企业需要不断提 高产品质量和降 低成本,以保持
竞争优势
未来市场预测
市场需求:随着环保意识的提高,醇硫醇酚的市场需求将不断增加
技术进步:随着技术的不断进步,醇硫醇酚的生产成本将逐渐降低
应用领域:醇硫醇酚的应用领域将不断扩大,包括医药、化工、食品等领域 市场竞争:随着市场竞争的加剧,醇硫醇酚的价格将逐渐下降,但品质将不断提 高
相关法律法规与标准
环境保护法:规定了环境保护的基本原 则和措施
安全生产法:规定了安全生产的基本原 则和措施
危险化学品安全管理条例:规定了危险 化学品的安全管理要求
职业病防治法:规定了职业病防治的基 本原则和措施
化学品安全技术规范:规定了化学品的 安全技术要求
国际标准:如ISO 14001环境管理体系标准、 ISO 45001职业健康安全管理体系标准等
醇硫醇酚的定义
醇硫醇酚具有较强的抗氧化性和生 物活性,对多种疾病具有治疗作用
添加标题
添加标题
添加标题
添加标题
醇硫醇酚是一种重要的有机合成中 间体,广泛应用于医药、农药、染 料等领域
醇硫醇酚的合成方法有多种,包括 氧化法、还原法、缩合法等
醇硫醇酚的分类
醇硫醇酚按化学结构可分为单醇硫醇酚 和多醇硫醇酚
药物研发:用于药物研发, 如药物筛选、药物优化等
药物合成:用于合成多种药物, 如抗生素、抗肿瘤药物等
药物生产:用于药物生产, 如药物合成、药物纯化等
醇硫醇酚在食品添加剂中的应用
食品添加剂领域
醇硫醇酚在食品保鲜中的应用
添加标题
应用领域:醇硫 醇酚的应用领域 将不断扩大,如 医药、化工、食
品等领域
市场竞争:随着 市场竞争的加剧, 企业需要不断提 高产品质量和降 低成本,以保持
竞争优势
未来市场预测
市场需求:随着环保意识的提高,醇硫醇酚的市场需求将不断增加
技术进步:随着技术的不断进步,醇硫醇酚的生产成本将逐渐降低
应用领域:醇硫醇酚的应用领域将不断扩大,包括医药、化工、食品等领域 市场竞争:随着市场竞争的加剧,醇硫醇酚的价格将逐渐下降,但品质将不断提 高
相关法律法规与标准
环境保护法:规定了环境保护的基本原 则和措施
安全生产法:规定了安全生产的基本原 则和措施
危险化学品安全管理条例:规定了危险 化学品的安全管理要求
职业病防治法:规定了职业病防治的基 本原则和措施
化学品安全技术规范:规定了化学品的 安全技术要求
国际标准:如ISO 14001环境管理体系标准、 ISO 45001职业健康安全管理体系标准等
醇硫醇酚的定义
醇硫醇酚具有较强的抗氧化性和生 物活性,对多种疾病具有治疗作用
添加标题
添加标题
添加标题
添加标题
醇硫醇酚是一种重要的有机合成中 间体,广泛应用于医药、农药、染 料等领域
醇硫醇酚的合成方法有多种,包括 氧化法、还原法、缩合法等
醇硫醇酚的分类
醇硫醇酚按化学结构可分为单醇硫醇酚 和多醇硫醇酚
药物研发:用于药物研发, 如药物筛选、药物优化等
药物合成:用于合成多种药物, 如抗生素、抗肿瘤药物等
药物生产:用于药物生产, 如药物合成、药物纯化等
醇硫醇酚在食品添加剂中的应用
食品添加剂领域
醇硫醇酚在食品保鲜中的应用
添加标题
《有机化学醇硫醇酚》PPT课件

( 2 ) 机 制 1 ) 羟 基 质 子 化 2 ) 脱 水 成 正 碳 离 子 3 ) 消 去 - H 成 烯
H HH +H H慢H H-H + H
CC
CC
C C
CC
快 H O H H O H 2
H快H
( 3 ) 脱 水 活 性 顺 序 : 叔 醇 > 仲 醇 > 伯 醇
编辑ppt
15
( 4 ) 遵 循 扎 依 切 夫 S a y t z e f f 规 则
编辑ppt
21
第二节 硫醇
一、结构与命名
(一)结构 (二)命名
R-SH -SH 巯基
在相应的醇名称中加上“硫”字。 结构复杂时,把-SH 作为取代基。
C H 3S H C H 3C H 2S H H O H 2CC H 2S H
甲 硫 醇 乙 硫 醇
2-巯 基 乙 醇
m eth an ethiol eth an eth iol 2-m ercap toeth an ol
a、反应现象:产物卤代烷不溶解,叔醇立即变浑浊; 仲醇十几分钟浑浊;伯醇常温不反应。
b、应用:鉴别伯、仲、叔醇
范围:C6以下醇的鉴编辑别ppt。
19
(六)邻二醇类化合物的特性 1、与Cu(OH)2 呈深蓝色
CH2 OH HO CH OH+ Cu
HO CH2 OH
CH2 O Cu
CH O +2H2O
3) 系统命名法---结构比较复杂的醇,采用系统命名法
1 23 4 56 CH3CHCH2CH2CHCH3
OH
CH3
5-甲基-2-己醇
一般原则:1、选主链(含羟基所连碳且碳数最多) 2、编号(近羟基一端开始) 3、取代基在前,母体在后(羟基位置)
醇、硫醇、酚

CrO3 CH CH CH2OH C5H5N
CH CH CHO
• 欧芬脑尔(Oppenauer)氧化法:在异 丙醇铝或叔丁醇铝存在下,将仲醇和丙 酮一起反应,醇被氧化成酮,丙酮被还 原成异丙醇的反应。
O R2C HO H+ C H3C C H 3 Al[O C H (C H 3)2]3 O RC R + OH C H3C HC H 3
•在实际工作中,三卤化磷常用红磷与溴或 碘作用产生。如:
CH3CH2OH
P + I2
CH3CH2I
• 醇与PX5也可发生类似的反应,但与PX5 反应时,副产物较多,所以,这不是制 备卤代烃的好方法。
ROH + PCl5 ROH + POCl3 RCl + POCl3 + HCl (RO)3PO + 3HCl 磷酸酯
OH Na2Cr2O7 H2SO 4/
CH3 KMnO4/H H3C C OH CH3
O KMnO4/H CH2CH2COOH CH2CH2COOH
C H3C CH2 KMnO4/H C H C O + CO + H O 3 2 2 CH3 CH
3
(2)用温和的氧化剂氧化(选择性氧化):
沙瑞特(Sarrett)试剂:CrO3/C5H5N 琼斯(Jones)试剂: CrO3/稀H2SO4 活性二氧化锰。
(二)二元醇的反应
1、脱水反应 邻二醇分子内脱水:生成不稳定的烯醇, 再重排成醛或酮 分子间脱水:共轭二烯烃、环醚
2、pinacol重排
CH3 CH3 H3C C C CH3 H2SO4 CH3 H3C C C CH3
OH OH
CH3 O
H+
CH CH CHO
• 欧芬脑尔(Oppenauer)氧化法:在异 丙醇铝或叔丁醇铝存在下,将仲醇和丙 酮一起反应,醇被氧化成酮,丙酮被还 原成异丙醇的反应。
O R2C HO H+ C H3C C H 3 Al[O C H (C H 3)2]3 O RC R + OH C H3C HC H 3
•在实际工作中,三卤化磷常用红磷与溴或 碘作用产生。如:
CH3CH2OH
P + I2
CH3CH2I
• 醇与PX5也可发生类似的反应,但与PX5 反应时,副产物较多,所以,这不是制 备卤代烃的好方法。
ROH + PCl5 ROH + POCl3 RCl + POCl3 + HCl (RO)3PO + 3HCl 磷酸酯
OH Na2Cr2O7 H2SO 4/
CH3 KMnO4/H H3C C OH CH3
O KMnO4/H CH2CH2COOH CH2CH2COOH
C H3C CH2 KMnO4/H C H C O + CO + H O 3 2 2 CH3 CH
3
(2)用温和的氧化剂氧化(选择性氧化):
沙瑞特(Sarrett)试剂:CrO3/C5H5N 琼斯(Jones)试剂: CrO3/稀H2SO4 活性二氧化锰。
(二)二元醇的反应
1、脱水反应 邻二醇分子内脱水:生成不稳定的烯醇, 再重排成醛或酮 分子间脱水:共轭二烯烃、环醚
2、pinacol重排
CH3 CH3 H3C C C CH3 H2SO4 CH3 H3C C C CH3
OH OH
CH3 O
H+
有机化学第七章醇硫醇酚

第九页,编辑于星期一:二十三点 十一分。
第十页,编辑于星期一:二十三点 十一分。
第十一页,编辑于星期一:二十三点 十一分。
第十二页,编辑于星期一:二十三点 十一分。
第十三页,编辑于星期一:二十三点 十一分。
第十四页,编辑于星期一:二十三点 十一分。
第十五页,编辑于星期一:二十三点 十一分。
第一页,编辑于星期一:二十三点 十一分。
第二页,编辑于星期一:二十三点 十一分。
第三页,编辑于星期一:二十三点 十一分。
第四页,编辑于星期一:二十三点 十一分。
第五页,编辑于星期一:二十三点 十一分。
第六页,编辑于星期一:二十三点 十一分。
第七页,编辑于星期一:二十三点 十一分。
第八页,编辑于星期一:二十三点 十一分。
第五十八页,编辑于星期一:二十三点 十一分。
第五十九页,编辑于星期一:二十三点 十一分。
第六十页,编辑于星期一:二十三点 十一分。
第六十一页,编辑于星期一:二十三点 十一分。
第六十二页,编辑于星期一:二十三点 十一分。
第六十三页,编辑于星期一:二十三点 十一分。
第六十四页,编辑于星期一:二十三点 十一分。
第四十四页,编辑于星期一:二十三点 十一分。
第四十五页,编辑于星期一:二十三点 十一分。
第四十六页,编辑于星期一:二十三点 十一分。
第四十七页,编辑于星期一:二十三点 十一分。
第四十八页,编辑于星期一:二十三点 十一分。
第四十九页,编辑于星期一:二十三点 十一分。
第五十页,编辑于星期一:二十三点 十一分。
第二十三页,编辑于星期一:二十三点 十一分。
第二十四页,编辑于星期一:二十三点 十一分。
第二十五页,编辑于星期一:二十三点 十一分。
第7章醇、硫醇、酚

一、醇的结构、分类和命名
1. 结构 Sp3不等性杂化
110℃
醇羟基中的氧原子认为是sp3不等性杂化,利
用两个单电子的sp3轨道形成C-O和O-H键,C-OH的键角接近于110°,余下两对未共用电子对分
别在另两个sp3轨道。
H H C H
sp 109°
3
O
sp
3
H
甲醇的棍棒模型
2. 分类
(1)根据羟基所连烃基结构不同分类 饱和脂肪醇 CH3CH2OH CH2=CHCH2OH
三氧化铬溶于硫酸中配成的试剂成为铬酸试剂
(橙色),铬酸试剂能氧化伯醇或仲醇,反应前 Cr2O72-为橙红色,反应后生成的Cr3+是绿色。故铬 酸试剂可用作醇的鉴别。C=C、C≡C 与铬酸反应 较慢,不能很快观察到颜色变化,故可鉴别开。这
一性质是使用呼吸分析仪检查汽车驾驶员是否酒后
驾车的理论依据。
CH 3CH2OH +
(三)醇的脱水反应
分子内 醇脱水 分子间 烯 醚
(1)分子内脱水生成烯
醇在浓 H2SO4 或 H3PO4 催化下加热,分子内脱水生成烯。
H2C CH2 H OH
浓H 2SO 4 170 ℃
浓 H2SO4 100 ℃
H 2C CH2
+ H2O
H2C CH CH3 H OH
H2C CH CH3 + H2O
2Cr2O7
CH 3COOH + Cr3+
橙色
绿色
四、甲醇、乙醇的功能与毒性(自学)
第二节 硫醇(Mercaptan)
硫和氧在元素周期表中属于同一主族,因此 它们的性质基本上是相似的,在有些有机化合物
中氧的位置可以被硫代替,如硫醇RSH, 硫醚
1. 结构 Sp3不等性杂化
110℃
醇羟基中的氧原子认为是sp3不等性杂化,利
用两个单电子的sp3轨道形成C-O和O-H键,C-OH的键角接近于110°,余下两对未共用电子对分
别在另两个sp3轨道。
H H C H
sp 109°
3
O
sp
3
H
甲醇的棍棒模型
2. 分类
(1)根据羟基所连烃基结构不同分类 饱和脂肪醇 CH3CH2OH CH2=CHCH2OH
三氧化铬溶于硫酸中配成的试剂成为铬酸试剂
(橙色),铬酸试剂能氧化伯醇或仲醇,反应前 Cr2O72-为橙红色,反应后生成的Cr3+是绿色。故铬 酸试剂可用作醇的鉴别。C=C、C≡C 与铬酸反应 较慢,不能很快观察到颜色变化,故可鉴别开。这
一性质是使用呼吸分析仪检查汽车驾驶员是否酒后
驾车的理论依据。
CH 3CH2OH +
(三)醇的脱水反应
分子内 醇脱水 分子间 烯 醚
(1)分子内脱水生成烯
醇在浓 H2SO4 或 H3PO4 催化下加热,分子内脱水生成烯。
H2C CH2 H OH
浓H 2SO 4 170 ℃
浓 H2SO4 100 ℃
H 2C CH2
+ H2O
H2C CH CH3 H OH
H2C CH CH3 + H2O
2Cr2O7
CH 3COOH + Cr3+
橙色
绿色
四、甲醇、乙醇的功能与毒性(自学)
第二节 硫醇(Mercaptan)
硫和氧在元素周期表中属于同一主族,因此 它们的性质基本上是相似的,在有些有机化合物
中氧的位置可以被硫代替,如硫醇RSH, 硫醚
《有机化学醇硫醇酚》课件
多酚
多酚是含有多个羟基的酚,例 如咖啡因。
1 定义
醇是由羟基(-OH)取代烃基得到的化合物。
2 性质
醇具有溶解性强、可与酸发生酯化反应等特点。
不同种类的醇以及它们的命名方法
一元醇
一元醇是含有一个羟基的醇, 例如甲醇。
二元醇
二元醇是含有两个羟基的醇, 例如乙二醇。
三元醇
三元醇是含有三个羟基的醇, 例如甘油。
醇的制备方法
1
氢醇法
通过羰基化合物的加氢反应得到醇。
硫醇的定义和性质
1 定义
硫醇是含有硫原子的类似醇的有机化合物。
2 性质
硫醇具有特殊的气味,可溶于有机溶剂,容 易发生氧化反应。
不同种类的硫醇以及它们的命名方法
一硫醇
一硫醇是含有一个硫原子的硫 醇,例如巯基甲烷。
二硫醇
二硫醇是含有两个硫原子的硫 醇,例如二巯基硫。
多硫醇
多硫醇是含有多个硫原子的硫 醇,例如巯基乙烷。
硫醇的制备方法
1
还原反应
通过还原硫酸盐或硫醇醚制备硫醇。
2
硫化反应
通过硫化物与硒醇反应制备硫醇。
3
亲电加成反应
通过亲电物质与硫醇反应制备含硫化合物。
硫醇的主要用途
1 化学合成
硫醇用于有机合成反应中的硫化、酰化和叔 碳与炔烃的氧化反应。
2 医药领域
硫醇作为医药合成中的中间体,广泛应用于 药物制备。
《有机化学醇硫醇酚》 PPT课件
这个PPT课件将带您深入了解有机化学醇硫醇酚的知识,包括定义、性质、 命名方法、制备方法、主要用途以及在生活中的应用。
什么是有机化学醇硫醇酚?
有机化学醇硫醇酚是一类重要的有机化合物,具有醇、硫醇和酚的结构特点。 这些化合物在生物、化工和医药领域有着广泛的应用。
《醇、硫醇、酚》PPT课件

CH 3
HO OH 3,5-二羟基甲苯
OH OH
儿茶酚catechol
整理ppt
COOH OH
邻-羟基苯甲酸 (水杨酸)
29
酚的结构:
苯酚
OH
O采取sp2杂化,未杂化的p轨道(有一对电
子)与苯环的大p键形成p,p-共轭体系。
➢ O电子云密度,C-O极性 , p,p-共轭 不易断裂——难取代。
➢ O-H极性,H易离去——弱酸 性。
OH SO 3H
浓 H2SO4, 100 ℃
OH
SO 3H
整理ppt
35
3. 与FeCl3显色 用此显色反应可鉴别含酚-OH或具有烯醇式结
构—C=C—OH的化合物。
电影片断: FeCl3检验酚类
整理ppt
36
4. 氧化反应 酚极易氧化,邻、对二元酚更易氧化。
OH K H 2C 2S2O 4 O r7 O
40
作业:
p111 7-5/(1)(3)(6)(10), 7-6/(1)(2)(5), 78/(2)(4), 7-9/(1)(3)(5) 阅读 section5 全文,翻译p13 第五段, p14/5.2 第一段
整理ppt
41
与FeCl3显色
整理ppt
THE END39
2、鉴别下列化合物练习
1、完成反应式
1.CH 3CH 2CHC3 H浓2H SO 4 OH
2. HO
CH 3 KHM + n4O
CH 3
3.
+ B2r
OH
4. HO
CH 2CHC3+H NaOH OH
1,2-丙二醇 叔丁醇 苯甲醇 苯酚 儿茶酚
整理ppt
07章 醇、硫醇、酚

2+
NaOOC CH CH COONa S Hg S
CH2 CH CH2 OH SH SH
CH2 CH CH2 SH SH SO3Na
BAL
(三)氧化反应
[O] [H]
KMnO4
2 R SH
R S S
R
CH3SH
CH3SO3H
.. [O] R S. R .
O ↑ S R .. R O
CH3
S
CH3
CH3CH2CH CH2 H2 O CH3CH2CHCH3 H2SO4 OH (1:1) :) 19% CH3CH CHCH3 81%
R CH CH R' H OH
+ 快 R CH CH R' + H H + OH2
慢
RCH
CHR'
快 消消 β -H
R
+ CH CH H
R' + H O 2
甲基1, 迁移 甲基 2迁移
33-苯 基 -2-丁 醇
5. 多元醇 多元醇 选择连有尽可能多的羟 基的碳链作主链, 基的碳链作主链,依羟基数称某二 某三醇等。 醇、某三醇等。
CH2CH2CH2 OH OH
1, 1,3-丙 二 醇
二、Physical Properties of Alcohol
三、Chemical Properties of Alcohol
..
极性大, 极性大 , 易断裂 H 可质子化 易断裂, 易断裂 ,可发生亲核 取代反应和消去反应 可氧化
C
C H
O ..
1. 醇与金属钠反应
2 ROH
+ 2 Na
H R
2 RONa + H2↑
NaOOC CH CH COONa S Hg S
CH2 CH CH2 OH SH SH
CH2 CH CH2 SH SH SO3Na
BAL
(三)氧化反应
[O] [H]
KMnO4
2 R SH
R S S
R
CH3SH
CH3SO3H
.. [O] R S. R .
O ↑ S R .. R O
CH3
S
CH3
CH3CH2CH CH2 H2 O CH3CH2CHCH3 H2SO4 OH (1:1) :) 19% CH3CH CHCH3 81%
R CH CH R' H OH
+ 快 R CH CH R' + H H + OH2
慢
RCH
CHR'
快 消消 β -H
R
+ CH CH H
R' + H O 2
甲基1, 迁移 甲基 2迁移
33-苯 基 -2-丁 醇
5. 多元醇 多元醇 选择连有尽可能多的羟 基的碳链作主链, 基的碳链作主链,依羟基数称某二 某三醇等。 醇、某三醇等。
CH2CH2CH2 OH OH
1, 1,3-丙 二 醇
二、Physical Properties of Alcohol
三、Chemical Properties of Alcohol
..
极性大, 极性大 , 易断裂 H 可质子化 易断裂, 易断裂 ,可发生亲核 取代反应和消去反应 可氧化
C
C H
O ..
1. 醇与金属钠反应
2 ROH
+ 2 Na
H R
2 RONa + H2↑
醇硫醇酚

很弱,不存在分子间缔合,而以单分子形式存在,也不能与
水形成氢键,因此其沸点和水溶度都比相应的醇要低得多。
C2H5OH
bp (℃)
78
sol(g/100g水)
混溶
C2H5SH
35 1.5
CH3SCH3
38
硫醇的另一特性是: 一般≤9C的硫醇 都有恶臭。工业上利用它作为臭味剂。
7
第七章 醇、硫醇、酚
第一节 醇 (一、结构分类命名)
CH2O Cu + 2H2O CH2O
蓝色
+ CH2—CH—CH2
OH OH OH
Cu(OH)2 -2H2O CH2—CH—CH2 O O OH
Cu
甘油铜(蓝色)
21
第七章 醇、硫醇、酚
第一节 醇 (三、化学性质)
(二) 醇与无机含氧酸的酯化反应
醇可与含氧无机酸(如硝酸、亚硝酸、硫酸 和磷酸等)反应,生成相应的无机酸酯,其中 的 N、P 和 S 都是通过 O 与烷基相连的。
RC CH + NaNH2
RC CNa + NH3 (pKa=34)
HC≡CNa + R-OH ——> HC≡CH + RONa
酸性序: H2O > R-OH > HC≡CH > NH3 > R-H 碱性序: OH- < RO- < HC≡C- < NH2- < R-
醇钠在有机合成中可用作引入烷氧基的试剂。
第七章
醇 Alcohols 硫醇Sulfur Alcohols 酚 Phenols
1
第七章 醇、硫醇、酚
第七章 醇、硫醇、酚
醇、酚、醚都是烃的含氧衍生物,也可看作 水的烃基衍生物。碳与氧以单键相连(C—O)。
水形成氢键,因此其沸点和水溶度都比相应的醇要低得多。
C2H5OH
bp (℃)
78
sol(g/100g水)
混溶
C2H5SH
35 1.5
CH3SCH3
38
硫醇的另一特性是: 一般≤9C的硫醇 都有恶臭。工业上利用它作为臭味剂。
7
第七章 醇、硫醇、酚
第一节 醇 (一、结构分类命名)
CH2O Cu + 2H2O CH2O
蓝色
+ CH2—CH—CH2
OH OH OH
Cu(OH)2 -2H2O CH2—CH—CH2 O O OH
Cu
甘油铜(蓝色)
21
第七章 醇、硫醇、酚
第一节 醇 (三、化学性质)
(二) 醇与无机含氧酸的酯化反应
醇可与含氧无机酸(如硝酸、亚硝酸、硫酸 和磷酸等)反应,生成相应的无机酸酯,其中 的 N、P 和 S 都是通过 O 与烷基相连的。
RC CH + NaNH2
RC CNa + NH3 (pKa=34)
HC≡CNa + R-OH ——> HC≡CH + RONa
酸性序: H2O > R-OH > HC≡CH > NH3 > R-H 碱性序: OH- < RO- < HC≡C- < NH2- < R-
醇钠在有机合成中可用作引入烷氧基的试剂。
第七章
醇 Alcohols 硫醇Sulfur Alcohols 酚 Phenols
1
第七章 醇、硫醇、酚
第七章 醇、硫醇、酚
醇、酚、醚都是烃的含氧衍生物,也可看作 水的烃基衍生物。碳与氧以单键相连(C—O)。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
4、产物醇钠是强碱,易水解
R O N a + H 2 O R O H + N a O H
碱 性 R - R O - H O -
碱 性 R 3 C O N a 编辑R ppt2 C H O N a R C H 2 12O N a
(二)与无机含氧酸的反应
R O H + H O N O 2 R O N O 2 + H 2 O
二、物理性质 1、色态味 C1—C4低级醇为无色透明液体,酒味; 较高级醇为粘稠液体; C12以上醇为蜡状固体。
2、沸点 a、随碳数目增多而升高; b、相同碳数醇,支链越多,沸点越低; c、比相近分子量烷烃沸点高(氢键)。
3、水溶性 甲醇、乙醇、丙醇都可与水混溶;
随醇分子量增加而水溶性降低,
C10醇以上几编辑乎ppt不溶于水。
3) 系统命名法---结构比较复杂的醇,采用系统命名法
1 23 4 56 CH3CHCH2CH2CHCH3
OH
CH3
5-甲基-2-己醇
一般原则:1、选主链(含羟基所连碳且碳数最多) 2、编号(近羟基一端开始) 3、取代基在前,母体在后(羟基位置)
编辑ppt
7
32
1
CH3CHCH2CH2OH
C 4 H2C 5 H3 3-甲 基 -1-戊 醇
编辑ppt
13
C H 3O H+H 2SO 4
O
O
C H 3O SO HC H 3O H C H 3O SO C H 3
O
硫 酸 氢 甲 酯
O
硫 酸 二 甲 酯
O
O
O
O
R O H+H O PO H
R O PO HR O H
O H -H 2O
-H 2O
O H
R O PO HR O H
-H 2O
O R
编辑ppt
1
1、防腐消毒用的乙醇、苯酚、 甲苯酚(其肥皂液为来苏儿);
2、用作润滑剂的甘油,可治疗便秘;
HO CH2
3、常用的重金属中毒的解毒剂二巯基丙醇;H S C H
HS CH2
4、具有抗菌和局部麻醉作用,常用于牙科止痛和 消毒的丁香酚;
HO
CH2CH=CH2
CH3-O
5、治疗伤风、感冒、头痛的水杨酸等
10
三、醇的化学性质:H
δ
RRCHC2
H
O CδH+酸 δH性, O生 - 成 H酯 +
氧化反应 形 H成C ,发生取代及消除反应
1、氧元素电负性大,C-O键和O-源自键极性大, 异裂可成RO-、正碳离子,发生取代反应; 2、醇羟基具有孤电子对,可质子化; 3、HO-吸电子诱导效应, -H活泼。
(一)与碱金属的反应
编辑ppt
COOH OH
2
•醇
• 结构、命名和分类 • 物理性质 • 化学性质
• 硫醇
• 结构、命名和分类 • 物理性质 • 化学性质
•酚
• 结构、命名和分类 • 物理性质 • 化学性质
编辑ppt
3
第一节
一、结构、分类和命名 (一)结构
sp3杂 化 轨道
HO
..
..
醇 (alchol)
1 0 8 .9 °
H31C2C CH33CH2C 4 H25CH62CH7CH3
OH
CH3
2,6-二 甲 基 -2-庚 醇
编辑ppt
8
C H 3C H 2C H 4 2C 3 H C 2 H 2 1C H 2C H 2O H C HC H 2 4 -丙 基 -5 -己 烯 -1 -醇
3
2 CH3 1
4
OH
5
2-甲 基 环 戊 醇
R O H + N a
编辑ppt
R O N a+ 1 2H 2 11
讨论: 1、 醇与钠比水与钠反应缓和。
酸 性 H 2 OR O HR H
2、低级醇反应顺利;高级醇较慢,甚至很难。
3、反应活泼性比较:
H 2 O C H 3 O H R C H 2 O H R 2 C H O H R 3 C O H
C H 2C H C H 2
C H 2 C H C H 2
+ 3 H O N O 2
+ 3 H 2 O
O H O H O H
O N O 2O N O 2 O N O 2
注:1、产物甘油三硝酸酯受热易分解爆炸;其 片剂含
于舌下可缓解心绞痛和胆绞痛(急救 药)。
2、磷酸酯的结构多包含在核酸、磷脂、ATP中。
OH CH2CHCH2CH3
1234
1-苯 基 -2-丁 醇
H3C CH3
H3C C C CH3 2 ,3 - 二 甲 基 - 2 ,3 - 丁 二 醇
1H2 O 3 OHC 42H -C2-HC2H
C3 H
OH OH
OH OH
1,3-丙二醇 1, 3 顺-丙 编1辑二 -甲pp醇 t 基-1,2-环顺 己1二乙 醇基1, 2 环 9 己 二 醇
伯 醇 (1° ) 仲 醇 (2° ) 叔 醇 (3° ) 甲 醇
编辑ppt
6
(三1))俗命C 名名3H C C :3H C H 如2 O 乙H醇H C 俗3 称H C C 酒3 O H 精,H 丙三醇O 称为H甘油等C2 。O HH 2) 简单异 的丁 一醇 元醇用普叔 通C 丁 命醇 3H 名法环 命己 名醇 。 苄 醇
CH
H
H
1 0 9 .3 °
H
sp3
sR p3 C H108.9°O H
O原 子 为 sp3杂 化 由 于 在 sp3杂 化 轨 道 上 有 未 共 用 电 子 对 ,
两 对 之 间 产 生 斥 力 , 使 得 ∠ C-O 小 -于 H
1编09 辑.p5 pt°
4
(二)分类
1.按烃基种类分
脂肪醇 脂环醇
R O PO R O R
烷 基 磷 酸 酯 二 烷 基 磷 酸 酯 三 烷 基 磷 酸 酯
烷基二磷酸酯、烷基三磷酸酯在生物化学中非常重要。
O OO
腺苷-O-P-O~P-O~P-O-
O- O- O编辑ppt ATP
第七章 醇、硫醇、酚
(alcohol ,thiol and phenol)
烃的含氧或硫衍生物。官能团:羟基、巯基。
通 式 :RO HRS HA r O H
醇 医学上的重要意义
硫 醇 酚
一、从分子水平研究生理病理及药理的重要物质基础;
二、硫醇类重金属解毒剂,可调整代谢、保护酶系;
三、常见的一些具体例子:
H2C CHCH2OH CH3CHCH3 OH
OH
CH3 H3C C OH
CH3
芳香醇
CH2OH
编辑ppt
5
2、按羟基数目分
C H 3C H 2O H 一 元 醇
C H 2 C H 2 C H 2C HC H 2 O HO H O HO HO H
多元 醇
3、按HO--连碳原子类型分
R
RC H 2 O HRC H O HR C O HC H 3O H R R
R O N a + H 2 O R O H + N a O H
碱 性 R - R O - H O -
碱 性 R 3 C O N a 编辑R ppt2 C H O N a R C H 2 12O N a
(二)与无机含氧酸的反应
R O H + H O N O 2 R O N O 2 + H 2 O
二、物理性质 1、色态味 C1—C4低级醇为无色透明液体,酒味; 较高级醇为粘稠液体; C12以上醇为蜡状固体。
2、沸点 a、随碳数目增多而升高; b、相同碳数醇,支链越多,沸点越低; c、比相近分子量烷烃沸点高(氢键)。
3、水溶性 甲醇、乙醇、丙醇都可与水混溶;
随醇分子量增加而水溶性降低,
C10醇以上几编辑乎ppt不溶于水。
3) 系统命名法---结构比较复杂的醇,采用系统命名法
1 23 4 56 CH3CHCH2CH2CHCH3
OH
CH3
5-甲基-2-己醇
一般原则:1、选主链(含羟基所连碳且碳数最多) 2、编号(近羟基一端开始) 3、取代基在前,母体在后(羟基位置)
编辑ppt
7
32
1
CH3CHCH2CH2OH
C 4 H2C 5 H3 3-甲 基 -1-戊 醇
编辑ppt
13
C H 3O H+H 2SO 4
O
O
C H 3O SO HC H 3O H C H 3O SO C H 3
O
硫 酸 氢 甲 酯
O
硫 酸 二 甲 酯
O
O
O
O
R O H+H O PO H
R O PO HR O H
O H -H 2O
-H 2O
O H
R O PO HR O H
-H 2O
O R
编辑ppt
1
1、防腐消毒用的乙醇、苯酚、 甲苯酚(其肥皂液为来苏儿);
2、用作润滑剂的甘油,可治疗便秘;
HO CH2
3、常用的重金属中毒的解毒剂二巯基丙醇;H S C H
HS CH2
4、具有抗菌和局部麻醉作用,常用于牙科止痛和 消毒的丁香酚;
HO
CH2CH=CH2
CH3-O
5、治疗伤风、感冒、头痛的水杨酸等
10
三、醇的化学性质:H
δ
RRCHC2
H
O CδH+酸 δH性, O生 - 成 H酯 +
氧化反应 形 H成C ,发生取代及消除反应
1、氧元素电负性大,C-O键和O-源自键极性大, 异裂可成RO-、正碳离子,发生取代反应; 2、醇羟基具有孤电子对,可质子化; 3、HO-吸电子诱导效应, -H活泼。
(一)与碱金属的反应
编辑ppt
COOH OH
2
•醇
• 结构、命名和分类 • 物理性质 • 化学性质
• 硫醇
• 结构、命名和分类 • 物理性质 • 化学性质
•酚
• 结构、命名和分类 • 物理性质 • 化学性质
编辑ppt
3
第一节
一、结构、分类和命名 (一)结构
sp3杂 化 轨道
HO
..
..
醇 (alchol)
1 0 8 .9 °
H31C2C CH33CH2C 4 H25CH62CH7CH3
OH
CH3
2,6-二 甲 基 -2-庚 醇
编辑ppt
8
C H 3C H 2C H 4 2C 3 H C 2 H 2 1C H 2C H 2O H C HC H 2 4 -丙 基 -5 -己 烯 -1 -醇
3
2 CH3 1
4
OH
5
2-甲 基 环 戊 醇
R O H + N a
编辑ppt
R O N a+ 1 2H 2 11
讨论: 1、 醇与钠比水与钠反应缓和。
酸 性 H 2 OR O HR H
2、低级醇反应顺利;高级醇较慢,甚至很难。
3、反应活泼性比较:
H 2 O C H 3 O H R C H 2 O H R 2 C H O H R 3 C O H
C H 2C H C H 2
C H 2 C H C H 2
+ 3 H O N O 2
+ 3 H 2 O
O H O H O H
O N O 2O N O 2 O N O 2
注:1、产物甘油三硝酸酯受热易分解爆炸;其 片剂含
于舌下可缓解心绞痛和胆绞痛(急救 药)。
2、磷酸酯的结构多包含在核酸、磷脂、ATP中。
OH CH2CHCH2CH3
1234
1-苯 基 -2-丁 醇
H3C CH3
H3C C C CH3 2 ,3 - 二 甲 基 - 2 ,3 - 丁 二 醇
1H2 O 3 OHC 42H -C2-HC2H
C3 H
OH OH
OH OH
1,3-丙二醇 1, 3 顺-丙 编1辑二 -甲pp醇 t 基-1,2-环顺 己1二乙 醇基1, 2 环 9 己 二 醇
伯 醇 (1° ) 仲 醇 (2° ) 叔 醇 (3° ) 甲 醇
编辑ppt
6
(三1))俗命C 名名3H C C :3H C H 如2 O 乙H醇H C 俗3 称H C C 酒3 O H 精,H 丙三醇O 称为H甘油等C2 。O HH 2) 简单异 的丁 一醇 元醇用普叔 通C 丁 命醇 3H 名法环 命己 名醇 。 苄 醇
CH
H
H
1 0 9 .3 °
H
sp3
sR p3 C H108.9°O H
O原 子 为 sp3杂 化 由 于 在 sp3杂 化 轨 道 上 有 未 共 用 电 子 对 ,
两 对 之 间 产 生 斥 力 , 使 得 ∠ C-O 小 -于 H
1编09 辑.p5 pt°
4
(二)分类
1.按烃基种类分
脂肪醇 脂环醇
R O PO R O R
烷 基 磷 酸 酯 二 烷 基 磷 酸 酯 三 烷 基 磷 酸 酯
烷基二磷酸酯、烷基三磷酸酯在生物化学中非常重要。
O OO
腺苷-O-P-O~P-O~P-O-
O- O- O编辑ppt ATP
第七章 醇、硫醇、酚
(alcohol ,thiol and phenol)
烃的含氧或硫衍生物。官能团:羟基、巯基。
通 式 :RO HRS HA r O H
醇 医学上的重要意义
硫 醇 酚
一、从分子水平研究生理病理及药理的重要物质基础;
二、硫醇类重金属解毒剂,可调整代谢、保护酶系;
三、常见的一些具体例子:
H2C CHCH2OH CH3CHCH3 OH
OH
CH3 H3C C OH
CH3
芳香醇
CH2OH
编辑ppt
5
2、按羟基数目分
C H 3C H 2O H 一 元 醇
C H 2 C H 2 C H 2C HC H 2 O HO H O HO HO H
多元 醇
3、按HO--连碳原子类型分
R
RC H 2 O HRC H O HR C O HC H 3O H R R
