浙江省医疗器械经营企业现场检查评 ..
浙江省药品监督管理局关于印发《浙江省<医疗器械经营企业监督管理办法>实施细则》(试行)的通知-

浙江省药品监督管理局关于印发《浙江省<医疗器械经营企业监督管理办法>实施细则》(试行)的通知正文:---------------------------------------------------------------------------------------------------------------------------------------------------- 浙江省药品监督管理局关于印发《浙江省<医疗器械经营企业监督管理办法>实施细则》(试行)的通知各市、县(市、区)药品监督管理局(分局):为加强医疗器械经营企业的监督管理,根据《医疗器械监督管理条例》和国家药品监督管理局《医疗器械经营企业监督管理办法》的规定,我局制定了《浙江省〈医疗器械经营企业监督管理办法〉实施细则》(试行),现印发给你们,自2003年8月1日起实施。
我局2000年10月10日发布的《浙江省医疗器械经营企业资格认可实施细则(试行)》同时废止。
浙江省药品监督管理局2003年6月30日浙江省《医疗器械经营企业监督管理办法》实施细则(试行)第一章总则第一条为加强对医疗器械经营企业的监督管理,规范医疗器械的经营行为,根据《医疗器械监督管理条例》和国家药品监督管理局《医疗器械经营企业监督管理办法》,结合我省实际,制定本细则。
第二条根据国家药品监督管理局《医疗器械分类目录》(2002年版)规定及《医疗器械分类规则》判定的管理类别,确定医疗器械经营企业的分类。
第三条凡在本省开办医疗器械经营企业,均应遵守本细则。
开办第一类医疗器械经营企业,应取得《医疗器械经营企业备案表》后,方可经营。
开办第二类、第三类医疗器械经营企业,应取得《医疗器械经营企业许可证》后,方可经营。
第四条各设区市药品监督管理局(下称“市局”)负责辖区内第一类医疗器械经营企业的备案和第二类医疗器械经营企业许可证的审批。
省药品监督管理局(下称“省局”)负责第三类医疗器械经营企业许可证的审批。
浙江省医疗器械经营企业现场检查评分表

5.3.6
对初次配镜者,应索取最近半年眼科医生的验光处方,或将眼科医生的检查记录及是否适合配戴角膜接触镜的意见登记在册(表格),并保存二年以上。
查制度、档案及询问。验配规占10分,按通则评分。抽查5位配戴者档案,每缺一份档案或记录不完整的扣5分,20分扣完为止。
30
5.3 经营验配软性角膜接触镜及护理用液
5.3.1
应至少配备1名中专以上学历或初级以上职称的相关专业人员(相关专业:眼视光学、视光与配镜专业、眼科学和光学仪器)。
查人员任命和有关证书,达不到要求的,不得分。如配有一名持有高级验光员以上(含高级)书人员(其资质的取得应获得劳动部门认可),可得18分。
20
5.3.5
有严格的验配管理规并有使用产品销售跟踪记录。对所有配戴者建立档案(包括配戴者编号、、性别、年龄、验配日期、验配机构、验配人员、产品名称、规格等),保存验配记录、复查记录。
查制度、档案及询问。验配规占10分,按通则评分。抽查5位配戴者档案,每缺一份档案或记录不完整的扣5分,10分扣完为止。
现场查看,必要时查储存设备清单,有一项不达要求者不得分;储存条件及设备设施的配置情况按通则评分。
15
2.7
效期产品应按顺序存放,先进先出,近效期先出,有便于识别的标记。
现场查看,必要时结合有关记录,按通则评分。
10
三、管理制度及记录
3.1
企业应建立健全产品质量管理制度,至少应包括:①产品采购索证制度,②进货验收制度,③仓库保管制度,④出库复核制度,⑤效期产品管理制度,⑥不合格品的确认和处理制度,⑦购销记录档案制度,⑧产品售后服务制度等。
查制度是否完备,容是否完整。缺一项制度不得分。抽查三项制度,其容完整性情况,按通则评分。
杭州市医疗器械经营许可评定标准

企业应当依据本规范建立覆盖医疗器械经营全过程的质量管理制度,并保存相关记录或者档案,是否制定了以下内容:1)质量管理机构或者质量管理人员的职责;2)质量管理的规定;3)采购、收货、验收的规定(包括采购记录、验收记录、随货同行单等);4)供货者资格审核的规定(包括供货者及产品合法性审核的相关证明文件等);5)库房贮存、出入库管理的规定(包括温度记录、入库记录、定期检查记录、出库记录等);6)销售和售后服务的规定(包括销售人员授权书、购货者档案、销售记录等);7)不合格医疗器械管理的规定(包括销毁记录等);8)医疗器械退、换货的规定;9)医疗器械不良事件监测和报告规定(包括停止经营和通知记录等);10)医疗器械召回规定(包括医疗器械召回记录等);11)设施设备维护及验证和校准的规定(包括设施设备相关记录和档案等);12)卫生和人员健康状况的规定(包括员工健康档案等);13)质量管理培训及考核的规定(包括培训记录等);14)医疗器械质量投诉、事故调查和处理报告的规定(包括质量投诉、事故调查和处理
企业在采购前有否审核供货者的合法资格、所购入医疗器械的合法性并获取加盖供货者公章的相关证明文件或者复印件,包括:1)营业执照;2)医疗器械生产或者经营的许可证或者备案凭证;3)医疗器械注册证或者备案凭证;4)销售人员身份证复印件,加盖本企业公章的授权书原件。授权书应当载明授权销售的品种、地域、期限,注明销售人员的身份证号码。
5.7
收货人员对符合收货要求的医疗器械,有否按品种特性要求放于相应待验区域,或者设置状态标示,并通知验收人员进行验收。需要冷藏、冷冻的医疗器械应当在冷库内待验。
*5.8
验收人员有否对医疗器械的外观、包装、标签以及合格证明文件等进行检查、核对,并做好验收记录,包括医疗器械的名称、规格(型号)、注册证号或者备案凭证编号、生产批号或者序列号、生产日期和有效期(或者失效期)、生产企业、供货者、到货数量、到货日期、验收合格数量、验收结果、验收人员姓名和验收日期等内容。验收不合格的还应当注明不合格事项及处置措施。
浙江省医疗器械经营企业现场检查评分表

仓库内应设有明显标识表记标帜:待验区、合格区、不合格区、发货区、退货区,不同品种分类码放,库存货位卡清楚。兼营医疗器械的经营企业,医疗器械产物应单独堆放并有序。
现场查看,无明显标识表记标帜扣5分,不执行分类码放扣5分,无货位卡扣5分;其余按通那么评分。兼营企业的产物,发现一处未单独堆放扣5分。
15
5.1经营第三类植入〔介入〕类医疗器械,不局限于6846、6877〔植入材料和人工器官、介入器材〕。
企业还应至少配备1名具有大专以上学历或中级以上职称的专业卫生技术人员。
查人员任命和有关证书。达不到要求的,不得分。
20
企业发卖人员应有中等教育以上学历,熟悉产物性能、适应范围和使用要求,了解有关医学常识和相关法规安然要求。
10
采购索证制度的执行。经营的产物应具备由供应商提供的产物注册证书和有关出产或经营资格证明〔加盖企业鲜章的复印件〕,并有购销凭证及协议。购销凭证至少包罗:产物名称、规格、购〔销〕数量、出产批号或出厂编号,购〔销〕单元,初度经营品种应成立质量审核制度,并成立档案。
抽查任意二个产物,有一个产物无证书或无凭证及协议的扣10分,扣完为止。对初度经营品种未予以必要审核或无审核档案的,每发现一个扣5分,扣完为止。
查抄方法同上。面积不符要求者,不得分。其它经营条件,现场查看及询问情况,按通那么评分。
15
仓库不克不及设置在居民住宅房〔能提供现实际用途已发生改变的证明文件除外〕。仓储面积不低于20平方米,经营品种体积较小者可视情放宽25%。零售连锁企业总部仓储面积不低于60平方米。
查抄方法同上。此中一项不符要求者,不得分。有理由不作仓库要求的,视为缺项。
抽三个产物,有一处账物卡不符扣5分,扣完为止。无产物保管、养护记录的,扣5至10分。
医疗器械经营企业现场核查验收细则

医疗器械经营企业现场核查验收细则一、引言医疗器械的质量和安全性直接关系到公众的健康和生命安全。
为了规范医疗器械经营企业的经营行为,确保所经营的医疗器械合法、安全、有效,特制定本现场核查验收细则。
本细则旨在明确现场核查的标准和要求,为监管部门和企业提供指导。
二、企业资质与人员要求(一)企业应依法取得营业执照,并在核准的经营范围内从事医疗器械经营活动。
(二)企业负责人应熟悉医疗器械监督管理的法律法规、规章规范和所经营医疗器械的相关知识。
(三)质量管理人应具有医疗器械相关专业大专以上学历或者中级以上专业技术职称,同时具有 3 年以上医疗器械经营质量管理工作经历。
(四)企业应配备与经营规模和经营范围相适应的质量管理人员和售后服务人员,且上述人员应经过相关培训并考核合格。
三、经营场所与设施设备(一)企业应有与经营规模和经营范围相适应的、相对独立的经营场所。
经营场所应整洁、卫生、通风良好,不得设在居民住宅内、军事管理区(不含可租赁区)以及其他不适合经营的场所。
(二)经营场所的面积应符合以下要求:1、经营第二类医疗器械的,经营场所面积不得少于 40 平方米。
2、经营第三类医疗器械的,经营场所面积不得少于 60 平方米。
3、从事体外诊断试剂批发业务的,经营场所面积不得少于 100 平方米。
(三)企业应具有与经营规模和经营范围相适应的储存条件,包括符合医疗器械产品特性要求的常温库、阴凉库、冷库等仓储设施设备。
1、常温库温度应为 0℃-30℃,阴凉库温度不应高于 20℃,冷库温度应为 2℃-8℃。
2、仓库应划分待验区、合格品区、不合格品区、发货区等专用区域,并采取有效的隔离措施。
3、仓库内应配备符合要求的货架、托盘、温湿度监测设备、防虫防鼠设施等。
四、质量管理体系文件(一)企业应建立覆盖医疗器械经营全过程的质量管理体系文件,包括质量管理制度、部门及岗位职责、操作规程等。
(二)质量管理制度应至少包括:采购、验收、贮存、销售、运输、售后服务等环节的质量管理制度。
医疗器械《经营许可证》现场检查项目

医疗器械《经营许可证》现场检查项目医疗器械《经营许可证》是指医疗器械经营企业在经过相关审批程序后才能获得的一种执照,它是医疗器械企业正常开展经营活动的必备证件。
为确保医疗器械企业的质量管理体系符合相关要求,保障医疗器械的安全性、有效性和可靠性,相关部门会进行现场检查,以查验医疗器械企业是否符合相关要求。
本文将详细介绍医疗器械《经营许可证》现场检查的项目。
1.企业规模和场地设施现场检查会对医疗器械企业的规模和场地设施进行审查。
包括企业的注册资金、经营面积、生产车间、仓储区域等。
检查人员会查看企业的房屋产权证明、环境卫生等相关证照,并评估企业场地是否符合医疗器械的安全性、生产流程和质量管理的要求。
2.质量管理体系现场检查会对医疗器械企业的质量管理体系进行全面检查。
包括企业的质量手册、质量管理制度、质量目标和管理责任等。
检查人员会评估企业的质量文化、管理制度是否完善,是否有有效的质量控制措施,并对企业的质量风险管理、市场监测和不良事件报告进行审核。
3.采购管理现场检查还会对医疗器械企业的采购管理进行审查。
包括企业的供应商评审制度、采购合同管理、样品确认和验收等。
检查人员会评估企业的供应商选择标准、采购程序、样品确认和验收流程是否符合相关规定,以确保采购的医疗器械符合标准要求。
4.生产过程控制5.销售和售后服务现场检查还会对医疗器械企业的销售和售后服务进行审查。
包括销售合同管理、产品配送和售后服务制度等。
检查人员会评估企业的销售渠道和销售行为是否合法规范,是否有完善的售后服务体系,以确保医疗器械的合法销售和良好使用效果。
总之,医疗器械《经营许可证》现场检查项目主要包括企业规模和场地设施、质量管理体系、采购管理、生产过程控制、销售和售后服务等方面。
企业需要严格按照相关要求进行准备和整改,以获得检查人员的认可,并顺利通过现场检查。
只有通过了现场检查,医疗器械企业才能获得《经营许可证》,正常经营医疗器械。
浙江省医疗器械经营企业现场检查评分标准-浙江省医疗器械经

浙江省医疗器械经营企业现场检查评分标准□企业自查□现场检查说明:(一)本标准根据《医疗器械经营企业监督管理办法》(国家药品监督管理局令第19号)和《浙江省<医疗器械经营企业监督管理办法>实施细则》(试行)制定。
(二)本标准适用于浙江省医疗器械经营企业资格认可的现场考核, 也是医疗器械经营企业进行自查和各级药品监督管理部门对医疗器械经营企业进行日常监管(包括年度验证)的依据。
(三)本标准共5项32条, 计600分;其中: 第一至第四部分一般规定各100分, 第五部分专项规定分为规定Ⅰ和规定Ⅱ各100分。
第一部分: 人员与机构, 项目编号1.1至1.5;第二部分: 场地及设施, 项目编号2.1至2.6;第三部分: 管理制度及记录, 项目编号3.1至3.4;第四部分: 销售与售后服务, 项目编号4.1至4.5。
第五部分: 专项规定Ⅰ, 项目编号5.1.1至5.1.6;专项规定Ⅱ, 项目编号5.2.1至5.2.6。
(四)对新开办的医疗器械经营企业的现场审核, 重点审核人员资质、经营场所、仓储条件和管理制度的建立, 年度验证和换证则须审核全部内容。
(五)合格判定的标准: 每部分得分不低于应得分的80%, 为“通过”;否则为“不通过”。
(六)不宜量化的条款按照评分通则进行打分, 即实得分等于标准分乘以评分系数。
评分系数及含义为:1.达到规定要求的系数为1.0;2.基本达到规定要求的系数为0.8;3.工作已开展但有缺陷的系数为0.5;4.达不到要求的系数为0。
(七)缺项的处理:对不适用的检查项目为缺项, 缺项不计分, 但需说明理由。
得分率=实得分÷应得分×100%。
(八)一次性使用无菌医疗器械经营企业资格认可, 按照原国家药品监督管理局《一次性使用无菌医疗器械经营企业审查评分办法》执行, 单独进行现场验收。
浙江省医疗器械经营企业现场检查评分标准浙江省医疗器械经营企业现场检查评分表□企业自查□现场检查。
医疗器械经营企业现场验收标准

医疗器械经营企业现场验收标准医疗器械经营企业是医疗器械的重要流通环节,其经营质量直接关系到医疗器械产品的质量和安全。
为了确保医疗器械经营企业的经营活动符合相关法律法规和标准要求,对其进行现场验收是十分必要的。
本文将就医疗器械经营企业现场验收标准进行详细介绍,以便相关部门和人员能够准确、全面地进行验收工作。
一、证照齐全。
在进行医疗器械经营企业现场验收时,首先要核查其证照是否齐全。
包括《医疗器械经营许可证》、《医疗器械经营备案证》等相关证照,必须保证有效并符合经营范围。
二、库房环境。
医疗器械经营企业的库房环境对产品的质量和安全有着直接的影响。
验收人员需对其库房环境进行全面检查,包括温度、湿度、通风等条件是否符合要求,以及是否存在有害物质、异味等影响产品质量的因素。
三、产品储存。
医疗器械产品的储存是关键的一环,验收人员需要对医疗器械经营企业的产品储存情况进行仔细检查。
包括产品的分类、标识、包装是否完好,是否存在受潮、变质、破损等情况,以及是否按照要求进行分类存放。
四、销售管理。
医疗器械经营企业的销售管理直接关系到产品的流通和安全,验收人员需对其销售管理制度进行全面审查。
包括销售记录、产品追溯体系、产品召回制度等是否健全,是否存在无证销售、假冒伪劣产品等违法行为。
五、质量管理。
医疗器械经营企业应建立健全的质量管理体系,验收人员需对其质量管理制度进行全面检查。
包括质量管理文件、质量控制记录、不合格品处理等是否符合相关要求,是否存在质量管理混乱、无序等情况。
六、人员素质。
医疗器械经营企业的从业人员素质直接关系到经营活动的规范和质量,验收人员需对其从业人员的培训情况进行审查。
包括是否具有相关从业资格证书、是否进行定期培训等,以及是否存在无证操作、无培训上岗等情况。
七、设备设施。
医疗器械经营企业的设备设施对产品的质量和安全有着重要影响,验收人员需对其设备设施进行全面检查。
包括设备设施的完好情况、是否定期维护、是否存在超范围使用等情况。
医疗器械经营企业现场检查整改报告

医疗器械经营企业现场检查整改报告目录一、内容描述 (2)1.1 背景介绍 (2)1.2 目的和意义 (2)二、检查概述 (3)2.1 检查时间 (4)2.2 检查范围 (4)2.3 检查内容 (6)三、发现的问题 (7)3.1 设备设施问题 (8)3.2 人员资质问题 (8)3.3 文件管理问题 (9)3.4 运营管理问题 (10)3.5 其他问题 (10)四、整改措施 (11)4.1 设备设施整改 (12)4.2 人员培训 (13)4.3 文件完善 (14)4.4 运营改进 (15)4.5 其他措施 (16)五、整改效果评估 (17)5.1 整改后的设备设施状况 (18)5.2 人员资质和能力提升 (19)5.3 文件管理的规范性 (20)5.4 运营效率和质量的提升 (21)六、总结与展望 (23)6.1 整改工作成果总结 (23)6.2 未来改进方向 (24)一、内容描述本次医疗器械经营企业现场检查旨在深入贯彻国家相关法律法规,加强医疗器械市场监管,确保公众用械安全有效。
通过实地走访、资料审查及人员询问等方式,全面检查了企业的经营条件、质量管理、销售记录及售后服务等关键环节。
1.1 背景介绍未按照《医疗器械经营监督管理办法》建立健全医疗器械进货查验、销售记录等管理制度;未按照《医疗器械经营质量管理规范》对医疗器械进行分类管理、定期检查和维护保养;未按照《医疗器械广告审查发布管理办法》对医疗器械广告进行审查和发布;未按照《医疗器械生产监督管理办法》对医疗器械生产企业进行资质审核和监督检查;未按照《医疗器械网络销售监督管理办法》对医疗器械网络销售进行监管。
1.2 目的和意义本次现场检查整改报告的目的是对医疗器械经营企业在经营过程中存在的问题进行全面梳理和深入分析,确保企业严格按照相关法律法规和行业标准进行操作,保障公众使用医疗器械的安全性和有效性。
其意义在于:促进医疗器械经营企业规范化运营,提高企业管理水平和风险防范能力,确保企业持续健康发展。
浙江省医疗器械生产企业信用评价指标及评分标准
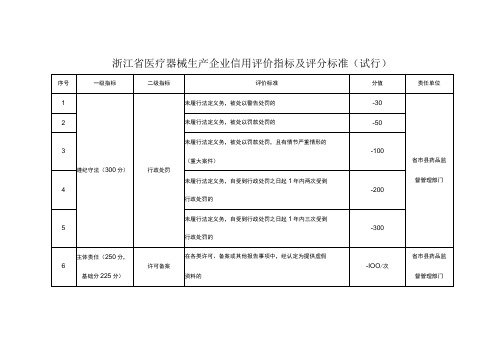
浙江省医疗器械生产企业信用评价指标及评分标准(试行)
2 .各项二级指标的加减总分超出其相应的一级指标权重分值的,加减总分以其所属一级指标分值为上限;
3 .遵纪守法指标项下,案件信息应在结案后使用,同起案件存在多个扣分项的,取最高扣分项;
4 .正向激励指标项下,相应的荣誉奖励以及注册批件等需提供盖有公章的相关证明材料,标准起草、创新认定加分仅限一次;
5 .符合正文第十五条和第十六条情形,经审核同意进行信用修复的,清除扣分值的50%o。
医疗器械经营企业现场检查验收细则

医疗器械经营企业现场检查验收细则为了确保医疗器械的质量和安全性,保障患者的生命健康,医疗器械经营企业在开始运营前需要进行现场检查验收。
本文将详细介绍医疗器械经营企业现场检查验收的细则和要求。
一、设备条件1. 办公室设施:医疗器械经营企业应设有统一的办公室,办公区域面积应满足企业规模需要,布局合理,明确划分各个功能区域。
2. 仓库条件:医疗器械经营企业的仓库应保证通风、干燥、无致病微生物和灰尘等污染物,仓库内设备摆放整齐,各区域功能划分明确。
3. 冷链设备:对于需要冷藏和冷冻的医疗器械,医疗器械经营企业应具备相应的冷链设备,并能保持合适的温度要求。
二、人员要求1. 企业负责人:医疗器械经营企业的负责人应具备相关的医疗器械经营管理知识和经验,并能够有效组织和管理企业的日常运营。
2. 质量管理人员:医疗器械经营企业应聘请具备相关背景的质量管理人员,负责监督并保证医疗器械的质量和安全性。
3. 库房管理员:医疗器械经营企业的库房管理员应具备一定的仓库管理经验,能够做好医疗器械的分类、摆放和出库入库管理工作。
三、管理规范1. 进货验收:医疗器械经营企业在进货时,应严格按照供应商提供的合格证明和检测报告进行验收,并与实际产品进行对照检查,确保所进货物与合同一致,并能够正常使用。
2. 清单台账:医疗器械经营企业应建立完善的器械清单和库存台账,每一个进货的医疗器械都应有相应的记录,方便随时查阅和盘点。
3. 库存管理:医疗器械经营企业应严格按照医疗器械的特性和规定,对各类器械进行分类存放,避免交叉污染和混乱管理。
4. 质量追溯:医疗器械经营企业应建立完善的质量追溯系统,对进货、销售和退货等环节进行严密监管,保证医疗器械的质量和来源可追溯。
5. 售后服务:医疗器械经营企业应设立健全的售后服务体系,及时响应用户的需求和投诉,并保证及时提供维修和退货服务。
四、环境要求1. 清洁卫生:医疗器械经营企业的办公室、仓库和操作区域等应保持清洁整洁,定期进行清洁消毒。
医疗器械经营企业现场核查验收细则

医疗器械经营企业现场核查验收细则一、引言医疗器械的质量和安全性直接关系到公众的健康和生命安全。
为了加强对医疗器械经营企业的监督管理,规范医疗器械市场秩序,保障医疗器械的质量和安全,特制定本现场核查验收细则。
二、适用范围本细则适用于医疗器械经营企业的开办、变更、延续等现场核查验收工作。
三、核查验收依据1、《医疗器械监督管理条例》2、《医疗器械经营监督管理办法》3、《医疗器械经营质量管理规范》4、其他相关法律法规和规范性文件四、人员与机构1、企业法定代表人、负责人、质量管理人员应当熟悉医疗器械监督管理的法律法规、规章规范和所经营医疗器械的相关知识,并经过培训考核合格。
2、企业应当配备与经营规模和经营范围相适应的质量管理人员,质量管理人员应当在职在岗,不得兼职。
3、从事体外诊断试剂的质量管理人员中,应当有 1 人为主管检验师,或具有检验学相关专业大学以上学历并从事检验相关工作 3 年以上工作经历。
4、企业应当设置质量管理机构或者配备质量管理人员,行使质量管理职能,在企业内部对医疗器械的质量具有裁决权。
五、经营场所与设施设备1、企业应当具有与经营范围和经营规模相适应的经营场所和库房,经营场所和库房的面积应当满足经营要求。
2、经营场所应当整洁、卫生,具有与经营的医疗器械相适应的办公设施设备。
3、库房应当符合医疗器械储存的要求,具有避光、通风、防潮、防虫、防鼠等设施设备,以及温湿度监测、调控设备。
4、经营对温湿度有特殊要求的医疗器械,应当配备符合其储存要求的设施设备。
5、经营冷藏、冷冻医疗器械的,应当配备与其经营规模和品种相适应的冷库、冷藏车、冷藏箱、保温箱等设施设备,并具有温度监测、显示、记录、调控、报警的功能。
六、质量管理文件1、企业应当建立覆盖医疗器械经营全过程的质量管理制度,包括采购、验收、贮存、销售、运输、售后服务等环节。
2、企业应当制定相应的工作程序和操作规程,确保各项质量管理制度的有效实施。
3、企业应当建立医疗器械质量管理档案,包括供货者资质、产品资质、采购验收记录、销售记录、不合格品处理记录等。
2023年医疗器械经营企业现场检查标准

3. 合同变更与解决方案:审查企业是否在需要变更合同条款时,严格按照合同约定的程序进行变更,并评估企业是否有效解决了由于合同履行中的争议或问题而引起的纠纷。
4. 合同记录和归档:检查企业是否建立了符合法规要求的合同记录和归档制度,确保合同文件完整、有效,并便于监管人员查阅。
2. 人员配备和管理:检查企业是否按照相关法律法规要求,配备了专业的医疗器械经营管理人员,包括从业人员的资质、背景和经验等,并核查其是否经过规范的培训和持续教育。
3. 内部交流和协作机制:检查企业是否建立了清晰有效的内部交流和协作机制,保障各部门之间的信息共享、工作协调和问题处理等。
4. 职责分工明确:检查企业是否明确各部门和人员的职责,确保相关工作的落实情况,并核查企业是否建立了相应的责任追究制度。
资质认证文件
1. 资质证书:检查企业是否具备相关资质证书,并核实证书的有效期和适用范围。
2. 产品注册证明:确认企业所经营的医疗器械是否具备必要的产品注册证明,并核实证明文件的真实性和合规性。
3. 许可证/许可证明:核查企业是否拥有必要的经营许可证或许可证明,以确保企业经营医疗器械的合法性和合规性。
培训计划
完整性
产品知识
法律法规
培训方式
培训对象
培训实施
销售技巧
培训周期
培训计划与实施
04
采购销售合同及备案情况
Procurement and sales contracts and filing status
1. 合同签订情况:检查企业是否与供应商、客户签订了合同,并评估合同的合法性和合规性。要确保合同明确了双方的权责,并具备明确的产品规格、数量、价格、交付期限等条款。
医疗器械经营企业现场核查验收细则

医疗器械经营企业现场核查验收细则医疗器械经营企业现场核查验收细则一、引言医疗器械经营企业现场核查验收是对经营企业进行全面检查和评估,以验证其是否符合相关法律法规和规范要求。
本旨在提供一份详尽的细则,以供参考使用。
二、企业基本信息核查1. 企业名称和注册地址核查1.1 核实企业名称是否与注册信息一致1.2 核查企业注册地址是否合法有效2. 经营许可证核查2.1 核实许可证的有效性和经营范围2.2 核查许可证上的企业名称是否一致2.3 核查许可证是否有变更3. 企业组织结构核查3.1 核实企业组织结构是否规范合理3.2 核查组织架构图和职责分工是否清晰三、设备及场所核查1. 设备齐全性核查1.1 核查仪器设备清单与实际设备是否一致1.2 核查仪器设备是否符合国家标准和相关要求1.3 核查设备是否经过定期检修和校准2. 环境和场所核查2.1 核查经营场所是否与许可证上的地址一致2.2 核查经营场所是否符合卫生要求和消防安全标准 2.3 核查经营场所是否保持整洁有序2.4 核查场所内是否有一定的保密措施和安全管理制度四、库存管理核查1. 药品和器械库存核查1.1 核查库存清单与实际库存是否一致1.2 核查库存药品和器械的有效期是否符合规定1.3 核查库存药品和器械的存储条件是否符合要求2. 库存管理制度核查2.1 核查库存管理制度的完整性和合规性2.2 核查库存盘点和报损处理制度的执行情况五、质量管理核查1. 质量管理体系核查1.1 核查质量管理体系是否建立和有效1.2 核查质量管理文件的编制和执行情况2. 整改和预防措施核查2.1 核查质量事故和投诉处理程序是否规范2.2 核查质量问题的整改和预防措施是否跟进落实2.3 核查员工的质量意识和培训情况六、人员资质核查1. 人员持证情况核查1.1 核查员工的从业资格证书是否齐全1.2 核查员工的资格证书有效期是否符合要求1.3 核查员工的岗位与资质是否相符2. 培训和教育情况核查2.1 核查员工培训情况的记录和档案2.2 核查员工是否定期参加相关培训和教育七、附件清单本所涉及附件如下:1. 企业营业执照副本复印件2. 经营许可证复印件3. 设备清单及设备维护记录4. 员工持证情况表八、法律名词及注释本所涉及的法律名词及其注释如下:1. 经营许可证:指医疗器械经营企业获得的经营许可证书,用于合法经营医疗器械产品。
医疗器械经营企业现场检查整改报告

医疗器械经营企业现场检查整改报告尊敬的各位领导:首先,非常感谢监管部门对我们医疗器械经营企业进行的现场检查,这对于我们提升经营管理水平、保障公众健康安全具有重要意义。
在此次检查中,我们也认识到了企业存在的一些问题和不足之处,现将整改情况向各位领导汇报如下:一、问题概述在现场检查中,我们主要被指出存在以下几个方面的问题:1、医疗器械陈列摆放不规范,部分产品未按照分类要求放置。
2、部分员工对医疗器械相关法律法规和专业知识掌握不够熟练。
3、进货验收记录存在信息不全的情况。
4、仓库温湿度控制措施不够完善。
二、整改措施及落实情况1、针对医疗器械陈列摆放不规范的问题,我们立即组织员工对仓库和销售区域进行了全面整理。
按照医疗器械的类别、用途、规格等进行了细致的分类,并制定了明确的陈列标准和标识。
同时,加强了日常的巡检,确保陈列始终保持规范整齐。
就拿我们整改仓库陈列这件事来说,那可真是费了一番功夫。
仓库里的各种医疗器械琳琅满目,一开始大家都有些无从下手。
但是,为了能够彻底整改到位,我们专门成立了一个小组,大家一起研究分类标准,还互相比赛看谁整理得又快又好。
经过几天的努力,仓库终于变得井井有条,每一种医疗器械都找到了自己的“专属位置”。
2、为了提高员工对法律法规和专业知识的掌握程度,我们组织了多次内部培训。
邀请了行业专家和法律人士进行授课,通过案例分析、互动问答等形式,让员工们更加深入地理解相关知识。
培训结束后,还进行了严格的考核,确保每一位员工都能够达到要求。
在培训过程中,有一位员工小王,之前对法律法规总是一知半解。
但是通过这次培训,他像是突然开了窍,不仅认真听讲做笔记,还主动向专家请教问题。
在最后的考核中,他取得了优异的成绩,现在已经成为了我们团队中的“法规小达人”。
3、对于进货验收记录信息不全的情况,我们重新梳理了进货流程,明确了每一个环节需要记录的信息,并制定了详细的表格。
要求验收人员严格按照规定填写,同时加强了审核环节,确保记录的完整性和准确性。
医疗器械经营企业现场核查验收细则

附件1:医疗器械经营企业现场检查验收细则一、医疗器械经营企业现场检查验收细则一(二、三类医疗器械经营企业)二、医疗器械经营企业现场检查验收细则二(角膜接触镜及护理用液专营企业)三、医疗器械经营企业现场检查验收细则三(助听器、家用理疗康复仪器等单一第二类医疗器械专营企业)四、医疗器械经营企业现场检查验收细则四(药物零售兼营医疗器械企业)医疗器械经营企业现场检查验收细则编制阐明一、合用范围本检查验收细则由医疗器械经营企业检查验收细则一(二、三类医疗器械经营企业)、医疗器械经营企业检查验收细则二(角膜接触镜及护理用液专营企业)、医疗器械经营企业检查验收细则三(助听器、家用理疗康复仪器等单一第二类医疗器械专营企业)、医疗器械经营企业检查验收细则四(药物零售兼营医疗器械企业)共四部分构成,分别合用于上述四类企业旳开办、许可事项变更、换证检查和平常监管。
二、评估措施(一)本检查验收细则设置有重点项目(条款前加注“*”)和一般项目。
现场检查时,应对所列重点项目和一般项目进行全面检查,并逐项做出符合规定或者不符合规定旳评估。
凡不完整、不齐全、不符合规定旳项目为缺陷项目。
重点项目不符合规定为严重缺陷,一般项目不符合规定为一般缺陷。
(二)现场检查时,检查人员应针对新开办、许可事项变更、换证和平常监管等不同样状况确定对应旳检查项目。
1、二、三类医疗器械经营企业新开办检查项目为机构与人员、经营场所和储存条件、质量管理制度。
变更许可事项(不含增长经营范围)检查项目为对应变更内容旳规定条款。
换证和增长经营范围检查项目为检查验收细则旳所有条款。
2、角膜接触镜及护理用液专营企业、助听器、家用理疗康复仪器等单一第二类医疗器械专营企业和药物零售兼营医疗器械企业新开办、换证、增长经营范围检查项目为检查验收细则旳所有条款。
变更许可事项(不含增长经营范围)检查项目为对应变更内容旳规定条款。
(三)合理缺项:由于企业经营范围限定或经营管理旳实际状况,使企业实际未开展或未波及有关经营管理工作内容所对应旳检查验收细则中不需要进行现场检查旳项目为合理缺项。
浙江省食品药品监督管理局关于印发浙江省医疗器械经营质量管理规范实施细则的通知

浙江省食品药品监督管理局关于印发浙江省医疗器械经营质量管理规范实施细则的通知文章属性•【制定机关】浙江省食品药品监督管理局•【公布日期】2018.01.12•【字号】浙食药监规〔2018〕1号•【施行日期】2018.03.01•【效力等级】地方规范性文件•【时效性】现行有效•【主题分类】质量管理和监督正文浙江省食品药品监督管理局关于印发浙江省医疗器械经营质量管理规范实施细则的通知浙食药监规〔2018〕1号各市市场监督管理局(食品药品监督管理局):为加强医疗器械经营监管,规范医疗器械经营行为,提升服务水平,保障安全、有效,促进产业发展,根据《医疗器械监督管理条例》《医疗器械经营监督管理办法》(国家食品药品监督管理总局第8号令)、国家食品药品监督管理总局《关于施行医疗器械经营质量管理规范的公告》(2014年第58号公告)和《关于印发医疗器械经营质量管理规范现场检查指导原则的通知》(食药监械监〔2015〕239号)以及省食品药品监督管理局《关于实施〈医疗器械经营质量管理规范〉有关事项的通知》(浙食药监规〔2015〕26号)精神,省局制定了《浙江省医疗器械经营质量管理规范实施细则》(以下简称《实施细则》),现印发给你们,并就有关事项通知如下:一、医疗器械经营方式分批发、零售、零售连锁三种。
各市市场监管局(食品药品监管局)对第三类医疗器械批发、零售、零售连锁经营企业,依法实施许可;对第二类医疗器械批发、零售、零售连锁经营企业,依法给予备案。
医疗器械零售连锁企业,是指经营同类医疗器械、使用统一商号,在同一总部的管理下,采取统一采购配送、统一质量标准、采购与销售分离、实行规模化经营的组织形式。
零售连锁企业总部按批发经营企业管理,零售连锁企业门店按零售经营企业管理。
二、《实施细则》对第二类、第三类医疗器械批发、零售经营企业,第一类医疗器械经营者,以及医疗器械零售连锁企业实施《医疗器械经营质量管理规范》的要求进行细化。
浙江省医疗器械经营企业检查验收标准

浙江省医疗器械经营企业检查验收标准第一条根据《医疗器械经营企业许可证管理办法》的有关规定,制定本标准。
第二条本标准适用于医疗器械经营企业的开办审查、变更许可事项审查、换发许可证审查和日常监督检查。
第三条企业负责人应具有中专以上学历或初级以上职称。
了解国家及地方有关医疗器械监督管理的法规、规章。
第四条企业应根据经营规模和经营范围设立医疗器械质量管理机构或落实专职的医疗器械质量管理人员。
第五条质量管理机构负责人或专职质量管理人员应具有国家认可的医疗器械相关专业学历或职称,熟悉国家及地方有关医疗器械监督管理法规、规章、规定和所经营产品的技术标准。
仅经营二类产品的,质量管理机构负责人或专职质量管理人员应具有与申请经营产品相关专业中专以上学历或初级以上职称;经营三类产品的,质量管理机构负责人或专职质量管理人员应具有与申请经营产品相关专业大专以上学历或中级以上职称。
第六条经营植入(介入)类医疗器械的,还应至少配备1名具有大专以上学历或中级以上职称的专业卫生技术人员。
第七条经营有特殊验配要求的医疗器械的,还应至少配备相关专业的中专以上学历或初级以上职称的卫生技术人员和专业验配人员各1名。
第八条企业负责人、质量管理机构负责人或专职质量管理人员、专业卫生技术人员、验配人员应在职在岗,不得相互兼任,也不得在其他医疗器械生产、经营单位兼职兼岗。
第九条医疗器械兼营企业应设立相对独立的组织机构;有专门指定的部门负责人。
第十条企业应有技术培训和售后服务人员。
承担技术培训和售后服务的人员一般应具有中专以上学历或初级以上职称,并经有关部门或生产商、销售商、代理机构组织的培训取得相关证明。
如由供应商提供培训及售后服务的,应具有与供应商签订明确责任的协议书。
第十一条企业应落实仓库保管人员。
仓库保管人员应了解所经营产品的储存条件要求,熟悉产品的有关标识及储存设备、设施的使用。
第十二条企业销售人员应了解其销售的医疗器械产品的主要性能、适应范围、禁忌症等基本情况。
医疗器械经营企业现场核查标准及记录范文.docx

附件十医疗器械经营企业现场核查标准和记录被核查企业名称:现场核查时间:年月日□首次□再次检查结果条款检查内容与要求检查方法备注符合不符合1、企业管理人员(法定代表人、负责人、质量管理人、仓储负责人)可通过考试或现场答卷等方式熟悉国家医疗器械监督管理的法考查。
企业应有三人以上参加,规、规章,以及我省对医疗器械的成绩均应达到 70%分以上管理规定。
2、设置质量管理机构或专职质量管查组织机构图、机构设置文件、理人员,职能包括质量管理、质量人员与职能的规定验证等。
13、质量管理人专职在岗,具有与经营范围和规模相适应的资质:机a) 经营第三类医疗器械的,应具有构国家认可的、与经营产品相关专业与(医疗器械、生物医学工程、机械、人电子)大专以上学历或相关专业中员级以上技术职称;经营一次性使用无菌器械的,还应查花名册、任用文件、劳动合同、身份证、学历、(或职称、否决项有一名以上内审员。
b) 经营第二类医疗器械的,应具有内审员、专业技术培训)证书原件、询问个人简历国家认可的、与经营产品相关专业(医疗器械、生物医学工程、机械、电子)中专以上学历或相关专业初级以上技术职称。
c)经营助听器或者隐形眼镜及护理用液的,应经国家认可的第三方机构或所授权经营的生产企业(包括进口总代理商)验配技术培训。
检查结果条款检查内容与要求检查方法备注符合不符合4、设置与经营范围和规模相适应的查组织机构图、机构设置文件、组织机构。
明确各组织机构的职能。
人员与职能的规定5、具有与经营规模及经营产品相适查制度的相关规定、售后服务应的技术培训和售后服务能力,或记录,查所具有的技术培训和约定由具有相关合法资质的第三方售后服务能力的证明文件或与1提供技术支持。
提供技术支持的、具有相关合否决项机法资质的第三方签订的协议等构文件原件与6、经营第二类、第三类医疗器械的,人技术培训和售后服务人员应当具有员与所经营产品相关专业中专以上学查组织机构图、机构设置文件、历或初级以上职称。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
“We involve you.”
• We hold several one hour classroom reviews of basic machining process theory and the relationships between filtration, cutting fluid chemistry, biology, and metallurgy.
“All FIVE disciplines are related and mutually influential”
$ $
$$ $ $
$ Tools
Metallurgy
$
$ Coolants
$
Filtration $
$
Machine
$
$$ $$
$
$
$
The Costs of Manufacturing
• We stay focused and are driven to reduce your cost of manufacturing.
Sequence of events for a plant wide* process improvement program. Overview
Identify top 15 to 20 high cost tools or high volume tools General audience classroom training Identify tool and coolant system issues Investigate issues and root causes Present findings, reports and recommendations Incorporate improvements into standard operating procedures Follow up key issues and findings
or wheel material choice 7. Improper resharpening or
redressing 8. Misdirected coolant flow 9. Pump sucking air 10. Restricted coolant flow
11. Foam 12. Contamination by hydraulic
*A plant wide program has the greatest impact on costs and involves the greatest number of individuals who can affect the processes.
Following are some slides taken from the presentations.
P. Chip nests (stringy chips)
H. Poor tool life/wheel life
(These 20 influential components are investigated.)
1. Concentration control 2. Microorganisms/fungus 3. Biocide levels 4. Wrong product choice 5. Improper speeds and feeds 6. Wrong tool material choice
2. Improve the surface finish during the machining processes. A. More accurate form generation. B. Attain tighter tolerances. C. Better subsequent processes. (Better coating, assembly, etc.) D. Less residual compressive stresses in parts.
浙江省医疗器械经营企业现场检查评 ..
Machining Efficiencies, Inc. is dedicated to improving the manufacturing performance of machining and grinding operations.
We focus on improving our clients profitability by identifying specific corrective action that will reduce the process costs.
Failure Modes of inserts
1. Built Up Edge phenomenon 2. Chipping Wear 3. Flaking 4. Spalling 5. Fracture 6. Flank / Nose / Face Wear 7. Notching Wear 8. Thermal Cracking (Shock) (Fatigue) 9. Crater Wear (Diffusion Wear) 10. Deformation Wear 11. Cobalt Leaching
• Causes – Excessive loads on tool – Built Up Edge (BUE) – Intermittent contact with hard inclusions – Machine or part fixture vibration – Lack of rigidity of tool holder setup – Improper selection of insert geometry / substrate / coating – Re-circulated fines / micro particles in coolant – If coated, coating may be too thick
Chipping Wear Identification & Causes
• Identification – Ragged edge on insert – Poor (streaked) surface finish on parts – Irregular wear – Leads to catastrophic tool failure (masked cause)
fluids, way oils 13. Contamination by floor
cleaners or machine cleaners 14. Incorrect tool design/wheel application 15. Incorrect metallurgy of parts 16. Part fixturing 17. Part gauging 18. Prior part processing 19. Filter malfunction 20. Machine/spindle vibration
All of the failure modes are documented with microphotographs for future reference. There are four more failure modes associated with broaching, hobbing and other similar processes. They are not included in consideration of the document file size.
Chipping Wear Cure
• Cure – Aim coolant properly – Reduce Tramp Oil content in coolant – Use coolant with Extreme Pressure (EP) additives – Make sure the machine or fixture does not vibrate – Balance spindle – Strengthen tool holder – Select insert with high cobalt content – Decrease feed rate – De-scale surface of part – Improve filtration – positive barrier – Change coating (if used) or eliminate
Machine a better chip…….. It is the core of your business
1. Reduce the cost of manufacturing A. With greater tool life. (Lower tooling costs) B. With less tool change set ups. (Less downtime)
Identify ALL the Problem(s) with your central system
(“Poor tool life or wheel life are used as examples here.”)
A. Odor B. Rust and Stain C. Loss of filter efficiency D. Poor emulsification E. Residual films F. Dermatitis G. Foaming H. Poor tool life or wheel life I. Poor microfinish J. Poor part size control K. Paint removal L. Smoke or excessive misting M. Clinkering of chips or swarf N. Fungus O. Seals or V Belts
