临床试验用药品温湿度记录表-丽水中心医院
研究实验室温湿度记录表
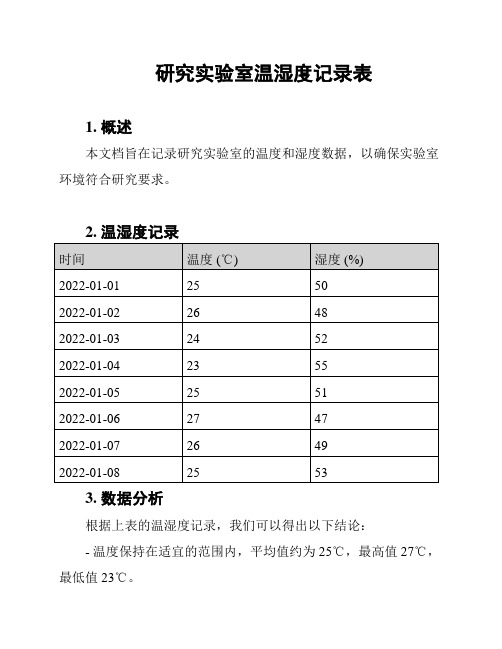
研究实验室温湿度记录表
1. 概述
本文档旨在记录研究实验室的温度和湿度数据,以确保实验室环境符合研究要求。
3. 数据分析
根据上表的温湿度记录,我们可以得出以下结论:
- 温度保持在适宜的范围内,平均值约为25℃,最高值27℃,最低值23℃。
- 湿度保持在适宜的范围内,平均值约为50%,最高值55%,最低值47%。
4. 结论
本研究实验室的温湿度记录表显示,实验室的温湿度符合研究要求,并维持在适宜的范围内。
这有助于保证实验室内的实验质量和研究结果的准确性。
5. 建议
在继续进行实验室研究时,建议继续监测和记录温湿度数据,并确保实验室内的温湿度继续保持在适宜的范围内。
以上是本次研究实验室温湿度记录表的内容。
如有需要,可随时查阅。
药品温湿度记录表范本-概述说明以及解释

药品温湿度记录表范本-范文模板及概述示例1:药品温湿度记录表范本是一种记录药品存储环境信息的工具,常用于药品仓库、医院、药店等地方。
下面是一个药品温湿度记录表范例,您可以根据实际需求进行修改和补充:药品名称:__________________ 药品批号:________________记录日期:__________________ 负责人:__________________温度()湿度()________________ ________________________________ ________________________________ ________________________________ ________________________________ ________________备注:________________________________________________________使用说明:1. 每天记录药品存储环境的温度和湿度。
2. 根据数据记录情况,在相应日期下填写温度和湿度数据。
3. 如有异常情况,请在备注栏中详细说明原因,并采取相应的措施保证药品质量安全。
4. 如需添加更多日期记录,请在空白处补充。
注意事项:1. 温湿度数据应准确记录,可使用温湿度记录仪等设备来测量。
2. 药品存储环境应符合规定的温湿度范围,确保药品质量不受影响。
3. 定期检查药品存储环境设备的工作状态,确保其正常运行。
4. 如有异常情况或设备故障,应及时报告上级或负责人,并采取措施进行修复或更换。
以上是一个药品温湿度记录表的范本,您可以根据实际情况进行调整和修改。
记录药品存储环境的温湿度数据可以帮助监测和控制药品质量,保证药品的有效性和安全性。
示例2:药品温湿度记录表范本药品温湿度记录表是一种重要的记录文档,用于监测药品在储存和运输过程中的温度和湿度情况。
这些信息对于确保药品的安全性和有效性至关重要。
临床试验药物温湿度记录表
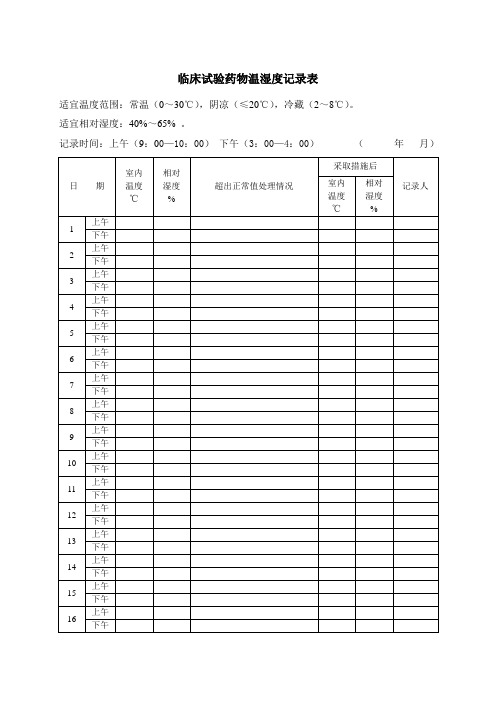
适宜温度范围:常温(0~30℃),阴凉(≤20℃),冷藏(2~8℃)。
适宜相对湿度:40%~65%。
记录时间:上午(9:00—10:00) 下午(3:00—4:00)(年月)
日 期
室内
温度
℃
相对
湿度
%
超出正常值处理情况
采取措施后
记录人
室内
温度
℃
相对
湿度
%
1
上午
下午
2
上午
下午
3
日 期
室内
温度
℃
相对
湿度
%
超出正常值处理情况
采取措施后
记录人
室内
温度
℃
相对
湿度
%
17
上午
下午
18
上午
下午
19
上午
下午
20
上午
下午
21
上午
下午
22
上午
下午
23
上午
下午
24
上午
下午
25
上午
下午
26
上午
下午
27
上午
下午
28
上午
下午
29
上午
下午
30
上午
下午
31
上午
下午
上午
下午
4
上午
下午
5
上午
下午
6
上午
下午
7
上午
下午
8
上午
下午
9
上午
下午
10
上午
下午
11
上午
下午
12
温湿度计内校记录表
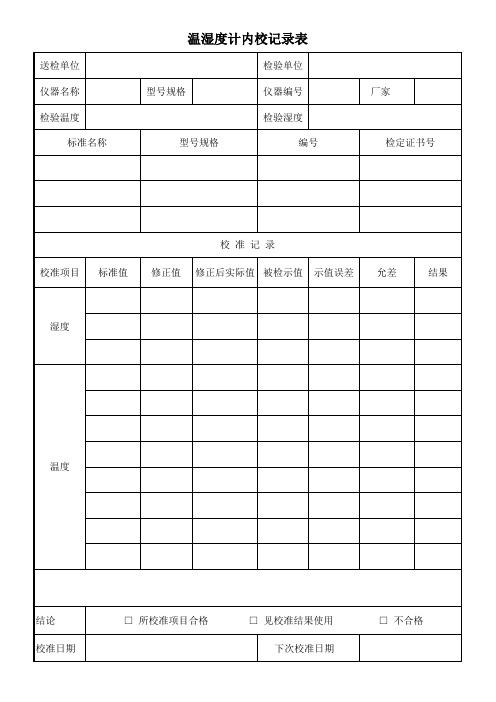
送检单位 仪器名称 检验温度
标准名称
温湿度计内校记录表
检验单位
型号规格
仪器编号
检验湿度
型号规格
编号
厂家 检定证书号
校准项目 标准值
校准记录 修正值 修正后实际值 被检示值 示值误差
允差
结果
湿度
温度
Hale Waihona Puke 结论 校准日期□ 所校准项目合格
□ 见校准结果使用 下次校准日期
□ 不合格
校准员:
核准:
药品温湿度记录表范本

药品温湿度记录表范本全文共四篇示例,供读者参考第一篇示例:药品的储存温湿度是非常重要的,它会直接影响药品的质量和有效性。
药品在储存过程中需要遵循一定的温湿度要求,避免受到不良环境影响。
为了记录药品的温湿度情况,以便监控和管理药品质量,制作一份药品温湿度记录表非常必要。
一、表格标题药品温湿度记录表二、表格内容1. 表格列名- 药品名称- 药品批号- 存储地点- 存储温度(℃)- 存储湿度(%)- 记录时间- 填表人员2. 表格填写要求在填写药品温湿度记录表时,需要根据实际情况填写相关信息,确保记录准确可靠。
每次记录包括药品名称、药品批号、存储地点、存储温度、存储湿度、记录时间和填表人员。
3. 表格使用方法填写药品温湿度记录表时,需要注意以下几点:- 按照规定的时间间隔记录药品的温湿度情况,如每天、每周或每月记录一次;- 在填写表格时务必填写准确的信息,包括药品名称、批号、存储地点、温湿度等;- 若发现药品存储温湿度不在规定范围内,需及时报告相关部门处理,避免影响药品质量。
4. 表格样例```| 药品名称| 药品批号| 存储地点| 存储温度(℃)| 存储湿度(%)| 记录时间| 填表人员||--------------|------------|--------------|--------------|--------------|--------------|-------------|| 阿莫西林| 20210101 | 医院药房| 25 | 60 | 2022-01-01 | 张三|| 氯化钾| 20210201 | 药品库| 20 | 50 | 2022-01-05 | 李四|| 维生素C | 20210301 | 家庭药柜| 30| 70 | 2022-01-10 | 王五|```以上是药品温湿度记录表的样例,填写规范、准确地记录药品的温湿度情况,有助于保障药品的质量和有效性。
在实际使用中,可根据需要对表格进行调整,适应实际情况的记录需求。
2020年药房温湿度记录表(精选干货)
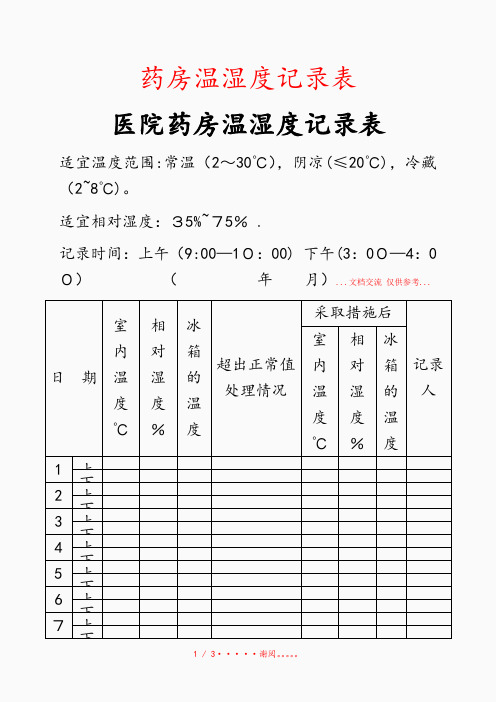
药房温湿度记录表医院药房温湿度记录表适宜温度范围:常温(2~30℃),阴凉(≤20℃),冷藏(2~8℃)。
适宜相对湿度:35%~75% .记录时间:上午(9:00—10:00) 下午(3:00—4:00)(年月)...文档交流仅供参考...日期室内温度℃相对湿度%冰箱的温度超出正常值处理情况采取措施后记录人室内温度℃相对湿度%冰箱的温度1上下2上下3上下4上下5上下6上下7上下下9上下10上下11上下12上下1上下1上下1上下1上下医院药房温湿度记录表适宜温度范围:常温(2~30℃),阴凉(≤20℃),冷藏(2~8℃)。
适宜相对湿度:35%~75%。
记录时间:上午(9:00—10:00)下午(3:00—4:00) ( 年月)...文档交流仅供参考...日期室内温度℃相对湿度%冰箱的温度超出正常值处理情况采取措施后记录人室内温度℃相对湿度%冰箱的温度下 18 上下 1上下 2上下 2上下 2上下 2上下 2上下 2上下 26 上下 2上下 2上下 29 上下 30 上下 31 上下下。
温湿度确认记录表(完善版)
AITH UCKY
设备名称: 日期 上午 实测 下午 湿度 加班 上午 实测 下午 温度 加班 1 2 3 4 使用部门: 5 6 7 8 9
温湿度确认记录表
设备编号: 仪器负责人: 年/月:
10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30
备注
确认签名 说明: 1.请将每日确认的结果填写在表格中,若发现异常应在“备注”进行记录并跟进 2.为确保测试中心设备处于良好测试状态,并能提供准确测试结果,测试中心室内温度控制在:23℃± 5℃以内,湿度控制在:25%-75%以内。 3.当室内温、湿度超过规定值时,应立即采取对应的加温、降温措施进行调节。 4.记录时间:1-4月份、11-12月份的填写时间是上午8:00,下午16:00,加班20:00; 5-10月份的填写时间是11:00,14:30,加班18:30。 5.温湿度计应放置于远离室内冷热源位置,以确保能得到更精确的数据。
药房温湿度记录表模版

药房温湿度记录表模版医院药房温湿度记录表以下是排调中心卫生院药房的温湿度记录表。
适宜的温度范围为常温(~30℃)、阴凉(≤20℃)和冷藏(2~8℃),适宜的相对湿度为40%~65%。
记录时间为上午(9:00—10:00)和下午(3:00—4:00),记录的年月为每个月。
室内温度和相对湿度记录在表格中。
如果温度或湿度超出正常值,采取措施并在“超出正常值处理情况”栏中记录。
记录人和日期也在表格中列出。
请注意,下面的表格有17到31号的记录,这些记录不在原始表格中。
室内温度和相对湿度记录表:室内温度(℃)和相对湿度(%)记录在以下表格中:日期|上午温度|上午湿度|下午温度|下午湿度|采取措施后|超出正常值处理情况|1|℃| |℃| | | |2|℃| |℃| | | |3|℃| |℃| | | |4|℃| |℃| | | |5|℃| |℃| | | |6|℃| |℃| | | |7|℃| |℃| | | |8|℃| |℃| | | |9|℃| |℃| | | |10|℃| |℃| | | |11|℃| |℃| | | |12|℃| |℃| | | |13|℃| |℃| | | |14|℃| |℃| | | |15|℃| |℃| | | |16|℃| |℃| | | |17|℃| |℃| | | |18|℃| |℃| | | | 19|℃| |℃| | | | 20|℃| |℃| | | | 21|℃| |℃| | | | 22|℃| |℃| | | | 23|℃| |℃| | | | 24|℃| |℃| | | | 25|℃| |℃| | | | 26|℃| |℃| | | | 27|℃| |℃| | | | 28|℃| |℃| | | | 29|℃| |℃| | | | 30|℃| |℃| | | | 31|℃| |℃| | | |。
药房温湿度记录表【可编辑范本】

上午
下午
3
上午
下午
4
上午
下午
5
上午
下午
6
上午
下午
7
上午
下午
8
上午
下午
9
上午
下午
10
上午
下午
11
上午
下午
12
上午
下午
13
上午
下午
14
上午
下午
15
上午
下午
16
上午
下午
医院药房温湿度记录表
适宜温度范围:常温(2~30℃),阴凉(≤20℃),冷藏(2~8℃)。
适宜相对湿度:35%~75%。
记录时间:上午(9:00-10:00) 下午(3:00—4:00)(年月)
医院药房温湿度记录表
适宜温度范围:常温(2~30℃),阴凉(≤20℃),冷藏(2~8℃)。
适宜相对湿度:35%~75%。
记录时间:上午(9:00-10:00) 下午(3:00—4:00)(年月)
日期
室内
温度
℃
相对
湿度
%
冰箱的温度
超出正常值处理情况
采取措施后
记录人
室内
温度
℃
相对
湿度
%
冰箱的温度
1
上午
下午
日期
室内
温度
℃正常值处理情况
采取措施后
记录人
室内
温度
℃
相对
湿度
%
冰箱的温度
17
上午
下午
18
上午
下午
19
上午
下午
20
上午
下午
药房温湿度记录表 (完整版)
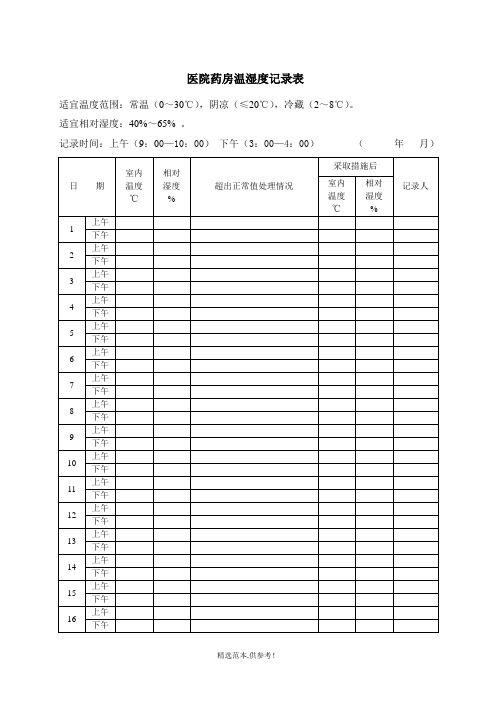
记录时间:上午(9:00—10:00) 下午(3:00—4:00)(年月)
日 期
室内
温度
℃
相对
湿度
%
超出正常值处理情况
采取措施后
记录人
室内
温度
℃
相对
湿度
%
1
上午
下午
2
上午
下午
3
上午
下午
4
上午
下午
5
上午
下午
6
上午
下午
7
上午
下午
8
上午
下午
9
上午
下午
10
上午
下午
11
上午
下午
12
采取措施后
记录人
室内
温度
℃
相对
湿度
%
17
上午
下午
18
上午
下午
19
上午
下午
20
上午
下午
21
上午
下午
22
上午
下午
23
上午
下午
24
上午
下午
25
上午
下午
26
上午
下午
27
上午
下午
28
上午
下午
29
上午
下午
30
上午
下午
31
上午
下午
【本文档内容可以自由复制内容或自由编辑修改内容期待你的好评和关注,我们将会做得更好】
上午
下午
13
上午
下午
14
上午
下午
15
上午
药店温湿度记录表[1](干货分享)
](https://img.taocdn.com/s3/m/c965f0adf242336c1fb95e29.png)
药店温湿度记录表
温湿度记录表
(年月)
适宜温度范围: ~ ℃适宜相对湿度范
围:~%
填表说明
1、本表是对库房或营业场所温湿度条件进行监测、调控的工作记录。
2、本表应根据制度及职责规定由指定人员负责.
3、表中“适宜温湿度范围”应根据所储存、陈列的药品储存条件要求
设定。
4、本表应逐日按时记录不得空缺。
5、每日上下午应固定时间进行观察记录。
上午9:00-9:30,下午4:
00-4:30。
、
6、当温湿度条件超出或接近临界点时,应由养护员及保管员采取有效
调控措施。
如温度超出正常范围时开空调升温或降温,湿度超出正常范围时开空调除湿,或拖地加湿。
7、如果超出正常范围,一般在采取措施后1小时,应再进行观察、记
录。
8、所采取的调控措施,应能将温湿度条件有效控制在规定范围内.规定
范围:常温库(营业大厅)为0~30℃,冷库(冷藏箱)为2~10℃。
9、上班时即开空调的在上、下午记录温湿度时,在正常范围内只填写调
控措施和调控后温湿度。
药房温湿度记录表
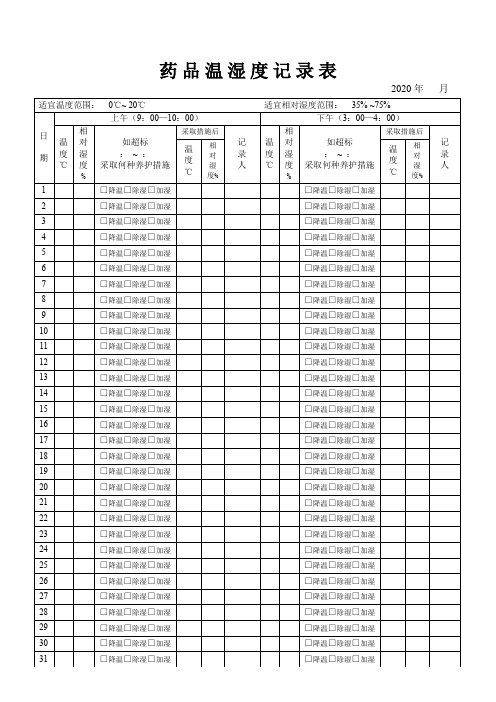
药品温湿度记录表2020年月适宜温度范围:0℃~ 20℃适宜相对湿度范围:35% ~75%日期上午(9:00—10:00)下午(3:00—4:00)温度℃相对湿度%如超标:~ :采取何种养护措施采取措施后记录人温度℃相对湿度%如超标:~ :采取何种养护措施采取措施后记录人温度℃相对湿度%温度℃相对湿度%1 □降温□除湿□加湿□降温□除湿□加湿2 □降温□除湿□加湿□降温□除湿□加湿3 □降温□除湿□加湿□降温□除湿□加湿4 □降温□除湿□加湿□降温□除湿□加湿5 □降温□除湿□加湿□降温□除湿□加湿6 □降温□除湿□加湿□降温□除湿□加湿7 □降温□除湿□加湿□降温□除湿□加湿8 □降温□除湿□加湿□降温□除湿□加湿9 □降温□除湿□加湿□降温□除湿□加湿10 □降温□除湿□加湿□降温□除湿□加湿11 □降温□除湿□加湿□降温□除湿□加湿12 □降温□除湿□加湿□降温□除湿□加湿13 □降温□除湿□加湿□降温□除湿□加湿14 □降温□除湿□加湿□降温□除湿□加湿15 □降温□除湿□加湿□降温□除湿□加湿16 □降温□除湿□加湿□降温□除湿□加湿17 □降温□除湿□加湿□降温□除湿□加湿18 □降温□除湿□加湿□降温□除湿□加湿19 □降温□除湿□加湿□降温□除湿□加湿20 □降温□除湿□加湿□降温□除湿□加湿21 □降温□除湿□加湿□降温□除湿□加湿22 □降温□除湿□加湿□降温□除湿□加湿23 □降温□除湿□加湿□降温□除湿□加湿24 □降温□除湿□加湿□降温□除湿□加湿25 □降温□除湿□加湿□降温□除湿□加湿26 □降温□除湿□加湿□降温□除湿□加湿27 □降温□除湿□加湿□降温□除湿□加湿28 □降温□除湿□加湿□降温□除湿□加湿29 □降温□除湿□加湿□降温□除湿□加湿30 □降温□除湿□加湿□降温□除湿□加湿31 □降温□除湿□加湿□降温□除湿□加湿。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
注:可根据试验项目具体情况增减资料
机构临床试验资料归档清单
试验题目
申办方
专业组/PI
文件名
Title of Document
原件/复印件
Original / Copy
有
yes
无
no
不适用
NA
备注
A1 试验准备阶段
1 药物/器械临床试验申请表Original □□□
2 研究者简历/资质证书及更新Original □□□
3 CFDA批件(转让,需附转让证明) Copy □□□
4 伦理批件/参会委员名单及更新Copy □□□
5 申办者/合同研究组织资质证明,申
办方委托证明
Copy □□□
6 研究者手册及更新/ 产品说明书Copy □□□
7 试验方案及方案更新(版本、日期)Copy □□□
8 试验方案签署页Original/ Copy □□□
9 设盲试验的破盲规程Copy □□□
10 知情同意书及更新件(版本、日期)Copy □□□
11 招募广告Copy □□□
12 受试者日记(样本)Copy □□□
13 病例报告表及更新件(样本)Copy □□□
14 药检报告及新的药检报告Copy □□□
Title of Document Original / Copy yes no NA A1 试验准备阶段
15 试验用药品的标签* Copy □□□
16 医疗器械注册产品技术要求或相关
国家及行业标准
Copy □□□
17 首次用于植入人体的医疗器械,应提
供动物试验报告;其它需要由动物试
验确认安全性的产品,也应当提交动
物试验报告
Copy □□□
18 国家食品药品监督管理局认可的医
疗器械检测机构出具的一年内注册
型式检验报告和自检报告
Copy □□□
19 进口器械需提供原生产地注册批文
及进口医疗器械注册证书(国内器械
免)
Copy □□□
20 临床试验机构的设施和条件能够满
足试验的综述
Copy □□□
21 试验用医疗器械的研制符合适用的
医疗器械质量管理体系相关要求的
声明
Copy □□□
22 临床研究申办者承诺书及承担研究
相关损害赔偿的说明或保险证明
Copy □□□
23 研究中心合同/保密协议Original □□□
24 其它□□□
文件名
Title of Document
原件/复印件
Original / Copy
有
yes
无
no
不适用
NA
备注
A2 试验进行阶段
1 研究者会议(日程,出席签到,会议
记录)
Copy □□□
2 试验启动会记录(出席签到、会议记
录、培训资料)
Copy □□□
3 任务授权表及更新Copy □□□
4 实验室正常值范围及更新件Copy □□□
Title of Document Original / Copy yes no NA
A2 试验进行阶段
5 实验室资质证书Copy □□□
6 临床研究方案更新(版本、日期)Copy □□□
7 方案签署页的更新件Copy □□□
8 知情同意书更新件(版本、日期)Copy □□□
9 伦理批件及组成名单更新表Original □□□
10 试验药物运送记录(快递单)Copy □□□
11 试验药物交接记录表Copy □□□
12 应急信件交接记录表Copy □□□
13 试验相关用品交接表Copy □□□
14 生物样本运送记录Original □□□
15 试验药物召回(如果适用)Copy □□□
16 试验药物发放、回收记录表Original □□□
17 药物温度记录表Original □□□
18 生物样本温度记录表Original □□□
19 已签字的知情同意书Original □□□份
20 受试者筛选、入选表Original □□□
21 受试者鉴认代码表Original □□□
22 原始医疗资料Original □□□份
23 方案违反表/方案违反登记记录Original □□□
24 相关联系往来沟通记录(包括确认函
/跟进表、通话、沟通报告等)
Original □□□
25 研究者致申办者/EC/CFDA的严重不
良事件报告
Copy □□□
Title of Document Original / Copy yes no NA
A2 试验进行阶段
26 紧急揭盲记录表Original □□□
27 中期或年度报告Copy □□□份
28 其他□□□
文件名
Title of Document
原件/复印件
Original / Copy
有
yes
无
no
不适用
NA
备注
B1 试验结束阶段Study Close-down
1 随机应急信封记录表Copy □□□
2 药物退回记录(研究者-申办方)Copy □□□
3 试验相关用品回收记录Copy □□□
4 致研究者感谢信Original □□□
5 致伦理信告试验结束Original □□□
6 受试者完成编码目录(完整)Original □□□
7 试验总结报告Copy □□□
8 研究分中心报告Copy □□□
9 统计分析报告Copy □□□10监查员研究文件交接核查清单Original □□□11其他□□□备注:
交接人:交接日期
接收人:接收日期。
