硝酸钾的制备和提纯共31页文档
实验4-2 硝酸钾的制备

实验4-2 硝酸钾的制备一、实验目的:1.掌握硝酸钾的制备方法;2.了解硝酸钾的性质、用途及保存方法。
二、实验原理:硝酸钾是一种重要的无机化工原料,广泛应用于化肥、火药、玻璃、陶瓷等行业。
硝酸钾可由硝酸银和氯化钾反应制备。
反应方程式如下所示:AgNO3 + KCl → AgCl↓ + KNO3在反应中,硝酸银和氯化钾之间发生置换反应,生成硝酸钾和氯化银。
反应产物通过过滤或沉淀法得到。
三、实验仪器:蒸馏装置、滴液漏斗、pH计、电热板、磁力搅拌器、量筒、烧杯、漏斗、试管、玻璃棒、布、滤纸等。
四、实验步骤:1.向滴液瓶中加入50 mL的硝酸银溶液(0.1 M),并用去离子水定容至100 mL。
3.将硝酸银溶液倒入烧杯中,加热至70-80℃,搅拌均匀。
4.向硝酸银溶液中滴加氯化钾溶液,同时用pH计监测溶液的酸碱度,控制在7左右。
5.溶液放置冷却,产生白色沉淀,用布包在试管中,等沉淀全部收集到试管中。
6.沉淀物用去离子水洗涤,使其纯净。
7.沉淀物放入烘箱中,干燥至恒重。
8.称取干燥的硝酸钾,记录其质量。
五、实验注意事项:1.化学试剂具有一定的危害性,操作时必须注意安全,在试验中要戴上防护镜、手套等,避免与皮肤、眼睛接触,防止误吸、误食。
2.配制溶液时,应按照比例加入试剂,静置后再用玻璃棒搅拌均匀,避免加入过量的试剂。
3.滴加氯化钾溶液时,不能一次性加入,要逐滴滴加,同时用pH计控制反应的酸碱度。
4.反应过程中产生的气体,不能滞留在实验室内,要及时排除。
6.干燥时间不能过长,以免影响反应产物的结晶性。
七、实验结果与分析:本实验中,硝酸银溶液和氯化钾溶液反应生成硝酸钾,反应方程式为:根据反应比例计算,本实验中应加入19.84 g氯化钾溶液(0.1 M)才能使硝酸银被完全反应。
实验中可得硝酸钾质量应为14.84 g,实际称取得硝酸钾质量与理论值相差较大,这可能是由于反应过程中有氯化银和其他杂质和因为干燥时间太长导致反应产物失重等因素影响,同时也提示我们在实验操作中应该更加细心和谨慎。
硝酸钾生产工艺(DOC)
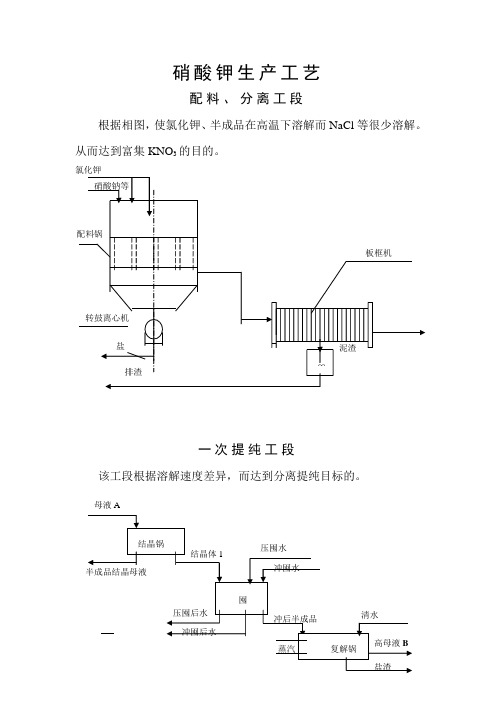
硝酸钾生产工艺配料、分离工段根据相图,使氯化钾、半成品在高温下溶解而NaCl等很少溶解。
从而达到富集KNO3的目的。
一次提纯工段该工段根据溶解速度差异,而达到分离提纯目标的。
母液A二次提纯工段该工段是重复上一工段的重要部分,再次提高产品质量,原理也与上类同,为高温溶解,低温结晶NaCl 溶解速度快等原理。
成品加工工段经以上工段主离子含量已达到合格,而水份较高。
通过干燥器使水份含量达到合格,产品粒度不均通过振动筛使之合格,装袋,即可向外销售,而完成生产工序。
高母液B离心水(同冲囤后水)螺旋输送机硝酸钾,分子式为KNO3。
无色透明棱柱晶体或粉末,溶于水、稀乙醇、甘油,不溶于无水乙醇和乙醚。
无嗅无毒,味咸辣有清凉感。
空气中不潮解。
在334℃分解放出氧,400℃时分解放出氧气,生成亚硝酸钾,继续加热则生成氧化钾。
是强氧化剂,与易燃物,有机物接触能引起燃烧爆炸,并发生有毒和刺激性气体。
与炭或硫一起加热时,能发强光而燃烧。
[1]硝酸钾 - 主要用途医药工业主要用于生产青霉素钾盐、利福平和利尿、发汗、清凉的药剂。
食品工业用于配肉,并在午餐肉中起防腐剂作用。
机械工业用于热处理(金属淬火)作淬火之盐浴。
玻璃工业用于玻璃器皿生产,起耐温硬化玻料的作用,还用作玻璃澄清剂。
农业上用作农作物和花卉的复合肥料。
[1]分析试剂,用于锰、钠的微量分析。
复分解法硝酸钠与氯化钾经复分解反应得硝酸钾和氯化钠。
利用它们的不同溶解度可将其分离。
此法工业上应用较多。
先把硝酸钠溶于热水中,在搅拌下按硝酸钠:氯化钾=100:85的配料比逐渐加入氯化钾,经蒸发浓缩,当温度为119°C时,氯化钠结晶析出。
将分离氯化钠后的母液缓慢冷却,硝酸钾即结晶析出。
经过滤、洗涤和干燥即得产品。
危害性爆炸物危险特性:与有机物、硫磷等混合可爆储运特性:库房通风; 轻装轻卸; 与有机物、还原剂、木炭、硫磷易燃物分开存放可燃性危险特性:高热放出氧气; 遇有机物、还原剂、木炭、硫、磷等易燃物可燃; 燃烧产生有毒氮氧化物烟雾防护措施工程控制:生产过程密闭,加强通风。
六、硝酸钾的制备和提纯

无机化学实验
化学化工学院
关键技术:
无机化学实验
化学化工学院
实验步骤:
无机化学实验
化学化工学院
无机化学实验
化学化工学院
无机化学实验
化学化工学院
思考题:
1、产品的主要杂志是什么? 2、能否将除去氯化钠后的滤液直接冷却制备硝 酸钾? 3、考虑在母液中留有硝酸钾,粗略计算本实验 实际得到的最高产量。
无机化学实验
化学化工学院
实验六 硝酸钾的制备与提纯
实验目:
1、学习利用各种易溶盐在不同温度时溶解度的差异来制 备易溶盐的原理和方法; 2、学习重结晶的原理和方法; 3、学习掌握热过滤的操作; 4、进一步巩固蒸发、结晶、过滤等基本操作。
无机化学实验
化学化工学院
实验用品:
仪器:循环水泵、热过滤漏斗、烧杯 液体药品:
NaNO3固体、KCl固体、 饱和KNO3溶液、AgNO3溶液
无机化学实验
化学化工学院
实验原理:
NaNO3 + KCl = NaCl + KNO3
复分解反应,其实质是: 发生复分解反应的两种物质在水溶液中相互交换离子, 结合成难电离的物质——沉淀、气体、水,使溶液中离 子浓度降低,化学反应即向着离子浓度降低的方向进行。
无机化学实验
化学化工学院
无机化学实验
化学化工学院
文档硝酸钾设计实验

硝酸钾的制备和提纯探讨课本实验(一)一、实验目的1、观察验证盐类溶解度和温度的关系;2、利用物质溶解度随温度变化的差别,学习用转化法制备硝酸钾;3、熟悉溶解、蒸发、结晶、过滤等技术,学会用重结晶法提纯物质。
二、实验原理复分解法是制备无机盐类的常用方法。
不溶性盐利用复分解法很容易制得容易制得,但是可溶性盐则需要根据温度反应中几种盐类溶解度的不同影响来处理。
本实验用NaNO3和KCl通过复分解来制取KNO3,其反应为:NaNO3 + KCl ===NaCl + KNO3三、基本操作1、玻璃仪器(烧杯、量筒、蒸发皿、表面皿)使用;2、实验室用的纯水;3、化学试剂;4、加热与冷却;5、固、液分离;*(1)6、查物质的溶解度数据表;*(2)7、重结晶;*(3)8、减压过滤;*(4)9、表面皿的洗涤和使用;表一:硝酸钾,氯化钾,硝酸钠,氯化钠在不同温度下的溶解度(g/100g水)温度(°c)0 10 20 30 40 60 80 100 K N O3 13. 3 20.9 31. 6 45.8 63.9 110 169 24 6 K C l 27. 6 31.0 34.0 37.0 40.0 45. 5 51. 1 56.7 NaNO3 7 3 80 88 9 6 10 4 12 4 148 180 N a C l 35.7 35.8 36.0 36. 3 36. 6 37. 3 38. 4 39.8四、实验步骤1、硝酸钾的制备a用表面皿在台秤上称取用表面皿在台秤上称取NaNO3 8.5g,KCl7.5g 放入烧杯中,加入15ml蒸馏加热至沸,使固体溶解.b待溶液蒸发至原来体积的2/3时便可停止加热,趁热用热滤漏斗进行过滤。
c将滤液冷却至室温,滤液中便有晶体析出。
d用减压过滤的方法分离并抽干此晶体,即得粗产品。
e吸干晶体表面的水分后转移到已称重的洁净表面皿中,用台秤称量,计算粗产品的百分产率。
2、重结晶法提纯KNO3将粗产品放在50mL烧杯中(留0.1g粗产品作对比纯度检验用),加入计算量的蒸馏水并搅拌之,用小火加热,直至晶体全部溶解为止。
硝酸钾的制备和提纯(精)

(℃ )
20的
倍数
KNO3 13. 20.9 31.6 45.8 63.9 110 169 246 7.85 3
KCl 27. 31.0 34.0 37.0 40.0 45.5 51.1 56.7 1.8 6
NaNO3 73 80 88 96 104 124 148 180 2.1
NaCl 35. 35.8 36.0 36.3 36.6 37.3 38.4 39.8 1.1 7
②温度计的水银球处于 `蒸馏烧瓶支管处
③冷凝水的方向:
下进上出
升华
可分离出固体混合物中的易升华物质
层析
分离溶液中的微量物质
练习: 用于分离或提纯物质的已学方法有:
A.萃取
B.分液
D.加热分解 E.蒸发
C.过滤 F.蒸馏
下列各组混合物的分离或提纯应选用上述哪种方法最合
适?(把选用方法的标号填入括号内) (1)除去Ca(OH)2溶液中悬浮的Ca(OH)2 颗粒( C ) (2)把饱和食盐水中的食盐提取出来( E ) (3)除去酒精中溶解的微量食盐( F ) (4)把溴水中的溴提取出来 ( A ) (5)用自来水制取医用蒸馏水 ( F ) (6)除去氧化钙中的碳酸钙 ( D ) (7)分离柴油和水的混合物 ( B )
A、③④⑥⑤②① B、③④⑥②⑤①
C、③⑥④②⑤① D、③④②⑥⑤①
粗盐溶解
难溶杂质
滤液
((Na+、Cl-、Ca2+、Mg2+、SO42-)
沉淀
滤液 ((Na+、Cl-)
蒸发结晶
NaCl固体
粗盐提纯的步骤
①用托盘天平准确称取5克食盐 ②在烧杯中,用20毫升水加以溶解 ③过滤取滤液 ④在滤液中滴加足量BaCl2溶液 ⑤再加稍过量的Na2CO3溶液 ⑥过滤取滤液 ⑦向所得滤液中滴加适量稀盐酸直至不冒气泡为止 ⑧蒸发结晶
硝酸钾的制备和提纯

溶解度的差异
结晶
NaNO3 + KCl = NaCl + KNO3 溶解度随温度变化: 大 小 小 大
思路:
高温下, 达到饱和的NaCl先结 晶分离;然后, 在低温下, KNO3达饱和,得到产品。
溶解
蒸发
热过滤
结晶
思考2:
这样得到的晶体是否纯净?若 不纯,应如何提纯?
初次结晶得到的晶体中 常会混有少量NaCl 杂质。将所得晶体溶于少量水中,然后进行 冷却、 结晶、过滤,如此反复的操作。
(2)晶体B的主要成分是__K_N_O__3 __,含有的少量杂质是__N_a_C__l ___, 要除去晶体 B中的少量杂质的方法是_重__结_晶___________.
(3)用少量热水淋洗晶体也是一种除去晶体中少量杂质的方法, 这种方法适用于晶体 _A___(填A或B)
交流与讨论:
阅读P16
谢谢大家!
《实验化学》专题1
物质的分离与提纯
硝酸钾的制备和提纯
我们在以前的学习中学过一些 实验方法,可用于混合物的分离和 提纯,请同学们回忆一下,你了解 哪些分离、提纯的方法?
过滤
通常用来分 离液体和不溶的 固体。
1、常压过滤
2、减压过滤 (也称抽滤或吸滤)
3、热过滤
结晶
1.蒸发结晶
注意事项:a、蒸发皿中的 溶液不超过容积的2/3; b、加热时要不断搅拌,以 免溶液溅出; c、当析出大量晶体时就应 熄灭酒精灯,利用余热蒸 发至干。
(℃ )
20的
倍数
KNO3 13. 20.9 31.6 45.8 63.9 110 169 246 7.85 3
KCl 27. 31.0 34.0 37.0 40.0 45.5 51.1 56.7 1.8 6
硝酸钾的制备
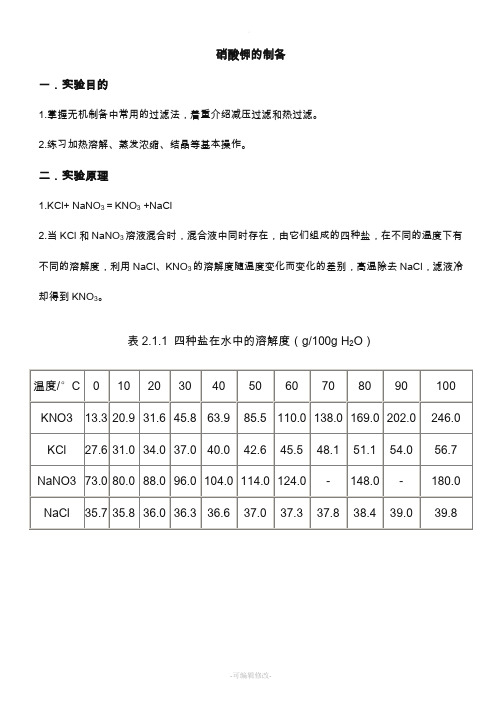
硝酸钾的制备一.实验目的1.掌握无机制备中常用的过滤法,着重介绍减压过滤和热过滤。
2.练习加热溶解、蒸发浓缩、结晶等基本操作。
二.实验原理1.KCl+ NaNO3=KNO3 +NaCl2.当KCl和NaNO3溶液混合时,混合液中同时存在,由它们组成的四种盐,在不同的温度下有不同的溶解度,利用NaCl、KNO3的溶解度随温度变化而变化的差别,高温除去NaCl,滤液冷却得到KNO3。
表2.1.1 四种盐在水中的溶解度(g/100g H2O)三.主要仪器与试剂1 仪器烧杯量筒热过滤漏斗减压过滤装置电子天平。
2 试剂NaNO3(s)、KCl(s)。
四.操作步骤五.实验结果及分析结果:1.上述得到的粗KNO3产品重量为:6.7g2.重结晶后得到的产品重量为:5.00g分析: 1.KCl+NaNO3=KNO3+NaCl7585 101597.5g8.5g10.1g 5.9g★最后体积为:(15*2/3+7.5)*3/4=13.1★母液中留有的硝酸钾:21.2g/100g*13.1g=2.8g ★(在283k时的KNO3溶解度为21.2g/100g水)★本实验粗产品的理论产量是:10.1g-2.8g=7.3g★粗产品的产率为:6.7/7.3*100%=91.8%2 . 理论重结晶率为:(167g-21.2g)/167g*100%=87.3%实际重结晶率为:5.0 /6.7*100%=74.6% (在353k时的溶解度为167g/100g水)六.问题及思考题●问题:1.产品的主要杂质是什么?怎样提纯?答:主要杂质是NaCl,可以通过重结晶来提纯。
2.能否将除去氯化钠后的滤液直接冷却制取硝酸钾?答:不能。
滤液直接冷却可以得到较多的硝酸钾,但会混氯化钠,产品纯度下降。
3.考虑在母液中留有硝酸钾,粗略计算本实验实际得到的最高产量。
答:设室温为293K,此时硝酸钾的溶解度为31.6g/100g水,氯化钠的溶解度为36g/100g水,则10mL水可溶解硝酸钾3.2g ,氯化钠为3.6g ,则析出硝酸钾为10.1-3.2 = 6.9g ,氯化钠为4-3.6 = 0.4g ,故共析出7.3g晶体。
硝酸钾的制备和提

(℃ )
20的
倍数
KNO3 13. 20.9 31.6 45.8 63.9 110 169 246 7.85 3
KCl 27. 31.0 34.0 37.0 40.0 45.5 51.1 56.7 1.8 6
NaNO3 73 80 88 96 104 124 148 180 2.1
NaCl 35. 35.8 36.0 36.3 36.6 37.3 38.4 39.8 1.1 7
(1)晶体A的主要成分是__N__a_C_l__,含有的少量杂质是
___K_N_O__3__,要除去晶体 A中的少量杂质的方法是 __加__少__量__水__溶_解__蒸__发. 再过滤
(2)晶体B的主要成分是_K__N_O_3___,含有的少量杂质是
___N_a_C_l___,要除去晶体 B中的少量杂质的方法是 ___重__结__晶________.
溶解度的差异
结晶
课前自主学案
自主学习
一、实验原理 1.盐的溶解度随温度的变化 氯化钠的溶解度随温度变化_不__大___,而氯化钾、 硝酸钠和硝酸钾在高温时具有较大的溶解度。 温度降低时,氯化钾、硝酸钠的溶解度明显减 小,而_硝__酸__钾___的溶解度则急剧下降。
实验思路:
高温下, 达到饱和的NaCl先结 晶分离;然后, 在低温下, KNO3达饱和,得到产品。
3.影响晶粒生成的条件 晶体颗粒的大小与结晶条件有关,溶质的溶解度 越小,或溶液的浓度越高,或溶剂的蒸发速度越 快,或溶液冷却的越快,析出的晶粒就越细小; 反之,可得到较大的晶体颗粒。在实际操作中, 常根据需要,控制适宜的结晶条件,以得到大小 合适的晶体颗粒。
练习: 用于分离或提纯物质的已学方法有:
溶剂而使溶液饱和析出晶体通过降低温度使溶液冷却达
硝酸钾的制备与提纯实验报告

大学化学实验报告本黔南民族师范学院姓名:江边实验室:无机周次:周五实验柜台: 11指导老师:章文伟硫酸亚铁铵的制备一.实验目的1. 学会利用溶解度的差异制备硫酸亚铁铵。
2. 从实验中掌握硫酸亚铁、硫酸亚铁铵复盐的性质3. 掌握水浴、减压过滤等基本操作4. 学习pH 试纸、吸管、比色管的使用5. 学习用目测比色法检验产品质量。
二.原理铁屑溶于稀硫酸生成硫酸铁。
硫酸铁与硫酸铵作用生成溶解度较小的硫酸亚铁铵。
三.仪器及药品洗瓶、250ml 烧杯、10ml 量筒、50ml 量筒、吸滤瓶、比色管、铁粉、盐酸2mol/L 、3mol/L 硫酸、四.实验步骤1. 硫酸亚铁制备2. 硫酸亚铁铵的制备3. Fe 3+的限量分析五.记录1.实验现象:①小火加热硝酸钠和氯化钾混合溶液过程中,烧杯内会有氯化钠晶体析出。
②热过滤后,漏斗滤纸上出现氯化钠白色晶体。
③滤瓶内液温降低后,出现白色针状的硝酸钾晶体。
④硝酸钾溶液加热浓缩后静置,降至室温出现较多的硝酸钾晶体。
⑤抽滤后漏斗上出现干燥的硝酸钾晶体。
2.产量:粗产品:2.78g3.理论产量:KCl+NaNO3===K NO3+NaClm (K NO3) =(8.5*101.1)/85=10.1g4.产率:2.78/10.1=27.5%六.思考题1.怎样利用溶解度差别从氯化钾—硝酸钠制备硝酸钾?当硝酸钠和氯化钾溶液混合时,溶液中会有硝酸钾、氯化钠、硝酸钠和氯化钾四种盐。
在不同温度下它们在水中溶解度不同,特别是在较高温度,硝酸钾在水中的溶解度比氯化钠的要大得多,所以在冷却过程中氯化钠首先析出,趁热过滤后滤液中即含有硝酸钾。
2.实验成败的关键在何处,应采取哪些措施才能使试验成功?①热过滤分离氯化钠和硝酸钾时要趁热快速,否则液温下降后硝酸钾也会和氯化钠一起析出,减低产量。
②减压过滤时注意不出现穿滤现象。
滤纸不可过大,要全部紧贴漏斗底部,可以用双层滤纸。
3.产品的主要杂质是什么?怎样提纯?产品的主要杂质是氯离子,通过重结晶可以除去。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
11、用道德的示范来造就一个人,显然比用法律来约束他更有价值。—— 希腊
12、法律是无私的,对谁都一视同仁。在每件事上,她都不徇私情。—— 托马斯
13、公正的法律限制不了好的自由,因为好人不会去做法律不允许的事 情。——弗劳德
14、法律是为了保护无辜而制定的。——爱略特 15、像房子一样,法律和法律都是相互依存的。——伯克
56、书不仅是生活,而且是现在、过 去和未 来文化 生活的 源泉。 ——库 法耶夫 57、生命不可能有两次,但许多人连一 次也不 善于度 过。— —吕凯 特 58、问渠哪得清如许,为有源头活水来 。—— 朱熹 59、我的努力求学没有得到别的好处, 只不过 是愈来 愈发觉 自己的 无知。 ——笛 卡儿
拉
60、生活的道路一旦选定,就要勇敢地 走到底 ,决不 回头。 ——左
