常用缓冲溶液的配制和PH计校正溶液配置方法
常用缓冲溶液的配制及PH计校正溶液配置方法

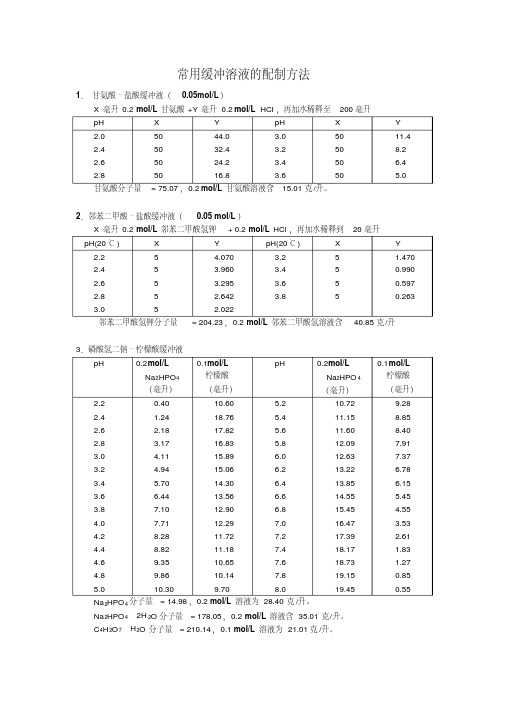
常用缓冲溶液的配制方法1.甘氨酸–盐酸缓冲液(0.05mol/L)2.邻苯二甲酸–盐酸缓冲液(0.05 mol/L)邻苯二甲酸氢钾分子量= 204.23,0.2 mol/L邻苯二甲酸氢溶液含40.85克/升3.磷酸氢二钠–柠檬酸缓冲液24Na2HPO4·2H2O分子量= 178.05,0.2 mol/L溶液含35.01克/升。
C4H2O7·H2O分子量= 210.14,0.1 mol/L溶液为21.01克/升。
4.柠檬酸–氢氧化钠-盐酸缓冲液① 使用时可以每升中加入1克克酚,若最后pH 值有变化,再用少量50% 氢氧化钠溶液或浓盐酸调节,冰箱保存。
5.柠檬酸–柠檬酸钠缓冲液(0.1 mol/L )6872柠檬酸钠Na 3 C 6H 5O 7·2H 2O :分子量294.12,0.1mol/L 溶液为29.41克/毫升。
6.乙酸–乙酸钠缓冲液(0.2 mol/L )Na 2Ac·3H 2O 分子量 = 136.09,0.2 mol/L 溶液为27.22克/升。
7.磷酸盐缓冲液242Na 2HPO 4·12H 2O 分子量 = 358.22,0.2 mol/L 溶液为71.64克/升。
Na 2HPO 4·2H 2O 分子量 = 156.03,0.2 mol/L 溶液为31.21克/升。
(2)磷酸氢二钠–磷酸二氢钾缓冲液(1/15 mol/L )242KH 2PO 4分子量 = 136.09,1/15M 溶液为9.078克/升。
8.磷酸二氢钾–氢氧化钠缓冲液(0.05M )9.巴比妥钠-盐酸缓冲液(18℃)10.Tris–盐酸缓冲液(0.05M ,25℃)50毫升0.1M 三羟甲基氨基甲烷(Tris )溶液与X 毫升0.1N 盐酸混匀后,加水稀释至100三羟甲基氨基甲烷(Tris )HOCH2 CH2OH CHOCH2 NH2分子量=121.14;0. 1M 溶液为12.114克/升。
PH计校准及缓冲液配置

标准缓冲溶液(均用pH标准缓冲物质配制)1.1 苯二甲酸氢钾标准缓冲溶液:c(KHC8H4O4)=0.05 mol/L(25℃时,pH=4.003)。
苯二甲酸氢钾的pH标准缓冲物质,有小塑料袋和瓶装两种,配制方法如下:a)袋装配制法:在250 mL(或500 mL)量瓶中(根据袋中标准缓冲物质量,选择量瓶大小),按袋上的说明配制成所需的浓度。
保存于聚乙烯瓶中。
b)瓶装配制法:称取5.10 g苯二甲酸氢钾(KHC8H4O4预先在115℃±5℃,烘2~3 h,于干燥器中冷却),溶于水并稀释至500 mL,混匀。
保存于聚乙烯瓶中。
1.2 0.025 mol/L磷酸二氢钾(KH2PO4)和0.025 mol/L磷酸氢二钠(Na2HPO4)混合标准缓冲溶液(25℃时,pH=6.864):磷酸二氢钾和磷酸氢二钠的pH标准缓冲物质,有小塑料袋装(混合磷酸盐)和瓶装(两种pH 标准缓冲物质分别包装)两种。
配制方法如下:a)袋装配制法:在量瓶(根据袋上说明确定量瓶大小)中按袋上说明配制成所需浓度后,保存于聚乙烯瓶中。
b)瓶装配制法:迅速称取3.40 g磷酸二氢钾(KH2PO4)和3.55 g磷酸氢二钠(Na2HPO4)(均预先在115±5℃烘2~3 h,于干燥器中冷却)溶于蒸馏水,转入1 000 mL量瓶中,加水至标线,混匀。
1.3 0.008 695 mol/L磷酸二氢钾(KH2PO4)和0.030 43 mol/L磷酸氢二钠(Na2HPO4)标准混合缓冲溶液(25℃时,pH=7.413):磷酸二氢钾和磷酸氢二钠两种pH标准缓冲物质分别用瓶包装,配制方法如下:迅速称取1.18 g磷酸二氢钾和4.31 g磷酸氢二钠(均预先在115℃±5℃烘2~3 h,于干燥器中冷却),溶于水,全量移入1 000 mL量瓶中,加水至标线,混匀。
保存于聚乙烯瓶中。
1.4 硼砂标准缓中溶液:c(Na2B4O7·10H2O)=0.010 mol/L(25℃时,pHs=9.182)。
(推荐)常用缓冲溶液的配制和PH计校正溶液配置方法

常用缓冲溶液的配制方法1.甘氨酸–盐酸缓冲液(0.05mol/L)X毫升0.2 mol/L甘氨酸+Y毫升0.2 mol/L HCI,再加水稀释至200毫升2.邻苯二甲酸–盐酸缓冲液(0.05 mol/L)X毫升0.2 mol/L邻苯二甲酸氢钾 + 0.2 mol/L HCl,再加水稀释到20毫升邻苯二甲酸氢钾分子量 = 204.23,0.2 mol/L邻苯二甲酸氢溶液含40.85克/升3.磷酸氢二钠–柠檬酸缓冲液24Na2HPO4·2H2O分子量 = 178.05,0.2 mol/L溶液含35.01克/升。
C4H2O7·H2O分子量 = 210.14,0.1 mol/L溶液为21.01克/升。
4.柠檬酸–氢氧化钠-盐酸缓冲液①使用时可以每升中加入1克克酚,若最后pH值有变化,再用少量50% 氢氧化钠溶液或浓盐酸调节,冰箱保存。
柠檬酸C6H8O7·H2O:分子量210.14,0.1 mol/L溶液为21.01克/升。
柠檬酸钠Na3 C6H5O7·2H2O:分子量294.12,0.1 mol/L溶液为29.41克/毫升。
227.磷酸盐缓冲液(1)磷酸氢二钠–磷酸二氢钠缓冲液(0.2)Na2HPO4·2H2O分子量 = 178.05,0.2 mol/L溶液为85.61克/升。
Na2HPO4·12H2O分子量 = 358.22,0.2 mol/L溶液为71.64克/升。
Na2HPO4·2H2O分子量 = 156.03,0.2 mol/L溶液为31.21克/升。
Na2HPO4·2H2O分子量 = 178.05,1/15M溶液为11.876克/升。
KH2PO4分子量 = 136.09,1/15M溶液为9.078克/升。
8.磷酸二氢钾–氢氧化钠缓冲液(0.05M)X毫升0.2M K2PO4 + Y毫升0.2N NaOH加水稀释至29毫升9.巴比妥钠-盐酸缓冲液(18℃)巴比妥钠盐分子量=206.18;0.04M溶液为8.25克/升10.Tris–盐酸缓冲液(0.05M,25℃)50毫升0.1M三羟甲基氨基甲烷(Tris)溶液与X毫升0.1N盐酸混匀后,加水稀释至100CHOCH2 NH2分子量=121.14;0.1M溶液为12.114克/升。
常用缓冲溶液的配制和PH计校正溶液配置方法之欧阳道创编
常用缓冲溶液的配制方法1.甘氨酸–盐酸缓冲液(0.05mol/L)X毫升0.2 mol/L甘氨酸+Y毫升0.2 mol/L HCI,再加水稀释至200毫升甘氨酸分子量= 75.07,0.2 mol/L甘氨酸溶液含15.01克/升。
2.邻苯二甲酸–盐酸缓冲液(0.05 mol/L)X毫升0.2 mol/L邻苯二甲酸氢钾+ 0.2 mol/L HCl,再加水稀释到20毫升邻苯二甲酸氢钾分子量= 204.23,0.2 mol/L邻苯二甲酸氢溶液含40.85克/升3.磷酸氢二钠–柠檬酸缓冲液Na2HPO4分子量= 14.98,0.2 mol/L溶液为28.40克/升。
Na2HPO4·2H2O分子量= 178.05,0.2 mol/L溶液含35.01克/升。
C4H2O7·H2O分子量= 210.14,0.1 mol/L溶液为21.01克/升。
4.柠檬酸–氢氧化钠-盐酸缓冲液①使用时可以每升中加入1克克酚,若最后pH值有变化,再用少量50% 氢氧化钠溶液或浓盐酸调节,冰箱保存。
5.柠檬酸–柠檬酸钠缓冲液(0.1 mol/L )柠檬酸C6H8O7·H2O :分子量210.14,0.1 mol/L 溶液为21.01克/升。
柠檬酸钠Na3 C6H5O7·2H2O :分子量294.12,0.1 mol/L溶液为29.41克/毫升。
6.乙酸–乙酸钠缓冲液(0.2 mol/L )Na2Ac·3H2O 分子量 = 136.09,0.2 mol/L 溶液为27.22克/升。
7.磷酸盐缓冲液(1)磷酸氢二钠–磷酸二氢钠缓冲液(0.2)Na2HPO4·2H2O 分子量 = 178.05,0.2 mol/L 溶液为85.61克/升。
Na2HPO4·12H2O 分子量 = 358.22,0.2 mol/L 溶液为71.64克/升。
Na2HPO4·2H2O 分子量 = 156.03,0.2 mol/L 溶液为31.21克/升。
PH计校准及缓冲液配置
标准缓冲溶液(均用pH标准缓冲物质配制)1.1 苯二甲酸氢钾标准缓冲溶液:c(KHC8H4O4)=0.05 mol/L(25℃时,pH=4.003)。
苯二甲酸氢钾的pH标准缓冲物质,有小塑料袋和瓶装两种,配制方法如下:a)袋装配制法:在250 mL(或500 mL)量瓶中(根据袋中标准缓冲物质量,选择量瓶大小),按袋上的说明配制成所需的浓度。
保存于聚乙烯瓶中。
b)瓶装配制法:称取5.10 g苯二甲酸氢钾(KHC8H4O4预先在115℃±5℃,烘2~3 h,于干燥器中冷却),溶于水并稀释至500 mL,混匀。
保存于聚乙烯瓶中。
1.2 0.025 mol/L磷酸二氢钾(KH2PO4)和0.025 mol/L磷酸氢二钠(Na2HPO4)混合标准缓冲溶液(25℃时,pH=6.864):磷酸二氢钾和磷酸氢二钠的pH标准缓冲物质,有小塑料袋装(混合磷酸盐)和瓶装(两种pH 标准缓冲物质分别包装)两种。
配制方法如下:a)袋装配制法:在量瓶(根据袋上说明确定量瓶大小)中按袋上说明配制成所需浓度后,保存于聚乙烯瓶中。
b)瓶装配制法:迅速称取3.40 g磷酸二氢钾(KH2PO4)和3.55 g磷酸氢二钠(Na2HPO4)(均预先在115±5℃烘2~3 h,于干燥器中冷却)溶于蒸馏水,转入1 000 mL量瓶中,加水至标线,混匀。
1.3 0.008 695 mol/L磷酸二氢钾(KH2PO4)和0.030 43 mol/L磷酸氢二钠(Na2HPO4)标准混合缓冲溶液(25℃时,pH=7.413):磷酸二氢钾和磷酸氢二钠两种pH标准缓冲物质分别用瓶包装,配制方法如下:迅速称取1.18 g磷酸二氢钾和4.31 g磷酸氢二钠(均预先在115℃±5℃烘2~3 h,于干燥器中冷却),溶于水,全量移入1 000 mL量瓶中,加水至标线,混匀。
保存于聚乙烯瓶中。
1.4 硼砂标准缓中溶液:c(Na2B4O7·10H2O)=0.010 mol/L(25℃时,pHs=9.182)。
pH计校准方法和标准缓冲液配置

pH计校准方法和标准缓冲液配置本文分享pH计校准所需工具、标准缓冲液配置方法,以及pH计校准方法、步骤及开展pH计校准工作的注意事项。
掌握这些pH计校准技能,对仪表人用好酸度计实惠多多。
pH计的应定期检定校准,使精密度和准确度符合要求。
怎么校准,或者说是怎样校正酸度计。
以下是昌晖仪表制造有限公司整理出来的资料。
有直接用配置好的标准缓冲液校准,有的需要自己配置标准缓冲液再校准,下面就看看这两种不同的前提,相同的校准方法步骤,供需要的朋友参考。
pH计校准所需工具/原料标准缓冲液(应选择与供试液pH值接近的标准缓冲液),目前标准溶液有7种,在我国一般使用以下3种溶液:(pH值在25时)①邻苯二甲酸氢钾(KHC8H4O4)4.003pH;0.05M②混合磷酸盐(Na2HPO4):磷酸二氢钾和磷酸氢二钠混合盐溶液6.864 pH;0.025M③硼砂(Na2B4O7·10H2O)9.182 pH:0.01M这三种标准缓冲液的配置方法如下:①pH4,邻苯二甲酸氢钾标准缓冲液精密称取在115±5干燥2-3小时的邻苯二甲酸氢钾[KHC8H4O4]10.12g,加水使溶解并稀释至1000ml。
②pH7,磷酸盐标准缓冲液(pH7.4)精密称取在115±5干燥2-3小时的无水磷酸氢二钠4.303g与磷酸二氢钾1.179g,加水使溶解并稀释至1000ml。
另补充:磷酸盐标准缓冲液(pH6.8)精密称取在115±5干燥2-3小时的无水磷酸氢二钠3.533g与磷酸二氢钾3.387g,加水使溶解并稀释至1000ml。
③pH9,硼砂标准缓冲液精密称取硼砂[Na2B4O7·10H2O]3.80g(注意:避免风化),加水使溶解并稀释至1000ml,置聚乙烯塑料瓶中,密塞,避免与空气中二氧化碳接触。
pH计校准步骤/方法1、实验室使用的pH计校准方法①常用的实验室PH计仪器校正时,要把仪器的斜率调到最大,并拨开电极上部的橡胶塞,使小孔露出,否则在进行校正时,会产生负压,泞致溶液不能正常进行离子交换,会使测量数据不准确。
常用缓冲溶液的配制和PH计校正溶液配置方法之欧阳德创编
常用缓冲溶液的配制方法1.甘氨酸–盐酸缓冲液(0.05mol/L)X毫升0.2 mol/L甘氨酸+Y毫升0.2 mol/L HCI,再加水稀释至200毫升甘氨酸分子量= 75.07,0.2mol/L甘氨酸溶液含15.01克/升。
2.邻苯二甲酸–盐酸缓冲液(0.05 mol/L)X毫升0.2mol/L邻苯二甲酸氢钾+ 0.2mol/L HCl,再加水稀释到20毫升邻苯二甲酸氢钾分子量= 204.23,0.2mol/L邻苯二甲酸氢溶液含40.85克/升3.磷酸氢二钠–柠檬酸缓冲液Na2HPO4分子量= 14.98,0.2mol/L溶液为28.40克/升。
Na2HPO4·2H2O分子量 = 178.05,0.2 mol/L溶液含35.01克/升。
C4H2O7·H2O分子量= 210.14,0.1mol/L溶液为21.01克/升。
4.柠檬酸–氢氧化钠-盐酸缓冲液①使用时可以每升中加入1克克酚,若最后pH值有变化,再用少量50% 氢氧化钠溶液或浓盐酸调节,冰箱保存。
5.柠檬酸–柠檬酸钠缓冲液(0.1 mol/L)柠檬酸C6H8O7·H2O:分子量210.14,0.1 mol/L溶液为21.01克/升。
柠檬酸钠Na3C6H5O7·2H2O:分子量294.12,0.1 mol/L溶液为29.41克/毫升。
6.乙酸–乙酸钠缓冲液(0.2 mol/L)Na2Ac·3H2O分子量 = 136.09,0.2 mol/L溶液为27.22克/升。
7.磷酸盐缓冲液(1)磷酸氢二钠–磷酸二氢钠缓冲液(0.2)Na2HPO4·2H2O分子量 = 178.05,0.2 mol/L溶液为85.61克/升。
Na2HPO4·12H2O分子量= 358.22,0.2mol/L 溶液为71.64克/升。
Na2HPO4·2H2O分子量 = 156.03,0.2 mol/L溶液为31.21克/升。
常用缓冲溶液的配制和PH计校正溶液配置方法之欧阳引擎创编

常用缓冲溶液的配制方法欧阳引擎(2021.01.01)1.甘氨酸–盐酸缓冲液(0.05mol/L)X毫升0.2 mol/L甘氨酸+Y毫升0.2 mol/L HCI,再加水稀释至200毫升甘氨酸分子量= 75.07,0.2 mol/L甘氨酸溶液含15.01克/升。
2.邻苯二甲酸–盐酸缓冲液(0.05 mol/L)X毫升0.2 mol/L邻苯二甲酸氢钾+ 0.2 mol/L HCl,再加水稀释到20毫升邻苯二甲酸氢钾分子量= 204.23,0.2 mol/L邻苯二甲酸氢溶液含40.85克/升3.磷酸氢二钠–柠檬酸缓冲液Na2HPO4分子量 = 14.98,0.2 mol/L 溶液为28.40克/升。
Na2HPO4·2H2O 分子量 = 178.05,0.2 mol/L 溶液含35.01克/升。
C4H2O7·H2O 分子量 = 210.14,0.1 mol/L 溶液为21.01克/升。
4.柠檬酸–氢氧化钠-盐酸缓冲液① 使用时可以每升中加入1克克酚,若最后pH 值有变化,再用少量50% 氢氧化钠溶液或浓盐酸调节,冰箱保存。
5.柠檬酸–柠檬酸钠缓冲液(0.1 mol/L )柠檬酸C6H8O7·H2O :分子量210.14,0.1 mol/L 溶液为21.01克/升。
柠檬酸钠Na3 C6H5O7·2H2O :分子量294.12,0.1 mol/L 溶液为29.41克/毫升。
6.乙酸–乙酸钠缓冲液(0.2 mol/L )Na2Ac·3H2O 分子量 = 136.09,0.2 mol/L 溶液为27.22克/升。
7.磷酸盐缓冲液(1)磷酸氢二钠–磷酸二氢钠缓冲液(0.2)Na2HPO4·2H2O分子量= 178.05,0.2 mol/L溶液为85.61克/升。
Na2HPO4·12H2O分子量= 358.22,0.2 mol/L溶液为71.64克/升。
2021年常用缓冲溶液的配制和PH计校正溶液配置方法
常用缓冲溶液的配制方法欧阳光明(2021.03.07)1.甘氨酸–盐酸缓冲液(0.05mol/L)X毫升0.2 mol/L甘氨酸+Y毫升0.2 mol/L HCI,再加水稀释至200毫升甘氨酸分子量= 75.07,0.2 mol/L甘氨酸溶液含15.01克/升。
2.邻苯二甲酸–盐酸缓冲液(0.05 mol/L)X毫升0.2 mol/L邻苯二甲酸氢钾+ 0.2 mol/L HCl,再加水稀释到20毫升邻苯二甲酸氢钾分子量= 204.23,0.2 mol/L邻苯二甲酸氢溶液含40.85克/升3.磷酸氢二钠–柠檬酸缓冲液Na2HPO4分子量= 14.98,0.2 mol/L溶液为28.40克/升。
Na2HPO4·2H2O分子量= 178.05,0.2 mol/L溶液含35.01克/升。
C4H2O7·H2O分子量= 210.14,0.1 mol/L溶液为21.01克/升。
4.柠檬酸–氢氧化钠-盐酸缓冲液①使用时可以每升中加入1克克酚,若最后pH值有变化,再用少量50% 氢氧化钠溶液或浓盐酸调节,冰箱保存。
5.柠檬酸–柠檬酸钠缓冲液(0.1 mol/L)柠檬酸C6H8O7·H2O:分子量210.14,0.1 mol/L溶液为21.01克/升。
柠檬酸钠Na3 C6H5O7·2H2O:分子量294.12,0.1 mol/L溶液为29.41克/毫升。
6.乙酸–乙酸钠缓冲液(0.2 mol/L)Na2Ac·3H2O分子量= 136.09,0.2 mol/L溶液为27.22克/升。
7.磷酸盐缓冲液(1)磷酸氢二钠–磷酸二氢钠缓冲液(0.2)Na2HPO4·2H2O分子量= 178.05,0.2 mol/L溶液为85.61克/升。
Na2HPO4·12H2O分子量= 358.22,0.2 mol/L溶液为71.64克/升。
Na2HPO4·2H2O 分子量 = 156.03,0.2 mol/L 溶液为31.21克/升。
常用缓冲溶液的配制和PH计校正溶液配置方法
10.57
9
Na2CO 2·10H 2O 分子量 =286.2;0.1M 溶液为 28.62 克/ 升。 N2HCO 3分子量 =84.0;0.1M 溶液为 8.40 克 /升。
pH
0.2 mol/L
0.1mol/L
Na2HPO4
柠檬酸
(毫升)
(毫升)
pH
0.2mol/L
Na2HPO 4 (毫升)
2.2
0.40
10.60
5.2
10.72
2.4
1.24
18.76
5.4
11.15
2.6
2.18
17.82
5.6
11.60
2.8
3.17
16.83
5.8
12.09
3.0
4.11
15.89
3.5
6.5
7.6
1.5
8.5
8.4
4.5
5.5
7.8
2.0
8.0
8.7
6.0
4.0
8.0
3.0
7.0
9.0
8.0
2.0
硼砂 Na2B4O7·H 2O,分子量 =381.43;0.05M 溶液( =0.2M 硼酸根)含 19.07 克 / 升。
硼酸 H 2BO 3,分子量 =61.84,0.2M 溶液为 12.37 克 /升。
0.25
6.00
8.67
9.90
0.10
5.00
8.18
10.00
0
6.98
6.00
4.00
Na2HPO 4·2H 2O 分子量 = 178.05, 1/15M 溶液为 11.876 克 /升。 KH 2PO4 分子量 = 136.09, 1/15M 溶液为 9.078 克 /升。
常用缓冲溶液的配制和PH计校正溶液配置方法

常用缓冲溶液的配制和P H计校正溶液配置方法精选文档TTMS system office room 【TTMS16H-TTMS2A-TTMS8Q8-常用缓冲溶液的配制方法1.甘氨酸–盐酸缓冲液(L)X毫升 mol/L甘氨酸+Y毫升 mol/L HCI,再加水稀释至200毫升甘氨酸分子量 = , mol/L甘氨酸溶液含克/升。
2.邻苯二甲酸–盐酸缓冲液( mol/L)X毫升 mol/L邻苯二甲酸氢钾 + mol/L HCl,再加水稀释到20毫升邻苯二甲酸氢钾分子量 = , mol/L邻苯二甲酸氢溶液含克/升3.磷酸氢二钠–柠檬酸缓冲液Na2HPO4分子量 = , mol/L溶液为克/升。
Na2HPO4·2H2O分子量 = , mol/L溶液含克/升。
C 4H2O7·H2O分子量 = , mol/L溶液为克/升。
4.柠檬酸–氢氧化钠-盐酸缓冲液①使用时可以每升中加入1克克酚,若最后pH值有变化,再用少量50%氢氧化钠溶液或浓盐酸调节,冰箱保存。
5.柠檬酸–柠檬酸钠缓冲液( mol/L)柠檬酸C 6H 8O 7·H 2O :分子量, mol/L 溶液为克/升。
柠檬酸钠Na 3 C 6H 5O 7·2H 2O :分子量, mol/L 溶液为克/毫升。
6.乙酸–乙酸钠缓冲液( mol/L )Na 2Ac·3H 2O 分子量 = , mol/L 溶液为克/升。
7.磷酸盐缓冲液(1)磷酸氢二钠–磷酸二氢钠缓冲液()Na2HPO4·2H2O分子量 = , mol/L溶液为克/升。
Na2HPO4·12H2O分子量 = , mol/L溶液为克/升。
Na2HPO4·2H2O分子量 = , mol/L溶液为克/升。
(2)磷酸氢二钠–磷酸二氢钾缓冲液(1/15 mol/L)1M溶液为克/升。
Tris溶液可从空气中吸收二氧化碳,使用时注意将瓶盖严。
缓冲溶液的配制和PH计校正溶液配置方法

缓冲溶液的配制和PH计校正溶液配置方法缓冲溶液是由一种酸和一种碱或它们的盐所组成的溶液,能够稳定pH值。
缓冲溶液通常用于实验室的化学分析、生物学实验和工业生产中。
下面是一种常见的缓冲溶液的配制方法:1.选择合适的酸和碱:首先要根据需要稳定的pH值选择合适的酸和碱。
常用的酸包括盐酸、硫酸和醋酸,常用的碱包括氢氧化钠和氢氧化铵。
2.确定理论浓度:根据所需缓冲溶液的体积和理论浓度,计算所需的酸和碱的摩尔量。
3.酸和碱的配制:将所需量的酸和碱分别加入不同的容器中,并用去离子水稀释,直至达到理论浓度。
4.混合酸和碱:将酸和碱的溶液缓慢地倒入一个干净的容器中,同时搅拌,直到达到所需pH值。
5.最后的稳定性调整:如果溶液的pH值不稳定,可以使用其他酸或碱来调整pH值,直到稳定。
PH计校正溶液配置方法:pH计是一种用于测量溶液酸碱性的仪器,它需要定期校正以保证测量的准确性。
下面是一种常见的pH计校正溶液的配置方法:1.选择标定溶液:根据pH计的测量范围和需求,选择两个标定溶液。
一般来说,一种标定溶液应该是酸性的(pH值低于7),另一种标定溶液应该是碱性的(pH值高于7)。
常用的酸包括盐酸和硫酸,常用的碱包括氢氧化钠和氢氧化铵。
2.确定理论浓度:根据所需标定溶液的体积和理论浓度,计算所需的酸和碱的摩尔量。
3.酸和碱的配制:将所需量的酸和碱分别加入不同的容器中,并用去离子水稀释,直至达到理论浓度。
4.调整pH值:使用pH计测量标定溶液的实际pH值,如果与预期值不相符,使用其他酸或碱来调整pH值,直到达到所需的实际pH值。
5.校正pH计:按照pH计的使用说明书,将pH计插入标定溶液中,根据pH计的操作步骤进行校正。
6.记录和保管:记录标定溶液的批号、浓度和pH值,并妥善保存,以备后续校正或参考。
在配制缓冲溶液和pH计的校正溶液时,注意使用精密的仪器和试剂,并严格按照操作规程进行操作,以保证实验的精确性和准确性。
常用缓冲溶液配制和PH计校正溶液配置方法

常用缓冲溶液的配制方法1.甘氨酸–盐酸缓冲液(0.05mol/L)甘氨酸分子量 = 75.07,0.2 mol/L甘氨酸溶液含15.01克/升。
2.邻苯二甲酸–盐酸缓冲液(0.05 mol/L)邻苯二甲酸氢钾分子量 = 204.23,0.2 mol/L邻苯二甲酸氢溶液含40.85克/升3.磷酸氢二钠–柠檬酸缓冲液Na2HPO4分子量 = 14.98,0.2 mol/L溶液为28.40克/升。
Na2HPO4·2H2O分子量 = 178.05,0.2 mol/L溶液含35.01克/升。
C4H2O7·H2O分子量 = 210.14,0.1 mol/L溶液为21.01克/升。
4.柠檬酸–氢氧化钠-盐酸缓冲液液或浓盐酸调节,冰箱保存。
柠檬酸C 6H 8O 7·H 2O :分子量210.14,0.1 mol/L 溶液为21.01克/升。
柠檬酸钠Na 3 C 6H 5O7·2H 2O :分子量294.12,0.1 mol/L 溶液为29.41克/毫升。
227.磷酸盐缓冲液(1)磷酸氢二钠–磷酸二氢钠缓冲液(0.2)Na 2HPO 4·2H 2O 分子量 = 178.05,0.2 mol/L 溶液为85.61克/升。
Na 2HPO 4·12H 2O 分子量 = 358.22,0.2 mol/L 溶液为71.64克/升。
Na 2HPO 4·2H 2O 分子量 = 156.03,0.2 mol/L 溶液为31.21克/升。
Na 2HPO 4·2H 2O 分子量 = 178.05,1/15M 溶液为11.876克/升。
KH 2PO 4分子量 = 136.09,1/15M 溶液为9.078克/升。
8.磷酸二氢钾–氢氧化钠缓冲液(0.05M )巴比妥钠盐分子量=206.18;0.04M 溶液为8.25克/升10.Tris –盐酸缓冲液(0.05M ,25℃)50毫升0.1M 三羟甲基氨基甲烷(Tris )溶液与X 毫升0.1N 盐酸混匀后,加水稀释至100毫升。
标准缓冲液的配制方法和PH计校正液(带目录)

标准缓冲液的配制⽅法和PH计校正液(带⽬录)标准缓冲液的配制及常⽤数据⼀、标准缓冲液pH值与温度对照表 (2)⼆、常⽤缓冲溶液的配制⽅法 (2)1.⽢氨酸–盐酸缓冲液(0.05mol/L) (2)2.邻苯⼆甲酸–盐酸缓冲液(0.05 mol/L) (2)3.磷酸氢⼆钠–柠檬酸缓冲液 (2)4.柠檬酸–氢氧化钠-盐酸缓冲液 (3)5.柠檬酸–柠檬酸钠缓冲液(0.1 mol/L) (3)6.⼄酸–⼄酸钠缓冲液(0.2 mol/L) (3)7.磷酸盐缓冲液 (3)8.磷酸⼆氢钾–氢氧化钠缓冲液(0.05M) (4)9.巴⽐妥钠-盐酸缓冲液(18℃) (4)10.Tris–盐酸缓冲液(0.05M,25℃) (4)1×TE Buffer (5)50×TAE Buffer 配制⽅法: (5)马来酸 M=116 (5)11.硼酸–硼砂缓冲液(0.2M硼酸根) (5)11.硼酸-硼砂缓冲液(0.2M硼酸根) (6)12.⽢氨酸–氢氧化钠缓冲液(0.05M) (6)13.硼砂-氢氧化钠缓冲液(0.05M硼酸根) (6)14.碳酸钠-碳酸氢钠缓冲液(0.1M) (6)15.“PBS”缓冲液 (6)三、实验室中常⽤酸碱的⽐重和浓度 (7)四、硫酸铵饱和度的常⽤表 (8)常见蛋⽩质分⼦量参考值(单位:dalton) (8)常见蛋⽩质等电点参考值(单位:pH) (9)元素的原⼦量表 (10)PH计校正溶液配置的标准⽅法 (13)⼀、标准缓冲液pH值与温度对照表⼆、常⽤缓冲溶液的配制⽅法1.⽢氨酸–盐酸缓冲液(0.05mol/L)⽢氨酸分⼦量= 75.07,0.2 mol/L⽢氨酸溶液含15.01克/升。
2.邻苯⼆甲酸–盐酸缓冲液(0.05 mol/L)X3.磷酸氢⼆钠–柠檬酸缓冲液Na 24Na 2HPO 4-2H 2O 分⼦量 = 178.05,0.2 mol/L 溶液含35.01克/升。
C 4H 2O 7·H 2O 分⼦量 = 210.14,0.1 mol/L 溶液为21.01克/升。
常用缓冲溶液的配制和PH计校正溶液配置方法之欧阳学创编

常用缓冲溶液的配制方法1.甘氨酸–盐酸缓冲液(0.05mol/L)X毫升0.2 mol/L甘氨酸+Y毫升0.2 mol/L HCI,再加水稀释至200毫升甘氨酸分子量 = 75.07,0.2 mol/L甘氨酸溶液含15.01克/升。
2.邻苯二甲酸–盐酸缓冲液(0.05 mol/L)X毫升0.2mol/L邻苯二甲酸氢钾+ 0.2mol/L HCl,再加水稀释到20毫升邻苯二甲酸氢钾分子量= 204.23,0.2mol/L邻苯二甲酸氢溶液含40.85克/升3.磷酸氢二钠–柠檬酸缓冲液Na2HPO4分子量= 14.98,0.2mol/L溶液为28.40克/升。
Na2HPO4·2H2O分子量= 178.05,0.2mol/L溶液含35.01克/升。
C4H2O7·H2O分子量= 210.14,0.1mol/L溶液为21.01克/升。
4.柠檬酸–氢氧化钠-盐酸缓冲液①使用时可以每升中加入1克克酚,若最后pH值有变化,再用少量50% 氢氧化钠溶液或浓盐酸调节,冰箱保存。
5.柠檬酸–柠檬酸钠缓冲液(0.1 mol/L)柠檬酸C6H8O7·H2O:分子量210.14,0.1mol/L溶液为21.01克/升。
柠檬酸钠Na3C6H5O7·2H2O:分子量294.12,0.1 mol/L溶液为29.41克/毫升。
6.乙酸–乙酸钠缓冲液(0.2 mol/L)Na2Ac·3H2O分子量 = 136.09,0.2 mol/L溶液为27.22克/升。
7.磷酸盐缓冲液(1)磷酸氢二钠–磷酸二氢钠缓冲液(0.2)Na 2HPO 4·2H 2O 分子量 = 178.05,0.2 mol/L 溶液为85.61克/升。
Na 2HPO 4·12H 2O 分子量 = 358.22,0.2 mol/L 溶液为71.64克/升。
Na 2HPO 4·2H 2O 分子量 = 156.03,0.2 mol/L 溶液为31.21克/升。
常用缓冲溶液的配制和PH计校正溶液配置方法

常用缓冲溶液的配制和PH计校正溶液配置方法随着科学技术的不断发展和应用的不断推进,缓冲溶液的配制和pH 计校正溶液的配置方法已经成为实验室中常见的操作。
本文将介绍一些常用的缓冲溶液的配制方法和pH计校正溶液的配置方法。
缓冲溶液是指具有稳定pH值的溶液。
在化学实验和生物实验中,常需要进行pH的调节和保持。
常用的缓冲溶液有磷酸盐缓冲溶液、醋酸盐缓冲溶液、碳酸氢根缓冲溶液等。
下面将介绍一些常用缓冲溶液的配制方法:1.磷酸盐缓冲溶液的配制方法:a. 配制PH=7.0的磷酸盐缓冲溶液,可以依次将1mol/L的磷酸二氢钾和1mol/L的磷酸二氢钠分别稀释至10mmol/L,然后按照比例混合得到所需的pH=7.0的磷酸盐缓冲溶液。
b. 配制PH=6.8的磷酸盐缓冲溶液,可以依次将1mol/L的磷酸二氢钾和1mol/L的磷酸二氢钠分别稀释至10mmol/L,然后按照比例混合得到所需的pH=6.8的磷酸盐缓冲溶液。
c.配制其他pH值的磷酸盐缓冲溶液,可以根据需要调整磷酸二氢钾和磷酸二氢钠的浓度比例,以达到所需的pH值。
2.醋酸盐缓冲溶液的配制方法:a. 配制PH=4.0的醋酸盐缓冲溶液,可以将0.1mol/L的醋酸钠溶液和0.1mol/L的醋酸溶液按照比例混合得到所需的pH=4.0的醋酸盐缓冲溶液。
b. 配制PH=5.0的醋酸盐缓冲溶液,可以将0.01mol/L的醋酸钠溶液和0.1mol/L的醋酸溶液按照比例混合得到所需的pH=5.0的醋酸盐缓冲溶液。
c.配制其他pH值的醋酸盐缓冲溶液,可以根据需要调整醋酸钠和醋酸的浓度比例,以达到所需的pH值。
3.碳酸氢根缓冲溶液的配制方法:a. 配制PH=9.0的碳酸氢根缓冲溶液,可以将0.1mol/L的碳酸氢钠溶液和0.1mol/L的盐酸溶液按照比例混合得到所需的pH=9.0的碳酸氢根缓冲溶液。
b. 配制PH=10.0的碳酸氢根缓冲溶液,可以将0.01mol/L的碳酸氢钠溶液和0.1mol/L的盐酸溶液按照比例混合得到所需的pH=10.0的碳酸氢根缓冲溶液。
常用缓冲溶液的配制及PH计校正溶液配置方法

常用缓冲溶液的配制及PH计校正溶液配置方法缓冲溶液是在化学实验和生物实验中常用的一种溶液,它可以维持溶液的pH值在一定范围内稳定不变。
下面我将介绍几种常用的缓冲溶液的配制方法以及pH计校正溶液的配置方法。
一、Phosphate Buffered Saline (PBS) 缓冲溶液PBS是一种用于细胞培养、免疫沉淀等实验中常用的缓冲溶液。
配制方法:1.加入8g氯化钠(NaCl)、0.2g磷酸二氢钠(NaH2PO4)和2.16g 磷酸氢二钠二水合物(Na2HPO4·2H2O)到适量的去离子水中。
2.搅拌溶解,直至溶液变清澈,如有需要可以调整pH值。
3.用去离子水稀释至1L,装入干净的烧瓶中。
二、Tris Buffered Saline (TBS) 缓冲溶液TBS是一种用于免疫学实验中常用的缓冲溶液。
配制方法:1. 加入3g氯化钠(NaCl)、2.42g三羟甲基氨基甲烷(Tris)到适量的去离子水中。
2.搅拌溶解,直至溶液变清澈,如有需要可以调整pH值。
3.用去离子水稀释至1L,装入干净的烧瓶中。
三、Glycine Buffered Saline (GBS) 缓冲溶液GBS可以用于免疫沉淀、酶抗体共轭实验等实验中。
配制方法:1. 加入6.05g氯化钠(NaCl)、0.72g糖苷酸(Glycine)到适量的去离子水中。
2.搅拌溶解,直至溶液变清澈,如有需要可以调整pH值。
3.用去离子水稀释至1L,装入干净的烧瓶中。
pH计校正溶液用于校正pH计,在实验中保证pH计的准确性。
配制方法:1.首先准备三种校正溶液:pH4.00、pH7.00和pH10.00。
2.分别加入适量的草酸二钾二水合物(K2C2O4·2H2O)、磷酸柠檬二钠五水合物(Na2HPO4·5H2O)、盐酸(HCl)到三个烧杯中。
3.搅拌溶解,直至草酸二钾二水合物、磷酸柠檬二钠五水合物、盐酸完全溶解。
4.分别用去离子水稀释至1L,装入干净的烧瓶中。
常用缓冲溶液的配制和PH计校正溶液配置方法

常用缓冲溶液的配制方法1 .甘氨酸-盐酸缓冲液(0.05mol/L )X毫升0.2 mol/L 甘氨酸+Y毫升0.2 mol/L HCI,再加水稀释至200毫升甘氨酸分子量,甘氨酸溶液含克升。
2 .邻苯二甲酸-盐酸缓冲液(0.05 mol/L )X毫升0.2 mol/L 邻苯二甲酸氢钾+ 0.2 mol/L HCl,再加水稀释到20毫升邻苯二甲酸氢钾分子量, 邻苯二甲酸氢溶液含克升Na2HPO4 分子量=14.98 , 0.2 mol/L 溶液为28.40 克/升。
Na2HPO42H2O 分子量=178.05 , 0.2 mol/L 溶液含35.01 克/升。
C4H2O7H2O 分子量=210.14 , 0.1 mol/L 溶液为21.01 克/升。
4 •柠檬酸-氢氧化钠-盐酸缓冲液① 使用时可以每升中加入 1克克酚,若最后p H 值有变化,再用少量 50%氢氧化钠溶液或浓盐酸调节,冰箱保存。
柠檬酸C6H8O7H2O:分子量210.14 , 0.1 mol/L 溶液为21.01克/升。
柠檬酸钠Na 3 C6H5O7 2H 2O :分子量294.12 , 0.1 mol/L 溶液为29.41克/毫升。
2•分子量,溶液为克升。
7 •磷酸盐缓冲液Na 2HPO 4 •22O 分子量 =178.05 , 0.2 mol/L 溶液为 85.61 克/升。
Na 2HPO 4 • 122O 分子量 =358.22 , 0.2 mol/L 溶液为 71.64 克/ 升。
Na 2HPO 4 •22O 分子量 =156.03, 0.2 mol/L 溶液为 31.21 克/升。
2 4 •22O分子量, 溶液为克升。
KH2PO4 分子量=136.09 , 1/15M8 .磷酸二氢钾-氢氧化钠缓冲液(0.05M )2 4 溶液为9.078克/升。
9 .巴比妥钠-盐酸缓冲液(18巴比妥钠盐分子量溶液为克升10 . Tris -盐酸缓冲液(0.05M ,25 C)50毫升0.1M三羟甲基氨基甲烷(Tris)溶液与X毫升0.1N盐酸混匀后,加水稀释至100 毫升。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
常用缓冲溶液得配制方法
1.甘氨酸–盐酸缓冲液(0、05mol/L)
X毫升0、2 mol/L甘氨酸+Y毫升0、2 mol/L HCI,再加水稀释至200毫升
2.邻苯二甲酸–盐酸缓冲液(0、05mol/L)
X毫升0、2mol/L邻苯二甲酸氢钾+ 0、2 mol/LHCl,再加水稀释到20毫升
邻苯二甲酸氢钾分子量= 204、23,0、2 mol/L邻苯二甲酸氢溶液含40、85克/升
24
Na2HPO4·2H2O分子量=178、05,0、2 mol/L溶液含35、01克/升。
C4H2O7·H2O分子量=210、14,0、1 mol/L溶液为21、01克/升。
①使用时可以每升中加入1克克酚,若最后pH值有变化,再用少量50% 氢氧化钠
溶液或浓盐酸调节,冰箱保存。
5.柠檬酸–柠檬酸钠缓冲液(0、1 mol/L)
柠檬酸C6H8O7·H2O:分子量210、14,0、1mol/L溶液为21、01克/升。
柠檬酸钠Na3C6H5O7·2H2O:分子量294、12,0、1 mol/L溶液为29、41克/毫升。
Na2Ac·3H2O分子量= 136、09,0、2mol/L溶液为27、22克/升。
7.磷酸盐缓冲液
242
Na2HPO4·12H2O分子量= 358、22,0、2mol/L溶液为71、64克/升。
Na2HPO4·2H2O分子量= 156、03,0、2mol/L溶液为31、21克/升。
Na2HPO4·2H2O分子量= 178、05,1/15M溶液为11、876克/升。
KH2PO4分子量=136、09,1/15M溶液为9、078克/升。
8.磷酸二氢钾–氢氧化钠缓冲液(0、05M)
9.巴比妥钠-盐酸缓冲液(18℃)
10.Tris–盐酸缓冲液(0、05M,25℃)
50毫升0、1M三羟甲基氨基甲烷(Tris)溶液与X毫升0、1N盐酸混匀后,加水稀释至100
三羟甲基氨基甲烷(Tr is)H OCH2 CH2OH C
HOCH 2 NH 2
分子量=121、14;
0、 1M 溶液为12、114克/升。
T ris 溶液可从空气中吸收二氧化碳,使用时注意将瓶盖严。
2472硼酸H2BO 3,分子量=61、84,0、2M 溶液为12、37克/升。
硼砂易失去结晶水,必须在带塞得瓶中保存。
硼砂Na 2B 4O 7·10H 2O,分子量=381、43;0、05M 溶液(=0、2M 硼酸根)含19、07克/升。
硼酸H 2BO 3,分子量=61、84, 0、2M 溶液为12、37克/升。
硼砂ﻩ易失去结晶水,必须在带塞得瓶中保存。
1
2.甘氨酸–氢氧化钠缓冲液(0、05M )
甘氨酸分子量=75、07;0、2M 溶液含15、01克/升。
13.硼砂-氢氧化钠缓冲液(0、05M硼酸根)
硼砂Na2B4O7·10H2O,分子量=381、43;0、05M溶液为19、07克/升。
14.碳酸钠-碳酸氢钠缓冲液(0、1M)
2+2+
Na2CO2·10H2O分子量=286、2;0、1M溶液为28、62克/升。
N2HCO3分子量=84、0;0、1M溶液为8、40克/升。
PH计校正溶液配置得标准方法
1)pH4,邻苯二甲酸氢钾标准缓冲液:ﻫ精密称取在115±5℃干燥2~3小时得邻苯二甲酸氢钾[KHC8H4O4]10、12g,加水使溶解并稀释至1000ml。
ﻫ2)pH7,磷酸盐标准缓冲液(pH7、4):
精密称取在115±5℃干燥2~3小时得无水磷酸氢二钠4、303g与磷酸二氢钾1、179g,加水使溶解并稀释至1000ml。
另补充:磷酸盐标准缓冲液(pH6、8) 精密称取在115±5℃干燥2~3小时得无水磷酸氢二钠3、533g与磷酸二氢钾3、387g,加水使溶解并稀释至1000ml。
ﻫ3)pH9,硼砂标准缓冲液:ﻫ精密称取硼砂[Na2B4O7·10H2O]3、80g(注意:避免风化),加水使溶解并稀释至1000ml,置聚乙烯塑料瓶中,密塞,避免与空气中二氧化碳接触。
