常用pH缓冲液
最全常用缓冲液配方及缓冲范围

最全常用缓冲液配方及缓冲范围缓冲液是一种能够维持溶液pH值相对稳定的溶液。
它可以减少酸碱反应的影响,使物质在酸碱环境中保持稳定。
在生命科学实验室和工业生产中,常用的缓冲液有许多种。
下面是最常用的一些缓冲液配方及其缓冲范围。
1. Phosphate缓冲液:Phosphate缓冲液通常由磷酸二氢盐和磷酸氢二盐组成。
它的pH范围为2.1-7.4,在生物化学和细胞生物学实验中得到广泛应用。
配方1:-0.1M磷酸二氢盐,pH2.0-2.8-0.2M磷酸氢二盐,pH5.8-7.4配方2:-0.1M磷酸二氢盐,pH2.1-3.1-0.2M磷酸氢二盐,pH5.6-7.42. Tris缓冲液:Tris缓冲液由三羟甲基氨基甲烷(Tris)和其酸盐组成。
它的pH范围为7-9,在分子生物学和生化实验中广泛使用。
配方:- 1 M Tris HCl,pH 7.4-9.0- 1 M Tris base,pH 7.0-9.23.MES缓冲液:MES缓冲液是一种针对中性pH值(5.5-6.7)的缓冲液,常用于细胞生物学和酶活性实验。
配方:-0.1MMES,pH5.5-6.74.HEPES缓冲液:HEPES缓冲液是一种适用于细胞培养和酶活性实验的缓冲液,其pH 范围为6.8-8.2配方:-0.1MHEPES,pH6.8-8.25.CAPS缓冲液:CAPS缓冲液是一种适用于生化实验的缓冲液,其pH范围为9.7-11.1配方:-0.1MCAPS,pH9.7-11.1这些是最常用的缓冲液配方及其缓冲范围,可以根据实验的需要选择合适的缓冲液。
需要注意的是,在配制缓冲液时应使用高纯度的化学品,并根据实验要求精确控制缓冲液的pH值。
此外,在实验过程中应注意缓冲液的保存和稳定性,以确保实验结果的准确性。
常见pH值的磷酸盐缓冲液的配制

常见pH值的磷酸盐缓冲液的配制1、磷酸盐缓冲液取磷酸二氢钠38.Og,与磷酸氢二钠5.04g,加水使成1000m1,即得。
2、磷酸盐缓冲液(pH2.0)甲液:取磷酸16.6m1,加水至IooOm1,摇匀。
乙液:取磷酸氢二钠71.63g,加水使溶解成1000m1.取上述甲液72.5m1与乙液27.5m1混合,摇匀,即得。
3、磷酸盐缓冲液(pH2.5)取磷酸二氢钾100g,加水800m1,用盐酸调节PH至2.5,用水稀释至1000m1σ4、磷酸盐缓冲液(pH5.0)取0.2mo1∕1磷酸二氢钠溶液一定量,用氢氧化钠试液调节PH值至5.0,即得o5、磷酸盐缓冲液(pH5.8)取磷酸二氢钾8.34g与磷酸氢二钾0∙87g,加水使溶解成IOOOm1,即得。
6、磷酸盐缓冲液(pH6.5)取磷酸二氢钾0.68g,加0.1mo1∕1氢氧化钠溶液15.2m1,用水稀释至IOOrn1,即得。
7、磷酸盐缓冲液(pH6.6)取磷酸二氢钠1.74g、磷酸氢二钠2.7g与氯化钠1.7g,加水使溶解成400m1,即得。
8、磷酸盐缓冲液(含胰酶)(pH6.8)取磷酸二氢钾6.8g,加水500m1使溶解,用0.1mo1∕1氢氧化钠溶液调节PH 值至6.8;另取胰前10g,加水适量使溶解,将两液混合后,加水稀释至IOOom1,即得。
9、磷酸盐缓冲液(pH6.8)取0.2mo1∕1磷酸二氢钾溶液250m1,加0.2mo1/1氢氧化钠溶液118m1,用水稀释至IOOOm1,摇匀,即得。
10、磷酸盐缓冲液(pH7.0)取磷酸二氢钾0.68g,加0.Imo1/1氢氧化钠溶液29.Im1,用水稀释至100m1,即得。
11、磷酸盐缓冲液(pH7.2)取0.2mo1∕1磷酸二氢钾溶液50m1与0.2mo1∕1氢氧化钠溶液35m1,加新沸过的冷水稀释至200m1,摇匀,即得。
12、磷酸盐缓冲液(pH7.3)取磷酸氢二钠1.9734g 与磷酸二氢钾0.2245g,加水使溶解成1000m1,调节PH 值至7.3,即得。
常用缓冲溶液的配制及PH计校正溶液配置方法

常用缓冲溶液的配制方法1.甘氨酸–盐酸缓冲液(0.05mol/L)2.邻苯二甲酸–盐酸缓冲液(0.05 mol/L)邻苯二甲酸氢钾分子量= 204.23,0.2 mol/L邻苯二甲酸氢溶液含40.85克/升3.磷酸氢二钠–柠檬酸缓冲液24Na2HPO4·2H2O分子量= 178.05,0.2 mol/L溶液含35.01克/升。
C4H2O7·H2O分子量= 210.14,0.1 mol/L溶液为21.01克/升。
4.柠檬酸–氢氧化钠-盐酸缓冲液① 使用时可以每升中加入1克克酚,若最后pH 值有变化,再用少量50% 氢氧化钠溶液或浓盐酸调节,冰箱保存。
5.柠檬酸–柠檬酸钠缓冲液(0.1 mol/L )6872柠檬酸钠Na 3 C 6H 5O 7·2H 2O :分子量294.12,0.1mol/L 溶液为29.41克/毫升。
6.乙酸–乙酸钠缓冲液(0.2 mol/L )Na 2Ac·3H 2O 分子量 = 136.09,0.2 mol/L 溶液为27.22克/升。
7.磷酸盐缓冲液242Na 2HPO 4·12H 2O 分子量 = 358.22,0.2 mol/L 溶液为71.64克/升。
Na 2HPO 4·2H 2O 分子量 = 156.03,0.2 mol/L 溶液为31.21克/升。
(2)磷酸氢二钠–磷酸二氢钾缓冲液(1/15 mol/L )242KH 2PO 4分子量 = 136.09,1/15M 溶液为9.078克/升。
8.磷酸二氢钾–氢氧化钠缓冲液(0.05M )9.巴比妥钠-盐酸缓冲液(18℃)10.Tris–盐酸缓冲液(0.05M ,25℃)50毫升0.1M 三羟甲基氨基甲烷(Tris )溶液与X 毫升0.1N 盐酸混匀后,加水稀释至100三羟甲基氨基甲烷(Tris )HOCH2 CH2OH CHOCH2 NH2分子量=121.14;0. 1M 溶液为12.114克/升。
常用的45种缓冲溶液的配制

1.乙醇-醋酸铵缓冲液(pH3.7)取5mol/L醋酸溶液15.0ml,加乙醇60ml和水20ml,用10mol/L氢氧化铵溶液调节pH值至3.7,用水稀释至1000ml,即得。
2.三羟甲基氨基甲烷缓冲液(pH8.0)取三羟甲基氨基甲烷12.14g,加水800ml,搅拌溶解,并稀释至1000ml,用6mol/L盐酸溶液调节pH值至8.0,即得。
3.三羟甲基氨基甲烷缓冲液(pH8.1)取氯化钙0.294g,加0.2mol/L三羟甲基氨基甲烷溶液40ml使溶解,用1mol/L盐酸溶液调节pH值至8.1,加水稀释至100ml,即得。
4.三羟甲基氨基甲烷缓冲液(pH9.0)取三羟甲基氨基甲烷6.06g,加盐酸赖氨酸3.65g、氯化钠5.8g、乙二胺四醋酸二钠0.37g,再加水溶解使成1000ml,调节pH值至9.0,即得。
5.乌洛托品缓冲液取乌洛托品75g,加水溶解后,加浓氨溶液4.2ml,再用水稀释至250ml,即得。
6.巴比妥缓冲液(pH7.4)取巴比妥钠4.42g,加水使溶解并稀释至400ml,用2mol/L盐酸溶液调节pH值至7.4,滤过,即得。
7.巴比妥缓冲液(pH8.6)取巴比妥5.52g与巴比妥钠30.9g,加水使溶解成2000ml,即得。
8.巴比妥-氯化钠缓冲液(pH7.8)取巴比妥钠5.05g,加氯化钠3.7g及水适量使溶解,另取明胶0.5g加水适量,加热溶解后并入上述溶液中。
然后用0.2mol/L盐酸溶液调节pH值至7.8,再用水稀释至500ml,即得。
9.甲酸钠缓冲液(pH3.3)取2mol/L甲酸溶液25ml,加酚酞指示液1滴,用2mol/L氢氧化钠溶液中和,再加入2mol/L甲酸溶液75ml,用水稀释至200ml,调节pH值至3.25~3.30,即得。
10.邻苯二甲酸盐缓冲液(pH5.6)取邻苯二甲酸氢钾10g,加水900ml,搅拌使溶解,用氢氧化钠试液(必要时用稀盐酸)调节pH值至5.6,加水稀释至1000ml,混匀,即得。
ph缓冲溶液的配制方法

ph缓冲溶液的配制方法PH缓冲溶液是指在一定范围内,具有缓冲pH值的溶液,适用于化学、生物、医药等各个领域的实验和应用。
在实验中,通常需要制备一定浓度和pH值的缓冲溶液,以保证实验结果的准确性和可重复性。
本文将介绍几种常见的缓冲溶液配制方法。
一、磷酸缓冲液(PBS)磷酸缓冲液是一种常用的生物化学实验缓冲液,可以用于细胞培养、酶活性测定、免疫学实验等等。
其配制方法如下:1. 准备250ml坐标瓶,称取1.37g Na2HPO4·12H2O和0.26g KH2PO4。
3. 将两个溶液混合,加入NaCl使溶液最终重量达到250g,调节pH值至7.4-7.6,如果pH值过低,可加入1M NaOH调节,反之加入1M HCl。
二、三氯醋酸缓冲液(TCA)三氯醋酸缓冲液是一种酸性缓冲液,适用于蛋白质的沉淀和提取等实验。
其配制方法如下:1. 准备250ml坐标瓶,在其中加入11.9g三氯乙酸,加入去离子水至250ml。
2. 调节溶液pH值至2.0-2.5,可使用无水HCl或NaOH来调节pH值。
3. 再加入去离子水,使溶液最终体积达到500ml,并根据需要添加NaCl和KCl等。
五、TRIS缓冲液TRIS缓冲液是一种常用的生化和细胞学实验用缓冲液,其缓冲范围在7.0~9.2之间。
其配制方法如下:1. 准备500ml坐标瓶,称取12.11g Tris-Base。
3. 在室温下缓慢加入0.1M HCl溶液,同时使用pH计监测溶液pH值,当pH值达到所需值时停止加入。
4. 将溶液体积补至500ml,并调节pH值。
可根据实验需要调节缓冲液中的NaCl或其他化学物质的浓度。
以上就是几种常见缓冲溶液的配制方法,需要注意的是在配制过程中,一定要严格按照实验要求和操作规程进行,以获得准确的实验结果。
同时,制备的缓冲液要遵循使用前检测pH值、滤过消毒等规定操作,以保证实验的可重复性和安全性。
常用缓冲液配方及缓冲范围

常用缓冲液配方及缓冲范围缓冲液是一种水溶液,其中含有在酸性或碱性条件下能够保持pH稳定的化学物质。
缓冲液广泛应用于生物化学、分子生物学、生物技术和医学等领域的实验和研究中。
下面是一些常用的缓冲液配方及其应用范围。
1. Tris缓冲液Tris缓冲液是一种中性缓冲液,常用于生物化学和分子生物学实验。
它的配方通常为:- 10 mM Tris base-1mMEDTA-向溶剂中调整pH至7.4Tris缓冲液可用于DNA和RNA的电泳、酶反应、细胞培养等实验中。
2.PBS缓冲液PBS(磷酸盐缓冲液)是一种常用的生物学缓冲液,具有缓冲能力强和与生物体液成分相似的特点。
它的配方通常为:-137mMNaCl-2.7mMKCl-10mMNa2HPO4-2mMKH2PO4-向溶剂中调整pH至7.4PBS缓冲液可用于细胞培养、免疫荧光染色、蛋白质凝胶电泳等实验中。
3.TAE缓冲液TAE(三乙酸缓冲液)是一种常用的核酸电泳缓冲液,其配方为:- 40 mM Tris base-20mM醋酸-1mMEDTA-向溶剂中调整pH至8.0TAE缓冲液可用于DNA和RNA的琼脂糖凝胶电泳,如聚丙烯酰胺凝胶电泳()和琼脂糖凝胶电泳(agarose gel electrophoresis)。
4. Tris-HCl缓冲液Tris-HCl缓冲液是一种常用的酸性或碱性缓冲液。
它的配方基于Tris缓冲液,在Tris缓冲液基础上调整pH的方法是在配方中加入稀盐酸或稀氢氧化钠。
例如,对于Tris-HCl缓冲液的配方为:- 50 mM Tris base-向溶剂中加入HCl调整pH至所需的值(通常为7.2至9.0)Tris-HCl缓冲液可用于酶反应、蛋白质组学研究、PCR等实验中。
这只是一些常用的缓冲液配方,根据不同实验需求和物质稀释要求,还有其他许多缓冲液的配方。
对于缓冲液的选择,关键在于根据实验要求选取适当的缓冲体系,并对缓冲液中所需的化学物质浓度、pH值等进行精确调整。
常用缓冲溶液的配置

1 乙醇-醋酸铵缓冲液(pH3.7)取5mol/L醋酸溶液15.0ml,加乙醇60ml和水20ml,用10mol/L氢氧化铵溶液调节pH值至3.7,用水稀释至1000ml,即得。
2 三羟甲基氨基甲烷缓冲液(pH8.0)取三羟甲基氨基甲烷12.14g,加水800ml,搅拌溶解,并稀释至1000ml,用6mol/L盐酸溶液调节pH值至8.0,即得。
3 三羟甲基氨基甲烷缓冲液(pH8.1)取氯化钙0.294g,加0.2mol/L三羟甲基氨基甲烷溶液40ml使溶解,用1mol/L盐酸溶液调节pH值至8.1,加水稀释至100ml,即得。
4 三羟甲基氨基甲烷缓冲液(pH9.0)取三羟甲基氨基甲烷6.06g,加盐酸赖氨酸3.65g、氯化钠5.8g、乙二胺四醋酸二钠0.37g,再加水溶解使成1000ml,调节pH值至9.0,即得。
乌洛托品缓冲液取乌洛托品75g,加水溶解后,加浓氨溶液4.2ml,再用水稀释至250ml,即得。
巴比妥缓冲液(pH7.4)取巴比妥钠4.42g,加水使溶解并稀释至400ml,用2mol/L盐酸溶液调节pH值至7.4,滤过,即得。
巴比妥缓冲液(pH8.6)取巴比妥5.52g与巴比妥钠30.9g,加水使溶解成2000ml,即得。
巴比妥-氯化钠缓冲液(pH7.8)取巴比妥钠5.05g,加氯化钠3.7g及水适量使溶解,另取明胶0.5g加水适量,加热溶解后并入上述溶液中。
然后用0.2mol/L盐酸溶液调节pH值至7.8,再用水稀释至500ml,即得。
甲酸钠缓冲液(pH3.3)取2mol/L甲酸溶液25ml,加酚酞指示液1滴,用2mol/L氢氧化钠溶液中和,再加入2mol/L甲酸溶液75ml,用水稀释至200ml,调节pH值至3.25~3.30,即得。
邻苯二甲酸盐缓冲液(pH5.6)取邻苯二甲酸氢钾10g,加水900ml,搅拌使溶解,用氢氧化钠试液(必要时用稀盐酸)调节pH值至5.6,加水稀释至1000ml,混匀,即得。
常用缓冲溶液的配制和PH计校正溶液配置方法
3.5
6.5
7.6
1.5
8.5
8.4
4.5
5.5
7.8
2.0
8.0
8.7
6.0
4.0
8.0
3.0
7.0
9.0
8.0
2.0
硼砂 Na2B4O7·H 2O,分子量 =381.43;0.05M 溶液( =0.2M 硼酸根)含 19.07 克 / 升。
硼酸 H 2BO 3,分子量 =61.84,0.2M 溶液为 12.37 克 /升。
5
2.365
8.0
5
Y (毫升) 2.963 3.500 3.950 4.280 4.520 4.680
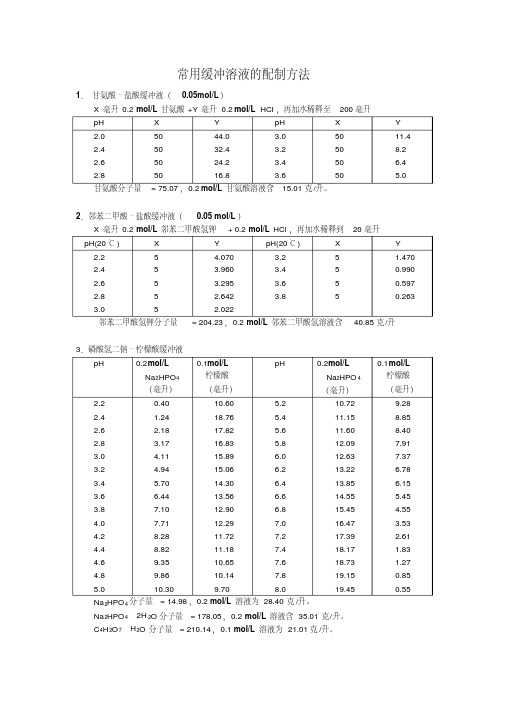
9.巴比妥钠 - 盐酸缓冲液( 18℃)
pH
0.04M 巴比妥 0.2V 盐酸
pH
钠溶液
0.04M 巴 比 0.2N 盐酸 (毫 妥钠溶液 ( 毫 升 )
6.8
100
18.4
8.4
7.0
100
17.8
10.0
90.0
7.1
67.0
33.0
6.0
12.3
87.7
7.2
72.0
28.0
6.1
15.0
85.0
7.3
77.0
23.0
6.2
18.5
81.5
7.4
81.0
19.0
6.3
22.5
77.5
7.5
84.0
16.0
6.4
26.5
73.5
7.6
87.0
13.0
6.5
31.5
68.5
7.7
89.5
常用的三种标准缓冲溶液

常用的三种标准缓冲溶液
1. 磷酸盐缓冲溶液,磷酸盐缓冲溶液是一种常用的生物化学和
分子生物学实验中使用的缓冲溶液。
常见的磷酸盐缓冲溶液包括磷
酸盐缓冲液(PBS)、Tris-HCl缓冲液等。
磷酸盐缓冲溶液的pH范
围广,能够在不同的实验条件下稳定维持所需的pH值。
2. 乙酸/乙酸钠缓冲溶液,乙酸/乙酸钠缓冲溶液是另一种常用
的生物化学实验中使用的缓冲溶液。
它主要由乙酸和乙酸钠组成,
能够在酸性条件下有效地维持所需的pH值。
乙酸/乙酸钠缓冲溶液
在许多生化实验中被广泛应用,如蛋白质电泳、核酸电泳等。
3. 碳酸氢盐缓冲溶液,碳酸氢盐缓冲溶液是一种常用的生物化
学实验中使用的缓冲溶液,由碳酸氢盐和碳酸盐组成。
碳酸氢盐缓
冲溶液通常用于在生理pH范围内进行实验,如细胞培养、酶反应等,能够有效地维持稳定的pH值。
这三种标准缓冲溶液在生物化学、分子生物学和生物医学实验
中被广泛应用,能够提供稳定的pH环境,保证实验的准确性和可重
复性。
在实验设计和操作中,选择合适的缓冲溶液对于实验结果的
准确性和稳定性至关重要。
(完整)常用缓冲溶液常用浓度及pH范围

10。9—12。0
Na2HPO42O Mr=358.22
氯化钾-盐酸缓冲液(0.2mol/L)
1。0-2。2
氯化钾Mr=74.55
氯化钾-氢氧化钠缓冲液(0。2mol/L)
12.0—13.0
氯化钾Mr=74.55
邻苯二甲酸氢钾Mr=204.23
磷酸氢二钠-磷酸二氢钠缓冲液(0.2mol/L)
5。8-8.0
Na2HPO4·2H2O Mr=178。05
Na2HPO4·12H2O Mr=358。22
NaH2PO4·H2O Mr=138。01
NaH2PO4·2H2O Mr=156.03
磷酸氢二钠-磷酸二氢钾缓冲液(1/15 molL)
柠檬酸-氢氧化钠—盐酸缓冲液
2.2—6。5
柠檬酸Mr=192。06
柠檬酸—柠檬酸钠缓冲液(0.1mol/L)
3.0—6。6
柠檬酸Mr=192.06
柠檬酸钠Mr=257.96
乙酸-乙酸钠缓冲液(0。2mol/L)
3。6-5.8
乙酸钠Mr=81。76
乙酸Mr=60。o5
邻苯二甲酸氢钾—氢氧化钠缓冲液
4.1-5.9
4。92-8.18
Na2HPO4·2H2O Mr=178。05
KH2PO4Mr=136.09
磷酸二氢钾-氢氧化钠缓冲液(0。05mol/L)
5。8—8.0
KH2PO4Mr=136。09
巴比妥钠—盐酸缓冲液(18℃)
6.8-9.6
巴比妥钠Mr=206。18
Tris-盐酸缓冲液(0.05mol/L25℃)
常用缓冲溶液常用浓度及pH范围
缓冲液名称及常用浓度
配制pH范围
各种缓冲液配制方法

各种缓冲液配制方法不同缓冲液的缓冲范围pH缓冲液是化学实验室中常用的一种试剂,可以帮助维持溶液的酸碱度。
下面介绍三种常用缓冲液的配制方法和缓冲范围。
一、甘氨酸-盐酸缓冲液(0.05 mol/L)配制方法:取X毫升0.2 mol/L甘氨酸和Y毫升0.2 mol/L 盐酸,加入适量的水稀释至200毫升。
缓冲范围:pH值在2.2至3.6之间,X和Y的取值见上表。
二、邻苯二甲酸-盐酸缓冲液(0.05 mol/L)配制方法:取X毫升0.2 mol/L邻苯二甲酸氢钾和Y毫升0.2 mol/L盐酸,加入适量的水稀释至20毫升。
缓冲范围:pH值在2.2至3.8之间,X和Y的取值见上表。
三、磷酸氢二钠-柠檬酸缓冲液配制方法:根据上表中的数据,取相应的0.2 mol/L和0.1 mol/L的Na2HPO4和柠檬酸,加入适量的水稀释至20毫升。
缓冲范围:pH值在2.2至8.0之间,具体取值见上表。
以上缓冲液的配制方法和缓冲范围可根据实验需要进行调整和改变。
在实验过程中,正确选择缓冲液可以提高实验的成功率和准确性。
以下是已经修改好的文章:柠檬酸的浓度可以用毫升表示,其浓度数据如下:9.28 mL8.85 mL8.40 mL7.91 mL7.37 mL6.78 mL6.15 mL5.45 mL4.55 mL3.53 mL2.61 mL1.83 mL1.27 mL0.85 mL0.55 mL对于Na2HPO4,其分子量为141.98,0.2 mol/L的溶液需要28.40 g/L。
而Na2HPO4·2H2O的分子量为178.05,0.2 mol/L的溶液需要35.61 g/L。
最后,Na2HPO4·12H2O的分子量为358.22,0.2 mol/L的溶液需要71.64 g/L。
对于C6H8O7·H2O,其分子量为210.14,0.1 mol/L的溶液需要21.01 g/L。
以下是柠檬酸-氢氧化钠-盐酸缓冲液的相关数据:pH: 2.2.3.1.3.3.4.3.5.3.5.8.6.5钠离子浓度(mol/L): 0.20.0.20.0.20.0.20.0.35.0.45.0.38柠檬酸(g) 氢氧化钠(g) 盐酸(mL)C6H8O7·H2O NaOH 97% HCl (浓)210 210 210210 245 285266 84 8383 144 186156 160 116106 45 68105 126最终体积(L):10使用时可以每升中加入1克酚。
常用缓冲溶液常用浓度及pH范围

Na2HPO4·2H2O Mr=178.05
KH2PO4 Mr=136.09
磷酸二氢钾-氢氧化钠缓冲液(0.05mol/L)
5.8-8.0
KH2PO4 Mr=136.09
巴比妥钠-盐酸缓冲液(18℃)
6.8-9.6
巴比妥钠Mr=206.18
Tris-盐酸缓冲液(0.05mol/L25℃)
磷酸氢二钠-氢氧化钠缓冲液
10.9-12.0
Na2HPO4·2H2O Mr=178.05
Na2HPO4·12H2O Mr=358.22
氯化钾-盐酸缓冲液(0.2mol/L)
1.0-2.2
氯化钾Mr=74.55
氯化钾-氢氧化钠缓冲液(0.2mol/L)
12.0-13.0
氯化钾Mr=74.55
邻苯二甲酸氢钾Mr=204.23
磷酸氢二钠-磷酸二氢钠缓冲液(0.2mol/L)=178.05
Na2HPO4·12H2O Mr=358.22
NaH2PO4·H2O Mr=138.01
NaH2PO4·2H2O Mr=156.03
磷酸氢二钠-磷酸二氢钾缓冲液(1/15 molL)
8.6-10.6
甘氨酸Mr=75.07
硼砂-氢氧化钠缓冲液(0.05mol/L)
9.3-10.1
硼砂Na2B4O7·10H2O Mr=381.43
碳酸钠-碳酸氢钠缓冲液(0.1mol/L)
9.16-10.83
碳酸钠Mr=286.2
碳酸氢钠Mr=84.0
碳酸钠-氢氧化钠缓冲液(0.025mol/L)
9.6-11.0
常用缓冲溶液常用浓度及pH范围
令狐采学
缓冲液名称及常用浓度
配制pH范围
常用pH缓冲溶液的配制和pH值

(一)溶液配制注意事项1.药品要有较好的质量试剂分为优级纯(保证试剂,Guaranteed reagent,G.R.)、分析试剂(Antalytical reagent,A.R.)化学纯(Chemical pure,C.P.)和实验试剂(Laboratory reagent,L.R.)等等。
工业用的化学试剂,杂质较多,只在个别情况下应用,如配洗液用的硫酸、配干燥剂的氯化钙等。
2.药品称量要精确。
3.配制试剂用水应用新鲜的去离子水或双蒸馏水,比电阻值在50万欧姆以上,pH在5.5~7.0之间才可应用,在组织培养等特殊用途时应注意此项要求,配制一般化验用溶液只要求用双蒸馏水或去离子水。
4.配好后的溶液,应立即除菌处理(如高压灭菌、抽滤或加抑菌物质),以防杂菌生长。
(二)0.067()Mol/L磷酸缓冲液1.磷酸二氢钾溶液的配制:称取磷酸二氢钾(KH2PO4,A.R.)9.08g,用蒸馏水溶解后,倾入1 000ml容量瓶内,再稀释至刻度(1000ml)。
2.1/15Mol/L磷酸二氢钠溶液的配制:称取无水磷酸氢二钠(Na2HPO4,A.R.)9.47g(或者Na2HPO4·2H2O11.87g)用蒸馏水溶解后,放入1 000ml容量瓶内,再加蒸馏水稀释至刻度(1 000ml)。
3.按附表的比例,配制成不同pH值的缓冲溶液。
附表1磷酸盐缓冲液配制法(单位:毫升)5.8 8.0 92.0 7.1 66.6 23.45.9 9.9 90.1 7.2 72.0 28.06.0 12.2 87.8 7.3 76.8 23.26.1 15.3 84.77.3 80.8 19.26.2 18.6 81.47.5 84.1 15.96.3 22.4 77.6 7.6 87.0 13.06.4 26.7 73.37.7 89.4 10.66.5 31.8 68.27.8 91.58.56.6 37.5 62.5 7.9 93.2 6.86.7 43.5 56.5 8.8 94.7 5.36.8 49.6 50.4 8.1 95.8 4.26.9 55.4 44.6 8.2 97.0 3.07.0 61.1 38.9 8.4 98.0 2.0(三)0.15Mol/L PB液附表2 0.15Mol/LPB液配制法pH 0.15Mol/L Na2HPO4(ml)0.15Mol/L NaH2PO4(ml)6.4 26.5 73.56.6 37.5 62.56.8 49.0 51.07.2 72.0 28.07.4 81.0 19.07.6 87.0 13.0Na2HPO4·2H2O分子量=175.05 0.15Mol/L溶液含26.7g/L。
ph缓冲剂

PH为3、4、5、6、7、8、9、10、11 缓冲液体系柠檬酸–柠檬酸钠缓冲液(50mmol/L)A液:称取柠檬酸10.5g溶于500ml蒸馏水中,制成50mmol/L柠檬酸作为母液备用。
B液:称取柠檬酸钠14.7g溶于500ml蒸馏水中,制成50mmol/L柠檬酸钠作为母液备用。
将以上两种溶液按以下比例量取:PH A液/ml B液/ml3 93 74 65.5 34.55 41 59磷酸盐缓冲液(50mmol/L)A液:称取二水磷酸二氢钠3.9g溶于500ml蒸馏水中,制成50mmol/L磷酸二氢钠作为母液备用。
B液:称取十二水磷酸氢二钠8.975g 溶于500ml蒸馏水中,制成50mmol/L 磷酸氢二钠作为母液备用。
将以上两种溶液按以下比例量取:PH A液/ml B液/ml6 87.7 12.37 39.0 61.08 5.3 94.7Tris-Hcl缓冲液(50mmol/L)PH 0.1 mol/LHCl(ml) 0.1 mol/LTris(ml)8.9 7.0 50.00.1 mol/LTris:称取1.211gTris溶于100ml蒸馏水中制成。
0.1 mol/LHCl:量取1ml浓盐酸(12mol/L)溶于119ml蒸馏水中制成。
将以上两种溶液按以上比例混合均匀后,加蒸馏水定容到100ml即可。
碳酸氢钠-氢氧化钠缓冲液(50mmol/L)A液:称取0.21g碳酸氢钠溶于50ml蒸馏水中制成50mmol/L碳酸氢钠作为母液备用。
B液:称取0.4g氢氧化钠溶于100ml蒸馏水中制成0.1mol/L氢氧化钠。
将以上两种溶液按以下比例量取:PH A液/ml B液/ml10 50 10.711 50 22.7以上两种溶液混合均匀后加水定容至100ml即可。
ph标准缓冲液

ph标准缓冲液PH标准缓冲液。
PH标准缓冲液是一种用于调节溶液酸碱度的重要试剂,广泛应用于生物化学、生物工程、医药等领域。
它能够稳定溶液的PH值,使实验结果更加准确可靠。
本文将介绍PH标准缓冲液的基本原理、常见类型及其应用。
一、基本原理。
PH标准缓冲液是一种能够在一定范围内稳定溶液PH值的溶液。
其基本原理是利用缓冲液中的酸碱成分对氢离子浓度进行调节,从而抵消外界对溶液PH值的影响。
当外界有酸或碱加入时,缓冲液能够吸收或释放氢离子,使溶液的PH值保持相对稳定。
这种稳定性对于许多生化实验至关重要,因为许多生物体内的酶活性、代谢等都对PH值非常敏感。
二、常见类型。
PH标准缓冲液根据PH值的不同分为多种类型,常见的有PH 4.01、PH 6.86、PH 7.00、PH 9.18等。
这些缓冲液分别适用于不同范围的PH值调节,可以满足实验室在不同领域的需求。
此外,还有一些特殊用途的缓冲液,比如在生物学实验中常用的PBS缓冲液,其PH值在7.2-7.6之间,适用于生物细胞的培养和实验。
三、应用。
PH标准缓冲液在生物化学、生物工程、医药等领域有着广泛的应用。
在生物化学实验中,常常需要调节溶液的PH值以适应不同的实验条件,比如酶活性的测定、蛋白质的结晶等。
在生物工程领域,培养基的PH值对于细胞培养和发酵过程至关重要,PH标准缓冲液能够帮助维持培养基的稳定性。
在医药领域,一些药物的稳定性和溶解性也与PH值密切相关,因此PH标准缓冲液也被广泛应用于药物研发和生产过程中。
综上所述,PH标准缓冲液作为一种重要的试剂,在生物化学、生物工程、医药等领域发挥着重要作用。
它的稳定性和准确性对于实验结果的可靠性至关重要,因此在实验中的选择和使用需要特别注意。
希望本文能够帮助您更好地了解PH标准缓冲液的基本原理、常见类型及其应用,为您的实验工作提供一些帮助。
常用pH缓冲液配置方法及注意事项

常用pH缓冲液配置方法及注意事项常用pH缓冲溶液的配制和pH值序号溶液名称配制方法pH值1氯化钾-盐酸13.0 ml 0.2 mol/L HCl 与25.0 ml 0.2 mol/L KCl混合均匀后,加水稀释至100 ml1.72氨基乙酸-盐酸在500 ml 水中溶解氨基乙酸150 g,加480 ml浓盐酸,再加水稀释至1L2.33一氯乙酸-氢氧化钠在200 ml 水中溶解2 g 一氯乙酸后,加40 g NaOH,溶解完全后再加水稀释至1 L2.84邻苯二甲酸氢钾-盐酸把25.0 ml 0.2 mol/L的邻苯二甲酸氢钾溶液与6.0 ml0.1 mol/L HCl混合均匀,加水稀释至100 ml3.65邻苯二甲酸氢钾-氢氧化钠把25.0 ml 0.2 mol/L的邻苯二甲酸氢钾溶液与17.5ml 0.1 mol/L NaOH混合均匀,加水稀释至100 ml4.86六亚甲基四胺-盐酸在200 ml水中溶解六亚甲基四胺40 g,加浓HCl 10 ml,再加水稀释至1 L5.47磷酸二氢钾-氢氧化钠把25.0 ml 0.2 mol/L的磷酸二氢钾与23.6 ml 0.1mol/L NaOH混合均匀,加水稀释至100 ml6.88硼酸-氯化钾-氢氧化钠把25.0 ml 0.2 mol/L的硼酸-氯化钾与4.0 ml 0.1mol/L NaOH 混合均匀,加水稀释至100 ml8.09氯化铵-氨水把0.1 mol/L 氯化铵与0.1 mol/L 氨水以2:1比例混合均匀9.110硼酸-氯化钾-氢氧化钠把25.0 ml 0.2 mol/L 的硼酸-氯化钾与43.9 ml 0.1mol/L NaOH混合均匀,加水稀释至100 ml10.011氨基乙酸-氯化钠-氢氧化钠把 49.0 ml 0.1 mol/L 氨基乙酸-氯化钠与51.0 ml0.1 mol/L NaOH混合均匀11.612磷酸氢二钠-氢氧化钠把 50.0 ml 0.05 mol/L Na2HPO4与26.9 ml 0.1 mol/L NaOH 混合均匀,加水稀释至100 ml12.013氯化钾-氢氧化钠把 25.0 ml 0.2 mol/L KCl与66.0 ml 0.2 mol/L NaOH混合均匀,加水稀释至100 ml13.0一、常用溶液的配制(一)溶液配制注意事项1.药品要有较好的质量试剂分为优级纯(保证试剂,Guaranteed reagent,G.R.)、分析试剂(Antalytical reagent,A.R.)化学纯(Chemical pure,C.P.)和实验试剂(Laboratory reagent,L.R.)等等。
化学分析常用缓冲试剂和探头保护液配制
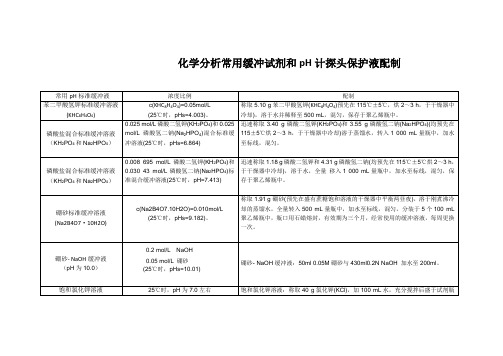
化学分析常用缓冲试剂和pH计探头保护液配制常用pH标准缓冲液浓度比例配制苯二甲酸氢钾标准缓冲溶液(KHC8H4O4) c(KHC8H4O4)=0.05mol/L(25℃时,pHs=4.003)。
称取5.10 g苯二甲酸氢钾(KHC8H4O4)预先在115℃±5℃,烘2~3 h,于干燥器中冷却),溶于水并稀释至500 mL,混匀,保存于聚乙烯瓶中。
磷酸盐混合标准缓冲溶液(KH2PO4和Na2HPO4)0.025 mol/L磷酸二氢钾(KH2PO4)和0.025mol/L磷酸氢二钠(Na2HPO4)混合标准缓冲溶液(25℃时,pHs=6.864)迅速称取3.40 g磷酸二氢钾(KH2PO4)和3.55 g磷酸氢二钠(Na2HPO4)(均预先在115±5℃烘2~3 h,于干燥器中冷却)溶于蒸馏水,转入1 000 mL量瓶中,加水至标线,混匀。
磷酸盐混合标准缓冲溶液(KH2PO4和Na2HPO4)0.008 695 mol/L磷酸二氢钾(KH2PO4)和0.030 43 mol/L磷酸氢二钠(Na2HPO4)标准混合缓冲溶液(25℃时,pH=7.413)迅速称取1.18 g磷酸二氢钾和4.31 g磷酸氢二钠(均预先在115℃±5℃烘2~3 h,于干燥器中冷却),溶于水,全量移入1 000 mL量瓶中,加水至标线,混匀,保存于聚乙烯瓶中。
硼砂标准缓冲溶液(Na2B4O7·10H2O) c(Na2B4O7.10H2O)=0.010mol/L(25℃时,pHs=9.182)。
称取1.91 g硼砂(预先在盛有蔗糖饱和溶液的干燥器中平衡两昼夜),溶于刚煮沸冷却的蒸馏水,全量转入500 mL量瓶中,加水至标线,混匀。
分装于5个100 mL聚乙烯瓶中,瓶口用石蜡熔封,有效期为三个月,经常使用的缓冲溶液,每周更换一次。
硼砂- NaOH缓冲液(pH为10.0)0.2 mol/L NaOH0.05 mol/L 硼砂(25℃时,pHs=10.01)硼砂- NaOH缓冲液:50ml 0.05M硼砂与430ml0.2N NaOH 加水至200ml。
标准缓冲液pH值与温度对照表
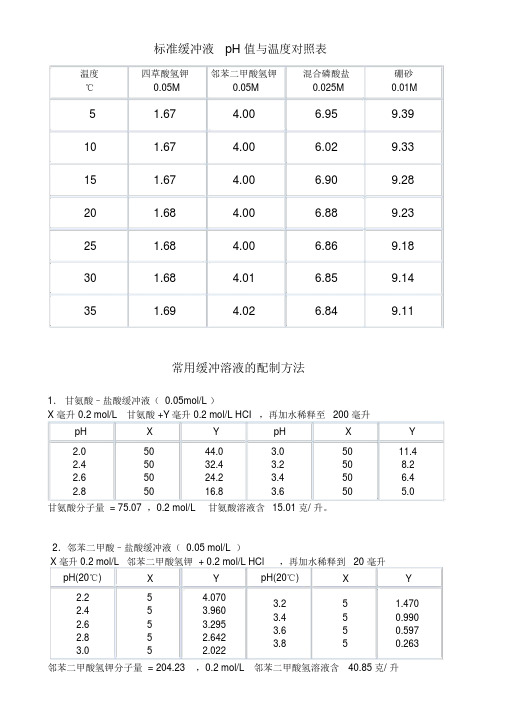
标准缓冲液pH 值与温度对照表温度四草酸氢钾邻苯二甲酸氢钾混合磷酸盐硼砂℃0.05M0.05M0.025M0.01M5 1.67 4.00 6.959.3910 1.67 4.00 6.029.3315 1.67 4.00 6.909.2820 1.68 4.00 6.889.2325 1.68 4.00 6.869.1830 1.68 4.01 6.859.1435 1.69 4.02 6.849.11常用缓冲溶液的配制方法1.甘氨酸–盐酸缓冲液( 0.05mol/L )X 毫升 0.2 mol/L甘氨酸 +Y毫升 0.2 mol/L HCI,再加水稀释至200 毫升pH X Y pH X Y2.05044.03.05011.42.45032.43.2508.22.65024.23.450 6.42.85016.83.650 5.0甘氨酸分子量 = 75.07 ,0.2 mol/L甘氨酸溶液含15.01 克/ 升。
2.邻苯二甲酸–盐酸缓冲液( 0.05 mol/L )X 毫升 0.2 mol/L邻苯二甲酸氢钾 + 0.2 mol/L HCl,再加水稀释到20 毫升pH(20℃)X Y pH(20℃)X Y2.25 4.0703.25 1.4702.453.9603.450.9902.653.2953.650.5972.85 2.6423.850.2633.05 2.022邻苯二甲酸氢钾分子量 = 204.23,0.2 mol/L邻苯二甲酸氢溶液含40.85 克/ 升3.磷酸氢二钠–柠檬酸缓冲液0.2mol/L0.1mol/L0.2mol/L0.1mol/LpH Na2HPO4柠檬酸pH Na2HPO4柠檬酸(ml)(ml)(ml)(ml)2.20.4010.60 5.210.729.282.4 1.2418.76 5.411.158.852.6 2.1817.82 5.611.608.402.83.1716.83 5.812.097.913.04.1115.896.012.637.373.24.9415.066.213.22 6.783.4 5.7014.30 6.413.85 6.153.6 6.4413.56 6.614.555.453.87.1012.90 6.815.454.554.07.7112.297.016.47 3.534.28.2811.727.217.39 2.614.48.8211.187.418.17 1.834.69.3510.657.618.73 1.274.89.8610.147.819.150.855.010.309.708.019.450.55 Na2HPO4分子量 = 142.98,0.2 mol/L溶液为 28.40克/ 升。
常用pH缓冲液配置方法及注意事项
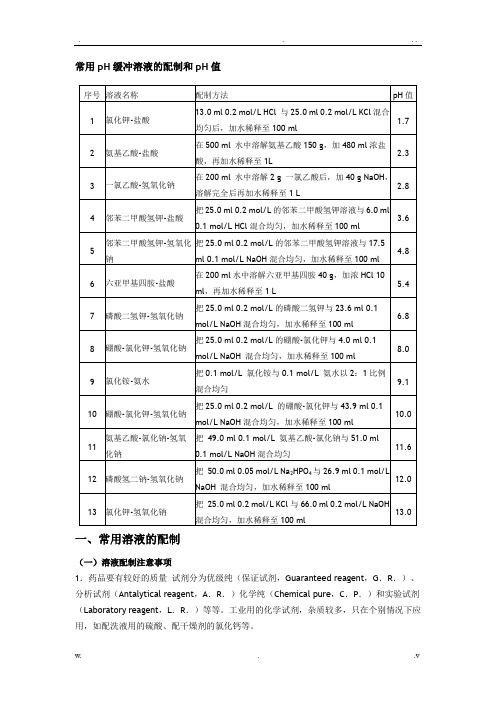
常用pH缓冲溶液的配制和pH值一、常用溶液的配制(一)溶液配制注意事项1.药品要有较好的质量试剂分为优级纯(保证试剂,Guaranteed reagent,G.R.)、分析试剂(Antalytical reagent,A.R.)化学纯(Chemical pure,C.P.)和实验试剂(Laboratory reagent,L.R.)等等。
工业用的化学试剂,杂质较多,只在个别情况下应用,如配洗液用的硫酸、配干燥剂的氯化钙等。
2.药品称量要精确。
3.配制试剂用水应用新鲜的去离子水或双蒸馏水,比电阻值在50万欧姆以上,pH在5.5~7.0之间才可应用,在组织培养等特殊用途时应注意此项要求,配制一般化验用溶液只要求用双蒸馏水或去离子水。
4.配好后的溶液,应立即除菌处理(如高压灭菌、抽滤或加抑菌物质),以防杂菌生长。
(二)0.067(1/15)Mol/L磷酸缓冲液1.1/15Mol/L磷酸二氢钾溶液的配制:称取磷酸二氢钾(KH2PO4,A.R.)9.08g,用蒸馏水溶解后,倾入1000ml容量瓶内,再稀释至刻度(1000ml)。
2.1/15Mol/L磷酸二氢钠溶液的配制:称取无水磷酸氢二钠(Na2HPO4,A.R.)9.47g(或者Na2HPO4·2H2O 11.87g)用蒸馏水溶解后,放入1000ml容量瓶内,再加蒸馏水稀释至刻度(1000ml)。
3.按附表的比例,配制成不同pH值的缓冲溶液。
(三)0.15Mol/L PB液Na2HPO4·2H2O分子量=175.05 0.15Mol/L溶液含26.7g/L。
Na2HPO4·12H2O分子量=358.22 0.15Mol/L溶液含53.7g/L。
NaH2PO4·H2O分子量=138.00 0.15Mol/L溶液含20.7g/L。
NaH2PO4·2H2O分子量=156.03 0.15Mol/L溶液含23.4g/L。
最全常用缓冲液配方及缓冲范围

最全常用缓冲液配方及缓冲范围缓冲液是一种能够帮助控制溶液酸碱性的化学物质,它可以通过接受或释放氢离子来防止溶液的pH值发生剧烈变化。
缓冲液在许多科学实验、生物学研究、工业生产以及医药领域中都有广泛应用。
常用的缓冲液配方包括以下几种:1.乙二胺四乙酸(EDTA)缓冲液:EDTA缓冲液是一种用来稳定金属离子浓度、防止金属离子的沉淀和垢痕形成的缓冲液。
其配方如下:-0.1MEDTA(乙二胺四乙酸)溶液10mL- 0.2 M Tris-HCl缓冲液(pH 8.0) 90 mL-蒸馏水900mL2.乙醇胺缓冲液:乙醇胺缓冲液通常用于DNA或RNA的电泳和杂交实验中。
其配方如下:-1M乙醇胺9mL-0.5MEDTA1mL-蒸馏水90mL将乙醇胺缓冲液通过添加适量的盐酸来调节pH值至所需的范围。
3.乙二醇缓冲液:乙二醇缓冲液常用于蛋白质的纯化和储存过程中。
其配方如下:-0.2M乙二醇10mL- 0.1 M Tris-HCl 缓冲液(pH 7.0) 90 mL按需添加其他添加剂如蛋白酶抑制剂或抗菌剂。
4.磷酸盐缓冲液:磷酸盐缓冲液是一种常用的生物学缓冲液,适用于酶反应、DNA/RNA杂交等实验。
常用的三种pH值的配方如下:-pH5.8:0.05MNa2HPO4溶液和0.05MNaH2PO4溶液的体积比为1:4-pH7.0:0.1MNa2HPO4溶液和0.1MNaH2PO4溶液的体积比为1:9-pH8.0:0.2MNa2HPO4溶液和0.2MNaH2PO4溶液的体积比为1:95.PBS缓冲液:PBS缓冲液是一种常用的生物学缓冲液,适用于细胞培养、免疫染色、蛋白质浸泡实验等。
其配方如下:-8gNaCl-0.2gKCl-1.44gNa2HPO4-0.24gKH2PO4-蒸馏水1L将以上成分溶解在蒸馏水中,调节pH至7.4这些缓冲液可以满足大多数实验和应用的需求,每种缓冲液的最佳使用范围可能略有不同。
在实验前应该仔细阅读相关文献,了解所使用缓冲液的特点和最适宜的pH范围。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
资料]常用pH缓冲溶液的配制和pH值
常用pH缓冲溶液的配制和pH值
常用pH缓冲溶液的配制和pH值
一、常用溶液的配制
(一)溶液配制注意事项
1.药品要有较好的质量试剂分为优级纯(保证试剂,Guaranteed reagent,
G.R.)、分析试剂(Antalytical reagent,A.R.)化学纯(Chemical pure,C.P.)和实验试剂(Laboratory reagent,L.R.)等等。
工业用的化学试剂,杂质较多,只在个别情况下应用,如配洗液用的硫酸、配干燥剂的氯化钙等。
2.药品称量要精确。
3.配制试剂用水应用新鲜的去离子水或双蒸馏水,比电阻值在50万欧姆以上,pH在5.5~7.0之间才可应用,在组织培养等特殊用途时应注意此项要求,配制一般化验用溶液只要求用双蒸馏水或去离子水。
4.配好后的溶液,应立即除菌处理(如高压灭菌、抽滤或加抑菌物质),以防杂菌生长。
(二)0.067(1/15)Mol/L磷酸缓冲液
1.1/15Mol/L磷酸二氢钾溶液的配制:称取磷酸二氢钾(KH
2PO
4
,A.R.)9.08g,
用蒸馏水溶解后,倾入1 000ml容量瓶内,再稀释至刻度(1 000ml)。
2.1/15Mol/L磷酸二氢钠溶液的配制:称取无水磷酸氢二钠(Na
2HPO
4
,A.R.)
9.47g(或者Na
2HPO
4
·2H
2
O 11.87g)用蒸馏水溶解后,放入1 000ml容量瓶内,
再加蒸馏水稀释至刻度(1 000ml)。
3.按附表的比例,配制成不同pH值的缓冲溶液。
附表1 磷酸盐缓冲液配制法(单位:毫升)
(三)0.15Mol/L PB液
附表2 0.15Mol/LPB液配制法
Na 2HPO 4·2H 2O 分子量=175.05 0.15Mol/L 溶液含26.7g/L 。
Na 2HPO 4·12H 2O 分子量=358.22 0.15Mol/L 溶液含53.7g/L 。
NaH 2PO 4·H 2O 分子量=138.00 0.15Mol/L 溶液含20.7g/L 。
NaH 2PO 4·2H 2O 分子量=156.03 0.15Mol/L 溶液含23.4g/L 。
(四)0.2Mol/L PB 缓冲液 附表3 0.2mol/L PB 缓冲液配制法
0.2Mol/L Na 2HPO 4·2 H 2O 溶液35.61g/L
Na 2HPO 4·12 H 2O 溶液含71.64g/L
0.2Mol/LNaH 2PO 4·H 2O 溶液含27.60g/L
NaH 2PO 4·2 H 2O 溶液含31.21g/L
欲配0.1Mol/L PB 缓冲液则在0.2Mol/L PB 缓冲液的基础上加H 2O 稀释1倍即可。
欲配制PBS 液时,则在溶液中加0.85%的NaCl 溶液即可。
(五)无钙镁离子磷酸缓冲盐水(PBS )
(0.15Mol/L PH 7.2)
NaCl 8.0g KCl 0.2g Na 2HPO 4 1.15g
(如为Na 2HPO 4·12H 2O ,则为2.89g )
KH 2PO 4 0.2g
将上述试剂依次溶于1 000ml 去离子水中,完全溶解后,115℃高压灭菌10min~15min ,存在4℃冰箱中备用。
此液可用于配制和稀释细胞分散剂以及洗
涤细胞培养物。
(六)硼酸盐缓冲液(Borate saline buffer )
1.硼酸(H3BO 3)
0.2Mol/L 硼酸:硼酸12.37g 加水至1 000ml 。
2.硼砂(Na 2B 4O 7)
0.05Mol/L 硼砂:硼砂19.07g 加水至1 000ml 。
附表4 不同pH 的0.2Mol/L 硼酸缓冲液配制法
(七)巴比妥缓冲液
1.pH8.2离子强度0.05Mol/L巴比妥缓冲液
巴比妥钠 47.6g
蒸馏水 3 000ml
1.17N HCl 55.0ml
(1.17 N HCl=193ml浓HCl加1 807ml蒸馏水)
⑴ 将4.76g巴比妥钠溶于3 000ml蒸馏水。
⑵ 加1.17 N HCl 55ml。
⑶ 用HCl调节pH到8.2,并加蒸馏水至4 265ml。
2.pH8.4 0.06Mol/L巴比妥缓冲液
巴比妥 1.84g
巴比妥钠 10.30g
加蒸馏水至 1 000.00ml
3.pH8.6 0.06Mol/L巴比妥缓冲液
巴比妥 1.66g
巴比妥钠 12.76g
加蒸馏水 1 000.00ml
(八)0.2Mol/L醋酸盐缓冲液见表附表5
附表5 0.2Mol/L醋酸盐缓冲液配制法
(九)三羟甲基甲烷—盐酸缓冲液(Tris—HCl缓冲液)
不同pH,0.05Mol/L
25ml0.2Mol/L三羟甲基氨基甲烷加хml0.1NHCl,加水稀释至100ml(见下表)
附表6 Tris—HCl缓冲液配制法
三羟甲基氨基甲烷(Tris)
分子量=121.14
0.2Mol/L三羟甲基氨基甲烷:Tris24.23g,加水至1 000ml。
0.1NHCl:取HCl8.6ml,加水至1 000ml。
(十)0.5Mol/L pH9.5碳酸盐缓冲液
NaHCO
3
3.70g
Na
2CO
3
0.60g
溶于600.00ml蒸馏水中即得。
不用时塞紧瓶塞,以免吸收空气中二氧化碳使PH下降。
最好小量配制。
(十一)甘油磷酸缓冲液
1.配制pH8.0磷酸缓冲液
0.1Mol/L Na
2HPO
4
94.50ml
0.1N NaH
2PO
4
5.50ml
混合即可
2.9份甘油与1份pH8.0磷酸缓冲液混合,即为甘油磷酸缓冲液。
用途:用于免疫荧光试验。
(十二)Hank’s 液
1.贮存液 NaCl 80.00g KCl 4.00g Na 2HPO 4·12 H 2O 1.52g
KH 2PO 4 0.60g 葡萄糖 4.00g 0.4%酚红液 50.00ml 双馏水加至 100.00ml 115℃高压灭菌15min ,冰冻保存。
2.工作液 贮存液 1份 双馏水 9份
115℃高压灭菌15min 。
临用时用灭菌的5.6%NaHCO 3液调pH 值至7.2左右(溶
液呈橙红色)。
(十三)萘(钠)氏试剂(Nessler’s reagent)
配方1:氯化汞 6.0g
碘化钾 12.4g 20%NaOH 30ml 加蒸馏水至 100ml 配方2:碘化汞 11.5g
碘化钾 8g
蒸馏水 50ml
(完全溶解后)过滤,加20%NaOH 50ml。
用途:检测溶液中氨离子。
(十四)阿氏(Alsever’s)液
葡萄糖 2.05g
柠檬酸钠 0.80g
氯化钠 0.42g
蒸馏水 100ml
溶解后,以10%柠檬酸调节pH至6.1,过滤,分装,10磅10min灭菌,4℃保存。
(十五)青、链霉素混合液(简称S.P.液或双抗液)
青霉素(40万U) 5支
链霉素(200万μg) 1支
分别溶于100ml灭菌无离子水中或共同溶于200ml灭菌无离子水中,混合后分装小瓶,置-10℃~-20℃冰箱保存备用(1万单位μg/ml)。
临用时,按1%的量加入营养液或其他溶液中,最后浓度是青霉素100U/ml,链
霉素100ug/ml。
(十六)洗液(清洁液)
配方1:重铬酸钾 150g
蒸馏水 300ml
浓硫酸 3 000ml
将重铬酸钾加入蒸馏水中,使之自然溶解或水浴溶解,亦可在大坩埚中加热溶解,然后慢慢加入浓硫酸,边加边搅拌,见发热过剧则稍停,冷却后再继续加。
此为强洗液。
盛清洁液的容器要坚固,上加厚玻璃盖,操作时要穿橡皮围裙、长统胶靴、戴
上眼镜和厚胶皮手套,以保安全。
洗液一旦变绿,表示铬酸已经还原,失去了氧化能力,不宜再用。
如将这样洗液加热,再加适量重铬酸钾,又可重新使用。
配方2:浓硫酸 50%
蒸馏水 50%
重铬酸钾 5%
此为中等强度洗液。
配方3:重铬酸钾 100g
蒸馏水 1 000ml
加热溶解,冷却后缓慢加入
工业硫酸 100ml
此液为弱洗液,为棕红色。
使用此液时,必须预先用热肥皂水将玻璃器皿洗净,经自来水冲洗,沥干然后才能浸入,否则该洗液很快失效。
