软件测试文档集模板(医疗器械)
医疗器械 软件验证报告(模板) (1)

ScanKey()
全局数据结构,SERVER 在运行时系统该数据结 构一直有效,相关单元初 始化顺序是否合理,是否 完成初始化功能 依次按每个按键,看是否 能达到预期的效果
3.5.1. 3
3.5.1. 4
3.5.1. 5
屏幕显 示
A 路输出
B 路输出
依据需求,可 以显示系统 信息,参数, 运行状态
第 2 页 共 14 页
3. 软件需求规格
3.1 硬件需求
MCU:STM8S105c4t6 显示屏:LCD 显示 外设器件:A 探头、B 探头、探头连接线 IO 设备:不适用
3.2 编程工具需求
编程语言: C 语言 编译器 ST Visual Develop 编程调试工具: ST-Link/V2
确认
通过软件的需 求分析规格参 数确认
结 论
风险降 低
代码逻辑 不清晰程 序执行有 错误
功能不能达到预期需求, 代码没有谨慎 1.详细的模块设计.
对疗效有影响
编写
2.通过流程图来编写代码
通过软件设计 风 险 降 流程图来确定 低
不完整的 信息显示
用户看到不完整的信息, 屏幕显示部分 仔细进行代码设计,进行单 参考
1. 软件描述和操作需求
1.1 软件信息
版本号: 1.0 日期:
1.2 软件分类
软件控制生命支持或者维持 设备
不 控制传递有害的 能量
是
控制治疗传递
软件失效会引起死亡 或者严重损害吗?
不
提供诊断信息作为治疗的基 础
不
软件失效会引起不严重 损害吗?
不 是
提供重要的监护
符号
不
更高分类等级考虑
软件不直接作用于人体,当参数错误的时候,会导致激光功率不正常,所以我们把软件分类为 B
医疗器械软件描述模板
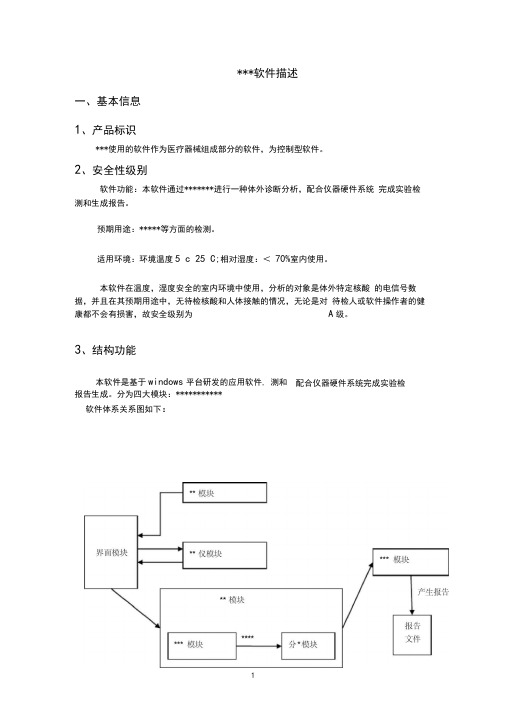
***软件描述一、基本信息1、产品标识***使用的软件作为医疗器械组成部分的软件,为控制型软件。
2、安全性级别软件功能:本软件通过*******进行一种体外诊断分析,配合仪器硬件系统完成实验检测和生成报告。
预期用途:*****等方面的检测。
适用环境:环境温度5 c 25 C;相对湿度:<70%室内使用。
本软件在温度,湿度安全的室内环境中使用,分析的对象是体外特定核酸的电信号数据,并且在其预期用途中,无待检核酸和人体接触的情况,无论是对待检人或软件操作者的健康都不会有损害,故安全级别为A级。
3、结构功能本软件是基于windows平台研发的应用软件, 测和配合仪器硬件系统完成实验检报告生成。
分为四大模块:***********软件体系关系图如下:4、 硬 件关系软件系统通过路由器连接PC 机和测试塔,将测试数据返回PC 机器,并通过路由 器进行实时通讯,通过PC 机控制测试塔进行相应操作。
5、 运 行环境Windows Xp sp3(32 位) Visual studio 2008 .Net framework 2.0 无 无 网络环境:以太6、 适 用范围本软件需与 *** 系统配套使用,主要用于分析设备仪器返回的数据并产生报 告。
7、 禁 忌症无。
8、 上 市历史经查询,目前市面上暂无同类产品(包含本软件组件)批准上市。
二、 实现过程1、 开 发综述开发语言: C#.net开发工具: 1)支持软件 Visual Studio 2008 ; 2)应用软件:无 开发方法: 面向对象生存周期模型: 瀑布模型开发人员数量: 1开发时间: 7 个月工作量: 7 月 / 人代码行总数: 40497控制文档总数:软件环境:1) 、系统软2、风险管理详见资料4《安全风险分析管理报告》。
3、需求规格详情见”D** 系统需求规格书.doc”。
4、生存周期本软件开发采用瀑布模型方式进行开发。
首先进行项目立项,经过调研分析,确认方案后,再进行开发设计,设计完成后进行配置测试和缺陷管理。
软件测试文档集模板医疗器械

XXXX医学科技有限公司产品名称:xxxx系统产品型号:XTM300软件版本:V1.0.0.0文档版本:A/0软件测试文档集文档制订:xxx文档审核:xxx测试执行:xxx文档签发:xxx发布日期:2016.3.1目录1. 测试过程概述1.1 测试任务 (3)1.2 参加测试人员 (3)1.3 测试时间 (3)1.4 测试环境 (3)1.4.1 硬件环境 (3)1.4.2 软件环境 (4)2.测试内容&测试计划2.1 测试内容 (4)2.2 通过-失败准则 (4)2.3 测试方案····································4-52.3 测试用例·····································5-83.测试异常情况报告 (8)4. 测试结论 (8)5.术语表····································8-91. 测试过程概述1.1 测试任务和目的本次测试主要是遵循GB/T25000.51-2010的要求,测试xxxxxxxx 系统与该标准的符合性。
医疗器械软件确认报告模板

软件确认报告
编制/日期:_____________
审核/日期:_____________
批准/日期:_____________
一、引言
1.1 目的:
通过测试报告反馈及时解决由程序中的错误引发的问题。
适用于XX治疗仪,型号XX
1.2 背景:
软件系统的名称:
任务提出者:
开发者:
本系统包括XX治疗仪嵌入式软件系统。
1.3 参考资料:
1)软件需求说明书
2)软件详细设计说明
3)产品使用说明书
4)技术要求
5)软件验证报告
二、测试方法
参考《系统测试报告》
三、测试机构和人员
测试机构:
测试人员:
四、测试记录、分析统计
五、测试结果
六、评价
6.1 软件能力:
软件能力达到《软件需求说明书》规定的能力要求;
软件相关的产品性能符合技术要求。
6.2 缺陷和限制:
无明显缺陷
6.3 建议:
无
6.4 测试结论:
经测试,软件功能符合产品设计要求,判定合格。
如何编制医疗器械软件描述文档(附模板)

据CFDA 2015年8月5日发布的《国家食品药品监督管理总局关于发布医疗器械软件注册技术审查指导原则的通告(2015年第50号)》所有包含软件的第二类、第三类医疗器械产品,软件开发方式无论是自主开发、部分采用现成软件和全部采用现成软件,均应在首次注册时提交软件描述文档。
软件描述文档的详略程度、条款要求均因安全性级别和开发方式的不同而有所差异。
1.针对自主研发的医疗器械软件,软件描述文档包括基本信息、实现过程和核心算法(详见附件)。
2.部分采用现成软件对于部分采用现成软件的方式,三种安全性级别的现成软件的要求相同,制造商均应在软件描述文档相应条款中描述(详见表1)。
3.全部采用现成软件对于全部采用现成软件的方式,三种现成软件的要求有所不同:(1)成品软件:制造商应提供外购合同复印件或声明、软件描述文档(不适用条款说明理由),成品软件如已在中国上市提供注册证复印件;(2)遗留软件:制造商应提供遗留软件证明性文件(如YY/T 0664或IEC 62304实施之前的注册证或上市批书复印件)、软件描述文档(不适用条款说明理由)、上市后临床评价资料;(3)外包软件:制造商应提供外包合同复印件或声明、软件描述文档(不适用条款说明理由)。
1.基本信息1.1产品标识软件名称:型号:版本号:制造商:生产地址:1.2安全性级别明确软件安全性级别(A级、B级、C级),详述确定理由。
1.3结构功能本软件是基于Windows平台研发的应用于PC平台的软件,包含XXXXXXXXXX等X个部分。
1.3.1软件体系结构图:1.3.2用户界面关系图1.3.3功能描述:1.3.3.1XXXX模块功能描述1.3.3.2XXXX模块功能描述1.3.4外部接口1.4硬件关系1.4.1物理拓扑图:1.4.2关系描述:1.5运行环境1.5.1网络布局1.5.2服务器硬件配置1.5.3客户端配置要求1.6适用范围1.7禁忌症1.8注册历史中国情况:国外情况:2.实现过程2.1开发综述开发语言:开发工具:管理工具:开发人员数量:开发时间:工作量:代码行总数:控制文档总数:2.2风险管理详见资料8《安全风险分析管理报告》2.3需求规范详见《软件需求说明书》。
医疗器械软件研究模板【范本模板】

医疗器械软件描述文档1.基本信息1.1.产品标识软件名称:软件型号:软件版本号:软件制造商:软件生产地址:1.2.安全性级别软件的安全性级别为A/B/C级.理由如下:a)软件的预期用途为:b)软件的功能包括:c)如果软件失效,可能导致以下后果(按软件各功能失效逐条描述,如果软件失效的时候由硬件降低失效后果或危害发生概率,可以做说明,并由此降低安全性级别):1)……2)……3)……1.3.结构功能1.3.1.组成模块、各模块功能及模块相互关系依据软件设计规格给出体系结构图(如图1.3-1所示)。
嵌入式软件(SDS)体系结构图——示例1独立式软件(SDS)体系结构图—-示例2图1。
3-1 XXX体系结构图1.3.2各模块功能说明注:1、每个软件模块一份表单。
2、软件功能项目列表需列出与测试相关的所有功能(包括各级子功能).3、功能说明栏目应填写:功能项目概述、边界值规定(数据有效性)、安全说明等信息。
4、功能列表上所列出来的功能必须是可以实现或演示的。
5、功能名称与软件、文档保持一致。
6、软件功能项目列表根据需要列出(可增加或删减子功能列)。
1.3.2.用户界面设计采用广泛应用的图形用户界面(GUI),即诸如窗口、菜单、对话框、滚动条等。
用户主界面见图1。
3—2.图1.3—2 XXX用户主界面1.3.3.外部接口XXX可使用VISUAL C++ 提供的对SQL SERVER 的接口,进行对数据库的所有访问。
XXX可使用SQL SERVER 的对数据库的备分命令,以做到对数据的保存。
在网络软件接口方面,使用一种无差错的传输协议,采用滑动窗口方式对数据进行网络传输及接收.1.4.硬件关系1.4.1.物理拓扑图嵌入式软件物理拓扑关系表格形式——示例1硬件软件分类零件种类功能显示部分血压显示7工具LED 血压值显示最高血压・最低血压、脈拍を表示时刻显示7工具LED 時刻显示显示现在时刻压力单位显示LED mmHg / kPa 显示显示血压值以及压力值的单位开关部分开始/关闭开关开始/关闭开关读取控制开始测量血压测量时停止测量背面功能设定开关背面功能设定开关读取控制时刻的设定等、主机功能设定的更改打印部分打印切纸打印控制测量结果的打印、打印后切纸血压测量部分泵、电磁阀、压力传感器血压测定控制测量时加压、减压控制、脉搏信号处理以及测量值的确定安全监视用压力传感器压力安全检测控制压力监测、急排控制袖带驱动部分袖带驱动用马达袖带控制袖带的卷曲、固定、开放语音部分扬声器语音控制测量通知外部进出力部串行通信串行进出力测量结果出力、指令输入记忆存储U盘设定值记忆存储控制功能设定内容的保持嵌入式软件物理拓扑关系表格形式——示例2独立式软件物理拓扑关系表格形式--示例3图1。
医疗器械软件标准测试

医疗器械软件标准测试本文作者任海萍女士,博士、国家食品药品监督管理局中检所医疗器械质量监督检验中心;奚廷斐先生,主任、研究员、博士生导师,中国生物医学工程学会常务理事、生物材料分会主任委员,人工器官分会副主任委员,全国医疗器械生物学评价标准化技术委员会主任委员;汤京龙先生,助理研究员;王硕先生、王建宇先生,实习研究员;陆颂芳女士,主任技师。
关键词: 医疗器械软件标准测试一概述随着计算机技术的发展,越来越多的医用电气设备中使用了计算机软件技术,其安全性是非常重要的,而它的复杂性超过了那些单纯的治疗和/或诊断医用电气设备。
同时,越来越多的软件被用于在医疗监视下对患者进行诊断、治疗或监护。
医疗器械的许多重要功能,越来越多地依靠软件进行控制,因此,医疗器械中软件错误导致的后果可能非常严重。
而软件产品可能在六个月内就已经过时了。
从而,在医疗器械生产企业和管理部门之间存在着矛盾:生产企业必须尽快使新的含软件器械上市,但同时,管理部门必须保护公众免受与软件相关的器械故障造成的危害。
2003年开始,我国国家食品药品监督管理局将相关软件纳入了医疗器械管理。
软件质量已成为大家共同关注的焦点。
由于我国目前医疗器械管理的技术基础主要是产品的第三方测试,因此,软件测试是否充分、有效,直接影响到软件产品的质量,也影响着是否能够对医疗器械软件进行有效管理。
但是,由于软件产品的特殊性,我国至今尚未形成医疗器械软件产品测试的国家标准和行业标准。
本文通过对美国FDA的医疗器械软件管理、软件工程以及软件测试情况的介绍,希望能为我国加强医疗器械软件的管理、尽快制定技术标准提供参考。
二软件的特殊性美国FDA对于作为医疗器械组件、部件或附件的软件、本身就是医疗器械的软件(例如模拟重建血管系统软件)、加工制造医疗器械时使用的软件(例如加工器械时使用的逻辑控制程序)以及器械制造商在质控系统中所使用的软件(例如记录和保存器械历史记录的软件)都根据其特定的使用要求进行验证。
医疗器械用软件设计模板

医疗器械用软件设计模板1. 引言本文档旨在提供医疗器械用软件设计的模板和指导,以确保设计的合规性和可靠性。
医疗器械软件的设计过程应参照相关法规和标准,以确保产品的安全性和有效性。
2. 软件需求分析在软件设计之前,需要进行充分的需求分析,确定软件的功能和性能要求。
需求分析应包括以下步骤:- 定义软件的用途和目标;- 确定用户需求和期望;- 确定适用的法规和标准;- 定义软件的功能和界面要求;- 确定性能和可靠性要求。
3. 系统架构设计系统架构设计是将软件分解为不同模块和组件的过程。
在医疗器械软件设计中,需考虑以下因素:- 系统的可扩展性和可维护性;- 分层架构设计,确保模块的独立性;- 实时性和响应性的要求。
4. 数据流图设计数据流图是描述系统流程和数据传输的图形工具。
在医疗器械软件设计中,数据流图需要考虑以下因素:- 合规性和隐私保护;- 数据的准确性和一致性;- 数据传输的安全性。
5. 界面设计用户界面是用户与软件进行交互的平台,设计良好的用户界面能提高用户体验。
在医疗器械软件设计中,界面设计应注重以下方面:- 易用性和易读性;- 考虑用户的特殊需求和能力;- 考虑界面的安全性。
6. 数据库设计数据库设计是为了存储和管理软件中的数据。
在医疗器械软件设计中,数据库设计需要考虑以下因素:- 数据的安全性和保密性;- 数据的完整性和可靠性;- 合规性要求。
7. 软件测试和验证软件测试和验证是确保软件的正确性和合规性的过程。
在医疗器械软件设计中,需要进行以下测试和验证:- 单元测试和集成测试;- 功能测试和性能测试;- 需求追踪和验证。
8. 结论本文档提供了一份医疗器械用软件设计的模板和指导,从需求分析到测试验证,完整了解了医疗器械软件设计的过程和关键要点。
在实际设计中,应参照相关法规和标准,并根据具体需求进行适当的调整和优化。
只有合规和可靠的软件设计才能确保医疗器械的安全和有效使用。
---Please let me know if you need any further assistance.。
医疗器械 软件标准 测试

医疗器械软件标准测试本文作者任海萍女士,博士、国家食品药品监督管理局中检所医疗器械质量监督检验中心;奚廷斐先生,主任、研究员、博士生导师,中国生物医学工程学会常务理事、生物材料分会主任委员,人工器官分会副主任委员,全国医疗器械生物学评价标准化技术委员会主任委员;汤京龙先生,助理研究员; 王硕先生、王建宇先生,实习研究员; 陆颂芳女士,主任技师。
关键词: 医疗器械软件标准测试一概述随着计算机技术的发展,越来越多的医用电气设备中使用了计算机软件技术,其安全性是非常重要的,而它的复杂性超过了那些单纯的治疗和/或诊断医用电气设备。
同时,越来越多的软件被用于在医疗监视下对患者进行诊断、治疗或监护。
医疗器械的许多重要功能,越来越多地依靠软件进行控制,因此,医疗器械中软件错误导致的后果可能非常严重。
而软件产品可能在六个月内就已经过时了。
从而,在医疗器械生产企业和管理部门之间存在着矛盾: 生产企业必须尽快使新的含软件器械上市,但同时,管理部门必须保护公众免受与软件相关的器械故障造成的危害。
2003年开始,我国国家食品药品监督管理局将相关软件纳入了医疗器械管理。
软件质量已成为大家共同关注的焦点。
由于我国目前医疗器械管理的技术基础主要是产品的第三方测试,因此,软件测试是否充分、有效,直接影响到软件产品的质量,也影响着是否能够对医疗器械软件进行有效管理。
但是,由于软件产品的特殊性,我国至今尚未形成医疗器械软件产品测试的国家标准和行业标准。
本文通过对美国FDA的医疗器械软件管理、软件工程以及软件测试情况的介绍,希望能为我国加强医疗器械软件的管理、尽快制定技术标准提供参考。
二软件的特殊性美国FDA对于作为医疗器械组件、部件或附件的软件、本身就是医疗器械的软件(例如模拟重建血管系统软件)、加工制造医疗器械时使用的软件(例如加工器械时使用的逻辑控制程序)以及器械制造商在质控系统中所使用的软件(例如记录和保存器械历史记录的软件)都根据其特定的使用要求进行验证。
医疗器械软件测试计划标准模板

测试计划开发单位:Prepared by Date 拟制日期Reviewed by Date 评审人日期Approved by Date批准日期修订记录文档修改记录目录1引言 (5)1.1测试目的 (5)1.2标识 (5)1.3系统概述 (5)1.4文档概述 (5)2引用文件 (5)3术语 (6)4软件测试环境 (6)5测试策略 (6)6测试用例格式规范 (10)6.1编号规则 (10)6.2测试用例记录 (10)7 测试规程 (10)7.1测试准备 (10)7.2测试执行 (10)7.3停止准则 (11)7.4回归测试 (11)7.5争议处理 (11)8人员与职责 (11)9测试进度安排 (12)10总结阶段 (12)10.1编写测试报告 (12)10.2测试工作总结 (12)10.3测试验收 (12)10.4测试归档 (12)1引言1.1测试目的本文档是依照用户文档集的要求制定的系统测试计划,此开发计划编写的目的使整个测试工作有序进行,指导测试人员的工作,为测试提供依据。
提供系统化、规范化、工程化、实用化的测试技术规范,尽早发现故障。
1.2标识文档标识:软件名称:1.3系统概述1.4文档概述本文档是依照《软件与软件工程软件与软件质量要求和评价(SQuaRE)第51部分:就绪可用软件产品(RUSP)的质量要求和测试细则》标准中对测试文档集的要求以及软件测试计划的要求。
它标识了测试项、需测试的特性、测试任务、任务负责人、测试环境、测试设计技术、测试的进入和退出准则和选择的合理性等。
本文档的读者为测试人员、开发人员、项目管理者。
系统测试阶段,测试工作必须依照本文档执行。
本文档属于保密文件。
2引用文件3术语测试环境:执行测试用例所必需的硬件和软件配置。
测试目标:在规定的的条件下,待测量的已标识的软件特征的集合,它通过将实际的行为与要求的行为进行比较而测量。
测试计划:说明预期的测试活动的范围、途径、资源和进度的文档。
医疗器械软件测试计划标准模板

测试计划开发单位:Prepared by Date 拟制日期Reviewed by Date 评审人日期Approved by Date批准日期修订记录文档修改记录目录1引言 (5)1.1测试目的 (5)1.2标识 (5)1.3系统概述 (5)1.4文档概述 (5)2引用文件 (5)3术语 (6)4软件测试环境 (6)5测试策略 (6)6测试用例格式规范 (10)6.1编号规则 (10)6.2测试用例记录 (10)7 测试规程 (10)7.1测试准备 (10)7.2测试执行 (10)7.3停止准则 (11)7.4回归测试 (11)7.5争议处理 (11)8人员与职责 (11)9测试进度安排 (12)10总结阶段 (12)10.1编写测试报告 (12)10.2测试工作总结 (12)10.3测试验收 (12)10.4测试归档 (12)1引言1.1测试目的本文档是依照用户文档集的要求制定的系统测试计划,此开发计划编写的目的使整个测试工作有序进行,指导测试人员的工作,为测试提供依据。
提供系统化、规范化、工程化、实用化的测试技术规范,尽早发现故障。
1.2标识文档标识:软件名称:1.3系统概述1.4文档概述本文档是依照《软件与软件工程软件与软件质量要求和评价(SQuaRE)第51部分:就绪可用软件产品(RUSP)的质量要求和测试细则》标准中对测试文档集的要求以及软件测试计划的要求。
它标识了测试项、需测试的特性、测试任务、任务负责人、测试环境、测试设计技术、测试的进入和退出准则和选择的合理性等。
本文档的读者为测试人员、开发人员、项目管理者。
系统测试阶段,测试工作必须依照本文档执行。
本文档属于保密文件。
2引用文件3术语测试环境:执行测试用例所必需的硬件和软件配置。
测试目标:在规定的的条件下,待测量的已标识的软件特征的集合,它通过将实际的行为与要求的行为进行比较而测量。
测试计划:说明预期的测试活动的范围、途径、资源和进度的文档。
医疗器械验证报告模板

医疗器械验证报告模板英文回答:Medical Device Verification Report Template.Introduction.The purpose of this template is to provide a standardized format for documenting the verification of a medical device. Verification is a process of assessing whether the medical device meets its specified requirements. The template includes sections for identifying the medical device, the verification activities performed, and the results of the verification activities.Section 1: Medical Device Identification.Device Name:Device Model Number:Manufacturer:Serial Number:Date of Manufacture:Software Version (if applicable): Section 2: Verification Activities. Test Procedure:Test Equipment:Test Results:Acceptance Criteria:Pass/Fail:Section 3: Verification Results.Summary of Verification Activities: Conclusions:Recommendations:Section 4: Signatures.Verifier:Date:Quality Assurance Representative: Date:中文回答:医疗器械验证报告模板。
软件测试文档集模板(医疗器械)

XXXX医学科技有限公司产品名称:xxxx系统产品型号:XTM300软件版本:V1.0.0.0文档版本:A/0软件测试文档集文档制订:xxx文档审核:xxx测试执行:xxx文档签发:xxx发布日期:2016.3.1目录1. 测试过程概述1.1 测试任务 (3)1.2 参加测试人员 (3)1.3 测试时间 (3)1.4 测试环境 (3)1.4.1 硬件环境 (3)1.4.2 软件环境 (4)2.测试内容&测试计划2.1 测试内容 (4)2.2 通过-失败准则 (4)2.3 测试方案····································4-52.3 测试用例·····································5-83.测试异常情况报告 (8)4. 测试结论 (8)5.术语表····································8-91. 测试过程概述1.1 测试任务和目的本次测试主要是遵循GB/T25000.51-2010的要求,测试xxxxxxxx 系统与该标准的符合性。
医疗器械软件描述文档模板
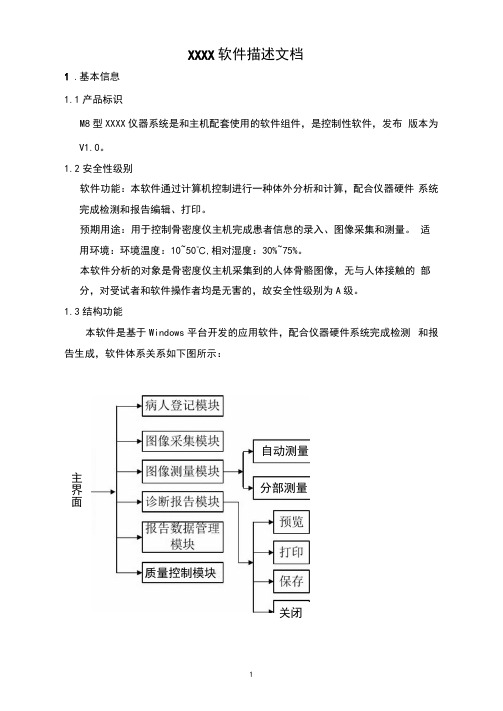
XXXX 软件描述文档1 .基本信息1.1 产品标识M8型XXXX 仪器系统是和主机配套使用的软件组件,是控制性软件,发布 版本为V1.0。
1.2 安全性级别软件功能:本软件通过计算机控制进行一种体外分析和计算,配合仪器硬件 系统完成检测和报告编辑、打印。
预期用途:用于控制骨密度仪主机完成患者信息的录入、图像采集和测量。
适用环境:环境温度:10~50℃,相对湿度:30%~75%。
本软件分析的对象是骨密度仪主机采集到的人体骨骼图像,无与人体接触的 部分,对受试者和软件操作者均是无害的,故安全性级别为A 级。
1.3 结构功能本软件是基于Windows 平台开发的应用软件,配合仪器硬件系统完成检测 和报告生成,软件体系关系如下图所示:主界面关闭 分部测量 自动测量质量控制模块电源适配器 1. 5运行环境 1. O. 1硬件配置 CPU : Intel Celeron 2. 0G 以上; 内存:2G 以上; 硬盘:200 GB 以上; 显示器:15寸液晶显示器以上。
1. 5. 2软件环境 中文Windows 7系统以上,无必要支持性软件。
1. 5. 3网络条件 无。
1.6适用范围 1.6.1 适用范围:用于通过对XXXXXXXX,评估患者骨骼及邻近组织的骨密度和矿 物质含量,供临床诊断用。
1.6 . 2禁忌症:儿童和孕妇。
1.7 注册历史 1.4硬件关系信号板1主控板详见硬件拓扑图本软件是M8型XXXX仪器的软件组件,为首次注册。
2.实现过程1.1开发综述本软件构件采用VC++语言进行开发、开发工具为Visual Studio 2010:开发方法为面向对象的结构化开发,通过与硬件配合来验证功能和测试准确性;开发人员为3人;首次开发时间为1个月,修正和维护时间为6个月;软件开发总工作量为3人210天2.2风险管理本软件是G3型数字化双能X射线骨密度仪的软件组件,风险管理内容详见注册资料8.风险分析资料。
医疗器械软件开发全套文档模板(含软件风险管理、软件测试等)

医疗器械-软件开发描述文档文档目录软件基本信息 (2)软件实现过程 (6)软件风险管理报告 (16)软件集成测试计划 (25)系统测试计划 (27)用户软件测试计划 (41)软件基本信息产品名称:1、产品标识:2、安全性级别××是一种××软件,所以随之而来的软件安全性问题也极为重要。
(a) ××软件是一种抽象的逻辑产品,其存在形式是虚拟和动态的……..(b) 软件质量的测度十分困难,其质量的控制重点在软件的需求分析和设计阶段,开发过程中产生错误的难以追踪;……;(c) 硬件有老化现象,失效曲线似浴盆,硬件的维护可通过纠错、修复或更换失效的系统重新恢复功能。
而软件的维护复杂,只有通过修改代码来排错。
同时软件可能在使用中随着缺陷的发现和消除,而使性能提高。
软件的修改看似比硬件容易,却比硬件更难于控制。
看上去无关紧要的软件代码修改会在软件的其他地方引起无法预测的、十分关键的问题;(d) 软件的失效防护困难。
对硬件可采用预防性维护技术预防故障,采用断开失效部件的办法诊断故障,而软件则不能采用这些技术;但软件的失效会毫无征兆的出现,会因执行一条未经验证的路径而出现故障;而同一软件的冗余不能提高可靠性。
(e) 软件的失效是系统性失效,其失效的条件有时比较复杂。
因此,可能会无法清晰地洞察其原因,而误归结其为系统中硬件的随机失效。
导致无法及时排除软件中的故障,造成隐患的长期存在。
以上论述了××软件的复杂性,以及出现问题无法预测性和软件的实效防护困难。
××软件一旦出现问题则很可能导致患者×××或者对患者造成严重的伤害,例如,×××软件一旦在运行过程中失效,机器停止工作则很可能导致患者由于××而变为×××,所以××软件安全性级别为××级。
医疗器械-软件设计和开发-验证报告-模板范例

医疗器械软件设计开发验证报告记录编号:目录第一部分总则 (2)一、概述 (2)二、验证方案 (2)1、验证目的 (2)2、验证范围 (2)3、相关文件 (2)4、职责 (2)5、验证条件 (3)6、验证方法 (3)7、验证合格标准及评价分析 (7)8、验证实施计划 (7)9、验证周期 (8)10、数据收集 (8)第二部分测试确认 (8)一、功能性测试: (8)二、性能测试: (9)三、可靠性和安全性测试 (9)四、用户场景测试 (9)五、准确性测试 (10)1 普通碱基测试 (10)2 修饰碱基测试 (16)3 兼并碱基测试 (53)4 含RNA碱基测试 (59)5 含mRNA碱基测试 (63)6 含特殊碱基I序列测试 (65)7 含特殊碱基U序列测试 (67)第三部分结论 (70)第一部分总则一、概述本次验证严格按照验证方案要求实施,整个过程稳定可控,验证过程没有出现偏差,Filemaker 的各项性能符合相关规定。
二、验证方案1、验证目的通过验证以证明使用Filemaker软件设计的Filemaker数据库系统在适用性、准确性、稳定性、可控性、安全性和保密性方面可以满足公司质量管理体系和用户的要求与需要。
2、验证范围使用Filemaker软件设计的以下功能模块:Filemaker.fp73、相关文件4、职责4.1 验证委员会负责验证方案的审批;负责验证的协调工作,以保证本验证方案规定项目的顺利实施;负责验证数据及结果的审核;负责验证报告的审批。
验证委员会名单:4.2 验证小组负责验证方案的起草、修改;负责组织本验证方案的实施;负责验证数据的统计、分析、审核,报验证委员会审核;负责验证报告的编写,并报验证委员会。
验证小组名单:5、验证条件●Filemaker Server Advance 9.2,数据库托管服务器端;●Windows Server 2003,数据库托管服务器端操作系统;●Filemaker Pro 11.0,数据库客户端;●Windows XP,数据库客户端操作系统;●Internet Explorer 7.0,Web Publishing 访问客户端。
医疗器械用软件确认模板

医疗器械用计算机软件确认报告1.1 软件描述软件名称: 软件版本: 软件厂商: 1.2 主要功能CRM 、供应链、生产创造、人力资源等。
本方案是为了确认软件安装的有效性、符合性,通过完整的安装、测试,以确认该系统的安装 后的各项性能符合相关要求。
本确认的范围是包含软件及其关联设备、设施。
4.2计划验证时间按照验证主计划,本系统计划验证时间为:文件名称 软件操作说明编码 26.1 GB/T19001—ISO9001 质量体系设计、开辟、生产、安装和服务质量保证模式 6.2 GB/T19000.3—ISO9000-3 软件开辟、供应和维护中的使用指南 6.3 GB8566—88 《计算机软件开辟规范》注释计算机控制系统验证设定值 实际值 印刷电路板缩写 CSV SV PV PCB验证职责负责对验证小组成员进行本方案的培训;负责本方案的实施,负责跟踪所有偏差缺陷均已整改;验证报告的生成、审核和批准,以便对该方案进行最终 批准。
负责起草验证方案和报告; 按验证方案实施验证, 采集、 整理验证数据,完成验证记录和报告。
执行前确认方案已批准,并经过培训;参预验证偏差的调查和处理,确认通过偏差修订和解决 方案;确认验证过程中的变更在实施前已经批准。
验证职务组长组员组员所在部门总经办技术部IT姓名8.1 培训方案审批后,由验证起草人员对方案实施过程中涉及人员进行培训,以保证方案顺利实施,并 做好培训记录,培训记录见附表表(一)。
8.2 安装确认程序 8.2.1 安装文件检查核对相应的安装说明书或者手册文件、使用说明书是否存在。
8.2.2 安装环境、条件确认依据说明书要求配置相关电源、主机、显示器、及其他附属设备设施。
8.3.3 安装确认执行说明书安装步骤,执行安装过程。
并注意过程中的排错记录。
9.1 偏差、漏项、变更说明对验证中的偏差、漏项、变更进行说明。
9.2 评价和建议根据验证结果进行评价和建议。
9.3 报告审核和批准对报告进行审核和批准输入/输出 人机界面 设计确认 安装确认 运行确认 性能确认 不间断电源I/O OIP DQ IQ OQ PQ UPS培训项目:软件确认方案培训培训内容:软件确认方案、软件的使用操作方法姓名部门及职务培训人培训结果编制人/日期:附件二:一、确认目的1 、确认软件安装的准确性;2 、确认安装条件是否符合要求。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
XXXX医学科技有限公司
产品名称:xxxx系统
产品型号:XTM300
软件版本:V1.0.0.0
文档版本:A/0
软件测试文档集
文档制订:xxx
文档审核:xxx
测试执行:xxx
文档签发:xxx
发布日期:2016.3.1
目录
1. 测试过程概述
1.1 测试任务 (3)
1.2 参加测试人员 (3)
1.3 测试时间 (3)
1.4 测试环境 (3)
1.4.1 硬件环境 (3)
1.4.2 软件环境 (4)
2.测试内容&测试计划
2.1 测试内容 (4)
2.2 通过-失败准则 (4)
2.3 测试方案····································4-5
2.3 测试用例·····································5-8
3.测试异常情况报告 (8)
4. 测试结论 (8)
5.术语表····································8-9
1. 测试过程概述
1.1 测试任务和目的
本次测试主要是遵循GB/T25000.51-2010的要求,测试xxxxxxxx 系统与该标准的符合性。
1.2 参加测试人员
1.3 测试时间
2016年3月1日
1.4 测试环境
1.4.1 硬件环境
CPU:四核2.0 GH以上内存:8G以上
显卡:独立显卡1G以上
显示器:支持 1280*1024以上,32 位真彩显示
硬盘:500G以上光驱:CD-ROM(24X)
1.4.2 软件环境
操作系统:Window 7 以上 64Bit 或更新版本
2.测试说明&测试计划
2.1 测试内容
对于xxxxxxxx系统的以下全部功能的测试:
1)GB25000.52-2010中5.3的要求
2)xxxx 功能 3)xxxx功能
4)xxxx功能 5)xxxx功能
2.2 通过-失败准则
如果软件的测试按照2.4测试用例的执行步骤进行测试未出现异常则即测试通过,否则测试失败。
2.3 测试计划
2.4 测试用例
3. 测试异常情况报告
按照2.2的测试计划对xxxxxxxx系统对软件进行测试,暂未发现异常。
4. 测试结论
通过以上2.4测试用例测试全部项目合格,软件测试通过。
5. 术语表。
