物理化学第五章化学平衡小结
化学平衡知识小结

化学反应速率及化学平衡知识小结华北油田第三中学石建辉一、影响化学反应速率的因素及其影响结果内因:反应物的性质外因:浓度↗,v↗;压强↗,v↗(气体);温度↗,v↗;催化剂,v↗(正催化剂),S固体表面积↗,v↗。
其它(超声波,放射线,电磁波,,扩散速率,溶剂等)注意:改变压强只有引起反应物浓度变化才能引起速率变化。
二、影响化学平衡移动的因素及影响结果:勒沙特列原理(平衡移动原理):浓度:在其它条件不变的情况下,增大反应物的浓度或减小生成物的浓度,平衡向正反应方向移动;反之向逆反应方向移动压强:在其它条件不变的情况下,增大压强会使平衡向气体系数和缩小的方向移动;减小压强平衡向气体系数和增大的方向移动;注意:①对于气体系数和不变的反应来说,改变压强平衡不移动;②若平衡混合物都是固体或液体,改变压强平衡也不移动;③压强变化必须改变了反应物浓度引起了正、逆反应速率不再相等,才能使平衡移动。
温度:在其它条件不变时,升高温度平衡向吸热方向移动;降低温度平衡向放热方向移动。
(温度改变时,平衡一般都要移动)催化剂:同等程度改变正逆反应速率,故不影响平衡移动,但可改变达到平衡的时间。
三、1、增大某一反应物浓度,平衡向正反应方向移动,与原平衡比较:生成物浓度增大,其他反应物浓度减小,转化率增大,而此反应物浓度增大,转化率减小。
(举一反四)2、恒温恒容通入不反应气体,虽然压强增大,但反应混合物的浓度不变,化学反应速率不变,则化学平衡不移动。
3、恒温恒压通入不反应气体,体积增大,反应混合物各组分的浓度均减小,相当于减小压强,平衡向气体系数和增大的方向移动四、等效平衡:1、无论恒温恒压还是恒温恒容,只要起始原料量相当,达到相同平衡。
即达到平衡时各组分的量不变,各组分的浓度不变,各组分的百分含量不变。
2、恒温恒压时,起始原料量成比例增加或减少,达到平衡时各组分的量成比例增加或减少,各组分的浓度不变,各组分的百分含量不变。
3、恒温恒容时,对于反应前后气体系数和不变的反应,起始原料量成比例增加或减少,达到平衡时各组分的量成比例增加或减少,各组分的浓度成比例增加,各组分的百分含量不变。
化学平衡知识点总结

化学平衡知识点总结我给你讲讲化学平衡这事儿。
化学平衡啊,就像是一场在微观世界里的拔河比赛,两边的队伍都有自己的力量。
我就这么瞅着那些分子、原子,它们在那反应容器里啊,乱哄哄的,可又有着自己的规矩。
我记得我刚开始学化学平衡的时候,那老师啊,戴着个厚厚的眼镜,镜片后面的眼睛总是瞪得大大的,像两颗铜铃。
他站在讲台上,拿着粉笔在黑板上“嘎吱嘎吱”地写着那些方程式,一边写还一边说:“都看好了啊,这化学平衡就像你们在操场上排队,两边的人数得差不多,要是一边人太多了,那就不平衡了。
”我当时就想啊,这分子原子又不是人,咋还排队呢?化学平衡有个概念叫可逆反应,这就像两个人在吵架,你一句我一句,谁也不服谁。
反应正向进行着,可同时啊,逆向也在偷偷进行。
比如说氮气和氢气合成氨这个反应,氮气和氢气就像两个急性子的小伙子,想凑到一块儿变成氨,可是氨呢,又像个不安分的小家伙,时不时地又想变回氮气和氢气。
这反应啊,就在这正反应和逆反应之间找平衡,就像在走钢丝一样,小心翼翼的。
平衡常数K可是个关键的东西,就像是这个反应的一个标准。
我当时算这个平衡常数啊,那脑袋都大了。
你看,那些物质的浓度在方程式里进进出出的,就像一群调皮的小鬼在捣乱。
我就跟同桌说:“这化学平衡咋这么麻烦呢?这平衡常数就像个密码,我怎么都解不开。
”同桌就笑我:“你就慢慢算呗,像数钱一样仔细点儿。
”我一听就来气了:“这能跟数钱比吗?数钱多开心,算这个我脑袋都快炸了。
”还有啊,影响化学平衡的因素那可不少。
温度、压强、浓度,这些就像是外界的干扰因素。
就像一群人在安静地做着自己的事儿,突然来了几个捣乱的。
温度升高或者降低,就像天气突然变热或者变冷,那些分子原子的活动就不一样了。
压强呢,就像有人在外面使劲儿推这个反应容器,里面的分子原子就得重新调整自己的位置。
浓度要是变了,那就像有新的队员加入或者有队员离开拔河比赛,两边的力量就不平衡了,反应就得向着重新平衡的方向进行。
我曾经做实验的时候,看到那些颜色变化啊,就像是在看一场魔术表演。
化学平衡知识点总结

化学平衡知识点总结化学平衡是化学反应中的一个重要概念,它描述了化学反应的正向和逆向反应达到平衡时的状态。
在化学平衡中,反应物与生成物的浓度或压力保持恒定,但反应仍然在进行。
以下是一些关于化学平衡的知识点的总结。
1. 平衡常数(K):平衡常数是描述化学平衡状态的一个量,它的值取决于反应物和生成物之间的物质浓度或气体压力的比例。
平衡常数越大,说明反应在正向方向上偏向生成物;反之,平衡常数越小,说明反应在逆向方向上偏向反应物。
2. 反应商(Q):反应商是在任意反应条件下的反应物和生成物的浓度或压力比值。
当反应商等于平衡常数(Q=K)时,化学反应处于平衡状态;当反应商小于平衡常数(Q3. 影响平衡的因素:化学平衡受到温度、浓度或压力、催化剂等因素的影响。
通过改变这些因素,可以改变反应的正向和逆向速率,从而改变反应的平衡位置。
4. 改变浓度或压力:通过改变反应物或生成物的浓度或压力,可以影响平衡位置。
加入更多的反应物会使反应偏向生成物,而加入更多的生成物则会使反应偏向反应物。
这是基于浓度对反应速率的影响的。
对于气体反应,增加压力会使反应偏向物质量较少的一侧,而减小压力则会使反应偏向物质量较多的一侧。
5. 温度的影响:改变温度可以改变平衡常数的值。
在一些反应中,增加温度会使平衡常数增大,反应偏向生成物;而在其他反应中,增加温度会使平衡常数减小,反应偏向反应物。
这是因为反应的平衡常数受到温度的影响,不同反应具有不同的温度依赖性。
6. 催化剂的作用:催化剂是一种可以加速化学反应速率的物质。
催化剂对反应的速率没有影响,但可以降低反应物质的活化能。
催化剂的存在可以改变化学平衡状态的时间尺度,但不能改变化学平衡位置。
综上所述,化学平衡是化学反应中重要的概念之一。
了解化学平衡的基本知识和影响因素对于理解和控制化学反应过程具有重要意义。
对于实际应用中涉及平衡反应的问题,我们可以通过改变浓度、压力和温度等条件,来控制反应的平衡位置和速率,以满足实际需求。
化学平衡知识点总结

化学平衡知识点总结化学平衡是化学反应过程中产物和反应物浓度达到一定比例后的状态。
在平衡状态下,反应物和产物的浓度不再改变,但反应仍在进行。
化学平衡的基本概念:1. 反应速率的相互制约:在化学反应中,反应物分子之间发生相互碰撞并形成产物,反应速率取决于反应物浓度。
当反应速率达到最大值时,产物与反应物浓度之间将建立一个平衡,并保持恒定。
2. 动态平衡:化学平衡是一个动态过程,指在反应物和产物浓度不再变化的情况下,反应仍然进行,反应物转化为产物的速率等于产物转化为反应物的速率。
化学平衡的标志:1. 反应速率不再改变:在平衡状态下,反应物和产物的浓度不再改变,反应速率不再提高或降低。
2. 可逆反应:化学反应可以进行正向和逆向两个方向的转化。
平衡状态下,正向反应速率等于逆向反应速率。
化学平衡的平衡常数:1. 平衡常数:平衡常数(K)是描述化学反应系统达到平衡时反应物和产物浓度之间的关系,它的大小决定了反应的进行方向和倾向性。
平衡常数等于正向反应的浓度乘积与逆向反应浓度乘积的比值,取决于温度。
2. 平衡常数的影响因素:平衡常数受温度的影响,温度升高将导致平衡常数的增大或减小;反应物或产物浓度的变化也会改变平衡常数的数值。
化学平衡的移动方式:1. 影响平衡常数的移动方式:通过改变反应物或产物的浓度,可以影响平衡的移动方向,使反应向产物方向移动或向反应物方向移动。
2. 改变浓度对平衡的影响:增加反应物浓度、减少产物浓度或减少反应物浓度、增加产物浓度,都会导致反应偏离平衡,达到新的平衡状态。
化学平衡的影响因素:1. 温度的影响:温度升高通常会导致平衡常数的增大,反应向生成热量较大的方向移动。
2. 压力的影响:对涉及气体的反应,改变压力会改变反应物和产物之间的分布,但对于涉及气体和溶液的反应,改变压力的影响较小。
3. 浓度的影响:增加反应物浓度将使反应向产物方向移动,减少反应物浓度将使反应向反应物方向移动。
4. 催化剂的影响:催化剂可以提高反应速率,但不会改变平衡常数。
化学平衡移动规律总结

化学平衡移动规律总结化学反应是物质转化的过程,而化学平衡则是在反应物和生成物浓度达到一定比例时的状态。
化学平衡的移动规律是指在一定条件下,平衡位置如何随着外界条件的改变而发生变化的规律。
下面将从温度、压力、浓度和催化剂四个方面来总结化学平衡的移动规律。
一、温度影响在化学反应中,温度的改变会影响反应物和生成物的速率以及平衡位置。
根据Le Chatelier定律,当温度升高时,反应速率会增加。
对于吸热反应,升高温度会使平衡位置向右移动,生成物浓度增加;而对于放热反应,升高温度会使平衡位置向左移动,生成物浓度减少。
二、压力影响在气相反应中,压力的改变对平衡位置有一定影响。
根据Le Chatelier定律,当压力增加时,平衡位置会向反应物浓度较小的一侧移动,以减少压力。
对于反应物和生成物摩尔数相等的反应,压力的改变不会影响平衡位置。
而对于摩尔数不相等的反应,压力的增加会使平衡位置向摩尔数较小的一侧移动。
三、浓度影响在溶液中的反应中,溶液浓度的改变会导致平衡位置的移动。
根据Le Chatelier定律,当浓度增加时,平衡位置会向生成物浓度较小的一侧移动,以减少浓度差。
而当浓度减少时,平衡位置会向生成物浓度较大的一侧移动,以增加浓度差。
四、催化剂影响催化剂可以加速化学反应的速率,但不参与反应。
催化剂的加入不会改变平衡位置,因为它同样影响反应物和生成物的速率。
催化剂提供了一个更低的活化能路径,使反应更容易进行,但并不改变反应的平衡位置。
化学平衡的移动规律可以通过调节温度、压力和浓度来实现。
根据Le Chatelier定律,当这些条件发生改变时,平衡位置会向着减少影响的一侧移动,以达到新的平衡状态。
催化剂的加入可以提高反应速率,但不会改变平衡位置。
这些规律的理解和应用对于理解和控制化学反应过程具有重要意义。
化学平衡移动的总结

化学平衡移动的总结化学平衡是化学反应过程中,反应物与生成物浓度达到一定比例时的一种状态。
在这种状态下,反应物与生成物的浓度之间的比值保持不变,称为平衡常数。
化学平衡的移动是指改变化学平衡条件,使得反应物与生成物的浓度发生变化。
本文将对化学平衡移动进行总结,包括影响化学平衡移动的因素以及如何通过改变这些因素来移动平衡。
一、影响化学平衡移动的因素1. 温度:温度是影响化学平衡移动的重要因素之一。
根据Le Chatelier原理,当反应放热时,提高温度会使平衡向反应物一侧移动,反之则向生成物一侧移动。
这是因为提高温度会增加反应物的动能,促使反应向吸热方向进行,从而使平衡移动。
2. 压力(或浓度):对于气体反应,压力的改变会影响化学平衡的移动方向。
当压力增加时,平衡会向压力较小的一侧移动,以减小压力。
而对于溶液反应,则可以通过改变浓度来移动平衡。
增加反应物浓度会使平衡向生成物一侧移动,反之亦然。
3. 物质的添加或去除:向平衡体系中添加或去除某种物质,会导致平衡移动。
当某种物质被添加到平衡体系中时,平衡会向减少该物质的一侧移动,以恢复平衡。
而当某种物质被去除时,平衡会向补充该物质的一侧移动。
二、移动化学平衡的方法1. 温度控制:通过改变温度,可以移动化学平衡。
例如,对于放热反应,可以通过提高温度来向生成物一侧移动平衡;对于吸热反应,则可以通过降低温度来移动平衡。
2. 压力(或浓度)控制:对于气体反应,可以通过改变压力来移动平衡。
增加压力会使平衡向压力较小的一侧移动,减小压力则相反。
对于溶液反应,可以通过改变浓度来移动平衡。
增加反应物浓度会使平衡向生成物一侧移动,减小反应物浓度则相反。
3. 物质的添加或去除:通过向平衡体系中添加或去除物质,可以移动平衡。
添加某种物质会使平衡向减少该物质的一侧移动,去除某种物质则相反。
三、案例分析1. 铵氨水的制备:铵氨水(氨水和铵盐的混合物)可以通过以下反应制备:NH3(g) + H2O(l) ⇌ NH4OH(aq)在该反应中,平衡向生成物一侧移动。
(完整版)化学平衡知识点总结,推荐文档

“”建议收藏下载本文,以便随时学习!+ O22H O2HmA(g) + nB(g) pC(g) + qD(g)nB(g) pC(g)我去人也就有人!为UR扼腕入站内信不存在向你偶同意调剖沙mA(g) + nB(g) pc(g) + qD(g) + (【总结】增大反应物浓度或减小生成物浓度,化学平衡向正反应方向移动;减小反应物浓度或增大生成物浓度,化学平衡向逆反应方向移动。
增大压强,化学平衡向系数减小的方向移动;减小压强,平衡会向系数增大的方向移动。
升高温度,平衡向着吸热反应的方向移动;降低温度,平衡向放热反应的方向移动。
催化剂不改变平衡移动的方向移动。
平衡移动原理对所有的动态平衡都适用,如对后面将要学习的电离平衡,水解平衡也适用。
五、有关化学平衡的计算1、主要类型有:①求起始浓度、转化浓度、平衡浓度。
②求某反应物的转化率、平衡气体混合物中各成分的体积分数等。
2、化学平衡的计算模式—三段式法设a(mol·L-1)、b(mol·L-1)分别为A、B两物质的起始浓度,mx(mol·L-1)为反应物A的转化浓度,nx(mol·L-1)为反应物B的转化浓度,则mA(g) + nB(g) pC(g) + qD(g)c始(mol·L-1) a b 0 0Δc(mol·L-1)mx nx px qxC平(mol·L-1)a-mx b-nx px qx物质浓度的变化关系反应物:平衡浓度=起始浓度-转化浓度生成物:平衡浓度=起始浓度+转化浓度以上三种浓度中,只有转化浓度之比等于化学方程式中计量数之比六化学平衡常数1.概念:对于一定条件下的可逆反应(aA+bB cC+dD),达到化学平衡时,生成物浓度的乘幂的乘积与反应物浓度的乘幂的乘积之比为一常数,记作Kc,称为化学平衡常数(浓度平衡常数)。
2.平衡常数的意义平衡常数的大小反映了化学反应进行的程度(也叫反应的限度)。
化学平衡总结
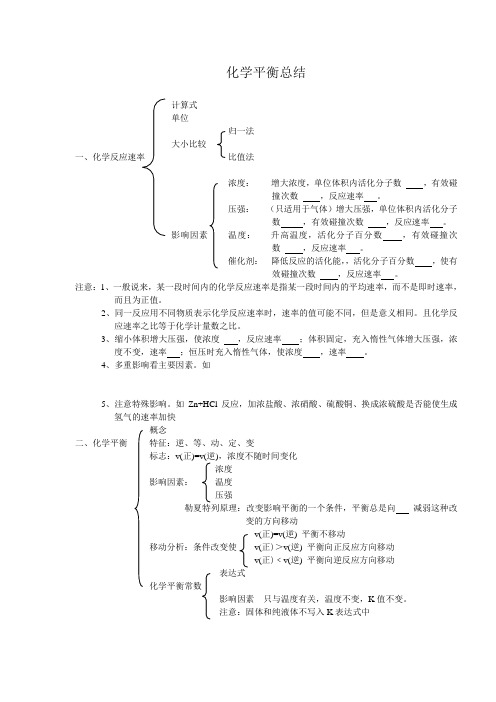
化学平衡总结计算式单位归一法大小比较一、化学反应速率比值法浓度:增大浓度,单位体积内活化分子数,有效碰撞次数,反应速率。
压强:(只适用于气体)增大压强,单位体积内活化分子数,有效碰撞次数,反应速率。
影响因素温度:升高温度,活化分子百分数,有效碰撞次数,反应速率。
催化剂:降低反应的活化能,,活化分子百分数,使有效碰撞次数,反应速率。
注意:1、一般说来,某一段时间内的化学反应速率是指某一段时间内的平均速率,而不是即时速率,而且为正值。
2、同一反应用不同物质表示化学反应速率时,速率的值可能不同,但是意义相同。
且化学反应速率之比等于化学计量数之比。
3、缩小体积增大压强,使浓度,反应速率;体积固定,充入惰性气体增大压强,浓度不变,速率;恒压时充入惰性气体,使浓度,速率。
4、多重影响看主要因素。
如5、注意特殊影响。
如Zn+HCl反应,加浓盐酸、浓硝酸、硫酸铜、换成浓硫酸是否能使生成氢气的速率加快概念二、化学平衡特征:逆、等、动、定、变标志:v(正)=v(逆),浓度不随时间变化浓度影响因素:温度压强勒夏特列原理:改变影响平衡的一个条件,平衡总是向减弱这种改变的方向移动v(正)=v(逆) 平衡不移动移动分析:条件改变使v(正)>v(逆) 平衡向正反应方向移动v(正)﹤v(逆) 平衡向逆反应方向移动表达式化学平衡常数影响因素只与温度有关,温度不变,K值不变。
注意:固体和纯液体不写入K表达式中三、化学平衡有关图像一、速率----时间图像1、温度升高温度,平衡向方向移动升高温度,平衡向方向移动2、压强(1)若a+b>c+d增大压强,平衡向方向移动减小压强,平衡向方向移动(2)若a+b=c+d增大压强,平衡向方向移动减小压强,平衡向方向移动2、浓度增大C的浓度,平衡向方向移动减小C 的浓度,平衡向方向移动3、使用催化剂平衡移动二、横坐标为时间的其他图像方法(1)定一议二(2)先柺先平,温高压大三、速率---温度(压强)图像方法: 看走势,比大小四、某一平衡量---温度(压强)图像注意:图像上任一点都是平衡时的对应量五、转化率----反应物用量比例对反应aA(g)+bB(g)==cC(g)+dD(g) 若则a/b=四、等效平衡(定义:同一可逆反应,由不同的起始状态达到平衡时,两平衡状态对应物质的百分含量相同。
化学平衡知识点总结

化学平衡 一、化学平衡 1、可逆反应 ⑴定义:在同一条件下,既能向正反应方向进行,同时又能向逆反应方向进行的反应叫做可逆反应。
用“”代替“==”。
⑵可逆反应中所谓的正反应、逆反应是相对的,一般把向右进行的反应叫做正反应,向左进行的反应叫做逆反应。
⑶在不同条件下能向两个方向进行的反应不叫可逆反应。
如: 2H 2 + O 22H 2O ;2H 2O2H 2↑+ O 2↑⑷可逆反应不能进行到底,在一定条件下只能进行到一定程度后达到平衡状态。
2、化学反应的限度 ⑴化学反应的限度就是研究可逆反应在一定条件下所能达到的最大限度。
⑵反应的转化率 反应物的转化率:α=%100 该反应物起始量反应物的转化量3、化学平衡 ⑴化学平衡状态:在一定条件下的可逆反应里,正反应速率和逆反应速率相等,反应物和生成物的浓度保持不变的状态,叫做化学平衡状态,简称化学平衡。
①化学平衡的微观标志(即本质):v 正=v 逆 ②化学平衡的宏观标志:反应混合物中各组分的浓度和体积分数保持不变,即随时间的变化,保持不变。
③可逆反应无论从正反应开始,还是从逆反应开始,或正、逆反应同时开始,都能达到化学平衡。
⑵化学平衡的特征 ①逆:化学平衡研究的对象是可逆反应。
②动:化学平衡是动态平衡,反应处于平衡态时,化学反应仍在进行,反应并没有停止。
③等:化学反应处于化学平衡状态时,正反应速率等于逆反应速率,且都不等于零。
④定:化学反应处于化学平衡状态时,反应混合物中各组分的浓度保持一定,体积分数保持一定。
对反应物,有一定的转化率,对生成物,有一定的产率。
⑤变:化学平衡是有条件的平衡,当外界条件变化,原有的化学平衡被破坏,在新的条件下,平衡发生移动,最终又会建立新的化学平衡。
二、判断可逆反应达到平衡的标志以可逆反应mA(g) + nB(g) pC(g) + qD(g)为例 1、直接标志 ⑴v 正=v 逆。
具体可以是:①A 、B 、C 、D 中任一种在单位时间内的生成个数等于反应掉的个数。
物理化学第五章化学平衡小结

第四章化学平衡核心内容: 恒T、p、Wˊ=0下,化学反应自发平衡反向自发主要内容:化学反应△G、K得计算及过程方向得判断。
一、内容提要1、化学反应自发进行与达到平衡得条件自发平衡反向自发其中,为B得化学计量数,对于产物取正值,对于反应物取负值。
2、理想气体化学反应得等温方程(分压得影响)与反应方向得具体判据<0 自发(Qp<)=0 平衡(Q p=)>0 反向自发(Qp>)式中:为标准摩尔反应吉布斯函数变化,为标准平衡常数,==f(T)3、理想气体化学反应平衡常数得其她表示法及其相互关系除了标准平衡常数外,实际应用中常用经验平衡常数K P 、K C、K n、K y(1)K P:==仅就是温度得函数,K P也只与温度有关。
(2)K C:理想气体P B V=n B RT p B==K C也只与温度有关(3)K y:p B=py BK y与温度与总压有关(4)K n:=K n与温度、总压与惰性气体有关。
综合以上各式得:=当时,=K p=K c=K y=K n4、有纯凝聚态物质参加得理想气体反应得标准平衡常数若理想气体化学反应中有纯固态或纯液态参加时,由于常压下纯凝聚态物质得化学势可近似为标准态化学势,即(cd表示凝聚态)因此其中即对参加反应得所有物质包括凝聚态物质求与。
即只考虑气相组分得平衡分压。
5、真实气体化学反应得标准平衡常数真实气体得化学势表达式为,代入可得:为组分B在指定条件下得逸度,,为B得逸度因子,它就是温度与总压得函数,也就是温度与压力得函数,对于理想气体=1 。
6、液态混合物或溶液得化学平衡常数对于液态混合物(或溶液)中得化学反应,由于任一组分得化学势为,代入可得:若反应系统为理想液态混合物或理想稀溶液,则=1,7、标准摩尔吉布斯函数变得计算方法由于,因此由可求得。
得计算主要有以下三种方法:①由计算:②计算③由相关反应计算8、化学反应得等压方程(温度得影响)上式就是范特霍夫方程得微分式,由此式可进行以下讨论:若,即吸热反应,,说明标准平衡常数随温度升高而增大,平衡右移,有利于反应正向进行。
化学平衡知识点总结

化学平衡基础知识 三、化学平衡 1、可逆反应⑴定义:在同一条件下,既能向正反应方向进行,同时又能向逆反应方向进行的反应叫做可逆反应。
用“”代替“==”。
⑵可逆反应中所谓的正反应、逆反应是相对的,一般把向右进行的反应叫做正反应,向左进行的反应叫做逆反应。
⑶在不同条件下能向两个方向进行的反应不叫可逆反应。
如:2H 2 + O 22H 2O ;2H 2O2H 2↑+ O 2↑⑷可逆反应不能进行到底,在一定条件下只能进行到一定程度后达到平衡状态。
2、化学反应的限度⑴化学反应的限度就是研究可逆反应在一定条件下所能达到的最大限度。
⑵反应的转化率 反应物的转化率:α=%100 该反应物起始量反应物的转化量3、化学平衡⑴化学平衡状态:在一定条件下的可逆反应里,正反应速率和逆反应速率相等,反应物和生成物的浓度保持不变的状态,叫做化学平衡状态,简称化学平衡。
①化学平衡的微观标志(即本质):v 正=v 逆②化学平衡的宏观标志:反应混合物中各组分的浓度和体积分数保持不变,即随时间的变化,保持不变。
③可逆反应无论从正反应开始,还是从逆反应开始,或正、逆反应同时开始,都能达到化学平衡。
⑵化学平衡的特征①逆:化学平衡研究的对象是可逆反应。
②动:化学平衡是动态平衡,反应处于平衡态时,化学反应仍在进行,反应并没有停止。
③等:化学反应处于化学平衡状态时,正反应速率等于逆反应速率,且都不等于零。
④定:化学反应处于化学平衡状态时,反应混合物中各组分的浓度保持一定,体积分数保持一定。
对反应物,有一定的转化率,对生成物,有一定的产率。
⑤变:化学平衡是有条件的平衡,当外界条件变化,原有的化学平衡被破坏,在新的条件下,平衡发生移动,最终又会建立新的化学平衡。
四、判断可逆反应达到平衡的标志 以可逆反应mA(g) + nB(g) pC(g) + qD(g)为例 1、直接标志 ⑴v 正=v 逆。
具体可以是:①A 、B 、C 、D 中任一种在单位时间内的生成个数等于反应掉的个数。
化学平衡移动的总结

化学平衡移动的总结化学平衡是指在一个封闭系统中,反应物和生成物在反应过程中达到一定比例的状态。
这个比例是由反应物的浓度和生成物的浓度决定的,称为平衡常数。
当平衡常数的值大于1时,反应偏向生成物的生成;当平衡常数的值小于1时,反应偏向反应物的生成。
化学平衡是化学反应中的一个重要概念,它可以帮助我们理解反应的趋势和速率。
在化学平衡中,反应物和生成物之间存在着动态平衡,即反应物和生成物的浓度在一定条件下保持不变。
这种平衡是由反应物和生成物之间的反应速率相等所决定的。
化学平衡的移动是指改变反应条件,使反应偏向反应物或生成物的生成。
这可以通过改变温度、压力、浓度和催化剂等因素来实现。
温度是影响化学平衡移动的重要因素之一。
根据Le Chatelier原理,当增加温度时,反应平衡会偏向吸热反应,即反应物的生成。
相反,当降低温度时,反应平衡会偏向放热反应,即生成物的生成。
这是因为在吸热反应中,增加温度可以提供所需的能量,促使反应向生成物方向进行;而在放热反应中,降低温度可以减少能量释放,使反应趋向于反应物的生成。
压力也可以影响化学平衡的移动。
对于气相反应来说,增加压力可以促使反应平衡偏向生成物的生成,因为增加压力会使分子间的碰撞频率增加,从而增加生成物的生成速率。
相反,降低压力会减少碰撞频率,使反应偏向反应物的生成。
需要注意的是,对于液相和固相反应来说,压力的变化对反应平衡几乎没有影响。
浓度也是影响化学平衡移动的重要因素之一。
增加反应物的浓度可以促使反应平衡偏向生成物的生成,因为增加反应物的浓度会增加反应物之间的碰撞频率,从而增加生成物的生成速率。
相反,增加生成物的浓度会减少生成物之间的碰撞频率,使反应偏向反应物的生成。
需要注意的是,对于液相和固相反应来说,浓度的变化对反应平衡几乎没有影响。
催化剂是一种可以影响化学平衡移动的物质。
催化剂可以降低反应的活化能,从而加快反应速率。
通过提供新的反应途径,催化剂可以使反应偏向生成物的生成,而不改变反应平衡的位置。
高中化学平衡移动知识点总结

高中化学平衡移动知识点总结化学是一门基础的自然科学。
在学习过程中,学生普遍感到化学“一听就懂,一学就会,一做就错”。
究其原因关键在于基本功不扎实。
化学知识点多而零碎,学习过程中若不能融会贯通,尤其是一些“特殊”之处,往往致使解题陷人“山重水复”之境。
为了理解、巩固和掌握这些知识,消除盲点。
今天给同学们准备了化学平衡相关知识点的总结,看完大家要多多记笔记,以后慢慢消化哦~一、化学平衡的移动01化学平衡的移动(1)定义达到平衡状态的反应体系,条件改变,引起平衡状态被破坏的过程。
(2)化学平衡移动的过程02影响化学平衡移动的因素(1)温度:在其他条件不变的情况下,升高温度,化学平衡向吸热反应方向移动;降低温度,化学平衡向放热反应方向移动。
(2)浓度:在其他条件不变的情况下,增大反应物浓度或减小生成物浓度,化学平衡向正反应方向移动;减小反应物浓度或增大生成物浓度,化学平衡向逆反应方向移动。
(3)压强:对于反应前后总体积发生变化的化学反应,在其他条件不变的情况下,增大压强,化学平衡向气体体积减小的方向移动;减小压强,化学平衡向气体体积增大的方向移动。
(4)催化剂:由于催化剂能同时同等程度地增大或减小正反应速率和逆反应速率,故其对化学平衡的移动无影响。
03勒夏特列原理在密闭体系中,如果改变影响化学平衡的一个条件(如温度、压强或浓度等),平衡就向能够减弱这种改变的方向移动。
二、外界条件对化学平衡移动的影响01外界条件的变化对速率的影响和平衡移动方向的判断在一定条件下,浓度、压强、温度、催化剂等外界因素会影响可逆反应的速率,但平衡不一定发生移动,只有当v正≠v逆时,平衡才会发生移动。
对于反应mA(g)+nB(g)pC(g)+qD(g),分析如下:02浓度、压强和温度对平衡移动影响的几种特殊情况(1)改变固体或纯液体的量,对平衡无影响。
(2)当反应混合物中不存在气态物质时,压强的改变对平衡无影响。
(3)对于反应前后气体体积无变化的反应,如H2(g)+I2(g)2HI(g),压强的改变对平衡无影响。
化学平衡总结知识点

化学平衡总结知识点化学平衡的基本概念化学平衡描述的是一个封闭系统中的化学反应。
在达到平衡状态时,反应物和产物的浓度不再发生明显的变化,但反应仍在进行,前进反应和反向反应同时进行,反应速率相等。
化学平衡可以用以下方程式表示:aA + bB ⇌ cC + dD在这个反应中,aA和bB是反应物,cC和dD是产物,a、b、c、d分别代表各个物质的系数。
平衡常数及其影响因素当一个反应达到平衡时,可以通过平衡常数K来描述反应物和产物之间的浓度关系。
平衡常数K的表达式为:K = [C]^c[D]^d / [A]^a[B]^b其中,[C]、[D]、[A]、[B]分别代表产物C、D和反应物A、B的摩尔浓度,a、b、c、d分别代表它们在平衡方程中的系数。
化学平衡的常数K是温度的函数,对于不同的反应,K的数值不同,且受到温度的影响。
在某些情况下,温度的变化可以改变反应的平衡位置,从而改变平衡常数K的数值。
影响化学平衡的因素还包括压力、浓度、温度等。
例如,在气相反应中,压力对平衡位置和K的数值都有影响。
同时,改变反应物或产物的浓度也可以影响平衡的位置和K的数值。
Le Chatelier原理Le Chatelier原理描述了一个系统受到外界影响时的反应。
根据这个原理,当一个反应系统处于平衡状态时,受到外界因素的影响,系统会通过改变反应的条件来恢复平衡。
具体来说,如果系统受到的影响是增加了某个反应物或减少了某个产物,系统会通过减少反应物或增加产物的方式来恢复平衡。
实际应用和计算化学平衡的概念在现实生活中有着广泛的应用。
例如在工业生产中,通过控制反应物和产物的浓度,可以提高产物的产率,从而节约成本。
此外,在环境保护方面,化学平衡的概念也有着广泛的应用,可以通过调整反应条件来减少有害物质的排放。
在化学平衡中,有时需要通过实验数据来计算平衡常数K的数值。
一种常见的计算方法是利用反应的初始浓度和平衡浓度之间的关系,根据K的定义式来计算K的数值。
化学平衡的知识点总结

化学平衡的知识点总结一、化学平衡的概念。
1. 定义。
- 在一定条件下的可逆反应里,当正反应速率与逆反应速率相等时,反应混合物中各组分的浓度保持不变的状态,叫做化学平衡状态。
例如,对于可逆反应N_2(g)+3H_2(g)⇌2NH_3(g),在一定温度、压强和催化剂等条件下,反应进行到一定程度时,正反应生成NH_3的速率和逆反应NH_3分解的速率相等,体系中N_2、H_2、NH_3的浓度不再发生变化,此时就达到了化学平衡状态。
2. 特征。
- 动:化学平衡是动态平衡,即达到平衡状态时,正、逆反应仍在进行,只是v_正=v_逆≠0。
例如在上述合成氨反应达到平衡时,N_2和H_2仍在不断反应生成NH_3,同时NH_3也在不断分解成N_2和H_2。
- 等:正反应速率等于逆反应速率,这是化学平衡状态的本质特征。
- 定:反应混合物中各组分的浓度保持不变,各组分的质量分数、物质的量分数、体积分数等也保持不变。
- 变:化学平衡状态是在一定条件下建立的,当外界条件(如温度、压强、浓度等)改变时,平衡可能会发生移动。
二、化学平衡常数。
1. 定义。
- 对于一般的可逆反应aA + bB⇌ cC + dD,在一定温度下达到化学平衡时,反应的平衡常数K=([C]^c[D]^d)/([A]^a[B]^b),其中[A]、[B]、[C]、[D]分别表示平衡时各物质的浓度。
例如对于反应2SO_2(g)+O_2(g)⇌2SO_3(g),其平衡常数K =frac{[SO_3]^2}{[SO_2]^2[O_2]}(温度一定)。
2. 意义。
- K值的大小可以反映反应进行的程度。
K值越大,说明反应进行得越完全,反应物的转化率越高;K值越小,说明反应进行的程度越小,反应物的转化率越低。
- 对于同一可逆反应,K只与温度有关,与反应物或生成物的浓度无关。
3. 应用。
- 判断反应进行的方向:通过比较某一时刻反应的浓度商Q=([C]^c[D]^d)/([A]^a[B]^b)(Q与K表达式相同,但Q是任意时刻的)与K的大小关系来判断反应进行的方向。
化学平衡知识归纳总结总

化学平衡知识归纳总结一、化学平衡化学平衡的涵义1、可逆反应:在同一条件下同时向正方向又向逆反应方向进行的反应..注意:“同一条件”“同时进行”..同一体系中不能进行到底..2、化学平衡状态在一定条件下的可逆反应里;正反应速率和逆反应速率相同时;反应混合物中各组分的浓度保持不变的状态叫化学平衡状态..要注意理解以下几方面的问题:1研究对象:一定条件下的可逆反应2平衡实质:V正=V逆≠0 动态平衡3平衡标志:反应混合物各组分的含量保持不变;可用六个字概括——逆、等、定、动、变、同..3、化学平衡状态的特征:1逆:化学平衡状态只对可逆反应而言..2等:正反应速率和逆反应速率相等;即同一物质的消耗速率与生成速率相等..3定:在平衡混合物中;各组分的浓度保持一定;不在随时间的变化而变化..4动:化学平衡从表面上、宏观上看好像是反应停止了;但从本质上、微观上看反应并非停止;只不过正反应速率于逆反应速率相等罢了;即V正=V逆≠0;所以化学平衡是一种动态平衡..5变:化学平衡实在一定条件下建立的平衡..是相对的;当影响化学平衡的外界条件发生变化时;化学平衡就会发生移动..6同:化学平衡状态可以从正逆两个方向达到;如果外界条件不变时;不论采取何种途径;即反应是由反应物开始或由生成物开始;是一次投料或多次投料;最后所处的化学平衡是相同的..即化学平衡状态只与条件有关而与反应途径无关..可逆反应达到平衡的标志1、同一种物质V正=V逆≠02、各组分的物质的量、浓度包括物质的量的浓度、质量分数等、含量保持不变..等效平衡1、等效平衡原理:相同条件下;同一可逆反应体系;不管从正反应开始;还是从逆反应开始;只要按反应方程式中的化学计量数之比投入反应物或生成物;建立起的平衡状态都是相同;这就是等效平衡的原理..由于化学平衡状态与条件有关;而与建立平衡的途径无关..因而;同一可逆反应;从不同的状态开始;只要达到平衡时条件温度、浓度、压强等完全相同;则可形成等效平衡.. 2、等效平衡规律1在定温、定容的条件下;对于反应前后气体分子数改变的可逆反应;只改变起始时加入物质的物质的量;如通过可逆反应的化学计量数比换算成同一半边的物质的物质的量与原平衡相同;则两平衡等效..2在定温、定容的条件下;对于反应前后气体分子数不变的可逆反应;只要反应物或生成物的物质的量的比值与原平衡相同;两平衡等效..主要是指转化率相同3在定温、定压下;改变起始时加入物质的物质的量;只要按化学计量数换算成同一半边的物质的物质的量之比与原平衡相同;则达到平衡后与原平衡等效..习题 1、可逆反应N 2+3H 2=2NH 3的正逆反应速率可用各反应物或生成物浓度变化来表示..下列各关系中能说明反应以达到平衡状态的是 A 3V 正N 2=V 正H 2 B V 正N 2=V 逆NH 3 C 2V 正H 2=3V 逆NH 3 D V 正N 2=3V 逆H 22、可逆反应:2NO 2=2NO+O 2在密闭容器中反应;达到平衡的标志是 ①单位时间生成nmolO 2的同时;生成2nmolNO 2②单位时间生成nmolO2的同时;生成2nmolNO③用NO2、NO、O2的物质的量浓度变化来表示的反应速率的比为2:2:1的状态④混合气体的颜色不再改变的状态⑤混合气体的密度不再发生改变的状态⑥混合气体的平均相对分子质量不再改变的状态A ①④⑥B ②③⑤C ①③④D ①②③④⑤⑥3、在一个固定容积的密闭容器中发生如下反应:2Ag+Bg=3Cg+Dg 当加入4molA和2molB;达到化学平衡时;C的物质的量的浓度为nmol/L..若维持温度不变;按下列四种配比为起始物质;达到平衡后;C仍未nmol/L的是A 2molA+1molB B 6molC+2molDC 3molC+1molD D 4molA+2molB+3molC4、2004年北京在一定温度下;一定体积的密闭容器中有如下平衡:H 2g+I2g=2HIg..已知H2和I2的起始浓度均为0.10mol/L时;达平衡时HI的浓度为0.16mol/L..若H2和I2的起始浓度增大为0.20mol/L时;则平衡时H2的浓度mol/L是A 0.16B 0.08C 0.04D 0.025、一定温度下;反应2SO2g+O2g=2SO3g达平衡时;nSO2:nO2:nSO2=2:3:4 ..缩小体积;反应再次达到平衡时;nO 2=0.08mol;nSO 3=1.4mol..此时SO 2的物质的量应为A 0.4molB 0.6molC 0.8molD 1.2mol6、2003年高考某温度下;在一容积可变的容器中;反应2Ag+Bg=2Cg 达到平衡时;A 、B 、C 的物质的量分别为4mol 、2mol 和4mol..保持温度和压强不变;对平衡混合物中的三者的物质的量做如下调整;可使平衡右移的是 A 均减半 B 均加倍 C 均增加1mol D 均减少1mol7、2004年高考恒温下;将amolN 2与bmolH 2的混合气体通入一个固定容积的密闭容器中;发生如下反应:N 2g+3H 2g=2NH 3g1若反应进行到某时刻t 时;nN 2=13mol;nNH 3=6mol;计算a 的值..2反应达平衡时;混合气体体积为716.8L 标准情况下;其中NH 3的含量体积分数为25%..计算平衡时NH 3的物质的量..3原混合气体与平衡混合气体的总物质的量之比写出最简整数比;下同; N 始:N 平=4原混合气体中;a:b=5达到平衡时;N 2和H 2的转化率之比为 6平衡混合气体中;nN 2:nH 2:nNH 3=8、2003年高考Ⅰ.恒温、恒压下;在一个容积可变的容器中发生如下反应:Ag+Bg=Cg(1)若开始时放入1molA和1molB;达到平衡后;生成amolC;这时A的物质的量为 mol(2)若开始时放入3molA和3molB;达到平衡后;生成C的物质的量为mol(3)若开始时放入xmolA;2molB和1molC;达到平衡后;A和C的物质的量分别是ymol和3amol;则x= mol;y= mol.平衡时;B的物质的量为甲.大于2mol 乙.等于2mol 丙小于2mol 丁.可能大于等于或小于2mol作出此判断的理由是4 若在3的平衡混合物中再加入3molC;带再次达到平衡后;C的物质的量得分数是 ..Ⅱ.若维持温度不变;在一个与Ⅰ反应前起始体积相同;且容积固定的容器中发生上述反应..5开始时放入1molA和1molB;达到平衡后生成bmolC..将b与1小题中的a进行比较 ..甲.a<b 乙.a>b 丙a=b 丁.不能比较a和b的大小作出此判断的理由是二、影响化学平衡的条件 合成氨工业 1、化学平衡的移动以及影响化学平衡的因素 1化学平衡的移动 ①移动过程表示一定条件下的化学平衡V 正=V 逆各组分的含量保持一定→ 条件改变平衡破坏V 正≠V 逆各组分含量发生变化→ 一定时间后 新条件下的新平衡V 正’=V逆’②化学平衡移动的概念达到化学平衡的反应;在条件改变后;平衡状态被破坏;然后在新的条件下达到新的平衡状态的过程;叫平衡移动.. 2影响化学平衡的条件及平衡移动的原理①以一般反应mAg+nBg==pCg+qg;△H=Q;为例来总结温度、浓度、压强和催化剂对反应速率以及化学平衡的影响..其规律如下表所示:②勒夏特列原理:如果改变影响化学平衡的一个条件浓度、压强或温度等;平衡就会向着能够减弱这种改变的方向移动对勒夏特列原理中“减弱这种改变”的正确理解应当是:升高温度时;平衡向着吸热反应方向移动;增加反应物;平衡向反应物减少的方向移动;增大压强时;平衡向体积缩小的方向移动..2、有关正、逆反应速率和化学平衡的图像1化学平衡种常见的几种图像①v-t图:既能表示反应速率变化;又能表示平衡移动的速率-时间图像..如图所示的A、B、C所示:A 图:t=0时;V正>V逆=0;表示反应由正反应开始;t=t1时;V正’>V逆’= V逆;表明改变条件的瞬间;V正变大;V逆不变;是加入了一种反应物;t>t1时;V正’>V逆’;表明平衡向正反应方向移动;随后又达到新的平衡..B 图:a.反映由正反应开始..b. V正、V逆在改变条件时同时增大..c.平衡向逆反应方向移动了..C 图:a.反映由正反应开始..b. V正、V逆在改变条件时同时倍数增大..c.平衡未移动..②转化率-时间图;如图A、B所示A图:先出现拐点的先达平衡;即“先拐先平”;说明T2>T1B图:同理说明P1>P2 先拐先平数值大③物质的含量-压强-温度图;如图所示中A、B对于上述图形;采用“定一议二”法;先确定一个量不变;讨论另外两个量的关系..3、合成氨适宜条件的选择1目的:尽可能加快反应速率和提高反应进行度..2依据:外界条件对化学反应速率和化学平衡影响的规律;结合合成氨反应的特点:正反映是体积缩小的放热反应;选择合成条件..3原则:①既要注意外界条件对二者影响的一致性;又要注意对二者影响的矛盾性..②既要注意温度、催化剂对反应速率影响的一致性;又要注意催化剂的活性而对温度的限制..③既要注意理论生产;又要注意实际可能性..适宜条件:500℃;铁触媒;2×107~5×107Pa;循环操作过程N 2与H 2体积比为1:3习题:1、2005年天津卷在密闭容器中;一定条件下;进行如下反应:NOg+COg=0.5N 2g+CO 2g;△H=-373.2kJ/mol;达到平衡后;为了提高该反应速率和NO 的转化率;采取的争取措施是A 加催化剂同时升高温度B 加催化剂同时增大压强C 升高温度同时充入N 2D 降低温度同时增大压强2、2005年北京卷在一定温度不同压强P1<P2下;可逆反应2Xg=2Yg+Zg 中;生成物Z 在反应混合物中体积分数与反应时间关系有以下图示;正确的是3、一定温度下;在恒容密闭容器中发生如下反应:2Ag+Bg=3Cg;若反应开始时充入2molA和2molB;平衡后A的体积分数为a%;其他条件不变时;若按下列四种配比作为起始物质;平衡后A的体积分数大于a的是A 2molCB 2molA 1molB和1molHe不参加反应C 1molB和1molCD 2molA;3molB和3molC4、对于如下反应:mAg+nBg=pCg+qg;当其他条件不变;温度分别为T1和T2时;反应物B的百分含量与反应时间的关系如图所示;据此下列正确的是A T1>T2B 正反应是吸热反应C T1<T2D逆反应是吸热反应5、如图曲线a表示放热反应Xg+Yg=Zg+Mg+Ns进行过程中X的转化率随时间变化的关系..若要改变起始条件;使反应过程按b曲线进行;可采取的措施是A 升高温度B 加大X的投入料C 加催化剂D 增大体积6、在体积一定的密闭容器中给定物质A、B、C的量;在一定条件下发生反应建立的化学平衡:aAg+bBg=xCg;符合如图所示的关系C%表示平衡混合气体中产物C的百分含量;T表示温度;P表示压强..在图Ⅱ中;y轴是指A 反应物A的转化率B 平衡混合气体中物质B的百分含量C 平衡混合气体的密度D 平衡混合气体的的平均摩尔质量7、某温度下的恒容密闭容器中发生入夏反应:2Zg=2Xg+Yg开始时只充入1molX和0.5molY的混合气体;达到平衡时;混合气体的压强比开始时减少了20%..若开始只充入1molZ的气体;达到平衡时;Z的分解率为A 20%B 40%C 60%D 80%答案:1 B;2 B;3 AB;4 AD;5 C;6 AD。
大学物理化学-化学平衡的总结

∑ ∆ rHθm =- ν B∆ CHθm (B)
B
∑ ∆ rSθm = ν BSθm (B)
B
B
3)由有关反应的 ∆ rGθm 来求所需
化学反应的∆ rGθm
因为,G 是状态函数。所以若在某一温度下,几个 化学反 应具有加和性时,这些反应的 ∆ rGθm 也有加和关系。
等压方程
⎛
⎜ ⎝
∂ ln Kθ ∂T
⎞
⎟ ⎠p
=
∆r
H
θ m
RT 2
此式为范特霍夫等压方程。它表明温度对标 准平衡常数的影响,与反应的标准摩尔反应 焓有关。
①升温有利于吸热反应,降温有利于放热反应
②改变温度使平衡发生移动是因为改变了 Kθ。
定积分式: ln
K
θ 2
K1θ
=
−
Δr
H
θ m
R
⎛1
⎜ ⎝
T2
−
Байду номын сангаас
1 T1
⎞ ⎟ ⎠
若已知
ΔrH
θ m
在恒T、恒V下,加入惰性气体对反 应无影响。
在恒T、恒P下,加入惰性气体对反应有 影响,且有利于的Σν B>0 反应
真实气体混合物中组分B的化学势:
∫ µ∗ B
=
µθ B
+
RTln(
PB
/
pθ )+
p
0 (VB
− RT
/
P)d p
= µθB
+ RT ln(
f
/
pθ )
f:气体的逸度(f = γp ,校正压力) 对理想气体:γ = 1 or f = p
以及
T1下
物理化学-第五章-化学平衡
( g )
3. 增加反应物的量对平衡移动的影响
aA bB yY zZ 恒温恒容条件下增加反应物量对反应平衡的影响:
在已达到平衡的系统中,加入反应物A,瞬间A的分压增加,其他组分分压不变,结果Jp减小, 温度一定,Kϴ不变,反应右移。 恒温恒压条件下增加反应物量并不总是使平衡右移: 当起始反应物配比1:1时,平衡后加入反应物,会使平衡左移。
Kθ的实验测定和平衡组成的计算
Kθ的计算 1. Kθ可由热力学计算得到,由△rGθm=-RTlnKθ计算 2. Kθ 可由实验测定得到,由平衡时Kθ= ∏(PB/Pθ)vB( 理想气 体)可得
平衡组成的特点
1. 反应条件不变,平衡组成不变 2. 一定温度下,正向与逆向反应平衡组成算出的Kθ应一致 3. 温度不变,改变原料配比所得的Kθ应相同
注意:溶剂A和溶质B的标准态不同。
A
B
B
(r b
B
B B
/ b )B
习题
五氯化磷分解反应 在200℃时的Kθ =0.312,计算: (1)200℃、200kPa下PCl5的离解度; ( 2 )组成 1 ∶ 5 的 PCl5 与 Cl2 的混合物,在 200 ℃ 、 101.325kPa下PCl5的离解度。
上式中△rHθ m=∑vB△fHθ m,B=-∑vB△cHθ m,B,△rSθ m=∑vBSθ m,B (2)通过△fGθ m来计算△rGθ m
△rGθ m=∑vB△fGθ m
(3)由相关线性反应计算,如果一个反应可由其他反应线 性组合得到,那么该反应的△rGm也可由相应反应的△rGm线
性组合得到
如 (3)=(1)+ 2*(2),那么 △rGθ m,3=△rGθ m,1+2△rGθ m,2
物理化学第五章化学平衡小结 (2)

第四章 化学平衡核心内容: 恒T 、p 、W ˊ=0下,化学反应自发0,,><=∆∑='B B W p T G μν平衡 反向自发主要内容:化学反应△G、K的计算及过程方向的判断。
一、内容提要1、化学反应自发进行与达到平衡的条件自发0,,><=∆∑='B B W p T G μν 平衡反向自发其中,B ν为B 的化学计量数,对于产物B ν取正值,对于反应物B ν取负值。
2、理想气体化学反应的等温方程(分压的影响)与反应方向的具体判据P m r m r Q RT G G ln +∆=∆θθp Q RT K RT ln ln +-=θθK Q RT pln= <0 自发 (Q p<θK )=0 平衡 (Q p=θK ) >0 反向自发(Qp>θK )式中:θθμνB B m r G ∑=∆为标准摩尔反应吉布斯函数变化,θK 为标准平衡常数,)ex p(RT G K mr θθ∆-==B p p eqB Bνθ)(∏=f(T)3、理想气体化学反应平衡常数的其她表示法及其相互关系除了标准平衡常数外,实际应用中常用经验平衡常数KP 、K C 、K n 、K y(1)K P :θK =∑∏=∏-BB B p p p p eq B BeqB B νθννθ)()()(θK =∑-B p K P νθ)( θK 仅就是温度的函数,K P 也只与温度有关。
(2)KC :理想气体PB V=n B RT pB=RT c RT Vn B B= θK =∑∏=∏=∏BB B B pRT c p RT c p p B B B B eqB B νθννθνθ)()()( ∑=BpRT K K C νθθ)( KC 也只与温度有关(3)K y:p B=py B=θK∑∏=∏=∏B BB B pp y p y p p p B B B B eqB B νθννθνθ)()()( ∑=Bpp K K y νθθ)(总K y 与温度与总压有关(4)K n :∑=BB BB n n pp =θK BB BB BeqB Bn npp pp ννθυθ)()()(∑∏=∏=∑∑B npp K n νθ)(K n 与温度、总压与惰性气体有关。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第四章 化学平衡
核心内容: 恒T 、p 、W ˊ=0下,化学反应
自发
0,,><
=∆∑='B B W p T G μν 平衡
反向自发
主要内容:化学反应△G 、K 的计算及过程方向的判断。
一、内容提要
1、化学反应自发进行和达到平衡的条件
自发
0,,><
=∆∑='B B W p T G μν 平衡
反向自发
其中,B ν为B 的化学计量数,对于产物B ν取正值,对于反应物B ν取负值。
2、理想气体化学反应的等温方程(分压的影响)
和反应方向的具体判据
P m r m r Q RT G G ln +∆=∆θ
θ
p Q RT K RT ln ln +-=θ
θ
K Q RT p
ln
= <0 自发 (Qp <θ
K )
=0 平衡 (Q p=θ
K ) >0 反向自发(Qp >θ
K )
式中:θ
θμνB B m r G ∑=∆为标准摩尔反应吉布斯函数变化,θ
K 为标准平衡常数,
)ex p(RT G K m r θ
θ
∆-==B p p eq
B B
νθ)(∏=f(T)
3、理想气体化学反应平衡常数的其他表示法及其相互关系
除了标准平衡常数外,实际应用中常用经验平衡常数K P 、K C 、K n 、K y
(1)K P :θK =∑∏=∏-B
B B p p p p eq B B
eq
B B νθννθ)()()(
θK =∑
-
B p K P νθ)( θ
K 仅是温度的函数,K P 也只与温度有关。
(2)K C :理想气体P B V=n B RT p B =RT c RT V n B B
=
θK =∑∏=∏=∏B
B B B p
RT c p RT c p p B B B B eq
B B νθννθνθ)()()( ∑=B
p
RT K K C νθθ
)
( K C 也只与温度有关
(3)K y :p B =py B
=θ
K
∑∏=∏=∏B B
B B p
p y p y p p p B B B B eq
B B νθννθνθ)()()( ∑=B
p
p K K y νθθ
)
(总 K y 与温度和总压有关
(4)K n :
∑=B
B B
B n n p
p =
θ
K B
B B
B B
eq
B B
n n
p
p p
p ννθ
υθ
)
()(
)
(
∑∏=∏
=
∑∑B n
p
p K n νθ
)
(
K n 与温度、总压和惰性气体有关。
综合以上各式得:
θ
K =
∑=∑=∑=∑∑B B B B n
p p K p p K p
RT K p K n y C P νθνθνθνθ
)()()()( 当∑=0B ν时,θK =K p =K c =K y =K n
4、有纯凝聚态物质参加的理想气体反应的标准平衡常数
若理想气体化学反应中有纯固态或纯液态参加时,由于常压下纯凝聚态物质的化学势可近似为标准态化学势,即)()(cd cd B B θ
μμ=(cd 表示凝聚态) 因此 P m r m r Q RT G G ln +∆=∆θ
其中
∑=∆ϑ
θ
μνB B m r G 即对参加反应的所有
物质包括凝聚态物质求和。
)
()()
()
(
g eq
g B g B B p
p
K νθ
θ
∏=
即θ
K 只考虑气相组分的平衡分压。
5、真实气体化学反应的标准平衡常数
真实气体的化学势表达式为
)ln(θθ
μμp p RT B
B B +=,
代入∑=∆B B rGm μν可得:
B
B
B p
p p f K eq
B B eq B B eq
B B νθννθθ
ϕ)
()()(∏⨯∏∏= B p ~ 为组分B 在指定条件下的逸度,
B B B p f ϕ=,eq
B
ϕ为B 的逸度因子,它是温度
和总压的函数,B
eq B
B νϕ)(∏也是温度和压力的函
数,对于理想气体
B eq B
B
νϕ)
(∏=1
B
p
p
K eq
B B νθθ
)
(∏=。
6、液态混合物或溶液的化学平衡常数 对于液态混合物(或溶液)中的化学反应,由于任一组分的化学势为
B B B a RT ln +=θ
μμ,代入∑=∆B B rGm μν可
得:
B B eq B
eq B B
B B B eq B B
a a K ννθ
χγχγ)
()(∏=∏=
B B eq B
B
eq B B
K ννθ
χγ)
()(∏∏=
若反应系统为理想液态混合物或理想稀溶液,则
B γ=1,1=∏B
B B
νγ
7、标准摩尔吉布斯函数变θ
m r G ∆的计算方法 由于θ
θ
K RT G m r ln -=∆,因此由θ
m r G ∆可求
得θ
K 。
θ
m r G ∆的计算主要有以下三种方法:
①由θm f G ∆计算θ
m r G ∆:θ
θνm f B m r G G ∆∑=∆
②θ
θθ
m r m r m
r S T H G ∆-∆=∆计算
θ
θ
νm f B m r H H ∆∑=∆
θ
θ
νm f B m r S S ∆∑=∆
③由相关反应计算θ
m r G ∆
8、化学反应的等压方程(温度的影响)
2)ln (RT
H T K
m r P θ
θ∆=∂∂
上式是范特霍夫方程的微分式,由此式可进行以下讨论:
若0>∆θ
m r H ,即吸热反应,0)ln (>∂∂P T K θ
,说明
标准平衡常数随温度升高而增大,平衡右移,有利于反应正向进行。
若0<∆θ
m r H ,即放热反应,0)ln (<∂∂P T
K θ
,说明标准平衡常数随温度升高而减小,平衡左移,不利于反应正向进行。
对范特霍夫方程的微分式进行积分,可进行有关计算:
①若温度变化范围不大,或0,=∑θ
υm P B C ,
θ
m r H ∆可看作常数时
不定积分式 C T
R H K m r +∆-=1
ln θ
θ
定积分式 )
11(ln 121
2
T T R H K K m r -∆-=θ
θθ )
11()()(121122T T H T T G T T G m r m r m r -∆=∆-∆θθ
θ
与前两式皆
为等价式。
②若温度变化范围不大,或0,≠∑θυm P B C ,θm r H ∆不能看作常数时
dT RT T H K K m r T T 212)(ln 21θ
θθ∆=⎰ 9、平衡移动原理
(1)升高温度,反应向吸热的方向进行;降低
温度,反应向放热的方向进行;
(2)升高压力,反应向分子数减少的方向进行;
降低压力,反应向分子数增多的方向进行;
(3)引入惰性气体(总压不变),反应向分子数
增多的方向进行;
(4)反应物的摩尔比对平衡转化率的影响
当反应物的摩尔比等于化学计量系数之此
时,产物的含量最大,但绝对值不一定最大。
1
225.40),(-⋅-=∆mol kJ s S Ag G m f θ。
