ICHQC一类二类三类溶剂
ICH Q3(R7)四类溶剂划分标准

ICHQ3C R7现行第四阶段版本2018年10月15日本指导原则由相应的ICH专家工作组制定,并根据ICH 进程已提交给管理当局征询意见。
在ICH进程的第四阶段,最后的草案被推荐给欧盟、日本、美国、加拿大和瑞士的管理机构采纳。
编码历史日期母指导原则:杂质:残留溶剂的指导原则Q3C 指导委员会经第二阶段后批准,并发布以便向公众征求意见。
1996年11月6日Q3C指导委员会经第四阶段后批准,并建议ICH的三个监管机构采纳。
1997年7月17日对母指导原则所含THF的PDE信息的修订Q3C(R1)注:2005年11月修订前本版本命名为Q3C (M):THF 四氢呋喃(THF)的每日允许暴露量(PDE):根据新的毒理学数据修订PDE。
指导委员会经第二阶段后批准THF的新PDE,并发布以便向公众征求意见。
2000年7月20日Q3C(R1)注:2005年11月修订前本版本命名为Q3C (M):THF 指导委员会经第四阶段后批准,并建议ICH的3个监管机构采纳。
2002年9月12日对母指导原则所含NMP的PDE信息的修订母指导原则:杂质:残留溶剂的指导原则对母指导原则所含异丙基苯的PDE信息的修订修订母指导原则所含甲基异丁基酮的PDE信息,并纳入三乙胺的PDE更正了乙二醇的PDE信息ICH第一部分: (1)1.引言 (1)2.指导原则的适用范围 (2)3.通则 (3)3.1 基于风险评估的残留溶剂的分类 (3)3.2 建立暴露限度的方法 (4)3.32类溶剂限度的表示方法 (4)3.4分析方法 (6)3.5残留溶剂的报告水平 (6)4.残留溶剂的限度 (7)4.1应避免的溶剂 (7)4.2应限制的溶剂 (8)4.3低潜在毒性的溶剂 (9)4.4没有足够毒理学数据的溶剂 (10)词汇表 (11)附录1:指导原则中包括的溶剂列表 (13)附录2:其他背景 (17)A2.1环境领域对有机挥发性溶剂的监管 (17)A2.2药物中的残留溶剂 (17)附录3:建立暴露限度的方法 (19)第二部分: (24)四氢呋喃的PDE (24)第三部分: (27)N-甲基吡咯烷酮(NMP)的PDE (27)第四部分: (30)异丙基苯的PDE (30)第五部分: (35)三乙胺的PDE和甲基异丁基酮的PDE (35)在1997年7月17日的ICH指导委员会会议上进入ICH进程第四阶段,并建议ICH的三方监管机构采纳该指导原则。
药典中溶剂按毒性分类

药典中溶剂按毒性分类:第一类溶剂是指已知可以致癌并被强烈怀疑对人和环境有害的溶剂。
在可能的情况下,应避免使用这类溶剂。
假如在生产治疗价值较大的药品时不可避免地使用了这类溶剂,除非能证实其合理性,残留量必须控制在规定的范围内,如苯(2ppm)、四氯化碳(4ppm)、1,2-二氯乙烷(5ppm)、1,1-二氯乙烷(8ppm)、1,1,1-三氯乙烷(1500ppm)。
第二类溶剂是指无基因毒性但有动物致癌性的溶剂。
按每日用药10克计算的每日答应接触量如下,乙腈(410ppm)、氯苯(360ppm)、氯仿(60ppm)、环己烷(3880ppm)、二氯甲烷(600ppm)、二氧杂环己烷(380ppm)、1,1,2-三氯乙烯(80ppm)、1,2-二甲氧基乙烷(100ppm)、2-乙氧基乙醇(160ppm)、2-甲氧基乙醇(50ppm)、环丁砜(160ppm)、1,2,3,4-四氢化萘(100ppm)、嘧啶(200ppm)、甲苯(890ppm)、甲酰胺(220ppm)、1,2-二氯乙烯(1 870ppm)、N,N-二甲基乙酰胺(1090ppm)、N,N-二甲基甲酰胺(880ppm)、乙烯基乙二醇(620ppm)、正己烷(290ppm)、甲醇(3000ppm)、甲基环己烷(1180ppm)、N-甲基吡咯烷酮(4840ppm)、二甲苯(2 170ppm)。
第三类溶剂是指对人体低毒的溶剂。
急性或短期研究显示,这些溶剂毒性较低,基因毒性研究结果呈阴性,但尚无这些溶剂的长期毒性或致癌性的数据。
在无需论证的情况下,残留溶剂的量不高于0.5%是可接受的,但高于此值则须证实其合理性。
这类溶剂包括戊烷、甲酸、乙酸、乙醚、丙酮、苯甲醚、1-丙醇、2-丙醇、1-丁醇、2-丁醇、戊醇、乙酸丁酯、三丁甲基乙醚、乙酸异丙酯、甲乙酮、二甲亚砜、异丙基苯、乙酸乙酯、甲酸乙酯、乙酸异丁酯、乙酸甲酯、3-甲基-1-丁醇、甲基异丁酮、2-甲基-1-丙醇、乙酸丙酯。
ICHQ3C(R6)残留溶剂培训

• 非遗传毒性动物致癌物质,或可能导致其他不可逆毒性如神经毒性或致畸性的溶剂。可能有 其他严重但可逆的毒性的溶剂。
– Ⅲ类:低潜在毒性的溶剂
• 对人体低潜在毒性的溶剂,无须制定基于健康的暴露限度。3类溶剂的PDE为每天50mg或 50mg以上
2021/3/7
CHENLI
5
LIMITS 残留溶剂的限度
– 1、异丙基苯(5000ppm → 70 ppm,Ⅲ类 → Ⅱ类)
– 2、甲基异丁基酮(5000ppm → 4500 ppm,Ⅲ类 → Ⅱ类)
2021/3/7
CHENLI
8
Ⅲ类溶剂限度
• 限度 – Ⅲ类溶剂的限度均为5000ppm(0.5%)
• 关注点 – 1、三乙胺(新增)
• 之前参考欧洲药品质量管理与医疗保健局(EDQM),规定
• 控制目的:由于残留溶剂没有治疗益处,故应尽可能除去所有残留溶剂,以 符合制剂质量标准、生产质量管理规范(GMP)或其他质量要求。
2021/3/7
CHENLI
4
残留溶剂分类
• ICH Q3C(R6)中,将溶剂分为三类: – Ⅰ类:应避免的溶剂
• 已知的人体致癌物,强疑似人体致癌物,以及环境危害物。
eg.乙腈的限度计算: 10001(04g.(1/ mdagy/)day) 410 ppm
2021/3/7
CHENLI
11
残留溶剂限度计算
• 原料药残留溶剂量能否超过限度?
– 若制剂的给药剂量超过 10g/day – 若原料、辅料中残留溶剂量超过限度
• 将制剂各成分所含的残留溶剂累加,每天的溶剂总量应低于PDE给定的值。
• ICH Q3C(R6)与《中国药典》(2015年)的对比
ICH杂质残留溶剂的指导原则QCR

ICH杂质残留溶剂的指导原则QCRICH杂质残留溶剂的指导原则QCR(Quality Control Residual Solvents)是国际药品监管机构-国际药品注册、技术和质量控制委员会(ICH)发布的一项指南,用于规范药品制造过程中的溶剂残留物的质量控制。
溶剂残留物是指在药品生产过程中添加的溶剂,但在制剂中未完全蒸发或被移除的溶剂。
导言溶剂在药品生产过程中广泛应用,包括分离、提取、结晶和纯化等步骤。
然而,溶剂中的残留物可能对人体产生毒性或对药品质量产生影响。
因此,在药品开发和生产过程中,需要对残留溶剂进行必要的质量控制。
溶剂分类ICHQCR指导原则将溶剂分为类1、类2A和类2B三类。
类1溶剂是无毒、无致畸、无致癌和生殖毒性的溶剂,如水、乙醇、甘油等。
这些溶剂的使用一般没有限制。
类2A溶剂是有潜在毒性或限制使用的溶剂,但在限定剂量下不会对人体产生危害。
这类溶剂的最大可容许残留量取决于药物用量、剂型和给药途径。
一些常见的类2A溶剂包括氯仿、氯化甲烷、二氯甲烷等。
类2B溶剂是有潜在毒性,并且在制剂中的残留量应尽量减少的溶剂。
这类溶剂的最大可容许残留量取决于药物用量和给药途径。
一些常见的类2B溶剂包括苯、乙酸乙酯、二甲基甲醚等。
质量控制要求ICHQCR指导原则确定了三种质量控制要求来管理溶剂残留物。
1. 可容许残留量(Permitted Daily Exposure, PDE):PDE是指人体每日接触该溶剂残留量的最大可容许量。
它可以通过毒理学评估和毒性数据来确定。
对于类1溶剂,PDE通常设置为无限大。
对于类2A和类2B 溶剂,PDE被用来确定最大可容许残留量。
2.可容许残留量限度:可容许残留量限度是指药品中残留溶剂的最大可容许浓度。
它根据预期剂量、给药途径和药物性质等因素来确定。
通过使用PDE和剂量预设的数学公式,可以计算出每种溶剂的可容许残留量限度。
3.分析方法:为了确保溶剂残留物的质量控制,需要使用适当的分析方法进行检测和分析。
药品的溶剂残留标准2002
乙酸异丁酯
50.0
0.5
2-乙氧基乙醇
1.6
0.016
乙酸异酯
50.0
0.5
乙二醇
6.2
0.062
乙酸甲酯
50.0
0.5
甲酰胺
2.2
0.022
3-甲基-1-丁醇
50.0
0.5
正己烷
2.9
0.029
丁酮
50.0
0.5
甲醇
30.0
0.3
甲基异丁基酮
50.0
0.5
2-甲氧基乙醇
0.5
0.005
异丁醇
50.0
0.5
甲基丁基酮
0.5
0.005
正戊烷
50.0
0.5
甲基环己烷
11.8
0.118
正戊醇
50.0
0.5
N-甲基吡咯烷酮
5.3
0.053
正丙醇
50.0
0.5
硝基甲烷
0.5
0.005
异丙醇
50.0
0.5
吡啶
2.0
0.02
乙酸丙酯
50.0
0.5
四氢噻吩
1.6
0.016
第四类溶剂(尚无足够毒理学资料)
50.0
0.5
1,2-二氯乙烯
18.7
0.187
乙酸乙酯
50.0
0.5
二氯甲烷
6.0
0.06
乙醚
50.0
0.5
1,2-二甲氧基乙烷
1.0
0.01
甲酸乙酯
50.0
0.5
N,N-二甲氧基乙酰胺
10.9
ICH常用有机溶剂分类及残留限度审批稿

I C H常用有机溶剂分类及残留限度YKK standardization office【 YKK5AB- YKK08- YKK2C- YKK18】ICH常用有机溶剂分类及残留限度2009-12-04 11:50残留溶剂无防治作用并可能对人体的健康和环境造成危害,本文对国际协调大会(ICH)制订的指导原则及各国执行情况作了较为详尽的介绍。
药品的残留溶剂,又称有机挥发性杂质,是指在活性药物成分、辅料和药品生产过程中使用和产生的有机挥发性化学物质。
药品还可被来自包装、运输、仓储中的有机溶剂污染。
药品生产商有责任确保终产品中的任何一种残留溶剂对人体无害。
各国药监部门曾使用不同的药品残留溶剂指导原则,为此国际组织展开了协调工作。
经相关程序讨论和审查后,国际协调大会的指导原则于1997年7月17日获得通过,被推荐至国际协调大会(ICH)的指导委员会采用。
该指导原则要求,如果某个药品的生产或纯化过程可导致溶剂残留,就应对这个药品进行检测,并且只检测生产过程或纯化中使用或产生的那种溶剂。
根据使用量的多少,可采用累加的方法计算药品中残留溶剂的量。
如果累加量低于或等于指导原则中的推荐量,则该药品无需进行残留溶剂检测;如果累加量高于推荐量,则必须对该药品进行残留溶剂检测。
该指导原则适用于颁布以后上市的所有剂型和给药途径,但不适用于在临床研究阶段使用的潜在新药和新辅料,也不适用于已上市的现有药物。
在某些情况如短期(小于30天)或局部应用下,视具体情况,溶剂的高残留量也可接受。
按照毒性大小和对环境的危害程度,该指导原则将溶剂分成三类(所列举的溶剂并不完全,应对合成和生产过程所有可能的残留溶剂进行评估):第一类溶剂是指已知可以致癌并被强烈怀疑对人和环境有害的溶剂。
在可能的情况下,应避免使用这类溶剂。
如果在生产治疗价值较大的药品时不可避免地使用了这类溶剂,除非能证明其合理性,残留量必须控制在规定的范围内,如:苯(2ppm)、四氯化碳(4ppm)、1,2-二氯乙烷(5ppm)、1,1-二氯乙烷(8ppm)、1,1,1-三氯乙烷(1500ppm)。
医药中常用有机溶剂分类及残留限度知识分享

医药中常用有机溶剂分类及残留限度医药中常用有机溶剂分类及残留限度医药中常用有机溶剂分类及残留限度药品的残留溶剂无治疗作用并可能对人体的健康和环境造成危害,本文对国际协调大会(ICH)制订的指导原则及各国执行情况作了较为详尽的介绍。
药品的残留溶剂,又称有机挥发性杂质,是指在活性药物成分、辅料和药品生产过程中使用和产生的有机挥发性化学物质。
药品还可被来自包装、运输、仓储中的有机溶剂污染。
药品生产商有责任确保终产品中的任何一种残留溶剂对人体无害。
各国药监部门曾使用不同的药品残留溶剂指导原则,为此国际组织展开了协调工作。
经相关程序讨论和审查后,国际协调大会的指导原则于1997年7月17日获得通过,被推荐至国际协调大会(ICH)的指导委员会采用。
该指导原则要求,如果某个药品的生产或纯化过程可导致溶剂残留,就应对这个药品进行检测,并且只检测生产过程或纯化中使用或产生的那种溶剂。
根据使用量的多少,可采用累加的方法计算药品中残留溶剂的量。
如果累加量低于或等于指导原则中的推荐量,则该药品无需进行残留溶剂检测;如果累加量高于推荐量,则必须对该药品进行残留溶剂检测。
该指导原则适用于颁布以后上市的所有剂型和给药途径,但不适用于在临床研究阶段使用的潜在新药和新辅料,也不适用于已上市的现有药物。
在某些情况如短期(小于30天)或局部应用下,视具体情况,溶剂的高残留量也可接受。
按照毒性大小和对环境的危害程度,该指导原则将溶剂分成三类(所列举的溶剂并不完全,应对合成和生产过程所有可能的残留溶剂进行评估):第一类溶剂是指已知可以致癌并被强烈怀疑对人和环境有害的溶剂。
在可能的情况下,应避免使用这类溶剂。
如果在生产治疗价值较大的药品时不可避免地使用了这类溶剂,除非能证明其合理性,残留量必须控制在规定的范围内,如:苯(2ppm)、四氯化碳(4ppm)、1,2-二氯乙烷(5ppm)、1,1-二氯乙烷(8ppm)、1,1,1-三氯乙烷(1500ppm)。
ICH_Q3c_杂质:残余溶剂的指导原则(中文版)纯净版

ICH_Q3c_杂质:残余溶剂的指导原则(中文版)纯净版杂质:残留溶剂的指导原则杂质:残留溶剂的指导原则1.介绍本指导原则旨在介绍药物中残留溶剂在保证人体安全条件下的可接受量,指导原则建议使用低毒的溶剂,提出了一些残留溶剂毒理学上的可接受水平。
药物中的残留溶剂在此定义为在原料药或赋形剂的生产中,以及在制剂制备过程中产生或使用的有机挥发性化合物,它们在工艺中不能完全除尽。
在合成原料药中选择适当的溶剂可提高产量或决定药物的性质,如结晶型。
纯度和溶解度。
因此.有时溶剂是合成中非常关键的因素。
本指导原则所指的溶剂不是谨慎地用作赋形剂的溶剂,也不是溶剂化物,然而在这些制剂中的溶剂含量也应进行测定,并作出合理的判断。
出于残留溶剂没有疗效,故所有残留溶剂均应尽可能.去,以符合产品规范、GMP 或其他基本的质量要求。
制剂所含残留溶剂的水平不能高于安全值,已知一些溶剂可导致不接受的毒性(第一类,表 1),除非被证明特别合理,在原药、赋形剂及制剂生产中应避免使用。
一些溶剂毒性不太大(第二类,表2)应限制使用,以防止病人潜在的不良反应。
使用低毒溶剂(第三类,表 3)较为理想。
附录 1 中列出了指导原则中的全部溶剂。
第 1 页共 18 页杂质:残留溶剂的指导原则表中所列溶剂并非详尽无遗,其他可能使用的溶剂有待日后补充列人。
第一、二类溶剂的建议限度或溶剂的分类会随着。
新的安全性资料的获得而调整。
含有新溶剂的新药制剂、其上市申请的安全性资料应符合本指导原则或原料药指导原则(Q3A 新原料药中的杂质)或新药制剂(Q3B 新药制剂中的杂质)中所述的杂质控制原则,或者符合上述三者。
2. 指导原则的范围指导原则范围包括原料药、赋形剂或制剂中所含残留溶剂.因此,当生产或纯化过程中会出现这些溶剂时。
应进行残留溶剂的检验。
也只有在上述情况下,才有必要作溶剂的检查。
虽然生产商可以选择性地测定制剂,但也可以从制剂中各成分的残留溶液水平来累积计算制剂中的残留溶剂。
溶剂分类

溶剂分类常用有机溶剂分类第一类溶剂是指已知可以致癌并被强烈怀疑对人和环境有害的溶剂。
在可能的情况下,应避免使用这类溶剂。
如果在生产治疗价值较大的药品时不可避免地使用了这类溶剂,除非能证明其合理性,残留量必须控制在规定的范围内,如:苯(2ppm)、四氯化碳(4ppm)、1,2-二氯乙烷(5ppm)、1,1-二氯乙烷(8ppm)、1,1,1-三氯乙烷(1500ppm)。
第二类溶剂是指无基因毒性但有动物致癌性的溶剂。
按每日用药10克计算的每日允许接触量如下: 2-甲氧基乙醇(50ppm)、氯仿(60ppm)、1,1,2-三氯乙烯(80ppm)、1,2-二甲氧基乙烷(100ppm)、1,2,3,4-四氢化萘(100ppm)、2-乙氧基乙醇(160ppm)、环丁砜(160ppm)、嘧啶(200ppm)、甲酰胺(220ppm)、正己烷(290ppm)、氯苯(360ppm)、二氧杂环己烷(380ppm)、乙腈(410ppm)、二氯甲烷(600ppm)、乙烯基乙二醇(620ppm)、N,N-二甲基甲酰胺(880ppm)、甲苯(890ppm)、N,N-二甲基乙酰胺(1090ppm)、甲基环己烷(1180ppm)、1,2-二氯乙烯(1870ppm)、二甲苯(2170ppm)、甲醇(3000ppm)、环己烷(3880ppm)、N-甲基吡咯烷酮(4840ppm)、。
第三类溶剂是指对人体低毒的溶剂。
急性或短期研究显示,这些溶剂毒性较低,基因毒性研究结果呈阴性,但尚无这些溶剂的长期毒性或致癌性的数据。
在无需论证的情况下,残留溶剂的量不高于0.5%是可接受的,但高于此值则须证明其合理性。
这类溶剂包括:戊烷、甲酸、乙酸、乙醚、丙酮、苯甲醚、1-丙醇、2-丙醇、1-丁醇、2-丁醇、戊醇、乙酸丁酯、三丁甲基乙醚、乙酸异丙酯、甲乙酮、二甲亚砜、异丙基苯、乙酸乙酯、甲酸乙酯、乙酸异丁酯、乙酸甲酯、3-甲基-1-丁醇、甲基异丁酮、2-甲基-1-丙醇、乙酸丙酯。
一二三类有机溶剂分类

一二三类有机溶剂分类集团文件发布号:(9816-UATWW-MWUB-WUNN-INNUL-DQQTY-
第一类有机溶剂
是指已知可以致癌并被强烈怀疑对人和环境有害的溶剂。
苯、四氯化碳、1,2-二氯乙烷、、1,1,1-三氯乙烷
第二类有机溶剂
是指无基因毒性但有动物致癌性的溶剂。
2-甲氧基乙醇、氯仿、1,1,2-三氯乙烯、1,2-二甲氧基乙烷、1,2,3,4-四氢化萘、2-乙氧基乙醇、环丁砜、嘧啶、甲酰胺、正己烷、氯苯、二氧杂环己烷、乙腈、二氯甲烷、乙烯基乙二醇、N,N-二甲基甲酰胺、甲苯、N,N-二甲基乙酰胺、甲基环己烷、1,2-二氯乙烯、二甲苯、甲醇、环己烷、N-甲基吡咯烷酮。
第三类有机溶剂
是指对人体低毒的溶剂。
这类溶剂包括:
戊烷、甲酸、乙酸、乙醚、丙酮、苯甲醚、1-丙醇、2-丙醇、1-丁醇、2-丁醇、戊醇、乙酸丁酯、三丁甲基乙醚、乙酸异丙酯、甲乙酮、二甲亚砜、异丙基苯、乙酸乙酯、甲酸乙酯、乙酸异丁酯、乙酸甲酯、3-甲基-1-丁醇、甲基异丁酮、2-甲基-1-丙醇、乙酸丙酯。
精心搜集整理,只为你的需要。
ICH常用有机溶剂分类及残留限度

ICH常用有机溶剂分类及残留限度2009-12-0411:50??????残留溶剂无防治作用并可能对人体的健康和环境造成危害,本文对国际协调大会(ICH)制订的指导原则及各国执行情况作了较为详尽的介绍。
????药品的残留溶剂,又称有机挥发性杂质,是指在活性药物成分、辅料和药品生产过程中使用和产生的有机挥发性化学物质。
药品还可被来自包装、运输、仓储中的有机溶剂污染。
药品生产商有责任确保终产品中的任何一种残留溶剂对人体无害。
????各国药监部门曾使用不同的药品残留溶剂指导原则,为此国际组织展开了协调工作。
经相关程序讨论和审查后,国际协调大会的指导原则于1997年7月17日获得通过,被推荐至国际协调大会(ICH)的指导委员会采用。
该指导原则要求,如果某个药品的生产或纯化过程可导致溶剂残留,就应对这个药品进行检测,并且只检测生产过程或纯化中使用或产生的那种溶剂。
根据使用量的多少,可采用累加的方法计算药品中残留溶剂的量。
如果累加量低于或等于指导原则中的推荐量,则该药品无需进行残留溶剂检测;如果累加量高于推荐量,则必须对该药品进行残留溶剂检测。
该指导原则适用于颁布以后上市的所有剂型和给药途径,但不适用于在临床研究阶段使用的潜在新药和新辅料,也不适用于已上市的现有药物。
在某些情况如短期(小于30天)或局部应用下,视具体情况,溶剂的高残留量也可接受。
???按照毒性大小和对环境的危害程度,该指导原则将溶剂分成三类(所列举的溶剂并不完全,应对合成和生产过程所有可能的残留溶剂进行评估):第一类溶剂是指已知可以致癌并被强烈怀疑对人和环境有害的溶剂。
在可能的情况下,应避免使用这类溶剂。
如果在生产治疗价值较大的药品时不可避免地使用了这类溶剂,除非能证明其合理性,残留量必须控制在规定的范围内,如:苯(2ppm)、四氯化碳(4ppm)、1,2-二氯乙烷(5ppm)、1,1-二氯乙烷(8ppm)、1,1,1-三氯乙烷(1500ppm)。
ICH Q C一类二类三类溶剂

一类溶剂:已知可致癌且对人和环境有害的溶剂,尽可能避免使用(事实上很多大公司如罗氏等已将这些甚至包括某些二类溶剂打入“黑名单”),如果实在无法避免,残留量必须控制在规定限度:苯(2ppm)四氯化碳(4ppm)1,2-二氯乙烷(5ppm)(我注意到隆莱还有使用)1,1-二氯乙烯(8ppm)1,1,1-三氯乙烷(1500ppm)二类溶剂:有动物致癌性的溶剂,按每日允许接触量计算的规定限度如下:乙腈(410ppm)氯苯(360ppm)氯仿(60ppm)(罗氏禁用)环己烷(3880ppm)1,2-二氯乙烯(1870ppm)二氯甲烷(600ppm)1,2-二甲氧乙烷(100ppm)N,N-二甲基乙酰胺(1090ppm)DMF(880ppm)二氧六环(380ppm)2-乙氧基乙醇(160ppm)乙二醇(620ppm)甲酰胺(220ppm)正己烷(290ppm)甲醇(3000ppm)乙二醇甲醚(50ppm)甲丁酮(50ppm)甲基环己烷(1180ppm)N-甲基吡咯烷酮(4840ppm)硝基甲烷(50ppm)吡啶(200ppm)环丁砜(160ppm)1,2,3,4-四氢化萘(100ppm)甲苯(890ppm)1,1,2-三氯乙烯(80ppm)二甲苯(2170ppm)三类溶剂:低毒溶剂,限度为≤0.5%,即5000ppm,如我们常用的乙醇、EA、TBME、丙酮、THF、庚烷、异丙醇等除上述三类溶剂外,还有一些溶剂如我们用过的石油醚、甲基四氢呋喃等尚无毒理资料,必须证明其残留量的合理性。
尤其石油醚,建议今后避免使用,尤其在后道反应最好避免,由于其成分复杂,无法测定准确残留量。
总之,在工艺开发阶段应优先选择三类溶剂,控制二类溶剂,尽量避免一类溶剂的使用。
ICH Q3c 杂质:残余溶剂的指导原则(中文版)

杂质:残留溶剂的指导原则杂质:残留溶剂的指导原则1.介绍 本指导原则旨在介绍药物中残留溶剂在保证人体安全条件下的 可接受量,指导原则建议使用低毒的溶剂,提出了一些残留溶剂毒理 学上的可接受水平。
药物中的残留溶剂在此定义为在原料药或赋形剂的生产中,以 及在制剂制备过程中产生或使用的有机挥发性化合物, 它们在工艺中 不能完全除尽。
在合成原料药中选择适当的溶剂可提高产量或决定药 物的性质,如结晶型。
纯度和溶解度。
因此.有时溶剂是合成中非常 关键的因素。
本指导原则所指的溶剂不是谨慎地用作赋形剂的溶剂, 也不是溶剂化物,然而在这些制剂中的溶剂含量也应进行测定,并作 出合理的判断。
出于残留溶剂没有疗效,故所有残留溶剂均应尽可能.去,以 符合产品规范、GMP 或其他基本的质量要求。
制剂所含残留溶剂的 水平不能高于安全值,已知一些溶剂可导致不接受的毒性(第一类, 表 1) ,除非被证明特别合理,在原药、赋形剂及制剂生产中应避免 使用。
一些溶剂毒性不太大(第二类,表 2)应限制使用,以防止病 人潜在的不良反应。
使用低毒溶剂(第三类,表 3)较为理想。
附录 1 中列出了指导原则中的全部溶剂。
第 1 页 共 18 页杂质:残留溶剂的指导原则表中所列溶剂并非详尽无遗, 其他可能使用的溶剂有待日后补充 列人。
第一、二类溶剂的建议限度或溶剂的分类会随着。
新的安全性 资料的获得而调整。
含有新溶剂的新药制剂、其上市申请的安全性资 料应符合本指导原则或原料药指导原则(Q3A 新原料药中的杂质) 或新药制剂(Q3B 新药制剂中的杂质)中所述的杂质控制原则,或者 符合上述三者。
2. 指导原则的范围 指导原则范围包括原料药、 赋形剂或制剂中所含残留溶剂. 因此, 当生产或纯化过程中会出现这些溶剂时。
应进行残留溶剂的检验。
也 只有在上述情况下,才有必要作溶剂的检查。
虽然生产商可以选择性 地测定制剂, 但也可以从制剂中各成分的残留溶液水平来累积计算制 剂中的残留溶剂。
医药中常用有机溶剂分类及残留限度

医药中常用有机溶剂分类及残留限度医药中常用有机溶剂分类及残留限度药品的残留溶剂无治疗作用并可能对人体的健康和环境造成危害,本文对国际协调大会(ICH)制订的指导原则及各国执行情况作了较为详尽的介绍。
药品的残留溶剂,又称有机挥发性杂质,是指在活性药物成分、辅料和药品生产过程中使用和产生的有机挥发性化学物质。
药品还可被来自包装、运输、仓储中的有机溶剂污染。
药品生产商有责任确保终产品中的任何一种残留溶剂对人体无害。
各国药监部门曾使用不同的药品残留溶剂指导原则,为此国际组织展开了协调工作。
经相关程序讨论和审查后,国际协调大会的指导原则于1997年7月17日获得通过,被推荐至国际协调大会(ICH)的指导委员会采用。
该指导原则要求,如果某个药品的生产或纯化过程可导致溶剂残留,就应对这个药品进行检测,并且只检测生产过程或纯化中使用或产生的那种溶剂。
根据使用量的多少,可采用累加的方法计算药品中残留溶剂的量。
如果累加量低于或等于指导原则中的推荐量,则该药品无需进行残留溶剂检测;如果累加量高于推荐量,则必须对该药品进行残留溶剂检测。
该指导原则适用于颁布以后上市的所有剂型和给药途径,但不适用于在临床研究阶段使用的潜在新药和新辅料,也不适用于已上市的现有药物。
在某些情况如短期(小于30天)或局部应用下,视具体情况,溶剂的高残留量也可接受。
按照毒性大小和对环境的危害程度,该指导原则将溶剂分成三类(所列举的溶剂并不完全,应对合成和生产过程所有可能的残留溶剂进行评估):第一类溶剂是指已知可以致癌并被强烈怀疑对人和环境有害的溶剂.在可能的情况下,应避免使用这类溶剂.如果在生产治疗价值较大的药品时不可避免地使用了这类溶剂,除非能证明其合理性,残留量必须控制在规定的范围内,如:苯(2ppm)、四氯化碳(4ppm)、1,2-二氯乙烷(5ppm)、1,1-二氯乙烷(8ppm)、1,1,1-三氯乙烷(1500ppm)。
第二类溶剂是指无基因毒性但有动物致癌性的溶剂。
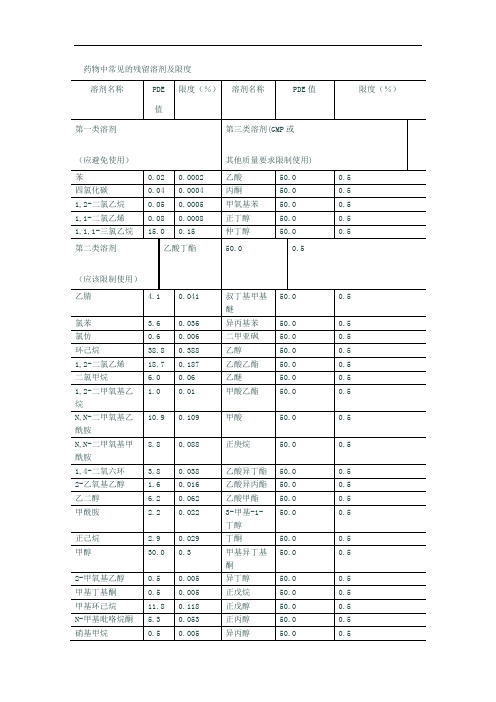
药物中常见残留溶剂及其限度
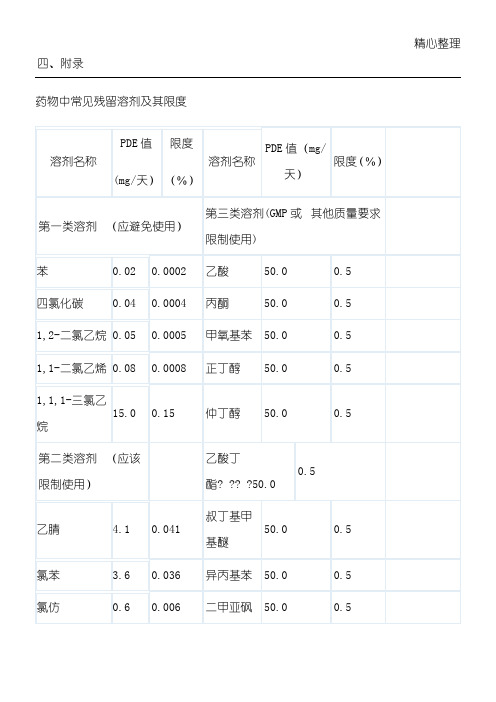
尚无足够毒性资料的溶剂
四氢化萘
1.0
0.01
1,1-二乙氧基丙烷
四氢呋喃
7.2
0.072
1,1-二甲氧基甲烷甲苯来自8.90.089
2,2-二甲氧基丙烷
1,1,2-三氯乙烯
0.8
0.008
异辛烷
二甲苯①
21.7
0.217
异丙醚
甲基异丙基酮
甲基四氢呋喃
石油醚
三氯乙酸
三氟乙酸
①通常含有60%间二甲苯,14%对二甲苯,9%邻二甲苯和17%乙苯
正庚烷
50.0
0.5
1,4-二氧六环
3.8
0.038
乙酸异丁酯
50.0
0.5
2-乙氧基乙醇
1.6
0.016
乙酸异丙酯
50.0
0.5
乙二醇
6.2
0.062
乙酸甲酯
50.0
0.5
甲酰胺
2.2
0.022
3-甲基-1-丁醇
50.0
0.5
正己烷
2.9
0.029
丁酮
50.0
0.5
甲醇
30.0
0.3
甲基异丁基酮
50.0
五、着者
《化学药物残留溶剂研究技术指导原则》课题研究组
50.0
0.5
环己烷
38.8
0.388
乙醇
50.0
0.5
1,2-二氯乙烯
18.7
0.187
乙酸乙酯
50.0
0.5
二氯甲烷
6.0
0.06
乙醚
50.0
0.5
1,2-二甲氧基乙烷
ich的分类

ich的分类Ich(简称ICH)是国际药品监管机构间合作的一个重要平台,旨在推动全球药品监管的协调与合作。
ICH的分类主要包括质量、安全和有效性三个方面。
本文将分别介绍这三个方面的内容。
一、质量质量是药品监管的重要方面,ICH在质量方面的工作主要涉及药品的生产、管理和控制。
ICH Q系列指南是ICH在质量方面的主要成果之一,如Q1A(R2) Stability Testing of New Drug Substances and Products、Q3C(R7) Impurities: Guideline for Residual Solvents、Q9 Quality Risk Management等。
ICH Q1A(R2) Stability Testing of New Drug Substances and Products指南规定了新药物及产品的稳定性测试的原则和方法,以确保药品在储存期限内的质量稳定性。
这对于药品的生产和使用具有重要意义,能够保证药品在储存和使用过程中的质量不受影响。
ICH Q3C(R7) Impurities: Guideline for Residual Solvents指南规定了药品中残留溶剂的限量要求,以保证药品的安全性和质量。
残留溶剂是药品生产过程中的一种不可避免的污染物,其含量过高可能对人体健康造成危害。
因此,该指南的制定对于保证药品的质量和安全性具有重要意义。
ICH Q9 Quality Risk Management指南指导药品制造商如何进行质量风险管理,以确保药品的质量和安全性。
这一指南强调了制造商在整个药品生产过程中应对可能的风险进行评估和控制,以最大程度地减少药品质量问题和安全隐患。
二、安全安全是药品监管的另一个重要方面,ICH在安全方面的工作主要涉及药品的临床试验、不良事件报告和风险评估等。
ICH E系列指南是ICH在安全方面的主要成果之一,如E6(R2) Good Clinical Practice、E2A Clinical Safety Data Management: Definitions and Standards for Expedited Reporting等。
ICH残留溶剂指南(中文翻译)

5.4残留溶剂在活性物质、赋形剂和药品中残留溶剂的级别限度International Conference on Technical Requirements for Registration of Pharmaceuticals for Human Use (ICH)已采用了关于残留溶剂的杂质指南,它规定了生产后允许残留在活性物质、赋形剂和药品中溶剂的含量限度。
本指南(文本复制见下文)不包括已上市的产品。
然而欧洲药典应用了存在的活性物质、赋形剂和药品指南中同样的原理,无论它们是否药典专论主题。
所有物质和产品都需要测定可能存在于物质或产品中的残留溶剂的含量。
如果异类溶剂的使用已被证明其合理性也已授权,那么它会在各个专论的测试部分受限定。
通常,药典专论不包括单一二类溶剂的测试限度,因为该类溶剂随生产商的不同变化很大。
因而生产工艺中使用该类溶剂时应通知主管当局。
这个通知也应随用于证明欧洲药典的实用型的档案一同提交,并在证明中提及。
当生产工艺中只使用了三类溶剂,可应用干燥失重测试,该测试应在单一专论中叙述。
如果三类溶剂的限度大于0.5%,并已经证明合理性和授权,那么还要求有该溶剂的指定的检测方法。
在这种情况下,限度在单一专论中给出,因为定义指的是无水和无溶剂的物质。
在所有情况下,应巴使用的溶剂通知主管当局。
至于二类溶剂,该通知已在适用性证明中提及。
当使用了一类残留溶剂或二类残留溶剂(或三类残留溶剂超过0.5%),应尽可能使用在一般方法(2.4.24)中叙述的方法学。
否则应使用经适当验证的方法。
_______________________杂质:残留溶剂指南(CPMP/ICH/283/95)1.引言2.指南的范围3.一般原则3.1.危险评估对溶剂的分类3.2.规定暴露限度的方法3.3.二类溶剂的限度叙述的选择3.4.分析规程3.5.残留溶剂的报告水平4.残留溶剂的限度4.1.避免使用的溶剂4.2.规定限度的溶剂4.3.低毒性潜能的溶剂4.4.未发现充分毒性数据的溶剂词汇表附录1. 溶剂列表包括指南附录2. 附加背景资料附录2.1: 有机挥发性溶剂的环境规程附录2.2: 药物中的残留溶剂附录3. 规定暴露限度的方法_______________________1.引言……(原文不清楚)。
有机残留溶剂量研究

合理 不合理
严格控制残留量 替代研究
临床研究前 临床研究期间 产品上市后
确定何种溶剂需进行研究的原则
意义和目的
保障临床用药安全,控制产品质量
与其他方面研究工作密不可分
进一步验证工艺控制的合理性 为确定合理可行的质量标准提供数据支持
思考的出发点
有机溶剂的毒性 产品的合成工艺
有机溶剂在合成过程中使用的步骤 后续溶剂的影响 中间体的影响 。。。。。。 有机溶剂的使用和残留与合成工艺密不可分,是评 价合成工艺优劣,筛选、确定合成工艺的重要 因素之一。
药物中有机溶剂的引入
第一类溶剂 原则:考虑其毒性,建议尽量避免使用。
当合成路线涉 及此类溶剂时 合成化学发展水平 判断使用 是否合理
第一类溶剂:无论任何步骤使用,均需进行研究 第二类溶剂:无论任何步骤使用,均需进行研究 第三类溶剂:无论任何步骤使用,均需进行研究 第四类溶剂:无论任何步骤使用,均需进行研究
质量标准的制订和修订
第一类溶剂:均需订入标准 由于第一类溶剂替代研究会在临床研究前、 临床研究期间、产品上讪后等不同阶段进行, 质量标准需替代研究结果的不断进行修订。
确定何种溶剂需进行研究的原则
EMEA
第一类溶剂:不建议使用。一旦作为起始原料、 溶剂,或者反应副产物,或者由其他溶剂带入 时,残留量需符合ICH相关规定。 残留量控制方法:随引入情况不同而不同
直接控制终端产品 控制中间体 控制引入第一类溶剂的物质
确定何种溶剂需进行研究的原则
有机残留溶剂量研究
前
言
定义:药物中的残留溶剂系指在原料药或辅 料的生产过程中,以及在制剂制备过程中使 用或产生的,但在工艺过程中未能完全去除 的有机溶剂。 研究的性质:杂质研究的范畴
ICHQC一类二类三类溶剂

一类溶剂:已知可致癌且对人和环境有害的溶剂;尽可能避免使用事实上很多大公司如罗氏等已将这些甚至包括某些二类溶剂打入“黑名单”;如果实在无法避免;残留量必须控制在规定限度:
苯2ppm
四氯化碳4ppm
1;2-二氯乙烷5ppm我注意到隆莱还有使用
1;1-二氯乙烯8ppm
1;1;1-三氯乙烷1500ppm
二类溶剂:有动物致癌性的溶剂;按每日允许接触量计算的规定限度如下:乙腈410ppm
氯苯360ppm
氯仿60ppm罗氏禁用
环己烷3880ppm
1;2-二氯乙烯1870ppm
二氯甲烷600ppm
1;2-二甲氧乙烷100ppm
N;N-二甲基乙酰胺1090ppm
DMF880ppm
二氧六环380ppm
2-乙氧基乙醇160ppm
乙二醇620ppm
甲酰胺220ppm
正己烷290ppm
甲醇3000ppm
乙二醇甲醚50ppm
甲丁酮50ppm
甲基环己烷1180ppm
N-甲基吡咯烷酮4840ppm
硝基甲烷50ppm
吡啶200ppm
环丁砜160ppm
1;2;3;4-四氢化萘100ppm
甲苯890ppm
1;1;2-三氯乙烯80ppm
二甲苯2170ppm
三类溶剂:低毒溶剂;限度为≤0.5%;即5000ppm;如我们常用的乙醇、EA、TBME、丙酮、THF、庚烷、异丙醇等
除上述三类溶剂外;还有一些溶剂如我们用过的石油醚、甲基四氢呋喃等尚无毒理资料;必须证明其残留量的合理性..尤其石油醚;建议今后避免
使用;尤其在后道反应最好避免;由于其成分复杂;无法测定准确残留量..总之;在工艺开发阶段应优先选择三类溶剂;控制二类溶剂;尽量避免一类溶剂的使用..。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
I C H Q C一类二类三类
溶剂
集团企业公司编码:(LL3698-KKI1269-TM2483-LUI12689-ITT289-
一类溶剂:已知可致癌且对人和环境有害的溶剂,尽可能避免使用(事实上很多大公司如罗氏等已将这些甚至包括某些二类溶剂打入“黑名单”),如果实在无法避免,残留量必须控制在规定限度:苯(2ppm)
四氯化碳(4ppm)
1,2-二氯乙烷(5ppm)(我注意到隆莱还有使用)
1,1-二氯乙烯(8ppm)
1,1,1-三氯乙烷(1500ppm)
二类溶剂:有动物致癌性的溶剂,按每日允许接触量计算的规定限度如下:
乙腈(410ppm)
氯苯(360ppm)
氯仿(60ppm)(罗氏禁用)
环己烷(3880ppm)
1,2-二氯乙烯(1870ppm)
二氯甲烷(600ppm)
1,2-二甲氧乙烷(100ppm)
N,N-二甲基乙酰胺(1090ppm)
DMF(880ppm)
二氧六环(380ppm)
2-乙氧基乙醇(160ppm)
乙二醇(620ppm)
甲酰胺(220ppm)
正己烷(290ppm)
甲醇(3000ppm)
乙二醇甲醚(50ppm)
甲丁酮(50ppm)
甲基环己烷(1180ppm)
N-甲基吡咯烷酮(4840ppm)
硝基甲烷(50ppm)
吡啶(200ppm)
环丁砜(160ppm)
1,2,3,4-四氢化萘(100ppm)
甲苯(890ppm)
1,1,2-三氯乙烯(80ppm)
二甲苯(2170ppm)
三类溶剂:低毒溶剂,限度为≤0.5%,即5000ppm,如我们常用的乙醇、EA、TBME、丙酮、THF、庚烷、异丙醇等
除上述三类溶剂外,还有一些溶剂如我们用过的石油醚、甲基四氢呋喃等尚无毒理资料,必须证明其残留量的合理性。
尤其石油醚,建议今后避免使用,尤其在后道反应最好避免,由于其成分复杂,无法测定准确残留量。
总之,在工艺开发阶段应优先选择三类溶剂,控制二类溶剂,尽量避免一类溶剂的使用。
