化学元素周期表-PPT课件
合集下载
初三化学元素周期表(完整版).pptx

57-71 La-Lu 镧 系
57
La
镧
58
Ce
铈
59
Pr
镨
60
Nd
钕
61
Pm
钷
62 Sm 钐 150.3 (shān)
63 Eu 铕 151.96 (yǒu)
64
Gd
钆
65
Tb
铽
66
Dy
镝
67 Ho 钬 164.9 (huǒ)
68 Er 铒 167.2 (ěr)
69 Tm 铥 168.9 (diū)
47.9 50.94
(guī) (lín) (liú) (lǜ) (yà) (jiǎ) (gài)
(tài) (fán)
65.38 69.72 72.5
(xīn) (jiā) (zhě)
83.8 85.467 87.62 88.906
(kè) (rú) (sī) (yǐ)
1
42
Mo
钼
43
Tc
锝
44 Ru 钌 161.0 (liǎo)
学海无 涯
初三化学元素周期表 原子序数 元素符号 元素名称 相对原子质量 元素名称读音
1 H 氢 1.0079 (qīng)
2 He 氦 4.0026 (hài)
3
Li
锂
4
Be
铍
5 B 硼 10.811 (péng)
6
C
碳
7
N
氮
8 O 氧 15.999 (yǎng)
9
F
氟
10
Ne
氖
11 Na 钠 22.9898 (nà)
钇
40 Zr 锆 91.22 (gào)
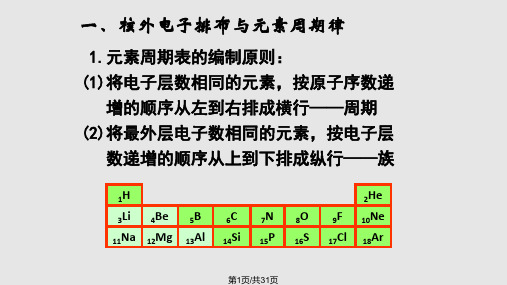
高三化学总复习之 元素周期律PPT课件
5
6
7
8
9
1 0
L K
8 2
3
11
1 2
III
B
IV B
VB
VI B
VII B
VIII
IB
II 1 B3
1 4
1 5
1 6
1 7
1 8
M L k
18 8 2
最4 外
1 9
2 0
2 1
2 2
2 3
24
25
26
2 7
2 8
2 9
3 0
3 1
3 2
3 3
3 4
3 5
3 6
层5 电
3
71
3
82
3 9
4 0
4 1
增 强
Rb Sr In Sn Sb Te I
酸 性 逐 渐 增 强
Cs Ba Tl Pb Bi Po At
碱性逐渐增强
第20页/共31页
3.气态氢化物的热稳定性
热稳定性增强
热 稳 定 性 减 弱
B CNO F
热
Si P S Cl
稳
定
As Se Br
性
Te I
增 强
At
热稳定性减弱
第21页/共31页
一、核外电子排布与元素周期律
1.元素周期表的编制原则: (1)将电子层数相同的元素,按原子序数递
增的顺序从左到右排成横行——周期 (2)将最外层电子数相同的元素,按电子层
数递增的顺序从上到下排成纵行——族
1H
2He
3Li 4Be 5B 6C 7N 8O 9F 10Ne
11Na 12Mg 13Al 14Si 15P 16S 17Cl 18Ar
人教版高中化学必修二第一章完整ppt课件

第一章 物质结构 元素周期律 第一节 元素周期表
ppt精选版
1
第1课时 元素周期表
ppt精选版
2
学习目标
1.简单了解元素周期表的发展历程。 2.了解元素周期表的编排规则及结构。 3.能描述元素在元素周期表中的位置。
ppt精选版
3
一、元素周期表的完善历程 1. 第一张元素周期表 (1)时间 1869 年,俄国化学家门__捷__列__夫__绘制出第一张元素周期 表,是化学发展史上的重要里程碑。 (2)编排原则 ①将元素按照_相__对__原__子__质__量_____由小到大依次排列。 ②将_化__学__性__质_相似的元素放在一个纵行。
答案:C
ppt精选版
28
解析:考查元素周期表的结构。对主族元素,其族序数 等于最外层电子数,但副族则不是;18 列构成 16 个族,其 中第Ⅷ族包含 3 列。
ppt精选版
29
3. 已知某离子的结构示意图为 的是( )
A. 该元素位于第二周期第ⅡA 族 B. 该元素位于第二周期第Ⅷ族 C. 该元素位于第三周期第ⅡA 族 D. 该元素位于第三周期 0 族
ppt精选版
18
4. 确定该元素在周期表中的位置,形式为“第几周期第 几族”,要注意分清主族、副族、0 族、第Ⅷ族
在应用上述方法推断元素的族序数时,要特别注意第 六、七周期第ⅢB 族的锕系和镧系元素,它们的每个空格都 有 15 种元素,其后的元素需再减去 14,然后定位。
ppt精选版
19
例 2 俄罗斯科学家用含 20 个质子的钙的一种原子轰击 含 95 个质子的镅原子,结果 4 次成功合成 4 个第 115 号元 素的原子。这 4 个原子生成数微秒后衰变成第 113 号元素。 下列有关叙述正确的是( )
ppt精选版
1
第1课时 元素周期表
ppt精选版
2
学习目标
1.简单了解元素周期表的发展历程。 2.了解元素周期表的编排规则及结构。 3.能描述元素在元素周期表中的位置。
ppt精选版
3
一、元素周期表的完善历程 1. 第一张元素周期表 (1)时间 1869 年,俄国化学家门__捷__列__夫__绘制出第一张元素周期 表,是化学发展史上的重要里程碑。 (2)编排原则 ①将元素按照_相__对__原__子__质__量_____由小到大依次排列。 ②将_化__学__性__质_相似的元素放在一个纵行。
答案:C
ppt精选版
28
解析:考查元素周期表的结构。对主族元素,其族序数 等于最外层电子数,但副族则不是;18 列构成 16 个族,其 中第Ⅷ族包含 3 列。
ppt精选版
29
3. 已知某离子的结构示意图为 的是( )
A. 该元素位于第二周期第ⅡA 族 B. 该元素位于第二周期第Ⅷ族 C. 该元素位于第三周期第ⅡA 族 D. 该元素位于第三周期 0 族
ppt精选版
18
4. 确定该元素在周期表中的位置,形式为“第几周期第 几族”,要注意分清主族、副族、0 族、第Ⅷ族
在应用上述方法推断元素的族序数时,要特别注意第 六、七周期第ⅢB 族的锕系和镧系元素,它们的每个空格都 有 15 种元素,其后的元素需再减去 14,然后定位。
ppt精选版
19
例 2 俄罗斯科学家用含 20 个质子的钙的一种原子轰击 含 95 个质子的镅原子,结果 4 次成功合成 4 个第 115 号元 素的原子。这 4 个原子生成数微秒后衰变成第 113 号元素。 下列有关叙述正确的是( )
第一节元素周期表(共40张PPT)
第ⅦA 族
与水缓慢反应
(2)原子结构特点 Cl2+H2O=HCl+HClO
静置后,液体分为两层。
通一过个以 12上C相质比量较同×,1点/思12考:钠和钾最的外性质层有 7个电子
静置后,液体分为两层。
和递变性。 (氧化性:Cl2 >I2)
核电荷数依次增多
不同点: 电子层数依次增多 上层无色,下层分别呈橙红色、紫红色
第一章 物质结构、元素周期律
第一节 元素周期表 一、元素周期表的结构
原子序数:依原子核电荷数由小到大的顺序给元素编号,这种
编号叫原子序数。
原子序数=核电荷数=质子数=核外电子数 (一)元素周期表的编排原则
1、横行: 把电子层数相同的各种元素按原子序数递增顺序
从左到右排列。
2、纵行: 把最外层电子数相同的各种元素按电子层数递增顺序 从上而下排成。
性逐渐增强,非金属性逐渐减弱。
2. 元素性质与原子结构有有密切的关系,主要与原子
核外的排布,特别是最外层电子数有关。原子结构
相似的一族元素,它们在化学性质上表现出相似性 和递变性。
1、砹(At)原子序数85,与F、Cl、Br、I同族,推测砹或
砹的化合物不可能具有的性质是( B)
A、砹易溶于某些有机溶剂 B、砹能与水剧烈反应
应越来越
,剧生烈成的氧化物越来越
。
最高复价杂氧化物对应水化物的碱性越来越 。
强
讨论1:Li与K 应如何保存? Li封存于固体石蜡中, 少量K保存于煤油中。
讨论2:碱金属与盐酸: 2R+2H+= 2R++H2 ↑ 讨论3:碱金属与盐溶液: 先与水反应
讨论4:Li+、Na+、K+、Rb+、Cs+也具有强还原性吗? 没有。 有较弱的氧化性。 氧化性: Li+ > Na+ > K+ > Rb+ > Cs+
人教版高中化学选修三课件:第一章 第二节 第二课时 元素周期律(29张PPT)

电负性
1.电负性 (1)概念 ①键合电子:原子中用于形成 化学键 的电子。 ②电负性:用来描述不同元素的原子对 键合电子 吸引力 的大小。电负性越大的原子,对键合电子的吸引力 越大 。 (2)衡量标准 电负性是由美国化学家 鲍林 提出的,他以氟的电负性为 4.0 作为相对标准,得出了各元素的电负性。
5.已知元素的电负性和原子半径一样,也是元素的一种基本性质,下表给
出14种元素的电负性:
元素 Al B Be C Cl F Li Mg N Na O P S Si
电负 1.5 2.0 1.5 2.5 3.0 4.0 1.0 1.2 3.0 0.9 3.5 2.1 2.5 1.8
1.离子半径大小比较的规律 (1)同种元素的离子半径:阴离子大于原子,原子大于阳离 子,低价阳离子大于高价阳离子。如r(Cl-)>r(Cl),r(Fe)>r(Fe2+) >r(Fe3+)。 (2)电子层结构相同的离子,核电荷数越大,半径越小。如 r(O2-)>r(F-)>r(Na+)>r(Mg2+)>r(Al3+)。 (3)带相同电荷的离子,电子层数越多,半径越大。如r(Li+) <r(Na+)<r(K+)<r(Rb+)<r(Cs+),r(O2-)<r(S2-)<r(Se2-)<r(Te2-)。
1.判断正误(正确的打“√”,错误的打“×”)。
(1)电负性是人为规定的一个相对数值,不是绝对标准 ( √ )
(2)元素电负性的大小反映了元素对键合电子引力的大小( √ )
(3)元素的电负性越大,则元素的非金属性越强
ቤተ መጻሕፍቲ ባይዱ
(√ )
(4)同一周期电负性最大为稀有气体元素
元素周期表_课件PPT

人类在长期的生产活动和科学实践中,逐步认识了元 素间的内在联系和元素性质变化的规律性。那么同族元素 间有哪些规律存在呢?让我们一起走进丰富多彩的物质世 界,共同探讨元素的性质与原子结构的关系。
●梳理导引 1.碱金属元素原子的最外层都有______________个 电子,都是活泼的金属;且随核电荷数增加,电子层数逐 渐______________,原子半径逐渐______________,金属 性逐渐____________。 2.碱金属单质的物理性质:都有______________的 金属光泽,质______________,密度______________,熔 点____________,导电性和导热性都____________;随着 核电荷数增加,碱金属单质的熔、沸点逐渐____________, 密度逐渐____________[特殊的ρ(K)<ρ(Na)]。
4.比较元素金属性强弱的方法 (1)根据金属活动性顺序表判断。自左至右金属性减弱, 即失电子能力减弱,如:Zn>Cu。 (2)根据元素周期表判断。同周期,从左至右金属性减 弱 。 同 主 族 , 自 上 而 下 金 属 性 增 强 。 如 : Na>Mg>Al , Na<K。 (3)根据元素的单质与水(或酸)反应置换出氢的难易程 度判断。置换反应越易发生的元素金属性越强。如钾与水 比钠与水反应剧烈,则K>Na(金属性)。
溶液分上 下两层,下层呈 红棕色
Cl2+ 2NaBr===2NaCl+Br2
b.将少量新制的饱 和氯水加入盛有KI溶液 的试管,振荡后加CCl4, 振荡,静置
溶液分上 下两层,下层呈 紫红色
+I2
Cl2+2KI===2KCl
实验
c.将少量溴水加 入盛有KI溶液的试管, 振荡后加CCl4,振荡,
人教版高中化学必修二第一章第一节 《元素周期表 》课件(共15张PPT)

B.原子的核外电子数
C.原子核内的质子数
√D.原子的中子数
1.原子序数为 x 的元素位于第IA族,那么原子序 数为 x+2 的元素肯定不会在( )
√ A.第 IA 族 B.第ⅢB族 C.第ⅢA族 D.0族
【提示】若x为氢元素,则A正确;若x为锂或钠, 则C正确;若x在第4、5、6、7周期,则B项正确。 故答案为D。
3.第ⅠA族和0族元素的原子序数
4.每周期元素的种数
一、元素周期表的结构 “三短”“四长”;“七主”“七副”“0族和Ⅷ族” 二、元素原子结构与其在周期表中位置的关系.
周期序数=电子层数 主族序数=最外层电子数
原子序数
核外电子排布
周期表中位置
1.不能作为元素周期表中元素排列顺序的依据是
A.原子的核电荷数
螺旋式元素周期表
金字塔式元素周期表
1869年,俄国化学家门捷列夫将 元素按照相对原子质量由小到大 依次排列,制出了第一张元素周 期表,这就是现代元素周期表的 雏形。
第一章 物质结构 元素周期律
第一节 元素周期表
【思考与交流】
周期表的结构
阅读教材P4、5页并结合周期表,讨论以下问题
1.元素周期表的编排原则是什么?周期表有多 少横行,多少纵行,多少族?
A.若X是氢,则Y是氦
√C.若X是氟,则W是硫
B.若Y是氦,则Z是钠 D.若Y是氟,则Z是铝
例.已知某主族元素的原子结构示意图如下,判断 其位于第几周期,第几族?
【提示】X为第4周期,第ⅠA族;Y为第5周期,第 ⅦA族。
【记一记】
周期表的结构
1.原子序数=核电荷数=质子数=核外电子数
2.周期序数=电子层数 主族序数=最外层电子数
人教版高中化学必修二《元素周期律》ppt课件

通过对前面所学知识的归纳和比较, 过程与方法
掌握“位、构、性”的关系。 培养学生辩证唯物主义观点,培养学 情感、态度 生科学创造品质以及理论联系实际的 与价值观 能力。
自学导引
一、元素周期表的分区 元素周期表中以B、Al、Si、Ge、As、Sb、Te、Po、 At为分界线。 1.金属元素在分界线的________。 2.非金属元素在分界线的________。 3.稀有气体在________一列。
第一章
物质结构 元素周期律
第二节 元素周期律
第3课时 元素周期表和元素周期律的应用
自学导引 规律技巧 典例导析
随堂演练 课时作业
三维目标
1.掌握元素周期表和元素周期律的应用。 2.了解元素周期表中金属元素、非金属元 知识与技能 素的区分。 3.掌握元素的性质、原子结构、元素在周 期表中的位置之间的关系。
无论是同周期还是同主族元素中,a/b的值越小,元 素的金属性越强,其最高价氧化物对应水化物的碱性就越 强;反之,a/b的值越大,元素的非金属性越强,其最高 价氧化物对应水化物的酸性就越强。
(4)对角线规则:沿金属元素与非金属元素分界线方向 对角(左上角与右下角)的两主族元素的化学性质相似,这 一规律以第二、三周期元素间尤为明显,如铍与铝的化学 性质相似。
7.正负化合价的代数和为零,且气态氢化物中含氢 百分率最高的元素是C。
8.所形成气态氢化物最稳定的元素是F。 9.最高价氧化物对应的水化物酸性最强的是Cl。 10.所形成的化合物种类最多的是C。 11.原子序数、电子层数、未成对电子(单电子)数三 者均相等的是H。 12.只有负价无正价的是F。
13.单质和其最高价氧化物都是原子晶体的是Si。 14.气态氢化物在水中的溶解度最大的是N。 15.最轻的金属是锂[ρ(Li)=0.535g/cm3]。 16.同位素之一的原子核中只有质子而没有中子的元 素是H。 17.最高价氧化物及其水化物具有两性的元素是Al。 18.其单质可作半导体材料的是Si。 19.地壳中含量最高的元素是氧[ω(O)=48.60%]。
《元素周期表》课件ppt课件

观察,可得 A是氮元素
B是 氧元素
C是
二、元素的性质与原子结构
1.碱金属元素
元素 元素 名称 符号
核电 荷数
最外层电子 电子
数
层数
原子结构
相同点
递变性
锂
碱
金 属
钠
元
素钾
铷
Li
3
Na
11
K
19
Rb
37
1
2
最
1
3
1
外 层 都 有
核电 原 电子 子 荷层 半 数数 径
1
4
个
逐逐 逐
电
渐渐 渐
子
增增 增
1
原子 序数
6
13 34 53 88
周期 2 3 4 5 7
族 IVA IIIA VIA VIIA IIA
课 堂 练
4.下列各表为周期表的一部分(表中为 原子序数),其中正确的是(D )
习 (A)
(B)
234
2
11
10 11
19
(C) 6
18 19
(D) 67
11 12 13
14
24
31 32
课 堂 5、元素X的原子获得3个电子或元素Y的原 练 子失去2个电子后,它们的电子层结构与 习 氖原子的电子层结构相同。X、Y两种元
H、Be 、 Al
。
族序数等于周期序数2倍的元素
有: C S
。
周期序数=族序数2倍的有: Li、Ca
。
课 堂 7. A、B、C是周期表中相邻的三种元素, 练 其中A、B是同周期,B、C是同主族。此三 习 种元素原子最外层电子数之和为17,质子数
人教版高中化学必修二课件1.1.1元素周期表(46张)

3周期第ⅤA族。 答案:(1)18 ⅢA (2)第3周期第ⅦA族
(3)2
O、S
8
(4)磷
第3周期第ⅤA族
9.根据下表回答问题:
(1)元素⑦在周期表中的位置是_________________________。
2.试确定53号元素所在族,并总结确定元素所在族的方法。 提示:54-53=1,即53号元素在氙的左侧第一格,即第ⅦA族。
确定元素所在族的方法是:找出与所给元素原子序数相近的 0
族元素。然后求该元素与0族元素的原子序数之差,如果该元 素原子序数小于0族元素,则该元素在0族元素左侧的差值列;
如果该元素原子序数大于0族元素,则该元素在0族元素下一周
素的种数。例如,氯和溴的原子序数之差为:35-17=18(溴所 在第4周期所含元素的种数)。
【典题训练】 我国的纳米基础研究能力已跻身于世界前列,曾制得一种合成 纳米材料,其化学式为RN。已知该化合物中的Rn+核外有28个电 子,则R元素位于元素周期表的( A.第3周期第ⅤA族 B.第4周期第ⅢA族 C.第5周期第ⅢA族 )
D.第4周期第ⅤA族
【解题指南】解答该类题时应注意:
(1)准确判断该化合物中Rn+的化合价及离子的原子序数与电 子数之间的关系。 (2)熟记并利用稀有气体元素的原子序数给元素定位。
【解析】选B。据化学式RN知N为-3价,则R为+3价,所以R的原 子序数为28+3=31;与31最邻近的稀有气体元素的原子序数为 36(氪:第4周期),所以31-36=-5,因此R元素也在第4周期, 8-|-5|=3,则R元素在第ⅢA族,故选B。
1.周期表从左到右18列对应的族序数 列数 1 2 3 4 5 6 7 8、9、10 Ⅷ 18 0
(3)2
O、S
8
(4)磷
第3周期第ⅤA族
9.根据下表回答问题:
(1)元素⑦在周期表中的位置是_________________________。
2.试确定53号元素所在族,并总结确定元素所在族的方法。 提示:54-53=1,即53号元素在氙的左侧第一格,即第ⅦA族。
确定元素所在族的方法是:找出与所给元素原子序数相近的 0
族元素。然后求该元素与0族元素的原子序数之差,如果该元 素原子序数小于0族元素,则该元素在0族元素左侧的差值列;
如果该元素原子序数大于0族元素,则该元素在0族元素下一周
素的种数。例如,氯和溴的原子序数之差为:35-17=18(溴所 在第4周期所含元素的种数)。
【典题训练】 我国的纳米基础研究能力已跻身于世界前列,曾制得一种合成 纳米材料,其化学式为RN。已知该化合物中的Rn+核外有28个电 子,则R元素位于元素周期表的( A.第3周期第ⅤA族 B.第4周期第ⅢA族 C.第5周期第ⅢA族 )
D.第4周期第ⅤA族
【解题指南】解答该类题时应注意:
(1)准确判断该化合物中Rn+的化合价及离子的原子序数与电 子数之间的关系。 (2)熟记并利用稀有气体元素的原子序数给元素定位。
【解析】选B。据化学式RN知N为-3价,则R为+3价,所以R的原 子序数为28+3=31;与31最邻近的稀有气体元素的原子序数为 36(氪:第4周期),所以31-36=-5,因此R元素也在第4周期, 8-|-5|=3,则R元素在第ⅢA族,故选B。
1.周期表从左到右18列对应的族序数 列数 1 2 3 4 5 6 7 8、9、10 Ⅷ 18 0
人教版必修2化学:1.1 元素周期表 课件(共70张PPT)
当 Na、K 投入到盐溶液中 时,不是从溶液中置换出相对不活泼 的金属,而是先与水发生反应生成碱 与氢气,然后生成的碱再与盐发生复 分解反应。例如:Na 与 CuSO4 溶液的总 反应式为:2Na+CuSO4+2H2O Cu(OH)2 ↓+Na2SO4+H2↑。
【例 1】 下列说法中不正确的是 () A.锂与水反应不如钠与水反应剧烈 B.还原性:K>Na>Li,故 K 可以从 NaCl
气的活泼性强于溴单质?
1.相似性
(1)与 H2反应:X2+H2
2HX
(2)与活泼金属(如 Na)反
应:2Na+X2 2NaX
(3)与 H2O 反应
2.递变性 (1)氧化性与还原性
(2)与 H2反应的难易及氢化物稳定性(由 F2→I2) ①与 H2反应越来越难,生成的氢化物的稳定性 逐渐减弱,还原性逐渐增强。②氢化物中 HCl、 HBr、HI 的熔、沸点依次升高。 (3)卤素单质与变价金属(如 Fe)反应
三、核素 1.质量数 (1)定义:忽略电子的质量,将原子核内所 有质子和中子的相对质量取近似整数值 相加所得的数值,叫该原子的质量数。 (2)数值关系:质量数(A)=质子数+中子数。 (3)原子表示方法
X→元素符号,如37 Cl 表示质量数 17
为 37、质子数为 17 的氯原子。
2.核素 (1)定义 具有一定数目质子和一定数目中子 的一种原子。 (2)氢的三种核素
1.相似性(用 R 表示碱金属元素)
2.递变性
(1)与 O2反应 从 Li→Cs,与 O2 反应越来越剧烈,产 物越来越复杂; 如 Li 与 O2 反应只能生成 Li2O,Na 与 O2 反应还可以生成 Na2O2,而 K 与 O2 反 应能够生成 KO2等。
元素周期表ppt课件

通过元素周期表,可以了 解不同元素之间的组合规 律,指导新型材料的合成 。
分析材料组成
利用元素周期表,可以对 材料进行定性和定量分析 ,确定其组成元素及其比 例。
在能源科学研究中的应用
能源转换与储存
元素周期表中的元素可以用于能 源转换和储存,如利用过渡金属 元素制备催化剂,提高能源利用
效率。
能源材料研究
元素周期表的结构与特点
结构
元素周期表主要包括多个周期和多个族,每个周期和每个族都有特定的元素组 成和性质特征。
特点
元素周期表具有周期性和重复性,元素的性质随着原子序数的增加呈现出规律 性的变化。
02
元素周期表中的元素分类
金属元素
定义
金属元素是指在周期表中的具有金属特性的元素 。
特点
金属元素通常具有较高的原子序数和相对较大的 原子质量,具有导电和导热性。
稀有气体元素的化学反应性能变化规律
• 稀有气体元素:稀有气体元素位于元素周期表零族,其化学反 应性能非常不活泼,几乎不与任何其他元素发生化学反应。
05
元素周期表在科学研究中的应用
在材料科学研究中的应用
预测材料性质
元素周期表可以用于预测 材料的物理、化学性质, 如硬度、熔点、电导率等 。
指导材料合成
化合物结构研究
通过元素周期表,可以研究化合物的结构,预测 化合物的性质,为合成和设计新的化合物提供理 论支持。
化学史教育
元素周期表的发展历程也是化学史的重要内容, 有助于学生了解化学学科的发展历程。
在研究生化学教学中的应用
科研实践应用
在研究生阶段,元素周期表是科研实践的重要工具,通过元素周期 表可以研究新型材料、新药物等。
同一周期内,从左到右,电负性逐渐 增大
分析材料组成
利用元素周期表,可以对 材料进行定性和定量分析 ,确定其组成元素及其比 例。
在能源科学研究中的应用
能源转换与储存
元素周期表中的元素可以用于能 源转换和储存,如利用过渡金属 元素制备催化剂,提高能源利用
效率。
能源材料研究
元素周期表的结构与特点
结构
元素周期表主要包括多个周期和多个族,每个周期和每个族都有特定的元素组 成和性质特征。
特点
元素周期表具有周期性和重复性,元素的性质随着原子序数的增加呈现出规律 性的变化。
02
元素周期表中的元素分类
金属元素
定义
金属元素是指在周期表中的具有金属特性的元素 。
特点
金属元素通常具有较高的原子序数和相对较大的 原子质量,具有导电和导热性。
稀有气体元素的化学反应性能变化规律
• 稀有气体元素:稀有气体元素位于元素周期表零族,其化学反 应性能非常不活泼,几乎不与任何其他元素发生化学反应。
05
元素周期表在科学研究中的应用
在材料科学研究中的应用
预测材料性质
元素周期表可以用于预测 材料的物理、化学性质, 如硬度、熔点、电导率等 。
指导材料合成
化合物结构研究
通过元素周期表,可以研究化合物的结构,预测 化合物的性质,为合成和设计新的化合物提供理 论支持。
化学史教育
元素周期表的发展历程也是化学史的重要内容, 有助于学生了解化学学科的发展历程。
在研究生化学教学中的应用
科研实践应用
在研究生阶段,元素周期表是科研实践的重要工具,通过元素周期 表可以研究新型材料、新药物等。
同一周期内,从左到右,电负性逐渐 增大
