化工热力学第五章 习题解答
化工原理第五章习题及答案学习资料

A、N/>N;E、N/=N;
C、N/VN;D、判断依据不足。
2、 对某双组分理想物系,当温度t=80C时,PA°106.7kpa,PB40kpa,液相
摩尔组成Xa0.4,则与此液相组成相平衡的汽相组成yA为。B
A、0.5;B、0.64;C、0.72;D、0.6
3、恒摩尔流假定主要前提是两组分的分子汽化潜热相近,它只适用于理想物 系。此
变化前、后塔的操作线
Z
y
A
y
Z
X
X
X
附图1
附图2
附图3
10、精馏塔塔顶某理论板上汽相的露点温度为右、液相的泡点温度为t2,塔底
某理论板上汽相的露点温度为t3、液相的泡点温度为t4,试按从大到小顺序将 以上4个温度排列如下:。tqt3>t2鮎
11、 简单蒸馏的主要特点是。
间歇、不稳定、分离程度不高
12、 测得在精馏塔操作中,离开某块理论板的两股物流的组成分别为0.82和
多;
D、液相中易挥发组分进入汽相和汽相中难挥发组分进入液相的现象同时 发生。
10、 对于某理想溶液的平衡蒸馏,若维持进料量F、物料温度tF、蒸发室压强
P不变,而将物料浓度Xf增加,贝U气相馏出物组成Xd,气相馏出物量
D。C、A
A、变大B、变小C、不变D不确定
11、 精馏塔设计时,若F、Xf、Xd、X、V均为定值,将进料热状态从q=1变 为q>1,则设计所需理论板数。B
18、对于二元理想溶液,x-y图上的平衡曲线离对角线越近,说明该物
系。不容易分离
19、在精馏塔设计中,若Xf、Xd、R、q、Xw相同,则直接蒸汽加热与间接蒸汽
加热相比,Nt,间Nt,直;—D。>,>
化工热力学第五章习题解答

第五章 习题解答1. 在一定压力下,组成相同的混合物的露点温度和泡点温度不可能相同。
(错,在共沸点时相同) 2. 在(1)-(2)的体系的汽液平衡中,若(1)是轻组分,(2)是重组分,则11x y >,22x y <。
(错,若系统存在共沸点,就可以出现相反的情况) 3. 纯物质的汽液平衡常数K 等于1。
(对,因为111==y x ) 4. 在(1)-(2)的体系的汽液平衡中,若(1)是轻组分,(2)是重组分,若温度一定,则体系的压力,随着1x 的增大而增大。
(错,若系统存在共沸点,就可以出现相反的情况)5. 下列汽液平衡关系是错误的i i Solvent i v i i x H Py *,ˆγϕ=。
(错,若i 组分采用不对称归一化,该式为正确)6. 对于理想体系,汽液平衡常数K i (=y i /x i ),只与T 、P 有关,而与组成无关。
(对,可以从理想体系的汽液平衡关系证明) 7. 对于负偏差体系,液相的活度系数总是小于1。
(对) 8. 能满足热力学一致性的汽液平衡数据就是高质量的数据。
(错) 9. 逸度系数也有归一化问题。
(错) 10. EOS +γ法既可以计算混合物的汽液平衡,也能计算纯物质的汽液平衡。
(错) 二、选择题1. 欲找到活度系数与组成的关系,已有下列二元体系的活度系数表达式,βα,为常数,请决定每一组的可接受性 。
(D ) A 2211;x x βγαγ== B 12211;1x x βγαγ+=+=C 1221ln ;ln x x βγαγ==D 212221ln ;ln x x βγαγ==2. 二元气体混合物的摩尔分数y 1=0.3,在一定的T ,P 下,8812.0ˆ,9381.0ˆ21==ϕϕ,则此时混合物的逸度系数为 。
(C ) A 0.9097 B 0.89827C 0.8979D 0.9092三、填空题1. 说出下列汽液平衡关系适用的条件(1) l i v i f f ˆˆ= ______无限制条件__________; (2)i l i i v i x y ϕϕˆˆ= ______无限制条件____________; (3)i i si i x P Py γ= _________低压条件下的非理想液相__________。
化工热力学习题及答案第五章蒸汽动力循环和制冷循环

第五章 蒸汽动力循环和制冷循环5-3设有一台锅炉,每小时产生压力为2.5MPa ,温度为350C 的水蒸汽4.5吨,锅炉的给水温度为30C,给水压力2.5MPa 。
已知锅炉效率为70%,锅炉效率: 如果该锅炉耗用的燃料为煤,每公斤煤的发热量为 29260J • kg -1,求该锅炉每小时的耗煤量。
2.5MPa 40 C H 2OH 169.77kJ kg内插得到 2.5MPa 30C H 2O H 169.7:86.3l28.04kJ kg查水蒸汽表2.0MPa 320 C H 2O H 3069.5kJ kg 1锅炉在等压情况下每小时从锅炉吸收的热量:出口压力P 1 0.008MPa 。
如果忽略所有过程的不可逆损失,试求: (1 )汽轮机出口乏气 的干度与汽轮机的作功量;(2)水泵消耗的功量;(3)循环所作出的净功;(4)循环热效率。
解:朗肯循环在 T —S 图上表示如下:1点(过热蒸汽)性质:p 1 6MPa , t 1 540 C ,解:查水蒸汽表2.5MPa 20 C H 2O H 86.3kJ kg 锅炉每小时耗煤量:mcoal13490235658.6kg h 10.7 292601(3125.87 128.04) 31490235kJ hQ m H 2O H(H 2 H 1)4.5 1035- 4某朗肯循环的蒸汽参数为:进汽轮机的压力5 6MPa ,温度t 1 540 C ,汽轮机蒸汽吸收的热量 染料可提供的热量内插得到2.0MPa 查水蒸汽表内插得到3.0MPa 内插得到2.5MPa2.0MPa 360 C H 2O350 C H 2OH3.0MPa 320 C H 2O 3.0MPa 360 C H 2O350 C H 2O H 350 C H 2OHH 3159.3kJ 3159.3 3069.540 H 3043.4kJ H 3138.7kJ 3138.7 3043.4kg30 kg kg403114.88 3136.8530 3069.5 3043.4 3125.87kJ 3136.85kJ 3114.88kJkg 1kg 1 kg 12点(湿蒸汽)性质:S g 8.2287kJ kg 1V l 1.0084 cm 3g 11-2过程在膨胀机内完成,忽略过程的不可逆性,则该过程为等熵过程,S 2 S 1 6.9999kJ kg 1 K 12点汽液混合物熵值:循环热效率旦 1326・9 6.°420.3958H 4 3517.0 179.922(2)乏气的干度;(3)循环的气耗率;(4 )循环的热效率; (5)分析以上计算的结果。
化工热力学(天大)第5章习题答案新

第五章 习 题 答 案5-10 某二组元液体混合物在恒定T 及p 下的焓可用下式表示:)(2121211025450300x x x x x x H +++= 式中H 单位为1mol J -⋅。
试确定在该温度、压力状态下(1)用1x 表示的1H 和2H ; (2)纯组分焓1H 和2H 的数值;(3)无限稀释下液体的偏摩尔焓∞1H 和∞2H 的数值。
解:(1)已知 )1025(450300212121x x x x x x H +++= (A ) 由于 211x x -=故 )1025(450300212121x x x x x x H +++=)]1(1025)[1()1(450300111111x x x x x x -+-+-+= 31211155140450x x x -+-= (B ) 根据 P T x Hx H H ⋅∂∂-+=))(1(11 P T x Hx H H ⋅∂∂-=)(112 其中 211.14510140)(x x x HP T -+-=∂∂ 则:)4510140)(1(1551404502111312111x x x x x x H -+--+-+-= 31211305010310x x x +-+= (C ) )4510140(1551404502111312112x x x x x x H -+---+-= 3121305450x x +-= (D) (2) 将11=x 及01=x 分别代入式(B ),得纯组元的焓1H 和2H 11mol J 300-⋅=H 12mol J 450-⋅=H(3)∞1H 和∞2H 是指在01=x 及11=x 时的1H 和2H 的极限值。
将01=x 代入式(C )中得 11mol J 310-∞⋅=H将11=x 代入式(D )中得 12mol J 475-∞⋅=H 5-11 在303K 、105Pa 下,苯(1)和环己烷(2)的液体混合物的摩尔体积V 和苯的摩尔分数1x 的关系如下:21164.28.164.109x x V --=13-⋅mol cm试导出1V 和2V 和V Δ的表达式。
《化工热力学》详细课后习题标准答案(陈新志)

- 1 - / 1052习题第1章 绪言一、是否题1. 孤立体系的热力学能和熵都是一定值。
(错。
和,如一体积等于2V 的绝热刚性容器,被一理想的隔板一分为二,左侧状态是T ,P 的理想气体,右侧是T 温度的真空。
当隔板抽去后,由于Q =W =0,,,,故体系将在T ,2V ,0.5P 状态下达到平衡,,,)2. 封闭体系的体积为一常数。
(错)3. 封闭体系中有两个相。
在尚未达到平衡时,两个相都是均相敞开体系;达到平衡时,则两个相都等价于均相封闭体系。
(对)4. 理想气体的焓和热容仅是温度的函数。
(对)5. 理想气体的熵和吉氏函数仅是温度的函数。
(错。
还与压力或摩尔体积有关。
)6. 要确定物质在单相区的状态需要指定两个强度性质,但是状态方程 P=P (T ,V )的自变量中只有一个强度性质,所以,这与相律有矛盾。
(错。
V 也是强度性质)7. 封闭体系的1mol 气体进行了某一过程,其体积总是变化着的,但是初态和终态的体积相等,初态和终态的温度分别为T 1和T 2,则该过程的;同样,对于初、终态压力相等的过程有。
(对。
状态函数的变化仅决定于初、终态与途径无关。
)8. 描述封闭体系中理想气体绝热可逆途径的方程是(其中),而一位学生认为这是状态函数间的关系,与途径无关,所以不需要可逆的条件。
(错。
) 9. 自变量与独立变量是一致的,从属变量与函数是一致的。
(错。
有时可能不一致)10. 自变量与独立变量是不可能相同的。
(错。
有时可以一致)三、填空题1. 状态函数的特点是:状态函数的变化与途径无关,仅决定于初、终态 。
2. 单相区的纯物质和定组成混合物的自由度数目分别是 2 和 2 。
3. 封闭体系中,温度是T 的1mol 理想气体从(P ,V )等温可逆地膨胀到(P ,V ),则所做的功为i i f f(以V 表示)或 (以P 表示)。
4. 封闭体系中的1mol 理想气体(已知),按下列途径由T 1、P 1和V 1可逆地变化至P,则mol ,温度为 和水 。
化工热力学课后答案

化工热力学课后答案(填空、判断、画图)第1章 绪言一、是否题1. 封闭体系的体积为一常数。
(错)2. 封闭体系中有两个相βα,。
在尚未达到平衡时,βα,两个相都是均相敞开体系;达到平衡时,则βα,两个相都等价于均相封闭体系。
(对) 3. 理想气体的焓和热容仅是温度的函数。
(对)4. 理想气体的熵和吉氏函数仅是温度的函数。
(错。
还与压力或摩尔体积有关。
)5. 封闭体系的1mol 气体进行了某一过程,其体积总是变化着的,但是初态和终态的体积相等,初态和终态的温度分别为T 1和T 2,则该过程的⎰=21T T V dT C U ∆;同样,对于初、终态压力相等的过程有⎰=21T T P dT C H ∆。
(对。
状态函数的变化仅决定于初、终态与途径无关。
)二、填空题1. 状态函数的特点是:状态函数的变化与途径无关,仅决定于初、终态 。
2. 封闭体系中,温度是T 的1mol 理想气体从(P i ,V i )等温可逆地膨胀到(P f ,V f ),则所做的功为()f i rev V V RT W ln =(以V 表示)或()i f rev P P RT W ln = (以P 表示)。
3. 封闭体系中的1mol 理想气体(已知igP C ),按下列途径由T 1、P 1和V 1可逆地变化至P 2,则A 等容过程的 W = 0 ,Q =()1121T P P R C igP⎪⎪⎭⎫ ⎝⎛--,U =()1121T PP R C igP⎪⎪⎭⎫⎝⎛--,H =1121T P P C ig P ⎪⎪⎭⎫ ⎝⎛-。
B 等温过程的 W =21lnP P RT -,Q =21ln P PRT ,U = 0 ,H = 0 。
第2章P-V-T关系和状态方程一、是否题1. 纯物质由蒸汽变成液体,必须经过冷凝的相变化过程。
(错。
可以通过超临界流体区。
)2. 当压力大于临界压力时,纯物质就以液态存在。
(错。
若温度也大于临界温度时,则是超临界流体。
化工热力学第五章作业讲解上课讲义

化工热力学第五章作业讲解第五章 例题一、填空题1.指出下列物系的自由度数目,(1)水的三相点 0 ,(2)液体水与水蒸汽处于汽液平衡状态 1 ,(3)甲醇和水的二元汽液平衡状态 2 ,(4)戊醇和水的二元汽-液-液三相平衡状态 1 。
2.说出下列汽液平衡关系适用的条件(1)l i v i f f ˆˆ= ______无限制条件__________;(2)i l i i v i x y ϕϕˆˆ= ______无限制条件____________; (3)i i s i i x P Py γ= _________低压条件下的非理想液相__________。
3.丙酮(1)-甲醇(2)二元体系在98.66KPa 时,恒沸组成x 1=y 1=0.796,恒沸温度为327.6K ,已知此温度下的06.65,39.9521==s s P P kPa 则 van Laar 方程常数是A 12=______0.587_____,A 21=____0.717____(已知van Laar 方程为 221112212112x A x A x x A A RT G E+=)4.在101.3kPa 下四氯化碳(1)-乙醇(2)体系的恒沸点是x 1=0.613和64.95℃,该温度下两组分的饱和蒸汽压分别是73.45和59.84kPa ,恒沸体系中液相的活度系数693.1,38.121==γγ。
1.组成为x 1=0.2,x 2=0.8,温度为300K 的二元液体的泡点组成y 1的为(已知液相的3733,1866),/(75212121==+=s s E t P P n n n n G Pa) ___0.334____________。
2.若用EOS +γ法来处理300K 时的甲烷(1)-正戊烷(2)体系的汽液平衡时,主要困难是MPa P s4.251=饱和蒸气压太高,不易简化;( EOS+γ法对于高压体系需矫正)。
3.EOS 法则计算混合物的汽液平衡时,需要输入的主要物性数据是ij Ci Ci Ci k P T ,,,ω,通常如何得到相互作用参数的值?_从混合物的实验数据拟合得到。
高等化工热力学智慧树知到答案章节测试2023年武汉科技大学

第一章测试1.压力增大,物质的焓()。
A:增大B:不变C:二者无关D:减小答案:A2.理想气体的焓仅仅是温度的函数A:对B:错答案:A3.热力学第一定律不能用于孤立系统A:对B:错答案:A4.热力学只有3个定律A:对B:错答案:B5.绝对零度以下是不可能达到的A:错B:对答案:B第二章测试1.吉布斯自由能()。
A:恒大于内能B:恒小于内能C:恒大于焓D:恒小于焓答案:D2.压力增大,物质的内能()。
A:不能确定B:减小C:不变D:增大答案:D3.内能()。
A:只是温度的函数B:既是温度的函数,也是体积的函数C:既是温度的函数,也是压强和体积的函数D:既是温度的函数,也是压强的函数答案:C4.热力学温度()。
A:恒大于等于零B:恒大于零C:恒小于零D:恒小于等于零答案:B5.下列属于强度性质的物理量是()。
A:焓B:熵C:内能D:温度答案:D6.地球是一个()。
A:敞开系统B:什么都不是C:孤立系统D:封闭系统答案:A7.温度升高,物质的恒压热容()。
A:二者无关B:降低C:升高D:都有可能答案:D8.气体绝热可逆膨胀过程中熵变()。
A:小于零B:都有可能C:等于零D:大于零答案:C9.压力升高,物质的恒压热容()。
A:二者无关B:不能确定C:升高D:降低答案:C10.下列属于内能的是()。
A:电子间的相互排斥能B:分子的转动动能C:原子能D:分子间的相互作用能E:物体的转动动能答案:ABCD11.下列属于容量性质的状态函数有()。
A:焓B:温度C:自由能D:熵E:内能答案:ACDE12.下列无法知道绝对值的热力学函数有()。
A:熵B:自由能C:分子势能D:内能E:焓答案:ABDE13.熵与下列哪些因素有关()。
A:压强B:物质的质量C:温度D:分子量E:组成答案:ABCDE14.下列过程中熵增大的有()。
A:精馏B:结晶C:干燥D:吸收E:萃取答案:DE15.在一个隔离系统中,功可以完全转变成热,但热不能完全转变成功。
化工热力学习题答案 第一至五、第七章

第一章 绪论一、选择题(共3小题,3分)1、(1分)关于化工热力学用途的下列说法中不正确的是( ) A.可以判断新工艺、新方法的可行性。
B 。
优化工艺过程。
C 。
预测反应的速率。
D.通过热力学模型,用易测得数据推算难测数据;用少量实验数据推算大量有用数据。
E 。
相平衡数据是分离技术及分离设备开发、设计的理论基础.2、(1分)关于化工热力学研究特点的下列说法中不正确的是( ) (A )研究体系为实际状态。
(B )解释微观本质及其产生某种现象的内部原因. (C )处理方法为以理想态为标准态加上校正。
(D )获取数据的方法为少量实验数据加半经验模型。
(E )应用领域是解决工厂中的能量利用和平衡问题.3、(1分)关于化工热力学研究内容,下列说法中不正确的是( ) A.判断新工艺的可行性. B.化工过程能量分析。
C.反应速率预测。
D 。
相平衡研究参考答案一、选择题(共3小题,3分) 1、(1分)C 2、(1分)B 3、(1分)C第二章 流体的PVT 关系一、选择题(共17小题,17分)1、(1分)纯流体在一定温度下,如压力低于该温度下的饱和蒸汽压,则此物质的状态为( )。
A .饱和蒸汽 B.饱和液体 C .过冷液体 D 。
过热蒸汽2、(1分)超临界流体是下列 条件下存在的物质。
A 。
高于T c 和高于P cB 。
临界温度和临界压力下C 。
低于T c 和高于P cD 。
高于T c 和低于P c3、(1分)对单原子气体和甲烷,其偏心因子ω,近似等于 . A 。
0 B. 1 C. 2 D 。
34、(1分)0.1Mpa ,400K 的2N 1kmol 体积约为__________A 3326LB 332。
6LC 3.326LD 33.263m5、(1分)下列气体通用常数R 的数值和单位,正确的是__________ A K kmol m Pa ⋅⋅⨯/10314.833B 1。
987cal/kmol KC 82。
化工热力学第五章答案(全)
习 题 五一 是否题5-1 汽液平衡关系ˆˆV L i i f f =的适用的条件是理想气体和理想溶液。
解:否。
适用所有气体和溶液。
5-2 汽液平衡关系s i i i i py p x γ=的适用的条件是低压条件下的非理想液相。
解:是。
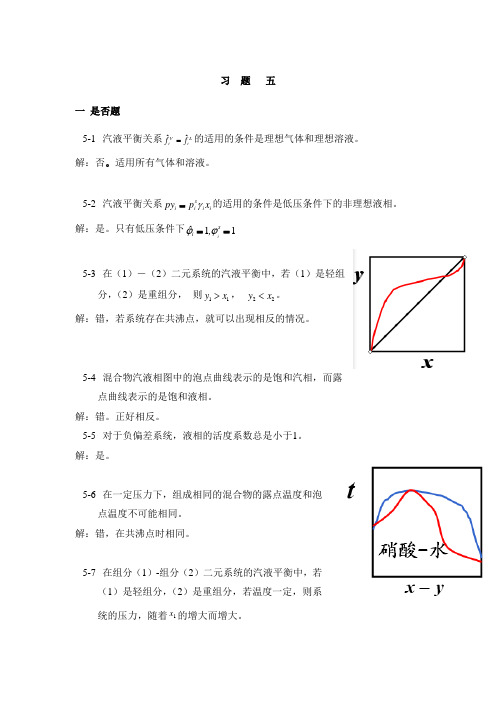
只有低压条件下11==i s i ˆ,ϕϕ5-3 在(1)-(2)二元系统的汽液平衡中,若(1)是轻组分,(2)是重组分, 则11y x >, 22y x <。
解:错,若系统存在共沸点,就可以出现相反的情况。
5-4 混合物汽液相图中的泡点曲线表示的是饱和汽相,而露点曲线表示的是饱和液相。
解:错。
正好相反。
5-5 对于负偏差系统,液相的活度系数总是小于1。
解:是。
5-6 在一定压力下,组成相同的混合物的露点温度和泡点温度不可能相同。
解:错,在共沸点时相同。
5-7 在组分(1)-组分(2)二元系统的汽液平衡中,若(1)是轻组分,(2)是重组分,若温度一定,则系统的压力,随着1x 的增大而增大。
解:错,若系统存在共沸点,就可以出现相反的情况。
5-8 理想系统的汽液平衡 K i 等于1。
解:错,理想系统即汽相为理想气体,液相为理想溶液,11==i s i ˆ,ϕϕ,1=i γ,但K i 不一定等于1。
5-9 对于理想系统,汽液平衡常数K i ,只与 T 、p 有关,而与组成无关。
解:对,对于 理想系统s s si i i i i i i y p p K x p p ϕϕ===,只与 T 、p 有关,而与组成无关。
5-10 能满足热力学一致性的汽液平衡数据就是高质量的数据。
解:错。
热力学一致性是判断实验数据可靠性的必要条件,但不是充分条件。
即符合热力学一致性的数据,不一定是正确可靠的;但不符合热力学一致性的数据,一定是不正确可靠的。
5-11 当潜水员深海作业时,若以高压空气作为呼吸介质,由于氮气溶入血液的浓度过大,会给人体带来致命影响(类似氮气麻醉现象)。
化工热力学-第五章

f i = γ iV yi fi0V^VVLE源自 VLE时γ yfi
0V i i
γ L xi f i0L =
i
5P119 5-14
1 P V S S V ∴ γ i y i i Pi exp ∫S Vi dP RT Pi
1 P V γ iV y i exp ∫S Vi dP RT Pi
纯组分的PT图可用两维 纯组分的PT图可用两维 PT 坐标表示出来。 坐标表示出来。
P
溶化线 汽化线 S 2 三相点 V 相 相 1 升华线 T
纯组分的汽液平衡表现为自由度为1 纯组分的汽液平衡表现为自由度为1; 汽液平衡时, 一定,对应的T也一定, 汽液平衡时 , 当 P 一定 , 对应的 T 也一定 , 也就是说对 于纯物质具有固定的沸点。 于纯物质具有固定的沸点。 对于二元组分, 它没有固定的沸点, 对于二元组分 , 它没有固定的沸点 , 沸点是对于纯物 质而言的; 质而言的; 对于混合物,只有泡点。 对于混合物,只有泡点。 泡点:当第一个气泡在一定压力下出现时的温度。 泡点:当第一个气泡在一定压力下出现时的温度。 露点:当最后一滴液体在一定压力下全部汽化时的 露点: 温度。 温度。
二. 低压下互溶体系的汽液平衡相图
对理想溶液(或拉乌尔定律)产生偏差的情况有四种。 对理想溶液(或拉乌尔定律)产生偏差的情况有四种。 1.一般正偏差体系(甲醇-水体系) 1.一般正偏差体系(甲醇-水体系) 一般正偏差体系 2.一般负偏差体系(氯仿-苯体系) 2.一般负偏差体系(氯仿-苯体系) 一般负偏差体系 3.最大正偏差体系(乙醇-苯体系) 3.最大正偏差体系(乙醇-苯体系) 最大正偏差体系 4.最小负偏差体系(氯仿-丙酮体系) 4.最小负偏差体系(氯仿-丙酮体系) 最小负偏差体系
化工热力学第五章作业讲解

第五章 例题一、填空题1. 指出下列物系的自由度数目,(1)水的三相点 0 ,(2)液体水与水蒸汽处于汽液平衡状态 1 ,(3)甲醇和水的二元汽液平衡状态 2 ,(4)戊醇和水的二元汽-液-液三相平衡状态 1 。
2. 说出下列汽液平衡关系适用的条件(1) l i v i f f ˆˆ= ______无限制条件__________; (2)i l i i v i x y ϕϕˆˆ= ______无限制条件____________; (3)i i s i i x P Py γ= _________低压条件下的非理想液相__________。
3. 丙酮(1)-甲醇(2)二元体系在98.66KPa 时,恒沸组成x 1=y 1=0.796,恒沸温度为327.6K ,已知此温度下的06.65,39.9521==s s P P kPa 则 van Laar 方程常数是A 12=______0.587_____,A 21=____0.717____(已知van Laar 方程为 221112212112x A x A x x A A RT G E+=)4. 在101.3kPa 下四氯化碳(1)-乙醇(2)体系的恒沸点是x 1=0.613和64.95℃,该温度下两组分的饱和蒸汽压分别是73.45和59.84kPa ,恒沸体系中液相的活度系数693.1,38.121==γγ。
1. 组成为x 1=0.2,x 2=0.8,温度为300K 的二元液体的泡点组成y 1的为(已知液相的3733,1866),/(75212121==+=s s E t P P n n n n G Pa) ___0.334____________。
2. 若用EOS +γ法来处理300K 时的甲烷(1)-正戊烷(2)体系的汽液平衡时,主要困难是MPa P s4.251=饱和蒸气压太高,不易简化;( EOS+γ法对于高压体系需矫正)。
3. EOS 法则计算混合物的汽液平衡时,需要输入的主要物性数据是ij Ci Ci Ci k P T ,,,ω,通常如何得到相互作用参数的值?_从混合物的实验数据拟合得到。
化工热力学习题及答案第五章蒸汽动力循环和制冷循环

第五章蒸汽动力循环和制冷循环5-3设有一台锅炉,每小时产生压力为 2.5MPa,温度为350C的水蒸汽4.5吨,锅炉的给水温度为30C,给水压力2.5MPa。
已知锅炉效率为70%,锅炉效率:-蒸汽吸收的热量染料可提供的热量如果该锅炉耗用的燃料为煤,每公斤煤的发热量为29260J • kg-1,求该锅炉每小时的耗煤量。
1解:查水蒸汽表 2.5MPa 20C出0 H =86.3kJ kg12.5MPa 40C H2O H = 169.77kJ kg2.0MPa 360 C H2O H =3159.3kJ kg3159 3 _ 3069 5 “内插得到 2.0MPa 350CH2。
H二.A。
.30 3069—3136.85kJ kg3.0MPa 360 C H2O H =3138.7kJ kg锅炉在等压情况下每小时从锅炉吸收的热量:Q =m H2O H(H2 -HJ =4.5 1 03(3125.87-128.04) = 31490235kJ h‘锅炉每小时耗煤量:13490235mcoal 658.6kg h0.7X292605- 4某朗肯循环的蒸汽参数为:进汽轮机的压力 5 =6MPa,温度匕=540 C,汽轮机出口压力P1 =0.008MPa。
如果忽略所有过程的不可逆损失,试求:(1 )汽轮机出口乏气的干度与汽轮机的作功量;(2)水泵消耗的功量;(3)循环所作出的净功;(4)循环热效率。
解:朗肯循环在T—S图上表示如下:1点(过热蒸汽)性质:5 = 6MPa , 1 = 540 C ,内插得到 2.5MPa 30C H2O169.77 86.321= 128.04kJ kg查水蒸汽表 2.0MPa 320 C H2O H =3069.5kJ kg查水蒸汽表 3.0MPa 320 C H2O H =3043.4kJ kg内插得到 3.0MPa 350C H2O内插得到 2.5MPa 350C H2O3138.7 -3043.4 30 • 3043.4 =3114.882 kg,40H =3114.88 3136.85~25.87kJ 心H l =121.46kJ kg 4 S^ 0.4 2 26J kgH ^3517.0kJ kg J 5=6.9999^ kg -2点(湿蒸汽)性质:p 2 =0.008MPa , S 2 = S | =6.9999kJ kg 」K 」H l =173.88kJ kg JS =0.5 0 26J kg JH g =2577kJ kg J S g -8.228U kg J V l = 1.0084cm 3 g J1-2过程在膨胀机内完成,忽略过程的不可逆性,则该过程为等熵过程,S 2=S , =6.9999kJ kg 1 K J(1) 设2点干度为x ,由汽液混合物的性质计算可知:xS g (1 -x)S ] = S 26・9999 一 °592J 0.8398.2287-0.59262点汽液混合物熵值:H 2 =xH g (1_x)H 「2577 0.839 (1 -0.839) 173.88 =2190.10kJ kg ,汽轮机向外作功: W S = H 2 -比= —3117.0 2190.1 =-1326.9kJkg 」6 10666 1W p 二V^p =1.0084 (6 -0.008) 1010 = 6.042kJ kg0.008 106循环所做净功: W 净二-(W S W p )二 -(-1326.9 6.042) = 1320.86kJkg J 循环热效率H 4 =H 3 W p =H l W p -173.88 6.042 =179.922kJ kg'5- 16某蒸汽厂采用朗肯循环操作,已知进入汽轮机的蒸汽温度为500C ,乏气压力为0.004MPa ,试计算进入汽轮机的蒸汽压力分别为 4MPa 和14MPa 时,(1)汽轮机的作功量; (2)乏气的干度;(3)循环的气耗率;(4)循环的热效率;(5)分析以上计算的结果。
化工热力学习题解答第五~七章03级

2
以1kg水为计算基准,注意单位一致
m m J / kg 2 s
g Z 9.8115 103 0.147kJ / kg
习 题 解 答
1
上一内容
下一内容
回主目录
1.492 60 WS 0.409kJ / kg 0.2273 962.8
10080 4.186 Q 192.81kJ / kg 0.2273 962.8
21
(2)传热过程的损失功和热力学效率
Ex 转 m H 转 T0 S转
5160 273 380 例题 36 380 1000 298 36 ln 273 1000 22.4 3.491106 kJ Wid
蒸汽的用变化
上一内容 下一内容 回主目录
习 题 解 答
7
S汽=0.842 S2 S1 0.842 1.7164 7.2058 4.622kJ / K
例题
S总=S H2O S汽 =6.077-4.622=1.455kJ/K
-1883.7 S汽= 450
习 题 解 答
S 气 Q 9188 T 400
例题
Q 9188 S储 = =30.63J / K T储 300
习 题 解 答
13
上一内容
下一内容
回主目录
S总 S气 S储 19.14 30.63 11.49J / K
WL T0 S总 300 11.49 3447 J
上一内容 下一内容 回主目录
习 题 解 答
18
WS H H2 ' H1 2554.4 3373.3 818.9kJ / kg
化工热力学习题及详细解答

化工热力学习题及详细解答习题 (2)第1章绪言 (2)第2章 P-V-T关系和状态方程 (4)第3章均相封闭体系热力学原理及其应用 (8)第4章非均相封闭体系热力学 (13)第5章非均相体系热力学性质计算 (19)第6章例题 (27)答案 (40)第1章绪言 (40)第2章 P-V-T关系和状态方程 (44)第3章均相封闭体系热力学原理及其应用 (51)第4章非均相封闭体系热力学 (68)第5章非均相体系热力学性质计算 (87)附加习题 (103)第2章 (103)第3章 (104)第4章 (107)第5章 (109)习题第1章 绪言一、是否题1. 孤立体系的热力学能和熵都是一定值。
2. 封闭体系的体积为一常数。
3. 封闭体系中有两个相βα,。
在尚未达到平衡时,βα,两个相都是均相敞开体系;达到平衡时,则βα,两个相都等价于均相封闭体系。
4. 理想气体的焓和热容仅是温度的函数。
5. 理想气体的熵和吉氏函数仅是温度的函数。
6. 要确定物质在单相区的状态需要指定两个强度性质,但是状态方程 P=P (T ,V )的自变量中只有一个强度性质,所以,这与相律有矛盾。
7. 封闭体系的1mol 气体进行了某一过程,其体积总是变化着的,但是初态和终态的体积相等,初态和终态的温度分别为T 1和T 2,则该过程的⎰=21T T V dT C U ∆;同样,对于初、终态压力相等的过程有⎰=21T T P dT C H ∆。
8. 描述封闭体系中理想气体绝热可逆途径的方程是γγ)1(1212-⎪⎪⎭⎫⎝⎛=P P T T (其中igV ig P C C =γ),而一位学生认为这是状态函数间的关系,与途径无关,所以不需要可逆的条件。
9. 自变量与独立变量是一致的,从属变量与函数是一致的。
10. 自变量与独立变量是不可能相同的。
二、填空题1. 状态函数的特点是:___________________________________________。
化工热力学课后习题答案

第1章绪言一、是否题3. 封闭体系中有两个相。
在尚未达到平衡时,两个相都是均相敞开体系;达到平衡时,则两个相都等价于均相封闭体系。
(对)4. 理想气体的焓和热容仅是温度的函数。
(对)5. 理想气体的熵和吉氏函数仅是温度的函数。
(错。
还与压力或摩尔体积有关。
)第2章P-V-T关系和状态方程一、是否题2. 纯物质由蒸汽变成液体,必须经过冷凝的相变化过程。
(错。
可以通过超临界流体区。
)3. 当压力大于临界压力时,纯物质就以液态存在。
(错。
若温度也大于临界温度时,则是超临界流体。
)4. 由于分子间相互作用力的存在,实际气体的摩尔体积一定小于同温同压下的理想气体的摩尔体积,所以,理想气体的压缩因子Z=1,实际气体的压缩因子Z<1。
(错。
如温度大于Boyle温度时,Z>1。
)7. 纯物质的三相点随着所处的压力或温度的不同而改变。
(错。
纯物质的三相平衡时,体系自由度是零,体系的状态已经确定。
)8. 在同一温度下,纯物质的饱和液体与饱和蒸汽的热力学能相等。
(错。
它们相差一个汽化热力学能,当在临界状态时,两者相等,但此时已是汽液不分)9. 在同一温度下,纯物质的饱和液体与饱和蒸汽的吉氏函数相等。
(对。
这是纯物质的汽液平衡准则。
)10. 若一个状态方程能给出纯流体正确的临界压缩因子,那么它就是一个优秀的状态方程。
(错。
)11. 纯物质的平衡汽化过程,摩尔体积、焓、热力学能、吉氏函数的变化值均大于零。
(错。
只有吉氏函数的变化是零。
)12. 气体混合物的virial系数,如B,C…,是温度和组成的函数。
(对。
)13. 三参数的对应态原理较两参数优秀,因为前者适合于任何流体。
(错。
三对数对应态原理不能适用于任何流体,一般能用于正常流体normal fluid)14. 在压力趋于零的极限条件下,所有的流体将成为简单流体。
(错。
简单流体系指一类非极性的球形流,如Ar等,与所处的状态无关。
)二、选择题1. 指定温度下的纯物质,当压力低于该温度下的饱和蒸汽压时,则气体的状态为(C。
(整理)化工热力学课后习题答案

.................2习题第1章 绪言一、是否题1. 孤立体系的热力学能和熵都是一定值。
(错。
和,如一体积等于2V 的绝热刚性容器,被一理想的隔板一分为二,左侧状态是T ,P 的理想气体,右侧是T 温度的真空。
当隔板抽去后,由于Q =W =0,,,,故体系将在T ,2V ,0.5P 状态下达到平衡,,,)2. 封闭体系的体积为一常数。
(错)3. 封闭体系中有两个相。
在尚未达到平衡时,两个相都是均相敞开体系;达到平衡时,则两个相都等价于均相封闭体系。
(对)4. 理想气体的焓和热容仅是温度的函数。
(对)5. 理想气体的熵和吉氏函数仅是温度的函数。
(错。
还与压力或摩尔体积有关。
)6. 要确定物质在单相区的状态需要指定两个强度性质,但是状态方程 P=P (T ,V )的自变量中只有一个强度性质,所以,这与相律有矛盾。
(错。
V 也是强度性质)7. 封闭体系的1mol 气体进行了某一过程,其体积总是变化着的,但是初态和终态的体积相等,初态和终态的温度分别为T 1和T 2,则该过程的;同样,对于初、终态压力相等的过程有。
(对。
状态函数的变化仅决定于初、终态与途径无关。
)8. 描述封闭体系中理想气体绝热可逆途径的方程是(其中),而一位学生认为这是状态函数间的关系,与途径无关,所以不需要可逆的条件。
(错。
) 9. 自变量与独立变量是一致的,从属变量与函数是一致的。
(错。
有时可能不一致)10. 自变量与独立变量是不可能相同的。
(错。
有时可以一致)三、填空题1. 状态函数的特点是:状态函数的变化与途径无关,仅决定于初、终态 。
2. 单相区的纯物质和定组成混合物的自由度数目分别是 2 和 2 。
3. 封闭体系中,温度是T 的1mol 理想气体从(P ,V )等温可逆地膨胀到(P ,V ),则所做的功为i i f f(以V 表示)或 (以P 表示)。
4. 封闭体系中的1mol 理想气体(已知),按下列途径由T 1、P 1和V 1可逆地变化至P,则.................mol ,温度为 和水 。
化工热力学(下册)第二版夏清第5章干燥标准答案

第5章 干燥的习题解答1.已知湿空气的总压强为50Pa,温度为60℃,相对湿度为40%,试求: (1)湿空气中水汽的分压; (2)湿度;(3)湿空气的密度。
解:(1)湿空气的水汽分压,V S p P ϕ=由附录查得60C o 时水的饱和蒸汽压19.92S p KPa = 0.419.927.97V p KPa =⨯= (2) 湿度0.6220.6227.970.118/507.97VVP H kg kg p P ⨯===--绝干气(1) 密度553273 1.0131027360 1.01310(0.772 1.244)(0.772 1.2440.118)2732735010H t v H P +⨯+⨯=+⨯⨯=+⨯⨯⨯⨯32.27m =湿空气/kg 绝干气 密度 3110.1180.493/2.27H H H kg m v ρ++==湿空气 2.在总压101.33KPa 下,已知湿空气的某些参数,利用湿空气的H-I 图查出本题附表中空格内的数值,并给出序号4中各数值的求解过程示意图。
习题2附表解:上表中括号内的数据为已知,其余值由图H I -查得。
分题4的求解示意图如附图所示,其中A 为状态点。
3.干球温度为20℃、湿度为0.009kg 水/kg 绝干气的温空气通过预热器加热到50℃后,再送至常压干燥器中,离开干燥器时空气的相对温度为80%,若空气在干燥器中经历等焓干燥过程,试求:(1)1m 3原温空气在预热过程中始的变化; (2)1m 3原温空气在干燥器中获得的水分量。
解:(1)31m 原湿空气在预热器中焓的变化当0020,0.009/t C H kg kg ==o 绝干气时,由H I -图查出043/I KJ kg =绝干气。
当01050,0.009/t C H H kg kg ==o =绝干气时,由H I -图查出174/I KJ kg =绝干气1kg 绝干空气在预热器中焓的变化为:744331I ∆=-=/KJ kg 绝干气 原湿空气的比容为5273 1.0131027320(0.772 1.244)(0.772 1.2440.009)273273H t v H P +⨯+=+⨯⨯=+⨯⨯30.84m =湿空气/kg 绝干气31m 原湿空气的焓变为 33136.9/0.84H I KJ m v ∆==湿空气 (2)31m 原湿空气在干燥器中获得的水分当01050,0.009/t C H H kg kg ===o 绝干气时,在H I -图上确定空气的状态点,由该点沿等焓线向右下方移动与80%ϕ=的线相交,交点即为离开干燥器时空气的状态点。
化工热力学习题及答案第五章蒸汽动力循环和制冷循环

化⼯热⼒学习题及答案第五章蒸汽动⼒循环和制冷循环第五章蒸汽动⼒循环和制冷循环5-3 设有⼀台锅炉,每⼩时产⽣压⼒为2.5MPa ,温度为350℃的⽔蒸汽4.5吨,锅炉的给⽔温度为30℃,给⽔压⼒2.5MPa 。
已知锅炉效率为70%,锅炉效率:染料可提供的热量蒸汽吸收的热量=B η。
如果该锅炉耗⽤的燃料为煤,每公⽄煤的发热量为29260kJ ·kg -1,求该锅炉每⼩时的耗煤量。
解:查⽔蒸汽表 2.5MPa 20℃H 2O 13.86-?=kg kJ H 2.5MPa 40℃H 2O 177.169-?=kg kJ H 内插得到 2.5MPa 30℃H 2O 104.12823.8677.169-?=+=kg kJ H查⽔蒸汽表 2.0MPa 320℃H 2O 15.3069-?=kg kJ H 2.0MPa 360℃H 2O 13.3159-?=kg kJ H 内插得到 2.0MPa 350℃H 2O 185.31365.306930405.30693.3159-?=+?-=kg kJ H查⽔蒸汽表 3.0MPa 320℃H 2O 14.3043-?=kg kJ H 3.0MPa 360℃H 2O 17.3138-?=kg kJ H内插得到 3.0MPa 350℃H 2O 188.31144.304330404.30437.3138-?=+?-=kg kJ H内插得到 2.5MPa 350℃H 2O 187.3125285.313688.3114-?=+=kg kJ H锅炉在等压情况下每⼩时从锅炉吸收的热量:131231490235)04.12887.3125(105.4)(2-?=-??=-?=h kJ H H H m Q O H锅炉每⼩时耗煤量: 16.658292607.013490235-?=?=h kg mcoal5-4 某朗肯循环的蒸汽参数为:进汽轮机的压⼒MPa p 61=,温度C t ?=5401,汽轮机出⼝压⼒MPa p 008.01=。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第五章 习题解答
1. 在一定压力下,组成相同的混合物的露点温度和泡点温度不可能相同。
(错,在共沸点
时相同) 2. 在(1)-(2)的体系的汽液平衡中,若(1)是轻组分,(2)是重组分,则11x y >,22x y <。
(错,若系统存在共沸点,就可以出现相反的情况) 3. 纯物质的汽液平衡常数K 等于1。
(对,因为111==y x )
4. 在(1)-(2)的体系的汽液平衡中,若(1)是轻组分,(2)是重组分,若温度一定,
则体系的压力,随着1x 的增大而增大。
(错,若系统存在共沸点,就可以出现相反的情况)
5. 下列汽液平衡关系是错误的i i Solvent i v i i x H Py *,ˆγϕ=。
(错,若i 组分采用不对称归一化,该式为正确)
6. 对于理想体系,汽液平衡常数K i (=y i /x i ),只与T 、P 有关,而与组成无关。
(对,可以从理想体系的汽液平衡关系证明)
7. 对于负偏差体系,液相的活度系数总是小于1。
(对) 8. 能满足热力学一致性的汽液平衡数据就是高质量的数据。
(错) 9.
逸度系数也有归一化问题。
(错)
10. EOS +γ法既可以计算混合物的汽液平衡,也能计算纯物质的汽液平衡。
(错) 二、选择题
1. 欲找到活度系数与组成的关系,已有下列二元体系的活度系数表达式,βα,为常数,
请决定每一组的可接受性 。
(D ) A 2211;x x βγαγ== B 12211;1x x βγαγ+=+=
C 1221ln ;ln x x βγαγ==
D 2
1
2221ln ;ln x x βγαγ== 2. 二元气体混合物的摩尔分数y 1=0.3,在一定的T ,P 下,8812.0ˆ,9381.0ˆ21==ϕ
ϕ,则此时混合物的逸度系数为 。
(C ) A 0.9097 B 0.89827
C 0.8979
D 0.9092
三、填空题
1. 说出下列汽液平衡关系适用的条件
(1) l i v i f f ˆˆ= ______无限制条件__________; (2)i l i i v i x y ϕϕ
ˆˆ= ______无限制条件____________; (3)i i s i i x P Py γ= _________低压条件下的非理想液相__________。
2. 丙酮(1)-甲醇(2)二元体系在98.66KPa 时,恒沸组成x 1=y 1=0.796,恒沸温度为327.6K ,已
知此温度下的06.65,39.9521==s
s P P kPa 则 van Laar 方程常数是
A 12=______0.587_____,A 21=____0.717____ (已知van Laar 方程为 2
21112212112x A x A x x A A RT G E +=)
3. 组成为x 1=0.2,x 2=0.8,温度为300K 的二元液体的泡点组成y 1的为(已知液相的
3733,1866
),/(75212121==+=s s
E t P P n n n n G Pa) ___0.334___。
4. 若用EOS +γ法来处理300K 时的甲烷(1)-正戊烷(2)体系的汽液平衡时,主要困
难是MPa P s
4.251=饱和蒸气压太高,不易简化;
( EOS+γ法对于高压体系需矫正)。
5. EOS 法则计算混合物的汽液平衡时,需要输入的主要物性数据是ij Ci Ci Ci k P T ,,,ω,通常如何得到相互作用参数的值?_从混合物的实验数据拟合得到。
6. 由Wilson 方程计算常数减压下的汽液平衡时,需要输入的数据是Antoine 常数A i ,B i ,C i ;
Rackett 方程常数α,β;能量参数),2,1,)((N j i ii ij =-λλ,Wilson 方程的能量参数是如何得到的?能从混合物的有关数据(如相平衡)得到。
四、计算题
1. 一个由丙烷(1)-异丁烷(2)-正丁烷(3)的混合气体,7.01=y ,
2.02=y ,1.03=y ,
若要求在一个30℃的冷凝器中完全冷凝后以液相流出,问冷凝器的最小操作压力为多
少?(用软件计算)
解:x1=y1,x2=y2,x3=y3. 活度系数近似为1,查表计算各物质的饱和蒸气压即可求得最小压力为 0.863MPa
2. 在常压和25℃时,测得059.01=x 的异丙醇(1)-苯(2)溶液的汽相分压(异丙醇的)是
1720Pa 。
已知25℃时异丙醇和苯的饱和蒸汽压分别是5866和13252Pa 。
(a)求液相异丙醇的活度系数(对称归一化);(b)求该溶液的E G 。
解:由1111γx P Py s =得55866
059.01720
5866059.010*********≈⨯=⨯==
y x P Py s γ
同样有:()813252
059.011720
1013252
222≈⨯--=
=
x P Py s γ
28ln 941.05ln 059.0ln ln 2211≈⨯+⨯=+=γγx x RT
G E
16.495715.298314.82-⋅=⨯⨯=∴mol J G E
3. 苯(1)-甲苯(2)可以作为理想体系。
(a)求90℃时,与x 1=0.3 的液相成平衡的汽相组成和泡点压力;(b) 90℃和101.325kPa 时的平衡汽、液相组成多少? (c)对于x 1=0.55和y 1=0.75的平衡体系的温度和压力各是多少? (d)y 1=0.3的混合物气体在101.325KPa 下被冷却到100℃时,混合物的冷凝率多少? 解:查出Antoine 方程常数
K)(15.36315.27390=+=T ,由Antoine 方程得
(a )
kPa 136,995.126
.5315.36342
.27699419.6ln 11=-=--
=s s P P
同样得kPa 2.542=s P 由理想体系的汽液平衡关系得
52
.074.783.0136kPa 74.787.02.543.01361
112211=⨯===⨯+⨯=+=P x P y x P x P P s s s
(b) 由
()576.012.54136325.1011112211=→-+=→+=x x x x P x P P s
s 773.0325.101576.0136111=⨯==P x P y s (c)由2221
11,x P Py x P Py s s
==得
⎪⎪⎭
⎫ ⎝⎛=-→=122121122121ln ln ln x y x y P P x y x y P P s
s s s 即
K 64.36955.025.045.075.0ln 65.5465.30760580.726.5342.27699419.6≈→⎪⎭
⎫
⎝⎛⨯⨯=-+---
T T T
所以
kPa 6.66,4.163
21==s s
P P kPa 84.119
2211=+=x P x P P s s (d )K)(15.37315.273100=+=T ,由Antoine 方程得
kPa 1.74,.180
21==s s P P ()743.0,257.011.74180325.1012111==→-+=x x x x
544.0,456.0325.101257.018021==⨯=y y
设最初混合物汽相有10mol ,即苯3mol ,甲苯7mol 。
冷凝后汽、液相分别为(10-a)和a mol ,
则:mol 839.7257
.0456.03
456.010456.0)10(257.03=--⨯=
→-+=a a a
冷凝率:%39.7810
839.710==a 五、图示题
描述下列二元y x T --图中的变化过程D C B A →→→:这是一个等压定(总)组成
的降温过程。
A 处于汽相区,降温到B 点时,即为露点,开始有液滴冷凝,随着温度的继续下降,产生的液相量增加,而汽相量减少,当达到C 点,即泡点时,汽相消失,此时,液相的组成与原始汽相组成相同。
继续降温到达D 点。
描述下列二元y x P --图中的变化过程D C B A →→→:这是一等温等压的变组成过程。
从A 到B ,是液相中轻组分1的含量增加,B 点为泡点,即开始有汽泡出现。
B 至C 的过程中,系统中的轻组分增加,汽相相对于液相的量也在不断的增加,C 点为露点,C 点到D 点是汽相中轻组分的含量不断增加。
1. 将下列T-x-y 图的变化过程A →B →C →D →E 和P-x-y 图上的变化过程F →G →H →I →J
表示在P-T 图(组成=0.4)上。
