初三化学化学除杂分离和提纯试题(有答案和解析)
九年级化学化学除杂分离和提纯真题汇编(含答案)及解析

九年级化学化学除杂分离和提纯真题汇编(含答案)及解析一、中考化学除杂分离和提纯1.除去下列物质中的少量杂质,所选用的试剂及操作方法均正确的是A .AB .BC .CD .D【答案】C 【解析】 【分析】 【详解】A 、HCl 和二氧化碳都会与氢氧化钠反应,在除去杂质的同时也会除去HCl ,故A 错误;B 、碳酸氢钙在加热条件下生成碳酸钙、水和二氧化碳,生成的碳酸钙对于氯化钙(固体)也是杂质,故B 错误。
C 、硫酸镁能与适量氢氧化钡溶液反应生成硫酸钡沉淀和氢氧化镁沉淀,再过滤,能除去杂质且没有引入新的杂质,符合除杂原则,故C 正确。
D 、硫酸和硝酸钡会生成硫酸钡沉淀和硝酸,生成的硝酸对于盐酸也是杂质,故D 错误。
故选:C 。
【点睛】除杂(提纯),是指除去杂质,同时被提纯物质不得改变。
除杂至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质。
2.下列哪种试剂最适合用来除去NaCl 溶液中混有的少量NaOH ( ) A .23Na CO 溶液 B .24H SO 溶液C .HCl 溶液D .2Ca(OH)溶液【答案】C 【解析】 【分析】 【详解】A 、23Na CO 溶液和NaOH 不反应,不能用于除去NaCl 溶液中混有的少量NaOH ,故A 错;B 、24H SO 溶液和NaOH 发生反应生成硫酸钠和水,会引入新杂质硫酸钠,故B 错;C、HCl溶液和NaOH发生反应生成氯化钠和水,不会引入新杂质,符合题意故C正确;Ca(OH)溶液和NaOH不反应,不能用于除去NaCl溶液中混有的少量NaOH,故D D、2错;故选:C。
【点睛】除杂的原则不引入新杂质,被提纯物质不能减少,杂质容易分离。
3.除去下列物质中含有的少量杂质,所用试剂或方法不正确的是()A.A B.B C.C D.D【答案】D【解析】【分析】除杂(提纯),是指除去杂质,同时被提纯物质不得改变。
【详解】A、CuO能与稀硫酸反应生成硫酸铜和水,再过滤,能除去杂质且没有引入新的杂质,符合除杂原则,故A正确;B、KCl易溶于水,MnO2难溶于水,可采取加水溶解、过滤、洗涤、烘干的方法进行分离除杂,故B正确;C、碳酸钠能与过量稀盐酸反应生成氯化钠、水和二氧化碳,盐酸具有挥发性,再蒸发除去盐酸,能除去杂质且没有引入新的杂质,符合除杂原则,故C正确;D、除去二氧化碳中的一氧化碳不能够点燃,当二氧化碳(不能燃烧、不能支持燃烧)大量存在时,少量的一氧化碳是不会燃烧的,故D不正确。
初中化学化学除杂分离和提纯及其解题技巧及练习题(含答案)及解析

初中化学化学除杂分离和提纯及其解题技巧及练习题(含答案)及解析一、中考化学除杂分离和提纯1.为除去下列物质中的少量杂质(括号内为杂质),下列操作方法能达到目的的是A.A B.B C.C D.D【答案】A【解析】【分析】【详解】A、铜在空气中充分灼烧能产生氧化铜,而氧化铜不能反应,可以用于除杂;故选项正确;B、生石灰与水反应产氢氧化钙,氢氧化钙能与二氧化碳反应产生碳酸钙,不能用于除杂;故选项错误;C、硝酸钡能与硫酸钠反应产生硫酸钡沉淀和硝酸钠,引入新的杂质硝酸根离子,不能用于除杂;故选项错误;D、氧化钙能与水反应产生氢氧化钙,不能用于除杂;故选项错误;故选:A。
2.欲除去下列物质中的少量杂质,所用试剂及方法不正确的是()A.A B.B C.C D.D【答案】C【解析】【分析】【详解】A、因为二氧化碳不与铜反应,氧气在加热条件下可以与铜反应,所以可以除掉氧气,故正确;B、CO2能与氢氧化钠溶液反应生成碳酸钠和水,CO不与氢氧化钠溶液反应,再通过浓硫酸进行干燥,能除去杂质且没有引入新的杂质,符合除杂原则,故正确;C、铁粉能与稀盐酸反应生成氯化亚铁和氢气,铜不与稀盐酸反应,反而会把原物质除去,不符合除杂原则,故错误;D、碳酸钾能与适量氯化钙溶液反应生成碳酸钙沉淀和氯化钾,再过滤,能除去杂质且没有引入新的杂质,符合除杂原则,故正确。
故选:C。
【点睛】除杂(提纯),是指除去杂质,同时被提纯物质不得改变。
除杂至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质。
3.下列除去杂质的方法中,正确的是A.A B.B C.C D.D【答案】C【解析】【分析】【详解】A、CO2与HCl都能与氢氧化钠反应,不能得到二氧化碳气体,选项说法错误;B、KClO3与MnO2混合加热能分解放出氧气除去氯酸钾,但是又引入二氧化锰新杂质,选项说法错误;C、Na2CO3能与盐酸反应生成氯化钠、二氧化碳和水,蒸干后能除去水分和氯化氢,得到纯净的氯化钠,选项说法正确;D、铁能与硫酸反应被溶解生成硫酸亚铁溶液,过滤得不到纯净的铁,选项说法错误;故选C4.下列关于物质除杂所选用方法正确的是A.A B.B C.C D.D【答案】A【解析】【分析】【详解】A、过量的Fe粉能与CuSO4溶液反应生成硫酸亚铁溶液和铜,再过滤,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确;B、浓硫酸具有吸水性,也能与氨气反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项所采取的方法错误;C、KClO3在二氧化锰的催化作用下生成氯化钾和氧气,二氧化锰作催化剂,反应前后质量不变,能除去杂质但引入了新的杂质二氧化锰,不符合除杂原则,故选项所采取的方法错误;D、Mg能与过量的稀硫酸反应生成硫酸镁和氢气,铜不与稀硫酸反应,反而会把原物质除去,不符合除杂原则,故选项所采取的方法错误。
中考化学溶液的除杂分离和提纯的综合题试题及详细答案
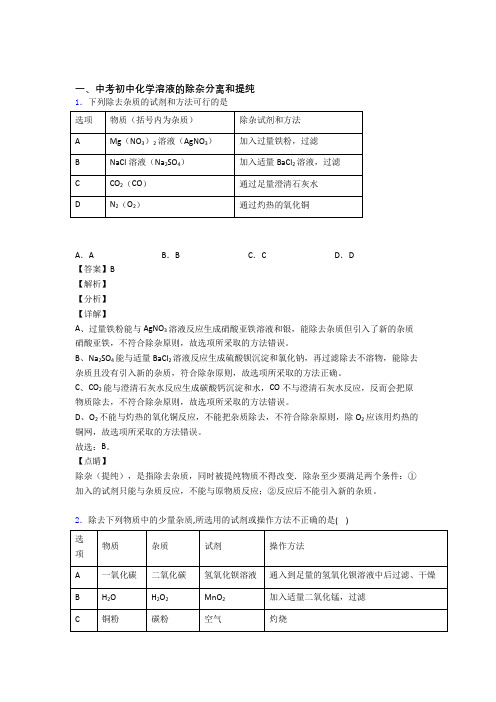
一、中考初中化学溶液的除杂分离和提纯1.下列除去杂质的试剂和方法可行的是A.A B.B C.C D.D【答案】B【解析】【分析】【详解】A、过量铁粉能与AgNO3溶液反应生成硝酸亚铁溶液和银,能除去杂质但引入了新的杂质硝酸亚铁,不符合除杂原则,故选项所采取的方法错误。
B、Na2SO4能与适量BaCl2溶液反应生成硫酸钡沉淀和氯化钠,再过滤除去不溶物,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确。
C、CO2能与澄清石灰水反应生成碳酸钙沉淀和水,CO不与澄清石灰水反应,反而会把原物质除去,不符合除杂原则,故选项所采取的方法错误。
D、O2不能与灼热的氧化铜反应,不能把杂质除去,不符合除杂原则,除O2应该用灼热的铜网,故选项所采取的方法错误。
故选:B。
【点睛】除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质。
2.除去下列物质中的少量杂质,所选用的试剂或操作方法不正确的是( )A.A B.B C.C D.D【答案】C【解析】【分析】根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变。
除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质。
【详解】A、将混合气体通入氢氧化钡溶液,二氧化碳和氢氧化钡反应生成碳酸钡沉淀和水,一氧化碳不反应,然后通过干燥除掉溶液中带入的水分,可得一氧化碳,选项正确;B、过氧化氢在二氧化锰的作用下生成水和氧气,过滤后液体只有水,选项正确;C、在空气中灼烧时,铜和碳都会与氧气发生反应,选项错误;D、碳酸钠能与过量的稀盐酸反应生成氯化钠、水和二氧化碳,所得溶液是氯化钠和氯化氢的混合溶液,蒸发结晶,可得氯化钠晶体,选项正确。
故选C。
3.除去下列物质中的少量杂质,所选用的试剂及操作方法不正确的是()A.A B.B C.C D.D【答案】D【解析】【分析】【详解】A、浓硫酸具有吸水性,可以去除氧气中水蒸气,正确。
中考化学 除杂分离和提纯 综合题附详细答案
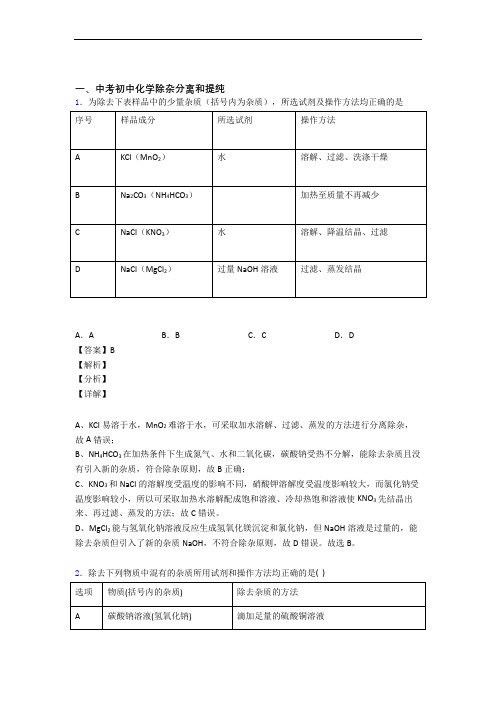
一、中考初中化学除杂分离和提纯1.为除去下表样品中的少量杂质(括号内为杂质),所选试剂及操作方法均正确的是A.A B.B C.C D.D【答案】B【解析】【分析】【详解】A、KCl易溶于水,MnO2难溶于水,可采取加水溶解、过滤、蒸发的方法进行分离除杂,故A错误;B、NH4HCO3在加热条件下生成氮气、水和二氧化碳,碳酸钠受热不分解,能除去杂质且没有引入新的杂质,符合除杂原则,故B正确;C、KNO3和NaCl的溶解度受温度的影响不同,硝酸钾溶解度受温度影响较大,而氯化钠受温度影响较小,所以可采取加热水溶解配成饱和溶液、冷却热饱和溶液使KNO3先结晶出来、再过滤、蒸发的方法;故C错误。
D、MgCl2能与氢氧化钠溶液反应生成氢氧化镁沉淀和氯化钠,但NaOH溶液是过量的,能除去杂质但引入了新的杂质NaOH,不符合除杂原则,故D错误。
故选B。
2.除去下列物质中混有的杂质所用试剂和操作方法均正确的是( )B铜粉(铁粉)加入足量的稀硫酸,过滤,洗涤,干燥C一氧化碳(二氧化碳)依次通过盛有石灰水、浓硫酸的洗气瓶D氯化钠溶液(氯化钙)向其中通入过量的二氧化碳气体,过滤A.A B.B C.C D.D【答案】B【解析】【分析】除杂(提纯),是指除去杂质,同时被提纯物质不得改变。
【详解】A、氢氧化钠和硫酸铜反应生成氢氧化铜和硫酸钠,引入了硫酸钠杂质,故A不正确;B、铁粉与足量稀硫酸反应生成硫酸亚铁溶液和氢气,铜不能与稀硫酸反应,再过滤、洗涤、干燥,能除去杂质且没有引入新的杂质,符合除杂原则,故B正确;C、石灰水吸收二氧化碳的能力较弱,将气体依次通过盛有石灰水、浓硫酸的洗气瓶不能除去杂质,故C不正确;D、二氧化碳不能与氯化钙溶液反应,故D不正确。
故选B。
【点睛】除杂条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质。
3.某混合溶液含有一定量的硝酸银、硝酸铜和硝酸钡,为逐一分离其中的金属元素,所加试剂均过量,且理论上氢氧化钠的消耗量最少。
九年级必备化学化学除杂分离和提纯技巧全解及练习题(含答案)含解析

九年级必备化学化学除杂分离和提纯技巧全解及练习题(含答案)含解析一、中考化学除杂分离和提纯1.欲除去下列物质中的少量杂质,所用试剂及方法不正确的是()A.A B.B C.C D.D【答案】C【解析】【分析】【详解】A、因为二氧化碳不与铜反应,氧气在加热条件下可以与铜反应,所以可以除掉氧气,故正确;B、CO2能与氢氧化钠溶液反应生成碳酸钠和水,CO不与氢氧化钠溶液反应,再通过浓硫酸进行干燥,能除去杂质且没有引入新的杂质,符合除杂原则,故正确;C、铁粉能与稀盐酸反应生成氯化亚铁和氢气,铜不与稀盐酸反应,反而会把原物质除去,不符合除杂原则,故错误;D、碳酸钾能与适量氯化钙溶液反应生成碳酸钙沉淀和氯化钾,再过滤,能除去杂质且没有引入新的杂质,符合除杂原则,故正确。
故选:C。
【点睛】除杂(提纯),是指除去杂质,同时被提纯物质不得改变。
除杂至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质。
2.下列除去杂质的方法中,正确的是A.A B.B C.C D.D【答案】C【解析】【分析】【详解】A、CO2与HCl都能与氢氧化钠反应,不能得到二氧化碳气体,选项说法错误;B、KClO3与MnO2混合加热能分解放出氧气除去氯酸钾,但是又引入二氧化锰新杂质,选项说法错误;C、Na2CO3能与盐酸反应生成氯化钠、二氧化碳和水,蒸干后能除去水分和氯化氢,得到纯净的氯化钠,选项说法正确;D、铁能与硫酸反应被溶解生成硫酸亚铁溶液,过滤得不到纯净的铁,选项说法错误;故选C3.除去下列物质中的少量杂质,所选用的试剂和操作方法都正确的是()A.A B.B C.C D.D【答案】B【解析】【分析】【详解】A、将混合气体通过足量的铜网,铜与氮气不反应,铜与氧气能在加热的条件下反应生成氧化铜,但是常温下铜与氧气不反应,常温下,通过足量的铜网,不能除去混合气体中的氧气,不符合题意;B、氯化钾能溶于水,二氧化锰不溶于水,加水溶解、过滤,除去二氧化锰,蒸发、结晶得到氯化钾,符合题意;C、活性炭具有吸附性,能吸附水中的色素和异味,故加活性炭可除去水中的臭味,过滤,除去活性炭,才能得到水,需加过滤步骤,不符合题意;D、将混合气体通过适量的氢氧化钠溶液,氢氧化钠与二氧化碳反应生成碳酸钠和水,虽然除去了杂质二氧化碳,但是一氧化碳通过氢氧化钠溶液会携带上水蒸气,引入了新的杂质水蒸气,不符合题意。
中考化学 溶液的除杂分离和提纯综合试题附答案
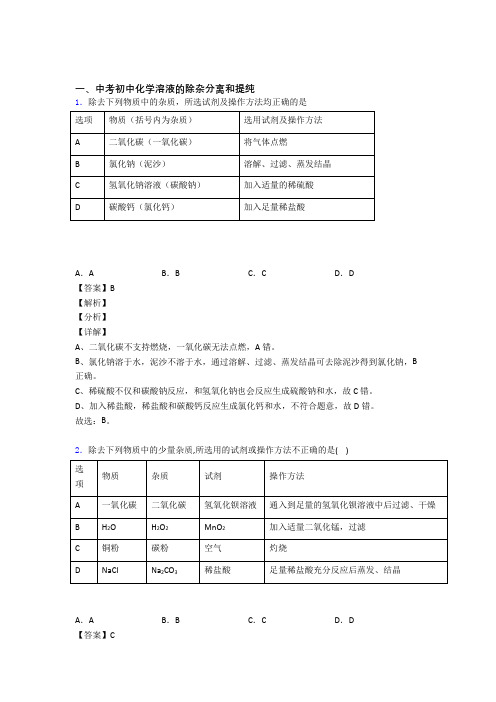
一、中考初中化学溶液的除杂分离和提纯1.除去下列物质中的杂质,所选试剂及操作方法均正确的是A.A B.B C.C D.D【答案】B【解析】【分析】【详解】A、二氧化碳不支持燃烧,一氧化碳无法点燃,A错。
B、氯化钠溶于水,泥沙不溶于水,通过溶解、过滤、蒸发结晶可去除泥沙得到氯化钠,B 正确。
C、稀硫酸不仅和碳酸钠反应,和氢氧化钠也会反应生成硫酸钠和水,故C错。
D、加入稀盐酸,稀盐酸和碳酸钙反应生成氯化钙和水,不符合题意,故D错。
故选:B。
2.除去下列物质中的少量杂质,所选用的试剂或操作方法不正确的是( )A.A B.B C.C D.D【答案】C【解析】【分析】根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变。
除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质。
【详解】A、将混合气体通入氢氧化钡溶液,二氧化碳和氢氧化钡反应生成碳酸钡沉淀和水,一氧化碳不反应,然后通过干燥除掉溶液中带入的水分,可得一氧化碳,选项正确;B、过氧化氢在二氧化锰的作用下生成水和氧气,过滤后液体只有水,选项正确;C、在空气中灼烧时,铜和碳都会与氧气发生反应,选项错误;D、碳酸钠能与过量的稀盐酸反应生成氯化钠、水和二氧化碳,所得溶液是氯化钠和氯化氢的混合溶液,蒸发结晶,可得氯化钠晶体,选项正确。
故选C。
3.为除去下列各物质中混有的少量杂质,采用的相应除杂方案正确的是A.A B.B C.C D.D【答案】C【解析】【分析】【详解】A、铜粉中含有氧化铜杂质,在空气中充分灼烧,铜与氧气在加热条件下反应生成氧化铜,不能除去杂质,反而将铜粉反应了。
故A不符合题意;B、NaCl溶液中含有Na2CO3杂质,加入适量稀硫酸,碳酸钠与稀硫酸反应生成硫酸钠、二氧化碳和水,可以除去碳酸钠,但是引入了新的杂质硫酸钠。
故B不符合题意;C、H2中含有CO2气体,通过足量NaOH溶液,氢氧化钠与二氧化碳反应生成碳酸钠和水,除去了二氧化碳,再对出来的氢气进行干燥,可以除去从氢氧化钠溶液中带出的水蒸气,从而得到纯净的氢气。
中考化学 分离和提纯除杂 综合题及详细答案
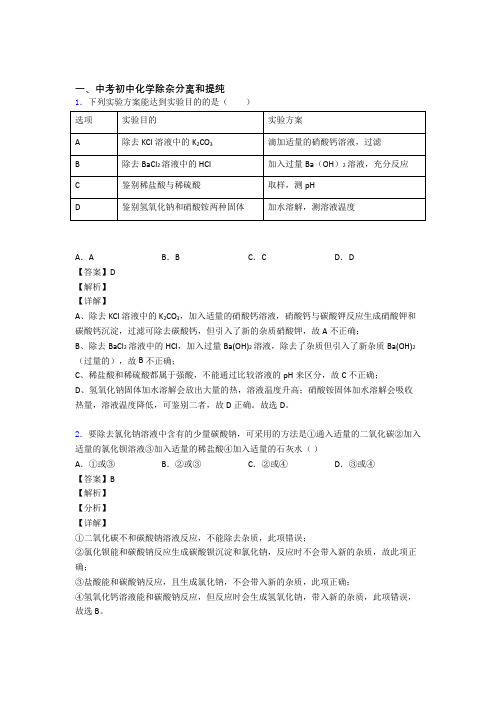
一、中考初中化学除杂分离和提纯1.下列实验方案能达到实验目的的是()A.A B.B C.C D.D【答案】D【解析】【详解】A、除去KCl溶液中的K2CO3,加入适量的硝酸钙溶液,硝酸钙与碳酸钾反应生成硝酸钾和碳酸钙沉淀,过滤可除去碳酸钙,但引入了新的杂质硝酸钾,故A不正确;B、除去BaCl2溶液中的HCl,加入过量Ba(OH)2溶液,除去了杂质但引入了新杂质Ba(OH)2(过量的),故B不正确;C、稀盐酸和稀硫酸都属于强酸,不能通过比较溶液的pH来区分,故C不正确;D、氢氧化钠固体加水溶解会放出大量的热,溶液温度升高;硝酸铵固体加水溶解会吸收热量,溶液温度降低,可鉴别二者,故D正确。
故选D。
2.要除去氯化钠溶液中含有的少量碳酸钠,可采用的方法是①通入适量的二氧化碳②加入适量的氯化钡溶液③加入适量的稀盐酸④加入适量的石灰水()A.①或③B.②或③C.②或④D.③或④【答案】B【解析】【分析】【详解】①二氧化碳不和碳酸钠溶液反应,不能除去杂质,此项错误;②氯化钡能和碳酸钠反应生成碳酸钡沉淀和氯化钠,反应时不会带入新的杂质,故此项正确;③盐酸能和碳酸钠反应,且生成氯化钠,不会带入新的杂质,此项正确;④氢氧化钙溶液能和碳酸钠反应,但反应时会生成氢氧化钠,带入新的杂质,此项错误,故选B。
3.除去下列物质中的少量杂质,所选试剂及操作都正确的是()A.A B.B C.C D.D【答案】D【解析】【分析】【详解】A、过量铁粉能与CuCl2溶液反应生成氯化亚铁溶液和铜,应再进行过滤,故选项所采取的方法错误;B、CO2能与氢氧化钠溶液反应生成碳酸钠和水,CO不与氢氧化钠溶液反应,应再进行干燥,故选项所采取的方法错误;C、Na2CO3能与适量CaCl2溶液反应生成碳酸钡沉淀和氯化钠,能除去杂质但引入了新的杂质氯化钠,不符合除杂原则,故选项所采取的方法错误;D、铁粉能与过量盐酸反应生成氯化亚铁溶液和氢气,铜不与过量盐酸反应,再过滤,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确。
九年级化学化学除杂分离和提纯题20套(带答案)含解析

C、混合固体加入过量的稀盐酸,碳酸钠与稀盐酸反应生成氯化钠、二氧化碳和水,盐酸具有挥发性,蒸发、结晶可除去杂质得到氯化钠,无需过滤,符合题意;
D、碳酸钙高温煅烧生成氧化钙和二氧化碳,高温煅烧至质量不再改变,可以除去杂质碳酸钙,不符合题意。
除杂选择试剂的原则是:不增(不引入新的杂质)、不减(不能将原物质反应掉)、不繁(整个过程不繁琐)。
6.除去下列物质中的杂质(括号内物质为杂质)的方法错误的是( )
A.N2(O2)——通过灼热的铜网
B.Fe(Fe2O3)——过量稀盐酸、过滤
C.H2(水蒸气)——通过浓硫酸的洗气瓶
D.NaOH溶液(Na2CO3)——适量Ca(OH)2溶液,过滤
C、二氧化碳中含有少量的一氧化碳不能点燃,且通入氧气引入新杂质,故错误;
D、氯化钾易溶于水,而二氧化锰难溶于水,故可以溶解过滤,除去二氧化锰,再蒸发获得氯化钾,故正确。故选D。
5.下列除去杂质的方法正确的是
选项
物质(括号内为杂质)
除去杂质的方法
A
CO2(CO)
点燃
B
FeCl2(CuCl2)
加水溶解、加入过量铁粉、过滤
故选C。
【点睛】
除杂选择试剂的原则是:不增(不引入新的杂质)、不减(不能将原物质反应掉)、不繁(整个过程不繁琐)。
8.下列实验目的对应实验方案正确的是()
实验目的
实验方案
A
鉴别铁粉、木炭粉、氧化铜粉末
加入足量的稀硫酸
B
鉴别碳酸铵、硫酸铵、硝酸铵三种氮肥
用氢氧化钡溶液
C
除去CO中少量H2O和CO2
(化学)九年级必备化学化学除杂分离和提纯技巧全解及练习题(含答案)及解析

(化学)九年级必备化学化学除杂分离和提纯技巧全解及练习题(含答案)及解析一、中考化学除杂分离和提纯1.除去下列物质中的少量杂质,所选用的试剂和操作方法都正确的是( )物质杂质试剂操作方法A K2CO3溶液K2SO4BaCO3加适量BaCO3,粉末,充分反应后,过滤B MgCl2溶液HCl过量Mg(OH)2过滤C CO2水蒸气足量NaOH固体干燥D CaCO3CaO无高温煅烧A.A B.BC.C D.D【答案】B【解析】【分析】除杂条件是不引入新的杂质,加入的物质不和原物质反应。
【详解】A、碳酸钡为沉淀,不能与硫酸钾发生反应,故A不正确;B、加入过量氢氧化镁,氢氧化镁能与盐酸反应生成氯化镁和水,再过滤掉剩余氢氧化镁得到氯化镁溶液,故B正确;C、氢氧化钠与原物质二氧化碳能发生反应,故C不正确;D、高温燃烧时原物质碳酸钙发生分解反应,故D不正确。
故选B。
【点睛】物质除杂时选择的药品要只与杂质发生反应,不与原物质反应,且在除杂时不能引入新杂质。
2.下列操作不能达到实验目的是()选项实验目的实验操作A除去CO2 中的少量CO点燃B检验一瓶气体是否为CO2倒入澄清的石灰水,振荡C鉴别CO2和CO分别通过灼热的氧化铜D鉴别H2O2溶液和H2O分别加入二氧化锰A.A B.B C.C D.D【答案】A【解析】【分析】【详解】A、除去CO2 中的少量CO可以通过灼热的氧化铜,不能点燃,A错误,符合题意;B、CO2通入澄清石灰水,澄清石灰水变浑浊,故通过澄清石灰检验CO2,B正确,不符合题意;C、CO具有还原性通过灼热的CuO会生成Cu和CO2,现象为黑色固体变为红色,二氧化碳不具有还原性,通过灼热氧化铜无现象,故可通过灼热的氧化铜鉴别CO2和CO,C正确,不符合题意;D、H2O2溶液加入二氧化锰会迅速反应产生大量氧气,H2O中加入二氧化锰没有现象,故可通过二氧化锰来鉴别H2O2溶液和H2O,D正确,不符合题意;故选:A3.下列除去杂质的方法,错误的是()A.除去 H2中的少量水蒸气:通过浓硫酸B.除去 CuO 中的少量碳粉:在空气中充分加热C.除去 CO2中少量的 CO:通过灼热的氧化铜D.除去 ZnCl2溶液中少量的 CuCl2:加入足量的铁屑充分反应后,过滤【答案】D【解析】【详解】A、浓硫酸具有很强的吸水性,能够用于干燥酸性或中性气体,氢气是中性气体,所以可以通过浓硫酸除去 H2中的少量水蒸气,A正确;B、除去 CuO 中的少量碳粉,在空气中充分加热,氧化铜不与氧气反应,而碳粉与氧气反应生成二氧化碳气体扩散,B正确;C、除去 CO2中少量的 CO,把气体通过灼热的氧化铜,二氧化碳气体不与氧化铜反应,而一氧化碳与氧化铜反应生成铜和二氧化碳,从而除去了一氧化碳还得到了二氧化碳,C正确;D、除去 ZnCl2溶液中少量的 CuCl2,向溶液中加入足量的铁屑充分反应后,过滤,铁与氯化铜反应生成铜和氯化亚铁,虽然除去了氯化铜,但又生成了氯化亚铁,引进了新杂质,D 错误。
化学除杂分离和提纯练习题(含答案)经典

化学除杂分离和提纯练习题(含答案)经典一、中考化学除杂分离和提纯1.下列哪种试剂最适合用来除去NaCl 溶液中混有的少量NaOH ( ) A .23Na CO 溶液 B .24H SO 溶液C .HCl 溶液D .2Ca(OH)溶液【答案】C 【解析】 【分析】 【详解】A 、23Na CO 溶液和NaOH 不反应,不能用于除去NaCl 溶液中混有的少量NaOH ,故A 错;B 、24H SO 溶液和NaOH 发生反应生成硫酸钠和水,会引入新杂质硫酸钠,故B 错;C 、HCl 溶液和NaOH 发生反应生成氯化钠和水,不会引入新杂质,符合题意故C 正确;D 、2Ca(OH)溶液和NaOH 不反应,不能用于除去NaCl 溶液中混有的少量NaOH ,故D 错; 故选:C 。
【点睛】除杂的原则不引入新杂质,被提纯物质不能减少,杂质容易分离。
2.下列除杂(括号内为杂质)选用的试剂或方法错误的是( ) A .Cu (CuO ):加入足量的稀盐酸,过滤,洗涤、烘干 B .NaCl 溶液(HCl ):加入过量碳酸钠,充分反应后过滤 C .CO 2 气体(CO ):将气体通过灼热的氧化铜层后收集气体 D .NaCl (泥沙):加适量水充分溶解,过滤、蒸发结晶 【答案】B 【解析】 【分析】 【详解】A 、在金属活动性顺序里,铜位于氢之前,不与稀盐酸反应,氧化铜能与稀盐酸反应生成氯化铜和水,加入足量稀盐酸,过滤、洗涤、干燥可得铜,不符合题意;B 、加入过量的碳酸钠,碳酸钠能与稀盐酸反应生成氯化钠、二氧化碳和水,碳酸钠过量,虽然除去了杂质,但是引入了新的杂质碳酸钠,符合题意;C 、将混合气体通过灼热的氧化铜,氧化铜能与一氧化碳在加热的条件下反应生成铜和二氧化碳,收集气体可得纯净的二氧化碳,不符合题意;D 、氯化钠溶于水,泥沙不溶于水,加适量水充分溶解,过滤、蒸发结晶,可得氯化钠,不符合题意。
故选B 。
【点睛】除杂选择试剂的原则是:不增(不引入新的杂质)、不减(不能将原物质反应掉)、不繁(整个过程不繁琐)。
初三化学化学除杂分离和提纯题20套(带答案)含解析

一、中考化学除杂分离和提纯
1.为除去下列物质中的少量杂质(括号内为杂质),下列操作方法能达到目的的是
选项
物质(杂质)
操作方法
A
CuO(Cu)
在空气中充分灼烧
B
CO2(H2O)
将气体通过装生石灰的干燥管
C
NaCl(Na2SO4)
加入适量硝酸钡溶液后过滤
C、加入足量的水,氧化钙与水反应生成氢氧化钙,碳酸钙难溶于水,过滤,除去了碳酸钙,但是也除去了原物质,符合题意;
D、氯化钾溶于水,二氧化锰不溶于水,加入足量的水溶解,过滤,除去二氧化锰,蒸发结晶得到氯化钾,不符合题意。
故选C。
【点睛】
除杂选择试剂的原则是:不增(不引入新的杂质)、不减(不能将原物质反应掉)、不繁(整个过程不繁琐)。
D、C粉在氧气流中加热生成二氧化碳气体,反而会把原物质除去,不符合除杂原则,故选项所采取的方法错误。
故选:A。
10.欲除去下列物质中的少量杂质,所用试剂及方法错误的是
序号
混合物
除杂试剂与方法
A
二氧化碳中混有少量一氧化碳
通过灼热的氧化铜
B
氧化钙中混有少量碳酸钙
加水溶解,过滤
C
氧气中混有少量水蒸气
通过浓硫酸干燥
B、浓硫酸具有吸水性,也能与氨气反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项所采取的方法错误;
C、KClO3在二氧化锰的催化作用下生成氯化钾和氧气,二氧化锰作催化剂,反应前后质量不变,能除去杂质但引入了新的杂质二氧化锰,不符合除杂原则,故选项所采取的方法错误;
D、Mg能与过量的稀硫酸反应生成硫酸镁和氢气,铜不与稀硫酸反应,反而会把原物质除去,不符合除杂原则,故选项所采取的方法错误。
【化学】初三化学化学除杂分离和提纯技巧和方法完整版及练习题含解析

【化学】初三化学化学除杂分离和提纯技巧和方法完整版及练习题含解析一、中考化学除杂分离和提纯1.如表中除去物质所含少量杂质的方法,错误的是()A.A B.B C.C D.D【答案】C【解析】试题分析:A、氧气通过灼热的铜网时可与铜发生反应生成氧化铜,而氮气不与铜反应,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确. B、碳酸钙高温煅烧生成氧化钙和二氧化碳,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确. C、盐酸能与过量氢氧化钙溶液反应生成氯化钙和水,能除去杂质但引入了新的杂质氢氧化钙(过量的),不符合除杂原则,故选项所采取的方法错误. D、氯化镁能与过量氢氧化钠溶液反应生成氢氧化镁沉淀和氯化钠,再过滤、向滤液中加适量稀盐酸除去过量的氢氧化钠,至溶液pH=7,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.故选C.考点:物质除杂或净化的探究;常见气体的检验与除杂方法;酸的化学性质;盐的化学性质.2.分离、提纯除杂、鉴别是化学实验的重要手段,下列实验设计不能达到实验目的的是A.A B.B C.C D.D【答案】B【解析】【分析】【详解】A、将粗盐中混有的泥沙分离,先加水溶解,过滤除去泥沙等不溶性物质,然后进行蒸发,得到氯化钠晶体,可以达到实验目的,不符合题意;B、除去 NaCl 固体中混有的少量CaCl2,先加过量的碳酸钠,碳酸钠与氯化钙反应生成碳酸钙和氯化钠,然后把碳酸钙过滤出来,但得到的氯化钠溶液中还含有过量的碳酸钠,不能达到实验目的,符合题意;C、除去MgCl2溶液中的少量MgSO4,加适量的BaCl2溶液,氯化钡与硫酸镁反应生成硫酸钡和氯化镁,然后把硫酸钡过滤出来,得到氯化镁溶液,可以达到实验目的,不符合题意;D、鉴别CaCO3、NaOH、NaCl、NH4NO3四种固体,分别加水溶解,观察并触摸容器外壁,不能溶解的是碳酸钙,溶解且容器外壁发热的是氢氧化钠,溶解没有并且容器外壁没有明显现象的是氯化钠,溶解且容器外壁冰冷的是硝酸铵,可以达到实验目的,不符合题意。
【化学】九年级化学化学除杂分离和提纯试题(有答案和解析)及解析

【化学】九年级化学化学除杂分离和提纯试题(有答案和解析)及解析一、中考化学除杂分离和提纯1.除去下列物质中的少量杂质,所选用的试剂及操作方法均正确的是A .AB .BC .CD .D【答案】C 【解析】 【分析】 【详解】A 、HCl 和二氧化碳都会与氢氧化钠反应,在除去杂质的同时也会除去HCl ,故A 错误;B 、碳酸氢钙在加热条件下生成碳酸钙、水和二氧化碳,生成的碳酸钙对于氯化钙(固体)也是杂质,故B 错误。
C 、硫酸镁能与适量氢氧化钡溶液反应生成硫酸钡沉淀和氢氧化镁沉淀,再过滤,能除去杂质且没有引入新的杂质,符合除杂原则,故C 正确。
D 、硫酸和硝酸钡会生成硫酸钡沉淀和硝酸,生成的硝酸对于盐酸也是杂质,故D 错误。
故选:C 。
【点睛】除杂(提纯),是指除去杂质,同时被提纯物质不得改变。
除杂至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质。
2.下列哪种试剂最适合用来除去NaCl 溶液中混有的少量NaOH ( ) A .23Na CO 溶液 B .24H SO 溶液C .HCl 溶液D .2Ca(OH)溶液【答案】C 【解析】 【分析】 【详解】A 、23Na CO 溶液和NaOH 不反应,不能用于除去NaCl 溶液中混有的少量NaOH ,故A 错;B 、24H SO 溶液和NaOH 发生反应生成硫酸钠和水,会引入新杂质硫酸钠,故B 错;C 、HCl 溶液和NaOH 发生反应生成氯化钠和水,不会引入新杂质,符合题意故C 正确;D 、2Ca(OH)溶液和NaOH 不反应,不能用于除去NaCl 溶液中混有的少量NaOH ,故D 错; 故选:C 。
【点睛】除杂的原则不引入新杂质,被提纯物质不能减少,杂质容易分离。
3.下列除杂(括号内为杂质)的试剂选用正确的是( )A .AB .BC .CD .D【答案】B 【解析】 【分析】 【详解】A 、CaCl 2溶液(盐酸)加入过量的Na 2CO 3溶液发生反应;2322Na CO 2HCl=2NaCl CO H O ++↑+ 2323Na CO CaCl =2NaCl CaCO ++↓会生成新杂质NaCl ,Na 2CO 3,被提纯CaCl 2会减少,不符合题意; B 、NaOH 溶液(Na 2CO 3溶液)加入适量的Ca(OH)2溶液发生反应;2323Na CO Ca(OH)=CaCO 2NaOH +↓+ 可以去除Na 2CO 3,符合题意;C 、CuO(Cu) 加入足量的稀H 2SO 4,CuO 会和稀H 2SO 4反应生成硫酸铜和水CuO 减少,不符合题意;D 、KCl 溶液(K 2SO 4溶液)加入适量的Ba(NO 3)2溶液发生反应;243234K SO Ba(NO )=2KNO BaSO ++↓ 虽然去除了K 2SO 4但是会产生新杂质KNO 3不符合题意; 故选:B 。
初三化学化学除杂分离和提纯解题技巧及经典题型及练习题(含答案)含解析
初三化学化学除杂分离和提纯解题技巧及经典题型及练习题(含答案)含解析一、中考化学除杂分离和提纯1.下列除去杂质的方法不正确的是()A.A B.B C.C D.D【答案】B【解析】【分析】【详解】A、氧气通过灼热的铜网时,可与铜发生反应生成氧化铜,而氮气不与铜反应,能除去杂质且没有引入新的杂质,故选项所采取的方法正确;B、氧化钙与水反应生成氢氧化钙,混合物加入水,会消耗主要物质,故选项所采取的方法错误;C、浓硫酸具有吸水性,且不与二氧化碳反应,能除去杂质且没有引入新的杂质,故选项所采取的方法正确。
D,AgNO3能与适量的氯化钾溶液反应生成氯化银沉淀和硝酸钾,能除去杂质且不引入了新的杂质,故选项所采取的方法正确。
故选B。
【点睛】除杂(提纯),是指除去杂质,同时被提纯物质不得改变。
加入试剂除杂时至少要满足两个条件:①加入的试剂只能与杂质反应,不能与主要物质反应;②反应后不能引入新的杂质。
2.除去下列物质中的杂质,所选用的方法正确的是()D铁粉(锌粉)加过量CuSO4溶液充分反应后过滤、洗涤、干燥A.A B.B C.C D.D【答案】C【解析】【分析】【详解】A、除去CO2中的HCl,把气体先通过过量氢氧化钠溶液,再通过浓硫酸,氢氧化钠溶液既能吸收氯化氢气体,也能吸收二氧化碳气体,A不正确;B、除去NaCl溶液中的Na2CO3,加稀硫酸至恰好不再产生气泡为止,碳酸钠与稀硫酸反应生成硫酸钠、水和二氧化碳,虽然除去了碳酸钠,但又生成了硫酸钠,引进新的杂质,B不正确;C、除去CuSO4溶液中的H2SO4,加过量氧化铜粉末,硫酸与氧化铜反应生成硫酸铜和水,从而除去了硫酸,过量的氧化铜用过滤除去,C正确;D、除去铁粉中的锌粉,加过量CuSO4溶液充分反应后过滤、洗涤、干燥。
铁和锌在金属活动性顺序中都排在铜的前面,都能与硫酸铜反应生成铜,所以最后得到固体只有铜,D不正确。
故选C。
【点睛】利用化学方法给混合物除去杂质时,既要把杂质除去,又不能引进新的杂质。
中考化学 除杂分离和提纯 综合题含详细答案

一、中考初中化学除杂分离和提纯1.为除去下表样品中的少量杂质(括号内为杂质),所选试剂及操作方法均正确的是A.A B.B C.C D.D【答案】B【解析】【分析】【详解】A、KCl易溶于水,MnO2难溶于水,可采取加水溶解、过滤、蒸发的方法进行分离除杂,故A错误;B、NH4HCO3在加热条件下生成氮气、水和二氧化碳,碳酸钠受热不分解,能除去杂质且没有引入新的杂质,符合除杂原则,故B正确;C、KNO3和NaCl的溶解度受温度的影响不同,硝酸钾溶解度受温度影响较大,而氯化钠受温度影响较小,所以可采取加热水溶解配成饱和溶液、冷却热饱和溶液使KNO3先结晶出来、再过滤、蒸发的方法;故C错误。
D、MgCl2能与氢氧化钠溶液反应生成氢氧化镁沉淀和氯化钠,但NaOH溶液是过量的,能除去杂质但引入了新的杂质NaOH,不符合除杂原则,故D错误。
故选B。
2.要除去氯化钠溶液中含有的少量碳酸钠,可采用的方法是①通入适量的二氧化碳②加入适量的氯化钡溶液③加入适量的稀盐酸④加入适量的石灰水()A.①或③B.②或③C.②或④D.③或④【答案】B【解析】【分析】【详解】①二氧化碳不和碳酸钠溶液反应,不能除去杂质,此项错误;②氯化钡能和碳酸钠反应生成碳酸钡沉淀和氯化钠,反应时不会带入新的杂质,故此项正确;③盐酸能和碳酸钠反应,且生成氯化钠,不会带入新的杂质,此项正确;④氢氧化钙溶液能和碳酸钠反应,但反应时会生成氢氧化钠,带入新的杂质,此项错误,故选B。
3.除去下列各物质中少量杂质,所选用的试剂和操作方法均正确的是()A.A B.B C.C D.D【答案】C【解析】【分析】【详解】A、CaCO3固体高温煅烧生成氧化钙和二氧化碳,反而会把原物质除去,不符合除杂原则,选项A错误;B、洗涤剂具有乳化作用,能将大的油滴分散成细小的油滴,振荡、搅拌后不能除去杂质,不符合除杂原则,选项B错误;C、铜粉在足量氧气中加热生成氧化铜,能除去杂质且没有引入新的杂质,符合除杂原则,选项C正确;D、KClO3在二氧化锰的催化作用下生成氯化钾和氧气,二氧化锰作催化剂,反应前后质量不变,能除去杂质但引入了新的杂质二氧化锰,不符合除杂原则,选项D错误。
中考化学 溶液的除杂分离和提纯 综合题附答案解析

一、中考初中化学溶液的除杂分离和提纯1.依据实验目的,下列设计的实验方案中不合理的是A.A B.B C.C D.D【答案】D【解析】【分析】【详解】A、分别把燃着的木条伸入盛放气体的集气瓶中,能继续燃烧的为氧气,木条熄灭的为氮气,能区分氧气和氮气,方案合理;B、分别与少量熟石灰混合后,研磨、闻气味,有刺激性气味的为氯化铵,无刺激性气味的为氯化钾,能鉴别氯化铵和氯化钾固体,方案合理;C、把洁净的铜丝浸入硝酸银溶液中,铜丝表面有银析出,说明铜的活动性比银强,能比较铜和银的金属活动性,方案合理;D、向溶液中滴加适量的氯化钙溶液,充分反应后过滤,虽然能除去碳酸钠,但会引入新的杂质氯化钠,方案不合理。
故选D。
2.除去下列物质中的少量杂质,所选用的试剂或操作方法不正确的是( )A.A B.B C.C D.D【答案】C【解析】【分析】根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变。
除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质。
【详解】A、将混合气体通入氢氧化钡溶液,二氧化碳和氢氧化钡反应生成碳酸钡沉淀和水,一氧化碳不反应,然后通过干燥除掉溶液中带入的水分,可得一氧化碳,选项正确;B、过氧化氢在二氧化锰的作用下生成水和氧气,过滤后液体只有水,选项正确;C、在空气中灼烧时,铜和碳都会与氧气发生反应,选项错误;D、碳酸钠能与过量的稀盐酸反应生成氯化钠、水和二氧化碳,所得溶液是氯化钠和氯化氢的混合溶液,蒸发结晶,可得氯化钠晶体,选项正确。
故选C。
3.除去下列物质中的少量杂质(括号内为杂质),所选用试剂及操作方法均正确的是A.A B.B C.C D.D【答案】D【解析】【分析】除杂质至少要满足两个条件:①一般加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质。
【详解】A、生石灰能与水反应生成氢氧化钙,但生成的氢氧化钙能与二氧化碳反应生成碳酸钙和水,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项错误;B、氢气、CO均能与灼热的氧化铜反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项错误;C、NaOH能与硫酸反应生成硫酸钠和水,能除去杂质但引入了新的杂质硫酸钠,不符合除杂原则,故选项错误;D、KNO3和NaCl的溶解度受温度的影响不同,硝酸钾溶解度受温度影响较大,而氯化钠受温度影响较小,所以可采取加热水溶解配成饱和溶液、冷却热饱和溶液使KNO3先结晶出来、再过滤、烘干的方法,故选项正确。
【化学】九年级化学化学除杂分离和提纯题20套(带答案)及解析
【化学】九年级化学化学除杂分离和提纯题20套(带答案)及解析一、中考化学除杂分离和提纯1.下列除去杂质的试剂和方法可行的是选项物质(括号内为杂质)除杂试剂和方法A Mg(NO3)2溶液(AgNO3)加入过量铁粉,过滤B NaCl溶液(Na2SO4)加入适量BaCl2溶液,过滤C CO2(CO)通过足量澄清石灰水D N2(O2)通过灼热的氧化铜A.A B.B C.C D.D【答案】B【解析】试题分析:A、铁粉与硝酸银反应,生成银和硝酸亚铁,引来新的杂质,错误;B、硫酸钠与适量氯化钡反应,生成硫酸钡和氯化钠,正确;C、CO与澄清石灰水不发生反应,错误;D、氧化铜与氧气不发生化学反应,错误。
故选B考点:除杂质问题。
2.除去下列物质中的杂质,所选方法正确的是()选项物质杂质除去杂质的方法A C CuO加入足量稀硫酸,过滤、洗涤、干燥B NaCl Na2CO3加入足量稀硫酸,蒸发结晶C CO2CO点燃D MnO2KCl加水溶解、过滤、蒸发A.A B.B C.C D.D【答案】A【解析】【分析】【详解】A、碳不与稀硫酸反应,氧化铜能与稀硫酸反应生成硫酸铜和水,待完全反应后,过滤、洗涤、干燥可得碳,符合题意;B、加入足量稀硫酸,碳酸钠能与稀硫酸反应生成硫酸钠、二氧化碳和水,氯化钠与稀硫酸不反应,虽然除去了碳酸钠,但是引入了新的杂质硫酸钠,硫酸,不符合题意;C、二氧化碳不燃烧,也不支持燃烧,二氧化碳中混有少量一氧化碳,无法点燃,不符合题意;D、二氧化锰不溶于水,氯化钾溶于水,加水溶解、过滤,洗涤、干燥可得二氧化锰,不符合题意。
故选A。
【点睛】除杂选择试剂的原则是:不增(不引入新的杂质)、不减(不能将原物质反应掉)、不繁(整个过程不繁琐)。
3.如表中除去物质中少量杂质的方法正确的是A.A B.B C.C D.D【答案】A【解析】试题分析:除杂质的原则:所加的物质只与杂质反应,不能引入新的杂质,A、除去氯化钙溶液中的稀盐酸,加入过量的碳酸钙,发生反应:CaCO3+2HCl==CaCl2+H2O+CO2↑,然后再过滤,即可得到氯化钙溶液,正确,B、除去硫酸钾溶中的氢氧化钾,加入适量的稀盐酸,发生反应:KOH+HCl==KCl+H2O,引入了新的杂质KCl,错误,C、除去二氧化碳中氯化氢,通过足量的氢氧化钠溶液,两者都会发生反应,错误,D、除去二氧化锰中的氯化钾,根据二氧化锰不溶于水,氯化钾溶于水,故加水溶解、过滤、洗涤、烘干即可,不需要蒸发、结晶,错误,故选A考点:物质的除杂4.下列实验操作不可以达到实验目的的是()A.A B.B C.C D.D【答案】C【解析】【分析】【详解】A、氧化铜能与稀硫酸反应,木炭粉不与稀硫酸反应,故取样、加稀硫酸,能与稀硫酸反应的是氧化铜,可以用稀硫酸鉴别,不符合题意;B、氢氧化钠能与二氧化碳反应生成碳酸钠和水,干燥,可得一氧化碳,不符合题意;C、氯化铵和硫酸铵都属于铵态氮肥,和熟石灰混合研磨,均能产生有刺激性气味的气体,无法用加熟石灰、研磨,鉴别,符合题意;D、加入过量的铁粉,铁能与氯化铜反应生成氯化亚铁和铜,过滤,除去过量的铁和铜,可得氯化铜,不符合题意。
(化学)九年级化学化学除杂分离和提纯题20套(带答案)含解析
(化学)九年级化学化学除杂分离和提纯题20套(带答案)含解析一、中考化学除杂分离和提纯1.如表中除去物质中少量杂质的方法正确的是A.A B.B C.C D.D【答案】A【解析】试题分析:除杂质的原则:所加的物质只与杂质反应,不能引入新的杂质,A、除去氯化钙溶液中的稀盐酸,加入过量的碳酸钙,发生反应:CaCO3+2HCl==CaCl2+H2O+CO2↑,然后再过滤,即可得到氯化钙溶液,正确,B、除去硫酸钾溶中的氢氧化钾,加入适量的稀盐酸,发生反应:KOH+HCl==KCl+H2O,引入了新的杂质KCl,错误,C、除去二氧化碳中氯化氢,通过足量的氢氧化钠溶液,两者都会发生反应,错误,D、除去二氧化锰中的氯化钾,根据二氧化锰不溶于水,氯化钾溶于水,故加水溶解、过滤、洗涤、烘干即可,不需要蒸发、结晶,错误,故选A考点:物质的除杂2.下列除去杂质的方法不正确的是()A.A B.B C.C D.D【答案】B【解析】【分析】【详解】A、氧气通过灼热的铜网时,可与铜发生反应生成氧化铜,而氮气不与铜反应,能除去杂质且没有引入新的杂质,故选项所采取的方法正确;B、氧化钙与水反应生成氢氧化钙,混合物加入水,会消耗主要物质,故选项所采取的方法错误;C、浓硫酸具有吸水性,且不与二氧化碳反应,能除去杂质且没有引入新的杂质,故选项所采取的方法正确。
D,AgNO3能与适量的氯化钾溶液反应生成氯化银沉淀和硝酸钾,能除去杂质且不引入了新的杂质,故选项所采取的方法正确。
故选B。
【点睛】除杂(提纯),是指除去杂质,同时被提纯物质不得改变。
加入试剂除杂时至少要满足两个条件:①加入的试剂只能与杂质反应,不能与主要物质反应;②反应后不能引入新的杂质。
3.下列除杂(括号内为杂质)选用的试剂或方法错误的是()A.Cu(CuO):加入足量的稀盐酸,过滤,洗涤、烘干B.NaCl 溶液(HCl):加入过量碳酸钠,充分反应后过滤C.CO2气体(CO):将气体通过灼热的氧化铜层后收集气体D.NaCl(泥沙):加适量水充分溶解,过滤、蒸发结晶【答案】B【解析】【分析】【详解】A、在金属活动性顺序里,铜位于氢之前,不与稀盐酸反应,氧化铜能与稀盐酸反应生成氯化铜和水,加入足量稀盐酸,过滤、洗涤、干燥可得铜,不符合题意;B、加入过量的碳酸钠,碳酸钠能与稀盐酸反应生成氯化钠、二氧化碳和水,碳酸钠过量,虽然除去了杂质,但是引入了新的杂质碳酸钠,符合题意;C、将混合气体通过灼热的氧化铜,氧化铜能与一氧化碳在加热的条件下反应生成铜和二氧化碳,收集气体可得纯净的二氧化碳,不符合题意;D、氯化钠溶于水,泥沙不溶于水,加适量水充分溶解,过滤、蒸发结晶,可得氯化钠,不符合题意。
中考化学溶液的除杂分离和提纯综合题附详细答案
一、中考初中化学溶液的除杂分离和提纯1.除去下列物质中混有的少量杂质,所用除杂试剂及操作方法均正确的是A.A B.B C.C D.D【答案】A【解析】【分析】【详解】A、加入过量的CuCl2溶液和铁充分反应,得到铜和氯化亚铁溶液,过滤得到铜,洗涤、干燥得到纯净的铜,符合题意;B、KC1中的杂质MnO2,加入足量的水溶解,是KC1溶解,MnO2不能溶解,过滤、洗涤、后面应该蒸发结晶才能得到KC1,不符合题意;C、NaCl中的杂质NaNO3,加入适量的硝酸银溶液是和主要物质NaCl发生反应,没有除去杂质NaNO3,不符合题意;D、Cu中的杂质C,在空气中灼烧,Cu、C都会与氧气反应,Cu反应生成氧化铜,C反应产生二氧化碳,主要物质被反应了,不符合题意。
故选A。
2.除去下列物质中的少量杂质(括号内为杂质),所选用试剂及操作方法均正确的是A.A B.B C.C D.D【答案】D【解析】【分析】除杂质至少要满足两个条件:①一般加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质。
【详解】A、生石灰能与水反应生成氢氧化钙,但生成的氢氧化钙能与二氧化碳反应生成碳酸钙和水,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项错误;B、氢气、CO均能与灼热的氧化铜反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项错误;C、NaOH能与硫酸反应生成硫酸钠和水,能除去杂质但引入了新的杂质硫酸钠,不符合除杂原则,故选项错误;D、KNO3和NaCl的溶解度受温度的影响不同,硝酸钾溶解度受温度影响较大,而氯化钠受温度影响较小,所以可采取加热水溶解配成饱和溶液、冷却热饱和溶液使KNO3先结晶出来、再过滤、烘干的方法,故选项正确。
故选D。
3.去下列各物质中混有的少量杂质,所用试剂及操作方法均正确的是()A.A B.B C.C D.D【答案】A【解析】【分析】【详解】A、硝酸银和氯化钠反应生成氯化银沉淀和硝酸钠,过滤得到硝酸钠溶液,该选项正确;B、碳酸钠和氯化钡反应生成碳酸钡沉淀和氯化钠,除去碳酸钠后引入氯化钡(过量)新杂质,该选项不正确;C、高温条件下铜和氧气反应生成氧化铜,该选项不正确;D、氧化钙和盐酸反应生成氯化钙和水,过量的氧化钙和水反应生成氢氧化钙,除去盐酸后引入新杂质氢氧化钙,该选项不正确。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
初三化学化学除杂分离和提纯试题(有答案和解析)一、中考化学除杂分离和提纯1.除去下列物质中的少量杂质,所选用的试剂和操作方法都正确的是()A.A B.B C.C D.D【答案】B【解析】【分析】【详解】A、将混合气体通过足量的铜网,铜与氮气不反应,铜与氧气能在加热的条件下反应生成氧化铜,但是常温下铜与氧气不反应,常温下,通过足量的铜网,不能除去混合气体中的氧气,不符合题意;B、氯化钾能溶于水,二氧化锰不溶于水,加水溶解、过滤,除去二氧化锰,蒸发、结晶得到氯化钾,符合题意;C、活性炭具有吸附性,能吸附水中的色素和异味,故加活性炭可除去水中的臭味,过滤,除去活性炭,才能得到水,需加过滤步骤,不符合题意;D、将混合气体通过适量的氢氧化钠溶液,氢氧化钠与二氧化碳反应生成碳酸钠和水,虽然除去了杂质二氧化碳,但是一氧化碳通过氢氧化钠溶液会携带上水蒸气,引入了新的杂质水蒸气,不符合题意。
故选B。
2.除去CO气体中少量CO2,可采用的方法是()A.把混合气体点燃B.把混合气体通过水中C.把混合气体通过灼热的CuO粉末D.把混合气体通过足量的澄清石灰水【答案】D【解析】【分析】【详解】A、一氧化碳能与氧气反应生成二氧化碳,反而会把原物质除去,不符合除杂原则,故选项错误。
B、二氧化碳能与水反应生成碳酸,但是碳酸不稳定会分解成二氧化碳和水,不能彻底除去杂质,故选项出错误。
C、一氧化碳能与灼热的氧化铜反应生成铜和二氧化碳,二氧化碳不能与灼热的氧化铜反应,反而会把原物质除去,不符合除杂原则,故选项错误。
D、CO2能与足量澄清石灰水反应生成碳酸钙和水,CO不与足量澄清石灰水反应,能除去杂质且没有引入新的杂质,符合除杂原则,故选项正确。
故选:D。
【点睛】根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.3.为除去粗盐中的泥沙、Ca2+、Mg2+、SO42-等杂质,可将粗盐溶于水,再进行下列五步操作:①过滤②加过量的氢氧化钠溶液③加稍过量的盐酸④加过量的碳酸钠溶液⑤加过量的氯化钡溶液⑥蒸发结晶。
正确的操作顺序是()A.④②⑤③①⑥B.②④⑤①③⑥C.②⑤④①③⑥D.⑤④②③①⑥【答案】C【解析】【详解】镁离子用氢氧根离子沉淀,加入过量的氢氧化钠可溶液以将镁离子沉淀;硫酸根离子用钡离子沉淀,加入过量的氯化钡溶液可以将硫酸根离子沉淀;至于先除镁离子,还是先除硫酸根离子都可以;钙离子用碳酸根离子沉淀,除钙离子加入过量的碳酸钠溶液转化为沉淀,但是加入碳酸钠溶液要放在加入的氯化钡溶液之后,这样碳酸钠会除去反应剩余的氯化钡;完全反应后,进行过滤,再加入稍过量盐酸除去反应剩余的氢氧根离子和碳酸根离子,最后蒸发结晶,所以正确的顺序为:②⑤④①③⑥或⑤②④①③⑥。
故选:C。
【点睛】根据镁离子用氢氧根离子沉淀,硫酸根离子用钡离子沉淀,钙离子用碳酸根离子沉淀,过滤要放在所有的沉淀操作之后,加碳酸钠要放在加氯化钡之后,可以将过量的钡离子沉淀,最后再用盐酸处理溶液中的碳酸根离子和氢氧根离子,进行分析解答。
4.除去下列物质中少量杂质(括号内为杂质),所用除去杂质的方法正确的是()选项待提纯的物质除去杂质的方法A FeSO4溶液(CuSO4)加入适量Zn粉,过滤B KCl( MnO2)加水溶解、过滤、洗涤、干燥A.A B.B C.C D.D【答案】D【解析】【分析】【详解】A、向混合溶液中加入适量锌粉,锌能与硫酸铜反应生成硫酸锌和铜,虽然除去了杂质,但是引入了新的杂质,不符合题意;B、氯化钾溶于水,二氧化锰不溶于水,加水溶解、过滤,可将二氧化锰除去,然后蒸发结晶可得氯化钾,不符合题意;C、向混合溶液中加入过量的氢氧化钠,氢氧化钠与氯化铁反应生成氢氧化铁和氯化钠,虽然除去了杂质,但是氢氧化钠过量,引入了新的杂质,不符合题意;D、将混合气体通过灼热足量的氧化铜,氧化铜与一氧化碳反应生成铜和二氧化碳,可将杂质除去,符合题意。
故选D。
【点睛】除杂选择试剂的原则是:不增(不引入新的杂质)、不减(不能将原物质反应掉)、不繁(整个过程不繁琐)。
5.除去下列各物质中混有的少量杂质(括号内为杂质),所用试剂及操作方法均正确的是()A.NaCl溶液(MgCl2)加入适量的NaOH溶液、过滤B.铁粉(Fe2O3)加入足量的稀盐酸,过滤C.CO气体(CO2)通入氧气点燃D.K2SO4溶液(K2CO3)加入足量的稀硫酸【答案】A【解析】【详解】A、MgC12能与适量的NaOH溶液反应生成氢氧化镁沉淀和氯化钠,再过滤,能除去杂质且没有引入新的杂质,故A正确;B、Fe2O3和Fe均能与足量的稀盐酸反应,不但能把杂质除去,也会将主要物质除去,故B错误;C、CO气体与氧气在点燃时生成二氧化碳,混合气体通入氧气点燃,会将主要物质除去,故C错误;D、K2CO3能与足量的稀硫酸反应生成硫酸钾、水和二氧化碳,能除去杂质但引入了新的杂质硫酸(过量的),故D错误。
故选A。
【点睛】解答本题的关键是要充分理解各种物质的性质,只有这样才能对问题做出正确的判断,另外需要注意的就是选用的除杂试剂不能与主要物质反应,反应后不能引入新的杂质,还需要根据实际情况控制所选试剂的量。
6.下列实验操作中不能达到实验目的的是A.A B.B C.C D.D【答案】A【解析】【详解】A、溶解后过滤得到氯化钠溶液,再蒸发才能够得到氯化钠固体,该选项不能达到实验目的;B、加入氯化钡溶液和稀硝酸后,产生白色沉淀的是稀硫酸,无明显现象的是盐酸,该选项能够达到实验目的;C、高温条件下碳酸钙分解生成氧化钙和二氧化碳,该选项能够达到实验目的;D、加入熟石灰研磨,能够产生刺激性气味的是氯化铵,无明显现象的是硫酸钾,该选项能够达到实验目的。
故选:A。
7.除去下列物质中的少量杂质,选用的试剂及操作方法均正确的是()A.A B.B C.C D.D【答案】D【解析】【详解】A、CO2和HCl气体均能与NaOH溶液反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项所采取的方法错误。
B、Na2CO3能与适量CaCl2溶液反应生成碳酸钙沉淀和氯化钠,能除去杂质但引入了新的杂质氯化钠,不符合除杂原则,故选项所采取的方法错误。
C、二氧化碳中的少量一氧化碳不能点燃,故选项所采取的方法错误。
D、KCl易溶于水,MnO2难溶于水,可采取加水溶解、过滤、蒸发的方法进行分离除杂,故选项所采取的方法正确。
故选:D。
8.除去下列物质中的少量杂质,所选用试剂及操作方法均正确的是()A.A B.B C.C D.D【答案】D【解析】【详解】A、镁粉能与氯化铜反应生成氯化镁和铜,镁粉也能和氯化亚铁反应生成氯化镁和铁,虽然除去了杂质,也除去了原物质,不符合题意;B、加适量的氯化钡,氯化钡能与硫酸钠反应生成硫酸钡沉淀和氯化钠,虽然除去了杂质,但是引入了新物质,不符合题意;C、加入足量的硝酸钡,硝酸钡能与硫酸反应生成硫酸钡沉淀和硝酸,虽然除去了杂质,但是引入了新的物质,不符合题意;D、二氧化锰不溶于水,氯化钾溶于水,通过加足量水、溶解、过滤、洗涤、干燥,可除去氯化钾,得到二氧化锰,符合题意。
故选D。
除杂选择试剂的原则是:不增(不引入新的杂质)、不减(不能将原物质反应掉)、不繁(整个过程不繁琐)。
9.除去下列物质中的少量杂质(括号内为杂质),拟定的实验方案可行的是A.MnO2固体(KC1):加入适量水溶解,过滤,蒸发B.氧气(水蒸气):通过装有足量无水氯化钙的干燥管C.二氧化碳(氯化氢气体):依次通过足量的氢氧化钠溶液和浓硫酸D.NaOH溶液(Na2CO3):加入适量的BaCl2溶液至恰好完全反应,过滤【答案】B【解析】【分析】根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变。
除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质。
【详解】A、KCl易溶于水,MnO2难溶于水,可采取加水溶解、过滤、洗涤、干燥的方法进行分离除杂,选项所采取的方法错误,不符合题意;B、无水氯化钙具有吸水性,且不与氧气反应,能除去杂质且没有引入新的杂质,符合除杂原则,选项所采取的方法正确,符合题意;C、CO2和HCl气体均能与NaOH溶液反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,选项所采取的方法错误,不符合题意;D、Na2CO3能与适量的BaC12溶液反应生成碳酸钡沉淀和氯化钠,能除去杂质但引入了新的杂质氯化钠,不符合除杂原则,选项所采取的方法错误,不符合题意。
故选:B。
10.下列实验操作一定能达到实验目的的是A.A B.B C.C D.D【答案】B【解析】A、除去KCl溶液中的CuCl2加入适量的NaOH溶液,NaOH溶液与CuCl2溶液反应生成Cu ( OH)2沉淀和NaCl,能除去CuCl2,但引入了新杂质NaCl;故选项错误;B、鉴别Ca( OH)2溶液和NaOH溶液时,加入Na2CO3溶液,Na2CO3溶液能与Ca(OH)2溶液反应产生CaCO3白色沉淀,Na2 CO3溶液与NaOH溶液不反应,无明显现象,可鉴别两者;故选项正确;C、分离食盐和泥沙时,加水溶解、过滤能除去不溶性的杂质泥沙,但还需要蒸发结晶得到食盐;故选项错误;D、检验二氧化碳应选择澄清石灰水,不能用燃着的木条,因为不燃烧且不支持燃烧的气体还有很多,如氮气等;故选项错误。
故选:B。
