第十六章 含氮有机化合物精品PPT课件
合集下载
高一化学氮及其化合物ppt课件.ppt
病原体侵入机体,消弱机体防御机能 ,破坏 机体内 环境的 相对稳 定性, 且在一 定部位 生长繁 殖,引 起不同 程度的 病理生 理过程
氮气
1、氮元素的存在及单质的物理性质
存 游离态形式存在于空气中 在 化合态形式存在于多种无机物及有机物中
物 理 无色无味的气体、密度比空气小; 性 难溶于水,1体积水溶解0.02体积的氮气。
思考题
1、1molMg在足量的氮气、空气、纯氧气、二
氧化碳气体中燃烧生成 的固体质量由大到小的 排列次序是_二__氧__化__碳__>__氧__气___>_空__气__>__氮__气_____.
点燃
2Mg + O2 →2MgO
点燃
3Mg + N2 → Mg3N2
(40g) (100/3g)
2Mg + CO2 →点燃2MgO +C (46g)
质
病原体侵入机体,消弱机体防御机能 ,破坏 机体内 环境的 相对稳 定性, 且在一 定部位 生长繁 殖,引 起不同 程度的 病理生 理过程
工业上怎样制取氮气?利用氮气的什么性质?
空气
液化
先气化 液态空气
氮气 b.p -195.8℃
后气化
氧气 b.p -183℃
病原体侵入机体,消弱机体防御机能 ,破坏 机体内 环境的 相对稳 定性, 且在一 定部位 生长繁 殖,引 起不同 程度的 病理生 理过程
氮的固定------把大气中的游离态氮转化为氮的化合物 1生物固氮
豆科作物根瘤中的固氮菌常温下将空气中的氮 气转化为硝酸盐。
病原体侵入机体,消弱机体防御机能 ,破坏 机体内 环境的 相对稳 定性, 且在一 定部位 生长繁 殖,引 起不同 程度的 病理生 理过程
含氮有机化合物—硝基化合物(药学有机化学课件)

【例如】
硝基对酚酸性的影响
苯酚 邻(或对)硝基苯酚 2,4-二硝基苯酚 2,4,6-三硝基苯酚
pKa=9.89 pKa=7.17 pKa=3.96 强酸
【例如】
HNO3 , H2SO4 50~55℃
NO2 发烟 HNO3 , H2SO4 95℃
NO2 NO2
三、硝当苯环上连有硝基时,尤其当硝基连 在邻位或对位时,硝基的吸电子作用可通过苯环传递到酚羟基
上,使酚的酸性增强。硝基数目越多,酸性越强。
有机化学/含氮有机化合物
芳香硝基化合物的 化学性质
一、还原反应
第一节 硝基化合物 酸衍生物
硝基化合物容易被还原,最终产物为伯胺。 常用还原剂是化学还原剂(酸性介质中的铁粉)
【例如】
NO2
Fe + HCl
NH2
苯胺
二、取代反应
第一节 硝基化合物 酸衍生物
由于苯环上硝基的强吸电子效应,使苯环上的 电子云密度降低较多,因此不利于亲电取代反应的 进行,硝基是间位定位基。
含氮有机化合物

β -硝基苯乙烯
3.2 胺
氨分子中一个,两个或三个氢原子被烃基取代所生成的化合物分 别称为伯胺(一级胺)、仲胺(二级胺)和叔胺(三级胺)。铵盐分 子中四个氢原子都被烃基取代生成的化合物称为季铵盐。
有些胺类化合物因其特殊的生理活性,与人类的生命活动及健康 密切相关。
H3C N H3C N + CH2 N CH2CH2OH S Cl-
Cl NO2
OH NO2
1.NaOH, 100℃ 2. H3O+
NO2 NO2
Cl + NH3 NO2 Cl NO2 + CH3NH2 NO2 Cl NO2 + CH3CH2OH NO2 F + CH3OK NO2
CH3OH
25℃
NH2
NO2 NHCH3 NO2 NO2 OCH2CH3
Et3N
20℃
CH3
(CH3CO)2O
CH3
1.Br2 2.OH-,H2O
CH3
NaNO2,HCl
CH3
H3PO2,H2O
CH3 Br
Br NH2
0~5 ℃
NH2
NHCOCH3
Br 25 ℃ N2Cl
NH2
1.HNO3,H2SO4 2.Sn+HC2
Br
N2Cl Br
H3PO2
Br
烷基供电子的诱导效应与水的溶剂化效应二者综合作用的结果,造
成了胺在水中的碱性强度次序。
H R2N H
H :O H H :O H
R3N-H
H :O H
仲胺的溶剂化情况
叔胺的溶剂化情况
芳香胺的碱性比氨和脂肪胺弱,这是由于氮原子上孤对电子通过 p-π 共轭部分地向苯环转移,形成更稳定的共轭体系,使氮原子与 质子的结合能力降低。
3.2 胺
氨分子中一个,两个或三个氢原子被烃基取代所生成的化合物分 别称为伯胺(一级胺)、仲胺(二级胺)和叔胺(三级胺)。铵盐分 子中四个氢原子都被烃基取代生成的化合物称为季铵盐。
有些胺类化合物因其特殊的生理活性,与人类的生命活动及健康 密切相关。
H3C N H3C N + CH2 N CH2CH2OH S Cl-
Cl NO2
OH NO2
1.NaOH, 100℃ 2. H3O+
NO2 NO2
Cl + NH3 NO2 Cl NO2 + CH3NH2 NO2 Cl NO2 + CH3CH2OH NO2 F + CH3OK NO2
CH3OH
25℃
NH2
NO2 NHCH3 NO2 NO2 OCH2CH3
Et3N
20℃
CH3
(CH3CO)2O
CH3
1.Br2 2.OH-,H2O
CH3
NaNO2,HCl
CH3
H3PO2,H2O
CH3 Br
Br NH2
0~5 ℃
NH2
NHCOCH3
Br 25 ℃ N2Cl
NH2
1.HNO3,H2SO4 2.Sn+HC2
Br
N2Cl Br
H3PO2
Br
烷基供电子的诱导效应与水的溶剂化效应二者综合作用的结果,造
成了胺在水中的碱性强度次序。
H R2N H
H :O H H :O H
R3N-H
H :O H
仲胺的溶剂化情况
叔胺的溶剂化情况
芳香胺的碱性比氨和脂肪胺弱,这是由于氮原子上孤对电子通过 p-π 共轭部分地向苯环转移,形成更稳定的共轭体系,使氮原子与 质子的结合能力降低。
医用化学第十六章 含氮有机化合物

一、杂环化合物的分类和命名 二、单杂环化合物的结构和芳香性 在所有的杂环母核中,凡是具有共轭双键体系的五元 环和六元环,都具有芳香性。现以单杂环化合物为例,来
分析它们的结构和芳香性的关系。
呋喃
噻吩
呋喃、噻吩、吡咯的轨道结构示意图
吡咯
这个p-π共轭体系中,五个原子分享六个π电子,电子离域 使环上各碳原子的电子云密度相对升高,因此,这类杂环进 行亲电性取代
二、胺的结构 脂肪胺具有类似氨的结构,是一个棱锥体结构。 胺的孤对电子位于棱锥体的顶端,决定了胺的某些化学性质, 例如碱性和亲核性。
氨、甲胺和三甲胺的结构
三、胺的性质 1.胺的碱性和成盐反应
R NH2 + H
RNH2 + HCl
NH2 + HCl
当铵盐与碱溶液作用时,可重新游离出原来的胺,说明胺 的碱性较弱。
O H N1 6 O
5 2 3 4
O C2H5 C2H5 O O H N N H C2H5 (CH2)4CH3 O
N
H
巴比妥
O H N O N H C2H5 C6H5 O
戊巴比妥
O H N O N H C2H5 CH3 CH2CH2CH CH3 O
苯巴比妥(鲁米那)
异戊巴比妥
四、磺胺及磺胺类药物 磺胺类药物是一类重要的抗菌药物,自上世纪三十年代 开始使用,至今仍为临床所采用。
N H2N SO 2NH N
H2N N N NH2 CH2 OCH3 OCH3 OCH3
磺胺嘧啶(SD)
三甲氧基苄氨嘧啶(TMP)
N
H2N
SO 2NH
O CH3
磺胺甲基异噁唑(SMZ)
第三节 杂环化合物
由碳原子和其它原子构成的环状结构称为杂环。 碳以外的原子称杂原子,常见的杂原子为氮、氧、 硫等。含有杂环结构的一类化合物称为杂环化合物。 环醚、内酯、交酯、环状酸酐、内酰胺等化合 物都不属于杂环化合物。 杂环化合物通常是指环系较为稳定,具有一定 程度芳香性的一类化合物,即芳杂环化合物。这类 化合物在结构上与芳香环相似,是一个闭合的共轭 体系,一般都符合4n+2规则。
《有机含氮化合物》课件

将硝基化合物或腈类化合物还原为 胺类。
重氮化反应
通过重氮盐与氢、醇、酚等反应, 生成相应的胺类化合物。
04
硝基化合物的合成
硝酸盐的还原
将硝酸盐通过加氢还原或电解 还原等方法得到硝基化合物。
重氮化反应
通过重氮盐与酸反应,生成相 应的硝基化合物。
氧化偶联
利用氧化剂将芳香烃或烯烃氧 化偶联成硝基化合物。
有机含氮化合物中的硝基 化合物可用作燃料添加剂 ,提高燃料的燃烧效率。
塑料和橡胶添加剂
一些有机含氮化合物可用 作塑料和橡胶的添加剂, 改善其性能。
表面活性剂
有机含氮化合物中的季铵 盐类化合物可用作表面活 性剂,如十二烷基三甲基 氯化铵等。
05
有机含氮化合物的前景 展望
新合成方法的研究
总结词
新合成方法的研究将为有机含氮化合物的制备提供更多可能性,有助于发现更高效、环保的合成路径 。
硝化反应
在浓硫酸和硝酸的混合酸中, 将有机物进行硝化反应得到硝
基化合物。
腈类化合物的合成
醛或酮的氰化
在酸性条件下,醛或酮与氰化钠或氰化钾反 应生成腈类化合物。
烯烃的氢甲酰化
在催化剂存在下,烯烃与氢氰酸反应生成相 应的腈类化合物。
重氮化反应
通过重氮盐与氰化钠或氰化钾反应,生成相 应的腈类化合物。
酯的氰解
03
颜色
有机含氮化合物的颜色多样,取决于其特定的结构。例如,含有共轭双
键的化合物可能呈现黄色或棕色,而含有苯环的化合物则可能呈现不同
的颜色。
化学性质
酸碱性
稳定性
有机含氮化合物可以表现出酸性和碱 性性质。例如,胺类化合物是碱性的 ,而许多硝基化合物和腈则是酸性的 。
重氮化反应
通过重氮盐与氢、醇、酚等反应, 生成相应的胺类化合物。
04
硝基化合物的合成
硝酸盐的还原
将硝酸盐通过加氢还原或电解 还原等方法得到硝基化合物。
重氮化反应
通过重氮盐与酸反应,生成相 应的硝基化合物。
氧化偶联
利用氧化剂将芳香烃或烯烃氧 化偶联成硝基化合物。
有机含氮化合物中的硝基 化合物可用作燃料添加剂 ,提高燃料的燃烧效率。
塑料和橡胶添加剂
一些有机含氮化合物可用 作塑料和橡胶的添加剂, 改善其性能。
表面活性剂
有机含氮化合物中的季铵 盐类化合物可用作表面活 性剂,如十二烷基三甲基 氯化铵等。
05
有机含氮化合物的前景 展望
新合成方法的研究
总结词
新合成方法的研究将为有机含氮化合物的制备提供更多可能性,有助于发现更高效、环保的合成路径 。
硝化反应
在浓硫酸和硝酸的混合酸中, 将有机物进行硝化反应得到硝
基化合物。
腈类化合物的合成
醛或酮的氰化
在酸性条件下,醛或酮与氰化钠或氰化钾反 应生成腈类化合物。
烯烃的氢甲酰化
在催化剂存在下,烯烃与氢氰酸反应生成相 应的腈类化合物。
重氮化反应
通过重氮盐与氰化钠或氰化钾反应,生成相 应的腈类化合物。
酯的氰解
03
颜色
有机含氮化合物的颜色多样,取决于其特定的结构。例如,含有共轭双
键的化合物可能呈现黄色或棕色,而含有苯环的化合物则可能呈现不同
的颜色。
化学性质
酸碱性
稳定性
有机含氮化合物可以表现出酸性和碱 性性质。例如,胺类化合物是碱性的 ,而许多硝基化合物和腈则是酸性的 。
大学有机化学课件含氮化合物详解演示文稿

R3N
蒸出物 R3N
蒸馏
残留物
Na C6H5SO2N -R
滤液 抽滤
Na 1. H3 O
C6H5SO2N -R
R-NH2
2. OH
C6H5SO2N -R2
滤饼 C6H5SO2N -R2
1. H3 O R2NH 2. OH
34
第34页,共89页。
三)、与亚硝酸的反应(P91)
1、脂肪胺与亚硝酸的反应
4
第4页,共89页。
三、硝基化合物的化学性质
1、脂肪族硝基化合物 ⑴、酸性
CH3-NO2
pKa: 10.2
H
O
R-CHN
O
假酸式 (硝基式)
CH3CH2-NO2 8.5
CH3-CH-CH3
NO2 7.8
OH
R-CHN
NaOH
O
酸式 (假酸式)
O-
R-CHN
Na+
O
5
第5页,共89页。
⑵、与羰基化合物的缩合反应
溶解
SO2-Cl + H-N-R2
仲胺
NaOH
SO2NR2
沉淀
SO2Cl + N-R3
叔胺
NaOH
R3N +
SO2O-Na+ + NaCl
不反应 (黄色油状物)
33
第33页,共89页。
用兴斯堡反应分离伯、仲、叔胺的混合物:
RNH2 R2NH R3N
C6H5SO2Cl NaOH
Na C6H5SO2N -R C6H5SO2N -R2
第二节 胺
胺类广泛地存在于生物界,具有极其 重要的生理作用。
绝大多数的药物含有胺的官能团——氨基。 蛋白质、核酸、许多激素、抗生素和生物
蒸出物 R3N
蒸馏
残留物
Na C6H5SO2N -R
滤液 抽滤
Na 1. H3 O
C6H5SO2N -R
R-NH2
2. OH
C6H5SO2N -R2
滤饼 C6H5SO2N -R2
1. H3 O R2NH 2. OH
34
第34页,共89页。
三)、与亚硝酸的反应(P91)
1、脂肪胺与亚硝酸的反应
4
第4页,共89页。
三、硝基化合物的化学性质
1、脂肪族硝基化合物 ⑴、酸性
CH3-NO2
pKa: 10.2
H
O
R-CHN
O
假酸式 (硝基式)
CH3CH2-NO2 8.5
CH3-CH-CH3
NO2 7.8
OH
R-CHN
NaOH
O
酸式 (假酸式)
O-
R-CHN
Na+
O
5
第5页,共89页。
⑵、与羰基化合物的缩合反应
溶解
SO2-Cl + H-N-R2
仲胺
NaOH
SO2NR2
沉淀
SO2Cl + N-R3
叔胺
NaOH
R3N +
SO2O-Na+ + NaCl
不反应 (黄色油状物)
33
第33页,共89页。
用兴斯堡反应分离伯、仲、叔胺的混合物:
RNH2 R2NH R3N
C6H5SO2Cl NaOH
Na C6H5SO2N -R C6H5SO2N -R2
第二节 胺
胺类广泛地存在于生物界,具有极其 重要的生理作用。
绝大多数的药物含有胺的官能团——氨基。 蛋白质、核酸、许多激素、抗生素和生物
氮及其氮的化合物课件

03
硝酸盐的种类
硝酸盐是一类无机化合物 的总称,包括硝酸钠、硝 酸钾、硝酸钙等。
硝酸盐的性质
硝酸盐易溶于水,具有较 高的稳定性,在自然界中 广泛存在。
硝酸盐的应用
硝酸盐是重要的工业原料 ,可用于制造化肥、炸药 、烟火等。
铵盐
铵盐的种类
铵盐是一类含氮的离子化 合物,常见的有氯化铵、 硫酸铵、硝酸铵等。
铵盐的性质
铵盐易溶于水,具有刺激 性气味,在加热时易分解 。
铵盐的应用
铵盐是重要的氮肥,也可 用于制造其他含氮化合物 和药物。
氰化物
氰化物的种类
氰化物是一类含碳和氮的化合物,常见的有氰化钠、氰化钾、氢 氰酸等。
氰化物的性质
氰化物具有剧毒,易溶于水,可在生物体内分解。
氰化物的作用与危害
氰化物在工业上用于电镀、金属热处理等,但如果不慎摄入或接触 ,会对人体造成严重危害,甚至致命。
氮气是一种非极性分子,不溶于水, 但可以溶于乙醇和乙醚等有机溶剂。
氮气的化学性质
氮气是一种惰性气体,化学性质不活 泼,常温下很难与其他物质发生反应 。
氮气是一种重要的工业气体,广泛应 用于化工、电子、航空航天等领域。
在高温或放电条件下,氮气可以与氧 气、氢气等物质发生反应,生成一氧 化氮、二氧化氮、氨气等化合物。
氮及其氮的化合物课件
目录
• 氮气 • 氮的氧化物 • 含氮无机化合物 • 氮的有机化合物 • 氮肥 • 总结与展望
01
氮气
氮气的物理性质
氮气的分子式为N2,是一种无色、 无味、无毒的气体。
氮气是一种双原子气体,其化学键是 共价键,分子之间是单键结合。
氮气的相对分子质量为28.0134,是 空气的主要成分之一,约占空气的 78%。
有机化学 含氮化合物PPT课件

RX R2NH
RX R3N
R4N+X--
四、与亚硝酸反应
亚硝酸(HNO2 )不稳定, 反应时由 亚硝酸钠与盐酸或硫酸作用而得。
1、脂肪胺与HNO2的反应:
第32页/共96页
RCH2CH2NH2 NaNO2 + HCl 低温
RCH2CH2N2Cl 重氮盐
分解 RCH2CH2 + N2 + Cl
生成的碳正离子可以发生各种不同 的反应生成烯烃、醇和卤代烃。
R4NX 季铵盐
ArNR2
R4NOH 季铵碱
必须注意区分“胺”、“铵”、“氨”的用法。
二、命名
1、简单的胺: 烃基数目 + 烃基名称 + 胺。
CH3NH2 (CH3)2NH CH3NHC2H5 CH3
NH2
甲胺
二甲胺 甲乙胺
第16页/共96页
对甲苯胺
2、多元胺: 烃基名称 + 氨基数目 + 胺。
NH2CH2CH2NH2
对于取代芳胺,当苯环上是供电子基 团,碱性增加,反之,当苯环上是吸电子 基团,碱性减小。
第23页/共96页
NH2
NH2
NH2
NO2
CH3
H
a
b
c
CH3CH2NH2 d
由于胺是弱碱,其盐与强碱作用可以 析出胺,通过该性质可以分离、提纯胺类 化合物:
RN+H3X--
+ NaOH
RNH2
第24页/共96页
RN
H OH2 H OH2 H OH2
H OH2 R2 N H OH2
2、芳香族胺ArNH2的碱性
第22页/共96页
H
R3
章含氮有机化合物精品PPT课件
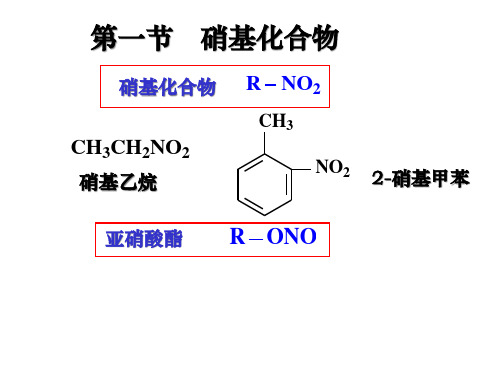
4.21
4.76
O2N
NH2 CH3
NH2
13.0
8.92
碱性强度:脂肪胺 > 氨 > 芳香胺
NH2 9.37
N
碱性强度: 二甲胺 > 甲胺 > 三甲胺 (在水溶液中) 三甲胺 > 二甲胺 > 甲胺 (在气体状态)
影响碱性强弱的因素:
电子效应:
3o胺 > 2o胺 > 1o胺
溶剂化效应: NH3 > 1o胺 > 2o胺 > 3o胺
[(CH3)2CH]4N+I-
碘化四异丙铵
CH2CH2OH CH3 N+ CH3 OH-
CH3
氢氧化(2-羟乙基)三甲铵 (俗名胆碱)
二、 胺的结构
sp3
N
105.9o
H3C 112.9oH H
孤电子对使胺具有亲核性、碱性;
CH3
H5C2
N+ ph CH2CH=CH2
R 3
N R 2
R 1
CH3
CH3CH2CH CH CH2
+N(CH3)3
2CH3CH2CH2CH=CH2 + CH3CH2CH=CHCH3 + 2N(CH3)3 + H2O
55.7%
1.3%
Hofmann消除规则 生成双键碳上烷基取代较少的烯烃
H
H
CH3CH2CH CH CH2 +N(CH3)3
H2CH CH CH2 ]
N(CH3)2 + HO NO 3o胺
ON
N(CH3)2 (绿色结晶)
5. 芳核亲电取代反应
1). 卤代
NH2
含氮有机化合物ppt课件

2.成盐 胺是弱碱,只能与强无机酸反应生成盐, 但遇到强碱又重新游离析出。
HCl + CH NH CH NH 3 2 3 3Cl OH 氯 化 甲 铵
—
HCl + — NH NH 3Cl 2 OH 氯 化 苯 铵
胺的成盐反应有两个重要用途: (1)制作针剂:把难溶于水的胺类药物变成 可溶于水的盐 。
铵 表示胺的盐或季铵类化合物。
1.简单胺的命名:
以胺为母体,把烃基的名称写在“胺”字前面。
烃基名(先小后大) + 胺
CH3NH2 甲胺
(C2H5)3N 三乙胺
CH3-NH-CH(CH3)2 甲异丙胺
CH 3 CH CH -NCH CH CH 3 2 2 2 3
NH NH 2 2 CH -CH -CH -CH -CH-C 3 2 2 3
O C — CH 3 CH CH NH CH O 3 2 3+ C — CH 3 甲 乙 胺 ( 仲 胺 ) O CH 3
酰 化 剂 (CH ) N 3 3
CH COO + CH CH N-COCH 3 3 2 3
不 反 应
三 甲 胺 ( 叔 胺 )
生成的酰胺在酸或碱催化下水解,可除去 酰基,恢复氨基。因此,在有机合成反应中, 常利用酰化反应保护氨基。 胺酰化反应的应用:
1.伯胺与HNO2的反应
HCl + [ R N N C l ] + ≡ + RNH H O HNO 2 2 2 脂 肪 伯 胺 脂 肪 重 氮 盐 ( 极 不 稳 定 )
低 温 或 室 温
ROH(混合物 ) +N HCl 2+
可定量测定-NH2
芳香伯胺与HNO2在低温下反应,生成芳香族 重氮盐——重氮化反应。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
NH CH3 NaNO2+HCl
NO N CH3
N-甲基-N-亚硝基苯胺
N-亚硝基化合物为黄色油状液体或固体,可用于 鉴别,毒性很强,它可以破坏生物体内的细胞蛋 白,是引起人类癌症的主要致癌物,在近300种N亚硝基化合物中约90%具有致癌作用。
(3) 叔胺与亚硝酸的反应 生成盐,无明显变化,可用于与伯、仲胺的区别。
R NH2 + HNO2 H+ R OH + H2O + N2
H 2 O
N H 2 + H N O 2 常 温
O H + N 2
NH2 + NaNO2 + HCl 0~5℃
N2+Cl + NaCl
(2) 仲胺与亚硝酸反应
C2H5
C2H5
NH NaNO2+HCl
N NO + H2O
C2H5
C2H5
N-亚硝基二乙胺
H2N
SO3H
对氨基苯磺酸
季铵类化合物的命名与无机铵盐和氢氧化铵的 命名相似。例如:
[(CH3)4N] + Cl- 氯化四甲铵
[(CH3)3NCH2CH3]+OH- 氢氧化三甲基乙基铵
注意“氨”、“胺”和“铵”的区别
二、胺的结构 N采取sp3杂化,脂肪胺具有类似氨的结构,是一
个棱锥体结构,胺的孤对电子位于棱锥体的顶端,决 定了胺的某些化学性质,例如碱性和亲核性。
R3N + HNO2
R3NH+ NO2
芳香叔胺与亚硝酸反应,发生芳环上的亲电取 代反应,生成C-亚硝基化合物,这是在强酸条件 下发生的反应,实际产物是红色盐酸盐,可用于 鉴别 。
CH3
CH3
N
CH3
CH3
N
NaNO2+HCl
N,N-二甲基苯胺
NO
N,N-二甲基对亚硝基苯胺
4.芳胺苯环的亲电取代反应
第十六章 有机含氮化合物
分子结构中含有碳氮键(C-N)的一类化合物。广 泛分布于自然界中,与日常生活及生命过程密切相关, 在生命科学中占有及其重要的地位 。
第一节 胺 一、胺的结构、分类和命名
氨分子中的氢原子被烃基所取代的衍生物称为胺。
(一) 分类 按烃基种类的不同分为:脂肪胺和芳香胺。 按氨基个数的不同分为:一元胺(含一个氨基)、二 元胺(含两个氨基)和多元胺(含两个以上的氨基)。
在适当的条件下,重氮盐可与芳胺或酚类化合物 作用,生成一类有颜色的偶氮化合物。这类反应 称为偶联反应。
N2+Cl +
中性或弱酸性
N(CH3)2
0℃
NN
N(CH3)2 + HCl
对二甲氨基偶氮苯(黄色)
N2+Cl +
OH 弱碱性
0℃
NN
OH + HCl
对羟基偶氮苯(桔黄色)
第二节 酰胺
一、酰胺的结构和命名 羧酸分子中羧羟基被氨基或烃氨基取代后的
NH2
NH2
+ 3Br2
Br
Br
Br 白
+ 3HBr
用于鉴别
5. 重氮化及重氮盐的偶联反应
低温条件下,芳香伯胺在强酸性溶液中与亚硝酸 反应,生成芳香重氮盐,该反应称为重氮化反应
NH2 + NaNO2 + HCl 0~5℃
N2+Cl + NaCl
Note:重氮盐在低温水溶液中较稳定,温度升高 时分解,放出氮气生成酚。
简单胺的命名是以胺为母体。
CH3NH2 甲胺
CH3CH2NHCH2CH3 H3NHCH2CH3
二乙胺
甲乙胺
NH2
CH2NH2
NH2
苯胺
苄胺
-萘胺
Note:当氮原子上同时连有芳香烃基和脂肪烃基 时,则以芳香胺作为母体,脂肪烃基作为取代 基写在母体名称前,并冠以“N” 字:
N H C H 3
C H 3 N
氨、甲胺和三甲胺的结构 三、胺的性质
1.胺的碱性和成盐反应
:
R NH2 + H OH
RNH2 + HCl
NH2 + HCl
[R NH3]+ + OH
RNH3+Cl
NH3+Cl
NH2.HCl
氯化苯铵 苯胺盐酸盐
Note:胺的碱性较弱,由I效应、空间效应和溶剂化 效应共同影响,结果:脂肪胺>氨>芳胺
H 2 N C2 O C 2 N 2 H O 5 ) 2 ( + H C C l H 普 鲁 卡 因
H 2 N C2 O C 2 N 2 H O 5 ) 2 . ( H C C 盐 酸 普 鲁 卡 因
2.酰化反应 伯胺和仲胺可与酰氯及酸酐反应,氮上氢
被酰基取代,叔胺氮原子上无氢原子,所以不 能发生酰化反应。
O
O
R C Cl + R'NH2 O R
R C Cl + NH R'
R C NHR' + HCl
伯胺、仲胺、叔胺(分别用1º胺、2º胺、3º胺来表 示),伯胺、仲胺、叔胺与伯醇、仲醇、叔醇不同。
CH3 CH CH3 NH2
伯胺
CH3 CH CH3 OH
仲醇
C H 3 N H C H 2 C H 3 (CH3)3N 仲 胺 叔 胺
季铵碱或季铵盐
- ( C H 3 ) 4 N + C l -
(二) 命名
C H 3
C H 3 N
C H 2 C H 3
N-甲基苯胺 N,N-二甲基苯胺 N-甲基-N-乙基苯胺
比较复杂的胺,则以烃等为母体,氨基作为取代基。
CH3 CH CH CH2 CH3 CH3 NH2
2-甲基-3-氨基戊烷
CH3 CH2 CH N(CH2CH3)2 CH3
2-二乙氨基丁烷
HOCH2CH2NH2 2-氨基乙醇
O
O
CH3 C NHCH3
C N (C H 3)2
N-甲基乙酰胺
O
N,N-二甲基苯甲酰胺
CH3 CH2 C NCH2CH3 CH3
N-甲基-N-乙基丙酰胺
二、酰胺的化学性质 1. 酸碱性 酰胺是近似中性的化合物,不能使石蕊试纸变色。
O
R C NH2
:
2.水解 在通常情况下酰胺水解较慢,但在酸或碱的
化合物称为酰胺,通式为:
O H (R')
R C N H (R")
酰胺氮上没有其他取代基的简单酰胺,命名时在 酰基名称后面加上“胺”字,称为“某酰胺”。例如:
O CH3 C NH2
CH3 O CH3 CH C NH2
O C NH2
乙酰胺
2-甲基丙酰胺
苯甲酰胺
酰胺氮上连有取代基时,将取代基的名称写 在酰胺名称之前,Байду номын сангаас加词首“N-”或“N,N-”, 以表示该取代基是直接与氮原子相连接的。例如:
O R
RCN R'
酰化对于药物的修饰具有重要的意义。药物分子中 引进酰基后,常可增加药物的脂溶性,有利于体内 的吸收,提高或延长其疗效,并可降低药物毒性。
O
乙酰化
HO
NH2
HO
NH C CH3
对羟基苯胺
扑热息痛
氨基易于被氧化,在有机合成及药物制备中常 用酰化反应来保护氨基。
3.与亚硝酸反应 (1) 伯胺与亚硝酸的反应
