第三章振动光谱作业
振动光谱

动,因此线性分子振动的自由度为3n-5。
基本振动类型---伸缩振动
伸缩振动:健合原子沿健轴方向的振动,健长改变,而健 角不改变。
(1)对称伸缩振动:两个原子相对于第三个原子作对称 的位移振动;
拉 曼
8102~ 1.3104~2.5 3.81014~ 1.6~101 可见光谱
4102 104
1015
光 谱
4102~ 2.5104~105 1015~1.5 101~102 紫外光谱
1102
1016
102~10-2 106~108
1016~1018 103~106 X 射线光谱
振动光谱基本原理---光的二重性
和0.05eV。
弹簧谐振子振动
●谐振子的振动势能有:
●体系的动能有: 根据虎克定律: ●谐振子的振动频度为:
式中,Ep是谐振子的振动势能, k为弹簧力常数,d为小球位移。
m为小球质量,v为小球运动速度。
双原子分子的谐振模型
如重心不变则有:
其中μ为折合质量
双原子分子的谐振模型
●设当两原子振动时的位移为R=r-re ,则分子振动势 能可表示为:
谐振子吸收或发射辐射地 必定依照△n=±1
的规律增减,这称为选律, 而这类吸收而产生的光 谱率称为基频。
倍频和差频
真实分子的振动不完全符合谐振子模型,在很 多情况下,可能出现△n>1;
●当△n=2,称为第一泛音带, ●当△n=3,称为第二泛音带, ●相反也可能出现ν1+ν2 和 ν1-ν2的红外吸收。
●用波长表示则: 光子量能量随波长的增加
振动光谱-1

在使频率降低,谱峰变宽,积分强度增加,它 是判断有无醇、酚和有机酸的重要依据。当无 氢键存在时,O—H或N—H成一尖锐的单峰出 现在频率较高的部分。
N—H伸缩振动在3500~3300cm-1区域,和 O—H谱带重叠。但峰形略比O—H尖锐。伯、 仲酰胺和伯、仲胺类在该区都有吸收谱带。
苯的衍生物在2000~1667cm-1区域出现面 外弯曲振动的倍频和组频谱带,它们的强 度较弱,但该区吸收峰的数目和形状与芳 核的取代类型有直接关系,在判别苯环取 代类型上非常有用。
4)部分单键振动及指纹区域 (1500~400cm-1 )
该区域的光谱比较复杂,一般较难找到它 们的归属。对鉴定有用的特征谱带主要有 C—H,O—H的变形振动以及C—O,C—N, C—X等的伸缩振动及芳环的C—H弯曲振动
环状结构也能使C=O伸缩振动的频率发生变化。羰基在七元环和六 元环上,其振动频率和直链分子的差不多。当羰基处在五元环或四元 环上时,其振动频率随环的原子个数减少而增加。这种现象可以在环 状酮,内酯以及内酰胺等化合物中看到。
3 氢键效应
氢键(分子内氢键;分子间氢键):对峰位,峰强产 生极明显影响,使伸缩振动频率向低波数方向移动,谱 带变宽;弯曲振动向高频移动,谱带变窄。
例1:
R-COR C=0 1715cm-1 ; R-COCl C=0 1800cm-1 ; F-COF C=0 1920cm-1 ;
?
R-COH C=0 1730cm -1 ; R-COF C=0 1920cm-1 ; R-CONH2 C=0 1928cm-1 ;
例2:
b.共轭效应
例1:
例2:
06-振动光谱

13
双原子分子振动可以近似地看作为简谐振动:
➢ 把两个质量为m1和m2的原子看作为两个刚性小球;
➢ 连接两原子的化学键设想为无质量的弹簧,原子间
的化学键长度看做是弹簧长度r ,键力常数看成为 弹簧力常数k 。
双原子分子的振动形式仅有一种:伸缩振动,即振动 时两原子之间距离(键长)发生改变。
14
1
振动光谱
振动光谱:vibrational spectrum 分子中同一电子能态中不同振动能级之间跃迁产 生的光谱。
振动光谱:包括
红外吸收光谱,IR
Infrared Absorption Spectrum
拉曼散射光谱
Raman Scattering Spectrum
1
红外吸收过程:当分子中某个基团的振动频率和红外 光的频率一致时,样品分子就吸收该频率的红外光能 量,从原来的基态跃迁到能量较高的激发态。
➢ 中红外光谱仪最为成熟、简单,而且目前已积累了该区大量 的数据资料,它是应用极为广泛的光谱区。
➢ 通常,中红外光谱法又简称为红外光谱法。
9
红外光与红外光谱
分子或原子基团吸收光能量具有量子化特征 分子运动状态由基态E0 跃迁到激发态E1、E2时, 它们的能量差:
能级跃迁示意图
△E1=hv1=E1-E0 △E2=hv2=E2-E0
8
名 称 λ/μm /cm-1
近红外区 0.75-2.5 13333-4000 中红外区 2.5-25 4000-400 远红外区 25-1000 400-10
主要能级跃迁类型
O-H、N-H、C-H键的倍频吸收 分子振动
分子转动、晶格振动
中红外区:最为有用,分子的振动能级跃迁
➢ 绝大多数有机化合物和无机离子的基频吸收带出现在该光区, 适于进行红外光谱的定性和定量分析。
振动光谱课件

振动光谱
五、吸收谱带的强度
• 红外吸收谱带的强度决定于偶极矩的变化大小。 • 振动时偶极矩变化越大,吸收强度愈大。一般极性比较强的分子
或基团吸收强度都比较大。 • 例如C=C,C=N,C-C,C-H等化学键的振动吸收谱带都比较弱
; • 而C=O,Si-O,C-Cl,C-F等的振动,其吸收谱带就很强。
振动光谱
第二节 红外光和红外光谱
• 1800年 英国天文学家Hershl发现红外光(又称红外 辐射或红外线)。
• 物质因受红外光的作用,引起分子或原子基团的振 动(热振动),从而产生对红外光的吸收。利用物 质对不同波长红外光的吸收程度进行研究物质分子 的组成和结构的方法,称为红外吸收光谱法,常以 IR表示。
• 2、振动必须引起偶极矩变化,才是IR活性的。即 正负电荷中心的间距发生变化。——IR活性振动。
• 3、如果振动引起极化率变化,才是Raman活性 的。在电磁波的作用下,正负电荷出现诱导偶极矩 ,有些振动是红外活性的,但非拉曼活性,有些相 反。有些是双活性的,有些是双非活性的。
振动光谱
•四、晶格振动
二、分子光谱与原子光谱
1、原子运动与原子光谱
原子的运动主要是电子在原子核周围运动,因此原子运动的 能量叫电子能,是电子在核周围运动、电子与电子之间以及电 子与核之间的作用产生的。原子光谱是原子中电子能级跃迁产 生的光谱。包括原子吸收与发射光谱。
振动光谱
2、分子运动与分子光谱
与原子运动相比,分子运动较复杂,主要有分子的整个平动、 分子绕其质心的转动、分子中原子核的振动及分子中电子的运 动。各状态的能量为平动能、转动能、振动能和电子能。分子 的总能量由以下几种能量组成:
结构化学 第三章习题(周公度)

解:H-O-O-H为非线性分子n=4简正振动数目为3n-6= 6
H-C≡C-H为线性分子n=4,简正振动数目为3n-5 = 7
26、画出SO2的简正振动方式,已知与3个基频对应的谱带波数分别为1361,1151,519cm-1,指出每种频率所对应的振动,说明是否为红外活性或拉曼活性。
解:SO2分子为V形结构,n=3,简正振动方式有3n-6= 3。
2、一个成键或反键电子的电离,核间距发生变化,垂直跃迁的几率最大,振动序列较长。
3、内层电子的电离,谱带常呈现带状谱带。
30由紫外光电子能谱实验知,NO分子的第一电离能为9.26eV,比CO的I1(14.01eV)小很多,试从分子的电子组态解释其原因
解:根据NO分子4(5σ)2(2π)1;
键级为2.5;而CF+比CF少一个(2π)电子,键级为3。
12、下列AB型分子:N2.NO,O2,C2,F2,CN,CO,XeF中,哪几个是得电子变为AB-后比原来中性分子键能大?哪几个是失电子变成AB+后比原来中性分子键能大?
振动光谱

振动光谱\基本原理\分子振动模型
/////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////
4.1.1 光与分子的相互作用 光是一种波,可以使用波的基本公式:
振动光谱\基本原理\光与分子的相互作用
/////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////
振动吸收的条件
1 振动频率与红外光光谱段的某频率相等; 2 必须有偶极距的变化。
我们把产生红外辐射吸收的振动称为红外活性振动, 把不发生吸收红外辐射的振动称为非红外活性振动。
链接:偶极矩μ=r×q。偶极距越大,键的极性越大。
振动光谱\红外光谱\红外光
/////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////
红外吸收光谱法31概述分子中基团的振动和转动能级跃迁
第三章红外吸收光谱法§ 3.1概述分子中基团的振动和转动能级跃迁产生:振-转光谱一、红外光区的划分红外光谱在可见光区和微波光区之间,波长范围约为0.75 ~ 1000 m,根据仪器技术和应用不同,习惯上又将红外光区分为三个区:近红外光区(0.75 ~ 2.5 m ),中红外光区(2.5~ 25 m ),远红外光区(25 ~ 1000 呵)。
近红外光区的吸收带(0.75 ~ 2.5皿)主要是由低能电子跃迁、含氢原子团(如O-H、N-H、C-H )伸缩振动的倍频吸收产生。
该区的光谱可用来研究稀土和其它过渡金属离子的化合物,并适用于水、醇、某些高分子化合物以及含氢原子团化合物的定量分析中红外光区吸收带(2.5 ~ 25 m )是绝大多数有机化合物和无机离子的基频吸收带(由基态振动能级(..=0)跃迁至第一振动激发态(..=1 )时,所产生的吸收峰称为基频峰)。
由于基频振动是红外光谱中吸收最强的振动,所以该区最适于进行红外光谱的定性和定量分析。
同时,由于中红外光谱仪最为成熟、简单,而且目前已积累了该区大量的数据资料,因此它是应用极为广泛的光谱区。
通常,中红外光谱法又简称为红外光谱法。
远红外光区吸收带(25 ~ 1000 m )是由气体分子中的纯转动跃迁、振动-转动跃迁、液体和固体中重原子的伸缩振动、某些变角振动、骨架振动以及晶体中的晶格振动所引起的。
由于低频骨架振动能灵敏地反映出结构变化,所以对异构体的研究特别方便。
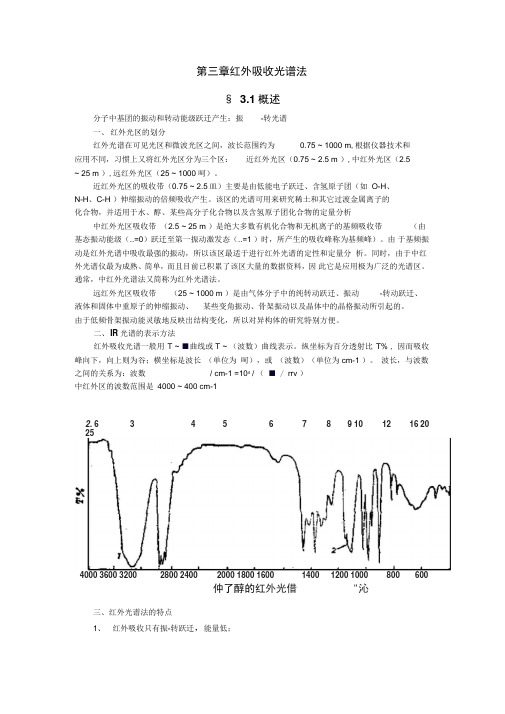
二、IR光谱的表示方法红外吸收光谱一般用T ~ ■曲线或T ~ (波数)曲线表示。
纵坐标为百分透射比T% , 因而吸收峰向下,向上则为谷;横坐标是波长(单位为呵),或(波数)(单位为cm-1 )。
波长,与波数之间的关系为:波数/ cm-1 =104/ (■ / rrv )中红外区的波数范围是4000 ~ 400 cm-12. 6 3 4 5 6 7 8 9 10 12 16 20254000 3600 3200 2800 2400 2000 1800 1600 1400 1200 1000 800 600仲了醇的红外光借"沁三、红外光谱法的特点1、红外吸收只有振-转跃迁,能量低;2、应用范围广,除单原子分子及单核分子外,几乎所有的有机物均有红外吸收;3、分子结构更为精细的表征:通过波谱的波数位置、波峰数目及强度确定分子基团和分子结构;4、气体、液体、固体样品都可测定;5、具有用量少;分析速度快;不破坏样品。
《振动光谱》课件

适用
核磁共振谱
原理:利用核磁共 振现象,测量样品 中的核磁共振信号
应用:广泛应用于 有机化合物、生物 大分子、金属离子 等的结构分析和定 量分析
特点:具有高灵敏 度、高分辨率、无 破坏性等优点
技术:包括核磁共 振波谱、核磁共振 成像等
紫外可见光谱
应用领域的拓展与深化
生物医学领域:用于蛋白质、核酸等生物 大分子的结构分析和功能研究
材料科学领域:用于新材料的研发和性能 优化
环境科学领域:用于污染物监测和治理
化学领域:用于化学反应机理的研究和反 应动力学的模拟
物理领域:用于量子力学和凝聚态物理的 研究
航空航天领域:用于航天器和航天材料的 性能测试和优化
振动光谱的原理
振动光谱是研究分子振动能级的一 种光谱技术
振动光谱可以分为红外光谱和拉曼 光谱两种
添加标题
添加标题
添加标题
添加标题
振动光谱的原理是利用分子振动能 级之间的跃迁来产生光谱信号
红外光谱和拉曼光谱的原理分别是 利用分子振动能级之间的跃迁和分 子振动能级之间的拉曼散射来产生 光谱信号
振动光谱的应用
THANK YOU
汇报人:
提高分辨率:通过 改进仪器和算法, 提高光谱分辨率, 实现更精确的测量
提高灵敏度:通过 改进仪器和算法, 提高光谱灵敏度, 实现更微弱信号的 检测
提高速度:通过改 进仪器和算法,提 高光谱测量速度, 实现更快速的测量
提高自动化程度: 通过改进仪器和算 法,提高光谱测量 的自动化程度,实 现无人值守的测量
紫外可见光谱是电磁波谱的一部分,波长范围为200-800nm 紫外可见光谱包括紫外光谱和可见光谱,其中紫外光谱的波长范围为200400nm,可见光谱的波长范围为400-800nm 紫外可见光谱的应用广泛,包括化学分析、生物医学、环境监测等领域
2013.9.23第三章 红外-答案

第三章红外光谱一、名词解释基频峰、倍频峰、费米共振、特征频率区、指纹区基频峰:当分子吸收一定频率的红外线后,振动能级从基态(V)跃迁到第一激发态(V1)时所产生的吸收峰,称为基频峰.倍频峰:如果振动能级从从基态(V0)跃迁到第二激发态(V2)、第三激发态(V3)……所产生的吸收峰称为倍频峰。
费米共振:当一振动的倍频(或组频)与另一振动的基频吸收峰接近时,由于发生相互作用而产生很强的吸收峰或发生裂分,这种倍频(或组频)与基频峰之间的振动偶合称费米共振.特征频率区:特征谱带区有机化合物的分子中一些主要官能团的特征吸收多发生在红外区域的 4000~1500cm-2 .该区域吸收峰比较稀疏, 容易辨认, 故通常把该区域叫特征谱带区 .红外光谱指纹区:红外吸收光谱上 1500~40Ocm—1的低频区, 通常称为,在核指纹区。
该区域中出现的谱带主要是 C—X (X=C,N s O)单键的伸缩振动以及各种弯曲振动对和确认有机化合物时用处很大。
二、填空1.红外光谱的产生是由于-—--—--——---—-————。
化学键的振动与转动跃迁.2。
红外光谱产生的条件是--——-——--——-———-—----—-———-—-、--—-—--——--———--—--——-----—--—--—————-———-——--—--—。
红外光谱产生的条件是辐射的能量满足跃迁所需能量,辐射引起偶极矩的变化。
3.红外光谱中影响基团频率位移的因素有外部因素和内部因素,内部因素主要有、、等.此外,振动耦合、费米共振等也会使振动频率位移.外部因素(样品的状态等)、电子效应(诱导效应、共轭效应和偶极场效应)、空间效应、氢键4.在红外光谱中,将基团在振动过程中有偶极矩变化的称为,相反则称为 .红外活性,非红外活性.5.基团-OH和—NH,—C≡N和-C≡CH,-C=C—和-C=N-的伸缩振动频率范围分别是cm—1, cm-1, cm-1。
4000—2500(3000)、 2500—2000 、2000—15006。
振动光谱和能谱仪习题 完整含答案版()

振动光谱和能谱仪习题(2016)一. 选择题1.红外光谱是( )A :分子光谱B :原子光谱C :吸光光谱D :电子光谱E :振动光谱2.当用红外光激发分子振动能级跃迁时,化学键越强,则( ) A :吸收光子的能量越大 B :吸收光子的波长越长 C :吸收光子的频率越大 D :吸收光子的数目越多 E :吸收光子的波数越大3.在下面各种振动模式中,不产生红外吸收的是( ) A :乙炔分子中对称伸缩振动 B :乙醚分子中不对称伸缩振动 C :CO 2分子中对称伸缩振动 D :H 2O 分子中对称伸缩振动E :HCl 分子中H -Cl 键伸缩振动4.下面五种气体,不吸收红外光的是( ) A:O H 2 B:2CO C:HCl D:2N5 分子不具有红外活性的,必须是( ) A:分子的偶极矩为零 B:分子没有振动 C:非极性分子D:分子振动时没有偶极矩变化 E:双原子分子6.预测以下各个键的振动频率所落的区域,正确的是( )A:O-H伸缩振动数在4000~25001-cm B:C-O 伸缩振动波数在2500~15001-cmC :N-H 弯曲振动波数在4000~25001-cmD:C -N 伸缩振动波数在1500~10001-cm E:C ≡N 伸缩振动在1500~10001-cm7.下面给出五个化学键的力常数,如按简单双原子分子计算,则在红外光谱中波数最大者是( )A:乙烷中C-H 键,=k 510⨯达因1-⋅cmB : 乙炔中C-H 键, =k 510⨯达因1-⋅cm C : 乙烷中C-C 键, =k 510⨯达因1-⋅cmD : CH 3C ≡N 中C ≡N 键, =k 510⨯达因1-⋅cmE:蚁醛中C=O 键, =k 510⨯达因1-⋅cm8.基化合物中,当C=O 的一端接上电负性基团则( ) A :羰基的双键性增强 B:羰基的双键性减小 C:羰基的共价键成分增加 D:羰基的极性键成分减小 E:使羰基的振动频率增大9.以下五个化合物,羰基伸缩振动的红外吸收波数最大者是( )A: B: C:D: E :10.共轭效应使双键性质按下面哪一种形式改变( ) A:使双键电子密度下降 B:双键略有伸长C:使双键的力常数变小 D.使振动频率减小 E:使吸收光电子的波数增加11.下五个化合物羰基伸缩振动的红外吸收波数最小的是( )A: B: C:D: E :12.下面四个化合物中的C=C 伸缩振动频率最小的是( ) A: B:C:D :13.两 个化合物(1) ,(2) 如用红外光谱鉴别,主要依据的谱带是( )A(1)式在~33001-cm 有吸收而(2)式没有B:(1)式和(2)式在~33001-cm 都有吸收,后者为双峰C :(1)式在~22001-cm 有吸收D:(1)式和(2)式在~22001-cm 都有吸收E: (2)式在~16801-cm 有吸收14.合物在红外光谱的3040~30101-cm 及1680~16201-cm 区域有吸收,则下面五个化合物最可能的是( )A :B :C :D :E :15. 一种能作为色散型红外光谱仪色散元件的材料为( )A 玻璃B 石英C 卤化物晶体D 有机玻璃16.预测H2S分子的基频峰数为()(A)4 (B)3 (C)2 (D)117.CH3—CH3的哪种振动形式是非红外活性的()(A)υC-C (B)υC-H (C)δasCH(D)δsCH18.化合物中只有一个羰基,却在1773cm-1和1736 cm-1处出现两个吸收峰,这是因为()(A)诱导效应(B)共轭效应(C)费米共振(D)空间位阻19.Cl2分子在红外光谱图上基频吸收峰的数目()A 0B 1C 2D 320. 红外光谱法, 试样状态可以()A 气体状态B固体, 液体状态C 固体状态 D气体, 液体, 固体状态都可以21. 红外吸收光谱的产生是由()A 分子外层电子、振动、转动能级的跃迁B 原子外层电子、振动、转动能级的跃迁C分子振动-转动能级的跃迁D 分子外层电子的能级跃迁22.色散型红外分光光度计检测器多()A 电子倍增器B 光电倍增管C高真空热电偶 D 无线电线圈23.一个含氧化合物的红外光谱图在3600~3200cm-1有吸收峰, 下列化合物最可能的()A CH3-CHOB CH3-CO-CH3C CH3-CHOH-CH3D CH3-O-CH2-CH324.某化合物在紫外光区204nm处有一弱吸收,在红外光谱中有如下吸收峰:3300-2500 cm-1(宽峰),1710 cm-1,则该化合物可能是()A、醛B、酮C、羧酸D、烯烃25.在红外光谱分析中,用KBr制作为试样池,这是因为:( )A KBr 晶体在 4000~400cm-1范围内不会散射红外光B KBr 在 4000~400 cm-1范围内有良好的红外光吸收特性C KBr 在 4000~400 cm-1范围内无红外光吸收D 在 4000~400 cm-1范围内,KBr 对红外无反射26.下面给出某物质的部分红外光谱(如图),已知结构Ⅰ、Ⅱ或Ⅲ,试问哪一结构与光谱是一致的,为什么结构Ⅱ。
第三章振动光谱作业

第三章振动光谱作业第三章振动光谱作业-标准化文件发布号:(9456-EUATWK-MWUB-WUNN-INNUL-DDQTY-KII第二章振动光谱作业1.红外光区的划分?红外光按波长不同划分为三个区域:近红外区域(1-2.5微米)/中红外区域(2.5-25微米)/远红外区域(25-1000微米)2.振动光谱有哪两种类型多原子分子的价键或基团的振动有哪些类型同一种基团哪种振动的频率较高哪种振动的频率较低振动光谱有红外吸收光谱和激光拉曼光谱两种类型。
价键或基团的振动有伸缩振动和弯曲振动。
其中伸缩振动分为对称伸缩振动和非对称伸缩振动;弯曲振动则分为面内弯曲振动(剪式振动、面内摇摆振动)和面外弯曲振动(扭曲振动、面外摇摆振动)。
伸缩振动频率较高,弯曲振动频率较低。
(键长的改变比键角的改变需要更大的能量)非对称伸缩振动的频率高于对称伸缩振动。
3. 说明红外光谱产生的机理与条件?产生机理:当用红外光波长范围的光源照射物质时,物质因受光的作用,引起分子或原子基团的振动,若振动频率恰与红外光波段的某一频率相等时就引起共振吸收,使光的透射强度减弱,使通过试样的红外光在一些波长范围内变弱,在另一些范围内则较强,用光波波长(或波数)对光的透过率作图,便可得到红外光谱产生条件:1)辐射应具有能满足物质产生振动-转动跃迁所需的能量,即振动的频率与红外光谱谱段的某频率相等。
2)辐射与物质间有相互偶合作用,即振动中要有偶极矩变化4.红外光谱图的表示法?红外光谱图的表示法:横坐标:波数cm-1或者波长μm纵坐标:透过率%或者吸光度A5. 红外光谱图的四大特征(定性参数)是什么?如何进行基团的定性分析如何进行物相的定性分析四大特征:谱带(或者说是吸收峰)的数目、位置、形状和强度。
进行基团的定性分析时,首先,观察特征频率区,根据基团的伸缩振动来判断官能团。
进行物相的定性分析:进行物相的定性分析:对于已知物:a、,观察特征频率区,判断官能团,以确定所属化合物的类型b、观察指纹频率区,进一步确定基团的结合方式c、对照标准谱图进行比对,若被测物质的与已知物的谱图峰位置和相对强度完全一致,则可确认为一种物质。
结构化学习题答案(3)

《结构化学》第三章习题3001 H 2+的H ˆ= 21∇2- a r 1 - b r 1 +R1, 此种形式已采用了下列哪几种方法: ------------------------------ ( )(A) 波恩-奥本海默近似 (B) 单电子近似(C) 原子单位制 (D) 中心力场近似3002 分析 H 2+的交换积分(β积分) H ab 为负值的根据。
3003 证明波函数 ()()()()b a b a ψψψψψψS S s 1s 121u s 1s 121g 221221--=++=是相互正交的。
3004 通过变分法计算得到的微观体系的能量总是:----------------- ( )(A) 等于真实基态能量(B) 大于真实基态能量(C) 不小于真实基态能量(D) 小于真实基态能量3006 什么叫分子轨道?按量子力学基本原理做了哪些近似以后才有分子轨道的概念?这些近似的根据是什么?3007 描述分子中 _______________ 空间运动状态的波函数称为分子轨道。
3008 对于"分子轨道"的定义,下列叙述中正确的是:----------------- ( )(A) 分子中电子在空间运动的波函数(B) 分子中单个电子空间运动的波函数(C) 分子中单电子完全波函数(包括空间运动和自旋运动)(D) 原子轨道线性组合成的新轨道3009 试述由原子轨道有效地形成分子轨道的条件。
3010 在 LCAO-MO 中,所谓对称性匹配就是指两个原子轨道的位相相同。
这种说法是否正确?3011 在LCAO-MO 方法中,各原子轨道对分子轨道的贡献可由哪个决定:----------------- ( )(A) 组合系数 c ij (B) (c ij )2(C) (c ij )1/2 (D) (c ij )-1/23012 在极性分子 AB 中的一个分子轨道上运动的电子,在 A 原子的φA 原子轨道上出现的概率为80%, B 原子的φB 原子轨道上出现的概率为20%, 写出该分子轨道波函数 。
材料物理专业《材料分析测试方法A》作业

材料物理专业《材料分析测试⽅法A》作业材料物理专业《材料分析测试⽅法A 》作业第⼀章电磁辐射与材料结构⼀、教材习题1-1 计算下列电磁辐射的有关参数:(1)波数为3030cm -1的芳烃红外吸收峰的波长(µm );(2)5m 波长射频辐射的频率(MHz );(3)588.995nm 钠线相应的光⼦能量(eV )。
1-3 某原⼦的⼀个光谱项为45F J ,试⽤能级⽰意图表⽰其光谱⽀项与塞曼能级。
1-5 下列原⼦核中,哪些核没有⾃旋⾓动量?12C 6、19F 9、31P 15、16O 8、1H 1、14N 7。
1-8 分别在简单⽴⽅晶胞和⾯⼼⽴⽅晶胞中标明(001)、(002)和(003)⾯,并据此回答:⼲涉指数表⽰的晶⾯上是否⼀定有原⼦分布?为什么?1-9 已知某点阵∣a ∣=3?,∣b ∣=2?,γ = 60?,c ∥a ×b ,试⽤图解法求r *110与r *210。
1-10 下列哪些晶⾯属于]111[晶带?)331(),011(),101(),211(),231(),132(),111(。
⼆、补充习题1、试求加速电压为1、10、100kV 时,电⼦的波长各是多少?考虑相对论修正后⼜各是多少?第⼆章电磁辐射与材料的相互作⽤⼀、教材习题2-2 下列各光⼦能量(eV )各在何种电磁波谱域内?各与何种跃迁所需能量相适应?1.2×106~1.2×102、6.2~1.7、0.5~0.02、2×10-2~4×10-7。
2-3 下列哪种跃迁不能产⽣?31S 0—31P 1、31S 0—31D 2、33P 2—33D 3、43S 1—43P 1。
2-5 分⼦能级跃迁有哪些类型?紫外、可见光谱与红外光谱相⽐,各有何特点? 2-6 以Mg K α(λ=9.89?)辐射为激发源,由谱仪(功函数4eV )测得某元素(固体样品)X 射线光电⼦动能为981.5eV ,求此元素的电⼦结合能。
第三章 红外吸收光谱分析-3

外部因素
外部因素主要指测定时物质的状态以及溶剂效应等因
素。 同一物质的不同状态,由于分子间相互作用力不同, 所得到光谱往往不同。 分子在气态时,其相互作用力很弱,此时可以观察到 伴随振动光谱的转动精细结构。 液态和固态分子间作用力较强,在有极性基团存在时, 可能发生分子间的缔合或形成氢键,导致特征吸收带 频率、强度和形状有较大的改变。 例如,丙酮在气态时的C-H为1742 cm-1 ,而在液态时 为1718 cm-1 。
C=O :→降低
注意:有时在化合物中,I效应与M效应同时存在,如果二者方 向不一致,这时应考虑哪个效应起主导作用。例如,饱和酯的 C=O为1735cm-1,比酮(1715cm-1)高,就是由于I效应大于M效应, 二者的净效应使得电子云密度由氧移向双键中间,使键力常数增 加的缘故。
当含有孤对电子的原子(O、S、N等)与具有多重键
游离羧酸的co键频率出现在1760cm1左右在固体或液体中由于羧酸形成二聚体co键频率出现在1700cm1当两个振动频率相同或相近的基团相邻具有一公共原子时由于一个键的振动通过公共原子使另一个键的长度发生改变产生一个微扰从而形成了强烈的振动相互作用
第三章 红外吸收光谱分析
3.3 基团频率和特征吸收峰
利用指纹区中苯环的C-H面外变形振动吸收峰 和2000~ 1667cm-1区域苯的倍频或组合频吸收 峰,可以共同配合确定苯环的取代类型。下图为不 同的苯环取代类型在2000~ 1667cm-1和 900~600cm-1区域的光谱。
指纹区
变形振动- 亚甲基
指纹区
变形振动 - 甲基
对称δ s(CH3)1380㎝-1
共轭效应- C效应
共轭效应使共轭体系中的电子云密度平 均化。 双键略有伸长,单键略有缩短,即双键 电子云密度降低,化学键力常数变小, 伸缩振动频率向低频方向移动。 共轭效应常引起C=O双键的双键性降低, 伸缩振动频率向低波数位移。
矿产

矿产资源开发利用方案编写内容要求及审查大纲
矿产资源开发利用方案编写内容要求及《矿产资源开发利用方案》审查大纲一、概述
㈠矿区位置、隶属关系和企业性质。
如为改扩建矿山, 应说明矿山现状、
特点及存在的主要问题。
㈡编制依据
(1简述项目前期工作进展情况及与有关方面对项目的意向性协议情况。
(2 列出开发利用方案编制所依据的主要基础性资料的名称。
如经储量管理部门认定的矿区地质勘探报告、选矿试验报告、加工利用试验报告、工程地质初评资料、矿区水文资料和供水资料等。
对改、扩建矿山应有生产实际资料, 如矿山总平面现状图、矿床开拓系统图、采场现状图和主要采选设备清单等。
二、矿产品需求现状和预测
㈠该矿产在国内需求情况和市场供应情况
1、矿产品现状及加工利用趋向。
2、国内近、远期的需求量及主要销向预测。
㈡产品价格分析
1、国内矿产品价格现状。
2、矿产品价格稳定性及变化趋势。
三、矿产资源概况
㈠矿区总体概况
1、矿区总体规划情况。
2、矿区矿产资源概况。
3、该设计与矿区总体开发的关系。
㈡该设计项目的资源概况
1、矿床地质及构造特征。
2、矿床开采技术条件及水文地质条件。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
矿产资源开发利用方案编写内容要求及审查大纲
矿产资源开发利用方案编写内容要求及《矿产资源开发利用方案》审查大纲一、概述
㈠矿区位置、隶属关系和企业性质。
如为改扩建矿山, 应说明矿山现状、
特点及存在的主要问题。
㈡编制依据
(1简述项目前期工作进展情况及与有关方面对项目的意向性协议情况。
(2 列出开发利用方案编制所依据的主要基础性资料的名称。
如经储量管理部门认定的矿区地质勘探报告、选矿试验报告、加工利用试验报告、工程地质初评资料、矿区水文资料和供水资料等。
对改、扩建矿山应有生产实际资料, 如矿山总平面现状图、矿床开拓系统图、采场现状图和主要采选设备清单等。
二、矿产品需求现状和预测
㈠该矿产在国内需求情况和市场供应情况
1、矿产品现状及加工利用趋向。
2、国内近、远期的需求量及主要销向预测。
㈡产品价格分析
1、国内矿产品价格现状。
2、矿产品价格稳定性及变化趋势。
三、矿产资源概况
㈠矿区总体概况
1、矿区总体规划情况。
2、矿区矿产资源概况。
3、该设计与矿区总体开发的关系。
㈡该设计项目的资源概况
1、矿床地质及构造特征。
2、矿床开采技术条件及水文地质条件。
