山中伸弥发明IPS细胞的介绍及启示
细胞重编程技术的应用与研究进展

细胞重编程技术的应用与研究进展细胞重编程技术是由日本学者山中伸弥和英国学者约翰·戴维·戈登于2006年发现,随即因其巨大的科学发现价值而引起全球科学界广泛关注。
这一技术可以将已经成熟的细胞转化为干细胞,即诱导多能干细胞(induced pluripotent stem cells,iPSCs),从而可以制备出特定器官的细胞,为人们未来的临床治疗带来无限可能。
首先,细胞重编程技术的应用:(1)医学领域:其最大的应用前景是在医学领域。
因为干细胞能够成为体内任何种类的细胞,包括肌肉、神经、心脏等器官的细胞,因此,干细胞成为了治疗某些疾病的理想来源。
干细胞治疗可以治疗癌症、胰岛素依赖性糖尿病、阿尔茨海默病、帕金森病、多发性硬化症、肾病等多种疾病,因为这些疾病都是由特定的细胞类型受损所致。
(2)研究领域:除了医学领域,细胞重编程技术还有广泛的应用前景,尤其是在放射生物学、毒理学、遗传学等方面的研究。
干细胞的推出为科学研究提供了无限的可能性。
(3)精准医疗领域:细胞重编程技术为精准医疗领域提供了巨大的帮助。
人类基因组计划已经解密并精细分析了人类的基因组序列,基因分而治之,就成了未来精准医疗的必经之路。
其次,细胞重编程技术的研究进展:(1)干细胞的特点:干细胞是指五种能够分化出多种细胞类型的细胞。
分别是:诱导干细胞、多能干细胞、祖细胞、成体干细胞以及胚胎干细胞。
而iPSCs即由已经成熟的细胞诱导而来的多能干细胞,与胚胎干细胞很相似。
(2)iPSCs的制备:iPSCs的制备主要包括方法集成、质量控制和功能评价三个步骤,其中方法集成步骤是关键所在。
该步骤包括:iPSCs转化两阶段、各种化学试剂和基因的低毒转化。
(3)iPSCs的遗传与表观改变:iPSCs虽然被认为是多能干细胞,但与胚胎干细胞相比,其有一定的遗传差异,包括单荷兹综合征、Sle和颜面发育不良等病例。
此外,iPSCs与胚胎干细胞相比,也存在不同的表观遗传学特征。
山中申弥的iPS研究历程

从整型医生到诺贝尔奖-山中伸弥的研究历程引言山中伸弥(Shinya Yamanaka)获得诺奖已经有几天了,虽然两年前在听完他的讲座后我兴致很高地写了两篇博客,这些天我却没有多少动力再写一篇完整的文章来介绍他的工作。
我一直对中国现在还盛行的规划性科研,应用导向型科研耿耿于怀。
这些所谓的重大项目在立项的当初对目标/前景写得宏大无比,之后却通常草草收场。
如果那些重大项目真的能实现立项当初的用意,那诺贝尔奖早就在中国遍地开花了。
广大科研人员都觉得这种运行模式是一个笑话,饶毅、施一公等大牛也重炮轰击,但是分钱游戏还在进行着。
而公众,包括相当一部分科研人员也并不了解科研的自身规律,总是一再地问做基础研究有什么用。
Shinya Yamanaka的成功是典型的小实验室自由探索的成功。
他的成功再一次提示,有相当多的科学突破是不可预测的。
如果中国有大批优质的小实验室得到稳定的资助,那么类似的科学突破就会随机但是必然地产生。
从这种意义上讲,展示Shinya Yamanaka在研究过程中的这种随机性和必然性,向公众科普科研活动是如何进行的,是值得我花一点时间的。
解析Shinya Yamanaka发现诱导干细胞(iPS)的来龙去脉比较简单,就是跟踪他顺次研究的基因: ApoBEC1-Nat1-Fbx15,最后发现iPS。
有趣的是他在顺次研究这些基因的时候转了两次方向:ApoB是血脂蛋白,研究它的剪切酶(或者叫编辑酶)ApoBEC1是为了调节血脂,但是却发现ApoBEC1过表达的小鼠得了肝癌;为了研究致癌机理,他找到ApoBEC1的下游蛋白Nat1,Nat1的敲除导致小鼠在胚胎期死亡,以及胚胎干细胞在体外无法分化;于是他又开始研究起胚胎干细胞,找到许多胚胎干细胞特异表达的基因,其中之一是Fbx15,最后用Fbx15敲除鼠建立assay(筛选方法/系统),幸运地筛选出了iPS。
整形外科到博士阶段Shinya Yamanka念高中时迷上柔道,因为受伤经常上医院,他在爸爸的建议下随后考入国立神户大学医学部,准备以后做一名整形外科医生。
诱导性多能干细(IPS细胞)

诱导性多能干细iPS细胞即诱导性多能干细胞。
诱导多能干细胞induced pluripotent stem cells iPS:2006年日本京都大学Shinya Yamanaka在世界著名学术杂志《细胞》上率先报道了诱导多能干细胞的研究。
他们把Oct3/4,Sox2、c-Myc和Klf4这四种转录因子基因克隆入病毒载体,然后引入小鼠成纤维细胞,发现可诱导其发生转化,产生的iPS细胞在形态、基因和蛋白表达、表观遗传修饰状态、细胞倍增能力、类胚体和畸形瘤生成能力、分化能力等方面都与胚胎干细胞相似。
1基本概念诱导多能干细胞(induced pluripotent stem cells, iPS cells)最初是日本人山中伸弥(Shinya Yamanaka)于2006年利用病毒载体将四个转录因子(Oct4, Sox2, Klf4 和c-Myc)的组合转入分化的体细胞中,使其重编程而得到的类似胚胎干细胞的一种细胞类型。
[1]随后世界各地不同科学家陆续发现其它方法同样也可以制造这种细胞。
2012年10月8日,John B. Gurdon 与Shinya Yamanaka 因此获得诺贝尔生理学和医学奖。
2研究历程iPS细胞2006年日本京都大学山中伸弥(Shinya Yamanaka)领导的实验室在世界著名学术杂志《细胞》上率先报道了iPS的研究。
他们把Oct3/4、Sox2、c-Myc和Klf4这四种转录因子引入小鼠胚胎或皮肤纤维母细胞,发现可诱导其发生转化,产生的iPS细胞在形态、基因和蛋白表达、表观遗传修饰状态、细胞倍增能力、类胚体和畸形瘤生成能力、分化能力等都与胚胎干细胞极为相似。
2007年11月,Thompson实验室和山中伸弥实验室几乎同时报道,利用ips技术同样可以诱导人皮肤纤维母细胞成为几乎与胚胎干细胞完全一样的多能干细胞。
所不同的是日本实验室依然采用了用逆转录病毒引入Oct3/4、Sox2、c-Myc和Klf4四种因子组合,而Thompson实验室采用了以慢病毒载体引入Oct4、Sox2加Nanog和LIN28这种因子组合。
细胞重编程技术的发展及其应用

细胞重编程技术的发展及其应用随着现代医学技术的不断进步,细胞重编程技术已成为当前热门话题之一。
细胞重编程技术是一种将成体细胞重新编程为相对干细胞(induced pluripotent stem cells, iPS细胞)的技术,近年来引起了人们的极大关注。
细胞重编程技术的背景细胞重编程技术是由两位日本科学家山中伸弥和吉野彰于2006年发明的。
在这项技术的帮助下,成体细胞(目前已经成功转化的种类包括亲子生殖细胞、神经细胞、肝细胞、心脏细胞等等)可以通过某些物质的作用来“发育”成为未分化的多潜能细胞状态,即iPS细胞。
这种技术的出现,从某种角度上讲,就是打破了细胞发育的“规则”,也为细胞生物学和医学带来了前所未有的革命性变化。
细胞重编程技术的原理细胞重编程技术的原理是越来越清晰和准确的,主要基于细胞内部的生物化学及遗传学,利用某些特殊的因子让成体细胞产生多能性,这一过程中包括转录因子和表观遗传调控因素的介入,从而实现细胞的“重编程”。
转录因子是一类具有转录激活功能的调节性蛋白质,这些蛋白质在基因表达上有非常重要的作用。
iPS细胞的形成过程中,通过在成体细胞中外源表达一些特定的转录因子,再通过补充一些特定的化学物质,就能使细胞发生某些“幻变”,进而促进其发育成为未分化状态的细胞。
表观遗传调控因素在iPS细胞培养和生长中也起着重要作用。
这些因素控制着基因表达和基因功能的重要性,通过在细胞质内分化分子发挥作用,帮助细胞完成干性转变,促进细胞的再生和“重编程”。
细胞重编程技术的应用细胞重编程技术的应用体现出了其广泛的应用前景和巨大的潜力,既包括基础研究,也逐渐透过临床应用研究,以解决人类健康问题。
基础研究领域应用:1. 疾病机制研究:iPS细胞技术可以使研究人员得到大量病变修建,从而对疾病发生机制进行深入研究。
例如,人类iPS细胞可以用于遗传学和肿瘤学等领域的基础研究。
2. 药物筛选:iPS细胞可以用于药物筛选,这有助于大量化、多样性、来自不同种族和疾病的样本进行大规模筛选。
iPS人工诱导多能干细胞综述

人工诱导多能干细胞的发展和面临的主要问题航天航空学院航03班徐越学号_2010011566诱导性多功能干细胞(iPSC),是通过导入特定基因或基因产物,将体细胞人工诱导成为类似于胚胎干细胞(ESC)的、具有多向分化能力的、可以持续分离生长的多功能干细胞。
这项技术由日本京都大学山中伸弥教授在2006年首先提出[1],因其乐观的应用价值而引起了科学界的广泛关注并迅速发展。
这篇文章将就iPS细胞的基本技术、发展及面临的问题等方面做一些综述。
一、历史背景上世纪八十年代小鼠ESC被成功分离和细胞体内重编程概念的建立,使再生医学得以建立和发展。
由于胚胎干细胞有多向分化能力,可以有效修复退化的或是受损的组织,治疗一些疑难杂症。
但是,基于胚胎干细胞的临床治疗面临着两个问题:1)植入异体胚胎干细胞可能导致机体的排异反应;2)每一个用于治疗的胚胎都有潜在发育成个体的能力,涉及到伦理问题。
iPS细胞的出现有希望使这两个问题得以解决。
二、技术概述人工诱导多能干细胞的大致过程是:1)取自体体细胞进行体外培养;2)利用“载体”等方法将特定基因或基因产物转入体细胞;3)用与ES细胞相似的条件进行体外培养;4)利用多能细胞标记等条件筛选出iPS细胞;5)生成嵌合体或诱导培养成组织并进一步应用。
1、细胞来源iPS细胞的来源全部取自体细胞。
2006年这一概念第一次被提出时,山中伸弥使用的是小鼠表皮成纤维细胞和尾尖成纤维细胞。
2007年,成人皮肤成纤维细胞也被成功诱导成iPS 细胞。
[2]后来的研究中,以成纤维细胞为细胞源最为常见。
2008年,从成年小鼠的肝脏和胃细胞诱导iPS细胞也获得了成功。
[5]在小鼠中,最常用的是表皮成纤维细胞和尾尖成纤维细胞,也有神经细胞、肌肉细胞、间充质干细胞等,2009年成熟的B细胞和T细胞也获得成功。
人类中新生儿的包皮、口腔黏膜、成人真皮最为常用,角质细胞、间充质细胞、脐带血细胞等也有应用。
有学者证明任意的体细胞都有被诱导成iPS细胞的能力,与细胞种类及人的年龄、性别等没有关系。
生物工程知识:细胞重编程——人类细胞再生的前沿技术

生物工程知识:细胞重编程——人类细胞再生的前沿技术细胞重编程是指通过在体外对人类细胞的基因进行改造,使这些细胞重新回到胚胎干细胞的状态,从而实现再生,也被称为iPS技术(induced pluripotent stem cell,诱导多能干细胞技术)。
iPS技术的诞生源于对干细胞的研究。
干细胞是一类特殊的细胞,它们拥有相当多的特征,如自我复制、分化和自我更新能力。
干细胞能够分化成多种细胞,有望成为治疗不同疾病所需要的种种细胞。
然而,从人体内获取干细胞并不容易,因此科学家开始探索如何将非干细胞转化成干细胞的方法。
2006年,著名的日本细胞学家山中伸弥(Shinya Yamanaka)利用质粒质谱技术和代码重编程的思想,将人普通成体细胞重编程为胚胎干细胞样细胞,而获得最早的iPS细胞,这项技术也被誉为生命科学的里程碑。
细胞重编程技术为人类的再生医学打开了无限可能,不仅能避免胚胎干细胞研究引发的伦理问题,还可以避免种种致命的安全隐患。
此外,此技术使用的细胞可以来源自患者自身身体不同部分的细胞,比如皮肤和其他组织细胞,这意味着细胞在治疗中几乎是无限制使用的。
细胞重编程技术正在被广泛应用于临床治疗疾病。
通过将全身病人的细胞重编程成干细胞,使它们分化出所需的细胞,并将它们重新注入病人体内,医生可以治疗众多分化障碍和器官疾病。
这种治疗方式可行性已经在实践中得到证明,最受欢迎的使用是治疗心脏和神经损伤,这些损伤是因生理/外伤等因素导致的细胞缺失。
随着技术的进步,细胞重编程就像一座新的桥梁,加速了再生医学领域的发展。
但是,这项技术仍处于不断发展和完善的阶段,它依然存在着一些限制和挑战。
例如,细胞重编程有一定的安全隐患,因为这种技术常常使用病毒输送基因,并且很难保证细胞重编程期间产生的iPS细胞不会突变。
因此,有必要进行深入的研究,以确保治疗安全。
细胞重编程技术的另一个潜在限制是高昂的成本。
当前,iPS细胞的制备仍需要较高的技术水平和昂贵的药品,这可能使治疗的成本成为制约因素。
IPS细胞简介
Thank you !
前言
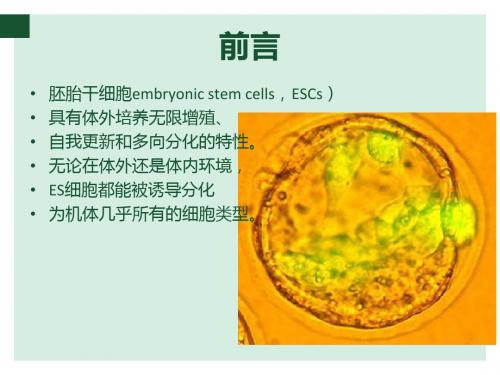
• • • • • • 胚胎干细胞embryonic stem cells,ESCs) 具有体外培养无限增殖、 自我更新和多向分化的特性。 无论在体外还是体内环境, ES细胞都能被诱导分化 为机体几乎所有的细胞类型。
IPS 细胞是什么
Induced pluripotent stem cells,即IPS细胞。什么是 IPS 细 胞呢?简单来说就是借助基因导入技术将某些特定因子 导入动物或人的体细胞,同时可选择性地在培养液中加 入特定的小分子物质,即可将体细胞重编程为和ES细胞 非常相似的多潜能干细胞。
山中申弥团队 诱导的IPS细胞
IPS细胞制备流程
基因导入方式
• 目前,通过逆转 录病毒、慢病毒、 腺病毒和 胞,进而将其重 编程为 iPS 细 胞.
IPS细胞发展历程
不同因子组合将人的不同类型细胞诱导为IPS细胞
IPS细胞现状和前景展望
诱导功能干细胞名词解释

诱导功能干细胞名词解释诱导功能干细胞(induced pluripotent stem cells,简称iPSCs)是一种可以转化为各类细胞的多能性干细胞。
与胚胎干细胞相似,诱导功能干细胞具有无限自我更新的能力,同时还可以分化为身体内大多数细胞类型。
诱导功能干细胞的发现可以追溯到2006年,由日本科学家山中伸弥和英国科学家托姆森爵士领导的研究团队共同取得了重要突破。
他们通过将特定基因(例如Oct3/4、Sox2、Klf4和c-Myc)导入成人体细胞中,成功使这些细胞回到类似胚胎干细胞的状态。
这种方法绕过了对胚胎的依赖,因此更为伦理和法律所接受。
使用诱导功能干细胞具有广泛的应用前景。
首先,它们可以作为研究工具,用于探究疾病发生、发展的机制。
将患者的成人细胞转化为诱导功能干细胞后,科学家可以将这些干细胞分化为受影响的细胞类型,并研究疾病相关基因突变对细胞功能的影响。
这有助于我们更好地了解疾病的本质,为药物研发和治疗方法提供新的思路。
其次,诱导功能干细胞还可以用于再生医学。
通过将患者的成人细胞转化为干细胞,科学家可以培养出与患者组织相匹配的细胞,用于组织修复。
这意味着将来可能能够用患者自己的细胞治疗他们患有的疾病,避免免疫排斥等问题。
然而,诱导功能干细胞研究仍然面临一些挑战和争议。
其中之一是要提高转化效率,目前该过程仍然相对低效。
此外,使用诱导功能干细胞的临床应用仍处于初级阶段,需要更深入的研究和安全性评估。
总之,诱导功能干细胞代表了一项具有重大意义的科学发现,对医学和生物学领域的发展具有巨大潜力。
随着技术的不断进步和研究的推进,诱导功能干细胞有望成为治疗疾病和解决器官短缺问题的重要手段。
高考语文作文素材人物之山中伸弥

2012年10月8日晚上,山中伸弥正拿着工具修洗衣机——家里的洗衣机发出异响,突然,手机响了,一接听,被告知自己获得了2012年诺贝尔生理学或医学奖。
当时他还不信,以为有人跟他开玩笑,因为他认为全世界有资格获得诺贝尔奖的研究者很多。
让山中伸弥获得诺贝尔奖的是被称为“生物学里程碑”式的贡献:山中的发现表明,完整的哺乳动物成熟细胞能够重新编程,被恢复为像胚胎一样的细胞。
这些诱导多能干细胞(iPS细胞)能够发育成为身体的各种组织。
这一发现彻底改变了人们对细胞和器官生长的理解,教科书因之改写,新的研究领域被建立起来。
通过对人体细胞的重新编程,科学家们创造出诊断和治疗疾病的新方法。
1.梦想参加奥运会山中出生于1962年,父亲是一位经营缝纫机零部件作坊的小老板。
受到父亲的影响,他从小着迷于动手制作、拆解各种各样的物件。
有一次,他把家里祖传的钟拆了,重新装完却发现多了3个零件,为此还遭了母亲的一顿打。
后来,山中考入了大阪的重点中学——大阪教育大学附属天王寺高中。
别的同学都在认真学习,山中却热衷于柔道,甚至为此骨折了10多次,他的梦想是参加奥运会。
人们只能感叹:“应该去考大阪体育大学附属高中,而不是在这里学习文化知识。
”高中3年很快就要过去,这个“失败”的学生将何去何从呢?按照传统,作为家中独子的山中应继承父业,但父亲认为他没有做生意的天分,劝他道:“你受了那么多次伤,为什么不当一个医生来减轻病人的痛苦呢?”山中曾读过日本当代著名医生德田虎雄的著作《只有生命是平等的》,并深受影响,父亲的这番话让他决心学医。
在最后的阶段,山中开始玩命学习,终于考入了著名的日本国立神户大学医学部,而且是热门的整形外科。
然而,即便是大学期间,山中也没有埋头读书,依旧热衷于体育。
在奉行刻苦勤勉的日本大学里,山中无疑是个异类。
然而,在山中困难的时候,正是对体育的爱好拉了他一把。
山中的科研团队一直受到资金不足的困扰,2011年,他决定参加“京都马拉松”来募集科研经费,最终他不但完成了比赛,还以4小时3分19秒刷新了个人纪录。
日本ips临床实验

日本ips临床实验随着医学科技的不断进步,再生医学领域也取得了重大突破。
由人体内的特定细胞重新培养出的诸如iPS(诱导多能干细胞)等细胞类型,为疾病的治疗和康复提供了全新的选项。
日本一直是再生医学领域的先驱之一,在该领域的研究和临床实验上有着卓越的贡献。
1. 介绍日本ips临床实验旨在通过应用诱导多能干细胞(iPS细胞)技术来治疗各种类型的疾病。
iPS细胞是在实验室中从成年人体内的成体细胞中重编程而来的多能干细胞。
这些细胞可以以任意的细胞类型发育,并且具有很大的治疗潜力。
2. iPS细胞的发现2006年,日本科学家山中伸弥和他的团队首次成功将成年皮肤细胞转化为多能干细胞,即iPS细胞。
这一突破性的发现引起了全球医学界的关注和赞誉,并为再生医学领域的研究开辟了新的道路。
3. 日本ips临床实验的突破自iPS细胞的发现以来,日本一直在临床实验中积极应用这一技术。
目前,日本已经进展到了临床试验的阶段,试图利用iPS细胞治疗多种疾病,包括心脏病、帕金森病和视网膜疾病等。
3.1 心脏病的治疗在心脏病的治疗方面,日本的研究人员采用iPS细胞改变了心脏病患者身体内的细胞。
这些iPS细胞被注射到患者的心脏中,以修复受损的心肌组织。
临床试验的结果表明,此项治疗方法取得了积极的效果,为心脏病患者带来了新希望。
3.2 帕金森病的治疗帕金森病是一种神经系统退行性疾病,也成为了iPS细胞研究的另一个重点。
日本的研究人员通过将iPS细胞转化为神经元,并将其移植到帕金森病患者的大脑中,来改善患者的症状。
临床试验的初步结果显示了治疗的潜力,为帕金森病患者提供了新的治疗选择。
3.3 视网膜疾病的治疗视网膜疾病是导致失明的主要原因之一。
为了治疗这类疾病,日本的研究人员尝试将iPS细胞转化为视网膜细胞,并将其移植到病人的眼睛中。
临床实验证实,通过这种治疗方式,患者的视力得到了显著改善,为失明患者带来了曙光。
4. 挑战与展望虽然日本的ips临床实验在再生医学领域取得了重要进展,但仍面临一些挑战。
诱导性多能干细胞的应用

诱导性多能干细胞的应用2006年,日本医学家山中伸弥等将4个转录因子基因导入已分化的小鼠皮肤成纤维细胞,将其重编程为类似于胚胎干细胞的多能性干细胞,即诱导性多能干细(Induced pluripotent stem cells,iPS cells)。
这项技术避免了干细胞研究领域的免疫排斥和伦理道德问题, 是生命科学领域的一次巨大革命。
与胚胎干细胞一样, iPS 细胞能够长期增殖并维持高度未分化状态, 在体内可分化为3个胚层来源的所有细胞, 进而参与形成机体所有组织和器官。
在体外, iPS 细胞可定向诱导分化出多种成熟细胞。
因此, iPS 细胞在理论研究和临床应用等方面都极具应用价值。
iPS细胞与再生医学是目前研究的热点。
如多项研究在人类血液疾病的小鼠模型中进行了iPS细胞应用的尝试,并取得了初步成功。
Hanna等在人源化的镰刀型贫血病小鼠模型上获取成纤维细胞,诱导建立了iPS细胞系,然后通过同源重组的方法将病变基因修正,接着把遗传修饰后的iPS细胞定向分化为造血干细胞,导入小鼠体内,贫血症状明显改善,这是首次利用iPS细胞进行的人类疾病治疗研究。
iPS技术在治疗神经系统疾病中显示了很大的用途。
Werning等对已建立的小鼠iPS细胞进行体外诱导培养,可以将其诱导分化为神经前体细胞和多巴胺能神经元,并移植到患有帕金森病小鼠体内能减轻其症状。
最近一项研究利用帕金森症患者的皮肤细胞培育出了iPS 细胞,并能将其分化为多巴胺神经元细胞,这是帕金森症患者大脑中所缺少的一种重要细胞。
因此,其有望成为治疗帕金森症等神经系统疾病的一种方法。
虽然iPS细胞技术在再生医疗领域的尝试与应用还远未成熟,但随着iPS细胞基础与临床研究的深入,iPS细胞必将开辟再生医学领域的新纪元。
IPS细胞

子区域。
返回
织等是亟待阐明的问题.
返回
胚胎干细胞(embryonic stem cells,ES cells)
是来源于哺乳动物囊胚内细胞团(inner cell mass,
ICM)的多潜能干细胞,具有无限自我更新和多向
分化能力.ES 细胞在疾病模型建立与机理研究、 细胞治疗、药物发现与评价等方面极具应用价 值. 返回
reprogrammed IPSCs)、筛选标准不严紧和IPS
细胞携带供体.细胞的表观遗传记忆和IPS 细胞 分化不定向都导致细胞异质性,异质性是导致 IPS细胞成瘤的潜在因素 d.IPS 细胞体外定向分化细胞的功能与行为研 究尚少,尤其在细胞治疗上,目的细胞是否会在 治疗靶位或迁移到非靶位点成瘤,或异位形成组
一、IPS细胞定义
诱导多潜能性干细胞(又称多潜能干细胞, induced pluripotent stem cells, IPS cells)是由 一些多能遗传基因导入皮肤等受体细胞中通 过基因重新编排方法,“诱导”普通细胞回 到最原始的胚胎发育状态,能够像胚胎干细 胞一样进行分化。
IPS细胞与胚胎干细胞(ES)形态相似、核 型、端粒酶活性、体外分化潜能均相同,同 时也能够表达相同的表面标志分子。
e.建立高效、安全、实用制备人 IPS细胞的方法, 即在阐明体细胞重编程为 IPS细胞机制的基础上建 立无遗传修饰的IPS细胞制备策略与方法(如仅利用 一些小分子物质即将人的细胞重编程为 IPS细胞) f.在前一项研究的基础上,探索一条简便制备 “个体特异的”或“疾病特异的”治疗型人 IPS细 胞的技术路线和方法
DNA甲基化:DNA的CG两个核苷酸的胞嘧
啶被选择性地添加甲基,形成5-甲基胞嘧啶,
常见于基因的5‘-CG-3’序列。DNA的甲基化可
山中伸弥发明IPS细胞的介绍及启示

数学统计:Pearson相 检查,发现其能够分化 Figure 5. Pluripotency of
关分析
为多种组织器官,说明 iPS Cells Derived from
其具有多能性。
MEFs
论点
证明方法
证明过程
论文对应部分
不仅是小鼠胚胎成纤 维细胞(MEFs)可被 诱导,其他分化程度
很高的体细胞也可被 诱导。
同上
将这四种因子又一起 Figure 6. 导入了小鼠尾尖成纤 Characterization of iPS 维细胞(TTFs),并进 Cells Derived from 行了与之前相同的检 Adult Mouse Tail-Tip 测,发现同样可以诱 Fibroblasts 导形成IPS细胞。
胞的多功能干细胞。 表观遗传学:染色质免 之处和差异发现ips细 iPS Cells
疫沉淀分析
胞只是类似ES细胞; Figure 4. Global Gene-
组织学:裸鼠皮下移植、同时对IPS细胞发育形 Expression Analyses by
免疫组化染色
成的畸胎瘤进行组织学 DNA Microarrays
组合在一起才能完成诱 导,其余情况均不可。
将24种因子全部加入小 Figure 1. Generation of 鼠MEF细胞中进行诱导 iPS Cells from MEF 可以得到IPS细胞,然 Cultures via 24 Factors 后将每种因子逐个去除,Figure 2. Narrowing
观察去除掉该因子后细 down the Candidate
胞能否诱导成功,最终 Factors 筛选出4个。
通过这四种转录因子的 分子生物学:RT-PCR、 研究IPS和ES在细胞形 Figure 3. Gene-
ips干细胞

细胞的筛选
a.形态学筛选不对供体细胞做任何额外遗传修饰的情况下,仅依靠形态学筛选的标准对细胞进行筛选也能够 分离出IPS细胞。
b.药物筛选利用基因重组技术建立了具有药物抗性基因的体细胞,并用特定药物进行筛选。
c.选用对多能性更为关键的基因(如Fbx25)作为报告基因原理是Fbx25对于多能性的维持和胚胎的发育来说 是不可缺少的基因
ips干细胞
诱导多能干细胞的简称
01 主要区别
03 细胞的鉴定 05 存在的风险
目录
02 细胞的筛选 04 研究方向 06 科研进展
2006年时,日本京都大学山中伸弥(Shinya Yamanaka)教授的团队发现只须将四个与干细胞特性相关的转 录因子Oct3/4、Sox2、c-Myc,以及Klf4(简称OSKM,也被称为「山中因子」Yamanakafactors),利用反转录 病毒的方式导入小鼠皮肤纤维母细胞后,即可以促使纤维母细胞重新再编程,形成具有多能性干细胞的分化能力。 这样的细胞,称为「诱导式多能性干细胞」(iPS细胞induced pluripotent stem cells,iPSCs)。
2014年9月15日首例iPS细胞眼部疾病手术实施
据共同消息,全球首例将诱导多能干细胞(iPS细胞)制成的视膜细胞移植入人体内的手术在完成一夜以后, 其负责手术的尖端医疗中心医院(位于神户市)眼科总部长栗本康夫(53岁)在术后说明情况时称:“没有发2015年12月京都大学iPS细胞研究所和武田制药启动iPS细胞应用研究联合项目
京都大学iPS细胞研究所(Center for iPS Cell Research and application,CiRA)和武田制药公司 (Takeda Pharmaceutical Company Limited,Takeda)2015年12月15日宣布:启动联合研究项目,开发诱导 多能干细胞(iPSC)的临床应用。这项“ips细胞应用Takeda-CiRA联合项目(T-CiRA)”将针对6个核心方向探 索干细胞在治疗领域的临床应用,包括癌症、心力衰竭、糖尿病、神经退行性疾病和难治性肌肉疾病。
人物素材之山中伸弥

诺贝尔奖得主曾被称为捣乱医生2012年10月8日晚上,山中伸弥正拿着工具修洗衣机——家里的洗衣机发出异响,突然,手机响了,一接听,被告知自己获得了2012年诺贝尔生理学或医学奖。
当时他还不信,以为有人跟他开玩笑,因为他认为全世界有资格获得诺贝尔奖的研究者很多。
让山中伸弥获得诺贝尔奖的是被称为“生物学里程碑”式的贡献:山中的发现表明,完整的哺乳动物成熟细胞能够重新编程,被恢复为像胚胎一样的细胞。
这些诱导多能干细胞(iPS 细胞)能够发育成为身体的各种组织。
这一发现彻底改变了人们对细胞和器官生长的理解,教科书因之改写,新的研究领域被建立起来。
通过对人体细胞的重新编程,科学家们创造出诊断和治疗疾病的新方法。
1.梦想参加奥运会山中出生于1962年,父亲是一位经营缝纫机零部件作坊的小老板。
受到父亲的影响,他从小着迷于动手制作、拆解各种各样的物件。
有一次,他把家里祖传的钟拆了,重新装完却发现多了3个零件,为此还遭了母亲的一顿打。
后来,山中考入了大阪的重点中学——大阪教育大学附属天王寺高中。
别的同学都在认真学习,山中却热衷于柔道,甚至为此骨折了10多次,他的梦想是参加奥运会。
人们只能感叹:“应该去考大阪体育大学附属高中,而不是在这里学习文化知识。
”高中3年很快就要过去,这个“失败”的学生将何去何从呢?按照传统,作为家中独子的山中应继承父业,但父亲认为他没有做生意的天分,劝他道:“你受了那么多次伤,为什么不当一个医生来减轻病人的痛苦呢?”山中曾读过日本当代著名医生德田虎雄的著作《只有生命是平等的》,并深受影响,父亲的这番话让他决心学医。
在最后的阶段,山中开始玩命学习,终于考入了著名的日本国立神户大学医学部,而且是热门的整形外科。
然而,即便是大学期间,山中也没有埋头读书,依旧热衷于体育。
在奉行刻苦勤勉的日本大学里,山中无疑是个异类。
然而,在山中困难的时候,正是对体育的爱好拉了他一把。
山中的科研团队一直受到资金不足的困扰,2011年,他决定参加“京都马拉松”来募集科研经费,最终他不但完成了比赛,还以4小时3分19秒刷新了个人纪录。
利用iPS细胞破解人与类人猿之间的差异

利用iPS细胞破解人与类人猿之间的差异日本京都大学的山中伸弥(Shinya Yamanaka)在2006年构建出小鼠iPSCs 后不久,紧接着人类的 iPSCs 也被构建出来,进而被授予了2012 年的诺贝尔生理学或医学奖。
现在科学家们常常会利用 iPSCs 生成很难从活体人类或动物处获得的细胞来构建疾病模型。
通过添加4 个重要因子的组合,可将皮肤细胞转化成 iPSC,随后再诱导 iPSC 在培养皿中形成肝、肺和脑细胞,并构建疾病模型。
索尔克生物研究所研究人员称,比较人类、黑猩猩和倭黑猩猩细胞可提供一些线索,来了解如感染、疾病、脑进化、适应或遗传多样性等生物学过程。
直到现在,黑猩猩和倭黑猩猩的细胞资源仍限于死后组织或血液。
而譬如现在,你就可以生成来自三个不同物种的神经元,比较它们来验证假说。
在新研究中,科学家们发现了人类和非人类灵长类动物细胞之间跳跃基因(又称作转座子)调控的差异。
转座子是指能够拷贝并粘贴自身到整个基因组的某些位点中去的一些DNA元件。
科学家们说,这些跳跃基因提供了一种方法进行快速的DNA洗牌,有可能塑造了我们的基因组进化。
Narvaiza和同事们鉴别了来自人类、黑猩猩和倭黑猩猩的 iPSCs 之间差异表达的基因。
让研究小组感到惊讶地是,其中有两个基因编码的蛋白质限制了一个叫做L1(long interspersed element-1)的跳跃基因。
与非人类灵长类动物的细胞相比较,人类 iPSCs 中这两个叫做APOBEC3B和PIWIL2的限制因子表达水平较高。
论文的共同领导者、Salk生物研究所高级研究员Carol Marchetto说:“我们并没有预料到这种情况,这些基因引起了我们的注意,因此它们成为了我们首先聚焦的对象。
”L1和其他的一些跳跃基因在我们的整个基因组中极为丰富。
很难预测这些dna片段会将自身插入到基因组的何处,它们可以产生不同的影响。
例如,它们有可能会完全破坏基因,调节它们或是导致它们被处理成全新的蛋白质。
自然辩证法-论创造性思维

科学研究中的创造性思维—以2012年诺贝尔医学奖获得者山中伸弥的IPS为例摘要在诸多成功的基础科学研究案例中,日本医学家山中伸弥的诱导多功能干细胞(IPS Cells,Induced Pluripotent Stem Cells)的研究,尤其是其“山中因子”的发现具有较强的示范性。
山中伸弥突破了胚胎干细胞研究的伦理道德,实现了对成年人皮肤细胞的重组,进而实现了逆转生命程序。
近6年以来,在研究与其相适应的病理模型过程中,山中伸弥团队都保持了持续创新。
通过剖析IPS这一研究案例中山中伸弥的创新思维,可以发现科学研究走向成功的共性因素,这对于我们掌握创新思维,并实现科技创新具有重要意义。
关键词山中伸弥;IPS;山中因子;创新思维科学研究是创造性的探索活动,无论基础研究或应用研究,都是探索未知的过程,都是为了解决尚未解决的问题。
在构建创新型国家的过程中,科技创新成为先导。
科技创新至少包含了思维、方法和工具的创新。
在这三个层面的创新中,思维和方法的创新尤其重要。
然而,科学研究有其内在的规律,任何创新都具有继承性,都需要建立在前人成果的基础之上。
创新虽是为超越,但创新的基础是传承。
通过对杰出科学家的学术思维和研究方法的研究,找到他们走向成功的关键因素,对我们这些科学研究的后继者们具有重要的意义。
山中伸弥的IPS研究具有源于医学需要的实践导向型的特点,他在实践中不断总结经验,并将感觉经验和理性思维有效地结合,从而在成人干细胞的重组领域开创了独特的研究思路和方法。
充分解析山中伸弥在IPS研究过程中的创新思维和方法,吸取其学术思想中的成功经验,有助于促进我们在科技研究中实现突破性进展。
一、创造性思维的逻辑科学研究的成败取决于两大因素:一是研究者对相关知识技能掌握和运用的能力;二是其思维能力。
前者是实现设想的基本保障,后者决定了研究水平的高度,是成功的关键。
成功者之说以能成功,就在于同时拥有这两种能力并能够有效地运用这两种能力。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
论文对应部分
Figure 6. Characterization of iPS Cells Derived from Adult Mouse Tail-Tip Fibroblasts Figure 6. Characterization of iPS Cells Derived from Adult Mouse Tail-Tip Fibroblasts Figure 7. Biochemical and Genetic Analyses of iPS Cells
汇报人:XXX
作者与成果介绍:
• 作者:山中伸弥(Shinya Yamanaka),日本京都大 学前沿医学研究所教授, 医学家 • 发表期刊:《Cell》 • 时间:2006.8.25
• 地位:2012年诺贝尔生理 学奖(John B. Gurdon, UK)
文章背景:
Sir Martin John Evans
研究思路:
• 基因选择性表达:每一种细胞的特性都是由特异性的蛋白决定的,正 常的体细胞中表达的基因决定其不能够继续分化,而ES细胞中特异性 表达的蛋白决定了其分化的多样性。
• 如果将这些维持胚胎干细胞多样性的特异性蛋白转入体细胞中,能否 使体细胞具有胚胎干细胞的特性?
研究过程:
over 100 factor s
只有Oct3/4、Sox2、c- 计算机统计分析 Myc和Klf4这四种转录 动物细胞培养 因子是必需的,且必须 形态学分析 组合在一起才能完成诱 导,其余情况均不可。
通过这四种转录因子的 分子生物学:RT-PCR、 研究IPS和ES在细胞形 确获得了类似胚胎干细 DNA微阵列技术 态、基因表达上的相似 胞的多功能干细胞。 表观遗传学:染色质免 之处和差异发现ips细 胞只是类似ES细胞; 疫沉淀分析 组织学:裸鼠皮下移植、 同时对IPS细胞发育形 免疫组化染色 成的畸胎瘤进行组织学 数学统计:Pearson相 检查,发现其能够分化 关分析 为多种组织器官,说明 其具有多能性。
IPSs能够像胚胎干细胞 显微注射 一样促进胚胎的发育。 组织学分析
略 ⑤进一步研究4种转录 real-time PCR、 因子在IPS与ES细胞中 western blot、southern 的表达情况,明确IPS blot。 与ES细胞在基因表达 水平上的差异。
文章创新之处:
“对于这样的研究, 我们实验室根本不 具备竞争力,所以 我想,反其道而行 之或许是条出路—— 不是让胚胎干细胞 变成什么,而是让 别的东西变成胚胎 干细胞。”
论点
不仅是小鼠胚胎成纤 维细胞(MEFs)可被 诱导,其他分化程度 很高的体细胞也可被 诱导。 同上
证明方法
证明过程
将这四种因子又一起 导入了小鼠尾尖成纤 维细胞(TTFs),并进 行了与之前相同的检 测,发现同样可以诱 导形成IPS细胞。 将绿色荧光蛋白基因 标记的IPSs显微注射至 小鼠囊胚,发现IPSs参 与了小鼠三胚层的分 化,说明IPS能够促进 胚胎的发育。
文章背景:
Obtained in human in 1998 Dr. James Thomson
在当时出现的问题:
• 引发伦理争议 利用试管婴儿技术获得受精卵的夫妇将多余胚胎捐赠给实验室, 用于其他研究。这种通过破坏胚胎来获取胚胎干细胞供人类研究的 做法引发了很大的伦理争议。 • 免疫排斥反应 利用胚胎干细胞形成的组织在给患者进行器官移植过程中会发生 免疫排斥反应。
• 突破惯性思维,敢于挑战所谓的“自然规律”——逆转生命的时钟。 • 在关于生物可能性的思考上更加开放——脑洞大开。
研究目标:
论文解决的关键问题:
Induced pluripotent stem cells,iPSs
2009年1月《环球科学》 文/Tim Hornyak
当历史学家为干细胞研究 撰写编年史时,山中伸弥 (Shinya Yamanaka)很可 能以一个“和事佬”的角 色被载入史册:这位日本 科学家用一种前所未有的 方式,终结了胚胎干细胞 领域旷日持久的伦理之争。
Induction of Pluripotent Stem Cells from Mouse Embryonic and Adult Fibroblast Cultures by Defined Factors
Kazutoshi Takahashi1 and Shinya Yamanaka1,2,*
论点
证明方法
证明过程
将24种因子全部加入 小鼠MEF细胞中进行诱 导可以得到IPS细胞, 然后将每种因子逐个去 除,观察去除掉该因子 后细胞能否诱导成功, 最终筛选出4个。
论文对应部分
Figure 1. Generation of iPS Cells from MEF Cultures via 24 Factors Figure 2. Narrowing down the Candidate Factors Figure 3. GeneExpression Profiles of iPS Cells Figure 4. Global GeneExpression Analyses by DNA Microarrays Figure 5. Pluripotency of iPS Cells Derived from MEFs
24 factor s
4 factor s
trasducti on in MEFs
iPS cells
得出的结论:
— iPS cells
使用了何种材料和方法支持论点?
• 证据充足:正文14页,图表数据7页,补充材料 41页。 • 方法技术: • 分子生物学方法:转基因技术、RT-PCR、DNA microarray、real-time PCR、western blot、southern blot • 表观遗传学方法:染色质免疫沉淀分析 • 组织学方法:裸鼠移植、免疫组化染色 • 数学统计方法:Pearson相关分析、Student's t test、one-factor ANOVA
