厦门大学 材料科学基础(二) 第四章-1 缺陷化学
【推荐下载】材料化学晶体缺陷化学PPT文档

热缺陷的平衡热力学
1. 基本假设 点缺陷是一种热缺陷,在一定温度下,它处在不断地产 生和消失的过程中,并满足热力学平衡条件。对热缺陷系统 可看作是等容过程。其自由能F、内能U和熵变S复合下列关
系:
F U T S F U T S
平衡时自由能最小,温 度一定时,有一定数目 的热缺陷存在,这时平 衡条件为:
nFren = N Exp(-UFren /RT)
3.浓度公式的讨论与应用
n Ne 或n Ne Schot
(USc h)ot kT
Sch o t
(USc h)ot RT
n Ne 或n Ne Fren
(UFr e)n kT
Fr en
(UFr e)n RT
3-13 3-14
⑴ 缺陷浓度与温度的关系
两种缺陷的浓度都随温度升高而增加,随温度的下降而 减少。当温度T→0时,缺陷浓度n→0,才会有完全有序的晶体 (completedly ordered solid phase),也就是完美的晶体(ideal perfect crystals),这正是热力学第三定律。
在三维尺寸较大,如镶嵌块,沉淀相,空洞,气泡等。
面缺陷——晶粒间界 体缺陷——空洞 体缺陷——包裹杂质
几何维度缺陷分类总结
点缺陷:在三维尺寸均很小,只在某些位置发生,只影
响邻近几个原子。 这种化合物在材料中有重要的作用,目前已发展出混合价态的固体化学和材料化学,在配位化学和生物化学中也有重要意义。
②可以以形成间隙正体离子缺形成陷来平:衡过在剩电三荷;维尺寸较大,如镶嵌块,沉淀相,空洞,
气泡等。
●从晶体的组成出发,可将缺陷分为: 本征缺陷 defects)或结构缺陷(Structural defects):产 生于晶体本身结构的缺陷。 由于这类缺陷产生的原因主要是热运动之故,又称之为 物理缺陷或热缺陷; 非本征缺陷(innative defects):主要由于外来原子进入 晶体而造成的缺陷。由于这类缺陷并非晶体本体组成,故又称 为杂质缺陷(Imourity defects)。又因这些缺陷主要来自化学 制备方面,故还称之为化学缺陷(Chemical defects)。 在缺陷讨论中,也可以将两类缺陷分类结合在一起:
材料科学基础 第4章 点缺陷和扩散

化、烧结等都产生了重要的影响。
30
二、离子晶体中的空位及间隙原子
肖脱基缺陷:为了保持晶体的电的中性,空位只能 以与晶体相同的正离子:负离子的空位比率小组的 方式产生。这些电中性的正离子-负离子-空位丛簇 称为。 弗兰克缺陷:以空位/间隙对形式存在的缺陷群。
29
关于空位的总结
空位是热力学上稳定的点缺陷,一定的温度对应一定的 平衡浓度,偏高或偏低都不稳定。
不同金属的空位形成能是不同的,一般高熔点金属的形 成能大于低熔点金属的形成能。
空位浓度、空位形成能和加热温度之间的关系密切。在 相同的条件下,空位形成能越大,则空位浓度越低;加 热温度越高,则空位浓度越大。 C平=exp[-Ev/kT+Sc/k]
23
空位迁移也要克服一定的“势垒”,也即空位迁移能Qfv。 迁移速率为: j=zexp(Sc/k)exp(-Qfv/kT)
金属熔点越高,空位形成能和迁移能越大。所以,在相 同条件下,高熔点金属形成的空位数比低熔点金属少。
24
5.材料中空位的实际意义
空位迁移是许多材料加工工艺的基础。
晶体中原子的扩散就是依靠空位迁移而实现的。 在常温下空位迁移所引起的原子热振动动能显著提高,再加上高 温下空位浓度的增多,因此高温下原子的扩散速度十分迅速。
53扩散分类1根据?c?t分类稳态扩散和非稳态扩散2根据?c?x分类?c?x0自扩散在纯金属和均匀合金中进行?c?x?0互扩散上坡扩散和下坡扩散3根据扩散途径分类体扩散晶界扩散表面扩散短程扩散沿位错进行的扩散4根据合金组织分类单相扩散多相扩散54二扩散的物理描述fick第一扩散定律影响原子移动的速率即扩散速率的因素
第2章 材料化学的理论基础-晶体缺陷化学PPT课件

点缺陷的分类
按几何位置及成分分类:
➢ 填隙原子 (离子) ➢空 位 ➢ 杂质原子
点缺陷的名称
根据点缺陷相对于理想晶体位置可能出现的偏差状态,可以赋 予点缺陷不同的名称:
1)填隙原子(离子):指原子或离子进入正常格点位置之间的 间隙位置,也称为间隙原子(离子)。
2)空位:正常结点位置出现的原子或离子空缺。 3)杂质原子(离子):晶体组成以外的原子进入晶格中,即
2-3-1 晶体缺陷及其分类
晶体缺陷(晶格的不完整性): 晶体中任何对完整周期性结构的偏 离就是晶体的缺陷。
1、 缺陷及其分类
晶体的缺陷
结构缺陷: 没有杂质的具有理想的化学配比 的晶体中的缺陷,如空位、填隙 原子、位错。
化学缺陷: 由于掺入杂质或同位素,或者化学 配比偏离理想情况的化合物晶体中 的缺陷,如杂质、色心等。
为杂质。杂质原子可以取代晶体中正常格点位置上的原子(离 子),成为替代原子(离子)或称为置换原子(离子);也可 进入正常格点位置之间的间隙位置,成为填隙的杂质原子(离 子)。
点缺陷:按缺陷产生的原因分类
➢热缺陷: 由于空位和填隙原子与温度有直接
的关系,或者说与原子的热振动有关的缺陷 称为热缺陷。即由于晶体内部质点热运动而 形成的缺陷称为热缺陷。
点缺陷有时候对材料性能又是有利的
彩色电视荧光屏中的蓝色发光粉的主要原料 是硫化锌 (ZnS) 。在硫化锌晶体中掺入约 0.0001% AgCl,Ag+ 和 Cl- 分别占据硫化锌晶体 中 Zn2+ 和 S2- 的位置,形成晶格缺陷,破坏了晶 体的周期性结构,使得杂质原子周围的电子能级 与基体不同。这种掺杂的硫化锌晶体在阴极射线 的激发下可以发出波长为 450 nm 的荧光。
《材料科学基础》课件之第四章----04晶体缺陷

41
刃位错:插入半原子面,位错上方,原子间距变小, 产生压应变,下方原子间距变大,拉应变。过渡处 切应变,滑移面处有最大切应力,正应力为0。x NhomakorabeaGb
2 (1 )
y(3x2 (x2
y2) y2 )2
y
Gb
2 (1
)
y(x2 y2) (x2 y2)2
z ( x y )
x
xy
Gb
2 (1 )
21
刃位错b与位错线 垂直
螺位错b与位错线 平行
bb
l
l
正
负
b
b
右旋
左旋
任意一根位错线上各点b相同,同一位错只有一个b。
有大小的晶向指数表示
b a [uvw] 模 n
b a u2 v2 w2 n
22
Burgers矢量合成与分解:如果几条位错线在晶体内
部相交(交点称为节点),则指向节点的各位错的伯氏矢量 之和,必然等于离开节点的各位错的伯氏矢量之和 。
不可能中断于晶体内部(表面露头,终止与 晶界和相界,与其他位错相交,位错环)
半原子面及周围区域统称为位错
18
2. 螺位错
晶体在大于屈服值的切应力作用下,以某晶面为滑移面发生滑移。由于位错线周围 的一组原子面形成了一个连续的螺旋形坡面,故称为螺位错。
几何特征:位错线与原子滑移方向相平行;位错线周围原子的配置是螺旋状的。
d
34
六、位错应变能
位错原子偏移正常位置,产生畸变应力, 处于高能量状态,但偏移量很小,晶格为弹 性应变。
位错心部应变较大,超出弹性范围, 但这部分能量所占比例较小, <10%,可以近似忽略。
35
1. 理论基础:连续弹性介质模型
厦门大学材料学院 材料科学基础 习题5

第四章作业:
(本章知识点多,计算题计算量较大,希望同学们认真复习本章讲的知识点并独
立完成作业。
)
1、试从自由能角度,结合图例,解释为什么会发生上坡扩散?
2、为研究稳态条件下间隙原子在面心立方金属中的扩散情况,在厚0.3mm的金属薄膜的一个端面(面积1000mm2)保持对应温度下的饱和间隙原子,另一端面
3、设有一条内径为40mm的厚壁管道,被厚度为0.2mm的铁膜隔开。
通过管
子的一端向管内输入氮气,以保持膜片一侧氮气浓度为1400mol/m3, 而另一
侧的氮气浓度为100mol/m3。
如在700℃下测得通过管道的氮气流量为2.9
×10-8mol/s,求此时氮气在铁中的扩散系数。
4、一块w(C)=0.1%的碳钢在930℃渗碳,渗到0.06cm的地方,碳的浓度达到
0.45%。
在t>0的全部时间,渗碳气氛保持表面成分为1%,假设
r
D=2.6×10-5exp(-140000/RT)(m2/s),
C
①计算渗碳时间。
②若将渗层加深2倍,则需多长时间?
③若规定w(C)=0.35%作为渗碳层厚度的量度,则在930℃时渗碳10h的渗层厚
度为870℃时渗碳10h的多少倍?
5、碳在α-Ti中的扩散系数在以下温度被确定。
①试确定公式
0exp()
D D
RT
=-是否适用;若适用,则计算出扩散常数D0和激活能Q。
②试求出500℃下的扩散系数。
厦门大学,829材料科学基础 部分简答题总结

原子结构1、原子间的结合键共有几种?各自的特点如何?【11年真题】答:(1)金属键:基本特点是电子的共有化,无饱和性、无方向性,因而每个原子有可能同更多的原子结合,并趋于形成低能量的密堆结构。
当金属受力变形而改变原子之间的相互位置时不至于破坏金属键,这就使得金属具有良好的延展性,又由于自由电子的存在,金属一般都具有良好的导电性和导热性能。
(2)离子键:正负离子相互吸引,结合牢固,无方向性、无饱和性。
因此,七熔点和硬度均较高。
离子晶体中很难产生自由运动的电子,因此他们都是良好的电绝缘体。
(3)共价键:有方向性和饱和性。
共价键的结合极为牢固,故共价键晶体具有结构稳定、熔点高、质硬脆等特点。
共价结合的材料一般是绝缘体,其导电能力较差。
(4)范德瓦尔斯力:范德瓦尔斯力是借助微弱的、瞬时的电偶极矩的感应作用,将原来稳定的原子结构的原子或分子结合为一体的键合。
它没有方向性和饱和性,其结合不如化学键牢固。
(5)氢键:氢键是一种极性分子键,氢键具有方向性和饱和性,其键能介于化学键和范德瓦耳斯力之间。
2、陶瓷材料中主要结合键是什么?从结合键的角度解释陶瓷材料所具有的特殊性能。
【模拟题一】答:陶瓷材料中主要的结合键是离子键和共价键。
由于离子键和共价键很强,故陶瓷的抗压强度很高、硬度很高。
因为原子以离子键和共价键结合时,外层电子处于稳定的结构状态,不能自由运动,故陶瓷材料的熔点很高,抗氧化性好、耐高温、化学稳定性高。
第二章固体结构1、为什么只有置换固溶体的两个组元之间才能无限互溶,而间隙固溶体则不能?【模拟题一】答:因为形成固溶体时,溶质原子的溶入会使溶剂结构产生点阵畸变,从而使体系能量升高。
溶质与溶剂原子尺寸相差较大,点阵畸变的程度也越大,则畸变能越高,结构的稳定性越低,溶解度越小。
一般来说,间隙固溶体中溶质原子引起的点阵畸变较大,故不能无限互溶,只能有限熔解。
2、空间点阵和晶体点阵有何区别?【模拟题四】答:空间点阵是晶体中质点排列的几何学抽象,用以描述和分析晶体结构的周期性和对称性,由于各阵点的周围环境相同,它只能有14种类型;晶体点阵又称晶体结构,是指晶体中实际质点的具体排列情况,它们能组成各种类型的排列,因此,实际存在的晶体结构是无限的。
材料科学基础习题第四章答案与翻译
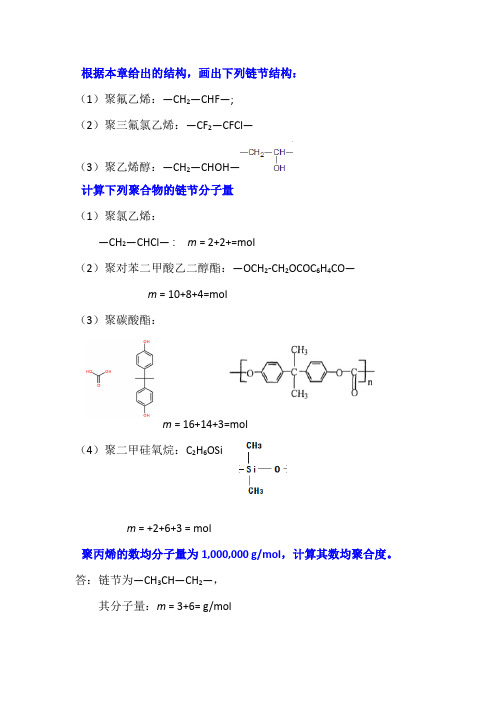
根据本章给出的结构,画出下列链节结构:(1)聚氟乙烯:—CH2—CHF—;(2)聚三氟氯乙烯:—CF2—CFCl—(3)聚乙烯醇:—CH2—CHOH—计算下列聚合物的链节分子量(1)聚氯乙烯:—CH2—CHCl— : m = 2+2+=mol(2)聚对苯二甲酸乙二醇酯:—OCH2-CH2OCOC6H4CO—m = 10+8+4=mol(3)聚碳酸酯:m = 16+14+3=mol(4)聚二甲硅氧烷:C2H6OSim = +2+6+3 = mol聚丙烯的数均分子量为1,000,000 g/mol,计算其数均聚合度。
答:链节为—CH3CH—CH2—,其分子量:m = 3+6= g/mol(a) 计算聚苯乙烯链节的分子量答:链节为CHC6H5CH2,分子量:m = 8+8=(b) 计算重均聚合度为25000的聚苯乙烯的重均分子量答:= 25000 g/mol = 2603800 g/mol下表列出了聚丙烯的分子量,计算(a) 数均分子量(b) 重均分子量(c) 数均聚合度(d) 重均聚合度x i w i 分子量分布(g/mol)8,00016,00016,00024,00024,00032,00032,00040,00040,00048,00048,00056,000答:(a)= 12000+20000+28000+36000+44000+52000 = 600+3200+6720+10080+8800+3640 = 33040 (g/mol)(b)= 12000+20000+28000+36000+44000+52000 = 240+2000+5600+10800+11880+10920 = 41440 (g/mol)(c)聚丙烯链节的分子量:m = g/mol(d)下表列出了某聚合物的分子量分布。
计算(a) 数均分子量(b) 重均分子量(c) 如果已知这一聚合物的重均聚合度为780,指出此聚合物为表所列聚合物中的哪一个为什么(d) 这一材料的数均聚合度为多少分子量分布(g/mol)x i w i15,00030,00030,00045,00045,00060,00060,00075,00075,00090,00090,000105,000105,000120,000120,000135,000答:(a)= 22500+37500+52500+67500+82500+97500+112500+127500 = 900+2625+8400+17550+19800+11700+9000+3825 = 73800 (g/mol)(b)= 22500+37500+52500+67500+82500+97500+112500+127500 = 225+1500+5775+16200+22275+15600+13500+ 6375 = 81450 (g/mol)(c)此聚合物为聚苯乙烯根据下面的分子量分布和重均聚合度为585的条件,判断是否为聚甲基丙烯酸甲酯均聚物分子量分布(g/mol)x i w i8,00020,00020,00032,00032,00044,00044,00056,00056,00068,00068,00080,00080,00092,000答:聚甲基丙烯酸甲酯链节分子式为:C5H8O2(—CH2CH3COOCH3C—);其分子量m = 5+8+2=mol重均分子量为:=14000+26000+38000+50000+62000+74000+86000=140+1300+4560+12500+16740+15540+7740=58520与条件相符,能形成均聚物高密度聚乙烯通过诱导氯原子随机取代氢而被氯化。
材料科学基础结构缺陷

b 的方向: 代表了畸变的方向;
四、位错的柏氏矢量( b )
Material
6. 柏氏矢量的表示方法
对于立方晶系,用与 b 同方向的晶向指数表示,即 b
中n是与点阵类型有关的常数。柏氏矢量的模
b
a n
a uvw,其 n u 2 v 2 w2 。
四、位错的柏氏矢量( b )
堆垛层错
因为并不是所有的位错线均能与观察截面相交 所以 ρ v > ρs
五、位错的运动
位错的运动根据其运动形式分为两类: 位错的滑移 Guidelines • – 刃型位错的滑移 – 螺型位错的滑移 • 位错的攀移 – 正攀移 – 负攀移
刃型位错的滑移
Material
刃型位错滑移的性质
一条刃型位错线滑移出整个晶体晶体后,晶体滑移上、下部分的相对滑 移量为一个b,在晶体表面形成一个宽度为b的台阶。若有n条位错线扫过 滑移面,则晶体产生nb的滑移量。
②利用 b 定义刃型位错 位错线与 b 相互垂直的位错,即 l b ;
四、位错的柏氏矢量( b )
Material
1. 刃型位错的柏氏矢量
③刃型位错的形成
晶体中刃型位错形成示意动画
刃型位错中包含的半原子面动画
四、位错的柏氏矢量( b )
Material
2. 螺型位错的柏氏矢量
Material
1-1 点缺陷的类型及形成
①类型:
点缺陷包括空位、间隙原子和置换原子等三类,其中间隙原子又 可分为同类间隙原子和异类间隙原子。 ②空位的形成: 原子由于热激活而离开其平衡位置。 ③空位的种类:
肖特基(Schottky)空位: 原子迁移到晶体表面所形成的空位。 弗兰克尔(Frankel)空位:原子迁移到晶体点阵的间隙中所形成 的空位。
材料科学基础2复习题及参考答案

材料科学基础2复习题及部分参考答案一、名词解释1、再结晶:指经冷变形的金属在足够高的温度下加热时,通过新晶粒的形核及长大,以无畸变的等轴晶粒取代变形晶粒的过程。
2、交滑移:在晶体中,出现两个或多个滑移面沿着某个共同的滑移方向同时或交替滑移。
3、冷拉:在常温条件下,以超过原来屈服点强度的拉应力,强行拉伸聚合物,使其产生塑性变形以达到提高其屈服点强度和节约材料为目的。
(《笔记》聚合物拉伸时出现的细颈伸展过程。
)4、位错:指晶体材料的一种内部微观缺陷,即原子的局部不规则排列(晶体学缺陷)。
(《书》晶体中某处一列或者若干列原子发生了有规律的错排现象)5、柯氏气团:金属内部存在的大量位错线,在刃型位错线附近经常会吸附大量的异类溶质原子(大小不同吸附的位置有差别),形成所谓的“柯氏气团”。
(《书》溶质原子与位错弹性交互作用的结果,使溶质原子趋于聚集在位错周围,以减小畸变,降低体系的能量,使体系更加稳定。
)6、位错密度:单位体积晶体中所含的位错线的总长度或晶体中穿过单位截面面积的位错线数目。
7、二次再结晶:晶粒的不均匀长大就好像在再结晶后均匀、细小的等轴晶粒中又重新发生了再结晶。
8、滑移的临界分切应力:滑移系开动所需要的最小分切应力。
(《书》晶体开始滑移时,滑移方向上的分切应力。
)9、加工硬化:金属材料在再结晶温度以下塑性变形时强度和硬度升高,而塑性和韧性降低的现象,又称冷作硬化。
(《书》随塑性变形的增大,塑性变形抗力不断增加的现象。
)10、热加工:金属铸造、热扎、锻造、焊接和金属热处理等工艺的总称。
(《书》使金属在再结晶温度以上发生加工变形的工艺。
)11、柏氏矢量:是描述位错实质的重要物理量。
反映出柏氏回路包含的位错所引起点阵畸变的总积累。
(《书》揭示位错本质并描述位错行为的矢量。
)反映由位错引起的点阵畸变大小的物理量。
12、多滑移:晶体的滑移在两组或者更多的滑移面(系)上同时进行或者交替进行。
13、堆垛层错:晶体结构层正常的周期性重复堆垛顺序在某二层间出现了错误,从而导致的沿该层间平面(称为层错面)两侧附近原子的错排的一种面缺陷。
缺陷化学在材料中的应用

缺陷化学在材料中的应用班级:粉体(2)班姓名:梁家胜学号: 1203012037成绩:摘要:缺陷化学是无机固体化学的一个分支,是研究固态晶体中的缺陷对物料的物化特性影响的学科。
缺陷的类型及其在新材料制备中的作用及通过分析固溶体和非化学计量化合物缺陷对材料物理化学性能的影响,说明缺陷化学是一种研究新型功能材料的有力手段,利用缺陷化学在新材料中的应用可能取得的重大突破及新的研究热点。
关键词:缺陷、点缺陷、材料、缺陷化学正文:现代科技尤其是空间、激光、能源与电子等尖端技术的发展,对各自的材料都提出了许多新的要求,如耐高低温、抗腐蚀、防老化、高强度、韧性好,以及对热、光、电、磁、声、记忆等具有特别的功能。
在满足这些特殊要求方面,缺陷化学日益显示出其理论意义和实际意义。
缺陷化学的实践基础,是固态晶体中普遍存在着“缺陷”。
按现传化学的观点分析,固态晶体中的分子、原子及离子等结晶质点,在晶格中的排列并不都是有序的,总存在着某些不完整性,即缺陷。
如此的晶体缺陷,会诱发出许多令科技工作者感兴趣的现象。
例如,固相间的扩散速度会加快;固相反应物的化学活性会提高;对电、磁、光等表现出某些特别的性能;可逆性及延展性良好等。
固态晶体中的缺陷分类有:点缺陷、线缺陷、面缺陷与体缺陷。
1.点缺陷点缺陷的产生,是由于晶格中的某些晶点(零维空间),没有被理论上应为它占据的分子、原子或离子听占有,出现空位或被杂质所占据的情况。
当然也可能出现部分晶点空着、部分晶点为杂质所占有的情况。
2.线缺陷线缺陷又称差排,即晶体晶格中的某排或某些排(一维空间)的分子、原子或离子等结晶质点,未按正常的理论规律进行排列,呈现出“错排”现象,线缺陷在晶体中并不罕见。
3.面缺陷所有的固态晶体都具有自由表面,这里是指晶体与真空或气体的相接触部分。
同时,自由表面也包括晶体内部的开孔孔隙、闭孔孔隙及裂缝的内自由表面晶体自由表面处的结晶质点,其配位数较晶体内部的少,不规则性也较晶体内部大,致使晶体表面的能级比晶体内部的高。
材料科学基础课后习题及答案

第二章答案2-1略。
2-2〔1〕一晶面在x、y、z轴上的截距分别为2a、3b、6c,求该晶面的晶面指数;〔2〕一晶面在x、y、z轴上的截距分别为a/3、b/2、c,求出该晶面的晶面指数。
答:〔1〕h:k:l==3:2:1,∴该晶面的晶面指数为〔321〕;〔2〕h:k:l=3:2:1,∴该晶面的晶面指数为〔321〕。
2-3在立方晶系晶胞中画出以下晶面指数和晶向指数:〔001〕与[],〔111〕与[],〔〕与[111],〔〕与[236],〔257〕与[],〔123〕与[],〔102〕,〔〕,〔〕,[110],[],[]答:2-4定性描述晶体构造的参量有哪些.定量描述晶体构造的参量又有哪些.答:定性:对称轴、对称中心、晶系、点阵。
定量:晶胞参数。
2-5依据结合力的本质不同,晶体中的键合作用分为哪几类.其特点是什么.答:晶体中的键合作用可分为离子键、共价键、金属键、范德华键和氢键。
离子键的特点是没有方向性和饱和性,结合力很大。
共价键的特点是具有方向性和饱和性,结合力也很大。
金属键是没有方向性和饱和性的的共价键,结合力是离子间的静电库仑力。
范德华键是通过分子力而产生的键合,分子力很弱。
氢键是两个电负性较大的原子相结合形成的键,具有饱和性。
2-6等径球最严密堆积的空隙有哪两种.一个球的周围有多少个四面体空隙、多少个八面体空隙.答:等径球最严密堆积有六方和面心立方严密堆积两种,一个球的周围有8个四面体空隙、6个八面体空隙。
2-7n个等径球作最严密堆积时可形成多少个四面体空隙、多少个八面体空隙.不等径球是如何进展堆积的.答:n个等径球作最严密堆积时可形成n个八面体空隙、2n个四面体空隙。
不等径球体进展严密堆积时,可以看成由大球按等径球体严密堆积后,小球按其大小分别填充到其空隙中,稍大的小球填充八面体空隙,稍小的小球填充四面体空隙,形成不等径球体严密堆积。
2-8写出面心立方格子的单位平行六面体上所有结点的坐标。
答:面心立方格子的单位平行六面体上所有结点为:〔000〕、〔001〕〔100〕〔101〕〔110〕〔010〕〔011〕〔111〕〔0〕〔0〕〔0〕〔1〕〔1〕〔1〕。
石德珂《材料科学基础》(第2版)配套题库【章节题库】第4章~第6章【圣才出品】

几何条件: 能量条件:
b
b
a [111]
前
后
b
2
2 a2
3b2 1 a2
前3
后3
几何条件和能量条件均满足。
7.一个 b=a/2
的螺位错在(111)面上运动。若在运动过程中遇到障碍物而发
生交滑移,请写出交滑移系统。
答:所有包含螺位错方向的面都是滑移面,对于 FCC 晶体滑移面(111)来说,只有
a)位错环及所受应力状况;b)位错环的平衡形状 图 4-2
答:位错环的平衡形状如图 4-2(b)所示。
6.若面心立方晶体中有 b= a [101]的单位位错及 b= a [121]的不全位错,此二位
2
6
错相遇能否进行位错反应?为什么?
答:能够发生反应。
4 / 69
圣才电子书 十万种考研考证电子书、题库视频学习平台
4.请说明什么是全位错和不全位错,并请写出 FCC、BCC 和 HCP 晶体中的最短单位 位错的柏氏矢量。
3 / 69
圣才电子书 十万种考研考证电子书、题库视频学习平台
答:全位错是指柏氏矢量等于点阵矢量的整数倍。 不全位错是指柏氏矢量不等于点阵矢量的滑移面上,正方形的两 边分别沿 x 和 y 轴,柏氏矢量沿 z 轴。如果位错环只能滑移,示意画出在以下两种应力分布 情况下位错环的平衡形状:
【答案】√
十万种考研考证电子书、题库视频学习平台
【解析】书写缺陷方程时要注意:(1)缺陷所带电荷的确定;(2)保持位置关系比例
不变。
2.非化学计量化合物结构缺陷也是一种杂质缺陷。( ) 【答案】× 【解析】非化学计量化合物是指有些化合物,其化学组成会明显的随着周围气氛的性质 和压力的大小的变化而发生组成偏离化学计量的现象,而非化学计量化合物结构缺陷正是由 此而产生的缺陷。
厦门大学 材料科学基础(二) 第四章-2 缺陷化学 点缺陷的类型及表示方法

杂质缺陷
杂质缺陷是指由外来杂质原子(离子)而引 入的各种缺陷
杂质缺陷 (a)置换型;(b)填Байду номын сангаас型
杂质原子(离子)可以使原有晶体的晶格 发生局部畸变
晶格畸变的几种情况 (a)、(b)置换型;(c)填隙型;(d)产生空位
电子缺陷和带电缺陷
电子和空穴在它们的附 近形成了一个附加的电 场,引起了周期势场的 畸变,造成了晶体的不 完整性。
电子缺陷和带电缺陷
弗仑克尔缺陷
在晶格热振动时,一些能量足够大 的原子离开平衡位置后,挤到晶格 间隙位置,成为填隙原子,而在原 来的位置上留下一个空位,这种缺 陷称为弗仑克尔缺陷。
氯化钠的晶体结构
萤石(CaF2)型结构
[CaF8] 和[FCa4]多面体图
肖特基缺陷
肖特基缺陷:正常结点上的原子/离 子,在能量起伏过程中获得足够的 能量后,离开平衡位置迁移到晶体 表面正常结点位置,在原来的位置 上留下空位。 一般在结构比较紧密,没有较大空 隙的晶体中或在阴、阳离子半径相 差较小的晶体中比较容易形成肖特 基缺陷。 肖特基缺陷
空位
杂质质点
由于外来杂质原子(或离子)进入晶格而产生。
根据缺陷产生的原因分类
热缺陷
处在晶格结点上的原子,由于热振动的能量起伏,有一部 分会离开正常位置,而造成的缺陷。 热缺陷是材料固有的缺陷,是本征缺陷的主要形式。根据 缺陷所处的位置,又分为弗仑克尔缺陷和肖特基缺陷。
杂质缺陷
4.7点缺陷和缺陷反应的表示
克罗格-明克(Kroger-Vink)符号
所带有效电荷 缺陷名称 在晶体中的位置
空位缺陷:用V表示。VM Vx VNa VCl 填隙原子:角标i表示间隙位置。Mi Xi Nai Cli 错位原子:Mx表示M原子被错放到X位置上。KNa 取代原子:LM表示L处在M的位置上,Li表示L处在间隙 位置上。CaMg
(完整版)厦大材料科学基础知识点总结.doc

第一章原子结构和键合原子中一个电子的空间和能量的描述(1)主量子数 ni:决定原子中电子能量和核间平均距离,即量子壳层,取正整数 K、L 、M 、N、O、 P、Q(2)轨道动量量子数 li :给出电子在同一量子壳层内所处的能级(电子亚层),与电子运动的角动量有关, s, p,d, f(3)磁量子数 mi:给出每个轨道角动量数或轨道数,决定原子轨道或子云在空间的伸展方向(4)自旋角动量量子数 si:表示电子自旋的方向,取值为 +1/2 或 -1/2 核外电子的排布规律(1)能量最低原理:电子总是占据能量最低的壳层,使体系的能量最低。
而在同一电子层,电子依次按 s,p,d,f 的次序排列。
(2)Pauli 不相容原理:在一个原子中不可能有运动状态完全一样的两个电子。
因此,主量子数为 n 的壳层,最多容纳2n2 电子。
(3)Hund 原则:在同一个亚能级中的各个能级中,电子的排布尽可能分占不同的能级,而且自旋方向相同。
原子间的键(见作业)第二章固体结构晶体结构的基本特征:原子(或分子、离子)在三维空间呈周期性重复排列。
即存在长程有序。
性能上两大特点:( 1)固定的熔点;( 2)各向异性空间点阵的概念将晶体中原子或原子团抽象为纯几何点(阵点)即可得到一个由无数几何点在三维空间排列成规则的阵列—空间点阵特征:每个阵点在空间分布必须具有完全相同的周围环境晶胞:代表性的基本单元(最小平行六面体)选取晶胞的原则:Ⅰ)选取的平行六面体应与宏观晶体具有同样的对称性;Ⅱ)平行六面体内的棱和角相等的数目应最多;Ⅲ)当平行六面体的棱角存在直角时,直角的数目应最多;Ⅳ)在满足上条件,晶胞应具有最小的体积。
晶体结构与空间点阵的区别:空间点阵是晶体中质点的几何学抽象,用以描述和分析晶体结构的周期性和对称性,由于各点阵的周围环境相同,只有14 种。
晶体是指晶体中实际质点(原子、离子和分子)的具体排列情况,它们能组成各种类型的排列,因此,实际存在的晶体结构是无限的。
厦门大学 材料科学基础(二) 第四章-1 缺陷化学ppt课件

克罗格和明克总结出了一套点缺陷的表示符号。
20世纪80年代
超导氧化物的研究。
7
4.5 缺陷化学的研究对象和内容
研究对象
点缺陷。包括点阵结点,空位、间隙原子、杂质原子导 带中的电子和价带中的电子空穴等。不包括声子和激子。
研究内容
点缺陷的生成、点缺陷的平衡、点缺陷之间的反应、点 缺陷的存在所引起的固体中载流子(电子和空穴)的变 化,点缺陷对固体性质的影响以及如何控制固体中点缺 陷的种类和浓度等。
质点进行热振动
➢ 产生声子和激子等
质点脱离其平衡位置
➢ 产生空位和填隙质点
外来杂质进入晶格
2
晶体结构中的缺陷对晶体物理化学性质的影响
半导体的导电性 晶体的颜色 固体的强度 扩散过程
3
4.2 点缺陷的热力学分析
S=klnW S:构型熵 k: 波尔兹曼常数 W:几率,正比于 1023
8
20世纪30年代
色心理论的提出 杂质缺陷的研究
20世纪40年代
半导体晶体管的发明对缺陷化学的促进。
6
20世纪60年代
克罗格(Kroger)和明克(Vink)采用了一种分区近似的 方法,首次求解得到晶体PbS中各类点缺陷的浓度以及 缺陷浓度随平衡气相分压变化曲线。采用化学理论(化 学反应平衡常数方程和质量作用定律)研究晶体缺陷获 得成功。
面缺陷
在二维方向上伸展的缺陷。例如,晶界。
体缺陷
三维尺寸上都比较大的缺陷。例如,杂质团聚体和空洞 。
5
4.4 缺陷化学的发展历史
缺陷化学:从理论上定性定量地把材料中的点缺 陷看作化学实物,并用化学的原理来研究缺陷的 产生、平衡尔缺陷模型;瓦格纳和肖脱基提 出了肖脱基缺陷模型。
材料科学基础课后习题答案

《材料科学基础》课后习题答案第一章材料结构的基本知识4. 简述一次键和二次键区别答:根据结合力的强弱可把结合键分成一次键和二次键两大类。
其中一次键的结合力较强,包括离子键、共价键和金属键。
一次键的三种结合方式都是依靠外壳层电子转移或共享以形成稳定的电子壳层,从而使原子间相互结合起来。
二次键的结合力较弱,包括范德瓦耳斯键和氢键。
二次键是一种在原子和分子之间,由诱导或永久电偶相互作用而产生的一种副键。
6. 为什么金属键结合的固体材料的密度比离子键或共价键固体为高?答:材料的密度与结合键类型有关。
一般金属键结合的固体材料的高密度有两个原因:(1)金属元素有较高的相对原子质量;(2)金属键的结合方式没有方向性,因此金属原子总是趋于密集排列。
相反,对于离子键或共价键结合的材料,原子排列不可能很致密。
共价键结合时,相邻原子的个数要受到共价键数目的限制;离子键结合时,则要满足正、负离子间电荷平衡的要求,它们的相邻原子数都不如金属多,因此离子键或共价键结合的材料密度较低。
9. 什么是单相组织?什么是两相组织?以它们为例说明显微组织的含义以及显微组织对性能的影响。
答:单相组织,顾名思义是具有单一相的组织。
即所有晶粒的化学组成相同,晶体结构也相同。
两相组织是指具有两相的组织。
单相组织特征的主要有晶粒尺寸及形状。
晶粒尺寸对材料性能有重要的影响,细化晶粒可以明显地提高材料的强度,改善材料的塑性和韧性。
单相组织中,根据各方向生长条件的不同,会生成等轴晶和柱状晶。
等轴晶的材料各方向上性能接近,而柱状晶则在各个方向上表现出性能的差异。
对于两相组织,如果两个相的晶粒尺度相当,两者均匀地交替分布,此时合金的力学性能取决于两个相或者两种相或两种组织组成物的相对量及各自的性能。
如果两个相的晶粒尺度相差甚远,其中尺寸较细的相以球状、点状、片状或针状等形态弥散地分布于另一相晶粒的基体内。
如果弥散相的硬度明显高于基体相,则将显著提高材料的强度,同时降低材料的塑韧性。
厦大材料科学基础知识点总结

第一章原子结构和键合原子中一个电子的空间和能量的描述(1)主量子数ni:决定原子中电子能量和核间平均距离,即量子壳层,取正整数K、L、M、N、O、P、Q(2)轨道动量量子数li:给出电子在同一量子壳层内所处的能级(电子亚层),与电子运动的角动量有关,s,p,d,f(3)磁量子数mi:给出每个轨道角动量数或轨道数,决定原子轨道或子云在空间的伸展方向(4)自旋角动量量子数si:表示电子自旋的方向,取值为+1/2 或-1/2核外电子的排布规律(1)能量最低原理:电子总是占据能量最低的壳层,使体系的能量最低。
而在同一电子层,电子依次按s,p,d,f的次序排列。
(2)Pauli不相容原理:在一个原子中不可能有运动状态完全一样的两个电子。
因此,主量子数为n的壳层,最多容纳2n2电子。
(3)Hund原则:在同一个亚能级中的各个能级中,电子的排布尽可能分占不同的能级,而且自旋方向相同。
原子间的键(见作业)第二章固体结构晶体结构的基本特征:原子(或分子、离子)在三维空间呈周期性重复排列。
即存在长程有序。
性能上两大特点:(1)固定的熔点;(2)各向异性空间点阵的概念将晶体中原子或原子团抽象为纯几何点(阵点)即可得到一个由无数几何点在三维空间排列成规则的阵列—空间点阵特征:每个阵点在空间分布必须具有完全相同的周围环境晶胞:代表性的基本单元(最小平行六面体)选取晶胞的原则:Ⅰ)选取的平行六面体应与宏观晶体具有同样的对称性;Ⅱ)平行六面体内的棱和角相等的数目应最多;Ⅲ)当平行六面体的棱角存在直角时,直角的数目应最多;Ⅳ)在满足上条件,晶胞应具有最小的体积。
晶体结构与空间点阵的区别:空间点阵是晶体中质点的几何学抽象,用以描述和分析晶体结构的周期性和对称性,由于各点阵的周围环境相同,只有14种。
晶体是指晶体中实际质点(原子、离子和分子)的具体排列情况,它们能组成各种类型的排列,因此,实际存在的晶体结构是无限的。
晶带所有相交于某一晶向直线或平行于此直线的晶面构成一个“晶带”。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
线缺陷
面缺陷
在二维方向上伸展的缺陷。例如,晶界。
三维尺寸上都比较大的缺陷。例如,杂质团聚体和空洞 。
体缺陷
4.4 缺陷化学的发展历史
缺陷化学:从理论上定性定量地把材料中的点缺 陷看作化学实物,并用化学的原理来研究缺陷的 产生、平衡及其浓度等问题的一门学科。
20世纪20年代
弗伦克尔提出了弗伦克尔缺陷模型;瓦格纳和肖脱基提
缺陷的存在所引起的固体中载流子(电子和空穴)的变 化,点缺陷对固体性质的影响以及如何控制固体中点缺 陷的种类和浓度等。
在一定浓度范围内,缺陷的生 成会导致系统吉布斯自由能的 下降。
在完整点阵结构的晶体中引入缺陷后能量的变化
4.3 缺陷的分类
根据缺陷的大小、形状和作用范围分类
点缺陷
在三维方向上尺度都很小的缺陷。例如,空位、间隙原子、 杂质原子等。 在一维方向上的缺陷,其它二维方向上尺度都很小。线缺 陷又称位错。
第四章 缺陷化学
4.1 理想晶体和实际晶体
对于理想晶体,其内部质点在三维空间严格按照空间格
子规律作周期性重复排列 ,而实际晶体总有原子或离 子并不按理想点阵排列,偏离了自,实际晶体总是或多或 少地存在着各式各样的缺陷。
对理想结构的偏离 质点进行热振动
20世纪70年代
克罗格和明克总结出了一套点缺陷的表示符号。
20世纪80年代
超导氧化物的研究。
4.5 缺陷化学的研究对象和内容
研究对象
点缺陷。包括点阵结点,空位、间隙原子、杂质原子导
带中的电子和价带中的电子空穴等。不包括声子和激子。
研究内容
点缺陷的生成、点缺陷的平衡、点缺陷之间的反应、点
出了肖脱基缺陷模型。
20世纪30年代
色心理论的提出 杂质缺陷的研究
20世纪40年代
半导体晶体管的发明对缺陷化学的促进。
20世纪60年代
克罗格(Kroger)和明克(Vink)采用了一种分区近似的
方法,首次求解得到晶体PbS中各类点缺陷的浓度以及 缺陷浓度随平衡气相分压变化曲线。采用化学理论(化 学反应平衡常数方程和质量作用定律)研究晶体缺陷获 得成功。
产生声子和激子等 产生空位和填隙质点
质点脱离其平衡位置
外来杂质进入晶格
晶体结构中的缺陷对晶体物理化学性质的影响 半导体的导电性 晶体的颜色 固体的强度 扩散过程
4.2 点缺陷的热力学分析
S=klnW S:构型熵 k: 波尔兹曼常数 W:几率,正比于 1023
G=H-TS
