考马斯亮蓝法测定蛋白质浓度Word版
考马斯亮蓝法测蛋白质含量

标准曲线制作—考马斯亮蓝法测卵白质含量之迟辟智美创作一、标准曲线一般用分光光度法测物质的含量,先要制作标准曲线,然后根据标准曲线查出所测物质的含量.因此,制作标准曲线是生物检测分析的一项基本技术.二、卵白质含量测定方法1、凯氏定氮法2、双缩脲法3、Folin-酚试剂法4、紫外吸收法5、考马斯亮蓝法三、考马斯亮蓝法测定卵白质含量—标准曲线制作(一)、试剂:1、考马斯亮蓝试剂:考马斯亮蓝G—250 100mg溶于50ml 95%乙醇,加入100ml 85% H3PO4,用蒸馏水稀释至1000ml,滤纸过滤.最终试剂中含0.01%(W/V)考马斯亮蓝G—250,4.7%(W/V)乙醇,8.5%(W/V)H3PO4.2、标准卵白质溶液:纯的牛血清血卵白,预先经微量凯氏定氮法测定卵白氮含量,根据其纯度同0.15mol/LNaCl配制成100ug/ml卵白溶液.(二)、器材:1、722S型分光光度计使用及原理().2、移液管使用().(三)、标准曲线制作:1、10ug、20 个点为ug、30 ug、40 ug、50 ug、60 ug),在坐标轴上绘制标准曲线.1)、利用标准曲线查出回归方程.2)、用公式计算回归方程.3)、或用origin作图,测出回归线性方程.即A595nm=a×X( )+6一般相关系数应过0.999以上,至少2个9以上.4)、绘图时近两使点在一条直线上,在直线上的点应该在直线两侧.(四)、卵白质含量的测定:样品即所测卵白质含量样品(含量应处置在所测范围内),依照把持步伐1把持,测出样品的A595nm,然后利用标准曲线或回归方程求出样品卵白质含量.一般被测样品的A595nm值在0.1—0.05之间,所以上述样品如果A595nm值太年夜,可以稀释后再测A595nm 值,然后再计算.(五)、注意事项:1、玻璃仪器要洗涤干净.2、取量要准确.3、玻璃仪器要干燥,防止温度变动.4、对比:用被测物质以外的物质作空白对比.药品的配制(磷酸缓冲液的配制)一、药品的配制步伐(一)、实验准备:1、准备所需的药品和玻璃仪器.2、洗涤.(怎样洗涤算干净?)(二)、计算:1、百分比浓度计算:1)、G/V比例如配1% NaCl,称1g NaCl溶于100ml 水.2)、V/V比:例如配75%乙醇100ml,75%×100%=100%×X, X=75ml.取75ml无水乙醇,加25ml蒸馏水.乙醇:乙醚:丙酮=2:1:2配500ml,各取200 ml,100ml,200 ml混合.3)G/V比:用的较少,如计算灰分中某种元素如Fe的含量.2、摩尔浓度计算:注:药品的分子量一般在标签中注明. 1)、0.1M或0.1mol/L NaCl配100ml.M=质量/体积(L)称取NaCl0.1×0.1×40=0.4g 摩尔数=G (g)/摩尔质量毫摩尔数=G(mg)/摩尔质量微摩尔数=G(ug)/摩尔质量称取NaCl0.1×0.1×40=0.4ug 3、混合溶液配制的计算:如配3uMEDTA,2.25mM NBT以及60uM 溶液100ml,用50mM磷酸缓冲液配制.注意:1、分别标定体积计算2、分别配制再混合,但总体积不能为100ml (三)、标量:1、根据需要选择分歧量程的天平根据要求去分歧精度的丈量器,如量筒或移液管.2、电子分析天平的使用.(四)、溶解:1、根据药品配置要求选择溶剂.蒸馏水,双蒸水,无离子水等.2、只能用烧杯溶解.注意加入溶剂只能加入总体积的2/3左右,剩余溶剂洗涤烧杯三次左右,直到洗涤干净.小知识:药品标签中一般标识有药品的溶解性能和分子式,可根据分子式和所学的知识判断药品的结构和性质特点(包括溶解性质).如酸碱两性物质的配制(AA、卵白质、核苷酸等)如果溶解性能欠好可以用稀酸或稀碱增进溶解,但pH应在被要求的范围内.3、加热增进溶解,但注意应在配制的范围内有的药品还需水溶加热较好.如:配0.1%的淀粉,水裕加热(温度在80-90.C),过量会糊化.(五)、定容:1、用容量瓶定容;2、用玻璃棒引流或用小漏斗;3、用溶剂加入到接近刻度,然后用滴管加入到刻度.要求刻度与液体凹面相切为止(眼睛可视);4、上下窑洞容量瓶几次,混合均匀即可.(注意不再定容了,防止溶液漏失落.)(六)、装入试剂瓶,贴上标签.标签应注明以下内容:药品浓度、名称、配制人、配制日期等.(七)、清理实验场所.二、磷酸缓冲液的配制.(一)、配制0.2mol/L即0.2M pH=6.8的磷酸缓冲液.用磷酸氢二钠—磷酸二氢钠做缓冲液.选用药品:Na2HPO4·12H2O(碱)和NaH2PO4·12H2O (酸)配缓冲液100ml.书中说明.(二)、计算:1、注:书中有注明配置的量.2、含有分歧结晶水的换算.书中配1/15mol/L的缓冲液配1L,书中用Na2HPO4·2H2O 需要11.87g/L但用Na2HPO4·12H2O需几多g?11.87=(178/358)×X,X=23.87g.(三)、分别配制缓冲液各100ml(根据需要确定配制的量).即:0.2M Na2HPO4·2H2O和NaH2PO4·2H2O100ml.(四)、按书中的量配制取量再混合.如:pH=6.8,分别去缓冲对49ml和51ml.(五)、用pH试纸ceni索赔的缓冲液的pH值,检测配置是否准确.(六)如配50mM pH =6.8的缓冲液100ml ,以你配制的母液稀释即可.计算:50×0.1=0.2×1000×X (L);X =0.025L;取0.2M pH=7.2的缓冲液25ml,用蒸馏水定容至100ml即可.。
实验一蛋白质含量测定考马斯亮蓝染色法

制作标准曲线:
编号
1 (空白)
2
3 4 5 6 7 样品
标准蛋白 (ml)
0.0
水
0.5
(ml)
0.1 0.15 0.2 0.3 0.4 0.5 0.5ml
0.4 0.35 0.3 0.2 0.1 0.0
浓度 (mg/ml)
0.0
0.05 0.075 0.1 0. 15 0.2 0.25
实验一蛋白质含量测定考马斯亮蓝染 色法
(3)紫外吸收法:
蛋白质中Trp,Phe,Tyr的残基中的苯环含有共 轭双键,吸收高峰在280nm处,所以蛋白质具有吸收 紫外光的性质,并且蛋白质溶液的光吸收值与其含 量成正比,可用作定量测定。
简单、灵敏、快速、不耗样品,低浓度的盐类不干 扰。
实验一蛋白质含量测定考马斯亮蓝染 色法
度最大处所对应的波长称为最大光吸收处。
同一种物质不同浓度的吸光度,在某一定波长下有差异, 在最大光吸收处吸光度的差异最大。这是分光光度法 进行物质定量分析的重要依据。
I0:表示入射光强度,It :表示光线通过溶液后的强度。
实验一蛋白质含量测定考马斯亮蓝染 色法
A=lg(I0/It)=-lgT=εb c
实验一蛋白质含量测定考马斯亮蓝染 色法
⑶吸收池
吸收池(即比色杯):用来盛装被测试的溶液。 光学比色杯和石英比色杯两种。
光学比色杯适用波长范围是400nm~2000nm ,只能 用于可见光。
石英比色杯可透过紫外光、可见光和红外光, 是 最 常 使 用 的 吸 收 池 , 使 用 波 长 范 围 是 180nm ~ 3000nm。
(2)T—透光度:描述入射光透过溶液的程度; (3)ε—摩尔吸光系数(是溶液的特征常数),在数值 上等于浓度为1mol/L、液层厚度为1cm时该溶液在 某一波长下的吸光度;单位mol·L-1; (4)b—样品光程(cm),通常使用1.0cm 的吸收 地,b=1cm (5)C—样品浓度(mol/L) 由上式可以看出:吸光度OD与物质的浓度“C”和溶 液吸光的厚度成正比。
蛋白质浓度的测定(考马斯亮蓝法)

生物 w.ebio Coomassie Dye-Based 蛋白质定量 易 ww O CH2CH3
另外,还要注意,玻璃仪器要洗涤干净并保持干燥,避免温度变化;取量要 准确;分光光度计十分灵敏,测定时要认真仔细。
五、问题与思考 1.为何制作蛋白质标准曲线? 2.酶活的一般定义?在提取过程,为何要测定蛋白质浓度?
易生物-领先的生物医药商务平台
四、注意事项: (一)蛋白质与考马斯亮蓝 G-250 结合的反应十分迅速,在 2min 左右反应达到
m 平衡;其结合物在室温下 1h 内基本稳定。如果测定要求很严格,可以在试剂加 o 入后的 5-20min 内测定光吸收,因为在这段时间内颜色是最稳定的。 .c (二)测定中,蛋白-染料复合物会有少部分吸附于比色杯壁上,实验证明此复 e 合物的吸附量是可以忽略的。测定完后可用乙醇将蓝色的比色杯洗干净。
制作标准曲线,然后根据标准曲线查出所测物质的含量。考马斯亮蓝法测定蛋白质浓度,是
利用蛋白质―染料结合的原理,定量的测定微量蛋白浓度的快速、灵敏的方法。考马斯亮蓝
G-250 存在着两种不同的颜色形式,红色和蓝色。它和蛋白质通过范德华力结合,在一定
蛋白质浓度范围内,蛋白质和染料结合符合比尔定律(Beer’s law)。此染料与蛋白质结合 后颜色有红色形式和蓝色形式,最大光吸收由 465nm 变成 595nm,通过测定 595nm 吸光医药商务平台
生物秀-专心做生物!
蛋白质含量的测定考马斯亮蓝染色法

1 2
洗涤
用洗涤液洗涤染色后的蛋白质样品,去除多余的 染料。
测量
使用分光光度计测量蛋白质样品的吸光度值。
3
结果计算
根据标准曲线和吸光度值计算蛋白质含量。
04
结果分析
数据记录与整理
数据记录
在实验过程中,应详细记录每个实验 组的吸光度值,包括空白对照组。
数据整理
将实验数据整理成表格,包括实验组 别、吸光度值以及相应的波长等。
VS
药物研发
在药物研发过程中,考马斯亮蓝染色法可 用于评估药物对蛋白质表达的影响,为新 药研发提供实验依据。
未来发展方向与挑战
技术优化
随着科学技术的不断发展,考马斯亮蓝染色法需要不断优化和完善, 以提高检测的灵敏度和特异性。
应用领域拓展
随着蛋白质组学研究的深入,考马斯亮蓝染色法的应用领域将进一 步拓展,为生命科学和医学研究提供更多支持。
蓝色与黄色
考马斯亮蓝染色后呈蓝色,与未结合蛋白质的黄色形成鲜明对比,便于观察和 检测。
颜色深浅与浓度正相关
随着蛋白质浓度的增加,染色后样品的颜色逐渐加深,通过比色法可测定出不 同浓度下的光密度值,进而计算出蛋白质浓度。
03
实验步骤
样品准备
样品收集
蛋白质提取
选择具有代表性的样品,确保样品新 鲜、无污染。
05
应用与展望
在生物学领域的应用
蛋白质表达分析
考马斯亮蓝染色法常用于检测细胞或组织中蛋白质的表达水平,有助于研究生物体的生 理和病理过程。
蛋白质分离与鉴定
通过考马斯亮蓝染色法对蛋白质进行染色,可以方便地对蛋白质进行分离和鉴定,为蛋 白质组学研究提供技术支持。
在医学领域的应用
(完整word版)考马斯亮蓝法测定蛋白质含量流程

考马斯亮蓝法测定蛋白质含量流程:该方法用于大多数蛋白质的定量是比较精确的,但不适用于小分子碱性多肽的定量。
如核糖核酸酶或溶菌酶。
去污剂的浓度超过0.2%影响测定结果。
如TritonX-100、SDS、NP-40等。
1.Bradford浓染液的配制:将100mg考马斯亮蓝G-250溶于50ml 95%乙醇,加入100ml85%的磷酸,然后,用蒸馏水补充至1000ml,此染液放4℃至少6个月保持稳定。
2.标准曲线蛋白质样本的准备:尽量使用与待测样本性质相近的蛋白质作为标准品,例如测定抗体,可用纯化的抗体作为标准。
如果待测样本是未知的,也可用抗体作为标准蛋白。
通常在20ug—150ug/100ul之间绘制标准曲线。
3.将待测样本溶于缓冲溶液中,该缓冲溶液应与制作标准曲线的缓冲溶液相同(最好用PBS)。
4.按1:5用蒸馏水稀释浓染料结合溶液,如出现沉淀,过滤除去。
5.每个样本加5ml稀释的染料结合溶液,作用5~30min。
染液与蛋白质结合后,将由红色变为蓝色,在595nm波长下测定其吸光度。
注意,显色反应不得超过30min.6.根据标准曲线计算待测样本的浓度。
注意:考马斯亮蓝和皮肤中蛋白质通过范德华力结合,反应快速,并且稳定,无法用普通试剂洗掉。
待一两周左右,皮屑细胞自然衰老脱落即可无碍。
适用范围考马斯亮蓝显色法的基本原理是根据蛋白质可与考马斯亮蓝G-250 定量结合。
当考马斯亮蓝G-250 与蛋白质结合后,其对可见光的最大吸收峰从465nm 变为595nm。
在考马斯亮蓝G-250 过量且浓度恒定的情况下,当溶液中的蛋白质浓度不同时,就会有不同量的考马斯亮蓝G-250 从吸收峰为465nm 的形式转变成吸收峰为595nm 的形式,而且这种转变有一定的数量关系。
一般情况,当溶液中的蛋白质浓度增加时,显色液在595nm 处的吸光度基本能保持线性增加,因此可以用考马斯亮蓝G-250 显色法来测定溶液中蛋白质的含量。
考马斯亮蓝G-250法测定蛋白质含量

蛋白质含量测定(考马斯亮蓝G-250法)一、目的考马斯亮蓝(Coomassie brilliant blue) G-250法是比色法与色素法相结合的复合方法,由Bradford于1976年建立,具有简便快捷,灵敏度高,稳定性好等特点,是一种较好的蛋白质定量测定常用方法。
通过本实验学习应用该法测定蛋白质含量的原理,复习分光光度计的使用及标准曲线的绘制等基本实验技能。
二、原理考马斯亮蓝G-250是一种染料,游离态呈红色,与蛋白质结合后转变为青色。
在0~1000μg 范围内,蛋白质-色素结合物在595 nm下的吸光度与蛋白质含量正相关,可用比色法测定。
三、仪器、试剂和材料1.仪器设备:(具塞刻度)试管吸管分光光度计2.试剂(1) 标准蛋白质溶液称取100 mg牛血清白蛋白,溶于蒸馏水并定容至100 ml,制成 1 mg/ml溶液。
(2) 考马斯亮蓝G-250蛋白试剂称取100 mg考马斯亮蓝G-250,溶于50 ml 95%乙醇中,加入85% (m/v)的磷酸100ml,最后用蒸馏水定容到1000 ml (此溶液在常温下可放置一个月)。
(3) 样品蛋白液(10~100 μg/ml)四、操作步骤1标准蛋白质含量(μg)为横坐标、吸光度为纵坐标,绘出标准曲线。
2.样品中蛋白质含量的测定取2支(具塞)试管,分别准确加入0.l ml样品蛋白液,再各加5 ml考马斯亮蓝G-50试剂,充分混合,放置2min后,以标准曲线0号试管做参比,在595 nm波长下比色,记录吸光度。
五、结果处理根据所测样品提取液的平均吸光度,在标准曲线上查得相应的蛋白质含量(μg/ml)六、思考题1.考马斯亮蓝G-250法测定蛋白质含量的原理是什么?还有哪些蛋白质定量法?2.如何正确使用分光光度计?。
考马斯亮蓝 法测定蛋白质含量

二、Bradford法(一)、原理:考马斯亮蓝G250 ( CBB- G-250)与蛋白质结合后形成蓝色的化合物,在595nm有最大吸收峰,且蓝色的深浅与蛋白浓度成正比。
这是一种快速、准确、重复性好的蛋白质定量方法。
该方法快速、准确、干扰因素少。
CBB- G-250在2分钟内即可完全与蛋白结合,并在2小时内保持稳定,该反应几乎不受钠、钾等阳离子的干扰,更不受蔗糖等碳水化合物的干扰。
但较高浓度的十二烷基硫酸钠(Soldium dodecyl sulfate),Triton X-100等对其有干扰,此影响可通过选择适当的对照品来消除。
(二)器材及试剂1、器材A. 分光光度计B. 微量加样器C. 移液管、试管及试管架D. 坐标纸2. 试剂(1)考马斯亮蓝G-250溶液:称取CBB- G-250 100毫克溶于50 ml 95%(V/V)乙醇溶液中,然后加入100毫升85%(V/V)磷酸,最后加蒸馏水定容至1000毫升。
(2)0.14mol/L 氯化钠溶液(生理盐水)(3)标准蛋白质溶液(0.1mg/ml):精确称取10.0毫克牛血清白蛋白,用生理盐水定容至100毫升。
(4) 血清样品(已稀释200倍)(5) 层析样品(三)、操作(标准曲线制作):取7支试管按下表操作:混匀,室温放置5分钟,在595nm测定各管O.D值并以蛋白浓度为横坐标,以O.D 值为纵坐标绘制标准曲线.以Bradford法测定层析分离蛋白内的蛋白浓度取试管从层析样品中各取20.0ul,加入生理盐水20ul,最后加入考马斯亮蓝G-250溶液5.0ml,混匀,以595nm 波长测定二者光密度,在标准曲线上查出其蛋白浓度以上需要购买的试剂有:1、标准蛋白质即牛血清白蛋白。
教学内容:实验八考马斯亮蓝法(Bradford法)测定蛋白质含量【实验目的】1. 掌握考马斯亮蓝染色法定量测定蛋白质的原理与方法2. 熟练分光光度计的使用和操作方法【实验原理】此方法是1976年Bradform建立。
考马斯亮蓝法测蛋白质

考马斯亮蓝法测蛋白质含量一、原理考马斯亮蓝G-250(Coomassie G-250)是一种甲基取代的三苯基甲烷,分子中磺酸基的蓝色染料,在465nm处有最大吸收值。
考马斯亮蓝G-250能与蛋白质通过范得华相互作用形成蛋白质—考马斯亮蓝复合物蓝色溶液,引起该染料的最大吸收λmax的位置发生红移,在595nm处有最大吸收值。
由于蛋白质—考马斯亮蓝复合物在595nm 处的光吸收远高于考马斯亮蓝在465nm处的光吸收,因此,可大大地提高蛋白质的测定灵敏度。
蛋白质—考马斯亮蓝复合物溶液颜色的深浅与蛋白质的浓度成正比。
利用溶液颜色的差异进行比色测定,适合于蛋白质类的定量分析,尤其适合于稀有蛋白质的微量分析。
考马斯亮蓝G-250试剂呈色反应颜色稳定、灵敏度高,最低测试蛋白质量在1ug左右。
二、操作步骤1. 标准曲线测定法分别取六只试管,其中一只加入1.0ml蒸馏水做空白,5只分别加入不同体积的浓度为100ug/ml牛血清清蛋白标准液,补充水到1.0ml。
然后每只试管加入5.0ml考马斯亮蓝G-250试剂,摇匀放置5min,在紫外-可见分光光度计595nm处测定吸光值。
以A595吸光值为纵坐标,牛血清清蛋白的ug数量为横坐标绘制标准曲线。
具体操作见下表。
蛋白质标准曲线测定加样在标准蛋白质测定时,为了减小误差,每一个浓度的蛋白质做3支平行管。
3.试剂配置a.牛血清清蛋白标准液结晶牛血清清蛋白或酪蛋白,预先经微量凯氏定氮法标定该蛋白质的百分含量或者根据牛血清清蛋白的消光系数是 6.6来计算其百分含量。
然后根据该蛋白的纯度配置成浓度为100 ug/ml的蛋白溶液。
b.考马斯亮兰G—250染料试剂:称100mg考马斯亮兰G—250,溶于50ml 95%的乙醇后,再加入100ml 85%的磷酸,用水稀释至1升三、数据及绘图。
考马斯亮蓝染色法测定蛋白质的含量
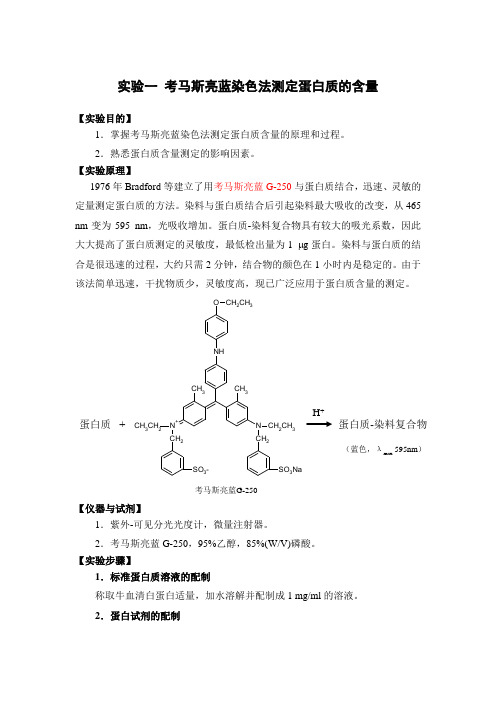
实验一 考马斯亮蓝染色法测定蛋白质的含量【实验目的】1.掌握考马斯亮蓝染色法测定蛋白质含量的原理和过程。
2.熟悉蛋白质含量测定的影响因素。
【实验原理】1976年Bradford 等建立了用考马斯亮蓝G-250与蛋白质结合,迅速、灵敏的定量测定蛋白质的方法。
染料与蛋白质结合后引起染料最大吸收的改变,从465 nm 变为595 nm ,光吸收增加。
蛋白质-染料复合物具有较大的吸光系数,因此大大提高了蛋白质测定的灵敏度,最低检出量为1 g 蛋白。
染料与蛋白质的结合是很迅速的过程,大约只需2分钟,结合物的颜色在1小时内是稳定的。
由于该法简单迅速,干扰物质少,灵敏度高,现已广泛应用于蛋白质含量的测定。
N CH 2CH 3CH 2N +CH 3CH 2CH 2NHCH 3CH 3O CH 2CH 3SO 3-SO 3Na蛋白质+ 蛋白质-染料复合物H +考马斯亮蓝G-250(蓝色,λmax595nm )【仪器与试剂】1.紫外-可见分光光度计,微量注射器。
2.考马斯亮蓝G-250,95%乙醇,85%(W/V)磷酸。
【实验步骤】1.标准蛋白质溶液的配制称取牛血清白蛋白适量,加水溶解并配制成1 mg/ml 的溶液。
2.蛋白试剂的配制称取100 mg考马斯亮蓝G-250,加入95%乙醇50 ml溶解,再加入85%(W/V)磷酸100 ml,将溶液用水稀释至1000 ml。
试剂的终浓度为0.01%考马斯亮蓝G-250,4.7%乙醇和8.5%(W/V)磷酸。
3.标准曲线的制作取标准蛋白质溶液5、10、20、50、100 μl于小试管中,用水稀释至0.1 ml,然后分别加入5 ml蛋白试剂,充分振荡混合,2分钟后于595 nm测定其吸光度值。
以0.1 ml水及5 ml蛋白试剂作为空白对照。
以蛋白浓度为横坐标,吸光度值为纵坐标,绘制标准曲线作为定量依据。
4.样品测定取含10~100 μg蛋白质溶液于小试管中,加水稀释至0.1 ml,然后加入5 ml 蛋白试剂,充分振荡混合,2分钟后于595 nm测定其吸光度值。
考马斯亮蓝染色法测定蛋白质浓度含(_Bradford_法)

反应化合物在595nm处有最大光吸收,化合物颜色 的深浅在一定范围内与蛋白质浓度成正比,,因
此可通过测定595nm处的光吸收值来计算蛋白的含
量。
考马斯亮蓝染色法的优点:
(1)灵敏度高(比Lowry法灵敏4倍),测 其最低蛋白质测量可达1mg。 (2)测定快速,简洁。只需加入一种试剂, 完成一个样品的测定,只需5min左右。 (3)此方法干扰物少 如干扰Lowry法的K+、 Na+、Mg+例子,Tris缓冲液、蔗糖、甘油、
思考题
1.考马斯亮蓝法测定蛋白质含量的原理 是什么? 2.为什么不能用试管刷来清洗比色皿? 3.能否将卫生纸塞入比色皿中吸干余液? 4.为什么最后要用95%的乙醇来润洗比 色皿?
尽管相对于其他方法来说尽管相对于其他方法来说??尽管相对于其他方法来说此法的干扰物较少尽管相对于其他方法来说此法的干扰物较少此法的干扰物较少此法的干扰物较少但但由于每种蛋白质与该染料的结合能力不同由于每种蛋白质与该染料的结合能力不同故故标准品的选择非常重要选择标准品的选择非常重要选择尽可能与待测蛋白尽可能与待测蛋白一致的样品一致的样品做标准能最大限度的提高该方法的做标准能最大限度的提高该方法的准确性
七.补充
蛋白质含量测定方法比较
蛋白质含量测定法,是生物化学研究中最
常用、最基本的分析方法之一。目前常用 的有四种古老的经典方法,即定氮法,双 缩尿法(Biuret法)、Folin-酚试剂法 (Lowry法)和紫外吸收法。另外还有一种 近十年才普遍使用起来的新的测定法,即 考马斯亮蓝法(Bradford法)。其中 Bradford法和Lowry法灵敏度最高,比紫外 吸收法灵敏10~20倍,比Biuret法灵敏100 倍以上。定氮法虽然比较复杂,但较准确, 往往以定氮法测定的蛋白质作为其他方法 的标准蛋白质。
考马斯亮蓝法测蛋白浓度

考马斯亮蓝法(Bradford)测蛋白浓度考马斯亮兰法:一种蛋白定量法具体操作步骤:(一)实验原理双缩脲法(Biuret法)和Folin—酚试剂法(Lowry法)的明显缺点和许多限制,促使科学家们去寻找更好的蛋白质溶液测定的方法。
1976年由Bradford建立的考马斯亮兰法(Bradford法),是根据蛋白质与染料相结合的原理设计的。
这种蛋白质测定法具有超过其他几种方法的突出优点,因而正在得到广泛的应用。
这一方法是目前灵敏度最高的蛋白质测定法。
考马斯亮兰G-250染料,在酸性溶液中与蛋白质结合,使染料的最大吸收峰的位置(lmax),由465nm变为595nm,溶液的颜色也由棕黑色变为兰色。
经研究认为,染料主要是与蛋白质中的碱性氨基酸(特别是精氨酸)和芳香族氨基酸残基相结合。
在595nm下测定的吸光度值A595,与蛋白质浓度成正比。
Bradford法的突出优点是:(1)灵敏度高,据估计比Lowry法约高四倍,其最低蛋白质检测量可达1mg。
这是因为蛋白质与染料结合后产生的颜色变化很大,蛋白质-染料复合物有更高的消光系数,因而光吸收值随蛋白质浓度的变化比Lowry法要大的多。
(2)测定快速、简便,只需加一种试剂。
完成一个样品的测定,只需要5分钟左右。
由于染料与蛋白质结合的过程,大约只要2分钟即可完成,其颜色可以在1小时内保持稳定,且在5分钟至20分钟之间,颜色的稳定性最好。
因而完全不用像Lowry法那样费时和严格地控制时间。
(3)干扰物质少。
如干扰Lowry法的K 、Na 、Mg2 离子、Tris 缓冲液、糖和蔗糖、甘油、巯基乙醇、EDTA等均不干扰此测定法。
此法的缺点是:(1)由于各种蛋白质中的精氨酸和芳香族氨基酸的含量不同,因此Bradford法用于不同蛋白质测定时有较大的偏差,在制作标准曲线时通常选用g—球蛋白为标准蛋白质,以减少这方面的偏差。
(2)仍有一些物质干扰此法的测定,主要的干扰物质有:去污剂、Triton X-100、十二烷基硫酸钠(SDS)和0.1N的NaOH。
考马斯亮蓝法测蛋白质含量实验报告

考马斯亮蓝法测蛋白质含量实验报告考马斯亮蓝法(Bradford assay)是一种常用于测定蛋白质含量的实验方法。
本文将对考马斯亮蓝法进行详细介绍,并展示一个实验报告的范例。
1. 引言蛋白质是生命体中不可或缺的重要分子,因此准确测定蛋白质的含量对于生物学研究至关重要。
考马斯亮蓝法是一种常用的蛋白质测定方法,其原理基于蛋白质与考马斯亮蓝染料之间的非共价结合。
2. 实验目的本实验的目的是利用考马斯亮蓝法测定给定溶液中蛋白质的含量。
3. 实验步骤3.1 准备工作首先,准备好所需的试剂和设备,包括考马斯亮蓝试剂、蛋白质标准品、显微管、离心机等。
3.2 制备标准曲线按照给定的浓度,分别取一系列蛋白质标准品,加入不同的显微管中。
然后,加入适量的考马斯亮蓝试剂,充分混合。
将显微管放入离心机中离心,使液体沉淀。
离心后,取出显微管,观察颜色变化,并使用分光光度计测定吸光度。
3.3 测定待测样品将待测样品加入显微管中,加入适量的考马斯亮蓝试剂,充分混合。
然后,将显微管放入离心机中离心,使液体沉淀。
离心后,取出显微管,观察颜色变化,并使用分光光度计测定吸光度。
4. 结果与讨论通过测定标准曲线,我们可以得到各个蛋白质标准品的吸光度与浓度之间的关系。
利用这个关系,我们可以计算出待测样品中蛋白质的浓度。
在实验中,我们观察到显微管中的液体颜色会随着蛋白质浓度的增加而加深。
这是因为考马斯亮蓝染料与蛋白质发生非共价结合,形成复合物,使溶液变色。
吸光度的测定则是通过分光光度计来实现的。
需要注意的是,考马斯亮蓝法对于某些物质的干扰较大,因此在实验中应该选择适当的样品稀释倍数,以确保测定结果的准确性。
5. 结论通过考马斯亮蓝法,我们成功测定了给定溶液中蛋白质的含量,并得到了标准曲线。
通过标准曲线,我们可以计算出待测样品中蛋白质的浓度。
6. 结束语考马斯亮蓝法是一种简单、快速且准确的测定蛋白质含量的方法。
它被广泛应用于生物学研究和实验室工作中。
实验六 蛋白质含量测定(考马斯亮蓝G-250法)

实验六蛋白质含量测定(考马斯亮蓝G-250法)一、目的蛋白质是细胞中最重要的含氮生物大分子之一,承担着各种生物功能。
蛋白质的定量分析是蛋白质构造分析的基础,也是农牧产品品质分析、食品营养价值比较、生化育种、临床诊断等的重要手段。
根据蛋白质的理化性质,提出多种蛋白质定量方法。
考马斯亮蓝G -250法是比色法与色素法相结合的复合方法,简便快捷,灵敏度高,稳定性好,是一种较好的常用方法。
通过本实验学习考马斯亮蓝G-250法测定蛋白质含量的原理,了解分光光度计的结构、原理和在比色法中的应用。
二、原理考马斯亮蓝G-250是一种染料,在游离状态下呈红色,当它与蛋白质结合后变为青色。
蛋白质含量在0~1000μg范围内,蛋白质一色素结合物在595nm下的吸光度与蛋白质含量成正比,故可用比色法测定。
三、仪器、试剂和材料1.仪器(1)分析天平(2)具塞刻度试管10ml×8(3)吸管0.lml×I,lml×Z,5ml×I(4)研钵(5)漏斗(6)离心管10ml(7)容量瓶10ml(8)离心机(9)721型分光光度计2.试剂(1)标准蛋白质溶液称取10mg牛血清白蛋白,溶于蒸馏水并定容至100ml,制成100 pg/ml的原液。
(2)考马斯亮蓝G-250蛋白试剂称取100mg考马斯亮蓝G-250,溶于50ml 90%乙醇中,加入85%(m/v)的磷酸100ml,最后用蒸馏水定容到1000ml。
此溶液在常温下可放置一个月。
3.材料绿豆芽四、操作步骤1盖上塞子,摇匀。
放置2min后在595 nm波长下比色测定(比色应在l h内完成)。
以牛血清白蛋白含量(μg)为横坐标,以吸光度为纵坐标,绘出标准曲线。
2.样品中蛋白质含量的测定(1)准确称取约200mg绿豆芽下胚轴,放入研钵中,加入5ml蒸馏水在冰浴中研成匀浆,离心(4000r/min,10min),将上清液倒入10ml容量瓶,再向残渣中加入2ml蒸馏水,悬浮后再离心10min,合并上清液,定客至刻度。
(完整word版)可溶性蛋白质含量的测定

植物体内可溶性蛋白质含量的测定方法:考马斯亮蓝G-250染色法1.原理:考马斯亮蓝G-250测定蛋白质含量属于染料结合法的一种。
考马斯亮蓝G-250在游离状态下呈红色,在稀酸溶液中,当它与蛋白质的疏水区结合后变为青色,前者最大光吸收在465nm,后者在595nm。
在一定蛋白质浓度范围内(1~100μg),蛋白质与色素结合物在595nM波长下的光吸收与蛋白质含量成正比,故可用于蛋白质的定量测定.蛋白质与考马斯亮蓝G-250结合在2min左右的时间内达到平衡,完成反应十分迅速,其结合物在室温下1h内保持稳定。
该反应快速灵敏、易于操作、干扰物质少(考马斯亮蓝G-250和蛋白质通过范德华力结合,受蛋白质的特异性影响较小,除组蛋白外,其他不同种类蛋白质染色强度差异不大),可测定微克级蛋白质含量,是一种比较好的蛋白质定量法。
但此方法也存在其缺点,考马斯亮蓝在蛋白质含量很高时线性关系偏低,且不同来源蛋白质与色素结合状况有差异。
2.仪器:721分光光度计;10ml量筒1个;研钵;烧杯;量瓶;移液管;1ml3支;5ml3支;10ml 具塞刻度试管14支。
3.试剂:90乙醇%(无水乙醇20瓶以下8元1瓶,每瓶500ml);85%磷酸(500ml磷酸标准溶液0。
1mol/ml,16元钱1瓶);考马斯亮蓝G-250(80元钱1瓶,1瓶10g);牛血清白蛋白。
考马斯亮蓝G-250溶液:称取100μg考马斯亮蓝G-250,溶50ml90%乙醇,85%的磷酸100ml,最后用蒸馏水定容到1000ml,贮放在棕色瓶中,此溶液在常温下可放置1个月。
4。
标准曲线的绘制4.1、0~100μg/ml标准曲线的制作:取6支试管,按表1数据配制0~100μg/ml血清白蛋白液各1ml.准确吸取所配各管溶液0。
1ml,分别放入10ml具塞试管中,加入5ml考马斯亮蓝G—250试剂,盖塞,反转混合数次,放置2min后,在595nm下比色,绘制标准曲线。
蛋白质的定量测定---考马斯亮蓝法测定蛋白质浓度

实验名称:蛋白质的定量测定---考马斯亮蓝法测定蛋白质浓度【实验原理】考马斯亮蓝法测定蛋白质浓度,是利用蛋白质-燃料结合的原理。
考马斯亮蓝G-250染料,在酸性溶液时呈茶棕色,最大吸收峰在465nm。
当与蛋白质结合后变成深蓝色,最大吸收峰转至595nm,且其光吸收值与蛋白质含量(10~100μg/ml蛋白质浓度)成正比,因此可用于蛋白质的定量测定。
【实验准备】一、材料(1)血清二、试剂(1)考马斯亮蓝试剂:考马斯亮蓝G-250 100mg溶于50ml 95%乙醇中,加入100ml 85%磷酸,用蒸馏水稀释至1000ml。
(2)标准蛋白质溶液:结晶牛血清蛋白,预先经微量凯氏定氮法测定蛋白氮含量,根基其纯度用0.15mol/L NaCl配置成1.0mg/ml蛋白溶液。
(3)0.9% NaCl溶液。
三、器材(1)试管和试管架(2)722型分光光度计(3)吸量管(4)移液枪【实验步骤】一、制作标准曲线取6支干燥洁净的试管,编号按下表加入试剂光度值(A595值)。
以吸光度值为纵坐标,蛋白质浓度为横坐标,绘出标准曲线。
二、血清蛋白质浓度测定测定方法同上。
1mL稀释血清加2.5mL考马斯亮蓝试剂,血清用0.9%NaCl稀释200倍,使其测定值在标准曲线的直线范围内。
用上述0号管调零,测出血清的A595值。
【实验结果】以吸光度A595值为纵坐标,牛血清白蛋白标准液浓度为横坐标绘制标准曲线。
(2)根据所测血清的值,在标准曲线上查出其相当于标准蛋白的量,乘以稀释倍数,从而计算出血清的蛋白质浓度(mg/ml)0.26 mg/ml【实验讨论】①必须在试剂加入后的5~20min内测定光吸收,因为在这段时间内颜色是最稳定的。
②测定中蛋白-染料复合物会有少部分吸附于比色杯壁上,测定完后可用乙醇将比色杯洗干净。
③不要将标准蛋白质和待测蛋白质搞混,以免造成实验结果的改变。
④考马斯亮蓝(CBB)显色法测定蛋白质含量的主要缺点之一是线性关系差.通过研究显色液组分对线性关系的影响,发现显色液H+浓度是影响线性关系的主要因素【1】。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
实验报告
学院:第二临床医学院专业:临床医学年级:2013级班级:1班姓名:学号:日期:2014,3,8 得分:实验课程:生物化学实验
实验名称:蛋白质的定量测定(五)——考马斯亮蓝法测定蛋白质浓度
【实验目的】
掌握考马斯亮蓝G-250测定蛋白质含量的原理和方法。
【实验原理】
考马斯亮蓝G-250(Coomassie G-250)是一种甲基取代的三苯基甲烷,分子中磺酸基的蓝色染料,在465nm处有最大吸收值。
考马斯亮蓝G-250能与蛋白质通过范得华相互作用形成蛋白质—考马斯亮蓝复合物蓝色溶液,引起该染料的最大吸收λmax的位置发生红移,在595nm处有最大吸收值。
由于蛋白质—考马斯亮蓝复合物在595n处的光吸收远高于考马斯亮蓝在465nm处的光吸收,因此可大大地提高蛋白质的测定灵敏度。
蛋白质—考马斯亮蓝复合物溶液颜色的深浅与蛋白质的浓度成正比。
利用溶液颜色的差异进行比色测定,适合于蛋白质类的定量分析尤其适合于稀有蛋白质的微量分析。
考马斯亮蓝G-250试剂呈色反应颜色稳定、灵敏度高,最低测试蛋白质量在1ug左右。
【试剂与器材】
试剂:
考马斯亮蓝试剂:考马斯亮蓝G-250溶于50ml95%乙醇,加入100ml质量浓度为0.85g/ml 的磷酸,用蒸馏水稀释到1000ml。
标准蛋白质溶液:结晶牛血清清蛋白,预先经微量凯氏定氮法标定该蛋白质的百分含量,然后根据该蛋白的纯度用0.15mol/LNacl配制成1.0mg/ml蛋白溶液。
器材:
试管和试管架
722型分光光度计
吸量管
移液枪
【实验步骤】
一、制作标准曲线
各管混匀后,静置3min,以0号管为空白管调零,在595nm波长下分别测定各管溶液的吸光度值(A595). 以A595值为纵坐标,蛋白质浓度为横坐标,绘制标准曲线。
二、待测蛋白质浓度测定
测定方法同上,1ml待测蛋白质家5ml考马斯亮蓝试剂,。
用上述0号管调零,测出血清的A595值。
【实验结果】
由仪器测量可得A595=0.179,可得标准蛋白质溶液为0.0790mg/ml.
【注意事项】
必须在试剂加入后的5~20min内测定光吸收,因为在这段时间内颜色是最稳定的。
测定中蛋白-染料复合物会有少部分吸附在比色杯壁上,测定完后可用乙醇将比色杯清洗干净。
【思考与讨论】
一、考马斯亮兰法的突出优点是:
(1)因为蛋白质与染料结合后产生的颜色变化很大,蛋白质-染料复合物有更高的消光系数,因而光吸收值随蛋白质浓度的变化比Lowry法要大的多。
(2)测定快速、简便,只需加一种试剂。
完成一个样品的测定,只需要5分钟左右。
由于染料与蛋白质结合的过程,大约只要2分钟即可完成,其颜色可以在1小时内保持稳定,且在5分钟至20分钟之间,颜色的稳定性最好。
因而完全不用像分钟之间,颜色的稳定性最好。
因而完全不用像Lowry法那样费时和严格地控制时间。
(3)干扰物质少。
如干扰Lowry法的K+、Na+、Mg2+、离子Tris缓冲液、糖和蔗糖、甘油、巯基乙醇、EDTA等均不干扰此测定法。
二、此法的缺点是:
(1)由于各种蛋白质中的精氨酸和芳香族氨基酸的含量不同,因此Bradford法用于不同蛋白质测定时有较大的偏差,在制作标准曲线时通常选用—球蛋白为标准蛋白质,以减少这方
面的偏差。
(2)仍有一些物质干扰此法的测定,主要的干扰物质有:去污剂、Triton X-100、十二烷基硫酸钠(SDS)和0.1N的NaOH(如同0.1N的酸干扰Lowary法一样)
(3)标准曲线也有轻微的非线性,因而不能用Beer定律进行计算,而只能用标准曲线来测定未知蛋白质的浓度。
三、试验时应当注意分光光度计、吸量管、移液枪的正确使用。
友情提示:本资料代表个人观点,如有帮助请下载,谢谢您的浏览!。
