爱博斯迪克风险评估报告文稿
医疗器械定期风险评价报告模版

医疗器械定期风险评价报告模版1.引言在本报告中,我们将对款医疗器械进行定期风险评价。
该器械是一种常见的治疗设备,用于特定疾病的诊断和治疗。
本评价旨在评估器械的安全性和有效性,并提供改进建议,以确保其在使用过程中的安全和有效性。
2.评估范围本次评估主要关注器械的设计和工程控制,包括但不限于材料选择、结构设计、制造工艺等方面。
同时,也将考虑器械的操作使用过程中可能存在的风险。
3.方法和数据收集我们采用了多种方法和手段进行风险评价,其中包括但不限于:-文献综述:收集和分析与该器械相关的科学文章、临床试验结果和相关文献;-实地考察:对器械的制造工厂、品控措施、研发流程进行考察和验证;-数据收集:收集相关的产品质量数据、医疗事故报告和客户反馈意见。
4.结果分析在对收集的数据进行综合分析后,我们对器械的风险进行了评估。
评估结果如下:-设计风险:器械的设计结构较为合理,没有明显的设计缺陷或安全隐患;-材料风险:所采用的材料符合相关的标准要求,不存在明显的毒性或刺激性风险;-制造风险:制造工艺和工艺控制符合相关的标准要求,并通过了ISO9001质量管理体系认证;-安全使用风险:通过对用户使用操作和培训情况的调查,发现用户普遍能正确使用器械,并无明显的误操作风险。
5.结论与建议综合评估结果,器械在设计、制造和使用过程中存在的风险较低。
但为了进一步提高器械的安全性和可靠性,我们建议:-器械生产和销售方应加强售后服务,提供定期维护和故障排除的支持;-加强用户培训和宣传,提高用户对器械正确使用方法的认知和理解;-建立完善的风险管理体系,及时收集和分析器械使用过程中的不良事件和风险信息。
7.附录本报告的附录中将包括风险评价的详细数据、图表和相关的实地调查报告等。
本报告为医疗器械定期风险评价的一个模版,具体的评价内容和结论还需要根据实际情况进行调整和完善。
同时,还需要注意根据相关的法规和标准要求撰写报告,并提供合适的技术支持和解决方案。
医疗器械定期风险评价报告(模板)

医疗器械定期风险评价报告(模板)⽬录XXXXX (3)定期风险评价报告 (3)1. 产品基本信息 (3)1.1 产品名称:XXX。
(3)1.2 型号规格:XXXX。
(3)1.3 注册证编号:XXX。
(3)1.4 结构组成:与产品技术要求保持⼀致。
(3)1.5 ⼯作原理: (3)1.6 适⽤范围: (3)1.7 有效期: (3)2. 国内外上市情况 (3)2.1国内外本报告期内上市情况汇总 (3)2.2 产品批准上市时提出的有关要求,特别是与风险控制有关的要求 (5)2.3 适⽤范围(预期⽤途)以及特殊⼈群情况 (5)3.既往风险控制措施 (5)4.不良事件报告信息 (6)4.1个例不良事件 (6)4.2群体不良事件 (9)5.其他风险信息 (9)5.1 持有⼈上市后研究 (9)5.2 ⽂献资料信息 (9)5.3 其他 (9)6.产品风险分析 (9)7. 结论 (10)8. 附件 (10)8.1医疗器械注册证; (10)8.2产品使⽤说明书(操作⼿册); (10)8.3参考⽂献; (10)8.4其他需要提交的资料。
(10)XXXXX定期风险评价报告1. 产品基本信息1.1 产品名称:XXX。
1.2 型号规格:XXXX。
1.3 注册证编号:XXX。
1.4 结构组成:与产品技术要求保持⼀致。
1.5 ⼯作原理:产品综述资料有描述,直接复制粘贴。
1.6 适⽤范围:同上1.7 有效期:XXX2. 国内外上市情况2.1国内外本报告期内上市情况汇总注:1.注册/备案状态:⾸次注册/备案、延续注册/备案、注销医疗器械注册证书。
2.注册/备案批准⽇期:如状态为注销医疗器械注册证书,填写证书注销时间。
3.如果产品涉及注销医疗器械注册证书或者撤市,请在备注栏简要说明原因。
2.2 产品批准上市时提出的有关要求,特别是与风险控制有关的要求;(⽐如应急审批时提出继续完成的事项)如⽆:我公司XXX于XX年XX⽉由XXXX批准获得医疗器械注册证,⽬前处于⾸个注册周期内,注册证有效期⾄XXXXX。
体外诊断试剂项目评估报告参考模板

体外诊断试剂项目评估报告参考模板
一、引言
引言部分介绍该报告撰写的目的和意义,评估的背景和目标,以及评估方法和准则的说明。
二、项目概述
项目概述部分对评估的体外诊断试剂项目进行全面的介绍,包括项目的背景和目标、项目的主要内容和范围、项目的重要性和需求等。
三、评估指标和方法
评估指标和方法部分介绍本次评估所采用的评估指标和方法,包括定量指标和定性指标,以及采取的评估方法和工具。
四、评估结果和分析
评估结果和分析部分根据采集的相关数据和信息,对项目的各项指标进行评估和分析,包括项目的目标完成情况、项目的效果和影响、项目的效率和可持续性等方面。
五、问题和挑战
问题和挑战部分识别和分析项目存在的问题和面临的挑战,包括项目的不足和不合理之处、项目的风险和隐患以及项目实施过程中可能遇到的困难等,提出可能的解决方案和建议。
六、总结与展望
总结与展望部分对整个评估过程进行总结,包括评估的主要结果和发现、评估的局限和不足,以及对项目未来发展的展望和建议。
八、附件
附件部分包括本次评估所使用的问卷、统计数据、调查报告等相关资料。
医疗器械定期风险评价报告模版

医疗器械定期风险评价报告模版报告标题:医疗器械定期风险评价报告
报告章节及内容:
1.引言:
1.1报告目的
1.2报告范围
1.3报告背景
2.风险评价概述:
2.1风险评价定义
2.2风险评价的重要性
2.3风险评价的方法
3.器械风险评价:
3.1器械描述
3.2相关法规标准说明
3.3器械原理及使用方法
3.4器械使用过程中的可能风险
4.风险评价方法:
4.1选择适当的风险评价方法
4.2资料收集
4.3风险识别
4.4风险分析
4.5风险评估
4.6风险管理
5.实施风险管理措施:
5.1风险控制措施
5.2风险预防措施
5.3风险监测和报告
6.风险评价结果与分析:
6.1风险程度评价
6.2风险因素分析
6.3风险控制措施效果评估
6.4风险与效益平衡考虑
7.结论:
7.1风险评价总结
7.2风险管理建议
8.1引用的相关法规标准
8.2引用的风险评价方法及工具
9.附录:
9.1相关表格与图表
9.2详细数据和风险评估结果
报告编写注意事项:
1.报告内容要客观、准确,避免主观臆断;
2.在风险评价过程中,要使用科学的方法和工具进行评价;
4.报告要清晰易懂,使用术语要简明扼要,便于非专业人士理解;
5.报告要完整,包含必要的章节和附录,确保评价结果详尽。
医疗器械定期风险评价报告

医疗器械定期风险评价报告1000字医疗器械定期风险评价报告一、前言本报告为医疗器械的定期风险评价报告,主要对医疗器械的安全性进行评估,并提出相应的改进意见和建议。
此评价主要基于医疗器械使用情况及实际应用中的医疗安全问题,旨在为医疗机构提供有关医疗器械安全的评估参考。
二、评估对象本次风险评价的对象为:心电图机、麻醉机、输液泵等常见的临床医疗器械。
三、评估方法1. 风险分析通过分析使用过程中的异常情况、不良事件及近期的安全警示,对器械在实际使用中所存在的风险进行评估。
2. 风险编号按照ISO14971标准进行风险等级划分,并对每一项风险进行编号。
3. 风险辨识确定风险源、事故机制、可能受伤害部位及受伤害的严重程度等,辨识可能的风险。
4. 风险评估针对各项风险进行概率和影响的评估,确定风险等级。
5. 风险管理在确定器械的风险等级后,采取相应的控制措施对风险进行有效的管理和控制。
四、结果分析1. 心电图机风险编号:ECG-01风险描述:电极接触不良,影响测量准确度风险等级:中等改进措施:增加提醒功能,提醒用户检查电极连接是否正常。
风险编号:ECG-02风险描述:使用过程中电极过热,烧伤患者风险等级:严重改进措施:加强电极散热设计,降低电极温度。
2. 麻醉机风险编号:ANES-01风险描述:氧气浓度超标或不足,导致氧气中毒或低氧血症风险等级:高风险改进措施:加强气路质量监控,增加气路故障报警功能。
风险编号:ANES-02风险描述:麻醉剂过量或过敏,导致意外死亡或严重后果风险等级:严重改进措施:严格地医嘱管理,确保用药合理、安全。
3. 输液泵风险编号:INF-01风险描述:输液泵设置错误,导致输液速度过快或过慢风险等级:中等改进措施:加强人员培训,提高用户操作技能。
风险编号:INF-02风险描述:输液管路堵塞,导致输液停止或过量风险等级:中等改进措施:注意管路的清洁,加强对管路的监控和维护。
五、结论和建议通过风险评估,发现医疗器械在实际使用过程中存在的风险问题,建议采取相应措施进行风险管理。
医疗器械风险分析报告通用版

医疗器械风险分析报告通用版报告摘要本报告旨在对医疗器械的风险进行分析和评估,以提供决策者和相关人员有效的参考信息。
通过对医疗器械使用环境、操作方式、设计特点和相关文献的综合分析,确定了可能存在的潜在风险,并提出了相应的风险控制措施和优化建议。
希望本报告能够为相关部门的决策和管理提供有益的指导。
1. 引言医疗器械在医疗诊断和治疗过程中起到重要的作用,但其使用也存在一定的风险。
本报告旨在全面分析和评估医疗器械的风险,并提供相应的控制和优化建议,以确保患者和医疗工作者的安全。
2. 风险识别在对医疗器械进行风险分析时,我们首先对其使用环境、操作方式、设计特点等因素进行了仔细研究和分析。
通过与相关文献的对比和实地考察,我们确定了医疗器械使用过程中可能存在的以下风险:2.1 过度曝光风险某些医疗器械在使用过程中可能导致患者接受过度的辐射,从而对患者的健康产生负面影响。
2.2 感染传播风险医疗器械在使用过程中可能受到不正确的清洁和消毒措施,导致感染病原体的传播。
2.3 设计缺陷风险一些医疗器械的设计可能存在缺陷,导致在使用过程中出现意外情况,对患者造成伤害。
3. 风险评估针对上述风险,我们根据风险的概率和影响程度,进行了风险评估。
评估结果显示,过度曝光风险属于较高级别风险,感染传播风险和设计缺陷风险属于中级别风险。
4. 风险控制措施为了降低医疗器械风险的发生和影响,我们提出了以下风险控制措施:4.1 过度曝光风险控制通过完善培训和操作规程,提高医疗工作者对辐射防护的意识和技能,合理控制辐射剂量,从而降低患者的过度曝光风险。
4.2 感染传播风险控制加强医疗器械清洁和消毒方面的培训,确保医疗工作者掌握正确的操作方法,规范清洁和消毒流程,从而减少感染病原体的传播。
4.3 设计缺陷风险控制医疗器械的设计应符合相关标准和规范,经过充分的验证和测试,减少设计缺陷的发生。
同时,应加强对医疗器械的监测和反馈机制,及时发现和处理潜在的问题。
(完整word版)风险评估(医疗设备)

一、风险定义医疗设备大量用于临床,如在使用及管理上不得当,可能会对使用者及患者带来伤害。
二、风险来源:1、医疗设备在使用中设备出现故障时对病人的伤害;2、由于使用者操作不当造成对病人的伤害;3、由于带有放射源或电离辐射、电磁辐射的医疗设备造成的人员的伤害;4、由电气安全引起的问题:医疗设备绝缘程度下降、保护接地5、不当等因素造成的人员的伤害;6、因机械、光学、化学等有害物质污染出现的安全问题;7、由于各设备的组合相互之间产生影响造成的人员的伤害。
8、其他可能对病人和工作人员造成伤害的风险。
三、风险准则说明:A:可接受的风险;R:合理可行降低(ALARP)的风险;U:不经过风险/收益分析即判定为不可接受的风险四、风险分类1、一类设备(S1):直接作用于人体,能维持人体生命体征,对使用者及患者有直接影响的设备,如X光机、呼吸机、麻醉机、除颤仪、宫腹腔镜、供应室消毒供应设备(等离子灭菌器、高温高压灭菌器)、检验科高温高压灭菌器、婴儿辐射台(保暖箱)。
2、二类设备(S2):直接作用于人体,对人体有少量影响,对人体生命无直接影响的设备,如妇科理疗设备(微波、短波、热疗),检验科设备(血液、尿、生化)、B超。
3、三类设备(S3):对使用者的诊疗起辅助作用,对人体有少量影响,如监护仪、输液泵、血压计、心电图等常规辅助设备。
四、巡检分类(医疗设备根据国家强检要求,需每年由第三方计量检验局进行强制检定,合格后才可应用于临床)1、一类设备:每周进行一次例行巡检,巡检项目由科室人员与设备组人员一同完成,巡检项目包括,通电测试,功能检查,以及常规维护。
2、二类设备:每半月进行一次例行巡检。
3、三类设备:每一个月进行一次例行巡检.。
医疗器械企业风险评估报告

医疗器械企业风险评估报告1.引言1.1 概述概述部分将介绍医疗器械企业风险评估的背景和意义。
医疗器械企业在日常经营活动中面临着各种风险,包括质量安全风险、市场风险、监管风险等,这些风险可能对企业经营造成严重影响甚至带来灾难性后果。
因此,进行风险评估对医疗器械企业的可持续发展具有至关重要的意义。
本报告将针对医疗器械企业风险评估的相关问题进行深入分析和探讨,旨在为企业提供有效的风险管理和控制方法,促进医疗器械行业的健康发展。
1.2 文章结构文章结构:本文主要分为引言、正文和结论三个部分。
在引言部分,我们将会概述医疗器械企业风险评估的重要性,并介绍本文的结构和目的。
正文部分将会详细介绍医疗器械企业风险评估的方法,并分析医疗器械企业常见的风险。
同时,我们还将通过实际案例进行风险评估分析。
在结论部分,我们将对本文进行总结,并提出对医疗器械企业风险评估的建议,展望未来可能的发展趋势。
通过这样的结构安排,我们将全面深入地探讨医疗器械企业风险评估的相关问题,为相关从业人员提供有益的参考和指导。
1.3 目的目的部分的内容应该是对本文的写作目的进行阐述。
在医疗器械企业风险评估报告中,我们的目的是通过系统性的评估和分析,帮助医疗器械企业更好地了解其面临的各种风险,并提出相应的应对策略和建议。
同时,本文还旨在为读者提供一种风险评估的方法,帮助他们在实际工作中更好地应对医疗器械企业所面临的各种风险。
通过对医疗器械企业的常见风险、风险评估方法和案例分析的介绍,本文旨在提高医疗器械企业的风险意识,促进其健康可持续发展。
2.正文2.1 风险评估方法在医疗器械企业风险评估中,有许多方法可供选择,每种方法都有其独特的优点和局限性。
在选择风险评估方法时,应综合考虑企业的实际情况和需求,以确保评估结果的准确性和可靠性。
一种常用的风险评估方法是定性风险评估,它主要依靠专家意见和经验来对风险进行分类和评估。
这种方法具有简单、快速的优点,但缺点是易受主观因素影响,评估结果的客观性和可比性较差。
医疗器械工作者需报告的风险评估结果

医疗器械工作者需报告的风险评估结果在医疗器械的开发和生产过程中,风险评估是一个至关重要的环节。
根据相关法规和准则,医疗器械工作者需要对其开发和生产的医疗器械进行风险评估,并将结果报告给相关机构和部门。
本文将介绍医疗器械工作者在进行风险评估时所需报告的内容和要求。
一、风险评估的背景与目的风险评估在医疗器械的开发和生产中具有重要意义。
其主要目的是评估医疗器械的使用过程中可能产生的风险,进而采取相应的控制措施来确保患者的安全和效果。
二、风险评估的内容1. 总体描述将医疗器械的整体情况进行描述,包括其特点、功能、适用范围等。
2. 风险识别在这一部分,需对可能存在的风险进行识别。
通过专业知识和相关实验研究,确定医疗器械使用过程中可能出现的危险和潜在危害。
3. 风险评估在风险评估阶段,需对风险进行定量或定性的评估。
可以使用一定的模型或指标,如风险矩阵、风险分级等,将风险进行分类和评估。
4. 风险控制风险控制是风险评估的重要环节。
在这一部分,需描述所采取的控制措施,包括但不限于设计优化、安全性能改进、警示标识等。
5. 风险验证对控制措施的有效性进行验证,确保控制措施能够有效降低风险。
三、报告的格式与要求1. 报告格式报告应采用清晰、简洁的语言描述,并符合相关规范和要求。
可以使用表格、图表等形式对风险评估结果进行展示。
2. 报告内容报告中需包含医疗器械的基本信息、风险识别结果、风险评估结果、风险控制措施以及风险验证结果。
同时,报告应当提供详细的数据支持和科学依据。
3. 报告提交要求报告应当按照相关规定提交给相关机构和部门。
提交时间和形式需符合相应的要求,确保报告的及时性和可查性。
四、风险评估结果的意义与应用1. 指导医疗器械生产和开发风险评估结果对医疗器械的生产和开发具有指导意义。
可以帮助生产者和开发者了解产品的风险情况,优化产品设计,并采取相应的改进措施。
2. 保障患者的安全风险评估结果的报告可以帮助相关部门对医疗器械的安全性进行评估和监控,从而保障患者的安全和权益。
爱博斯迪克风险评估报告文稿

风险查勘报告爱博斯迪科化学(上海)有限公司地理坐标(东经122°06′37′′,北纬31°29′44′′)上海市外高桥保税区美桂南路332号中国太平洋财产保险股份有限公司上海分公司【服务日期】2010.09.07【接洽人员】爱博斯迪科化学(上海)有限公司张敏安全健康环境主管【查勘人员】前言此次为爱博斯迪科(上海)有限公司所做的现场风险查勘是我公司对于重要客户提供的一项保险延伸服务。
此次服务是以我公司长期积累的风险管理经验,帮助企业进一步完善内部的风险管理体系,并就查勘中发现的若干隐患,提供风险改善建议。
此次查勘服务工作,承蒙爱博斯迪科(上海)有限公司HSE主管的大力帮助与配合,我们得以顺利完成此次风险查勘。
结合贵公司提供的资料和现场查勘的风险状况,我司经过细致地风险评价后,提交此份风险查勘报告,供贵公司在风险管理工作中参考,藉此共同防范事故发生于未然,避免无谓的财产损失和人员伤亡,以达到事故预防和损失控制的双重目的。
特别声明:查勘中所拍摄的现场照片和取得的资料将仅作为本报告的风险说明以及建立客户档案之专门用途,不会使用于其它任何用途。
目录项目投保情况-------------------------------------------------------- 05页一、项目概况-------------------------------------------------------- 06页二、环境概况-------------------------------------------------------- 07页三、生产概况-------------------------------------------------------- 10页四、消防和安保----------------------------------------------------- 14页五、风险评价-------------------------------------------------------- 16页六、风险改善建议---------------------------------------------------- 24页七、附件-------------------------------------------------------------- 29页项目投保情况1、Property All Risks (PD)Basic Coverage Laptops out ofPremiseFine ArtsBuildings Contents Constructionin ProgressStock(75%)TotalSum InsuredSum InsuredSumInsured0.00 127,355,934.15 0.00 24,140,683.99 151,496,618.14 499,360.91 0.00 2、Business Interruption following Property All Risks (BI/PD)Gross Profit (DB1) Salaries Auditor FeeTotal Sum Insured238,302,250.07 25,390,601.16 270,000.00 263,962,851.23 3、Machinery Breakdown (MB)Machinery & Equipments51,466,548.804、Business Interruption following Machinery Breakdown (BI/MB)Gross Profit (DB1) Salaries Auditor FeeTotal Sum Insured238,302,250.07 25,390,601.16 270,000.00 263,962,851.23一、项目概况汉高是一家拥有130多年历史的跨国集团,全球有125个国家和地区的消费者信赖汉高的品牌和技术。
688050爱博医疗2023年上半年经营风险报告
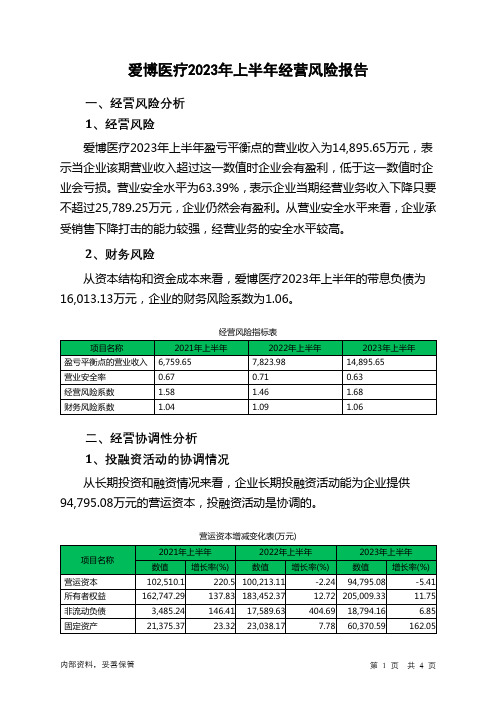
爱博医疗2023年上半年经营风险报告一、经营风险分析1、经营风险爱博医疗2023年上半年盈亏平衡点的营业收入为14,895.65万元,表示当企业该期营业收入超过这一数值时企业会有盈利,低于这一数值时企业会亏损。
营业安全水平为63.39%,表示企业当期经营业务收入下降只要不超过25,789.25万元,企业仍然会有盈利。
从营业安全水平来看,企业承受销售下降打击的能力较强,经营业务的安全水平较高。
2、财务风险从资本结构和资金成本来看,爱博医疗2023年上半年的带息负债为16,013.13万元,企业的财务风险系数为1.06。
经营风险指标表二、经营协调性分析1、投融资活动的协调情况从长期投资和融资情况来看,企业长期投融资活动能为企业提供94,795.08万元的营运资本,投融资活动是协调的。
营运资本增减变化表(万元)长期投资197.57 928.46 313.67 58.77 288.24 -8.112、营运资本变化情况2023年上半年营运资本为94,795.08万元,与2022年上半年的100,213.11万元相比有所下降,下降5.41%。
3、经营协调性及现金支付能力从企业经营业务的资金协调情况来看,企业经营业务正常开展,需要企业提供20,987.48万元的流动资金。
而企业投融资活动保证了企业经营活动的资金需求,经营业务是协调的。
经营性资产增减变化表(万元)项目名称2021年上半年2022年上半年2023年上半年数值增长率(%) 数值增长率(%) 数值增长率(%)存货5,351.67 -13.43 6,188.87 15.64 10,897.25 76.08 应收账款8,226.31 -7.04 10,323.62 25.5 14,560.23 41.04 其他应收款1,890.18 2,525.45 283.26 -85.01 955.46 237.31 预付账款1,530.7 71.51 2,383.41 55.71 4,190.92 75.84 其他经营性资产66,862.04 4,371.04 65,794.29 -1.6 2,445.29 -96.28 合计83,860.9 379.44 84,973.44 1.33 33,049.15 -61.11经营性负债增减变化表(万元)项目名称2021年上半年2022年上半年2023年上半年数值增长率(%) 数值增长率(%) 数值增长率(%)应付账款142.69 246.01 391.38 174.29 1,900.36 385.56 其他应付款4,809.15 363.04 6,588.13 36.99 5,751.64 -12.7 预收货款0 -100 0 - 0 - 应付职工薪酬1,419.2 134.33 1,703.76 20.05 2,672.99 56.89 应付股利0 - 3,891.54 - 0 -100 应交税金1,746.55 99.06 3,441.01 97.02 1,318.44 -61.68 其他经营性负债154.89 - 405.14 161.56 418.23 3.23 合计8,272.49 214.77 16,420.96 98.5 12,061.67 -26.554、营运资金需求的变化2023年上半年营运资金需求为20,987.48万元,与2022年上半年的68,552.48万元相比有较大幅度下降,下降69.38%。
688050爱博医疗2023年三季度财务风险分析详细报告

爱博医疗2023年三季度风险分析详细报告一、负债规模测算1.短期资金需求该企业经营活动的短期资金需求为25,191.93万元,2023年三季度已经取得的短期带息负债为0万元。
2.长期资金需求该企业权益资金能够满足长期性投资活动的资金需求,并且还有66,875.7万元的权益资金可供经营活动之用。
3.总资金需求该企业资金富裕,富裕41,683.77万元,维持目前经营活动正常运转不需要从银行借款。
4.短期负债规模根据企业当前的财务状况和盈利能力计算,企业有能力偿还的短期贷款规模为60,914.27万元,在持续经营一年之后,如果盈利能力不发生大的变化,企业有能力偿还的短期贷款规模是94,922.97万元,实际已经取得的短期带息负债为0万元。
5.长期负债规模按照企业当前的财务状况、盈利能力和发展速度,企业有能力在2年内偿还的贷款总规模为77,918.62万元,企业有能力在3年之内偿还的贷款总规模为86,420.79万元,在5年之内偿还的贷款总规模为103,425.15万元,当前实际的带息负债合计为15,833.13万元。
二、资金链监控1.会不会发生资金链断裂从当前盈利水平和财务状况来看,该企业不存在资金缺口。
如果当前盈利水平保持不变,该企业在未来一个分析期内有能力偿还全部负债。
该企业负债率低,发生资金链断裂的风险极小。
资金链断裂风险等级为0级。
2.是否存在长期性资金缺口该企业不存在长期性资金缺口,并且长期性融资活动为企业提供86,106.2万元的营运资金。
3.是否存在经营性资金缺口该企业经营活动存在资金缺口,资金缺口为25,191.93万元。
这部分资金缺口已被长期性融资活动所满足。
其中:应收账款增加7,919.66万元,预付款项减少605.37万元,存货增加7,226.82万元,其他流动资产减少60,181.58万元,共计减少45,640.47万元。
应付账款减少642.8万元,应付职工薪酬增加1,162.92万元,应交税费减少3,181.48万元,共计减少2,661.36万元。
医疗器械风险评估报告

风险评估报告制定:批准:日期:风险评估报告1前言本文是对XXX有限公司***医疗产品进行风险管理的报告。
报告中对所有的潜在危害及每一危害产生的潜在原因进行判定。
对于各种危害可能导致损害的严重程度和危害的发生概率进行了估计。
在某一风险水平不可接受时,采取了降低风险的控制措施,同时对采取风险控制措施后的剩余风险进行了评价。
最后,使所有的剩余风险的水平达到可以接受。
2适用范围此风险管理中适用于XXX有限公司生产的***医疗产品。
3应用资料3.1相关标准a) 93/42/EEC(“MDD”)医疗器械导则b) ISO 14971: 2007 医疗器械——风险管理对医疗器械的应用3.2有关产品的资料BOM表,样板申请单,工装夹具申请表,工艺流程,测试流程TEST,包装说明书,试产总结会议记录。
3.3其它信息来源顾客投诉,意外事故记录,专业文献中的文章,网络信息如FDA官方网站上提供的信息、医疗器械管理局网站公布的信息。
3.4定义3.4.1危害:产品对患者、操作者、其他人和环境造成伤害/或破坏的潜在危险。
3.4.2风险:一个危害的发生概率及其损害的严重程度。
3.4.3风险评价:判定风险的危害程度、发生概率并估计风险的可接收程度。
3.4.4ALARP:合理可行降低区。
3.5风险分析小组成员4产品说明4.1产品概况本风险管理的对象:。
4.2产品分类按MDD93/42/EEC的要求进行产品分类:属于1类。
4.3功能说明用途:用于。
4.4使用环境4.4.1产品使用环境:-50C~450C的环境下使用;4.4.2对使用者的要求:参照产品说明书要求。
5产品预期用途以及与安全有关的特征的判定(定性和定量特征清单)6危害判定(危害列表清单)F11 与现有设备相比,引起争议的模式或图像不适用功能性失效、维护和老化引起的危害G1 错误的数据转换不适用G2 维护规范缺少或不适当不适用G3 对医疗器械寿命中止缺少适当的决定不适用G4 电气、机械整合的丧失不适用G5 不适当的包装不适用G6 再次使用和(或)不适当的再次使用不适用G7 由重复使用造成的功能恶化不适用7风险评价7.1评价准则7.1.1严重度分级:按可能造成伤害的严重程度分等级名称代号说明轻度S1 轻度伤害或无伤中度S2 中等伤害致命S3 一人死亡或重伤灾难性S4 多人死亡或重伤7.1.2发生概率分级:按事件发生的概率分等级名称代号频次(每年)说明极少P1 极少发生(10-6)目前为止,全世界仅一个案例非常少P2 非常少发生(10-4~10-6)一万个人中仅一至两个很少P3 很少发生(10-3~10-4) 一千个人中仅一至两个偶尔P4 偶尔发生(~10-2)一百个人中仅一至两个有时P5 有时发生(~10-1)一百个人中有十来个经常P6 经常发生(>0.5)一半以上的人发生过7.1.3风险可接受准则风险=严重等级×概率等级风险大小可接受性(缩写代号)1~3 广泛可接受(ACC)4~11 合理可行(ALARP)12~30 不容许(NACC)7.2风险评价及风险控制对处于可广泛接受区的风险无需再采取控制措施,对处于合理可行区和不容许区的风险必须采取进一步的措施进行控制。
ergo风险评估报告

Ergo风险评估报告介绍本报告旨在对公司的ergo风险进行综合评估,并提供相应的解决方案。
ergo风险是指由于工作环境不符合人体工程学原理而导致的员工健康问题。
通过及时的评估和采取适当的措施,可以减少员工的健康问题、提高工作效率和员工满意度。
步骤一:数据收集在评估公司的ergo风险之前,我们需要收集相关数据。
以下是数据收集的几个关键步骤:1.工作环境观察:我们将观察员工的工作环境,包括办公桌、工作椅、电脑显示屏等。
我们将注意到任何不符合人体工程学原理的因素。
2.员工访谈:我们将采访员工,了解他们在工作中可能遇到的健康问题。
我们还将了解员工对工作环境的满意度和改进建议。
3.健康数据分析:我们将分析员工的健康数据,包括工作相关的疾病和伤害记录。
这将帮助我们确定存在的健康问题和他们的频率。
步骤二:风险评估基于收集的数据,我们将对公司的ergo风险进行评估。
以下是我们评估的几个关键因素:1.工作姿势:我们将评估员工在工作中的姿势,包括坐姿、站姿和手部动作。
我们将注意到任何不符合人体工程学原理的姿势。
2.劳动强度:我们将评估员工的劳动强度,包括重复动作、工作时间和劳动强度的变化。
这将帮助我们确定哪些员工可能面临较高的健康风险。
3.工作环境:我们将评估工作环境的布局和设备,包括办公桌、工作椅、计算机设备和工作区域的布局。
我们将确定是否存在潜在的ergo风险因素。
步骤三:风险解决方案根据风险评估的结果,我们将提供相应的解决方案。
以下是一些常见的ergo风险解决方案:1.调整工作姿势:我们将建议员工调整他们的工作姿势,以确保符合人体工程学原理。
这可能涉及调整座椅高度、使用腰靠、调整显示屏高度等。
2.提供培训:我们将为员工提供人体工程学培训,教授正确的工作姿势和动作。
这将帮助员工更好地理解如何保护自己免受ergo风险的影响。
3.更换设备:如果评估发现某些设备存在潜在的ergo风险,我们将建议公司更换这些设备。
这可能包括更舒适的工作椅、支持手腕的键盘和鼠标等。
医疗器械质量风险评估方案范本

医疗器械质量风险评估方案背景医疗器械作为治疗、检查、诊断、矫正等过程中必不可少的工具,是医疗保健服务的重要组成部分,但其安全性和有效性对患者的生命健康和医疗安全具有重要影响。
因此,医疗器械的质量控制十分关键,医疗器械质量的风险评估更是必不可少的一环。
意义医疗器械质量风险评估是通过对医疗器械的性能、功能、材料、生产工艺以及使用风险等进行综合评估,确定医疗器械的安全性和有效性,并在此基础上确定医疗器械的合理使用范围和使用条件,保证患者的生命健康和医疗安全。
医疗器械质量风险评估的结果还可以作为医疗器械注册、审批和监管的重要依据。
方案医疗器械质量风险评估的基础是明确医疗器械的功能、性能、材料和生产工艺等信息,并根据医疗器械的使用过程中可能引发的风险进行分析和评估。
第一步:明确医疗器械的信息在进行医疗器械质量风险评估之前,需要明确医疗器械的信息,包括但不限于:•医疗器械的品名、型号、用途、结构和性能等;•医疗器械的材料、设计和生产工艺等;•医疗器械的使用说明书、技术文件和检验报告等。
第二步:确定风险分析的目标根据医疗器械明确的信息,确定风险分析的目标,包括但不限于:•确定医疗器械使用过程中可能发生的危险和风险;•确定医疗器械使用过程中可能受到的影响和损失;•确定医疗器械使用过程中可能出现的不良事件和事故。
第三步:制定风险分析的计划根据风险分析的目标,制定风险分析的计划,其中需要包括但不限于:•选择风险分析的方法和工具;•确定风险分析的步骤和流程;•确定风险分析的参与人员和责任分工;•确定风险分析的时间和地点。
第四步:进行风险分析根据风险分析的计划,进行风险分析,其中需要包括但不限于:•根据医疗器械的信息,确定可能的危险和风险;•按照风险分析的流程,对医疗器械的危险和风险进行分析和评估;•确定医疗器械使用过程中可能产生的不良事件和事故。
第五步:制定风险控制措施根据风险分析的结果,制定风险控制措施,其中需要包括但不限于:•确定风险控制的优先级和重要性;•制定医疗器械的使用说明书、操作规程和保养维护规程等;•制定培训计划,对医疗器械的使用者进行培训;•制定监测和报告制度,对医疗器械的使用情况进行监测和报告。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
风险查勘报告爱博斯迪科化学(上海)有限公司地理坐标(东经122°06′37′′,北纬31°29′44′′)上海市外高桥保税区美桂南路332号中国太平洋财产保险股份有限公司上海分公司【服务日期】2010.09.07【接洽人员】爱博斯迪科化学(上海)有限公司张敏安全健康环境主管【查勘人员】前言此次为爱博斯迪科(上海)有限公司所做的现场风险查勘是我公司对于重要客户提供的一项保险延伸服务。
此次服务是以我公司长期积累的风险管理经验,帮助企业进一步完善内部的风险管理体系,并就查勘中发现的若干隐患,提供风险改善建议。
此次查勘服务工作,承蒙爱博斯迪科(上海)有限公司HSE主管的大力帮助与配合,我们得以顺利完成此次风险查勘。
结合贵公司提供的资料和现场查勘的风险状况,我司经过细致地风险评价后,提交此份风险查勘报告,供贵公司在风险管理工作中参考,藉此共同防范事故发生于未然,避免无谓的财产损失和人员伤亡,以达到事故预防和损失控制的双重目的。
目录项目投保情况-------------------------------------------------------- 05页一、项目概况-------------------------------------------------------- 06页二、环境概况-------------------------------------------------------- 07页三、生产概况-------------------------------------------------------- 10页四、消防和安保----------------------------------------------------- 14页五、风险评价-------------------------------------------------------- 16页六、风险改善建议---------------------------------------------------- 24页七、附件-------------------------------------------------------------- 29页项目投保情况1、2、3、4、一、项目概况汉高是一家拥有130多年历史的跨国集团,全球有125个国家和地区的消费者信赖汉高的品牌和技术。
汉高是财富500强企业。
通过品牌和技术,汉高有三大战略业务领域:家用护理,个人护理和汉高粘合剂、密封剂及表面处理。
2008年,汉高实现销售额141.31亿欧元,运营利润14.95亿欧元。
汉高全球总部位于德国的杜塞尔多夫。
汉高在全球超过125个国家拥有5万多名员工,其中80%以上为海外员工。
爱博斯迪科公司作为汉高集团的成员,将在电子行业提供更加全面的产品和服务。
爱博斯迪科化学(上海)有限公司位于外高桥保税区内,业务涉及三大品牌:Ablestik, Emerson & Cuming 以及Acheson。
Ablestik作为制造芯片粘合剂的世界领先公司,主要产品适用于半导体封装和微电子及光电集成的材料,包括导电及非导电粘合剂、胶膜等材料。
Emerson & Cuming作为全球性的专业配方材料供应商,致力于从产品设计到工艺生产提供全方位的解决方案。
主要产品包括灌封胶、粘合剂、导热界面材料、底部填充物、贴片胶等等。
Acheson致力于为印刷电路板工业提供卓越的导电油墨及非导电UV油墨材料,其材料应用于电子计算机键盘、薄膜开关、PCB生产等相关行业 Acheson 作为RFID电子材料领先供应商,其导电银油墨在业内享有盛誉。
企业员工职工人数为150人。
工作目前采用单班制。
二、环境概况【自然环境】上海位于北纬30°40’~31°53’,东经120°51’~122°12’,居我国南北海岸线的中心。
东临太平洋,南依杭州湾,西与江苏、浙江两省接壤,北为长江入海口。
气象上海地区属湿润的北亚热带海洋性季风气候,是东亚季风盛行的地区,温和湿润、光照充足,降水丰沛,四季分明。
冬季寒冷干燥,以西北风为主,夏炎热多雨,盛行东南风。
春秋短,冬夏长,严寒、酷暑期短,冬天约126天,夏天约110天,全年无霜期241天。
年平均气温16.5℃。
历年最高温度40℃,最低温度零下11℃。
上海市多年平均降雨量1100mm,雨日约131天。
有记录的最大年降雨量1678mm(1977),最小年降雨量702mm(1978)。
历年24小时内最大降雨量为394.5mm,1小时内最大降雨量为104mm。
年平均相对湿度79%。
汛期(5月-9月)有春雨、梅雨、秋雨三个雨期,降水量可占全年总降水量的60%以上,平均697.8毫米,平均月降水量100毫米以上,通常≥50毫米的暴雨分别出现在5月、8月、9月。
上海冬季平均气温5.2℃;春季平均气温15.6℃;夏季平均气温27.8℃;秋季平均气温19.9℃。
上海全年日照1909.4小时;10、50、100年一遇的计算雪压分别为0.1、0.2、0.25 KN/M2。
上海市常年主导风向为东南风,多年平均风速为3.9m/s。
每年7~9月常受来自太平样上的热带风暴侵袭。
每年平均受台风影响2次,最多年份可达4~7次。
强热带风暴10年中常有3~4次。
上海市多年平均雷暴日数为32.2天,属于中雷区。
每年的2月到11月均可能发生雷暴天气,6月到9月最频繁。
地质水文上海地区河湖众多,水网密布,境内水域面积697平方公里,相当于全市总面积的11%。
上海河网大多属黄浦江水系,主要有黄浦江及其支流苏州河、川扬河、淀浦河等。
黄浦江源自太湖,全长113公里,流经市区,江道宽度300~770米,平均360米,终年不冻,是上海的水上交通要道。
上海境内除西南部有少数丘陵山脉外,为坦荡低平的平原,是长江三角洲冲积平原的一部分,平均海拔高度4米左右。
陆地地势总体呈现由东向西低微倾斜。
【周边环境】爱博斯迪科化学(上海)有限公司周边环境如下:【厂区平面布置图】三、生产概况【生产工艺】企业拥有从生产导电胶、非导电胶的一系列完整产线,其基本流程如下:(高速剪切混合机)—(三混研磨机)———(冲压灌装机)——— (超低温冰箱)——— 【厂区主要建筑】建筑占地面积3994m 2,总使用面积8029m 2(加入银粉)搅拌 (液压系统)包装冷冻保存检验入库(辅料)混合分散 树脂(预热)设计方:中国海诚工程科技公司;施工方:中国建筑第一工程安装公司;注:(1)建筑抗震等级为7级;(2)厂区建筑物的维护状况基本为以下几类情况:A. 建筑物外墙的粉刷修补,一次/年;B.生产办公大楼楼顶防水层的检查和修缮,一次/年;C. 窗间墙等易渗水处的检查和修缮(汛期检查);【主要生产设备】【公用工程】【设备维护保养】公司生产设备维护由厂务部负责。
据介绍,目前厂务部有2个工程师、1个维修主管以及4个技术人员。
设备为日本井上进口设备,已运行多年,维护状况较好。
公司有健全的安全生产规章制度和事故应急措施,检修人员对设备进行日常巡查,执行操作挂牌制度。
【易燃及危险品】四、消防和安保1、最近的消防队为高桥消防大队,距离企业2公里。
高桥消防大队备有消防车5台,距离企业2公里,赶赴厂区所需时间为5分钟;2、企业有兼职消防队员2名,定期进行训练,但不与当地消防队同练;3、企业内部设有容积达700立方的消防水池。
据相关人员介绍,该水池在紧急情况下,可支撑消防用水达3小时左右;4、消防泵房位于地面,设备安置平面有垫高;主泵两台,均为通过FM认证设备;FIRE JOCKY PUMP 1 台,流量75~125L/S,扬程75~90m;FIRE DIESEL PUMP SET 1 台,流量75~125L/S,扬程75~90m;稳压泵2台,一用一备。
流量11m3/h,扬程75~75m;(据介绍,每周五有专人对其做开启运行测试)5、烟感和温感火灾自动报警系统做到生产建筑内部100%覆盖,报警信号接入消防控制中心(门卫室);水喷淋自动灭火系统做到生产建筑内部100%覆盖,喷头数量2100个;6、厂区按照相关规定配置有室内外消火栓和灭火器;厂区室外消火栓4个,市内消火栓19个;生产区域中,导电间、非导电间以及研磨间均设置一个二氧化碳灭火器箱;生产办公区、仓库、辅助设备间配置干粉灭火器;在洁净室和机房配置二氧化碳灭火器;7、消防设施的器材的季度、年度检查保养维护外包给专业公司;消防阀门、消防栓、雨淋阀、报警设备每季度检查1次;灭火器每月检查1次;烟感和温感火灾自动报警器、消火栓抽样测试每年1次;8、车间使用的危险化学品(多余的丙酮容器)按照日使用量存放在经FM认证的金属防爆槽和防爆柜中;7、企业HSE部门负责防火管理和安全工作,部门制定的紧急应变计划(RED BOOK)包括:化学品泄漏管理程序;易燃、可燃液体操作和储存流程;放热物质的操作;操作和储藏过氧化物有机物;火灾疏散/紧急应变程序;我们被告知,企业每年举行2次化学品泄漏、火灾疏散及逃生模拟演习;8、企业保安实行外包,目前白天有4人,夜间有3人,休息日有3人。
保安巡逻频度为1小时1次,并执行严格的人员、货物出入登记;五、风险评价(一)风险概述1、火灾、爆炸导电胶和非导电胶的生产主要是在剪切机中进行预热,再把树脂辅助材料按一定配比混合,最后冷冻保存的过程。
生产原料中固化剂、催化剂等为可燃物质,局部工艺段又使用易燃固体银粉。
依据中国国家消防标准,工厂的生产火灾危险性类别为丙类。
在生产过程中,合成树脂受机械摩擦、混合、搅拌可能产生一定的静电荷,一旦放电便产生火花,而设备故障、过热、物料受到冲击、电气短路等原因也会引燃可燃粉尘和化学易燃品。
同时在流水操作过程中,有关人员需使用到化学物品丙酮。
虽然使用量较少(10kg),但是如果对化学品管理使用不善,也可能引发意外事故。
目前整个厂区配有烟、温感火灾探测器和自动灭火系统,厂房仓库现配有喷淋系统,消防配置总体较好,而且全厂全面禁烟,有安全管理制度和重大危险源应急处理方案,安保设施亦较全,但企业方面仍需注意防止电气设备、线路老化短路起火的风险。
总体上分析,企业火灾风险中等。
2、停电事故目前企业所在区由南汇供电所两路进电,据介绍,近五年上海南汇供电所的供电一直都比较稳定,偶尔的2次停电都有事先通知,同时企业自身做好应对准备,未曾有过停电中断引起的损失。
但是一旦出现外部电力或内部变配电意外事故,导致电力供应中断,由于受企业生产工艺的影响,这段时间内将影响生产设备正在处理的中间产品,以及冰柜冷冻储存系统无法正常工作,导致部分中间产品受损。
