红外光谱的八个峰区
红外各基团特征峰对照表

红外各基团特征峰对照表一、红外吸收光谱中的重要区段:1) O-H、N-H伸缩振动区(3750~3000 cm-1)2) 不饱和碳上的C-H伸缩振动区(3300~3000 cm-1)不饱和碳(三键和双键、苯环)上的C-H的伸缩振动在3300~3000 cm-1区域中出现不同的吸收峰。
3) C-H伸缩振动区(3000~2700 cm-1)饱和碳上的C-H伸缩振动(包括醛基上的C-H)4) 叁键和累积双键区(2400~2100 cm-1)波数在2400~2100 cm-1区域内的谱带较少。
5) 羰基的伸缩振动区(1900~1650 cm-1)羰基的吸收最常见出现的区域为1755~1670 cm-1。
由于羰基的电偶极矩较大,一般吸收都很强烈,常成为IR光谱中的第一强峰。
6) 双键伸缩振动区(1690~1500 cm-1)该区主要包括C=C,C=N,N=N,N=O等的伸缩振动以及苯环的骨架振动(σ)。
C=C7) X-H面内弯曲振动及X-Y伸缩振动区(1475~1000 cm-1)这个区域主要包括C-H面内弯曲振动, C-O、C-X(卤素)等伸缩振动, 以及C-C 单键骨架振动等。
该区域是指纹区的一部分。
8) C-H面外弯曲振动区(1000~650 cm-1)烯烃、芳烃的C-H面外弯曲振动(σC-H)在1000~650 cm-1区。
苯环邻二取代:770~735cm-1;苯环间二取代:710~690、810~750cm-1;苯环对二取代:830~810cm-1具体对照表如下所示:(其中:VS:很强;W:弱;S:强;VW:很弱;m:中等;w:宽)1、O-H、N-H2、C-H3、C-H45、羰基的伸缩振动区(1900—1650 cm-1)67、X-H面内弯曲振动及X-Y伸缩振动区(1475—1000 cm-1)8二、指纹区和官能团区从第1-6区的吸收都有一个共同点,每一红外吸收峰都和一定的官能团相对应,此区域从而称为官能团区。
红外光谱各基团出峰位置
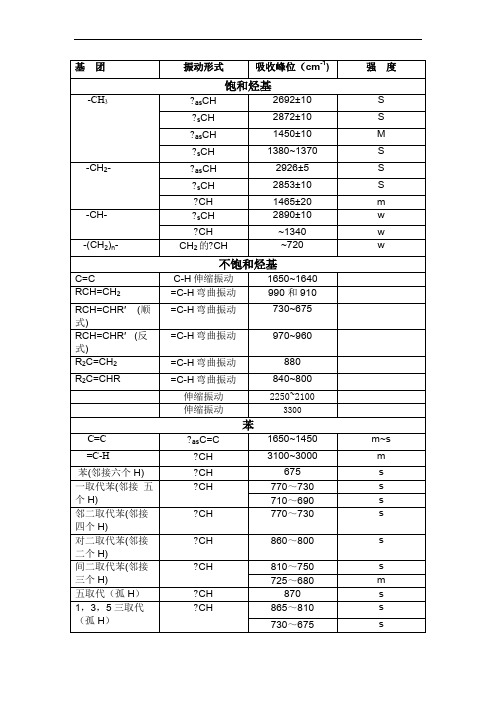
振动形式
吸收峰位(cm-1)
强 度
饱和烃基
-CH3
asCH
2692±10
S
sCH
2872±10
S
asCH
1450±10
M
sCH
1380~1370
S
-CH2-
asCH
2926±5
S
sCH
2853±10
S
CH
1465±20
m
-CH-
sCH
2890±10
w
CH
~1340
w
-(CH2)n-
CH2的CH
C-OH(酚)
C-O
1200~1300
s(宽)
醚
R-O-R’
asc-o-c
1210~1050
s(不特征)
Ar-O-R
asc-o-c
1300~1200
s(不特征)
Ar-O-R
sc-o-c
1055~1000
m(不特征)
R-OCH3
sCH3
2830~2815
m s
Ar-OCH3
sCH3
2850
s(宽)
羰基
s
R-NO2
sNO2
1385~1350
s
R-NO2
sC-N
920~830
w
Ar-NO2
asNO2
1550~1510
s
Ar-NO2
sNO2
1365~1300
s
Ar-NO2
sC-N
880~845
w
酮(RCOR’)
C=O
1720~1715
VS(很特征)
醛(RCHO)
红外光谱各个峰的归属

红外光谱中的各个峰的归属取决于它们对应的官能团或化学键。
以下是红外光谱中一些主要峰的归属:1.基频峰:分子吸收一定频率的红外线,振动能级从基态跃迁至第一振动激发态产生的吸收峰,基
频峰的峰位等于分子或者基团的振动频率,强度大,是红外的主要吸收峰。
2.泛频峰:分子的振动能级从基态跃迁至第二振动激发态、第三振动激发态等高能态时产生的吸收
峰,此类峰强度弱,难辨认,却增加了光谱的特征性。
3.特征峰和指纹峰:特征峰是可用于鉴别官能团存在的吸收峰,对应于分子中某化学键或基团的振
动形式,同一基团的振动频率总是出现在一定区域;而指纹区吸收峰特征性强,对分子结构的变化高度敏感,能够区分不同化合物结构上的微小差异。
具体到每个分子,红外光谱的各个峰归属需要根据具体的分子结构和官能团来确定。
因此,对于具体的红外光谱分析,需要结合分子的化学结构进行解析。
红外光谱特征吸收峰讲解

红外光谱特征吸收峰讲解在红外光谱中,红外光与物质分子相互作用,使得分子中不同的化学键发生振动,从而吸收特定的红外辐射能量。
这些振动涉及键的拉伸、弯曲、扭转等运动,其振动频率和强度与分子结构和化学键的性质有关。
因此,红外光谱特征吸收峰可以提供分子结构和化学键信息。
红外光谱的横坐标是波数(cm-1),波数是光的频率的倒数,与光的能量成反比。
而纵坐标则是吸光度,表示物质对红外光的吸收程度。
吸收峰的位置可以通过测量吸收带的最大峰值处的波数来确定。
下面介绍一些常见的红外光谱特征吸收峰:1. 羧酸吸收峰(1700-1715 cm-1):羧酸的OH键弯曲振动和C=O双键伸缩振动引起的强吸收峰。
该吸收峰可以用来鉴别羧酸。
2. 羧酸盐吸收峰(1560-1640 cm-1):与羧酸吸收峰相比,羧酸盐的C=O双键伸缩振动引起的吸收峰位置左移。
3. 醛和酮吸收峰(1690-1750 cm-1):与羧酸吸收峰类似,它们也是由于C=O双键伸缩而引起的吸收峰。
但醛和酮的吸收峰位置通常比羧酸略高。
4. 羧酸和酮醇吸收峰(3200-3550 cm-1):由于羟基(OH)的振动引起的宽吸收峰。
在红外光谱中,羧酸和酮醇的羟基吸收峰位置和形状相似。
5. 烷基的C-H伸缩振动吸收峰(2850-3000 cm-1):烷基的C-H键伸缩振动引起的吸收峰。
短直链烷烃的C-H伸缩振动吸收峰出现在2850-2960 cm-1的范围内,而长直链烷烃的C-H伸缩振动峰则出现在2960-3000 cm-16. 芳香族化合物的C-H伸缩振动吸收峰(3020-3100 cm-1):芳香环中C-H键伸缩振动引起的吸收峰的位置通常在3020-3100 cm-17. N-H伸缩振动吸收峰(3300-3500 cm-1):含氮化合物中的氮氢键伸缩振动引起的吸收峰。
在氮-氢键的存在下,吸收峰位置可能出现在3300-3500 cm-1之间。
这些是红外光谱中常见的一些特征吸收峰范围和其对应的化学结构或基团。
红外光谱总结

第2章红外光谱通常红外光谱(infrared spectroscopy, IR)就是指波长2〜25 pm的吸收光谱(即中红外区), 这段波长范I制反映出分子中原子间的振动与变角运动。
分子在振动的同时还会发生转动运动, 虽然分子的转动所涉及的能量变化较小,处在远红外区域,但转动运动影响振动的偶极矩变化, 因而在红外光谱区实际所测的谱图就是分子的振动与转动运动的加与表现,因此红外光谱又称为分子振转光谱。
红外光谱可以应用于化合物分子结构的测定、未知物鉴定以及混合物成分分析。
2、1红外光谱的基本原理2、1、1红外吸收光谱1、当一束具有连续波长的红外光通过物质,物质分子中某个基团的振动频率或转动频率与红外光的频率一样时,分子就吸收能量由原来的基态振(转)动能级跃迁到能屋较高的振 (转)动能级,分子吸收红外辐射后发生振动与转动能级的跃迁,该处波长的光就被物质吸收。
近红外区:O-H、N-H与C-H键的倍频吸收或组频吸收,吸收强度一般比较弱;中红外区:绝人多数有机与无机化合物的基频吸收所在,主要就是振动能级的跃迁; 远红外区:乡子纯转动能级跃迁及晶体的晶格振动。
3、波数(巧单位就是cm"。
波长与波数的关系就是:-_1 1044、胡克定律:7勺叫其中:一折合质量,"=叫+叫,单位为kg;K_七学键力常数,与化学键的键能呈正比,单位为Zm」; 亍——波数;c——真空中的光速。
(1)因为%三c> Kc=c> Kc_c,红外频率比三c> v c = c>v c-c Q(2)与碳原子城建的其她原子,随着其原子质屋的增人,折合质量也增人,则红外波数减小。
(3)与氢原子相连的化学键的折合质量都小,红外吸收在高波数区。
(4)弯曲振动比伸缩振动容易湾曲振动的K均较小,故弯曲振动吸收在低波数区。
5、光谱选律:原子与分子与电磁波作用发生能级跃迁就是要服从一定的规律的,这些规律由量子化学解释。
红外光谱官能团特征峰

红外光谱官能团特征峰红外光谱官能团特征峰一、前言红外光谱是一种分析物质分子结构的非常有力的手段,广泛应用于物质科学研究中。
在红外光谱谱图中,不同官能团所对应的特征峰可以为我们提供该物质的结构信息。
本文将详细介绍有关红外光谱中常见官能团的特征峰,以及这些峰的谱带位置和强度信息。
二、羟基官能团羟基官能团是一种非常常见的官能团,广泛存在于生物分子中。
在红外光谱谱图中,羟基官能团所对应的特征峰通常出现在3200-3600cm^{-1}的区域,并且具有比较高的峰强。
此外,酚类化合物中的羟基官能团也会表现出类似的特征峰。
三、胺基官能团胺基官能团是另一种常见的官能团,存在于很多有机物和生物分子中。
在红外光谱谱图中,胺基官能团所对应的特征峰出现在3300-3500cm^{-1}的区域,并且峰强度较高。
此外,氨基酸等生物分子中的胺基官能团也有类似的特征峰。
四、羰基官能团羰基官能团指的是带有碳氧双键的官能团,常见于酮和酯等有机化合物中。
在红外光谱谱图中,羰基官能团所对应的特征峰出现在1650-1750 cm^{-1}的区域,并且峰强度较高。
需要注意的是,醛类化合物中的羰基官能团与酮和酯的区别在于其特征峰位置稍有不同,出现在1700-1750 cm^{-1}的区域。
五、烷基官能团烷基官能团主要指的是单烷基、双烷基和三烷基等基团,常见于烷烃及其衍生物中。
在红外光谱谱图中,烷基官能团并没有明显的特征峰,但是可以通过一些指纹峰来进行鉴别。
例如,对于单烷基官能团,其CH_3和CH_2的拉伸振动谱带会出现在2850 cm^{-1}和2950 cm^{-1}的区域。
六、芳香官能团芳香官能团指的是苯环等碳环结构中的键与无机物键的官能团,常见于芳香族化合物中。
在红外光谱谱图中,芳香官能团所对应的特征峰通常出现在1400-1600 cm^{-1}的区域,具有较高的峰强。
此外,苯环上的苯基羟基等同样有特征峰,且位置和强度与羟基官能团类似。
第6章红外光谱

第六页,编辑于星期日:十七点 八分。
▪ 量子力学处理
对于双原子分子,由量子力学原理可推出如下公 式:
E
(1) h 2 2
k
υ=0、1、2、3…
υ为振动量子数
Eυ为与振动量子数υ相对应的体系能量;
利用经典力学原理可将上式改为:
E
(1)hv
2
υ=0、1、2、3…
从上式可看出,当υ=0时,体系能量不为零,这称作 零点能,产生跃迁的选律为△υ=±1。
3650~3580(游离) 3550~3450(二聚体) 3400~3200(多聚体) 3600-2500(分子内缔合)
1050(伯) 1100(仲) 1150(叔) 1200(酚)
1500~1250 650
尖 中强,较尖
强,宽 宽,散 强,有时发生裂分
面内弯曲,强,宽 面外弯曲,宽
第三十六页,编辑于星期日:十七点 八分。
第二十一页,编辑于星期日:十七点 八分。
CO1307 125 .4161160(cm1)
1216
CO1307
12 1730(cm1) 1216
1216
第二十二页,编辑于星期日:十七点 八分。
内部因素 诱导效应 共轭效应 空间效应 跨环效应 氢键
第二十三页,编辑于星期日:十七点 八分。
四、有机化合物的红外特征吸收
❖ 中红外光区 ❖ 2.5 ~ 25µm ❖ 4000~400cm-1
❖ 远红外光区 ❖ 25 ~ 1000µm
1、红外吸收光谱
第三页,编辑于星期日:十七点 八分。
2、红外光谱的表示方法
红外光谱的横坐标是波长(λ)或波数(σ) 纵坐标是透光率(T%)。
红外光谱峰是“倒峰”。
红外光谱的八个重要区段

红外光谱涉及到物质中分子的振动和转动。
不同的分子在红外光谱中表现出特定的吸收峰,这些峰对应于不同类型的分子振动和转动。
以下是红外光谱的八个重要区段,以波数表示:
1. 3650-3200 cm^-1:这个区段对应于羟基(-OH) 的伸缩振动。
这是醇、酚和羧酸等功能团的特征峰。
2. 3100-3000 cm^-1:这是烷基和芳香烃的C-H伸缩振动区段。
不同类型的碳氢键会在这个区段显示吸收峰。
3. 3000-2800 cm^-1:这个区段同样是C-H伸缩振动,但主要是饱和烷烃的伸缩振动。
通过观察峰的位置和强度,可以推断分子中碳氢键的饱和度。
4. 1800-1700 cm^-1:这个区段对应于羰基(C=O) 的伸缩振动,是醛、酮和羧酸等官能团的特征峰。
5. 1600-1500 cm^-1:这是芳香族化合物的C=C伸缩振动区段。
芳香环中的碳碳双键会在这个区段显示吸收峰。
6. 1450-1350 cm^-1:这个区段对应于甲基和亚甲基(CH3和CH2) 的弯曲振动。
7. 1300-1000 cm^-1:这个区段包括许多不同的振动,如C-O伸缩振动和C-N伸缩振动。
在这个区段,有时可以观察到一些特定官能团的指纹峰。
8. 700-600 cm^-1:这是指纹区,包含了分子中一些特殊键的振动。
例如,C-Cl和C-Br的振动通常在这个区段显示。
这些区段提供了红外光谱中一些常见官能团的指示,帮助化学家确定分子的结构和组成。
需要注意的是,不同的分子可能会在不同的波数范围内显示吸收峰,因此解释红外光谱时需要考虑多种可能性。
红外光谱的特征峰区

烯:3090~3010(m)
芳环:~3030
饱和C━H伸缩振动区域
3000~2800
C━H伸缩
烷烃:
━CH3:2962±10(s)
2872±10(s)
━CH2:2926±10(s)
2853±10(s)
3000cm-1为ν=C━H饱和与不饱和的分界线( 的ν=C━H吸收在3050 cm-1处)
1500(v);1450(m)
C=N伸缩
亚胺、肟1690~1640(v)
N=N伸缩
偶氮1630~1575(v)
饱和C━H面内弯曲振动区域
1475~1300
C━H面内弯曲
烷烃:
CH3:1470~1430(m)
1380~1370(s)
CH2:1485~1445(m)
CH:1340(w)
当存在>C(CH3)2和━C(CH3)3基团时,1380~1370 cm-1处为双峰
不饱和C━H面内弯曲振动区域
1000~650
=C━H面外弯曲
烯:
单取代: 995~985(s);915~905
顺式取代:~690(s)
反式取代:970~960(s)
同碳二取代:895~885
三取代:840~790(s)
芳烃:
5个相邻氢原子:770~730(vs)
710~640(s)
4个相邻氢原子:1770(s)
酯:1750~1735(s)
醛:1740~1720(s)
酮1725~1705(s)
酸:1725~1700(s)
酰胺:1690~1630(s)
酸酐两峰相距60 cm-1
双键伸缩振动区域
1675~1500
C=C伸缩
红外光谱学习必知知识

(1) 通常将红外光谱分为三个区域:近红外区(13330~4000cm-1)、中红外区(4000~400cm-1)和远红外区(400~10cm-1)。
通常所说的红外光谱即指中红外光谱。
(2) 按吸收峰的来源,可以将4000~400cm-1的红外光谱图大体上分为特征频率区(4000~1300cm-1 )以及指纹区(1300~400cm-1 )两个区域。
其中特征频率区中的吸收峰基本是由基团的伸缩振动产生,数目不是很多,但具有很强的特征性,因此在基团鉴定工作上很有价值,主要用于鉴定官能团。
如羰基,不论是在酮、酸、酯或酰胺等类化合物中,其伸缩振动总是在1700cm-1左右出现一个强吸收峰,如谱图中1700cm-1左右有一个强吸收峰,则大致可以断定分子中有羰基。
指纹区的情况不同,该区峰多而复杂,没有强的特征性,主要是由一些单键C-O、C-N和C-X(卤素原子)等的伸缩振动及C-H、O-H等含氢基团的弯曲振动以及C-C骨架振动产生。
当分子结构稍有不同时,该区的吸收就有细微的差异。
这种情况就像每个人都有不同的指纹一样,因而称为指纹区。
指|纹区对于区别结构类似的化合物很有帮助。
(3) 在定性分析过程中,除了获得清晰可靠的图谱外,最重要的是对谱图作出正确的解析。
所谓谱图的解析就是根据实验所测绘的红外光谱图的吸收峰位置、强度和形状,利用基团振动频率与分子结构的关系,确定吸收带的归属,确认分子中所含的基团或键,进而推定分子的结构。
简单地说,就是根据红外光谱所提供的信息,正确地把化合物的结构翻译”出来。
往往还需结合其他实验资料,如相对分子质量、物理常数、紫外光谱、核磁共振波谱及质谱等数据才能正确判断其结构。
红外光谱的分区-1400-2500cm :这是X-H单键的伸缩振动区。
2500-2000cm-1:此处为叁键和累积双键伸缩振动区1 、■2000-1500cm-:此处为双键伸缩振动区1500-600cm-1:此区域主要提供C-H弯曲振动的信息(4) 红外图谱的解析步骤1) 准备工作在进行未知物光谱解析之前,必须对样品有透彻的了解,例如样品的来源、外观,根据样品存在的形态,选择适当的制样方法;注意视察样品的颜色、气味等,它们住往是判断未知物结构的佐证。
红外各基团特征峰对照表

红外各基团特征峰对照表红外光谱技术是一种常用的分析方法,可以用于确定化学物质的结构和化学键的类型。
在红外光谱图中,各种化学基团具有独特的特征峰,这些特征峰的位置和强度可以提供有关分子结构的重要信息。
下面是一份红外各基团特征峰对照表,以帮助研究者快速准确地解读红外光谱图。
1. 羟基(OH):在红外光谱图中,羟基通常表现为宽而强的峰,位置在3200-3600 cm^-1附近。
注意,一些羧酸中的羟基可能会表现为更宽的峰。
2. 胺基(NH):胺基通常表现为尖锐的峰,位置在3200-3500 cm^-1附近。
胺基峰的强度通常比羟基峰要弱。
3. 酯基(C=O):酯基的特征峰通常出现在1740-1750 cm^-1附近。
这个峰是一个强吸收峰,显示出酯基的存在。
4. 羧基(C=O):羧基通常表现为一个宽而强的吸收峰,位置在1600-1800 cm^-1之间。
注意,羧酸中的羟基峰通常与羧基峰有重叠。
5. 脂肪烷基(C-H):脂肪烷基的特征峰通常出现在2850-3000cm^-1之间。
这个区域有多个吸收峰,每个峰对应于不同类型的C-H键。
6. 脂肪酸基(C-H):脂肪酸基的特征峰通常出现在2800-3000cm^-1之间。
与脂肪烷基相比,脂肪酸基中的羧基和烯丙基会导致峰的位置和强度发生变化。
7. 烯丙基(C=C):烯丙基的特征峰通常出现在1600-1680 cm^-1之间。
这个峰通常比较强,并且在红外光谱图中相对容易识别。
8. 芳香环(C=C):芳香环中的碳碳双键通常表现为一个强的吸收峰,位置在1400-1600 cm^-1之间。
注意,芳香环的不同取代基可能会导致峰的位置发生变化。
9. 卤代烷基(C-X):卤代烷基中的碳卤键(如C-Cl,C-Br和C-I)通常表现为一个尖锐的峰,位置在600-800 cm^-1之间。
不同卤素的特征峰位置有所不同。
10. 硫醇(S-H):硫醇的特征峰通常出现在2500-2600 cm^-1之间。
第三章 红外光谱

不特征
胺
类别
键和官能团
C=O R-CHO C=O
拉
1750-1680 2720
伸
(cm-1)
说
明
醛、酮
羧酸
1770-1750(缔合时在1710) 气相在3550,液固缔合时在 3000-2500(宽峰) 1800 1860-1800 1735 1690-1650 3520,3380(游离)缔合降低100 2260-2210 1800-1750
1670(弱-无)
ห้องสมุดไป่ตู้
无
共轭烯烃
与烯烃同
向低波数位移,变宽
与烯烃同
吸收峰 振
动
化合物
C=C,CC,C=C-C=C C-H拉伸 (或伸缩) 苯环 3310-3300 一取代 对称 2140-2100弱 无
C-H弯析
炔烃
较强
非对称二取代2260-2190弱
700-600 强
芳烃
取代芳烃
3110-3010中
一、红外光谱的八个峰区
4000-1500cm-1区域又叫官能团区. 该区域出现的吸 收峰,较为稀疏,容易辨认. 1500-400cm-1区域又叫指纹区. 这一区域主要是: C-C、C-N、C-O 等单键和各种弯曲振动的
吸收峰,其特点是谱带密集、难以辨认。
二、重要官能团的红外特征吸收
C-H拉伸(或伸缩)
1600中 1500强
1580弱 1450弱-无
670弱 倍频 2000-1650 一取代770-730, 710-690强 二取代
同芳烃
同芳烃
邻- 770-735强 间- 810-750强 710-690中 对- 833-810强
泛频 2000-1660
10第八章红外光谱

制作材料
工作温度
(二). 吸收池
红外吸收池使用可透过红外的材料制成窗片;不同的样品状 态(固、液、气态)使用不同的样品池,固态样品可与晶体混 合压片制成。
(三). 单色器
狭缝越窄,分辨率越高,但光源到达检测器的能量输出减少, 这在红外光谱分析中尤为突出。
(四). 检测器及记录仪
红外光能量低,因此常用热电偶、测热辐射计、热释电检测
2.了解试样的来源、性质及其它实验资料
可以缩小结构的推测范围。根据试样的元素分析值及相 对分子质量得出的分子式,可以计算不饱和度,进而估计分 子结构式中是否含有双键、三键及芳香环,并可验证光谱解 析结果的合理性。沸点、熔点等性质可作为光谱分析的旁证。
不饱和度的计算
2n 2 a b U 2
10.3
有机化合物基团的特征频率
总结大量红外光谱资料后,发现具有同一类型 化学键或官能团的不同化合物,其红外吸收频 率总是出现在一定的波数范围内,我们把这种 能代表某基团,并有较高强度的吸收峰,称为 该基团的特征吸收峰(又称官能团吸收峰)。
1 红外光谱的八个峰区
4000-1500cm-1区域又叫官能团区. 该区域出现的吸 收峰,较为稀疏,容易辨认.
10.5 红外光谱仪
一.主要部件
(t灯和硅碳棒。
类型 Nernst 灯
硅碳棒
特 点 高波数区(> 1000cm-1)有 Zr, Th, Y 1700oC 更强的发射;稳定性好; 氧化物 机械强度差; 但价格较高。 低波数区光强较大;波数 o 1200-1500 C 范围更广; SiC 坚固、发光面积大。
1)沸点低易挥发的样品:液体池法。
2)高沸点的样品:液膜法(夹于两盐片之间)。 3)固体样品可溶于CS2或CCl4等无强吸收的溶液中。
红外光谱法

三、分子振动频率的计算公式
例:HCl 分子,其振动形式为同时伸长和同时缩短。
Cl
H
近似为简谐振动:
或
c-光速,3×108 m/s
k-化学键的力常数,N/m μ-折合质量,kg
影响键力常数的主要因素:
a、键级
b、同一化学键成键原子的杂化状态
化学 键 C―C
C =C C≡C
键长 (nm) 0.154
O C Cl
νAr-C = 880~862 cm-1 νC=O = 1774 cm-1
1773 cm-1 1736 cm-1
(2)吸收峰减少的原因
① 红外非活性振动(有高度对称结构的分子,振动过程中不引起偶极矩 变化,虽有振动形式存在,但不产生红外吸收峰)。 ② 简并,即两种振动具有相同频率,只出现一个峰。 ③ 强峰往往要覆盖与它频率相近的弱而窄的峰。 ④ 吸收峰落在仪器的检测范围之外。 ⑤ 受仪器分辨率所限,有时挨的很近的两个峰仪器分辨不出,只表现为
3000
2000
-CC-H ~2120
1000
游离OH ~3600 缔合OH ~3300 -NH2 3300~ 3500 -NHR C=C-H
COOH ~3000 -SH 2600~2550 -COH 2820,2720 ~2850 ~2870 ~2925, CH2
~1370 ~1550 -NO2
②不对称伸缩振动(υas)
2)变形振动:键角发生周期性变化,键长不变的振动。
①面内变形振动
a、剪式振动(δ)
C H H
b、 面内摇摆振动(ρ)
②面外变形振动 a、面外摇摆振动(ω) b、面外扭曲振动(τ)
剪式振动
C
H H
H
红外各基团特征峰对照表

红外各基团特征峰对照表一、红外吸收光谱中的重要区段:1) O-H、N-H伸缩振动区(3750~3000 cm-1)2) 不饱和碳上的C-H伸缩振动区(3300~3000 cm-1)不饱和碳(三键和双键、苯环)上的C-H的伸缩振动在3300~3000 cm-1区域中出现不同的吸收峰。
3) C-H伸缩振动区(3000~2700 cm-1)饱和碳上的C-H伸缩振动(包括醛基上的C-H)4) 叁键和累积双键区(2400~2100 cm-1)波数在2400~2100 cm-1区域内的谱带较少。
5) 羰基的伸缩振动区(1900~1650 cm-1)羰基的吸收最常见出现的区域为1755~1670 cm-1。
由于羰基的电偶极矩较大,一般吸收都很强烈,常成为IR光谱中的第一强峰。
6) 双键伸缩振动区(1690~1500 cm-1)该区主要包括C=C,C=N,N=N,N=O等的伸缩振动以及苯环的骨架振动(σ)。
C=C 7) X-H面内弯曲振动及X-Y伸缩振动区(1475~1000 cm-1)这个区域主要包括C-H面内弯曲振动, C-O、C-X(卤素)等伸缩振动, 以及C-C 单键骨架振动等。
该区域是指纹区的一部分。
8) C-H面外弯曲振动区(1000~650 cm-1)烯烃、芳烃的C-H面外弯曲振动(σC-H)在1000~650 cm-1区。
苯环邻二取代:770~735cm-1;苯环间二取代:710~690、810~750cm-1;苯环对二取代:830~810cm-1具体对照表如下所示:(其中:VS:很强;W:弱;S:强;VW:很弱;m:中等;w:宽)1、O-H、N-H2、C-H3、C-H45、羰基的伸缩振动区(1900—1650 cm-1)6-178二、指纹区和官能团区从第1-6区的吸收都有一个共同点,每一红外吸收峰都和一定的官能团相对应,此区域从而称为官能团区。
官能团区的每个吸收峰都表示某一官能团的存在,原则上每个吸收峰均可以找到归属。
红外光谱的八个峰区

4个相邻氢原子:770~735(vs)
3个相邻氢原子:810~750(vs)
2个相邻氢原子:860~800(vs)
1个氢原子:900~860(m)
炔665~625(s)
≡C━H面
外外弯曲
双
缩
区2400~2100C≡C伸缩
C≡N伸缩
━N=C=O炔:RC≡CH2140~2100(s)
RC≡CR'2260~2190(vw)
腈2260~2240(m)
异氰酸酯2275~2240(s)
烯酮~2150
酸酐:1850~1800(s)
1790~1740(s)
酰卤:1815~1770(s)
酯:1750~1735(s)
体,ν
N━H吸收都比胺1º:3500(m)和3400(m)
2º:3500~3300(m)
ν
O━H吸收尖而弱亚胺:3400~3300(m)
酰胺:3350(m)和3180(m)
一取代酰胺:3320~3060(m)
醛基中的不饱和
C━H伸
缩振动
区域
饱和C━
H伸缩
振动区
域
叁键
累积
键伸
振动
域≡C━H伸缩炔3300(s)
醛:1740~1720(s)
酮1725~1705(s)
酸:1725~1700(s)
酰胺:1690~1630(s)
烯:1680~1620(v)
芳环:1600(v);1580(m)
1500(v);1450(m)
亚胺、肟1690~1640ห้องสมุดไป่ตู้v)
偶氮1630~1575(v)酸酐两峰相距60cm-1伸缩
━O=C=O
各类有机化合物的红外特征吸收

各类有机化合物的红外特征吸收2007-02-06 21:45:09| 分类:药物分析| 标签:|字号大中小订阅第一峰区(4000-2500cm-1)X-H 伸缩振动吸收范围。
(1). O-H醇与酚:游离态--3640~3610cm-1,峰形尖锐。
缔合态--3300cm-1附近,峰形宽而钝羧酸:3300~2500cm-1,中心约3000cm-1,谱带宽而散;(2) . N-H胺类:游离——3500~3300cm-1缔合——吸收位置降低约100cm-1伯胺:3500,3400 cm-1(吸收强度比羟基弱)仲胺:3400 cm-1(吸收峰比羟基要尖锐)叔胺:无吸收酰胺:伯酰胺:3350,3150 cm-1 附近出现双峰仲酰胺:3200 cm-1 附近出现一条谱带叔酰胺:无吸收(3). C-H烃类: 3300~2700 cm-1范围,3000 cm-1是分界线。
不饱和碳(三键、双键及苯环)>3000 cm-1饱和碳(除三元环外)<3000 cm-1饱和烃基:3000~2700 cm-1,四个峰-CH3:~2960(s)、~2870 cm-1(m)-CH2-:~2925(s)、~2850 cm-1(s)>CH-:~2890 cm-1炔烃:~3300 cm-1,峰很尖锐,与nOH 和nNH有重叠;烯烃、芳烃:3100~3000 cm-1两种氢易于混淆醛基:2820 cm-1,2740~2720 cm-1,两个中强峰,区别醛和酮的特征谱带。
巯基:2600~2500 cm-1,谱带尖锐,容易识别叁键:-C≡C-、-C≡N累积双键:>C=C=C<、-N=C=O、-N=C=S特点:谱带为中等强度吸收或弱吸收。
干扰少, 容易识别。
1.C≡C 2280~2100cm-1 乙炔及全对称双取代炔,无红外吸收。
2.C≡N 2250~2240cm-1,谱带较C≡C强。
C≡N与苯环或双键共轭,谱带向低波数位移20~30cm-1。
红外特征峰位置总结
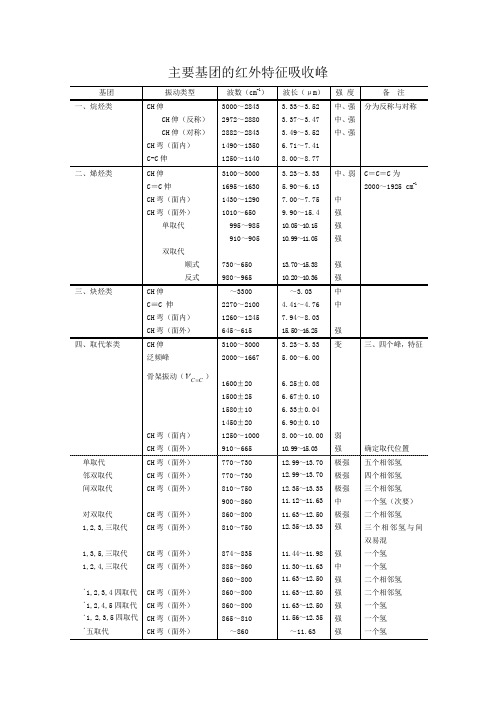
主要基团的红外特征吸收峰基团 振动类型 波数(cm-1) 波长(μm) 强 度 备 注一、烷烃类 CH伸CH伸(反称)CH伸(对称)CH弯(面内)C-C伸 3000~28432972~28802882~28431490~13501250~11403.33~3.523.37~3.473.49~3.526.71~7.418.00~8.77中、强中、强中、强分为反称与对称二、烯烃类 CH伸C=C伸CH弯(面内)CH弯(面外)单取代双取代顺式反式 3100~30001695~16301430~12901010~650995~985910~905730~650980~9653.23~3.335.90~6.137.00~7.759.90~15.410.05~10.1510.99~11.0513.70~15.3810.20~10.36中、弱中强强强强强C=C=C为2000~1925 cm-1三、炔烃类 CH伸C≡C 伸CH弯(面内)CH弯(面外)~33002270~21001260~1245645~615~3.034.41~4.767.94~8.0315.50~16.25中中强四、取代苯类 CH伸泛频峰骨架振动(CC)CH弯(面内)CH弯(面外) 3100~30002000~16671600±201500±251580±101450±201250~1000910~6653.23~3.335.00~6.006.25±0.086.67±0.106.33±0.046.90±0.108.00~10.0010.99~15.03变弱强三、四个峰,特征确定取代位置单取代邻双取代间双取代对双取代1,2,3,三取代1,3,5,三取代 1,2,4,三取代﹡1,2,3,4四取代 ﹡1,2,4,5四取代 ﹡1,2,3,5四取代 ﹡五取代 CH弯(面外)CH弯(面外)CH弯(面外)CH弯(面外)CH弯(面外)CH弯(面外)CH弯(面外)CH弯(面外)CH弯(面外)CH弯(面外)CH弯(面外)770~730770~730810~750900~860860~800810~750874~835885~860860~800860~800860~800865~810~86012.99~13.7012.99~13.7012.35~13.3311.12~11.6311.63~12.5012.35~13.3311.44~11.9811.30~11.6311.63~12.5011.63~12.5011.63~12.5011.56~12.35~11.63极强极强极强中极强强强中强强强强强五个相邻氢四个相邻氢三个相邻氢一个氢(次要)二个相邻氢三个相邻氢与间双易混一个氢一个氢二个相邻氢二个相邻氢一个氢一个氢一个氢六、醚类 C—O—C伸 1270~1010 强 或标C—O伸脂链醚 C—O—C伸 1225~1060 强饱和脂肪醛 C=O伸 ~1725 强OH弯(面外) 950~900 弱 3000cm为中心 脂肪酸链酸酐 C=O伸(反称) 1850~1800 强 共轭时每个谱带强十三、酰胺(脂肪与芳香酰胺数据类似) NH伸C=O伸NH弯(面内)C—N伸3500~31001680~16301640~15501420~14002.86~3.225.95~6.136.10~6.457.04~7.14强强强中伯酰胺双峰仲酰胺单峰谱带Ⅰ谱带Ⅱ谱带Ⅲ伯酰胺 仲酰胺 叔酰胺 NH伸(反称)(对称)C=O伸NH弯(剪式)C—N伸NH2面内摇NH2面外摇NH伸C=O伸NH弯+C—N伸C—N伸+NH弯C=O伸~3350~31801680~16501650~16201420~1400~1150750~600~32701680~16301570~15151310~12001670~1630~2.98~3.145.95~6.066.06~6.157.04~7.14~8.701.33~1.67~3.095.95~6.136.37~6.607.63~8.335.99~6.13强强强强中弱中强强中中两峰重合两峰重合十四、氰类化合物脂肪族氰α、β芳香氰 α、β不饱和氰 C≡N伸C≡N伸C≡N伸2260~22402240~22202235~22154.43~4.464.46~4.514.47~4.52强强强十五、硝基化合物R—NO2 Ar—NO2NO2伸(反称)NO2伸(对称)NO2伸(反称)NO2伸(对称)1590~15301390~13501530~15101350~13306.29~6.547.19~7.416.54~6.627.41~7.52强强强强。
红外各基团峰位置
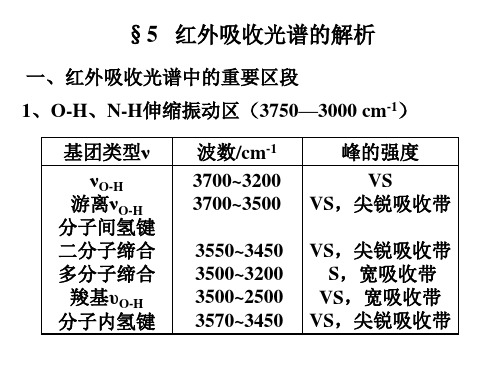
3、C-H伸缩振动区(3000—2700 cm-1) 基团类型ν -CH3 -CH2≡C-H -CHO 波数/cm-1 2960及2870 2930及2850 2890 2720 峰的强度 VS VS W W
4、叁键和累积双键区(2400—2100 cm-1)
基团类型ν R-C≡C-H RC≡CR` RC≡CR R-C≡N R-N=N=N R-N=C=N-R -C=C=C-C=C=O -C=C=N O=C=O R-N=C=O 波数/cm-1 2140~2100 2260~2190 无吸收 2260~2120 2160~2120 2155~2130 ~1950 ~2150 ~2000 ~2349 2275~2250 峰的强度 m 可变 S S S S
(5)、查阅标准谱图;
(6)、确定可能的结构。
五、解析谱图注意事项 1、IR光谱是测定化合物结构的,只有分子在振动的状 态下伴随有偶极矩变化者才能有红外吸收。对映异构体 具有相同的IR光谱,不能用IR光谱来鉴别这类异构体。
2、某些吸收峰不存在,可以确信某基团不存在;相反, 吸收峰存在并不是该基团存在的确认,应考虑杂质的干 扰。 3、在一个光谱图中的所有吸收峰并不能全部指出其归 属,因为有些峰是分子作为一个整体的特征吸收,而 有些峰则是某些峰的倍频或组频,另外还有些峰是多 个基团振动吸收的叠加。
四、谱图解析的步骤
经验 “四先、四后、一抓法” 即先特征,后指纹;先最强峰,后次强峰,再中强峰;先 粗查,后细查;先肯定,后否定;一抓是抓一组相关峰。
谱图具体解析步骤如下: (1)、了解样品的来源、纯度(要求98%以上)外观; (2)、收集相关信息;
(3)、由IR光谱确定基团及其结构 ;
(4)、推测可能的结构式;
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
红外光谱的八个峰区
饱和C━H面内
弯曲振动区域1475~1300
C━H面内
弯曲
烷烃:
CH3:1470~1430(m)
1380~1370(s)
CH2:1485~1445(m)
CH:1340(w)
当存在>C(CH3) 2和
━C(CH3) 3基团时,
1380~1370 cm-1处
为双峰
不饱和
C━H面内弯曲振动区域1000~650
=C━H面
外弯曲
烯:
单取代: 995~985(s);915~905
顺式取代:~690(s)
反式取代:970~960(s)
同碳二取代:895~885
三取代:840~790(s)
芳烃:
5个相邻氢原子:770~730(vs)
710~640(s)
4个相邻氢原子:770~735(vs)
3个相邻氢原子:810~750(vs)
2个相邻氢原子:860~800(vs)
1个氢原子:900~860(m)
≡C━H面
外外弯曲
炔665~625(s)
(二)分子式的确定:分子式应具有合理的不饱和度;同时符合氮规则。
利用同位素确定分子式。
由于存在同位素,质谱图中除了有质量为M的分子离子峰外,还有质量为M+1,M+2等的同位素峰。
计算其(M+1)/M、(M+2)/M的强度百分比,查表则可确定化合物的化学式。
或者对于分子式CxHyOmNzSv:
I(M+1)/(M)×100%=1.1x+0.37z+0.8v
I(M+1)/(M)×100%=(1.1x)2/200+0.2m+4.4v
即可确定分子式。
另外:分子中含1个Cl:M:M+2=3:1
分子中含2个Cl:M:M+2:M+4=9:6:1
分子中含1个Br:M:M+2=1:1
分子中含2个Br:M:M+2:M+4=1:2:1
分子中含1个Cl和1个Br:M:M+2:M+4=3:4:1
例:化合物的质谱图如下,推到其分子式。
解:设:分子离子峰:73
73–58 = 15 合理
(1.9/31) 100 = 1.1x+0.37z,
z=1, x=5, y=73–14–60= –1 (不合理)
z=1, x=4, y=73–14–48=11 (合理)
分子式 C4H11N, Ω =0
(三)结构式的确定:化合物生成离子的质量及强度,与该化合物本身的结
想是从总体到个体,由主峰到次峰,逐步分析)
以下是质谱图解析的一般过程:
A.考察谱图特点。
主要考察两个方面:分子离子峰的相对强度和谱图全貌特点。
根据分子离子峰确定分子量,同时可以初步判断化合物类型及是否含有Cl、Br、S等元素。
如果分子离子峰为基峰,碎片离子较少而且相对强度较低,可以断定是一个高度稳定的分子.
B.根据从分子离子峰及同位素峰确定化合物的组成式。
C.由组成式计算化合物的不饱和度,可确定化合物中环和双键的数目,有助于判断化合物的结构。
计算方法如下:
不饱和度U=四价原子数 - 一价原子数/2 + 三价原子数/2 + 1
D.研究高质量端离子峰。
质谱高质量端离子峰是由分子离子失去碎片形成的。
从分子离子失去的碎片可以确定化合物中含有哪些取代基。
常见的分子离子失去中性碎片的情况有:
E.研究亚稳离子峰(m*=m2*m2/m1)和小质量端离子峰,找出某些离子或碎片之间的关系,推测化合物的类型。
(这一步一般不要求)
F.通过上述各方面的研究,提出化合物的结构单元。
在根据化合物的分子量、分子式、样品来源、
物理化学性质等,提出一种或几种最有可能的结构。
G.最后为确保结果的准确性,将所得结构式按质谱断裂规律分解,看所得离子和所给未知物谱图是否一致。
以上是质谱解析总体小结。
接下来会采用几个例子来具体说明谱图解析的过程。
由于同组成员已对其中重排内容进行了详细地举例说明,所找到的例子也基本一样,故未对这块内容再进行举例;如有需要可参考他们的课程论文。
例1:某化合物含有C、H、O,由其谱图测得M:(M+1):(M+2)=100:8.9:0.79,试确定其结构式。
解:①该化合物的分子量M=136;
②根据M、M+1、M+2的比值,查表得未知物是C8H8O2。
③该化合物的不饱和度U=8-8/2+1
④由不饱和度为5和m/z77、51等峰可以判断化合物中含有苯环。
⑤高质量端质谱峰m/z105是m/z136失去质量为31的碎片(-CH2OH或–O-CH3)产生的,m/z105失
去质量为28的碎片(-CO、-C2H4)产生的。
因为质谱中没有m/z105对应的是而不是
⑥推断出化合物的结构式或
例2:已知化合物的质谱图,推测该和化合物结构
①由质谱图可以确定该户额何物的分子量M=164;
②由于 164:166=1:1, 164-85 = 79 (Br)
③分子中含有1个Br, 不含氮或含偶数氮
④m/z: 85(49), 86(3.2), 87(0.11)
x = 3.2/49×100/1.1≈6
⑤设x = 6, 则 y =13, 可能的分子式 C6H13Br, Ω =0 合理
设x = 5, w=1, 则 y =9, 可能的分子式 C5H9OBr, Ω =1 也合理
⑥由碎片离子可判断其为 C6H13Br。
