2-硝基-1,3苯二酚
阶段测试一

一、选择题(50×1分)1. 下列关于减压过滤的说法错误的是()(A)胶体沉淀可通过减压过滤进行分离(B)滤纸的大小应略小于漏斗内径(C)滤液由吸滤瓶上口倾出(D)抽滤结束时,应先拔掉橡皮管,再关减压泵2. 某实验报告中有如下记录,其中实验数据合理的是()(A)温度计上显示的室温读数为24.60 C(B)用100mL量筒量取5.26 mL稀H2SO4溶液(C)用广泛pH试纸测得溶液的pH值为3.5(D)用分析天平称取0.5360 g Na2CO33. 下列有关托盘天平的使用,说法错误的是()(A)托盘天平精确度不高,最大载荷为200 g的托盘天平的精密度为± 0.1 g(B)称量时,砝码放在托盘天平右侧(C)托盘天平不能称量热的物品。
(D)称量氯化钠固体,可以用称量纸称量,也可用烧杯称量(D)以上操作均不正确4. 下列实验室事故的处理方法,正确的是()(A)烫伤,立刻用冷水冲洗再处理,若皮肤未破,涂饱和碳酸氢钠于伤处,若皮肤已破,涂1 %的高锰酸钾溶液。
(B)受酸腐蚀,立刻用大量水冲洗再用肥皂水冲洗,最后用水冲洗。
(C)受碱腐蚀,立刻用大量水冲洗再用20%醋酸溶液洗,最后用水洗。
(D)被玻璃碎片割伤后应立即包扎伤口送医院治疗5. 下列说法正确的是()(A)金属钾保存在煤油中,白磷保存在水中(B)做完银镜反应的试管,不能留存,应立刻洗涤,因为久置会变成叠氮化银,易爆炸(C)高锰酸钾不能在硏钵中硏磨,否则引起爆炸(D)酸性溶液不能倒入水槽,碱性废液可倒入水槽,并要用水冲洗6. 下列说法错误的是()(A)酒精灯加热时应使用酒精灯的还原焰加热(B)开动离心机应先慢速,运转平稳后再转到快速(C)氧气钢瓶和氮气钢瓶分别是蓝色和黑色(D)分析纯和化学纯试剂标签的颜色分别是蓝色和红色7. 某学生做完实验以后,采用以下方法分别清洗所用仪器:(1)用HNO3清洗做过银镜反应的试管(2)用酒精清洗做过碘升华的烧杯(3)用浓HCl清洗做过KMnO4分解实验的试管(4)用HCl清洗长期存放过FeCl3溶液的试剂瓶(5)用NaOH溶液清洗盛过苯酚的试管你认为他的操作:()(A)(2)不对(B)(3)(4)不对(C)(4)(5)不对(D)全部正确8. 下列溶液中,在空气里既不易被氧化、也不易分解、且可以用无色玻璃试剂瓶存放的是()(A)硝酸(B)醋酸(C)氢氟酸(D)氢硫酸9. 欲配制和保存FeSO4溶液,应该采取的正确措施是()①把蒸馏水煮沸以赶走水中溶解的O2②溶解时加入少量稀硫酸③溶解时加入少许铁粉④溶解时加入少量盐酸⑤放入棕色瓶中(A)②③(B)②③⑤(C)①③④(D)①②③10. 在强酸性介质中,某些强氧化剂能将Mn2+ 氧化成MnO4-,该方法被用于Mn2+ 鉴定。
实验7 2-硝基-1,3-苯二酚的制备

实验7 2-硝基-1,3-苯二酚的制备 4学时 每组1瓶开水一、实验目的掌握2-硝基-1,3-苯二酚的制备原理和方法;掌握水蒸气蒸馏操作,巩固重结晶操作技能。
二、实验原理2-硝基-1,3-苯二酚的制备是一个巧妙地利用定位规律的例子。
它是通过间苯二酚先磺化、再硝化,最后去磺酸基而完成。
酚羟基为强的邻对位定位基,磺酸基为强的间位定位基,且是体积很大的基团,很容易通过水解而被除去。
间苯二酚磺化时,磺酸基先进入最容易起反应的4和6位,接着再硝化时,受定位规律支配,硝基只能进入位阻较大的2位,将硝化后的产物水解,即可得到产物。
因此,在反应中磺酸基同时起了占位、定位和钝化的三重作用。
OH HO 2OH HO HO 3S SO 3H 324OHHO HO 3S H 2SO 4NO 2三、仪器及试剂 仪器:水蒸气蒸馏装置 减压抽滤装置 回流装置一套试剂 :间苯二酚5.5g ,浓硫酸58g (31.6mL ),浓硝酸(d=1.42)3.9g (4mL ),乙醇,尿素1.250mL 烧杯中放5.5g 粉状间苯二酚[1],充分搅拌下小心加入25mL 浓硫酸(千万不能误加浓硝酸,爆炸!),此时反应液发热,生成白色磺化产物[2],(若无白色浑浊和自动升温,80℃水浴加热),表面皿盖住烧杯,室温放15min (充分磺化),然后在冰水浴中冷到0-10℃。
(防止后面硝化反应过快)2.锥形瓶中加入4mL 浓硝酸,摇荡下加5.6mL 浓硫酸,制成混酸并置冰浴中冷却到10度以下【可在冰水浴中配】。
用滴管将冷却好的混酸慢慢滴加到上述磺化后的产物中,并不停搅拌,控制反应温度不超过30℃(若超过,冰水冷之,防止氧化),滴完后继续搅拌5min ,室温放15min (充分硝化),期间密切关注温度不能超过30℃,(否则冰水冷却之),此时反应物呈亮黄色粘稠状(不应为棕色或紫色)【以上玻仪务必卷纸擦干,保证混酸浓度。
不要洗涤,直接擦干净,有点脏没关系,也可以先烘,后讲】。
1-3-苯二酚安全技术说明书MSDS

化学品安全技术说明书第一部分化学品及企业标识化学品中文名:1,3-苯二酚化学品英文名:1,3-benzenediol;m-benzenediol;resorcinol化学品别名:间苯二酚;雷琐酚CAS No.:108-46-3EC No.:203-585-2分子式:C6H6O2产品推荐及限制用途:工业及科研用途。
第二部分危险性概述紧急情况概述固体。
对皮肤有刺激性。
对眼睛有严重刺激性。
GHS危险性类别根据GB30000-2013化学品分类和标签规范系列标准(参阅第十六部分),该产品分类如下:皮肤腐蚀/刺激,类别2;眼损伤/眼刺激,类别2A;危害水生环境-急性毒性,类别1。
标签要素-象形图警示词:警告危险信息:造成皮肤刺激,造成严重眼刺激,对水生生物毒性极大。
防范说明预防措施:作业后彻底清洗。
避免释放到环境中。
穿戴防护手套/防护服/防护眼罩/防护面具。
事故响应:收集溢出物。
如发生皮肤刺激:求医/就诊。
如仍觉眼刺激:求医/就诊。
脱去被污染的衣服,清洗后方可重新使用。
如进入眼睛:用水小心冲洗几分钟。
如戴隐形眼镜并可方便地取出,取出隐形眼镜。
继续冲洗。
安全储存:不适用。
废弃处置:按照地方/区域/国家/国际规章处置内装物/容器。
物理化学危险:无资料。
健康危害:吸入该物质可能会引起对健康有害的影响或呼吸道不适。
意外食入本品可能对个体健康有害。
皮肤直接接触可造成皮肤刺激。
通过割伤、擦伤或病变处进入血液,可能产生全身损伤的有害作用。
本品能造成严重眼刺激。
眼睛直接接触可能会造成严重的炎症并伴随有疼痛。
眼睛直接接触本品可导致暂时不适。
环境危害:本品对水生生物毒性极大。
请参阅SDS第十二部分。
第三部分成分/组成信息√物质混合物第四部分急救措施一般性建议:急救措施通常是需要的,请将本SDS出示给到达现场的医生。
皮肤接触:立即脱去污染的衣物。
用大量肥皂水和清水冲洗皮肤。
如有不适,就医。
眼睛接触:用大量水彻底冲洗至少15分钟。
有机化学试验试题填空判断

有机化学试验试题填空判断有机化学实验⼀、填空题:1、苯甲酸⼄酯的合成反应中通常加⼊苯或环⼰烷的⽬的是。
答:及时带⾛反应中⽣成的⽔分,使反应平衡右移。
2、若回流太快,会引起现象。
答:液泛。
3、浓硫酸在酯化反应中的作⽤是和。
答:催化剂和吸(脱)⽔剂。
4、通常在情况下⽤⽔浴加热回流。
答:反应温度较低;物质⾼温下易于分解时。
5、分⽔器通常可在情况下使⽤。
答:将低沸点物质移出反应体系。
6、减压蒸馏通常是⽤于的物质。
答:常压蒸馏时未达沸点极易分解氧化活聚合(或沸点⾼、热稳定性差)。
7、减压蒸馏装置由、和三部分组成。
答:蒸馏、抽⽓(减压)、保护和测压8、当⽤油泵进⾏减压时,为了防⽌易挥发的有机溶剂、酸性物质和⽔汽进⼊油泵,降低油泵效率,必须在馏液接收器与油泵之间依次安装,,等吸收装置。
答:冷却肼、硅胶或CaCl2,NaOH,⽯蜡⽚。
9、⽔泵减压下所能达到的最低压⼒为。
答:当时室温下的⽔蒸⽓压。
10、减压⽑细管的作⽤是。
答:使少量空⽓进⼊,作为液体沸腾的⽓化中⼼,使蒸馏平稳进⾏。
11、减压蒸馏安全瓶的作⽤是。
答:调节系统压⼒及放⽓。
12、沸点与压⼒的关系是压⼒升⾼,沸点升⾼;压⼒降低,沸点降低。
答:压⼒升⾼,沸点升⾼;压⼒降低,沸点降低。
13、减压蒸馏时,往往需要⼀⽑细管插⼊烧瓶底部,它能冒出,成为液体的,同时⼜起搅拌作⽤,防⽌液体。
答:⽓泡、⽓化中⼼、暴沸。
14、减压蒸馏操作前,需要估计在⼀定压⼒下蒸馏物的,或在⼀定温度下蒸馏所需要的。
答:沸点、压⼒。
15、减压蒸馏前,应该将混合物中的在常压下⾸先除去,以防⽌⼤量进⼊吸收塔,甚⾄进⼊,降低的效率。
答:低沸点有机物、蒸馏、易挥发有机物、油泵、油泵。
16、减压蒸馏应选⽤壁厚耐压的或仪器,禁⽤底仪器,以防在受压⼒不均⽽引起爆炸,连接处亦需利⽤耐压像⽪管。
答:圆形、梨形、平。
17、苯甲醛发⽣Cannizzaro反应后的混合物中含有的苯甲醛,可通过洗涤法除去。
答:饱和亚硫酸氢钠。
大学部分常见有机化学实验

实验一乙酰苯胺的制备二.实验原理 NH 2+CH 3COOH3+H 2O芳香族酰胺通常用伯或仲芳胺与酸酐或羧酸反应制备,因为酸酐的价格较贵,所以一般选羧酸。
本反应是可逆的,为提高平衡转化率,加入了过量的冰醋酸,同时不断地把生成的水移出反应体系,可以使反应接近完成。
为了让生成的水蒸出,而又仅可能地让沸点接近的醋酸少蒸出来,本实验采用较长的分馏柱进行分馏。
实验加入少量的锌粉,是为了防止反应过程中苯胺被氧化。
1.合成(1).反应物量的确定:本实验反应是可逆的,采用乙酸过量和从反应体系中分出水的方法来提高乙酰苯胺的产率,但随之会增加副产物二乙酰基苯胺的生成量。
二乙酰苯胺很容易水解成乙酰苯胺和乙酸,在产物精制过程中通过水洗、重结晶等操作,二乙酰基苯胺水解成乙酰苯胺和乙酸,经过滤可除去乙酸,不影响乙酰苯胺的产率和纯度。
苯胺极易氧化,在空气中放置会变成红色,使用时必须重新蒸馏除去其中的杂质。
反应过程中加入少许锌粉。
锌粉在酸性介质中可使苯胺中有色物质还原,防止苯胺继续氧化。
在实验中可以看到,锌粉加得适量,反应混合物呈淡黄色或接近无色。
但锌粉不能加得太多,一方面消耗乙酸,另一方面在精制过程中乙酸锌水解成氢氧化锌,很难从乙酰苯胺中分离出来。
(2).合成反应装置的设计:水沸点为100℃,乙酸沸点为117℃,两者仅差17℃,若要分离出水而不夹带更多的乙酸,必须使用分馏反应装置,而不能用蒸馏的反应装置。
本实验用分馏柱。
一般有机反应用耐压、耐液体沸腾冲出的圆形瓶作反应器。
由于乙酰苯胺的熔点为114℃,稍冷即固化,不易从圆形瓶中倒出,因此用锥形瓶作反应器更方便。
分出的水量很少,分馏柱可以不连接冷凝管,在分馏柱支口上直接连尾接管,兼作空气冷凝管即可,使装置更简单。
为控制反应温度,在分馏柱顶口插温度计。
(3).操作条件的控制保持分馏柱顶温度低于105℃的稳定操作,开始缓慢加热,使反应进行一段时间,有水生成后,再调节反应温度使蒸汽缓慢进入分馏柱,只要生成水的速度大于或等于分出水的速度,即可稳定操作,要避免开始强烈加热。
大学部分常见有机化学实验

实验一乙酰苯胺的制备二.实验原理 NH 2+CH 3COOH3+H 2O芳香族酰胺通常用伯或仲芳胺与酸酐或羧酸反应制备,因为酸酐的价格较贵,所以一般选羧酸。
本反应是可逆的,为提高平衡转化率,加入了过量的冰醋酸,同时不断地把生成的水移出反应体系,可以使反应接近完成。
为了让生成的水蒸出,而又仅可能地让沸点接近的醋酸少蒸出来,本实验采用较长的分馏柱进行分馏。
实验加入少量的锌粉,是为了防止反应过程中苯胺被氧化。
1.合成(1).反应物量的确定:本实验反应是可逆的,采用乙酸过量和从反应体系中分出水的方法来提高乙酰苯胺的产率,但随之会增加副产物二乙酰基苯胺的生成量。
二乙酰苯胺很容易水解成乙酰苯胺和乙酸,在产物精制过程中通过水洗、重结晶等操作,二乙酰基苯胺水解成乙酰苯胺和乙酸,经过滤可除去乙酸,不影响乙酰苯胺的产率和纯度。
苯胺极易氧化,在空气中放置会变成红色,使用时必须重新蒸馏除去其中的杂质。
反应过程中加入少许锌粉。
锌粉在酸性介质中可使苯胺中有色物质还原,防止苯胺继续氧化。
在实验中可以看到,锌粉加得适量,反应混合物呈淡黄色或接近无色。
但锌粉不能加得太多,一方面消耗乙酸,另一方面在精制过程中乙酸锌水解成氢氧化锌,很难从乙酰苯胺中分离出来。
(2).合成反应装置的设计:水沸点为100℃,乙酸沸点为117℃,两者仅差17℃,若要分离出水而不夹带更多的乙酸,必须使用分馏反应装置,而不能用蒸馏的反应装置。
本实验用分馏柱。
一般有机反应用耐压、耐液体沸腾冲出的圆形瓶作反应器。
由于乙酰苯胺的熔点为114℃,稍冷即固化,不易从圆形瓶中倒出,因此用锥形瓶作反应器更方便。
分出的水量很少,分馏柱可以不连接冷凝管,在分馏柱支口上直接连尾接管,兼作空气冷凝管即可,使装置更简单。
为控制反应温度,在分馏柱顶口插温度计。
(3).操作条件的控制保持分馏柱顶温度低于105℃的稳定操作,开始缓慢加热,使反应进行一段时间,有水生成后,再调节反应温度使蒸汽缓慢进入分馏柱,只要生成水的速度大于或等于分出水的速度,即可稳定操作,要避免开始强烈加热。
2021届江苏省高考化学一轮复习专题演练:专题7《有机化学基础》综合练习(苏教版)

专题七有机化学基础留意事项:1. 本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。
满分120分,考试时间100分钟。
2. 答题前,请考生务必将自己的学校、班级、姓名填写在密封线内。
第Ⅰ卷(选择题共40分)不定项选择题(本题包括10小题,每小题4分。
每小题有一个或两个选项符合题意)1. 下列各项表达正确的是()A. 新戊烷的结构简式:(CH3)3CCH3B. 聚乙烯的结构简式:C. 硝基苯的结构简式:D. 乙烷分子的比例模型:2. (2021·新课标Ⅰ卷)乌洛托品在合成、医药、染料等工业中有广泛用途,其结构简式如右图所示。
将甲醛水溶液与氨水混合蒸发可制得乌洛托品。
若原料完全反应生成乌洛托品,则甲醛与氨的物质的量之比为()A. 1∶1B. 2∶3C. 3∶2D. 2∶13. (2021·海南高考)分子式为C4H10O并能与金属钠反应放出氢气的有机物有(不含立体异构)()A. 3种B. 4种C. 5种D. 6种4. (2021·新课标Ⅱ卷)分子式为C5H10O2并能与饱和NaHCO3溶液反应放出气体的有机物有(不含立体结构) ()A. 3种B. 4种C. 5种D. 6种5. (2021·海南高考)下列反应不属于取代反应的是()A. 淀粉水解制葡萄糖B. 石油裂解制丙烯C. 乙醇与乙酸反应制乙酸乙酯D. 油脂与浓NaOH反应制高级脂肪酸钠6. (2021·河北联考)NM-3和D-58是正处于临床试验阶段的小分子抗癌药物,结构如下:下列关于NM-3和D-58的叙述错误的是()A. 都能与NaOH溶液反应,缘由不完全相同B. 都能与溴水反应,缘由不完全相同C. 都不能发生消去反应,缘由相同D. 遇FeCl3溶液都显色,缘由相同7. 下列试验装置和操作正确的是()A. 分别苯和硝基苯B. 制取乙烯C. 制取氨气D. 制备酚醛树脂8. (2022·常州一模)有机物X和Y可作为“分子伞”给药物载体的伞面和中心作支撑架(未表示出原子或原子团的空间排列)。
(完整版)有机化学试题2
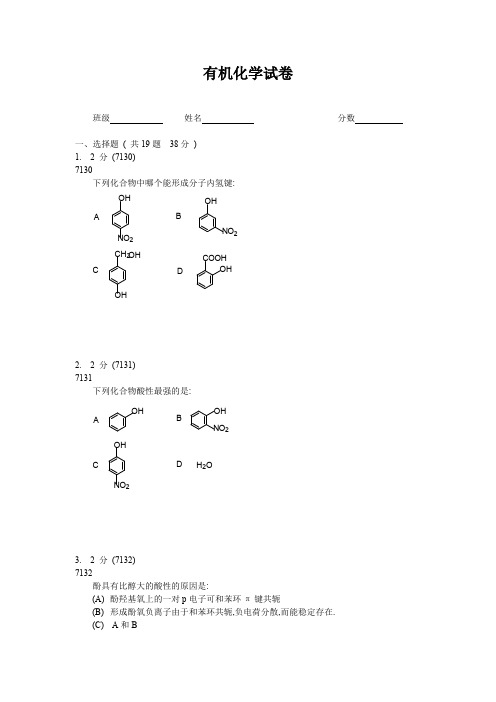
有机化学试卷班级姓名分数一、选择题 ( 共19题 38分 )1. 2 分 (7130)7130下列化合物中哪个能形成分子内氢键:OH OHNO 2NO 2ABOHCH 2OH COHCOOHD 2. 2 分 (7131)7131下列化合物酸性最强的是:OHAOHNO 2BOH NO 2CDH 2O3. 2 分 (7132)7132酚具有比醇大的酸性的原因是:(A) 酚羟基氧上的一对p 电子可和苯环π键共轭(B) 形成酚氧负离子由于和苯环共轭,负电荷分散,而能稳定存在.(C) A 和B(D) A , B 均不是4. 2 分 (7133)7133比较下列化合物的Pka,正确的是OHCOCH 312HOOCH 3C OHNH 23(A) 1 > 2 > 3 (B) 3 > 1 > 2( C) 2 > 1 > 3 (D) 2 > 3 > 15. 2 分 (7135)7135石炭酸的结构为下列何种 ?A OHCOOHCOOHCH 3BCCOOHCH 3D6. 2 分 (7136)7136对乙醇钠反应活性最强的是哪一个 ?ABrNO 2BrN Me 2BrNO 2Me Me -BrNMe 3Cl+BCD7. 2 分 (7137)7137香兰素(Vanillia)结构为何种?OHCHOCHOOHOHCHOOCH 3OHCOH OCH 3ABCD8. 2 分 (7138)7138水杨醛的结构为下列哪种?CH 3CHOCHOOHACH 3CHOBCCHOOHD9. 2 分 (7139)7139OHOH MeMeMeOHOHMeOHOH Me MeOHMeOCH 3ABCD*. 2 分 (7140)7140DCBA BrOOBr OOBrOOBr£ºH +OÌõ¼þϲúÎïΪÔÚÓëOHBr 11. 2 分 (7142)7142CH 3OH ·¢ÉúÇ×µçÈ¡´ú·´Ó¦µÄλÖÃÊÇ£ºABCD²»ÄÜÈ·¶¨12. 2 分 (7143)7143间叔丁基苯酚分别与溴反应, 与碘反应将得到下列哪一组产物?A 三溴衍生物, 三碘衍生物B二溴衍生物, 一碘衍生物C二溴衍生物, 二碘衍生物D一溴衍生物, 一碘衍生物13. 2 分(7145)7145含酚废水的环境危害甚大,处理其最佳方法为哪种?A溶剂萃取法B蒸汽吹脱法C磺化煤吸附法D生化法14. 2 分(7146)71462,4,6-三叔丁基苯酚是一种很有用的抗氧剂, 这是由于其能发生以下何种反应: A单电子转移B亲电取代C亲核取代D酸碱反应15. 2 分(7147)7147Óë·´Ó¦²úÎïÖ÷ÒªÊÇ1NaOH2OCl C COCl OH OHAOH OH OCl C O OOOH O OClC BCDOHOH16. 2 分 (7148)7148苯酚在NaOH 中与CHCl 3反应生成A 水杨醛B 苯甲醛C 邻羟基苯三氯甲烷D 邻羟基苯二氯甲烷17. 2 分 (7149)7149为了降低废水污染环境, 工业上通常采取以下何法生产苯酚:A 苯磺酸碱熔法B 异丙苯氧化法C 氯苯水解法D 苯和氯化氢氯化法18. 2 分 (7176)7176区别安息香酸和水杨酸可用以下何种方法?A. NaOH 水溶液B. Na 2CO 3水溶液C. FeCl 3水溶液D. I 2/OH -溶液19. 2 分 (7177)7177下面分离苯、苯胺、苯酚和苯甲酸混合物哪个方案可行?A. 乙醚, Na 2CO 3, NaOH, HCl B. 乙醚, NaOH, HCl C. 蒸馏D. 重结晶二、填空题 ( 共 3题 6分 )20. 2 分 (7134)7134写出水杨酸的结构式21. 2 分 (7141)7141写出下列反应的主要有机产物或所需之原料, 试剂(如有立体化学问题请注明)COOHHOCOO NaONa CH 2CCHCH 222. 2 分 (7144)7144写出下面反应的主要产物.CCO OO+2OHi s三、合成题 ( 共26题 119分 )23. 4 分 (7150)7150Óɱ½·ÓºÏ³É»¯ºÏÎïNOC 2H 5COCH 2CH 224. 4 分 (7151)7151如何完成下列转变OHCH 3OHCHO25. 4 分 (7152)7152ÓÉ1,4-ÝÁõ«ºÏ³ÉOOCH 3CH 326. 4 分 (7153)7153·ú±½ºÏ³É»¯ºÏÎïN N NNOHOH,Óɱ½·Ól t h i 27. 4 分 (7154)7154如何完成下列转变28. 4 分 (7155)7155Óɱ½·ÓºÏ³ÉOHCH 2CH 2CH 329. 4 分 (7156)7156Ïã²ÝÈ©ÓÉ()HO NH 2CHOOHOHºÏ³É½µÉöÉÏÏÙËØOHOHCHCH 230. 4 分 (7157)7157ÓÉÜîÏãÄÔ(CH CH OCH 3CH 3)ºÏ³ÉÀÒ°·()OHCH 2CH 2NH 231. 4 分 (7158)7158由苯酚合成苯基乙烯基醚OCHCH 232. 4 分 (7159)7159Óɼä¼×±½·ÓºÏ³É»¯ºÏÎïOCH 3NO 2NO 2C CH 3()3CH 333. 6 分 (7160)7160由甲苯合成苔黑酚(石蕊染料的母体):OHHO CH 334. 5 分 (7161)7161CH 3CH 3BrOHNH 2ÓɺϳÉ35. 4 分 (7162)7162CH 3NO 2CH 3OHBrÓɺϳÉ36. 8 分 (7163)71631,4-±½õ«DDQ O OCl ClCNCNÓɺϳÉ()37. 4 分 (7164)7164NO 2NO 2NO 2OHÓÉ·ú±½ºÏ³É¿àζËá()38. 4 分 (7165)7165HOCOCH 3ºÏ³ÉÓÉ(+-)CH CH 2NHCH 3HOOH39. 4 分 (7166)7166由间二苯酚合成2-硝基-1,3-二苯酚OHOH NO 240. 4 分 (7167)7167SCHON O 2OH ÓÉ,µÈÖ÷ÒªÔ-ÁϺϳɻ¯ºÏÎïSCH NOCH 2COOH41. 8 分 (7168)7168OOÓɼױ½,±½·ÓºÏ³É»¯ºÏÎï42. 4 分 (7169)7169OHOH CH CHCOOHCHOOHOCH 3ÓÉÏã²ÝÈ©()ºÏ³É»¯ºÏÎï43. 4 分 (7170)7170由邻苯二酚合成4-氨基-1,2-二甲氧基苯OCH 3OCH 3NH 244. 4 分 (7171)7171C HO OHCH 3CH 3Óɱ½,±ûͪºÏ³É45. 4 分 (7172)7172由苯酚, 苯甲醛等为主要原料合成化合物:CO OC OCH 3CHBrCHBr 46. 4 分 (7173)7173OHCH 3ÓɺϳÉOHCHO47. 6 分 (7174)7174如何完成下列转变ClBrOHBrBr 48. 6 分 (7175)7175如何完成下列转变CH 2CH 3OHC 2H5四、推结构题 ( 共18题 98分 )49. 4 分 (7101)7101某分子式为C 5H 12O 的化合物,含有5组不等性质子,从NMR 光谱图中见到: a. 在δ=0.9处出现二重峰 (6H)b. 在δ=1.6处出现多重峰 (1H)c. 在δ=2.6处出现八重峰 (1H)d. 在δ=3.6处出现单峰 (1H)e. 在δ=1.1ppm 处出现二重峰 (3H)试推测该化合物的结构。
2-硝基-1-3-苯二酚的制备

实验报告题目2-硝基-1,3-苯二酚的制备学院医药化工学院专业材料化学班级2011级材料化学(1)学号24学生姓名林娇娜指导教师朱仙弟完成日期2013年4月25日2-硝基-1,3-苯二酚的制备一、实验目的1、熟悉芳环上亲电取代反应定位原则。
2、掌握磺化、硝化的原理和实验方法。
3、在了解水蒸汽蒸馏原理的基础上,掌握水蒸汽蒸馏装置的安装和操作。
二、实验原理2-硝基-1,3-苯二酚不能由间苯二酚直接硝化来制备,会将间苯二酚先磺化,生成4,6-二羟基-1,3-苯二磺酸。
酚羟基为强的邻对位基,磺酸基为强的碱定位基,4,6-二羟基-1,3-苯二磺酸再硝化,受定位规律的支配,硝基只能进入2位,将硝化后的水解产物水解脱掉磺酸基,即可得到产物,反应中磺酸基同时起了站位和定位的双重作用。
2-硝基-1,3-苯二酚的制备是一个巧妙地利用定位规律的例子。
反应式如下:++OHOHH 2SO 42OHOH SO 3H3SH 2O2++24OHOH SO 3H HO 3SH 2OHNO 3OHOH SO 3HHO 3SNO 2++H 2SO 42H 2O2OHOH SO 3HHO 3SNO 2OHOHNO 2H+三、主要试剂和产物的物理常数名称规格相对分子质量相对密度/(g/cm 2) 熔点/℃沸点/℃溶解度/(g/100g 溶剂)用量或理论产量间苯二酚分析纯110.11 1.28 110.7 276.5 易溶于水 2.8g(0.025mol)13 mL(0.24 mol,98%)和浓硫酸分析纯98 1.84 10 338 易溶于水2.8 mL(0.052 mol,98%)硝酸分析纯63.01 1.41 -42 120.5 易溶于水 2 mL(0.032 mol,65%~68%)尿素分析纯60.06 1.335 132.7 196.6 108 0.1 g乙醇分析纯46.07 0.816 -114.3 78.4 15.9 5 mL 50%2-硝基-1,3-苯/ 155.11 0.7983 84.85 234 微溶于水约0.5 g 二酚四、实验装置图图a 回流装置图b 蒸馏装置五、实验步骤和现象时间试验步骤现象备注1、组装反应装置(图无固定夹拧紧a)2、加料将2.8 g(0.025mol)粉状间苯二酚放入100 mL的烧杯中,在充分搅拌下小心地加入13 mL(0.24 mol,98%)浓硫酸反应放热,立即生成白色的磺化物加浓硫酸的时候要在充分搅拌下小心地加入3、反应反应无在60~65反应15 min,冰水冷却到室温,用滴管滴加2.8 mL(0.052 mol,98%)浓硫酸和2 mL(0.032 mol,65%~68%)硝酸配成泠却好的混酸。
2-硝基-1_3-苯二酚地制备

实验报告题目2-硝基-1,3-苯二酚的制备学院医药化工学院专业材料化学班级2011级材料化学(1)学号1132230024学生姓名林娇娜指导教师朱仙弟完成日期2013年4月25日2-硝基-1,3-苯二酚的制备一、实验目的1、熟悉芳环上亲电取代反应定位原则。
2、掌握磺化、硝化的原理和实验方法。
3、在了解水蒸汽蒸馏原理的基础上,掌握水蒸汽蒸馏装置的安装与操作。
二、实验原理2-硝基-1,3-苯二酚不能由间苯二酚直接硝化来制备,会将间苯二酚先磺化,生成4,6-二羟基-1,3-苯二磺酸。
酚羟基为强的邻对位基,磺酸基为强的碱定位基,4,6-二羟基-1,3-苯二磺酸再硝化,受定位规律的支配,硝基只能进入2位,将硝化后的水解产物水解脱掉磺酸基,即可得到产物,反应中磺酸基同时起了站位和定位的双重作用。
2-硝基-1,3-苯二酚的制备是一个巧妙地利用定位规律的例子。
反应式如下:++OHOHH 2SO 42OHOH SO 3H 3SH 2O2++OHOH SO 3H HO 3SH 2OHNO 3OHOH SO 3HHO 3SNO 2++H 2SO 42H 2O2OHOH SO 3HHO 3SNO 2OHOHNO 2+三、主要试剂和产物的物理常数四、实验装置图图a 回流装置图b 蒸馏装置五、实验步骤和现象时间试验步骤现象备注1、组装反应装置(图a)无固定夹拧紧2、加料将2.8 g(0.025mol)粉状间苯二酚放入100 mL的烧杯中,在充分搅拌下小心地加入13 mL(0.24 mol,98%)浓硫酸反应放热,立即生成白色的磺化物加浓硫酸的时候要在充分搅拌下小心地加入3、反应反应无在60~65反六、实验结果2-硝基-1,3-苯二酚,桔红色片状结晶,纯2-硝基-1,3-苯二酚的mp为85~87 ℃,产量约0.5g七、注意事项1.本实验一定注意先磺化,后硝化。
否则会剧烈反应,甚至产生事故。
2.间苯二酚需在研钵中研成粉状,否则磺化不完全。
2-硝基-1,3-苯二酚的合成

7 、 加入尿素可与多余的硝酸作用生成络盐 CO(NH2)2·HNO3 , 加入尿素可与多余的硝酸作用生成络盐CO(NH 以免其生成NO 污染空气。 以免其生成NO2污染空气。 8 、 在水蒸气蒸馏操作中 , 馏液最初为橙黄色 , 很快冷凝管内 在水蒸气蒸馏操作中,馏液最初为橙黄色, 壁即会沉积大量橙红色固体粗产品, 壁即会沉积大量橙红色固体粗产品,为防止粗产品堵塞蒸馏通 道,本次水蒸气蒸馏不必安装尾接管导流,冷凝水的水流也尽 本次水蒸气蒸馏不必安装尾接管导流, 可能开至最小,当粗产品大量堵塞于冷凝管中、上部时, 可能开至最小,当粗产品大量堵塞于冷凝管中、上部时,也可 将冷凝水完全关闭,或将冷凝管中的冷凝水排空, 将冷凝水完全关闭,或将冷凝管中的冷凝水排空,利用烧瓶中 蒸出的热水蒸气将橙红色的粗产品固体融化为液体, 蒸出的热水蒸气将橙红色的粗产品固体融化为液体,当橙红色 液体被水蒸气冲击至冷凝管尾部并即将逸出橙黄色蒸汽时, 液体被水蒸气冲击至冷凝管尾部并即将逸出橙黄色蒸汽时,可 重新开启冷凝水。 使水蒸气蒸馏恢复正常状态。 重新开启冷凝水。 使水蒸气蒸馏恢复正常状态。
思考题答案
1、答:a. 磺化时,浓H2SO4氧化反应物; 磺化时, 氧化反应物; b. 硝化时,磺酸基被硝基置换; 硝化时,磺酸基被硝基置换; c. 间苯二酚本身的氧化(空气中即成醌显红色)。 间苯二酚本身的氧化(空气中即成醌显红色) 2、答:A. 先硝化的缺点: 先硝化的缺点: a. 产率低; 产率低; b. 剧烈的氧化反应,得不到硝化产物。 剧烈的氧化反应,得不到硝化产物。 B. 先磺化的优点: 先磺化的优点: a. -SO3H为致钝基团,可降低芳环活性,不易被氧化。 为致钝基团,可降低芳环活性,不易被氧化。 b. -SO3H可先占4、6位,迫使-NO2进入2位。 可先占4 迫使进入2 c. -SO3H与-OH定位效应一致,均为2位,所以-NO2易进入2位 OH定位效应一致 均为2 定位效应一致, 所以易进入2 d. 磺化反应可逆,可通常在稀酸中加热的方法将-SO3H水解掉。 磺化反应可逆,可通常在稀酸中加热的方法将水解掉。
2024年1月浙江省普通高校招生选考科目化学仿真模拟卷02(考试版)

2024年1月浙江省普通高校招生选考科目化学仿真模拟试卷02(考试时间:90分钟满分100分)可能用到的相对原子质量:H 1 Li 7 C 12 N 14 O 16 Na 23 Mg 24 Al 27 Si 28 S 32 Cl 35.5 K 39 Ca 40 Cr52 Mn 55 Fe 56 Co 59 Cu 64 Ge 73 Br82 Ag 108 Ba 137 Bi 209选择题部分一、选择题(本大题共16小题,每小题3分,共48分。
每个小题列出的四个备选项中只有一个是符合题目要求的,不选、多选、错选均不得分)1.化学与材料密切相关。
下列属于新型无机非金属材料的是( )A.酚醛树脂B.氮化硼陶瓷C.特种钢D.储氢合金2.下列化学用语表示正确的是( )A.羟基的电子式:B.基态氮原子的价层电子轨道表示式:C.PCl3的价层电子对互斥模型:D.的名称:3-溴丁烷3.重铬酸钾(K2Cr2O7)和铬酸钾(K2CrO4)应用广泛,下列说法不正确...的是( )A.Cr位于元素周期表d区,最外层电子数为1B.K2CrO4属于强电解质C.酸性K2Cr2O7溶液可将乙醇氧化为乙酸D.K2CrO4在碱性溶液中可转化为K2Cr2O74.物质的性质决定用途,下列两者对应关系不正确...的是( )A.碳化硅熔点很高,可用于制作砂轮磨料B.Al(OH)3呈弱碱性,可用于治疗胃酸过多C.生铁硬度大、抗压,可用于铸造机器底座D.Na2SO3有还原性,可用于水处理中脱氯(Cl2)5.下列有关说法不正确...的是( )6.工业上用S8(分子结构:)与CH4为原料制备CS2,发生反应:S8+2CH4=2CS2+4H2S。
设N A 为阿伏加德罗常数的值,下列说法正确的是( )A.S既是氧化剂,又是还原剂B.生成17gH S,断开S−S键数为NC.向溶液中通入少量CO2:+CO2+H2O→+ CO32D.向明矾溶液中滴加氢氧化钡至沉淀质量最大:Al3++2SO2+2Ba2++4OH=2BaSO↓+AlO+2H OD.1mol该物质与足量盐酸发生水解反应,最多可生成2molCO211.前四周期的元素X、Y、Z、Q、W的原子序数依次增大,基态X原子的半径是所有原子中最小的,Y与X可形成室温下X2Y、X2Y2两种无色液体,基态Z原子的M电子层上p轨道为半充满状态,Y、Q同主族,W原子的价层电子排布式为3d54s2,下列说法不正确...的是A.电负性:Z<Q<YB.简单离子半径:Z>Q>Y>ZC.同周期中第一电离能比Q大的元素有1种、、三种元素形成的某些化合物,可存在于某些使用后的碱性电池中D.X Y W12.2-硝基-1,3-苯二酚(桔红色针状晶体,难溶于水,沸点为88℃)可由间苯二酚经磺化、硝化等步骤合成,其中一步按图示装置(部分仪器略去)收集产品。
2-硝基-1,3-苯二酚1

2-硝基-1,3-苯二酚的制备〔实验目的〕1.熟悉芳环上亲电取代反应定位规则。
2.巩固水蒸气蒸馏操作。
〔实验原理〕2-硝基-1,3-苯二酚不能由间苯二酚直接硝化来制备,将间苯二酚先磺化,生成4,6-二羟基-1,3-苯二磺酸。
酚羟基为强的邻对位定位基,磺酸基为强的间位定位基,4,6-二羟基-1,3-苯二磺酸再硝化,受定位规律的支配,硝基只能进入2-位,将硝化后的产物水解脱掉磺酸基,即可得到产物,反应中磺酸基同时起了占位和定位的双重作用。
2-硝基-1,3-苯二酚的制备是一个巧妙地利用定位规律的例子。
反应式如下:+2H 2SO 4+2H 2O OHOHOHHO 3SOH3H+OHHO 3SOH3H HNO 324OHHO 3SSO 3HNO 2+H 2OOHOH2H 2SO 4OHHO 3SOH3HNO 2+2H 2O H NO 2+〔仪器和药品〕仪器:100mL 烧杯、水蒸气蒸馏装置药品:间苯二酚、浓硫酸、硝酸、尿素、乙醇 〔实验步骤〕将2.8g(0.025mol)粉状间苯二酚[1]放入100mL 烧杯中,在充分搅拌下小心地加入13mL (0.24mol ,98%)浓硫酸,此时反应放热,立即生成白色磺化物,然后使反应物在60~65℃反应15min 。
将烧杯放入冷水浴中冷至室温。
用滴管滴加预先用2.8mL(0.052mol ,98%)浓硫酸和2mL(0.032mol ,65%~68%)硝酸配成冷却好的混酸。
边滴加边搅拌,控制温度于30±5℃,在此温度下继续搅拌15min .将反应物移入圆底烧瓶中,小心加入7mL 水烯释之[2],温度控制在50℃以下。
再加入约0.1g 尿素[3],然后进行水蒸气蒸馏,在冷凝管壁上和馏出液中立即有桔红色固体出现[4]。
当无油状物蒸出时,即可停止蒸馏。
馏出液经水浴冷却后,过滤得粗产品。
用少量乙醇-水(约需5mL50%乙醇)混合溶剂重结晶,得约0.5g 桔红色晶体。
有机化学试验题简答题

有机化学实验试题简答题1、酯的合成通常为可逆反应,为了提高产率,通常采用什么方法使反应平衡右移?答:适量的催化剂;增加某一种反应物用量;移走产物之一2、何谓酯化反应?酯化反应有什么特点?有哪些物质可以作为酯化反应的催化剂?答:羧酸和醇在少量酸催化作用下生成酯的反应,称为酯化反应。
常用的酸催化剂有:浓硫酸,磷酸等质子酸,也可用固体超强酸及沸石分子筛等。
3、有机实验中,什么时候利用回流反应装置?怎样操作回流反应装置?答:有两种情况需要使用回流反应装置:一是反应为强放热的、物料的沸点又低,用回流装置将气化的物料冷凝回到反应体系中。
二是反应很难进行,需要长时间在较高的温度下反应,需用回流装置保持反应物料在沸腾温度下进行反应。
回流反应装置通常用球形冷凝管作回流冷凝管。
进行回流反应操作应注意:(1)根据反应物的理化性质选择合适的加热方式,如水浴、油浴或石棉网直接加热。
(2)不要忘记加沸石。
(3)控制回流速度,一般以上升的气环不超过冷凝管的1/3(即球形冷凝管的第一个球)。
过高,蒸气不易全部冷凝回到反应烧瓶中;过低,反应烧瓶中的温度不能达到较高值。
4、酯化反应中常用浓硫酸作为催化剂和脱水剂,除此之外,还有什么种类的物质可以作为酯化反应的催化剂,试至少举出两例。
答:如超强酸、固体酸、强酸性阳离子交换树脂、路易斯酸等。
5、在萃取和分液时,两相之间有时出现絮状物或乳浊液,难以分层,如何解决?答:(1)静置很长时间;(2)加入溶于水的盐类或溶剂,提高或降低某一种化合物的比重。
6、实验对带水剂的要求是什么?答:具有较低沸点;能与产物和水形成共沸物;难溶于水;易于回收;低毒等。
7、若分液时,上下层难以分层,可采取什么措施使其分层?答:可通过加入盐类增加水相的比重或加入有机溶剂减少有机相的比重。
8、催化酯化反应中,浓硫酸做催化剂的优缺点是什么?答:催化效率高。
但腐蚀设备,不能回收。
9、减压蒸馏中毛细管的作用是什么?能否用沸石代替毛细管?答:减压蒸馏时,空气由毛细管进入烧瓶,冒出小气泡,成为液体沸腾时的气化中心,这样不仅可以使液体平稳沸腾,防止暴沸,同时又起一定的搅拌作用。
2-硝基-1,3-苯二酚的制备实验
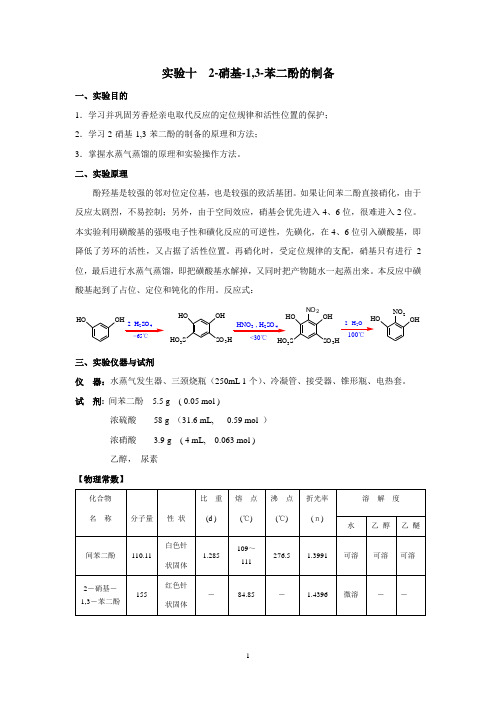
实验十2-硝基-1,3-苯二酚的制备一、实验目的1.学习并巩固芳香烃亲电取代反应的定位规律和活性位置的保护;2.学习2-硝基-1,3-苯二酚的制备的原理和方法;3.掌握水蒸气蒸馏的原理和实验操作方法。
二、实验原理酚羟基是较强的邻对位定位基,也是较强的致活基团。
如果让间苯二酚直接硝化,由于反应太剧烈,不易控制;另外,由于空间效应,硝基会优先进入4、6位,很难进入2位。
本实验利用磺酸基的强吸电子性和磺化反应的可逆性,先磺化,在4、6位引入磺酸基,即降低了芳环的活性,又占据了活性位置。
再硝化时,受定位规律的支配,硝基只有进行2位,最后进行水蒸气蒸馏,即把磺酸基水解掉,又同时把产物随水一起蒸出来。
本反应中磺酸基起到了占位、定位和钝化的作用。
反应式:HO OHHOHO3S SO3HOHHOHO3S SO3H2HONO224HNO3 , H2SO4<30℃NO2三、实验仪器与试剂仪器:水蒸气发生器、三颈烧瓶(250mL 1个)、冷凝管、接受器、锥形瓶、电热套。
试剂:间苯二酚 5.5 g ( 0.05 mol )浓硫酸58 g (31.6 mL, 0.59 mol )浓硝酸 3.9 g ( 4 mL, 0.063 mol )乙醇,尿素【物理常数】四、实验操作1.磺化:在250ml烧杯中,加入5.5g粉状的间苯二酚,在充分搅拌下加入25 mL 浓硫酸,反应放热,产生白色磺化产物,冷却到室温,然后用冰水浴冷却至0 ~10℃。
2.硝化:在锥形瓶中加入4 mL浓硝酸,在加入5.6 mL浓硫酸配制混酸并在冰水中冷却。
将此配制的混酸液在搅拌下慢慢用滴管滴入磺化产物中。
维持温度低于30℃,滴加完毕后,在室温放置15 min后,加入15 mL冰水稀释,维持温度低于50℃。
3.粗产物处理:将反应物转移到250 mL三颈烧瓶中,加入0.1g尿素,按教材p80 图3.6 进行水蒸气蒸馏,将产物全部蒸出,然后冷却,抽滤,粗产物用50% 乙醇的水溶液进行重结晶。
2-硝基-1,3-苯二酚的制备

实验9 2-硝基-1,3-苯二酚的制备Preparation of 2-nitroresorcinol【实验目的】1.学习在苯环上进行亲电取代反应的定位规律以及磺化反应的应用。
2.学习2-硝基-1,3-苯二酚的合成方法。
3.进一步熟悉机械搅拌、水蒸气蒸馏和重结晶等基本操作。
【实验原理】由1,3-苯二酚(俗名:雷琐酚,间苯二酚)合成2-硝基-1,3-苯二酚(又名2-硝基雷琐酚)时,由于苯环上的4,6位很容易硝化,反应过程中为了使4,6位不被硝化,必须先把这两个部位保护起来,等硝化反应完成以后在去掉保护基。
本实验采取的合成路线如下:反应物先磺化,在4,6位引入磺酸基,然后硝化,在2号位引入硝基,最后水蒸气蒸馏二磺酸硝化物的酸性溶液,除去磺酸基,生成2-硝基1,3-苯二酚。
【试剂与仪器准备】1.仪器: 烧杯,滴液漏斗,150ml 三颈瓶,布氏漏斗,抽滤瓶,真空水泵,机械搅拌器,500ml 圆底烧瓶,水蒸气蒸馏装置,锥形瓶、药品匙、滤纸等。
2.试剂:雷琐酚(A.R ),浓硫酸(C.P ),硝酸(C.P ,70~72%),95%乙醇,尿素(C.P )。
化合物的物理常数 【实验装置】1. 机械搅拌装置图参照下图稍作改动,因反应温度低于室温,反应混合物挥发度很小,可不用回流冷凝管。
即Y 型管也可不用,将温度计通过温度计套管插入反应瓶中即可。
OH OH 24OH SO 3H HO 3S 0~200C HNO 3OH OHSO 3HHO 3S NO 2水蒸气蒸馏OH OH NO 2图10-1 滴液控温的搅拌回流装置2.水蒸气蒸馏装置水蒸气蒸馏除需常压蒸馏的的仪器以外,还需要有水蒸气发生器和导管,另外需一长颈的圆底烧瓶,其装置如图1-2所示。
(a) (b)a水蒸气发生器; b蒸馏装置图10-2 水蒸气蒸馏装置(1)水蒸气可由水蒸气发生器产生,水蒸气发生器是铁质或铜质的,也可以用圆底烧瓶代替,发生器内盛的水约占总容量的一半,从侧面的玻管可知器内水量的多少,中间的玻管称为安全管,管内水柱的高低反映内部蒸气的压力。
实验7 2-硝基-1,3-苯二酚的制备

实验7 2-硝基-1,3-苯二酚的制备实验概述:本实验是通过对苯二酚的硝化反应得到2-硝基-1,3-苯二酚。
硝化反应是有机化学中一种常见的官能团转化反应,通常也是制备硝基含量高的有机化合物的重要手段。
实验原理:2-硝基-1,3-苯二酚是一种有机化合物,结构式为C6H4(NO2)2(OH)。
在苯二酚分子中,羟基(-OH)的亲电性很高,在硝化反应中易被硝化剂(nitration agent)亚硝酰离子(NO2+)亲电进攻。
硝化剂通常采用硝酸,硫酸和冰乙酸混合物(nitration mixture),反应温度一般在0-5℃下进行,反应时间一般20-30分钟。
硝化完成后,反应混合物中会同时产生2,4-硝基-苯甲酸等副产物。
这些副产物会在后续的反应中与目标产物混合在一起,并需要通过重结晶等手段进行分离纯化。
实验操作:实验器材:反应瓶,洗瓶,滴液管,漏斗,水槽,过滤装置,热水槽,烘干柜等。
实验试剂:苯二酚、浓硝酸、浓硫酸、冰乙酸等。
实验步骤:1.将苯二酚(1.00g)粉末加入干净的干燥量瓶中,加入氨水(1mL),摇匀使苯二酚溶解后得到1%左右的苯二酚溶液;2.在烘干柜中烘干烧杯和磨杵,称取硝酸(1.35g)和硫酸(5mL),加入烧杯中,将烧杯放入冰水中冷却至0℃以下;3.将苯二酚溶液分两次加入到硝酸、硫酸混合物中,每次加入时都要小心滴加,加完每次要慢慢搅拌,并保持反应温度在0-5℃之间;4.反应30分钟后,将反应混合物慢慢倒入500mL水中,搅拌使反应物充分溶解;5.滤掉沉淀,在温水中反复洗涤沉淀,收集所得的2-硝基-1,3-苯二酚固体;6.将所得固体在烘箱中烘干至恒重,记录数据并计算产率。
实验结果:实验过程中,我们通过加入硝化剂反应获得了2-硝基-1,3-苯二酚。
其中,苯二酚通过与硝酸、硫酸混合物发生硝化反应,生成了目标产物——2-硝基-1,3-苯二酚。
经过反应、水解和重结晶等多个步骤,最终获得了白色晶体形式的固体。
2-硝基-1,3-苯二酚的重结晶实验报告

2-硝基-1,3-苯二酚的重结晶实验报告重结晶实验是一种常用的纯化有机物的方法,所用到的化学试剂有水、无水乙醇、氯化钠、2-硝基-1,3-苯二酚等。
下面是2-硝基-1,3-苯二酚的重结晶实验报告。
1. 实验目的本次实验的目的是通过重结晶纯化2-硝基-1,3-苯二酚并测定其熔点。
2. 实验原理当有机物质与其相溶剂在室温下与开瓶状态下的相溶时,相溶液的浓度(即有机物的溶解度)远比加热后相溶液中的浓度要低,而加热到一定温度时相溶液中的有机物浓度会快速增加,随着温度继续升高,有机物浓度又会快速下降,最终在特定的温度范围内达到热平衡。
在这个温度范围内,有机物质的溶解度比开瓶状态下的有机物质浓度高20倍至30倍。
将相溶液恒温缓慢地降温,可以得到大量晶体,晶体产率较高。
这个降温过程,有机物质的溶解度随温度下降,晶体随之析出。
最终得到的晶体经洗涤、过滤、干燥后就是相对纯的有机物质。
3. 实验步骤(1)将1 g的2-硝基-1,3-苯二酚加入小烧杯中,加入约5 mL的无水乙醇溶解,并进行搅拌。
(2)将溶液温水浴加温至水沸腾,使2-硝基-1,3-苯二酚完全溶解,加入一个微小的结晶体用于溶液热辐射杂质。
(3)将热溶液过滤,将滤液移入小烧杯中,加入1 mL的水,然后加入5 mL无水乙醇搅拌混合,使其逐渐降温,直至晶体形成,停止搅拌,放置过夜使其充分析出。
(4)沉淀产物用少量无水乙醇洗涤,保留获得的2-硝基-1,3-苯二酚晶体。
(5)将洗涤过及的晶体过滤,沥干后放入烤箱中50℃干燥10~15min(6)将干燥后的晶体放入烧杯,并加热熔化计算熔点。
4. 实验结果通过本次实验,从溶液中得到2-硝基-1,3-苯二酚晶体,通过纯化操作使得纯度得到提高,经过过滤和干燥后,获得沉淀物重量为0.562 g。
测得获得的2-硝基-1,3-苯二酚晶体熔点为183~184℃。
5. 结论通过重结晶操作得到的2-硝基-1,3-苯二酚晶体较为纯净,熔点与实验室手册上给出的标准熔点185℃相比有所偏低,可能是由于实验中获得的晶体中掺杂了少量杂质所致。
03硝化过程
NHSO2Ph
H2N
作业答案-3
(3)将间甲基苯胺用乙酸酐进行N-酰化反应,形成 间甲基乙酰苯胺,然后在浓硫酸介质中,用理论量的 硝酸进行硝化,所得产物在稀硫酸或氢氧化钠水溶液 水解脱去乙酰基即得到目标分子
Me
NH2 Ac2O Me
NHAc Mixed acid
H2O
conc. H2SO4
Me
NHAc
4)在制备2-硝基-1,3-苯二酚时,将间苯二酚先溶解在约60℃的浓硫酸中, 然后用混酸硝化,最后水蒸气蒸馏;
5)在制备4,6-二硝基-1,3-苯二酚时,将间苯二酚先溶解在乙酸水溶液中, 滴加亚硝酸钠水溶液,同时加入少量亚硫酸氢钠;
6)将2-萘酚-NaOH-NaNO2按照1 : 1 : 1的摩尔比配成混合溶液,然后慢 慢加入到稀盐酸或稀硫酸中制备1-亚硝基-2-萘酚。
NH2 Ac2O
NHAc Mixed acid
Me
H2O Me
conc. H2SO4
NHAc
H2O
NH2
Me
NO2
NaOH or H2SO4
O2N
NO2
作业答案-5
(6)将邻硝基甲基在三氯化铁存在下,慢慢通入理 论量的氯气,会得到下面三种氯化混合物,将混合物 高效精馏、分布结晶即可得到目标分子
Cl
作业答案1mememenhnitrationreduction甲苯用混酸硝化经过高效精馏分离得到邻对以及少量间位的硝基甲苯它们分别催化还原得到相应的甲基苯胺1将邻甲基苯胺低温下溶解于浓硫酸中然后加入理论量的混酸浓硝酸或硝酸钠进行单硝化然后将反应物放入水中析出即得到目标分子nhmehno作业答案22将邻甲基苯胺在水介质中与苯磺酰氯反应形成磺酰胺然后在水苯混合介质中用硝酸氧化硝化最后在浓硫酸中温热水解脱去苯磺酰基再将反应物放入水中析出即得到目标分子nhmephsoclnhsophmehnophmewarmtemperatureme作业答案33将间甲基苯胺用乙酸酐进行n酰化反应形成间甲基乙酰苯胺然后在浓硫酸介质中用理论量的硝酸进行硝化所得产物在稀硫酸或氢氧化钠水溶液水解脱去乙酰基即得到目标分子nhnhacmixedacidnhacmememe作业答案4nhmememe4将对甲基苯胺低温下溶解于浓硫酸中然后加入理论量的混酸浓硝酸或硝酸钠进行单硝化然后将反应物放入水中析出即得到目标分子5将对甲基苯胺转变为对甲基乙酰苯胺然后在浓硫酸介质中用理论量的硝酸进行硝化所得产物在稀硫酸或氢氧化钠水溶液水解脱去乙酰基即得到目标分子nhnhacmixedacidnhacmememeclme6将邻硝基甲基在三氯化铁存在下慢慢通入理论量的氯气会得到下面三种氯化混合物将混合物高效精馏分布结晶即可得到目标分子作业答案67将粉状精萘于50时悬浮于上一批硝化废酸中然后加入混酸进行硝化然后分层经过水洗碱洗降温结晶得到1硝基萘催化氢化得到1萘胺在邻二氯苯中用理论量的浓硫酸在180进行烘焙磺化即得目标分子nh作业答案7811精萘于80时用过量浓硫酸磺化形成1萘磺酸接着向磺化液中加入发烟硝酸进行单硝化得到5和8硝基萘磺酸混合磺酸不用分离直接用铁粉还原或催化加氢得到周位酸与劳伦酸将还原溶液ph值调节45析出周位酸再将滤液ph值调节为35析出perigynousacidlorenzacid作业答案8910精萘于160时用过量浓硫酸磺化形成2萘磺酸接着向磺化液中滴加稍过量的发烟硝酸进行单硝化得到5和8硝基2萘磺酸混合磺酸不用分离直接用铁粉还原或催化加氢得到16与17克力夫1错误二硝基苯主要在第一个硝化器的酸相中形成因为第一锅酸相中硝酸浓度较高而且硫酸水之比较高其反应动力学属于快速传质瞬间型
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2-硝基-1,3苯二酚
在100ml的烧杯中放置2.8g粉状的间苯二酚,在充分的搅拌下小心加入13ml浓硫酸,此时反应液发热,立即生成白色的磺化产物,在室温放置15min,然后在冰水浴中冷至0~10℃。
在锥形瓶中加入2ml浓硝酸,在摇振下加入3ml浓硫酸制成混合酸并置与水浴中冷却。
用冷却好的混合酸慢慢滴加到上述磺化后的反应物中,并不停的搅拌,控制反应温度不超过30℃,反应物橙黄色粘稠状(不应为棕色或紫色)。
滴加完毕,在室温放置15min,然后小心加入15ml冰水稀释,保持反应温度不超过50℃。
将反应物转移到100ml三颈瓶中,加入约0.1g尿素,然后按图装置仪器进行水蒸气蒸馏,冷凝管壁和流出液中有橙红色固体产生,至冷凝管壁上无橙红色固体产生时,即可停止蒸馏。
将馏出液在水浴上冷却后,减压抽虑,粗产物用乙醇—水(约需5ml 50%乙醇)重结晶,得橘黄色片状结晶,产量约1g。
纯粹2-硝基-1,3苯二酚的熔点为84~85℃。
本实验约需4h。
