使用方法启普发生器制取氢气
实验三 氢气的制取与性质实验

实验三 安全性实验及其教学研究 ——氢 气 的 制 取 与 性 质 实 验一、氢气的制取1.相关知识:置换反应,氢气的物理性质与化学性质,气体的收集方法。
①置换反应:无机化学反应的基本类型之一,指一种单质和一种化合物生成另一种单质和另一种化合物的反应。
置换原则为活动性强的金属置换活动性弱的金属溶液。
本实验利用活泼金属Zn 置换稀H 2SO 4中的H +制备H 2,原理:Zn+H 2SO 4=H 2↑+ZnSO 4②氢气物理性质:无色无味无毒,密度比空气小的气体(在各种气体中,氢气的密度最小);温度-252.87℃时,转变成无色的液体,-259.1℃时,变成雪状固体。
③氢气化学性质:可燃性:纯氢的引燃温度为400℃,氢气可作为燃料,应用与航天、焊接、军事等方面;还原性:可用于冶炼某些金属材料等。
④气体收集方法:排水法:氢气难溶于水;向下排空气法:氢气密度比空气小。
2.实验用品:(请画实验装置图,并标明各药品和仪器名称)①实验仪器:启普发生器、烧杯、集气瓶、毛玻片、导管、水槽;②实验药品:锌粒、浓硫酸溶液、去离子水、硫酸铜溶液、凡士林。
3.实验步骤(用简洁明了的方法比如流程图表示):日期 2014 年4月8日; 第七周周二,下午; 姓名 陈博殷 学号20112401073 成绩 锌粒 稀硫酸氢气检查启普发 生器气密性 配制稀硫酸(1:4) 装入锌粒及稀硫酸 收集氢气 水槽集气瓶启普发生器开启旋塞,向球形漏斗中加水,当水充满容器下部的半球体时关闭旋塞,继续加水,使水上升到球形漏斗中。
静置片刻,观察水面是否下降,如下降说明漏气,在一段时间内不发生变化,表明气密性良好。
漏气处可能是容器上气体出口处的橡皮塞、导气管上的旋塞或长颈漏斗与容器接触的磨口处。
如漏气应塞紧橡皮塞或在磨口处涂一薄层凡士林。
(凡士林要涂抹均匀:仪器旋转润滑,磨口处整体颜色透明无白色。
将浓硫酸慢慢倒入水中,不断搅拌。
(稀硫酸稀释时,放出大量热,若把水倒入浓硫酸,水会像油花似的浮在浓硫酸上面,产生的高热会使水沸腾起来,使酸液飞溅,造成事故。
启普发生器
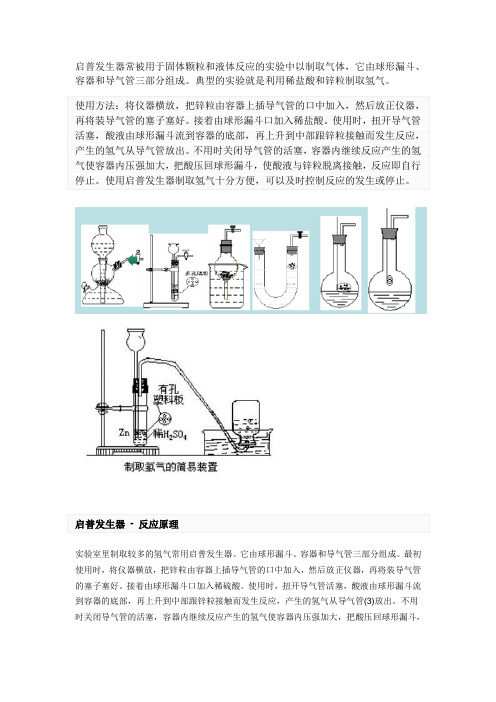
启普发生器常被用于固体颗粒和液体反应的实验中以制取气体,它由球形漏斗、容器和导气管三部分组成。
典型的实验就是利用稀盐酸和锌粒制取氢气。
实验室里制取较多的氢气常用启普发生器。
它由球形漏斗、容器和导气管三部分组成。
最初使用时,将仪器横放,把锌粒由容器上插导气管的口中加入,然后放正仪器,再将装导气管的塞子塞好。
接着由球形漏斗口加入稀硫酸。
使用时,扭开导气管活塞,酸液由球形漏斗流到容器的底部,再上升到中部跟锌粒接触而发生反应,产生的氢气从导气管(3)放出。
不用时关闭导气管的活塞,容器内继续反应产生的氢气使容器内压强加大,把酸压回球形漏斗,使酸液与锌粒脱离接触,反应即自行停止。
使用启普发生器制取氢气十分方便,可以及时控制反应的发生或停止。
1.发明启普发生器是化学实验室中最普通、应用最广的玻璃仪器,它设计上的巧妙,堪称化学仪器中的一绝。
仪器的发明人启普是荷兰的一名药物商人,曾经学过一些化学。
他根据前人制作的制取硫化氢气体的简易装置,设计出一种可以随时使反应发生或停止的气体发生装置,后人为纪念他,将这种装置叫做启普发生器。
2.工作原理(以用稀硫酸和锌粒制取氢气为例)打开活塞,容器内压强与外界大气压相同,球形漏斗内的稀硫酸在重力作用下流到容器中,与锌粒接触,产生氢气;关上活塞后,由于酸液继续与锌粒接触,氢气依然生成,此时容器内部压强大于外界大气压,压力将酸液压回球形漏斗,使酸液与锌粒脱离接触,氢气不再产生。
3.使用范围启普发生器是用固体与液体试剂在常温条件(不用加热)下起反应制取气体的典型装置。
如氢气、二氧化碳、硫化氢等均可以用它来制取。
但对于固体呈粉末状或固体与液体相遇后溶解或反应时产生高温者,如二氧化硫、二氧化氮等,都不适宜用此装置制取。
4. 规格启普发生器的规格以球形漏斗的容积大小区别,常用为250 mL或500 mL。
(1)使用前要检查装置气密性,排尽空气后再收集气体;(2)使用启普发生器制备氢气,应远离火源;(3)移动启普发生器时,要握住球形容器的蜂腰处,千万不可单手握住球形漏斗,以免底座脱落造成事故。
启普发生器

1、启普发生器是一个简单、有趣的组合仪器,由
荷兰人启普1864年发明。启普发生器是一种气体 发生器,它由球形漏斗、容器和导气管三部分组 成。它常被用于固体颗粒(或块状)和液体反应 的实验中以制取气体。典型的实验就是利用稀盐 酸(或稀硫酸)和锌粒制取氢气。
2、使用前应先检查装置的气密性。 方法:开启旋塞,向长颈漏斗中加水。当水 充满容器下部的半球体时,关闭旋塞。继 续加水,使水上升到长颈漏斗中。静置片 刻,若水面不下降,则说明装置气密性良 好,反之则说明装置漏气。如漏气,应塞 紧橡皮塞或在磨口处涂上一薄层凡士林。
பைடு நூலகம்
3、反应原理:使用时,把锌粒由容器上插导气管的 口中加入,然后放正仪器,再将装导气管的塞子 塞好。接着由球形漏斗口加入稀盐酸。使用时, 扭开导气管活塞,酸液由球形漏斗流到容器的底 部,再上升到中部跟锌粒接触而发生反应,产生 的氢气从导气管放出。不用时关闭导气管的活塞, 容器内继续反应产生的氢气使容器内压强加大, 把酸液压回球形漏斗,使酸液与锌粒脱离接触, 反应自行停止。
4、使用范围:启普发生器是用固体与液体试 剂在常温条件(不用加热)下起反应制取 气体的典型装置,能使固体和液体分离。 如氢气、二氧化碳等均可以用它来制取。 但对于固体呈粉末状或固体与液体相遇后 溶解都不适宜用此装置制取。 5、优点:符合“随开随用、随关随停”的原 则。能节约药品,控制反应的发生和停止, 可随时向装置中添加液体药品。
利用简易启普发生器制备氢气

[] I 张彩丽. 学教 学中培 养学生探究能力 的措施.农村 化 实用 科 技 信 息 , 09,O ) 2 0 (5 ( 接上页 ) 使其得以巩固和深入 , 形成问题解决策略的迁移能力。 5 教 师 要 适 当地 组 织 学 生 分 组 , 好 能 按 学 生 学 习 能 力 、 最 的强弱 交叉 分组 , 发挥互补优 势 , 以体现互助合作精神 。
一
、
简 启 普发 生器 的制作
简易启普 发生器是 根据普通启普发生器的结构和使用 原 理, 利用常用的化学实验器材或代用 品装配 而成 的。 1制作原理: . 在反应时打开一边 的弹簧夹, 使大气压压下漏 斗中的液体, 内压大于外压的情况 , 形成 就可以做到液体 与固体 相接触 ; 在关闭弹簧夹时 , 由于容器中正在反应 , 内压大于外 则使 压, 压强又把液体压回到漏斗上, 实现液相和固相的分离。 2 需要 的材料 : . 带有支管 的试 管 、 塑料 ( 橡胶 ) 隔板 、 长颈 漏斗 、 玻璃管 3 制作过程 : . 将塑料 隔板剪成 与试 管 口同样 大小 , 在塑 并 料 隔板 中央 开 一个 孔 ( 小 为 长颈 漏 斗 可 以插 下 即可 )再 在 塑 大 , 料隔板 四周开一圈稍微小一点 的孔 ; 接着将做 好的塑料隔板放 人带有支管的试管 中( 位置在离试管底部的三分之一处 )再在 ; 塑料隔板上放上几粒锌粒 , 在长颈漏 斗 中加入稀 硫酸 , 这样一 台简易的启普发生器就制作 而成 了。如下图一所示 :
二、 氢气 的制 备
简易启普发生器制作好后 , 再用导管连接 出来 , 用排水 利 法收集氢气 , 如下 图二所示 : 把弹簧夹打开时 , 酸液 由漏斗 流下 , 试管 中液面上 升与锌 粒接触 , 生反应 , 发 产生 的气体 由支管 口导 出, 在关 闭 弹簧夹 时 , 管中液面下 降 , 试 漏斗 中液面上升 , 酸液与锌粒脱离接 触 , 反应 自行停止 。 反应方程式 :n + H S 4 Z S 4+H2 z 2O = nO t
启普发生器

简介英文名:Gas generators启普发生器一种实验室常用的气体发生装置,是荷兰科学家启普(Petrus Jacobus Kipp 1808~1864)发明,并以他的姓命名。
它用普通玻璃制成,构造见图。
它由球形漏斗、容器和导气管三部分组成。
适用于块状固体与液体在常温下反应制取气体,如氢气、硫化氢等。
块状固体在反应中很快溶解、或变成粉末时,不能用启普发生器。
如果生成气体难溶于反应液,可以使用。
如二氧化碳可溶于水,但难溶于盐酸;故用石灰石与盐酸反应制二氧化碳时可用启普发生器。
注意!启普发生器不能用于加热!气密性检查使用前应先检查装置的气密性。
方法:开启旋塞,向球形漏斗中加水。
当水充满容器下部的半球体时,关闭旋塞。
继续加水,使水上升到长颈漏斗中。
静置片刻,若水面不下降,则说明装置气密性良好,反之则说明装置漏气。
漏气处可能是容器上气体出口处的橡皮塞、导气管上的旋塞或长颈漏斗与容器接触的磨口处。
如漏气,应塞紧橡皮塞或在磨口处涂上一薄层凡士林。
启普发生器具体操作固体试剂由容器上的气体出口加入,加固体前应在容器的球体中加入一定量的玻璃棉或放入橡胶垫圈,以防固体掉入半球体中。
加固体的量不得超过球体容积的1/3。
液体试剂从长颈漏斗口注入,注液方法与上述注水方法相同。
液体的量以反应时刚刚浸没固体,液面不高过导气管的橡胶塞为宜。
使用时,打开导气管上的旋塞,长颈漏斗中的液体进入容器与固体反应,气体的流速可用旋塞调节。
停止使用时,关闭旋塞,容器中的气体压力增大,将液体压回长颈漏斗,使液体和固体脱离,反应停止。
为保证安全,可在球形漏斗口加安全漏斗(见图),防止气体压力过大时炸裂容器。
特点:符合“随开随用、随关随停”的原则。
能节约药品,控制反应速率和反应的发生和停止,可随时向装置中添加药品。
2规格容量/ml 底直径/mm中球直径/mm上球直径/mm全高/mm容量/ml底直径/mm中球直径/mm上球直径/mm全高/mm25012082903141000175130140450 5001459811036020002101601705803发明者启普发生器的发明人叫启普,是荷兰人,他生于1808年3月5日,1864年2月3日病故,终年57岁。
启普发生器

启普发生器(Kipp's apparatus),是一种气体发生器,又称启氏气体发生器或氢气发生器。
它用普通玻璃制成,构造见图。
它由球形漏斗、容器和导气管三部分组成。
适用于块状固体与液体在常温下反应制取气体,如氢气、硫化氢等。
块状固体在反应中很快溶解、或变成粉末时,不能使用启普发生器使用前应先检查装置的气密性。
方法:开启导气管上的旋塞,向球形漏斗中加水。
当水充满容器下部的半球体时,关闭旋塞。
继续加水,使水上升到长颈漏斗中。
静置片刻,若水面不下降,则说明装置气密性良好,反之则说明装置漏气。
漏气处可能是容器上气体出口处的橡皮塞、导气管上的旋塞或长颈漏斗与容器接触的磨口处。
如漏气,应塞紧橡皮塞或在磨口处涂上一薄层凡士林。
特点:符合“随开随用、随关随停”的原则。
能节约药品,控制反应的发生和停止,可随时向装置中添加液体药品。
使用时,打开导气管上的旋塞(使容器内气压与外界大气压相等),球形漏斗中的液体进入容器与固体反应,气体的流速可用旋塞调节。
停止使用时,关闭旋塞,容器中的气体压强增大(因为容器中的反应仍在进行,仍有气体生成),将液体压回球形漏斗,使容器中液体液面降低,与固体脱离,反应停止。
为保证安全,可在球形漏斗口加安全漏斗,防止气体压力过大时炸裂容器。
注意事项1.使用前要检查装置气密性,排尽空气后再收集气体;2.使用启普发生器制备氢气,应远离火源;3.移动启普发生器时,要握住球形容器的蜂腰处,千万不可单手握住球形漏斗,以免底座脱落造成事故。
4、不能用于制乙炔。
因为:a.反应会产生糊状物Ca(OH)2,即氢氧化钙,堵住支管口;b.碳化钙(CaC2)与水反应较剧烈,难以控制反应速率;c.反应会放出大量热量,若操作不当,会炸裂启普发生器;5、向启普发生器中添加固体时,需用橡胶塞将球形漏斗口塞紧,然后取下容器上的橡胶塞加入固体。
液体需要更换时,也应塞紧漏斗口,然后拔下容器底部的液体出口塞,使废液缓缓流出,塞上液体出口塞后,再从球形漏斗口注液。
实验室制取氢气

实验室制取氢气⒈问:为什么制氢气可以用启普发生器?答:由于实验室制氢气所用的试剂为块状固体的锌和酸溶液,在不加热的情况下制取气体,且生成的氢气难溶于水,满足启普发生器的适用条件。
所以,可以用它来制取氢气。
⒉问:怎样检查启普发生器的气密性?答:检查启普发生器气密性的方法是:将启普发生器装置好后,先开启导气管的活塞,经由球形漏斗口注入水充满半球体至容器内浸没底部活塞。
检查半球体上的玻璃活塞是否有水渗出。
若漏水,要倒出容器内的水,取出活塞擦干,重新涂上凡士林,并塞紧后再检查。
若不漏水,则关闭导气管活塞,继续从球形漏斗注入水至漏斗的1/2处时止,标记好水面的位置,静置,然后观察水面是否下降,若水面不下降则表明不漏气。
如下降就表示漏气,检查出漏气的地方,加以调整或在漏斗与容器接口处涂上一薄层凡士林或调换导气管的橡皮塞。
⒊问:为何在启普发生器底座的容器中装有些碎玻璃片等?答:装碎玻璃片等是为了让它们去占据空间,目的是减少启普发生器中酸的用量。
⒋问:制氢简易装置中,长颈漏斗为什么一定要插入液面下?答:主要是为了避免漏气。
如果不将长颈漏斗插入液面下,生成的氢气可能从长颈漏斗里逸散掉,使收集到的氢气量减少或不能收集到氢气。
⒌问:为什么实验室一般都用锌制氢气?能否用常见的金属铁或活泼金属镁?答:实验室制取物质时须考虑,反应速度适中、原料易得而且价格便宜、操作简便及安全问题。
铁和镁都能与酸反应生成氢气,但由于镁与酸反应速度太快,不易控制,操作起来很不方便,而且镁的价格较高。
而铁与酸反应的速度较慢,而且铁片中常含有硫、磷等杂质,使生成的氢气不纯。
因此,实验室制氢气一般都不用铁和镁等。
只有锌与酸反应的速度较适中,而且价格也较低廉。
所以,实验室一般都用锌与稀硫酸反应来制取氢气。
⒍问:用于制氢气的锌,纯度高好还是低好?答:制氢气所用的锌纯度低一些好。
因为纯锌表面易吸附氢气,减少了锌表面与酸的接触机会,使反应速度减慢。
通常用废干电池壳来代替锌粒,其效果很好。
氢气的制备与性质

氢气的制备与性质化学一班第五实验小组一、实验原理Zn+H2SO4稀=ZnSO4+H2↑2H2+O22H2OH2+CuOCu+H2O二、实验操作过程与实验现象1、利用启普发生器制取氢气启普发生器如图所示由三部分组成.上面一部分是球形漏斗,下面一部分是玻璃球和玻璃半球所组成的容器,第三部分是带旋钮的导气管.启普发生器的适用范围:固液不加热反应;反应物是颗粒或块状;反应过程中易放热得不行;反应所产生的气体若溶于水或反应液也不能用.此外使用启普发生器是一定要远离火源.装料前,先检查各接缝处的气密性.方法是关住导气管上的旋钮,由漏斗处注入水后,在液面处划一记号,若数分钟内液面不下降,说明气密性好;若下降,可涂凡士林密封.同时再拧紧导气管处的橡皮塞.同时还要检漏,方法是打开导气管上的旋钮,向玻璃半球中注水,使液面高于排液口,然后用手触摸排液口,若其渗水,则气密性不好,涂抹凡士林;若不渗水,则气密性良好.给启普发生器中加水至将金属锌全部淹没处,倒水后量水的体积,这就是稀硫酸的体积.在球形漏斗颈适当位置用玻璃丝编绕数圈,或穿一塑料片,以阻止锌粒下落.将容器侧身由上口或侧口处加入用CuSO4溶液浸泡过的锌粒,再将漏斗插入,用玻璃棒将玻璃丝拨至容器细颈处后,将发生器放置,安上导气管,打开旋钮,由上口加入稀硫酸至淹没锌粒处,关上旋钮,固、液体分离,稀硫酸液面升至漏斗处.2、H2的性质(1)H2纯度的检验打开旋钮,用排水法收集一试管H2,管口向下移近火焰,放开拇指,若有尖锐的爆鸣声,证明氢气不纯,要继续收集并检验,直至发出轻微的“噗”声为止,此时H2以纯,可以使用.2H2在空气中燃烧检验纯度后,在导管上连接一玻璃管,点燃后,在深色背景下,可明显看到氢气在空气中安静的燃烧,发出淡蓝色火焰.在火焰上方罩一干净的烧杯,片刻烧杯内壁就有液滴沿壁流下.3H2与空气混合气的爆鸣取一小塑料瓶,在底部凿一火柴梗粗细小孔,食指堵住小孔,用排水法集满H2后倒放于桌面上口部垫上石棉网以保证空气流畅.点燃火柴,放开手指,用过火柴梗捅破小孔水膜,点燃H2,深色背景下因H2较纯,火焰燃烧平静,可看到淡蓝色火焰,过一会儿空气从盒底口流入,积聚到一定比例,发生爆鸣.当H2和空气的体积比为2:5时,产生的爆鸣声音最大.4H2吹肥皂泡取少量洗涤剂用蒸馏水配成溶液,,用橡皮管在洗涤液中蘸一下,管口仍朝下 ,慢慢开通H2流,待气泡出现后,将管口迅速反转朝上,轻轻摆动或用嘴吹气,泡泡脱离管口,用火在气泡上方点燃,随着“噗”的一声伴有黄色火球出现.5H2还原CuO先往试管内加入氧化铜,把氢气导气管伸入试管底部,先通入氢气一段时间是为了把氧气清除,否则加热后氧化铜会与氧气反应,影响试验再加热试管,使氢气还原氧化铜,看到黑色氧化铜全部变成红色时,停止加热,继续通入氢气若先停止通氢气,则收集氢气处的水会倒吸入试管内,使热试管炸裂 ,同时被还原的铜又会被氧气氧化,待试管冷却后,停止通氢气.反应方程式:反应方程式:CuO+H2 Cu+H2O装置如图:检查紫红色的金属铜中是否含有CuO,可将制成的紫红色金属铜取少量加入盛有稀H2SO4的试管中,观察溶液是否变蓝.CuO+H2SO4=Cu+CuSO4+H2O三、注意事项1使用启普发生器时,容器底座的活塞最好用绳子扎紧,以免H2压力过大因锌的颗粒小而落入酸液中不断反应使然,冲开活塞.2为使反应速率更快,先将锌粒浸在CuSO4溶液中直发黑,再给发生器中加入.3启普发生器使用完毕,用塞子堵住漏斗口,将发生器侧身,由下口倒出废酸液统一收集,拔下导气管塞子此处倒出余锌要回收,将发生器清水冲洗干净擦干净磨口处凡士林并垫一硬纸收藏.4启普发生器使用过程中若要再添酸或锌,产生H2后必须先验纯后使用,否则会出现不安全事故.5H2吹肥皂泡因玻璃管表面光滑,沾不住皂液,难以吹成,故用橡皮管.此外,还可用竹管来代替.6 H2与空气的混合气体发生爆鸣的极限为4%%体积分数.若筒内H2浓度过高即超过爆鸣上限时,点火后首先是它的安静燃烧.由于燃烧消耗H2 ,使筒内压强变小,空气便从下口源源不断地进入筒内,当H2的含量进入爆鸣范围,即发生爆鸣.四、相关文献及重点文献综述1一、提高制取氢气反应速度的方法往锌粒中放一团或几团随意曲折的铜或铁丝并使之与锌粒和酸液充分接触.这样可提高制取氢气的反应速度.原因是市售锌粒纯度较高, 往其中加人铜丝或铁丝可以在反应体系中形成铜锌或铁锌原电池, 加速锌的氧化过程, 从而提高氢气生成的速度.、往锌粒和酸液中倒人少量的硫酸铜溶液, 可以收到类似的效果.往锌粒中加人少量做氢气还原氧化铜实验时回收的铜的混和物, 可使制取氢气的反应速度大大提高, 同时回收的废物也得到了充分的利用.二、在试管口点燃氢气按课本上叙述的情况操作, 氢气燃烧及爆鸣现象不明显, 是因为实验中产生氢气的速度太慢所致.改进方法按一、提高制取氢气反应速度的方法之一进行操作, 当产生氢气速度较快时, 先用拇指堵住试管口一分钟,然后再将燃着的火柴放在试管口,如果氢气不纯净, 就能听到尖锐的爆鸣声如果氢气纯净,可观察到蓝色火焰,过一会儿,才能听到爆鸣声.三、反应产物的验证按课本方法将锌粒与稀硫酸反应后的液体倒人蒸发皿,加热使液体蒸发, 若蒸发的液体量少时, 出现的少量晶体看不清楚若蒸发的液体量多时, 需要的时间较长.再者蒸发皿本身是白色的瓷器, 硫酸锌晶体也是白色的, 当老师拿起蒸发皿让学生观察时, 多数学生看不清楚, 因此影响教学效果.改进方法把反应后的液体滴一滴到玻璃片上, 掂起一角, 使液滴向周围滚动, 然后将玻璃片反转,放在酒精灯外焰上来回烘烤, 半分钟后即可看到玻璃片上出现白色的硫酸锌晶体.因玻璃片是无色透明的平面, 白色固体沾在玻璃片上显得非常清晰, 故所有的学生都能看看得清清楚楚.实验改进后, 具备现象明显、有利于观察, 所需时间短、节约药品、成功率高等优点, 并且有些回收的废药品也得到了充分利用, 解决了课本实验中存在的不足, 同时也提高了课堂教学效果.七、参考文献1 第14卷第14期邢台师范高专学报陈秀玲胡章记。
氢气的制法和性质实验报告

氢气的制法和性质一、 实验原理1.一般在实验室制取氢气所选用的原料是金属锌和稀硫酸,其反应的原理如下:2442Zn+H SO (= ZnSO +H 稀) ↑2. 氢气的性质物理性质:1.通常情况下,无色无味气体;2. 密度比空气小;3. 难溶于。
化学性质:1.可燃性 2222H +O 2H O 点燃2.还原性 22H +CuO Cu+H O二、 实验操作过程与实验现象(一):启普发生器简介(1)构造启普发生器由三部分组成,上部是球形漏斗,下部是由玻璃球和玻璃半球组成的容器,第三部分是带旋钮的导气管。
启普发生器的规格以球形漏斗的容积大小来区别,常用为250 mL 或500 mL 。
(2)原理当打开导气管的活塞,球形漏斗中的液体落入容器与窄口上固体接触而产生气体;当关闭活塞,生成的气体将液体压入球形漏斗,使固、液体试剂脱离接触而反应暂行停止,可供较长时间反复使用。
(3)适用范围适用于固液不加热型反应,且反应时固体或颗粒不会迅速溶解。
对于反应过程中放出大量热的反应或者反应生成的气体易溶于水(或反应液)的均不可以使用启普发生器。
(4)注意事项1: 移动启普发生器时,要握住球形容器的蜂腰处,千万不可单手握住球形漏斗,以免底座脱落造成事故;2: 使用前应先查漏、查气密性;查漏:打开导气管上的旋钮,由球形漏斗处注入水,液面稍高过废液口,观察废液口是否有水渗出,若没有则不漏水。
若有则需旋紧此处的玻璃塞。
查气密性:关闭导气管上的旋钮,由球形漏斗处注入水,量大约是球形漏斗的1/2或2/3处停止,在液面处划一记号,若数分钟内液面不下降,则气密性良好。
反之则说明装置漏气,漏气处可能是,容器上气体出口处的橡皮塞、导气管上的旋塞或长颈漏斗与容器接触的磨口处。
如漏气,应塞紧橡皮塞或在磨口处涂上一薄层凡士林。
3:在容器中部窄口上面加一橡胶圈或紧密缠绕适量玻璃纤维,以防止固体落人容器下部,造成事故;4:加入试剂时,先加块状固体。
氢气的制备实验报告

氢气的制法与性质一、实验目的与要求1、熟悉启普发生器的原理和构造;2、掌握其操作技能;3、掌握演示H2的性质实验安全操作技能;4、初步掌握H2还原CuO实验的方法。
二、实验原理Zn+H2SO4(稀)=ZnSO4+H22H 2+O2=2H2O (条件:点燃)H2+CuO=Cu+H2O (条件:加热)三、仪器与药品仪器:启普发生器、烧杯、水槽、橡皮管、试管及试管架、玻璃导气管、玻璃尖嘴管、铁架台、凡士林、塑料瓶、玻璃棒、酒精灯、玻璃丝、火柴、蒸发皿、石棉网药品:洗涤剂溶液、CuSO4溶液、锌粒、稀H2SO4(1:4)、甘油、氧化铜四、实验内容1、利用启普发生器制取氢气启普发生器(如下图)由三部分组成。
上面一部分是球形漏斗,下面一部分是玻璃球和玻璃半球组成所组成的容器,第三部分是带旋钮的导气管。
装料前,先检查各接缝处的气密性。
方法是关住导气管的上旋钮,由漏斗处注入水后,在液面处划一记号,若数分钟内液面不下降,说明气密性好;若下降,可涂凡士林密封。
给启普发生器中加水至将金属锌粒全部淹没处,倒水后量水的体积,这就是稀硫酸的体积。
在球形漏斗颈适当位置用玻璃丝编绕数圈,以防止锌粒下降。
将容器侧身由上口或侧口处加入用CuSO4溶液浸泡过的锌粒,再将漏斗插入,用玻璃棒将玻璃丝拨至容器细颈处后,将发生器放直,安上导气管,打开旋钮,有上口加入稀硫酸(1:4)至淹没锌粒处,关上旋钮,固、液分离,稀硫酸液面升至漏斗处。
2、H2的性质⑴H2纯度的检验打开旋钮,用排水法收集一试管氢气,管口向下移近火焰,放开拇指,若有尖锐的爆鸣声,证明氢气不纯,要继续收集并检验,直至只发出轻微的“噗”声为止,此时氢气已纯,可以使用。
⑵氢气在空气中燃烧检验纯度后,在导管上连接一尖嘴玻璃管,点然后,在深色背景下,可明显看到氢气在空气中安静的燃烧,发出淡蓝色火焰。
在火焰上方罩一干净烧杯,片刻烧杯内壁就有液滴顺壁流下。
⑶H2与空气混合气的爆鸣取一端开口的易拉罐,在底部凿一火柴梗粗细小孔,排水法集满氢气后,倒置于桌面上,口部垫上石棉网以保证空气畅通。
启普发生器制取氢气实验步骤

启普发生器制取氢气实验步骤1. 实验准备嘿,朋友们,今天咱们要来搞个有趣的实验,制取氢气!你听说过启普发生器吗?这玩意儿可真是个神奇的工具,能让咱们从水中提取氢气。
哇,想想就觉得炫酷得很!不过,别急,咱得先准备好一切。
1.1 准备工具首先,咱们需要的东西不多,但每样都得用到哦。
准备一个启普发生器,这家伙看上去有点复杂,但其实没那么可怕。
然后,咱们还需要一些水,最好是蒸馏水,这样杂质少,不影响实验效果。
还有就是电源,毕竟没有电可做不了什么。
别忘了,安全第一,记得准备好护目镜和手套,保护好自己可不能马虎!1.2 材料清单好啦,材料清单来了!你需要:启普发生器、蒸馏水、电源、护目镜和手套。
听起来简单吧?没错,就是这些!记得把这些都准备好,不然实验就得“流产”了。
哈哈,咱们可不能让实验不如意!2. 实验步骤准备好了吗?那么开始吧!这个过程就像调皮的小孩子,虽然有点麻烦,但绝对有趣!2.1 组装设备首先,把启普发生器的各个部件组装好。
这就像搭积木,按照说明书上的步骤,认真点儿,别让它变成一堆废铁。
然后,找到水箱,把事先准备好的蒸馏水倒进去。
记得水位要在合适的范围内,不能太多也不能太少,正好就行。
接下来,连接电源,确保一切都妥妥的,千万别漏电哦!2.2 启动实验现在是时候启动设备了!打开电源,你会看到水开始冒泡,就像在喝汽水一样。
这是个好兆头,说明氢气正在生成。
哦,对了,氢气可轻易就能逃跑,所以要小心别让它“跑了”。
如果一切顺利,几分钟后,你就能在管道里看到气泡,真的是太神奇了,像是魔法一样!不过,别光顾着看,记得留意一下设备的温度,太热可不太好。
3. 收集氢气氢气生成了,接下来咱们得收集它。
真是激动人心的时刻!3.1 准备收集装置找一个干净的气体收集瓶,确保它能安全地储存氢气。
把收集瓶的嘴放在发生器的气体出口处,确保没有缝隙,氢气才能顺利进入瓶子里。
这样一来,你就可以在瓶子里看到氢气的身影了!要小心点,这可是易燃气体,万一点个火,哎呀,可就不得了了。
14初高中化学衔接——启普发生器的构造和原理

14初高中化学衔接——启普发生器的构造和原理启普发生器是一种常用的实验装置,主要用于制备氢气和二氧化碳气体。
它由一个酸和一个活性金属构成,通过酸和金属之间的反应产生气体。
启普发生器的构造主要包括反应瓶、气体收集瓶和导管,以及一些连接的管道和阀门。
反应瓶是一个固定的玻璃容器,通常是一个瓶子或一个棒状的容器。
它的顶部有一个开关按钮,可以用来控制气体的流动。
在反应瓶的底部有一个活性金属,如锌或铝箔,也可以加入一些稳定剂来增强反应效果。
气体收集瓶是一个密封的容器,用于收集由反应产生的气体。
它通常是一个漏斗形状的容器,有一个较小的孔,可以连接到导管,以便将气体引入其他设备或容器。
启普发生器的原理是基于酸和金属之间的化学反应。
常用的酸包括盐酸(HCl)或硫酸(H2SO4),金属一般是锌(Zn)或铝(Al)。
在反应过程中,酸会与金属发生反应,产生氢气和相应的盐。
反应的化学方程式可以表示为:2HCl+Zn→ZnCl2+H2↑H2SO4+Zn→ZnSO4+H2↑在这些反应中,酸会损失H+离子,而金属会失去电子,转化为正离子。
在高温和压力的作用下,金属会与酸反应更快。
氢气会通过导管流出,进入气体收集瓶中。
为了保持反应的持续进行,可以使用水槽或其他冷却装置对酸和金属进行冷却。
这样可以减缓反应速度,防止过热引起的危险。
启普发生器在实验中有着广泛的应用。
氢气通常用于气体收集实验、气体采样和潜水装置。
二氧化碳可以用于光合作用实验、小型温室和一些化学合成反应。
启普发生器的简单构造、易于操作和安全性使其成为化学实验室中最常用的装置之一总结起来,启普发生器是一种用于制备氢气和二氧化碳气体的实验装置。
它由反应瓶、气体收集瓶和导管等构成,通过酸和活性金属之间的化学反应产生气体。
启普发生器具有广泛的应用,并且在化学实验中具有重要的地位。
启普发生器的构造和使用方法

启普发生器的构造和使用方法启普发生器是一种常用的供电设备,它可以用于应急备用电源、户外活动、露营等场合。
以下是启普发生器的构造和使用方法的详细描述:1. 构造:启普发生器通常由发动机、发电机、控制器、燃油系统、排气系统、冷却系统和外壳等组成。
发动机通常采用内燃机,可以是汽油发动机或柴油发动机。
发电机负责将机械能转换为电能,控制器用于监控电流和电压等参数,保证发电机的正常运行。
燃油系统提供燃料,排气系统负责将燃烧后的废气排出,冷却系统则保证发动机正常工作温度。
外壳则用于保护整个设备。
2. 使用方法:在使用启普发生器之前,首先需要将其放置在平稳的地面上,并确保通风良好。
接着填充足够的燃料和机油,然后启动发动机。
在启动后,可以通过控制器监测电流和电压是否正常。
在使用过程中,需要严格按照说明书上的规定进行操作,防止发生故障。
使用完成后,及时清理发生器外壳和冷却系统,以确保下次使用时设备处于良好状态。
3. 安全注意事项:在使用启普发生器时,需要特别注意安全事项。
严禁在室内使用汽油发动机,以免产生一氧化碳中毒。
避免发动机运转过程中接触旋转部件,以免造成伤害。
严格按照规定放置燃料和机油,避免发生火灾或泄漏事故。
定期对发电机进行维护和保养,以保证设备的长期稳定运行。
4. 适用场合:启普发生器适用于许多场合,包括家庭备用电源、露营旅行、野外施工、移动活动等。
在停电或无法连接市电时,启普发生器可以提供紧急电力支持;在户外活动中,启普发生器可以提供电力供应,方便使用电器设备。
在露营或野外施工中,启普发生器也可以满足电力需求。
启普发生器由于其结构坚固、使用方便而受到人们的青睐,它是一种灵活、便携的电力设备,可以满足多种场合的电力需求。
使用方法启普发生器制取氢气

CaCO3 2HCl CaCl2 CO2 H2O
讨论
制取二氧化碳药品的选择
1、Na2CO3+2HCl ====2NaCl + H2O + CO2 2、CaCO3+H2SO4====CaSO4+H2O + CO2
解释:
1、不用碳酸钠和碳酸钙粉末与酸反应来 制取二氧化碳是因为反应速度太快,来不及收 集,且成本较高。 2、不用大理石与硫酸反应来制取二氧化 碳是因为反应生成的硫酸钙微溶于水,覆盖在 大理石的表面,阻止反应的进行。
CO2的实验室制法
你所知道的能生成CO2的反应有 哪些?能用化学方程式表示的,请 写出化学方程式。
1、上述这些反应能否用于实验室制取CO2? 简要说明理由。 2、根据以上分析,你认为实验室制取气体时, 从原理上来说,主要考虑哪些因素?
①原料来源
③生成物是否较纯
②反应条件
④生成的气体是否方便收集
探究与活动一:如何选择制取二氧化碳的药品?
实验方案实验现象反应速率在试管中加入少量碳酸钠粉末再滴加稀盐酸在试管中加入少量石灰石再滴加少量稀硫酸在试管中加入少量石灰石再滴加稀盐酸有大量气泡产生很快有大量气泡产生开始时有少量气泡产生很快反应停止1从以上实验的对比分析可以看出第组药品最适合用于实验室制取co适中慢且很快就停止反应cocaclhclcaco2hcl2nacl解释
①在试管中加入少量碳酸钠 有大量气泡产生 粉末,再滴加稀盐酸 很快 ②在试管中加入少量石灰石, 开始时有少量 慢,且很快 气泡产生, 再滴加少量稀硫酸 就停止反应 很快反应停止 ③在试管中加入少量石灰石, 有大量气泡产生 再滴加稀盐酸 适中
③ 组药 (1) 从以上实验的对比分析可以看出,第_____ 品最适合用于实验室制取CO2。 (2)试写出此反应的化学方程式:__________________
氢气的制取和性质

氢气的制取和性质
《氢气的制取和性质》教案
一、教学目标
1、知道氢气的实验室制备方法、收集方法和检查装置气密性的方法。
2、了解实验室制氢气的步骤、验证氢气的性质以及使用氢气的安全操作。
3、认识制氢气所需仪器的名称及知道这些仪器的连接和使用方法。
4、熟悉启普发生器的构造,熟练掌握其安装和安全操作。
5、知道实验室收集氢气的方法(排水法和向下排空气法)。
二、教学重点:
实验室制取氢气的方法、收集方法和检查气密性的方法。
三、教学难点:
制取氢气的仪器连接和组装,氢气的性质实验。
四、教学过程
氢气的制取和性质
一.氢气的实验室制法
反应原理:Zn+H2SO4=ZnSO4+H2↑
制备装置:启普发生器
收集方法:向下排空气法、向下排水法。
二.氢气的性质
物理性质:不溶于水,无色无味并,密度比空气小
化学性质:可燃性,还原性。
启普发生器——精选推荐

启普发生器别名气体发生器,启氏气体发生器,氢气发生器概述一种实验室常用的气体发生装置,是荷兰科学家启普(Petrus Jac obus Kipp 1808~1864)发明,并以他的姓命名。
它用普通玻璃制成,构造见图。
适用于块状固体与液体在常温下反应制取难溶的气体,如氢气,等。
块状固体在反应中很快溶解或变成粉末时,不能用启普发生器。
只要生成的气体难溶于反应液才可,如二氧化碳可溶于水,但难溶于盐酸,故用石灰石与盐酸反应制二氧化碳时可用启普发生器。
启普发生器不能加热。
使用前应先检查装置的气密性,方法是,开启旋塞,向长颈漏斗中加水,当水充满容器下部的半球体时关闭旋塞,继续加水,使水上升到长颈漏斗中。
静置片刻,若水面不下降,则说明装置气密性良好,反之则说明装置漏气。
漏气处可能是容器上气体出口处的橡皮塞、导气管上的旋塞或长颈漏斗与容器接触的磨口处。
如漏气应塞紧橡皮塞或在磨口处涂一薄层凡士林。
固体试剂由容器上的气体出口加入,加固体前应在容器的球体中加入一定量的玻璃棉或放入橡皮垫圈,以防固体掉入半球体中。
加固体的量不得超过球体容积的1/3。
液体试剂从长颈漏斗口注入,注液方法与上述注水方法相同。
液体的量以反应时刚刚浸没固体,液面不高过导气管的橡胶塞为宜。
使用时,打开导气管上的旋塞,长颈漏斗中的液体进入容器与固体反应,气体的流速可用旋塞调节。
停止使用时,关闭旋塞,容器中的气体压力增大,将液体压回长颈漏斗,使液体和固体脱离,反应停止。
为保证安全,可在球形漏斗口加安全漏斗(见图),防止气体压力过大时炸裂容器。
特点:符合随开随用随关随停的原则。
规格改进者启普(P.J.Kipp,1808—1864)是荷兰人,是一位稍通化学的药物商人。
19世纪初,他在前人工作基础上设计出这种实验室用的气体发生器,一直沿用到今天,基本上没有改型。
反应原理实验室里制取较多的氢气常用启普发生器。
它由球形漏斗、容器和导气管三部分组成。
最初使用时,将仪器横放,把锌粒由容器上插导气管的口中加入,然后放正仪器,再将装导气管的塞子塞好。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
球形 漏斗
活塞
导管 葫芦 形容器
打开活塞,容器内压强减小,液体从球 形漏斗流入仪器的中间部分与固体接触,放 出氢气;关闭活塞,容器压强增大,使液体 与固体脱离接触,停止制气。
使用方法(启普发生器制取氢气)
启普发生器:
适用范围:
固体 液体 气体
优点:
1、可制取大量的气体; 2、可控制反应随时发生、随时停止。
①在试管中加入少量碳酸钠 有大量气泡产 开始时有少量 慢,且很快 气泡产生, 再滴加少量稀硫酸 就停止反应 很快反应停止 ③在试管中加入少量石灰石, 有大量气泡产生 再滴加稀盐酸 适中
③ 组药 (1) 从以上实验的对比分析可以看出,第_____ 品最适合用于实验室制取CO2。 (2)试写出此反应的化学方程式:__________________
实验室制取氢气:
猜测:
实验室用金属锌和稀硫酸反应制取氢气, 采用排水法或向下排空气法收集,并用 点燃的方法来检验是否是氢气。
步骤:
反应原理 装置的选择 收集方法 检验方法
探究与活动二:如何选择制取CO2的实验装置?
回忆与思考:实验室有哪几种方法制取氧气?试填下表:
选用药 反应物 反应 品 状态 条件
氯酸钾 固体
反应的化学方程式
MnO2
发生 收集 装置 装置 a b
C或 e
C或 e
加热 2KClO3===== 2KCl+3O2
2 过氧化氢 固体+液体不需加热 2H OMnO 2 2===2H2O+O2↑ 二氧化锰
a
b
c
d
e
[知识迁移]:
实验室制取CO2是用石灰石与稀盐酸反应,反应物 固体、液体 ,反应时______ 不需要 的状态是_____________ (填“需 要”或“不需要”)加热,因此你认为制取CO2的 b 发生装置可以选择下图中的 _____。又因为CO2气 体可溶于水,且密度比空气大,因此收集方法应 c 选择下图的是_________ 。
a
b
c
d
e
f
g
常见的几种二氧化碳的制取装置
长颈漏斗为何要伸入液面下?
导管为何要伸入集气瓶底部?
1、怎样检验装置的气密性? 2、装药品(怎么往锥形瓶中 放大理石? )
澄清石灰水 变浑浊
2018/10/5
启普发生器:
荷兰化学家启普设计的气体发生器 装有固体的部位就是气体发生 的地方,气体在这里导出,液 体在这个部位可进可退。 工作原理:
CaCO3 2HCl CaCl2 CO2 H2O
讨论
制取二氧化碳药品的选择
1、Na2CO3+2HCl ====2NaCl + H2O + CO2 2、CaCO3+H2SO4====CaSO4+H2O + CO2
解释:
1、不用碳酸钠和碳酸钙粉末与酸反应来 制取二氧化碳是因为反应速度太快,来不及收 集,且成本较高。 2、不用大理石与硫酸反应来制取二氧化 碳是因为反应生成的硫酸钙微溶于水,覆盖在 大理石的表面,阻止反应的进行。
CO2的实验室制法
你所知道的能生成CO2的反应有 哪些?能用化学方程式表示的,请 写出化学方程式。
1、上述这些反应能否用于实验室制取CO2? 简要说明理由。 2、根据以上分析,你认为实验室制取气体时, 从原理上来说,主要考虑哪些因素?
①原料来源
③生成物是否较纯
②反应条件
④生成的气体是否方便收集
探究与活动一:如何选择制取二氧化碳的药品?
根据启普发生器的原理设计几种简易的制取气体装置
本节课,你学到了什么?
1)反应原理
2)反应装置 3)收集方法 二氧化碳实验 室制法 4)反应步骤 5)检验方法 6)检满方法
设计探究实验:
问题:在实验室如何制取氢气?
资料:
十六世纪末,瑞土化学家巴拉采尔斯把铁 放在硫酸中,铁片顿时和硫酸发生激烈的化学 反应,放出许多气泡——氢气。现在如果制取少 量的氢气,用的金属锌和稀硫酸反应。氢气是 无色无味且最轻的气体。 1780年,法国化学家 布拉克便把氢气灌入猪的膀胱中,制得了世界 上第一个、也是最原始的氢气球,它冉冉地飞 向高空。现在,人们就是往橡胶薄膜中灌入氢 气,大量制造氢气球。节日里放的彩色气球, 便灌着氢气。在气象台,人们差不多每天都要 放几个气球,探测高空的风云。氢在空气或氧 气中能燃烧,发出淡蓝色的火焰并生成水,因 此,它的希腊文原意,便是“水的生成者”。
a
b
c
d
e
小结:
确定实验室制取气体的发生装置应考虑的 反应物的状态 和___________ 反应条件 因素是___________ 。确定 气体的收集时应考虑的因素是气体的密度 __________ 气体的溶解性 。 和_____________
练习:
1 .硫化氢(H2S)是一种无色、有臭鸡蛋气味的气体, 其密度比空气的密度大,且能溶于水。实验室通常用块 状固体硫化亚铁(FeS)和稀硫酸混合,在常温下反应制 得硫化氢气体。如果你是实验员,你准备选下图中的 a 作发生装置,而收集方法选择图中的_________ d _____ 。
1、提出问题:
今有三组药品: ①碳酸钠(Na2CO3)与稀盐酸(HCl) ②石灰石(CaCO3 )与稀硫酸 (H2SO4) ③石灰石(CaCO3 )与稀盐酸(HCl) 要在实验室制取CO2气体,你认为哪一组最合适?
2、你的猜想:__________
3、设计实验方案、验证假设
实验方案 实验现象 反应速率
