2016年12月FDA批准新药概况
]获得FDA批准为突破性治疗的药物汇总
![]获得FDA批准为突破性治疗的药物汇总](https://img.taocdn.com/s3/m/5797c5dd33d4b14e8524682b.png)
突破性疗法资格(breakthrough therapy designation)是美国食品和药物管理局(FDA)于2012年7月创建,源于《美国食品和药物管理局安全及创新法案》(FDASIA)中制定的部分内容, 旨在加速开发及审查治疗严重的或威胁生命的疾病的新药。
作为继快速通道、加速批准、优先审评以后美国FDA的又一个新药评审通道,获得“突破性药物”认证的药物开发能得到包括FDA高层官员在内的更加密切的指导,保障在最短时间内为患者提供新的治疗选择。
截止2013年12月15日,美国FDA共收到132突破性药物资格申请,并授予36个药物“突破性疗法”资格,其中的27个被制药公司公开(见下表),癌症药物在突破性疗法药物占据大头,其它有疾病治疗领域有囊性纤维化及抗菌丙型肝炎, 遍及23个适应症。
其中罗氏旗下白血病药物Gazyva (Obinutuzumab, GA101), 强生淋巴瘤药物依鲁替尼(Ibrutinib, Imbruvica), 吉利德丙肝药物Sofosbuvir (Sovaldi)已获FDA批准上市。
另外亿腾医药(Eddingpharm)与Syndax Pharma达成协议,获得靶向治疗乳腺癌药物恩替诺特(entinostat)在中国地区的许可, 豪森药业(Hansoh Pharma)的PLK1抑制剂卡呋色替已进入I期临床。
另外恭喜深圳薇芯生物科技有限公司的西达本胺,其同靶点syndax的HDAC抑制剂Entinostat(MS-275)获得突破性治疗资格,算是一个me-better,薇芯生物在2008年1月2800万美元把中国外的专利许可卖给了美国沪亚生物。
目前已上市的两个HDAC抑制剂V orinostat(SAHA)和Romidepsin(FK228)的亚型选择性较差,属于第一代HDAC抑制剂。
MGCD0103、Entinostat(MS-275)、西达本胺等属于新一代的亚型选择性HDAC抑制剂,主要针对与肿瘤发生和发展密切相关的第I大类HDAC亚型(HDAC1、2、3)以及Ⅱb类的HDAC10。
FDA批准速效伟哥Stendra 等

FDA批准速效伟哥Stendra
美国生物医药公司Auxilium和Vivus近日宣布,勃起功能障碍(ED)药物 Stendra(avanfil)补充新药申请(sNDA)获FDA批准。该药是美国食品与药品管理局(FDA) 批准的唯一一种起效时间短至15分钟的ED药物,被誉为“速效伟哥”。特点是 立竿见影,服药15分钟后即可见效,可实现足够长时间的勃起,帮助完成性 生活。而辉瑞公司的万艾可(Viagra,伟哥)则需要在性行为前约一小时服 用。Stendra首次于2012年以多种剂量规格(50mg、100mg和200mg)获得 批准,属于一种5型磷酸二酯酶抑制剂,这类药物可用来帮助增加 流向阴茎的血流量。该公司表示,这款药物可以随食物或不随食 物使用,适度饮酒后使用亦可(3杯为上限,每杯约为含10g酒 精的饮料,通常是30ml 的烈酒或者100ml 的红酒)。
中药纯天然,就没有副作用吗?西药的用药方法以及禁忌都有哪些?请扫描二维码,登录《健康之家》微信,查询您想了解的中西药信息。
11 December
Copyright©博看网 . All Rights Reserved.
FDA批准化疗后的止吐新药Akynzeo
美国FDA批准Aky的恶心及呕吐。 Akynzeo是一种由两款药物组成的固定剂量胶囊复 方药物。口服帕洛诺司琼于2008年获得批准,这 款药物用于预防癌症化疗开始之后急性期(24小时 内)产生的恶心和呕吐。而奈妥吡坦(Netupitant)是 一种新药,用于预防癌症化疗开始后急性期与延 迟期(从化疗后25小时到120小时)产生的恶心和呕 吐。Akynzeo的有效性基于两项由1720名接受癌症 化疗受试者参与的临床试验。受试者被随机配给 Akynzeo或口服帕洛诺司琼。FDA药物评价与研究中 心办公室主任、医学博士Beitz表示,维持治疗产 品如Akynzeo,可帮助患者缓解癌症化疗副作用之 一的恶心及呕吐。在临床试验中,Akynzeo的常见 副作用有头痛、虚弱(无力)、疲劳、消化不良(食 滞)和便秘。
2016年9月份批准的新分子实体
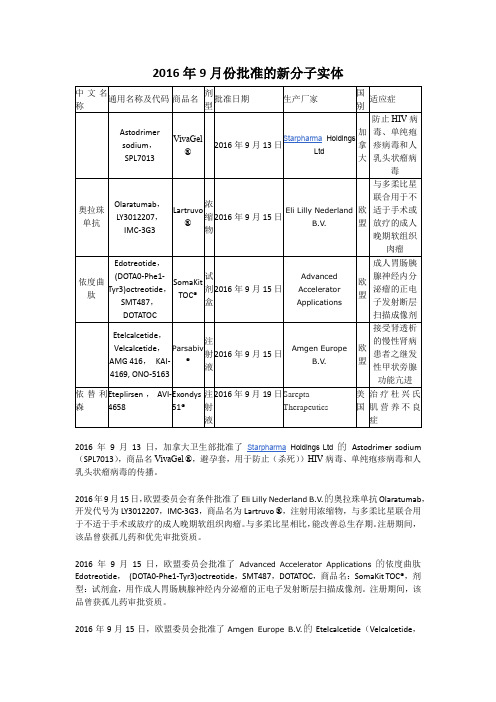
2016年9月份批准的新分子实体
2016年9月13日,加拿大卫生部批准了sodium (SPL7013),商品名VivaGel ®,避孕套,用于防止(杀死))HIV病毒、单纯疱疹病毒和人
乳头状瘤病毒的传播。
2016年9月15日,欧盟委员会有条件批准了Eli Lilly Nederland B.V.的奥拉珠单抗Olaratumab,开发代号为LY3012207,IMC-3G3,商品名为Lartruvo ®,注射用浓缩物,与多柔比星联合用于不适于手术或放疗的成人晚期软组织肉瘤。
与多柔比星相比,能改善总生存期。
注册期间,该品曾获孤儿药和优先审批资质。
2016年9月15日,欧盟委员会批准了Advanced Accelerator Applications的依度曲肽Edotreotide,(DOTA0-Phe1-Tyr3)octreotide,SMT487,DOTATOC,商品名:SomaKit TOC®,剂型:试剂盒,用作成人胃肠胰腺神经内分泌瘤的正电子发射断层扫描成像剂。
注册期间,该品曾获孤儿药审批资质。
2016年9月15日,欧盟委员会批准了Amgen Europe B.V.的Etelcalcetide(Velcalcetide,AMG 416,KAI-4169, ONO-5163),商品名:Parsabiv ®,剂型:注射液,用于接受肾透析的慢性肾病患者之继发性甲状旁腺功能亢进。
2016年9月19日,美国FDA批准了Sarepta Therapeutics的依替利森Eteplirsen(AVI-4658),商品名:Exondys 51®,注射液,用于治疗杜兴氏肌营养不良症。
,。
2016年美国FDA批准上市的药物

Briviact
(布立西坦)
brivaracetam
通过与突触囊泡蛋白2A(SV2A)结合而发挥抗癫痫作用
用于成年患者(16岁及以上)的部分发作癫痫的治疗
优时比(UCB)
2/18/2016
3
Anthim
obiltoxaximab
中和炭疽杆菌(anthrax)产生的毒素
用于吸入性炭疽的治疗及预防性治疗
用于检测一种罕见神经内分泌肿瘤
Advanced Accelerator Applications
6/1/2016
14
Epclusa
sofosbuvir and velpatasvir
复方制剂,活性成分包括靶向NS5B的sofosbuvir和靶向NS5A的velpatasvir
丙型肝炎
吉利德
6/28/2016
pimavanserin
一种血清素受体反相激动剂,靶向5-HT2A受体,降低其活性,从而减少中枢神经系统的兴奋程度
治疗出现幻觉/妄想等精神疾病的帕金森症
ACADIA Pharmaceuticals
4/29/2016
9
Tecentriq
atezolizumab
PD-L1抗体药物
膀胱癌
罗氏
5/18/2016
20
Eucrisa
crisaborole
非甾体PDE4抑制剂
2岁及以上儿童和成人患者轻度至中度特应性皮炎(湿疹,eczema)的治疗。
辉瑞(Pfizer)
12/14/2016
21
Rubraca
rucaparib
PARP抑制剂
用于治疗经过2种或更多化疗方法治疗的、BRCA基因缺失突变的恶性卵巢癌患者
2010年度FDA批准的21种新药

药物名称:Lumizyme(α-葡萄糖苷酶)
适应症:庞贝氏症(Pompe disease)
公司:健赞(Genzyme)
批准日期:2010年5月24日
药品类型:生物制品
简要说明:它是一种溶酶体内特异性糖原水解酶。该药品适用于治疗年龄≥8岁、无心脏肥大征象的晚发型(非婴儿期发病)Pompe病患者。所有的Pompe病患者通常会发生进行性肌无力及呼吸困难,但病情进展速度因发病年龄和脏器受累程度而有较大差异。症状出现于出生后数月内时,婴儿常表现出心脏显著增大并于1岁内死亡。当症状出现在儿童期、青少年期或成人期时,患者可能会发生持续进行性无力并因呼吸衰竭而过早死亡。
药物名称:Asclera (polidocanol)
适应症:小血管静脉曲张
公司:Chemische Fabrik Kresussler
批准日期:2010年3月30日
药品类型:小分子药物
简要说明:Asclera被批准用于治疗蜘蛛状血管病(管径小于1mm的微型静脉曲张)和网状静脉的(直径为1至3mm)的治疗。Asclera通过破坏血管内皮细胞而起作用。Asclera常见的不良反应包括注射部位受损血管渗血、水肿、瘀伤、变色和疼痛。
药物名称:EllaOne
适应症:紧急避孕
公司:HRA Pharma, Watson
批准日期:2010年8月13日
药品类型:小分子药物
简要说明:该药物可在无防护措施或避孕失败120小时(5天)内使用。EllaOne是处方药,只能用于紧急避孕不可作为常规避孕手段。
药物名称:芬戈莫德(Gilenya)
药物名称:Xiaflex (collagenase clostridium histolyticum)
FDA批准的放射性药物都有哪些?

FDA批准的放射性药物都有哪些?展开全文中华医学会核医学分会放射性药物学组整理1、药物名称:Carbon-11 choline(11C-胆碱)生产商:Mayo Clinic 商品名:—用途:前列腺癌复发诊断2、药物名称:Carbon-14 urea(14C-尿素)生产商:Kimberly-Clark 商品名:PYtest用途:胃中幽门螺杆菌感染诊断3、药物名称:Fluorine-18 florbetaben(18F-AV1)生产商:Piramal Imaging 商品名:Neuraceq™用途:阿尔茨海默(AD)患者和痴呆患者评价4、药物名称:Fluorine-18florbetapir(18F-AV45)生产商:Eli Lilly 商品名:Amyvid™用途:阿尔茨海默症诊断与治疗5、药物名称:Fluorine-18sodium fluoride(18F-氟化钠)生产商:Various 商品名:—用途:成骨能力的骨显像剂6、药物名称:Fluorine-18fludeoxyglucose(18F-FDG)生产商:Various 商品名:—用途:肿瘤、癫痫病灶糖代谢异常检测7、药物名称:Fluorine-18flutemetamol(18F-PIB)生产商:GE Healthcare 商品名:Vizamyl用途:阿尔茨海默(AD)患者和痴呆患者评价8、药物名称:Gallium-67 citrate(67Ga-柠檬酸)生产商:Lantheus MedicalImaging、Mallinckrodt商品名:—用途:霍奇金病、淋巴瘤、支气管癌以及一些急性炎症病变诊断9、药物名称:Indium-111capromab pendetide(111In-卡罗单抗喷地肽)生产商:AytuPharmaceuticals 商品名:ProstaScint®用途:前列腺癌患者、前列腺癌术后高度怀疑转移患者的检测10、药物名称:Indium-111 chloride(111In-氯化铟)生产商:GE Healthcare、Mallinckrodt 商品名:Indiclor™用途:用于放射性标记11、药物名称:Indium-111 pentetate(111In-DTPA)生产商:GE Healthcare 商品名:—用途:放射性核素脑池造影12、药物名称:Indium-111oxyquinoline(111In-羟基喹啉)生产商:GE Healthcare 商品名:—用途:用于自体白细胞标记,炎症及感染的诊断13、药物名称:Indium-111pentetreotide(111In-奥曲肽)生产商:Mallinckrodt 商品名:Octreoscan™用途:原发性和转移性内神经分泌肿瘤生长抑素受体定位14、药物名称:Iodine I-123iobenguane(123I-MIBG)生产商:GE Healthcare 商品名:AdreView™用途:原发或转移性嗜铬细胞瘤或神经母细胞瘤的辅助诊断15、药物名称:Iodine I-123 ioflupane(123I-氟潘)生产商:GE Healthcare 商品名:DaTscan™用途:对疑似帕金森症患者的评估16、药物名称:Iodine I-123sodium iodide capsules(123I-碘化钠胶囊)生产商:Cardinal Health、Mallinckrodt 商品名:—用途:甲状腺功能及形态学评价17、药物名称:Iodine I-125 humanserum albumin(125I-人血清白蛋白)生产商:IsoTex Diagnostics 商品名:Jeanatope用途:全血及血浆容量测定18、药物名称:Iodine I-125iothalamate(125I-酞酸盐)生产商:IsoT ex Diagnostics商品名:Glofil-125用途:肾小球滤过率的评价19、药物名称:Iodine I-131 humanserum albumin(131I-人血清白蛋白)生产商:IsoTex Diagnostics 商品名:Megatope用途:全血及血浆量、心脏输出、心脏及肺血容量、蛋白质周转研究、脑肿瘤定位等20、药物名称:Iodine I-131sodium iodide(131I-碘化钠)生产商:DRAXIMAGE、Mallinckrodt 商品名:HICON™用途:甲状腺疾病的诊断与治疗21、药物名称:MolybdenumMo-99 generator(钼锝发生器)生产商:GE Healthcare、Lantheus MedicalImaging、Mallinckrodt商品名:DRYTEC™、T echnelite、UltraTechneKow®DTE用途:放射性药物的制备22、药物名称:Nitrogen-13 ammonia(13N-氨水)生产商:Various 商品名:—用途:心肌灌注评价冠状动脉疾病23、药物名称:Radium-223 dichloride(223Ra-二氯化镭)生产商:Bayer HealthCarePharmaceuticalsInc. 商品名:Xofigo®用途:去势性前列腺癌治疗24、药物名称:Rubidium-82 chloride(82Ru-氯化铷)生产商:Bracco Diagnostics 商品名:Cardiogen-82®用途:心肌灌注显像剂25、药物名称:Samarium-153lexidronam(153Sm-EDTMP)生产商:Lantheus MedicalImaging 商品名:Quadramet®用途:减轻骨转移患者的疼痛26、药物名称:Strontium-89 chloride(89Sr-氯化锶)生产商:GE Healthcare商品名:MetastronTM用途:减轻骨转移患者的疼痛27、药物名称:T echnetium-99mbicisate(99mT c-ECD)生产商:Lantheus MedicalImaging 商品名:Neurolite®用途:脑卒中患者卒中的诊断与治疗28、药物名称:Technetium-99mdisofenin(99mTc-地索芬宁)生产商:Pharmalucence 商品名:Hepatolite®用途:急性胆囊炎诊断29、药物名称:Technetium-99mexametazine(99mTc-HMPAO)生产商:GE Healthcare 商品名:C eretec™用途:脑卒中患者血脑灌注、白细胞标记显像用用于腹腔感染及肠道炎症定位30、药物名称:T echnetium-99mmacroaggregatedalbumin (99mT c-MAA)生产商:DRAXIMAGE 商品名:—用途:肺灌注评价、腹静脉分流畅通性评价31、药物名称:Technetium-99mmebrofenin(99mT c-甲溴苯宁)生产商:Bracco Diagnostics、Pharmalucence 商品名:Choletec®用途:肝胆显像剂32、药物名称:Technetium-99mmedronate(99mTc-MDP)生产商:DRAXIMAGE、GE Healthcare、Pharmalucence 商品名:MDP-25、MDP Multidose用途:骨显像剂33、药物名称:Technetium-99mmertiatide(99mTc-MAG3)生产商:Mallinckrodt 商品名:TechnescanMAG3TM用途:肾动态显像34、药物名称:Technetium-99moxidronate(99mT c-HDP)生产商:Mallinckrodt 商品名:Tec hnescan™HDP用途:骨显像剂35、药物名称:Technetium-99mpentetate(99mT c-DTPA)生产商:DRAXIMAGE 商品名:—用途:脑显像、肾显像36、药物名称:T echnetium-99mpyrophosphate(99mTc-PYP)生产商:Mallinckrodt、Pharmalucence 商品名:Technescan™、PYP™用途:骨显像、心脏显像剂、血池显像剂37、药物名称:Technetium-99m redblood cells(99mT c-红细胞)生产商:Mallinckrodt 商品名:UltraTag™用途:血池造影、消化道出血定位38、药物名称:T echnetium-99msestamibi(99mTc-MIBI)生产商:Cardinal Health、DRAXIMAGE、Lantheus MedicalImaging、Mallinckrodt、Pharmalucence商品名:Cardiolite®用途:心肌灌注,用于检测缺血、评价心机功能,乳腺成像39、药物名称:Technetium-99msodium pertechnetate (99mT c-高锝酸钠)生产商:GE Healthcare、Lantheus MedicalImaging、Mallinckrodt商品名:—用途:脑显像、甲状腺显像、胎盘定位、膀胱显像等40、药物名称:Technetium-99msuccimer(99mT c-DMSA)生产商:GE Healthcare 商品名:—用途:肾显像41、药物名称:Technetium-99msulfur colloid(99mT c-硫胶体)生产商:Pharmalucence 商品名:—用途:肝、脾、骨髓显像等42、药物名称:Technetium-99mtetrofosmin(99mTc-替曲膦)生产商:GE Healthcare 商品名:MyoviewTM用途:心肌灌注剂43、药物名称:Technetium-99mtilmanocept(99mTc-替马诺噻)生产商:NavideaBiopharmaceuticals,Inc. 商品名:Lymphoseek®用途:淋巴结定位44、药物名称:Thallium-201chloride(201Tl-氯化铊)生产商:GE Healthcare、Lantheus MedicalImaging、Mallinckrodt商品名:—用途:心肌灌注显像45、药物名称:Xenon-133 gas(133Xe气体)生产商:Lantheus MedicalImaging 商品名:—用途:肺功能评估与肺显像、脑血流评估46、药物名称:Yttrium-90chloride(90Y-氯化钇)生产商:MDS Nordion、Eckert&ZieglerNuclitec商品名:—用途:放射性标记47、药物名称:Yttrium-90ibritumomab tiuxetan(90Y-替伊莫单抗)生产商:SpectrumPharmaceuticals商品名:Zevalin®用途:非霍奇金氏淋巴瘤治疗截止至2015年8月1日。
2019年9—10月FDA批准新药概况

2019年9—10月FDA批准新药概况自2019年9月1日至10月31日期间,美国食品药品监督管理局(FDA)批准了多种新药的上市,其中包括25种新的分子实体药(NME)和10种新的生物类似物(BLA)。
以下是部分新批准的药品和其适应症:1. Baxdela(delafloxacin mesylate):用于治疗轻至中度复杂性皮肤和皮下组织感染,包括压疮、足部感染和慢性感染等。
2. Balversa(erdafitinib):用于治疗接受过化疗并具有FGFR2或FGFR3变异体的晚期膀胱癌患者。
3. Bryhali(halobetasol propionate):用于治疗轻至中度程度的牛皮癣。
4. Caplyta(lumateperone):用于治疗精神分裂症成年患者。
5. Cenobamate(cenobamate):用于治疗难治性部分性癫痫。
6. Enhertu(fam-trastuzumab deruxtecan-nxki):用于治疗HER2阳性的晚期乳腺癌。
7. Esperoct(turoctocog alfa pegol):用于治疗血友病A。
8. Givlaari(givosiran):用于治疗引起急性间歇性卟啉症发作的成人患者。
9. Nubeqa(darolutamide):用于治疗非转移性前列腺癌。
11. Rozlytrek(entrectinib):用于治疗具有NTRK基因融合的实体肿瘤和ROS1阳性非小细胞肺癌。
12. Rybelsus(semaglutide):用于治疗II型糖尿病。
13. Turalio(pexidartinib):用于治疗成人患有滑膜肉瘤的患者。
14. Xpovio(selinexor):用于治疗多发性骨髓瘤。
这些新药的批准推动了医生和患者的疾病治疗方法的更新,也为药品制造商提供了新的市场机会。
但同时也需要注意,这些新药的临床效果和安全性需要在实际使用中进一步观察和验证。
2013年12月FDA批准新药概况

HC V 1 型 、4型感染 ,索非布 韦 +聚乙二醇 干扰素 +利
巴 韦林 治疗 的 S V R1 2 率为9 0 %,其 中 l a 、l b 、4亚 型
的S VR1 2率分 别 为 9 2 %、8 2 %、9 6 %。P H O T O N. 1 试 验
分 别为 9 5 %、7 8 %; 对于 H C V 3型 感 染 ,两5 6 %、6 3 %。P OS I T R O N试验 显示干 扰素耐 药 的 患 者 ,对 于 H C V 2型 、H C V 3型 感 染 ,索 非 布 韦 + 利 巴 韦林 组 S V R1 2率 分别 为 9 3 %、6 1 %,安慰 剂 组 为 0 %。F US I O N试 验 显 示 既 往接 受 治 疗 的 患者 ,索 非 布 韦 +利 巴韦林 1 6周治疗 组较索非布 韦 +利 巴韦林 1 2周 治 疗 组有 明显 提升 ,对 于 H C V2型感 染 的 S V R 1 2率 分 别为8 9 %、8 2 %; 对 于 HC V 3型感 染 的 S VR 1 2 率 分 别 为6 2 %、3 0 %。NE U T R 1 N O试验显示 既往未接受 治疗的
气量 ( F E V1 )为 主要 临床 终 点 ,相 比于芜 地 溴 铵 、维 兰特罗 、安慰剂 ,An o r o E l l i p t a 在F E V1 上分 别提升 1 6 7
苷酸类 似物 NS 5 B聚合 酶抑制 剂 ,能阻 断丙型肝 炎病毒 复制所需 的一种特 异性 蛋 白质 ,作 为组合抗病毒 治疗方 案 的一个 组分适用 为慢性丙 型肝 炎感染 的治疗。S o v a l d i 是接受 F D A批准的第 3 个 突破性治疗指定药物 ,也是在
美国和中国已批准的生物技术药物和分类

美国和中国已批准的生物技术药物和分类2015级研究生张锐15222105500151984 ~ 2014 年美国FDA审批上市的治疗性生物药物全球生物药物在1996年以后开始快速发展, 2001~2005年是生物药物成果最为显著的阶段。
肿瘤、免疫系统疾病、内分泌和代谢疾病、血液系统疾病、骨骼肌系统疾病是生物药物研究的重点领域,上市药物较多。
1984~2014年美国FDA共审批125个治疗性生物药物,其中首创性新药67个,占全部药物的53.60%;优于已有类似药物26个,占全部药物的20.80%;模仿跟进药物32个,占全部药物的25.60%。
1984~2014年美国FDA 审批的125个治疗性生物药物中,抗体药物为48个(38.40%),酶类药物19个(15.20%),干扰素12个(9.60%),融合蛋白类药物8个(6.40%),集落/造血刺激因子类药物8个(6. 40%),激素类药物8个(6.40%),生长因子类药物5个(4.00%)、肽类药物5个(4.00%)、溶栓类药物5个(4.00%)、毒素类药物5个(4.00%)、白细胞介素类药物2个(1.60%)。
1、抗肿瘤药首创性生物药物(Tab2)2、免疫疾病首创性生物药物(Tab3)3、胃肠道和新陈代谢及激素类首创性生物药物(Tab4)4、血液系统疾病首创性生物药物(Tab5)5、骨骼肌疾病首创性生物药物(Tab6)6、抗感染首创性生物药物(Tab7)7、泌尿和神经系统疾病首创性生物药物(Tab8)8、其他疾病首创性生物药物(Tab9)中国抗体药物产业现状截至2015 年6 月,共批准22 个抗体类药物上市,其中国内自主研发抗体药物10 种( 表1) ,进口抗体类药物12 种( 表2)。
美国FDA批准新药:仅比2008年多1个

产 品 ,2 0年 ,诺 华 与拜 耳达 成 了 一 07
项 合作 议 ,诺 华可 以推 i具有 自身 品 j I 牌 的 同类J 。所 以,本 文 作者 并 未把 品
■ 图l1 9 ~ 0 9 D 批准的新分子实体药物和生物制品的数目 9 6 2 0年F A
2 0 年批 准 C n y e 第 二 用 于遗 传 08 irz后 个 性 血 管 水肿 的产 品 。C n y e 一 种通 irz为
然 来 自专 业 的 制 药 公 司 ,卡 比 之 下 制 雕
B o h r p u iS 司 开 发 的重 组 人 抗 i t ea e t C 公
( a a l p i ) ,他 预 测 本 品将 会 同 S x g i tn F A 准 的 第 一 P 一 抑 制 剂 J n va D批 个D P 4 a u i ( i a l P i ) 样 达 到 数 十 亿 美 S t g i tn 元 的销 售 业 绩 。此 外 , 他 还看 好 由
肽 基 肽 酶 一 ( P ~ )抑 制 剂 O g z 4 D P4 nl a y
在 2 0 年 批 准 了2 个 新 药 , 译 者 将 其 09 6 进 行 了 对 比 , 发 现 国 内 作 者 将 诺 华
公 司 用 F多 发 性 硬 化 症 的 B 干 扰 素
批 准 , 而 是 F A 物 制 品 评 价 和 研 究 D生 中心 ( B R 批 准 市 的 , 是 由G C CE ) T
D a C r o a in y x o p r t o 公司 开 发 的用 于遗 传 性 管 水 肿 的血 浆 激 肽 释 放 酶 抑 制
剂K l i o ( c l a t d ),这 是继 a b t r e a ln ie
2013年5—7月FDA批准新药概况

2 0 1 3 年5 — 7 月F D A批准新 药概 况
2 0 1 3年 5月 ,F D A批 出 4个 新 分 子实 体 药 品 ( 表 1 ) ,分 别是治疗 慢性阻塞性 肺病药 品 B r e o E l l i p t a( 糠酸 氟替 卡 松 +三氟 甲磺 酸维 兰特 罗 ) 、治疗 前列 腺癌 药 品
5 结 语
综 上所 述 ,用 药 差 错 的 危 害性 不 言 而 喻 ,但 其在
参考文献
[ 1 ] Go u g h A W, Ba r s o u m NJ , Di F o n z o C J , e t a 1 . Co mp a r i s o n
o f t h e n e o n a t a l t o x i c i t y o f t wo a n t i v i r a l a g e n t s : v i d a r a b i n e
( 收 稿 日期 : 2 0 1 3 . 0 4 . 2 7)
上海 医药
2 0 1 3 年 第3 4 卷 第1 7 期 ( 9 月上 )
5 9
・
药 讯 荟 萃
・
该信号通路 活性增强 ,所 以 ME K s( MA P K / E R K 细胞外
信号调节激 酶 )就是 抗癌药 开发的热 门靶 点 。黑色 素瘤 是皮 肤病领先 的致 死原 因 ,约半数黑 色素瘤产 生在皮肤
实 际 操作 中是 可 以 预 防 的。 同样 ,在 英 文 中用 药 差错
( me d i c a t i o n e r r o r , ME) 明确定义为指在药物治疗过程 中 , 医疗专 业人员 、患者不 适 当地使 用药物 或 因而造 成患者
2019年9—10月FDA批准新药概况

2019年9—10月FDA批准新药概况2019年9—10月,美国食品和药物管理局(FDA)批准了多个新的药物上市,这些新药的批准意味着更多的治疗选择和希望将带给患者。
下面是2019年9—10月FDA批准新药的概况。
1. Erdafitinib(红带非替尼)Erdafitinib是首个用于治疗特定类型的晚期尿路上皮癌(UC)的口服靶向治疗药物。
它适用于接受了化疗并且在FGFR阴性的患者中,癌症仍然进展的情况。
该药物的批准是基于临床试验数据,数据显示患者的整体反应率为40%,平均持续时间为5.4个月。
2. Trikafta(伊瓦卡夫托)Trikafta是一种用于治疗囊性纤维化(CF)的三联疗法。
它适用于年龄为12岁及以上,拥有两个F508del突变的CF患者。
Trikafta的批准是基于两个关键临床试验的数据,这些数据显示该药物在患者中显著改善肺功能。
3. Reblozyl(利保替哌普)Reblozyl是一种用于治疗成年患者的贫血型β-地中海贫血或依赖性β地中海贫血(TDT)的药物。
这是一种注射给药,适用于患者在不再依赖于红细胞输血的情况下,提高了血红蛋白水平。
该药物的批准是基于一项关键临床试验,数据显示患者血红蛋白水平得到长期维持。
4. Pretomanid Tablets(前曼尼片剂)Pretomanid Tablets是一种用于与质子泵抑制剂和多药联合治疗(PMDT)一起治疗多耐药结核病和极耐药结核病的药物。
该药物是唯一获得批准的,用于这种疾病的三联疗法之一,批准是基于临床试验数据,数据显示PMDT的治疗成功率接近90%。
5. Wakix(瓦克希片)Wakix是一种用于治疗成人的强迫性睡眠癖(OSA)的药物。
这是一种新的口服非优势性选择性肌动蛋白2/4(HAR2/4)受体拮抗剂,用于调节清醒和睡眠状态。
该药物的批准是基于两个临床试验的数据,数据显示Wakix显著缩短了OSA患者的睡眠时间。
6. Vyndaqel and Vyndamax (tafamidis)(俾迪拉、维达马)Vyndaqel and Vyndamax是一种用于治疗心脏淀粉样形态决性心脏病(ATTR-CM)的药物。
2020年12月FDA批准新药概况

Gemtesa 为口服片剂,被批准用于治疗伴有急迫性 尿失禁、尿急和尿频症状的膀胱过度活动症成年患者。 Gemtesa 是一款 β3 肾上腺素能受体激动剂,它能够选择 性地激活 β3 肾上腺素能受体,这是膀胱平滑肌中最常见 的 β 肾上腺素能受体,从而舒张平滑肌,提高膀胱容量, 进而减轻膀胱过度活动症的症状。
被批准用于成人和儿童患者治疗由扎伊尔型埃博拉病毒 (Zaire ebolavirus)引起的感染,包括扎伊尔埃博拉病毒 RT-PCR 检测呈阳性的母亲所生的新生儿。Ebanga 是一
种从 1995 年刚果民主共和国埃博拉疫情的幸存者身上分 离的单克隆抗体,通过阻断病毒与细胞受体的结合,阻 止其进入细胞。
7 Ebanga(ansuvimab-zykl)
结合并抑制其蛋白水解活性。
Ebanga 为冻干粉,获“孤儿药”和“突破性药物”资格,
3 Klisyri(tirbanibulin)
Klisyri 局部外用被批准用于面部或头皮的光化性 角 化 病(actinic keratosis, AK) 的 局 部 治 疗,AK 是 一 种 由 于 皮 肤 暴 露 在 紫 外 线 下 导 致 的 皮 肤 癌 前 病 变。 Klisyri 是一种微管抑制剂,通过抑制微管的聚合,可以 促进增生细胞发生细胞凋亡,适用于面部或头皮 AK 的 局部治疗。
2020年12月FDA批准新药概况
2020 年 12 月,FDA 批 出 5 个 新 分 子 实 体 和 2 个 4 Orgovyx(relugolix)
新 生 物 制 品, 分 别 为 前 列 腺 癌 PET 显 像 药 物 镓 68 PSMA-11(68Ga PSMA-11)、治疗遗传性血管水肿药品 Orladeyo(berotralstat)、治疗光化性角化病药品 Klisyri (tirbanibulin)、治疗前列腺癌药品 Orgovyx(relugolix)、 治疗膀胱过度活动症药品 Gemtesa(vibegron)、治疗乳 腺癌药物 Margenza(margetuximab-cmkb)和治疗埃博拉
美国《植物药指南》和植物药发展简介

美国《植物药指南》和植物药发展简介窦金辉【摘要】The definition of new drugs in China and the US has no major differences on chemical drugs and biologics.However,Chinese medicines,which are regulated as over-the-counter (OTC) or prescription drugs in China,are mostly regulated as food and/or dietary supplements without FDA approved medicinal use for marketing.The FDA Guidance for Industry-Botanical Drug Products (2004) and the recently revised Guidance for Botanical Drug Development (2016) paved the way for Chinese herbal medicine and other botanical mixtures to be further developed as new drugs through clinical trials and other nonclinical studies.FDA recognizes the value of traditional medicines as part of the previous human experiences to support the safety and speed up early phase clinical trials of botanical products under investigational new drug (INDs) applications.The revised Guidance included addition recommendations for late phase development,like phase 2 trials and new drug applications (NDA),to resolve some of the unique challenges on batch-tobatch consistency (e.g.,a totality of evidence approach,including raw materialcontrol,bioassays,multiple-batch and multiple-dose clinical trials,and etc.).The approval of Veregen and Fulyzaq (now Mytesi) are new molecular entity / new chemical entity type of new drugs,treasured fruits from several hundred INDs studying botanicals.With those NDA examples,it is expected that further study of Chinese herbal medicines as new botanical drugsthrough further clinical and nonclinical development will be fruitful.On the other hand,long-term commitments are universal for new drug development.And it will also be true for bringing Chinese herbal medicines as botanical new drugs to international markets.It still takes time to see whether artesunate tablets can be verified through further clinical trials and achieve the same level of Coartem.%药物的定义在中美之间有很大差别.众多中药产品用来治病救人在中国早已习以为常,但美国则把中药当食品或膳食补充剂来监管,且在销售时不能标明有任何药用作用.美国食品药品监督管理局FDA的《植物药指南》为中药和其他草药未经纯化就能进入临床试验成为处方新药铺平了道路.《植物药指南》中允许推迟减免一些毒理实验以及让相对安全的中药直接进入二期临床试验.通过原药材种植采收及加工工艺来保证药品批次间的一致性也是《指南》的基本精神之一.2016年,修改版的《指南》还增加了用生物活性检测及多批次多剂量的临床试验来验证或保证质量控制的合理性等内容.借用中药的使用经验来研究中药或其有效组分之间的协同或加作用,有望成为中药以植物处方药走向世界的突破口.同时,数百获批进行临床试验的植物药品种只有Veregen和Fylyzaq (Mytesi)两个植物药上市,也说明把中药开发成为与新分子实体(New Molecule Entity)和新化学实体(New Chemical Entity)一样在多国上市的植物新药面临挑战.可以说,中药产品成为植物新药会是持久战,不宜急功近利.青蒿片剂能否经得起进一步的临床验证而与复方蒿甲醚”(Coartem)媲美,还需拭目以待.【期刊名称】《世界科学技术-中医药现代化》【年(卷),期】2017(019)006【总页数】5页(P936-940)【关键词】中药;植物药;美国FDA;《植物药指南》;临床试验申请;新药上市申请;批次间一致性;协同作用【作者】窦金辉【作者单位】密西西比大学牛津38677【正文语种】中文【中图分类】R281.2人类应用植物药有着悠久的历史,植物中含有能治病的物质(Plants that Heal)。
2012年美国食品药品管理局(FDA)批准新药回顾

2012年美国食品药品管理局(FDA)批准新药回顾2012年,美国食品药品管理局(FDA)共批准了39种新药,这一数字成为该机构自1996年以来批准新药数量的第二高——1996年FDA共批准53种新药,为历史之最,包括阿托伐他汀(立普妥)这样的“重磅炸弹”级药物。
对于制药行业和患者来说,这足以令人感到意外和惊喜,因为在2011年和2010年,FDA分别只批准了30和21种新药,2002~2011年年平均批准数为23种。
对于2012年有39种新药获批,有人认为系原研药企业正蓄势待发,以应对近年来由于专利到期、仿制药竞争带来的销售损失。
分析师预计,2012年批准的药物中有一些将获得数十亿美元的销售额,不过,FDA发言人、药学博士Li sa Kubaska表示:“FDA在2012年批准的新分子实体不断增加令人鼓舞,但现在就说FDA批准新药增加进入到一个长期的趋势还为时过早。
”1 1月17日,BTG制药公司的Voraxaze(Glucarpidase,羧肽酶)注射剂获得批准,用于治疗因肾功能衰竭而导致的甲氨蝶呤中毒(血液中甲氨蝶呤水平过高)。
Voraxaze是一种酶,可将甲氨蝶呤分解成可排出体外的成分,从而迅速降低其血液水平。
2 1月23日,LEO Pharma AS公司的外用凝胶PICATO(Ingenol mebutate,巨大戟醇甲基丁烯酸酯)获得批准,用于治疗光化性角化病。
光化性角化病是一种由累积日光暴露导致的癌前病变,可能进展为鳞状细胞癌。
该药是从澳大利亚植物Euphorbia peplus的汁液中提取的活性成分,母核为巨大戟醇,可诱导细胞凋亡,但其治疗的具体作用机制尚不明确。
3 1月27日,辉瑞公司的Inlyta(Axitinib,阿西替尼)获得批准,用于治疗其他药物治疗无效的晚期肾癌(肾细胞癌)。
Inlyta是一种小分子酪氨酸激酶抑制剂,对多个靶点有效,包括VEGF受体1、2和3。
4 1月30日,基因泰克公司的Erivedge(Vismodegib,维莫德吉)获得批准,用于治疗成人最常见的皮肤癌——基底细胞癌。
FDA批准戒烟新药伐仑克林

盐, 实现 了清洁生产 , 废水、 废气 , 度渣
经治理 达标排放 , 降低成 本达 l% 特别 . 5
或 ” 三无 药品 , 坚决反 对 和制止 同产
林 帮助戒烟的疗效优于安慰剂 ( 3 高
倍) ,其 中两项研 究 尚表 明伐仑 克林 治
疗 者 的 戒 烟 成 功 率 大 干 安 非 他 酮 (u rp o /y a )( I倍) B p o n Z b n 高 i . 伐 仑克林 耐受性 良好 , 其总 治疗 中 止率类似 于安慰荆 .最常见的副反应 则
是以水为溶媒, 活性炭、 盐酸等原料消
耗 大大减 少, V I 料成 本每 公 斤降 使 B原
低 了近 1 元 . 0
品中的恶意降价竞争, 自觉依 法维护医
药市 场秩 序 ;五是 不制作 虚 假 宣传 资
料 ,不套用 涉及版权 的他 人的 图 片、 文
为降低生产成本,提高产品产量, 将竞争对手拒之于国门 之外.公 司在每 年投入大量资金进行扩 能技术改造, 逐
维普资讯
医 1 化 工 l 5
醇 ,B V I中不残 留 甲醇 ,不舍 游 离硝 酸 的认证 , 不使用不具备 认证 资质机 构 颁 发 的证 书; 四是 不得销 售任何 过 期药 品 项l 床试验 的证实.6项试验 中有 5项 I 盘
属 随机 , 照研 究 , 对 它们 均显 示伐 仑 克
年提 高 VI B 产量 的基础 上 ,集 中 力量 , 在提 高收率上做文章 .公 司 自主研发 出
拥 有 自主知 识产权 、 术 水平 国 内领 先 技 的 V I 成 Y 一氯代 乙酰 丙醇新 工艺, B合 将 Y 一氯代 乙酰 丙醇 的收率 由 5 S 8 提
FDA批准治疗前列腺癌新药Degarelix注射剂

肺 炎 球 菌 稀 少 的 区域 ,应 用 第 二 代 头 孢 菌 素 经验 治
疗 社 区获 得 性 肺 炎 是 可 行 的 。C e t ea y 2 0 , h moh rp , 0 9
5 ()9 —0 ( 文) 52 : 7 1 4英
厄他培南与头孢 曲松在治疗复杂尿路感染 ,社 区获 得性肺炎 皮肤和软组织感染儿童的双盲试验 中安
全及 耐 受 性 比较
厄 他 培 南 已 被 证 明是 安 全 、 耐 受 性 好 可 有 效 治疗 成 人 复杂 尿路 感 染 、皮 肤 和 软 组 织 感 染 以 及 社
作用可达到并维持与手术切除睾丸后相同水平 。 在 该 项 临床研 究 中 ,总 共 6 0 患者 被 随机 分 为 2例 3 ,即 皮 下注 射2 0 e ae x 组 4 mgdgrl 负荷 剂 量 ,随后 每 i 月一 次 1 0 维 持 剂量 ;皮 下 注 射 2 0 e aei mg 6 4 mgd g rl x
度 。而 d g rl  ̄ 不会 在 治疗 初始 阶 段产 生 这 种 刺 e aei 0 x
结 论 : 中 度 耐 药 性 肺 炎 球 菌 引起 的 肺 炎 球 菌
性 肺 炎 患 者 可 使 用 头 孢 呋 辛 经 验 治 疗 。在 完全 耐 药
激 作 用 。在 一 项 历 时 1 个 月 的 多 中心 、标 签 公 开 、 2 随 机 性 对 比临 床 研 究 中 ,d g rl 对 睾 酮水 平 抑 制 e aei x
敏 感肺 炎链 球 菌 引起 类似 感 染 的 患者 为 对 照 。所 有
・
药监信 息 ・
美 国F DA于2 0 — .9 准 F ri g 1 公司 研 0 81 2 批 2 ern ¥J 药
新长效β2—受体激动剂三氟甲磺酸维兰特罗

新长效β2—受体激动剂三氟甲磺酸维兰特罗摘要三氟甲磺酸维兰特罗是一个经口吸入的长效选择性β2-受体激动剂,可持续作用24 h。
与沙美特罗相比,三氟甲磺酸维兰特罗起效更快、持续作用时间更长,在哮喘和慢性阻塞性肺病患者中的安全性和耐受性良好,一日1次的给药方案还可以改善患者的依从性,为哮喘和慢性阻塞性肺病患者提供了新的治疗选择。
关键词三氟甲磺酸维兰特罗慢性阻塞性肺病β2-受体激动剂“慢性阻塞性肺病(chronic obstructive pulmonary disease,COPD)全球创议”推荐,II~IV级COPD患者可使用长效β2-受体激动剂(long-acting beta2-agonist,LABA)治疗[1]。
“哮喘全球创议”也推荐,对低剂量吸入糖皮质激素(inhaled glucocorticosteroid,ICS)治疗疗效差的哮喘患者可联用ICS和LABA[2]。
由于吸入频次高及装置复杂,治疗依从性成为COPD和哮喘患者共同存在的医疗难题。
能快速起效且支气管扩张作用可持续24 h的新一代LABA因可给患者带来便捷,故有望提高治疗的依从性[3]。
三氟甲磺酸维兰特罗是一个新型经口吸入的选择性LABA,与ICS联用可以一日1次给药治疗COPD和哮喘患者[4-5]。
Theravance公司和葛兰素史克公司合作研发的糠酸氟替卡松-三氟甲磺酸维兰特罗复方干粉吸入剂(fluticasone furoate-vilanterol trifenatate/Relovair)也已完成Ⅱ期临床研究,并已开始进行Ⅲ期临床试验。
本文对三氟甲磺酸维兰特罗(以下简称为维兰特罗)作一介绍。
1 药理学特性维兰特罗是一个新型经口吸入的选择性LABA,具有支气管扩张作用。
有关实验证实,维兰特罗较沙美特罗起效更快、作用时间更持久。
此外,维兰特罗对β2-受体的亲合力较对β1-受体和β3-受体高1 000倍,具有高度选择性[6]。
tencentriq成分

tencentriq成分
(最新版)
目录
1.Tencetriq 的介绍
2.Tencetriq 的成分
3.Tencetriq 的适应症
4.Tencetriq 的副作用
5.Tencetriq 的注意事项
正文
Tencetriq 是一种治疗癌症的药物,由美国 FDA 批准上市。
它是一种口服药物,主要成分为 Tisagenlecleucel。
Tencetriq 的适应症包括复发或难治性大细胞性 B 淋巴瘤,这是成人和儿童的一种罕见癌症。
Tencetriq 的成分主要是 Tisagenlecleucel,这是一种基因修饰的T 细胞受体,能够识别并杀死带有 CD19 抗原的癌细胞。
Tencetriq 的治疗原理是通过提取患者的 T 细胞,对其进行基因修饰,使其具有识别并杀死癌细胞的能力,然后将这些 T 细胞重新注入患者体内,以达到治疗癌症的目的。
尽管 Tencetriq 的疗效显著,但是也会出现一些副作用,包括发热、寒战、头痛、乏力等。
因此,在使用 Tencetriq 时,需要定期进行检查,并注意观察患者的身体状况,一旦出现严重的副作用,需要立即停止使用。
在使用 Tencetriq 时,还有一些需要注意的事项。
首先,由于Tencetriq 是一种基因修饰的药物,可能会引起未知的副作用,因此,在使用前需要进行全面的检查,以确保患者的身体状况能够承受这种药物。
其次,由于 Tencetriq 是一种口服药物,需要注意药物的保存,防止药物受潮或变质。
2020年10—11月FDA批准新药概况

2020年10—11月FDA批准新药概况2020年10月,FDA批出1个新分子实体和1个新生物药物,分别为治疗COVID-19药品Veklury(瑞德西韦)和治疗埃博拉病毒药物Inmazeb(atoltivimab+ maftivimab+odesivimab-ebgn)。
11月,FDA批出3个新分子实体和1个新生物药物,分别为治疗早衰综合征药品Zokinvy(lonafarnib)、治疗高草酸尿症药品Oxlumo (lumasiran)、治疗肥胖症药品Imcivree(setmelanotide)和治疗神经母细胞瘤药物Danyelza(naxitamab-gqgk)。
1 Veklury(瑞德西韦)Veklury有注射液和冻干粉两种剂型,被正式批准用于治疗年龄在12岁及以上、体重至少40 kg的需要住院治疗的COVID-19患者,成为美国首个也是唯一一个获批的新冠肺炎治疗药物。
瑞德西韦是核苷类RNA依赖的RNA聚合酶竞争性抑制剂,通过阻碍SARS-CoV-2的复制而起作用。
2 Inmazeb(atoltivimab+maftivimab+odesivimab-ebgn)Inmazeb为注射液,被批准用于治疗由扎伊尔型埃博拉病毒引起的成人和儿童患者感染,包括感染检测呈阳性母亲的新生儿。
Inmazeb靶向埃博拉病毒表面表达的糖蛋白,这种糖蛋白通过与细胞表面的受体相结合,导致病毒和宿主细胞膜的融合,使病毒进入细胞。
组成Inmazeb的3种中和抗体可同时与这种糖蛋白结合,从而阻断病毒的附着和进入细胞。
3 Zokinvy(lonafarnib)Zokinvy为口服胶囊,被批准用于减少哈金森-吉尔福德早衰综合征(Hutchinson-Gilford progeria syndrome, HGPS)患者的死亡风险,以及治疗患有特定早衰样核纤层蛋白病的1~2岁的患者。
Zokinvy是一种首创性的口服法尼基转移酶抑制剂,可阻断早衰蛋白的法尼基化,故而降低早衰蛋白在细胞核中的积累,使得早老症儿童生存获益。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
( 被 辉 瑞 收购 ) 疹 ( 特 应 性 皮 炎 )患 者
20 0 m g、 3 00m g
n u s i n e r s e n S p i n r a z a注射 液 :
2 . 4 mg / ml
百健
1 E u c r i s a ( c r i s a b o r o l e )
E u c r i s a 最 严重不 良反应为 过敏 反应 。对 E u c r i s a 活
E u c r i s a 被批准在两 岁 以上患者 中治疗轻度至 中度特 应性皮 炎,特应 性皮炎是 一种 常见 的复发性慢 性炎性皮 肤疾病 ,通常被称为 “ 湿疹 ” ,湿疹是几种皮肤类 型炎症
性成分 c r i s a b o r o l e 过敏的患者禁用 。
E u c r i s a的剂型为软 膏,对皮 炎影 响区域每 天涂抹 两 次 ,为局部使用 ,不能 口服 、眼睛 内或阴道 内使用 。
的一般 术语和 统称。特应性 皮炎是众 多类型湿 疹 中最 常
见的,患者通常表现为 以炎症和瘙痒为特点 的慢性皮疹 , 通常在儿童期开始发作 ,可 以持续至成年 。 特应 性皮炎 的致病 原 因是遗传 、免疫和环 境因素 的 组合 。在特 应性 皮炎 中,皮肤 发展成 红色、鳞状 和结皮 状隆起 , 往往非常瘙痒 。 患者刮伤患部时可 导致皮肤肿胀 、 开裂、渗流透 明液体 ,最终病人皮肤会粗化和增厚 。
度 至 中度特 异性皮 炎的类 固醇 替代疗 法,业界预计 该药
的年 销售峰值将突破 2 0亿美元。 E u c r i s a的获批是基于 2个安慰剂对照Ⅱ I 期 临床 研究 的数 据,这些研 究共入 组了 1 5 2 2例年龄 2岁至 7 9岁的 轻度 至中度 特应性 皮炎患者。数据显示,与安慰剂相 比, 患者 接 受 E u c r i s a治疗 2 8 d后病 情实现 了显 著更 大程 度
s e q u e n c i n g ,NG S )的伴随诊断检 测。
N GS检 测可以检测 卵巢癌 患者肿瘤组织 中是否存在 有害的 B R C A基 因突变 。 如果检测 到一种或更 多种突变 , 患者才有 资格 以 R u b r a c a进行治疗 。B R C A 基 因参与修 复受损 的 D N A,正 常情况 下这种基 因致力 于阻止肿 瘤 的发展 。然而 ,这些基因的突变可 能导致卵巢癌等癌症 。 R u b r a c a是一种多聚二磷酸腺苷核 糖聚合 酶抑制剂 , 其阻止一种参 与修复 受损 D N A 的酶 。通过阻止这种酶 ,
2 Ru b r a c a( r u c a p a r i b )
R u b r a c a 获 “ 突破 性治 疗药物 ”和 “ 孤 儿 药 ” 指 定
以及 “ 优先审评 “ 地 位 ,通过加速 审批程序被 批准用于 经 过两 种或两种 以上化 疗的和 B R C A基因 ( 人乳腺癌 易 感基 因)突变相关 的晚期卵巢癌。 美 国 国家癌症研 究所预测,2 0 1 6年将有 2 2 2 8 0名
用于治疗两 岁及 以上 的轻度至 中度 湿 涂抹部位 疼痛 、烧灼感或刺痛
用 于肿瘤携 带一种特 定基 因突变 ( 有 恶 心 、 疲 乏 、 呕 吐 、 贫 血 、腹 痛 、 味 害的 B R C A) ,且 已使 用 两 种 或 多 种 觉 障 碍 、便 秘 、 食 欲 减 退 、腹 泻 、 血 化 疗 药物 治疗 过 的 晚期 卵巢 癌 女性 小板 减少 和 呼吸 困难 上 呼 吸道 感 染 、下 呼 吸 道 感 染和 便秘 用 于 治 疗 儿 童 和 成 人 脊 髓 性 肌 萎 缩
1 ) ,为 治疗湿 疹新 药 E u c r i s a( c r i s a b o r o l e ) 、治疗 卵巢癌
表1 2 0 1 6 年1 2 月F D A 批准新药
通用名 商 品名 剂型 / 规格 公司 用途 常见不 良反应
c r i s a b o r o l e E u c r i s a 外用乳膏 : 2 % A n a c o r r u c a p a r i b R u b r a c a 口服 片 剂 : C l o v i s
・
药 讯 荟 萃
・
2 0 1 6 年1 2 月F D AFra bibliotek批 准新药概 况
2 0 1 6年 1 2月 ,F D A批 出 3个新 分子 实体 药 品 ( 表 新药 R u b r a c a( r u c a p a r i b )和 治疗 脊 髓 性 肌 萎缩 症 药 物
S p i n r a z a( n u s i n e r s e n ) 。
E u c r i s a是 一 种 非 甾 体 4型 磷 酸 二 酯 酶 抑 制 剂
( p h o s p h o d i e s t e r a s . 4 ,P D E . 4 ) ,这 是 一 种 含 硼 的 小 分 子 抗 炎药 ,P D E . 4抑 制 作 用 导 致 增 加 细 胞 内环 磷 酸 腺 苷 ( c AMP )水平 ,但 其作用机 制 尚未完全清楚 。 此 次 批准 使 E u c r i s a成 为美 国 F D A在 过 去 1 5 年 批 准治疗特应性 皮炎 的首个新 分子实体 。E u c r i s a 定位为轻
妇 女被确 诊患有 卵巢癌 ,估计有 1 4 2 4 0人 会死 于这种
疾 病 。患 有 卵巢 癌 的女 性 中,约 1 5 %~ 2 0 % 的人 携 带 B R C A 基 因 突 变。F D A 还一 同批准 F o u n d a t i o n F o c u s C D x B R C A 伴 随 诊 断检 测 与 R u b r a c a一 起 使 用 ,它 是 F D A 批 准 的首 个 基于 新 一代 基 因测 序 ( n e x t . g e n e r a t i o n
