石灰化学成分(活性氧化钙和氧化镁合量)试验记录表
石灰石化验方法

方法】石灰石化学分析方法石灰石的化学成分大致含量范围如下:SiO2:0.2-10%Al2O3:0.2-2.5%Fe2O3:0.1-2%CaO:45-55%MgO:0.1-2.5%烧失量:36-43%一般要求石灰石的SiO2含量<2%,CaO含量>53.5%(CaCO3含量>95%)。
一、试样的制备试样必须具有代表性和均匀性,取样按GB/T 2007.1进行。
由大样缩分后的试样不得少于100 g,然后用鄂式破碎机破碎至颗粒小于13mm,再以四分法或缩分器将试样缩减至约25g,然后通过密封式制样机研磨至全部通过孔径为0.08mm方孔筛。
充分混匀后,装入试样瓶中,供分析用。
其余作为原样保存备用。
二、二氧化硅的测定:准确称取1.0g试样(精确至0.0001g),置于100ml蒸发皿中,加入5-6gNH4Cl,用平头玻璃棒混匀,盖上表面皿,沿皿口滴加10ml (1+1)HCl及8-10滴HNO3,搅拌均匀,使试料充分分解。
把蒸发皿置于沸水浴上,皿上放一玻璃三角架,再盖上表面皿加热,期间搅拌2次,待蒸发至干后再继续蒸发10-15min。
取下蒸发皿,加20ml(3+97)热HCl,搅拌,使可溶性盐类溶解,以中速定量滤纸过滤,用胶头扫棒以(3+97)热HCl擦洗玻璃棒及蒸发皿,并洗涤沉淀10-12次,滤液及洗液承接于500ml容量瓶中,定容至标线。
此即为试验溶液,用于测定CaO、MgO、Fe2O3、Al2O3用。
滤纸与沉淀置于已恒重的瓷坩埚(m2)中,先在电炉上以低温烘干,再升高温度使滤纸充分灰化,然后置于950℃高温炉中灼烧40min,取出,等红热退去后置于干燥器中冷却15-30min,称重。
如此反复灼烧,直至恒重。
记录沉淀及坩埚的质量(m1)。
注意事项:1、严格控制硅酸脱水的温度和时间。
硅酸溶胶加入电解质后并不立即聚沉,必须在沸水浴(可用大号烧杯加水煮沸代替水浴锅用)中蒸发干涸,时间为10-15min,温度严格控制在100-110℃以内。
建筑石灰试验方法第2部分:化学试验方法

建筑石灰试验方法第2部分:化学试验方法建筑石灰的质量对于工程质量至关重要。
本文将详细介绍建筑石灰试验方法第2部分:化学试验方法,以确保石灰质量的准确评估。
一、概述建筑石灰试验方法分为物理试验和化学试验两部分。
化学试验主要针对石灰的化学成分、活性氧化钙含量、氧化镁含量等进行检测。
本部分内容主要围绕化学试验方法展开,旨在为工程建设提供准确的石灰质量数据。
二、试验方法1.化学成分分析(1)样品准备:取适量石灰样品,经研磨后过180μm(80目)筛,混合均匀。
(2)试验方法:按照GB/T 176-2017《水泥化学分析方法》进行,采用X射线荧光光谱法(XRF)或化学分析法测定石灰中的氧化钙(CaO)、氧化镁(MgO)、三氧化硫(SO3)等化学成分。
2.活性氧化钙含量测定(1)样品准备:取适量石灰样品,经研磨后过180μm(80目)筛,混合均匀。
(2)试验方法:按照GB/T 14684-2011《建筑石灰》进行,采用乙二醇法测定活性氧化钙含量。
3.氧化镁含量测定(1)样品准备:取适量石灰样品,经研磨后过180μm(80目)筛,混合均匀。
(2)试验方法:按照GB/T 176-2017进行,采用原子吸收光谱法或化学分析法测定氧化镁含量。
三、结果判定1.化学成分分析结果需满足GB/T 14684-2011的要求。
2.活性氧化钙含量测定结果需满足GB/T 14684-2011的要求。
3.氧化镁含量测定结果需满足GB/T 14684-2011的要求。
四、注意事项1.试验过程中,应严格遵循相关标准,确保试验数据的准确性。
2.试验所用仪器设备应定期进行校准和检定,以保证试验结果的可靠性。
3.试验人员需具备相应资质,熟悉试验方法及操作流程。
4.样品处理和试验过程应避免污染和误差,确保试验结果的准确性。
通过以上建筑石灰试验方法第2部分:化学试验方法的介绍,希望能为工程建设中的石灰质量检测提供参考和指导。
T0812—1994石灰氧化镁测定方法

T 0812—1994 石灰氧化镁测定方法1 适用范围本方法适用于测定各种石灰的总氧化镁含量。
2 仪器设备2.1 方孔筛:0.15mm,1个。
2.2 烘箱:50~250℃,1台。
2.3 干燥器:φ25cm,1个。
2.4 称量瓶:φ30mm×50mm,10个。
2.5 瓷研钵:φ12~13cm,1个。
2.6 分析天平:量程不小于50g,感量0.0001g,1台。
2.7 天子天平:量程不小于500g,感量0.01g,1台。
2.8 电炉:1500W,1个。
2.9 石棉网:20cm×20cm,1块。
2.10 玻璃珠:φ3mm,1袋(0.25kg)。
2.11 具塞三角瓶:250mL,20个。
2.12 漏斗:短颈,3个。
2.13 塑料洗瓶:1个。
2.14 塑料桶:20L,1个。
2.15 下口蒸馏水瓶:5000mL,1个。
2.16 三角瓶:300mL,10个。
2.17 容量瓶:250mL、1000mL,各1个。
2.18 量筒:200mL、100mL、50mL、5mL,各1个。
2.19 试剂瓶:250mL、1000mL,各5个。
2.20 塑料试剂瓶:1L,1个。
2.21 烧杯:50mL,5个;250mL(或300mL),10个。
2.22 棕色广口瓶:60mL,4个;250mL,5个。
2.23 滴瓶:60mL,3个。
2.24 酸滴定管:50mL,2支。
2.25 滴定台及滴定管夹:各1套。
2.26 大肚移液管:25mL、50mL,各1支。
2.27 表面皿:7cm,10块。
2.28 玻璃棒:8mm×250mm及4mm×180mm,各10支。
2.29 试剂勺:5个。
2.30 吸水管:8mm×150mm ,5支。
2.31 洗耳球:大、小各1个。
3 试剂3.1 1﹕10盐酸:将1体积盐酸(相对密度1.19)以10体积蒸馏水稀释。
3.2 氢氧化铵—氯化铵缓冲溶液:将67.5g 氯化铵溶于300mL 无二氧化碳蒸馏水中,加浓氢氧化铵(氨水)(相对密度为0.90)570mL ,然后用水稀释至1000mL 。
高温煅烧石灰石实验结果记录表格

标题:高温煅烧石灰石实验结果详解在古代,人们发现高温煅烧石灰石可以得到一种新的物质,用于建筑、涂料等方面。
石灰石在高温下的变化引起了人们的好奇,也促使科学家进行了大量的实验来探索其奥秘。
在本文中,我们将深入研究高温煅烧石灰石的实验结果,并结合个人观点进行全面探讨。
实验一:温度对石灰石的影响1. 温度为800°C时石灰石经过800°C的高温煅烧后,发生了明显的变化。
其外观由灰白色变为浅黄色,质地变得更加坚硬。
在加热的过程中,石灰石释放出二氧化碳,产生了氧化钙。
这表明,800°C的高温已经使石灰石发生了部分煅烧,产生了新的化学物质。
2. 温度为1000°C时当温度升至1000°C时,石灰石的变化更加显著。
它的颜色更加深黄,质地变得更加坚硬,表面呈现出一些晶体结构。
此时,石灰石已经完全煅烧,变成了氧化钙。
实验二:煅烧时间的影响1. 煅烧时间为30分钟在800°C的温度下,煅烧30分钟后,石灰石的变化并不明显。
仍然保持着浅黄色,质地也没有太大的改变。
这表明,短时间的煅烧并不能使石灰石完全发生化学变化。
2. 煅烧时间为60分钟将石灰石煅烧60分钟后,其颜色变得更加深黄,质地更加坚硬。
虽然未达到完全煅烧的程度,但已经有了一定的变化。
结论与回顾:从以上实验结果可以得知,在高温下煅烧石灰石,石灰石会产生明显的变化,并最终转化为氧化钙。
温度和煅烧时间对石灰石的变化也有一定的影响。
在实际应用中,可以根据需要选择适当的温度和时间进行煅烧,以得到符合要求的氧化钙。
个人观点:高温煅烧石灰石是一个古老而神奇的实验,通过控制温度和时间,可以使石灰石转化为有用的化学物质。
这不仅在建筑、涂料等方面有着广泛的应用,也展示了人类对自然物质的探索和利用。
希望未来可以有更多的实验来深入研究石灰石高温煅烧的过程,以及其在环境保护和新材料研发方面的应用。
通过本文的全面讨论,相信你已经对高温煅烧石灰石有了更深入的了解。
石灰的氧化镁含量试验方法
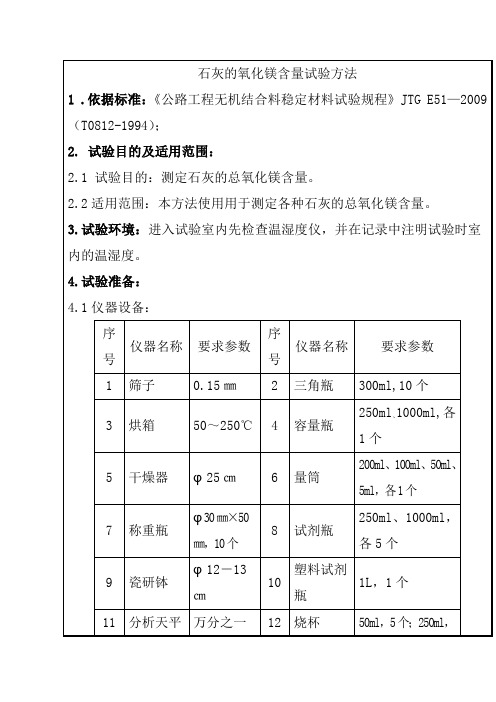
5.试验结果整理:
5.1 EDTA二钠标准溶液对氧化钙滴定度按下式计算:
(T0812-1)
式中:TCaO—EDTA标准溶液对氧化钙滴定度,即lmL EDTA标准溶液相当于氧化钙的毫克数;
各一套
21
具塞三角瓶
250ml,20个
22
大肚移液管
25ml、50ml,各1支
23
漏斗
短颈,3个
24
表面皿
7㎝,10块
25
塑料洗瓶
1个
26
玻璃棒
8㎜×250㎜及4㎜×180㎜各10支
27
塑料桶
20L
28
洗耳球
大、小各1个
29
下口蒸馏水瓶
5000ml
30
吸水管
8㎜×150㎜,5支
4.2试样及试剂准备:
9
瓷研钵
φ12-13㎝
10
塑料试剂瓶
1L,1个
11
分析天平
万分之一
12
烧杯
50ml,5个;250ml,10个
13
架盘天平
感量0.1g
14
棕色广口瓶
60ml,4个;250ml,5个
15
电炉
1500W
16
滴瓶
60ml,3个
17
石棉网
20㎝×20㎝
18
酸滴定管
50 ml,2支
19
玻璃珠
φ3㎜,一袋
20
滴定台及滴定夹
7.2一般来说,氧化镁的含量比氧化钙低v3\v4的差值(即滴定终点)很难控制,并且v3\v4的差值直接影响到氧化镁的含量,因此,在试验中应严格做好各步操作。
谈石灰试验中氧化钙及氧化镁的测定

山 西 建 筑
S HANXI ARC HI T E C I I UR E
V o 1 . 3 9 No . 2 5
1 石 灰试 验 的原 理
化钙溶 液 , 计算 1 m L E D T A二钠标 准溶 液相 当于氧 化钙 的毫克 1 ) 氧化钙含量试验是根据石灰中活性氧化钙与蔗糖 C 。 : H投 O 。 。 数。第三步计算 1 m L E D T A二钠标 准溶 液相 当于氧化镁 的毫克 化合而成水溶性 的蔗糖钙 C a O・ C , : H : O 。 。・ H : O, 而石灰 中的其 数。氧化镁含量试 验 的关键 点是称 取试样 用 减量法 。石灰 用盐
2 试 验 范 围
粒, 这样试验 时 , 滴定 终点 容易掌 握 , 否则 溶液 总是 在变 色 , 找不 本方 法适用于测定各种石 灰的有效 氧化钙 及总 氧化镁 含量 , 出终点 。6 ) 要 注意安 全 。石 灰试验 接触 的是 浓盐酸 、 浓 氨水 , 浓 酸性铬 兰 K 一萘酚绿 B 。 盐 酸加 热时要防止烫伤 , 浓 氨水 不要用鼻 子 闻, 而应是 用手扇 , 如
化钙 含量 试验 的 关键 点是 蔗糖要 迅 速覆 盖试 样 , 以 防试样 被碳
级, 这 时就需要做石灰试 验。通常工地上 要求 只做氧 化钙 和氧化
使试样 充分溶 解 。注意石 灰 的存 镁含量两项技术 指标 。在道路桥梁 这个行业 , 学 化学分 析专业 的 化。加入玻璃珠后要充分振荡 , 放时间 。因为有效 氧化 钙含量 是随着 石灰 的存 放时 间的增 长 而 人很少 , 几乎是工科 类专 业 的人 , 做这 个试 验就 有种 跨行 业 的感 减少的 。一定要 用 新 煮沸 并 已经 冷却 的蒸 馏 水 , 以消除 二 氧化 觉 。这时就不仅 需要 弄懂其试验原 理 , 还 要知道 化学分 析 的一般 碳。2 ) 氧 化镁 的测定 : 第 一步 配制 氧化钙 标准溶 液 , 精确称 量碳 知识 , 这样 才能保证试验 的准确性 。我在 此文 中总结 了做这项 试 酸钙 1 . 7 8 4 8 g , 这个称量一定要准 确 , 它影响后面 的相关试 验 , 关 验的经验及感受 , 以供大 家学 习和思考 。 系到氧化镁含量 的准 确测 定。第 二步 是用 E D T A标准 液标 定 氧
石灰有效氧化钙和氧化镁含量试验(简易法)记录表

委托单位:路线名称:工程名称:
委托编号:试样编号:试验日期:
石灰种类
石灰用途
石灰用途
样品编号
பைடு நூலகம்试件
编号
空瓶
质量
瓶+试样质量
(g)
试样
质量
(g)
盐酸
当量
浓度
盐酸
耗量(ml)
有效氧化镁和氧化钙合量(%)
单值
平均值
备注
试验:复核:负责人:单位:
依据:JTG E51-2009《公路工程无机结合料稳定材料试验规程》第39页
精度要求及结果整理
(CaO+MgO)%=(V×N×0.028/G)×100
式中:V滴定消耗盐酸标准液的体积(mL);
N盐酸标准液的摩尔浓度;
G样品质量(g);
0.028氧化钙的毫克当量,因氧化镁含量甚少,并且两者之毫克当量相差不大,故有效(CaO+MgO)%的毫克当量都以CaO的毫克当量计算。
本方法适用于氧化镁含量在5%以下的低镁石灰。
石灰试验

☞ 安定性:试验结果处理
烘干后,用肉眼检查饼块,无溃散、 暴突、裂缝称为体积安定性合格;若出 现三种现象中之一者,表示体积安定性 不合格。
☞ 游离水:仪器设备
1)FA2004万分之一天平; 2)称量瓶:30mm×60mm; 3)101-3A电热鼓风烘箱。
☞ 游离水:试验原理
当消石灰加热到105℃时,游离水会 逃逸,通过计算在此温度下的质量损 失,得到消石灰游离水百分含量
☞ 松散密度:试验原理
m=ρ*V
☞ 松散密度:试验步骤
➢称量容量筒(M0),精确至0.1g,置于工作 台上,用样品装满容量筒直至溢出; ➢用刮刀刮平,出去多余的样品,刮平过程中 引更避免容量筒震动和样品溢出。 ➢刮平后擦干净容量筒外壁,避免样品溢出, 用天平称量容量筒(M1)精确至0.1g。
☞ 松散密度:试验结果处理
☞有效氧化钙:标准盐酸溶液标定
➢然后加入2滴1g/L甲基红指示剂,记录滴定管中待标 定盐酸标准溶液的体积V1,用待标定的盐酸标准溶液 滴定至碳酸钠溶液出现红色;
☞有效氧化钙:标准盐酸溶液标定
➢将溶液加热至微沸,然后放在冷水中冷却至室温, 再用盐酸标准溶液滴定,如此反复,直至溶液出现浅 红色,煮沸不褪色为止。
☞产游浆离量水和:未仪消器化设残备渣量:仪器设备
1)SRJZ-1型石灰浆渣测定仪; 2)KD-2000电子天平; 3)玻璃量筒:500mL; 4)搪瓷盘; 5)钢板尺:量程为300mm ; 6)101-3A电热鼓风烘箱; 7)圆孔筛:孔径5mm,20mm。
☞产浆量和未消化残渣量:试验步骤
➢将4kg试样破碎全部通过20mm圆孔筛,其中小于5mm 以下粒度的试样量不大于30%,混均,备用,生石灰 粉样混均即可。 ➢在消化器中加入(320±1)mL温度为(20±2)℃的 水,然后加入(200±1)g生石灰(块状石灰则碾碎成 小于5mm的粒子)(M)。
石灰试验检测记录表
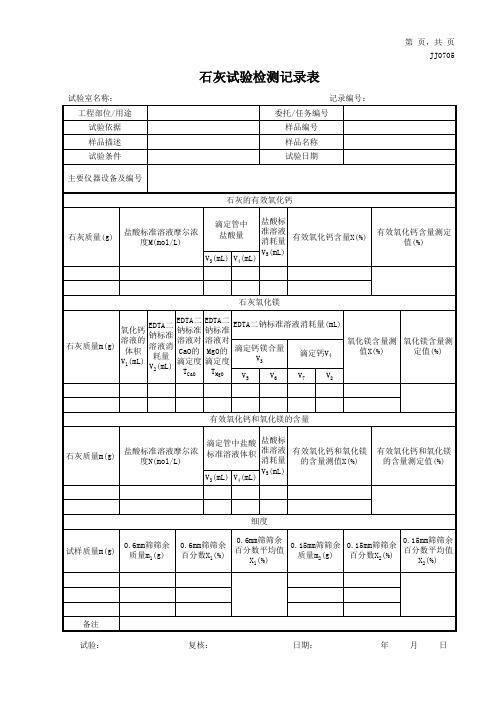
有效氧化钙和氧化镁的含量 滴定管中盐酸 盐酸标 盐酸标准溶液摩尔浓 标准溶液体积 准溶液 有效氧化钙和氧化镁 石灰质量m(g) 消耗量 度N(mol/L) 的含量测值X(%) V5(mL) V3(mL) V4(mL)
有效氧化钙和氧化镁 的含量测定值(%)
细度 0.6mm筛筛余 试样质量m(g) 质量m1(g) 0.6mm筛筛余 百分数X1(%) 0.6mm筛筛余 0.15mm筛筛余 0.15mm筛筛余 0.15mm筛筛余 百分数平均值 百分数平均值 质量m2(g) 百分数X2(%) X1(%) X2(%摩尔浓 度M(mol/L)
有效氧化钙含量测定 值(%)
石灰氧化镁 EDTA二 EDTA二 EDTA二钠标准溶液消耗量(mL) EDTA二 氧化钙 钠标准 钠标准 钠标准 溶液的 溶液对 溶液对 氧化镁含量测 氧化镁含量测 溶液消 石灰质量m(g) 体积 CaO的 MgO的 滴定钙镁合量 值X(%) 定值(%) 滴定钙V 4 耗量 V3 V1(mL) 滴定度 滴定度 V2(mL) TCaO TMgO V5 V6 V7 V8
第 页,共 页 JJ0705
石灰试验检测记录表
试验室名称: 工程部位/用途 试验依据 样品描述 试验条件 主要仪器设备及编号 石灰的有效氧化钙 滴定管中 盐酸量 V3(mL) V4(mL) 盐酸标 准溶液 有效氧化钙含量X(%) 消耗量 V5(mL) 委托/任务编号 样品编号 样品名称 试验日期 记录编号:
备注 试验: 复核: 日期: 年 月 日
石灰剂量试验记录

石灰剂量试验记录试验目的:研究不同的石灰剂量对土壤性质和作物产量的影响。
试验材料:1.土壤样本:选取一块土壤肥沃、质地较松散的试验区域作为土壤样本。
2.石灰:使用粉剂状生石灰作为试验用石灰剂。
试验设计:将试验区域划分为12个小区,每个小区面积相同,且土壤性质相似。
每个小区施加不同剂量的石灰,剂量范围为0 kg/hm^2、100 kg/hm^2、200 kg/hm^2、300 kg/hm^2、400 kg/hm^2和500 kg/hm^2、每个小区设置3个重复,共计36个试验单位。
试验步骤:1.准备工作:清理试验区域并将试验区域内杂草清除。
2. 土壤采样:在每个小区内随机取3个点,深度为20 cm,采集土壤样本,并将其混合均匀。
3.石灰添加:按照试验设计,在每个小区内施加相应剂量的石灰剂。
4.混合土壤:将石灰剂与土壤进行充分混合,确保石灰均匀分布在土壤中。
5.植株培育:在试验区域内栽植一种作物(如小麦或玉米),并根据实际需要进行适当的灌溉、施肥等管理措施。
6.生长期观测:每个小区内的作物进行生长期观测,包括植株生长情况、叶片颜色和形态等。
7.产量测定:收获作物后,对每个小区内的作物进行称重,并记录作物的产量。
8.土壤性质测定:在试验结束后,对每个小区的土壤样本进行土壤性质测定,包括土壤酸碱度、有机质含量和养分含量等。
试验结果:根据试验数据统计和分析,得出以下结论:1.不同剂量的石灰剂对土壤酸碱度有显著影响,随着石灰剂量的增加,土壤酸度减小,碱性增加。
2.石灰剂对土壤有机质含量有一定影响,适量的石灰剂可以促进有机质的分解释放,但高剂量的石灰剂会对土壤有机质产生一定的破坏作用。
3.石灰剂的添加对土壤中的氮、磷、钾等养分含量有一定影响,适量的石灰剂可以提高土壤养分的有效性,但过量的石灰剂可能导致养分流失。
4.石灰剂对作物产量有显著影响,适量的石灰剂可以提高作物的产量,但过量的石灰剂对作物生长不利。
结论:根据试验结果,适量的石灰剂可改善土壤性质,提高作物产量。
实验建筑材料石灰中钙镁含量测定

实验10 建筑材料石灰中钙镁含量测定教学目地与要求:1.学习盐酸直接滴定法测定钙镁含量地原理和方法;2.了解络合滴定法测定钙镁含量地原理和方法;3.让学生熟练掌握移取,称量,配制一定浓度标准溶液等操作;4.进一步熟练掌握滴定操作;5.学会如何合理地设计实验并培养学生地动手操作能力及创新意识. 教学重点与难点:重点:1.盐酸直接滴定法测定钙镁含量地原理和方法;2.培养学生地动手操作能力及创新意识.难点:1.盐酸直接滴定法测定钙镁含量地原理和方法;2.盐酸直接滴定中反应条件地控制.教学方法与手段:板书,学生操作,现场指导.学时分配:3学时.教学内容:898℃问题1:石灰有哪些用途?首先,概括一下在建筑、农业、工业上地用途,其中地熟石灰功不可没.建筑:三合土、石灰浆(Ca(OH)2+CO2=CaCO3↓+H2O).农业:配制波尔多液作为农药(Ca(OH)2+CuSO4=CaSO4+Cu(OH)2↓).将适量地熟石灰加入土壤,可以中和酸性,改变土壤地酸碱性.工业:制氢氧化钠(Ca(OH)2+Na2CO3=CaCO3↓+2NaOH).配制价格低廉地漂白粉(Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O).问题2:石灰地主要成分有哪些?石灰地主要成分是氧化钙(CaO),其次为氧化镁(MgO).问题3:建筑用石灰有哪些?建筑用石灰有:生石灰(块灰),生石灰粉,熟石灰粉(又称建筑消石灰粉、消解石灰粉、水化石灰)和石灰膏等几种形态.问题4:测定石灰中钙镁含量地意义?根据石灰中钙、镁含量地高低,可以判断石灰地质量等级,并根据其含量计算其参加量,有效地利用资源.问题5:测定石灰中钙镁含量地方法有哪些?测钙地方法:配位滴定法、酸碱滴定法(返滴定法和直接滴定法)、间接滴定法.配位滴定法:酸碱滴定法:1、返滴定法:用过量地盐酸标准溶液直接滴在碳酸钙样品上,剩余地盐酸用标准氢氧化钠溶液滴定;2、直接滴定法:T0811-1994.(p35)间接滴定法:将CaCO3转化为CaC2CO4后,用H2SO4溶解,再用KMnO4标准溶液滴定,把C2O42-氧化为CO2,当把C2O42-氧化完全后,滴入地KMnO4溶液不再褪色.测镁地方法:配位滴定法问题6:直接滴定法测定石灰中钙镁含量地原理?测钙:石灰加水,加酚酞,用盐酸滴定至红色消失(30s不变红)为终点.测钙镁:石灰加水,加酚酞,用盐酸滴定至红色消失(5min不变红)为终点.问题7:直接滴定法测定石灰中钙镁含量地用品?1、仪器:电子天平、电炉、容量瓶、酸式滴定管、量筒等.2、试剂:盐酸(0.5mol·L-1、1mol·L-1)、碳酸钠、石灰样品、酚酞(0.5g酚酞溶于50mL95%地乙醇中)、甲基橙(0.1%水溶液).问题8:直接滴定法测定石灰中钙镁含量地步骤?1.有效氧化钙地测定:1.1 配制盐酸溶液(0.5mol·L-1):将42mL浓盐酸稀释至1L.1.2 标定盐酸溶液地浓度:称取0.8—1.0g(精确至0.0001g)已在180℃烘干2h地碳酸钠(优级纯),记录为m(g),置于锥形瓶中,加100mL水使其完全溶解;然后加入2~3滴0.1%甲基橙指示剂,记录滴定管中待标定盐酸溶液地体积为V1,用盐酸溶液滴定至溶液由黄色变为橙红色;将溶液加热至微沸,并保持微沸3min,然后放在冷水中冷却至室温,如果此时橙红色变为黄色,再用盐酸滴定至溶液出现稳定橙红色为止,记录滴定管中盐酸溶液地体积V2,V2、V1地差值即为盐酸溶液地消耗量V(mL).盐酸溶液地浓度C=m/(V×0.053) (mol·L-1)1.3 测定石灰中有效氧化钙地含量:称取0.8—1.0g(精确至0.0001g)地石灰样品,记录为m1,放入锥形瓶中,加入50mL水,震荡15min,用水冲洗锥形瓶内壁,加入2~3滴酚酞指示剂,记录滴定管中待标定盐酸溶液地体积为V3,用已标定地盐酸溶液滴定(滴定速度以每秒2~3滴为宜)至溶液粉红色消失,并在30s内不再变红为终点,记录滴定管中盐酸溶液地体积V4,V4、V3地差值即为盐酸溶液地消耗量V5(mL).有效氧化钙地含量X(%)=(V5×C×0.028)÷m1×1002.有效氧化钙和氧化镁地测定:2.1 配制盐酸溶液(1mol·L-1):将83mL浓盐酸稀释至1L.2.2 标定盐酸溶液地浓度:称取1.5—2.0g(精确至0.0001g)已在180℃烘干2h地碳酸钠(优级纯),记录为m(g),置于锥形瓶中,加100mL水使其完全溶解;然后加入2~3滴0.1%甲基橙指示剂,记录滴定管中待标定盐酸溶液地体积为V1,用盐酸溶液滴定至溶液由黄色变为橙红色;将溶液加热至微沸,并保持微沸3min,然后放在冷水中冷却至室温,如果此时橙红色变为黄色,再用盐酸滴定至溶液出现稳定橙红色为止,记录滴定管中盐酸溶液地体积V2,V2、V1地差值即为盐酸溶液地消耗量V(mL).盐酸溶液地浓度C=m/(V×0.053) (mol·L-1)2.3 测定石灰中有效氧化钙和氧化镁地含量:称取0.8—1.0g(精确至0.0001g)地石灰样品,记录为m1,放入锥形瓶中,加入150mL水,加热5min但不要使液体沸腾,放入冷水中迅速冷却.加入2~3滴酚酞指示剂,记录滴定管中待标定盐酸溶液地体积为V3,用已标定地盐酸溶液滴定(滴定速度以每秒2~3滴为宜)至溶液粉红色消失,并在5min内不再变红为终点,记录滴定管中盐酸溶液地体积V4,V4、V3地差值即为盐酸溶液地消耗量V5(mL).有效氧化钙和氧化镁地含量X(%)=(V5×C×0.028)÷m1×100实验中应注意地问题:1、碳酸钠和石灰样品应烘干.2、配制盐酸溶液时应注意安全.3、测定有效氧化钙、氧化镁地含量时,滴定速度不宜过快,否则测定结果偏高.4、氧化镁分解缓慢,如果氧化镁含量高,则到达到达终点地时间会很长,从而增加了空气中二氧化碳地作用时间,影响测定结果.因此,在测定石灰中有效氧化钙和氧化镁地含量时,如果滴定过程超过半小时,测定结果只能作参考.结果与讨论:1、根据测定结果,评定所测石灰地质量等级.(GB 1595-79)2、分析影响测定结果地原因.课外学习网站:1、/b/16485549.html2、/view/57393cc9da38376baf1fae5a.html3、/p-379320167.html4、/download/explain.php?fileid=25606378&page=15、/view/e7b77c4d852458fb770b5662.html6、/view/15337d5f312b3169a451a4e3.html知识拓展:1、GB/T 3286.1-2012 石灰石、白云石化学分析方法氧化钙量和氧化镁量地测定2、JTG E51-2009:T0811-2009、T0812-209、T0813-20093、什么是碱-集料反应?碱-集料反应(Alkali-Aggregate Reaction, AAR)是指混凝土中地碱与集料中地碱活性成分发生化学反应,生成膨胀物质使混凝土内部产生自膨胀应力,造成混凝土开裂破坏,从而大大缩短混凝土建筑物地使用寿命,预防和抑制碱-集料反应是国内外混凝土界研究地重要领域之一.能力训练:测定蛋壳中钙镁含量.问题1:蛋壳中地主要成分有哪些?问题2:用哪种方法测定比较简单?问题3:测定中需要地实验用品有哪些?问题4:测定地原理是什么?问题5:设计一个简单地实验步骤.参考资料:1、/view/d9afd97b31b765ce050814c5.html2、/view/c32d477f168884868762d63e.html3、/view/ff777646be1e650e52ea9979.html4、/view/06c5c8e36294dd88d0d26b1b.html5、/view/09b26a5f69eae009581becd2.html素质提升:查阅资料,分析比较测定石灰中有效氧化钙和氧化镁地含量时络合滴定和盐酸直接滴定地优缺点.。
石灰石粉化验分析方法氧化钙氧化镁

.石灰石粉化验分析方法(氧化钙、氧化镁)方法提要:硼砂混合剂熔融,熔融物以硝酸加热浸取。
试样置于铂坩埚中以碳酸钾-化验试剂:小℃)中烘2)混合剂:先将碳酸钾放在干燥几天,硼砂放在烘箱(-硼砂(1+1105碳酸钾的重量,将碳酸钾与无水硼砂在玛瑙研钵中研细,混匀后贮存于茶色磨:1时后,然后按1 口瓶中。
6体积的水混合。
):将1体积的硝酸与硝酸(1+6 制备步骤:硼砂混合剂混匀,再以少许熔剂清洗玻璃棒,碳酸钾-0.5g试样于铂坩埚中,加2g称取约℃下并铺于试样表面。
盖上坩埚,从低温开始逐渐升高温℃至气泡停止发生后,在950-100分钟,然后用坩埚钳夹持铂坩埚旋转,使熔融物均匀地附于铂坩埚的内壁。
冷3-5继续熔融)的烧杯中,并继续1+6却至室温后将铂坩埚及盖一并放入加热至微沸的盛有100ml硝酸(最后将溶液冷却至室温,再用水清洗铂坩埚及盖,保持其微沸的状态,直至熔融物完成分解。
容量瓶定容,摇匀后供化验使用。
移入250ml 氧化钙的测定方法提要1为指CMP2%)掩蔽硅酸,三乙醇胺掩蔽铁、钼,以在PH大于12的溶液中,以氟化钾(标准溶液直接滴定钙。
钙离子与钙黄绿素生成络合物为绿色荧光,钙黄绿EDTA示剂,用素为橘红色,因此滴定终点时绿色荧光消失,而呈现橘红色。
2试验试剂1+1)盐酸(水中)溶于氟化钾(KF.2H2O100ml2%氟化钾:将2g 体积的水混合体积的三乙醇胺与21三乙醇胺(1+2):将CMP 指示剂:1g钙黄绿素+1g甲基百里香酚蓝+0。
2g酚酞+5g在105℃烘过的硝酸钾研磨细,存于磨口瓶中。
20%NaOH溶液0.002mol/l EDTA标准溶液3分析步骤准确吸取待测溶液25.00ml,放入100ml烧杯中,加5ml盐酸及5ml2%氟化钾溶液,并放置1 / 2 .指示剂,加入氢氧化CMP,加4ml三乙醇胺及适量的2分钟以上,然后用水稀释至200ml0.002 mol/l EDTA),用钾溶液调节溶液出现绿色荧光后再过量7-8ml(此时溶液PH大于12 标准溶液滴定至溶液绿色荧光消失(而呈现酒红色)。
石灰化学成分试验

2、仪器及试剂
3、EDTA标准溶液与氧化钙和氧化镁关系的标定
4、试验步骤
5、结果整理
有效氧化镁的百分含量按下式计算:
MgO TMgO ( V1 V2 ) 10 G 1000 100%
式中:TMgO——EDTA二钠标准溶液对氧化镁的滴定度 V1——滴定钙、镁含量消耗EDTA二钠标准溶 液体积(ml) V2——滴定钙消耗EDTA二钠标准溶液体积(ml) 250 10 ——总溶液对分取溶液的体积倍数 25 G——试样质量(g)
第五章 路面基定
1、试验目的
石灰的质量只要取决于有效氧化钙和氧化 镁的含量,它们的含量愈高,则石灰黏结力愈好。
2、仪器及试剂 3、试样 4、试验步骤
5、结果整理
有效氧化钙的百分含量按下式计算:
V C 0.028 C aO 100% G
式中:V——滴定时消耗盐酸标准溶液的体积(ml) C——盐酸标准溶液物质的量浓度(mol/ml) G——试样质量(g)
6、精密度
对同一石灰样品应取2个试样分别进行测定, 并取2次结果的平均值代表最终结果。
氧化镁的测定
1、试验目的
石灰中有效氧化钙和氧化镁含量愈高,石灰黏结 力愈好,按氧化镁含量可将石灰划分为钙质石灰或 镁质石灰。
6、精密度
对同一石灰样品应取2个试样分别进行测定, 并取2次结果的平均值代表最终结果。
石灰石、白云石中钙(氧化钙)和镁(氧化镁)的测定

常规化学分析中,对于石灰石、白云石中钙(氧化钙)和镁(氧化镁)的测定,一般先用酸溶解样品,再控制pH值为10的条件下测定钙镁合量,在pH值12~13的条件下测定氧化钙含量,然后用差减法求得氧化镁的含量。
笔者经过试验,拟定了首先将pH值控制在12~13的条件下,测出氧化钙含量,再改变pH值到10,测定氧化镁含量的钙镁连续滴定方法。
本法与常规方法相比,其最大特点就是能将2种离子连续滴定,且其精密度和准确度与常规方法基本一致。
1 试验部分1.1 主要试剂钙标准溶液:用基准碳酸钙配成浓度为2.0mg/ml的标准溶液;镁标准溶液:用经过EDTA标定的硫酸镁配成浓度1.0mg/ml的标准溶液;三乙醇胺(TEA)溶液:1∶1;孔雀绿(MG)溶液:0.1%;钙指示剂(NN):MNN∶MNaCl=1∶100;酸性铬蓝K-奈酚绿B(K-B):MK∶MB∶MNaCl=1∶2∶50;EDTA标准溶液:0.02mol/L。
1.2 试验原理吸取钙、镁标准溶液各5.00ml,置于250ml锥形瓶中,加入蒸馏水至溶液体积约为100ml,然后加入TEA溶液5ml,摇匀,再加孔雀绿溶液(MG)1~2滴,在摇动下滴加10% NaOH溶液至溶液的绿色刚好消失为止。
加适量的固体NN 指示剂,用EDTA标准溶液滴定至溶液由紫红色突变为纯蓝色即为终点(以消耗的EDTA溶液的体积计算CaO的含量)。
向滴定完钙的上述溶液中滴加盐酸溶液(1∶1)至溶液由蓝色变为紫红色并过量约1ml,摇匀。
然后用氨水溶液回滴至溶液呈蓝色,加入pH为10的氨缓冲溶液10ml,加适量K-B固体指示剂,摇匀,用EDTA标准溶液滴定至溶液由紫红色变为蓝色即为终点(以消耗的EDTA溶液体积计算MgO的含量)。
1.3 试样分析称取试样(于105℃左右烘干水分)0.5000g置于100ml烧杯中,加少量水湿润,分数次从烧杯嘴边加入1∶1 HCl 10ml左右(加盖表面皿),小心加热使试样完全溶解。
石灰试验检测记录表及报告
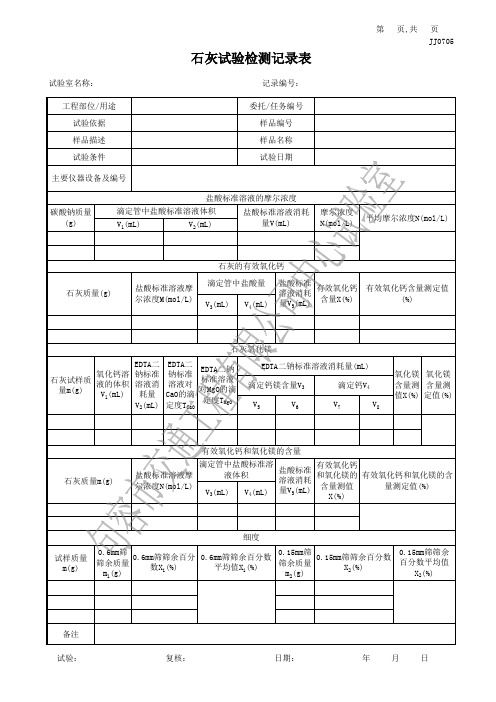
滴定管中盐酸标准溶 液体积
盐酸标准 溶液消耗
有效氧化钙 和氧化镁的 有效氧化钙和氧化镁的含
尔浓度N(mol/L) (mL)
含量测值 X(%)
量测定值(%)
细度
试样质量 m(g)
0.6mm筛 筛余质量
m1(g)
0.6mm筛筛余百分 数Xi(%)
0.6mm筛筛余百分数 平均值Xi(%)
耗量 V2(mL)
EDTA二 钠标准 溶液对 CaO的滴 定度TCaO
EDTA二钠 标准溶液 对MgO的滴 定度TMgO
EDTA二钠标准溶液消耗量(mL)
滴定钙镁含量V3
V5
V6
滴定钙V4
V7
V8
氧化镁 氧化镁 含量测 含量测 值X(%) 定值(%)
石灰质量m(g)
有效氧化钙和氧化镁的含量
盐酸标准溶液摩
0.15mm筛 筛余质量
m2(g)
0.15mm筛筛余百分数 X2(%)
0.15mm筛筛余 百分数平均值
X2(%)
备注 试验:
复核:
日期:
年
月
日
石灰试验检测记录表
第 页,共 页 JJ0705
试验室名称:
记录编号:
工程部位/用途 试验依据 样品描述 试验条件
委托/任务编号 样品编号 样品名称 试验日期
主要仪器设备及编号
碳酸钠质量 (g)
盐酸标准溶液的摩尔浓度
滴定管中盐酸标准溶液体积
V1(mL)
V2(mL)
盐酸标准溶液消耗 量V(mL)
摩尔浓度 N(mol/L)
平均摩尔浓度N(mol/L)
石灰质量(g)
盐酸标准溶液摩 尔浓度M(mol/L)
石灰的有效氧化钙
试表23 石灰化学分析试验报告
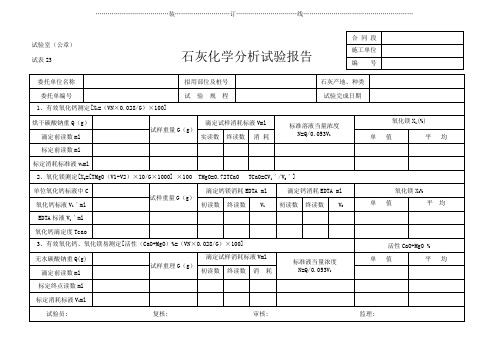
消耗
标定终点读数ml
标定消耗标液V1ml
试验员:复核:审核:监理:
石灰化学ቤተ መጻሕፍቲ ባይዱ析试验报告
委托单位名称
拟用部位及桩号
石灰产地、种类
委托单编号
试验规程
试验完成日期
1、有效氧化钙测定[X1=(VN×0.028/G)×100]
烘干碳酸钠重Q(g)
试样重量G(g)
滴定试样消耗标液Vml
标准溶液当量浓度N=Q/0.053V1
氧化镁X1(%)
滴定前读数ml
实读数
终读数
消耗
单值
平均
标定前读数ml
标定消耗标准液v1ml
2、氧化镁测定[X2=[TMgO(V1-V2)×10/G×1000]×100 TMgO=0.72TCaO TCaO=CV1ˊ/V2ˊ]
单位氧化钙标液中C
试样重量G(g)
滴定钙镁消耗EDTA ml
滴定钙消耗EDTA ml
氧化镁X2%
氧化钙标液V1ˊml
初读数
终读数
V1
初读数
终读数
V2
单值
平均
EDTA标液V1ˊml
氧化钙滴定度Tcao
3、有效氧化钙、氧化镁易测定[活性(CaO+MgO)%=(VN×0.028/G)×100]
活性CaO+MgO %
无水碳酸钠重Q(g)
试样重理G(g)
滴定试样消耗标液Vml
标准液当量浓度N=Q/0.053V1
单值
平均
滴定前读数ml
初读数
石灰的化学分析试验记录表

பைடு நூலகம்(mL)
EDTA对MgO的平均滴定度
(mL)
EDTA耗量
滴定钙镁含量
(mL)
滴定钙含量
(mL)
氧化镁含量
(%)
平均值
(%)
有效钙加氧化镁含量
(%)
未消化残渣含量试验
试样质量
(g)
未消化残渣质量
(g)
未消化残渣含量
(%)
未消化残渣平均含量
(%)
结论
备注:
试验:记录:复核:
委托单号
任务单号
样品描述
收样日期
检测规程
试验日期
主检仪器
试验环境
有效氧化钙含量测定试验
试样质量
(g)
盐酸溶液当量浓度
(N)
盐酸溶液耗量
(ml)
有效氧化钙含量
(%)
平均值
(%)
有效氧化镁含量测定试验
试样质量
(g)
吸取氧化钙标准溶液体积
(mL)
消耗EDTA标准溶液体积
(mL)
EDTA对MgO的滴定度
(mL)
建筑石灰试验方法第1部分

建筑石灰试验方法第1部分一、引言建筑石灰是建筑材料中常用的一种,其主要成分是氧化钙(CaO),也含有少量氧化镁(MgO)、氧化铁(Fe2O3)等杂质。
石灰具有吸湿性、碱性和可塑性等特点,因此在建筑中被广泛应用于制作砂浆、涂料、抹灰等方面。
为了保证建筑石灰的质量,需要对其进行试验。
本文将介绍建筑石灰试验方法的第1部分。
二、试验目的本试验旨在确定建筑石灰的主要物理性能指标,包括活性钙含量、细度和水合速率。
三、试验设备和材料1. 筛分机:用于将石灰进行筛分。
2. 烘箱:用于将石灰样品干燥至恒定质量。
3. 研钵和研棒:用于将石灰样品粉碎。
4. 电子天平:用于称量试样和药品。
5. 活性钙含量试剂盒:包括甲酸钾溶液、硫酸盐指示剂溶液等。
6. 细度试验器:包括细度筛、振动器等。
7. 水合速率试验器:包括水合器、温度计等。
8. 建筑石灰样品。
四、试验步骤1. 活性钙含量试验(1)取建筑石灰样品10克,加入50毫升甲酸钾溶液中,用玻璃棒搅拌均匀。
(2)将混合物倒入滤纸漏斗中过滤,收集过滤液。
(3)在过滤液中加入硫酸盐指示剂溶液,用0.025mol/L硝酸银标准溶液进行滴定,记录所需的硝酸银标准溶液体积V1。
(4)取另外10克建筑石灰样品,干燥至恒定质量后称重,记录称重值为m1。
(5)将干燥后的建筑石灰样品加入已知体积的容器中,并加入适量的水,在水中悬浮30分钟后静置,记录静置后的上清液体积V2。
(6)将上清液倒入活性钙含量试剂盒中进行试剂反应,按照试剂盒说明书进行操作,记录所需的硝酸银标准溶液体积V2。
(7)活性钙含量计算公式为:活性钙含量(%)=(V1-V2)×0.028×100/m1。
2. 细度试验(1)取建筑石灰样品100克,通过筛分机筛分,记录通过不同孔径的筛网的质量。
(2)将不同孔径的筛网放入细度试验器中,加入建筑石灰样品,启动振动器进行振动。
(3)振动时间为10分钟后停止振动,记录每个筛网上的残留物质量。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
工程名称:六合区六玉线红山窑段路面改造工程合同号:——编号:
试表304-2
委托单位名称
——
试验单位
监理试验室
委托单编号
——
试验规程
JTJ057-94
试验日期
2007.10.6
试验人签字
现场桩号
粒料拌和厂
复核人签字
试样描述
消石灰
主管签字
试
验
次
数
称
量
瓶
号
空
技术负责人:试验监理工程师:
瓶质量ຫໍສະໝຸດ (g)瓶与石灰试样的质量(g)
石灰试样
的质量(g)
盐酸的当量浓度
(N)
盐酸的消耗量
(ml)
活性CaO+MgO
含量(%)
(1)
(2)
(3)
(4)
(5)≡(4)-(3)
(6)
(7)
(8)
1
0.8351
0.9579
18.2
58.5
2
0.8286
0.9579
17.8
57.6
备注及评语
经检验,该石灰样为三级钙质消石灰,符合规范要求。
