核酸和蛋白质的化学合成与序列分析(金冬雁等编著)思维导图
生物化学思维导图生化思维导图
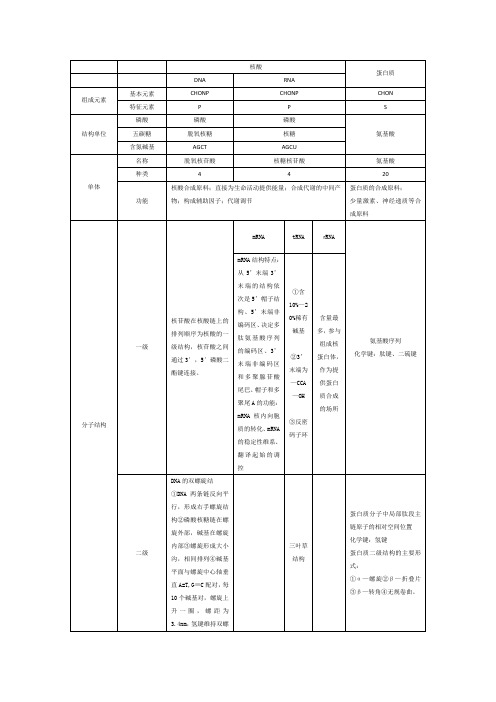
蛋白质
DNA
RNA
组成元素
基本元素
CHONP
CHONP
CHON
特征元素
P
P
S
结构单位
磷酸
磷酸
磷酸
氨基酸
五碳糖
脱氧核糖
核糖
含氮碱基
AGCT
AGCU
单体
名称
脱氧核苷酸
核糖核苷酸Leabharlann 氨基酸种类44
20
功能
核酸合成原料;直接为生命活动提供能量;合成代谢的中间产物;构成辅助因子;代谢调节
蛋白质的合成原料;
少量激素、神经递质等合成原料
三叶草结构
蛋白质分子中局部肽段主链原子的相对空间位置
化学键:氢键
蛋白质二级结构的主要形式:
①α—螺旋②β—折叠片③β—转角④无规卷曲。
三级
DNA超螺旋
①负超螺旋:顺时针右手螺旋的DNA双螺旋②正超螺旋:反方向围绕它的轴扭转而成
倒L形
在二级结构和模体等结构层次的基础上,由于侧链R基团的相互作用,整条肽链进行范围广泛的折叠和盘曲
化学键:疏水键、离子键、氢键、范德华力
四级
蛋白质分子中各个亚基的空间排布及亚基接触部位的布局
化学键:疏水键、氢键、离子键
理化性质
紫外吸收特征:共轭双键,260nm为吸收峰
紫外吸收特征:共轭双键,260nm为吸收峰
紫外吸收特征:肽键和芳香族氨基酸
变性
变性
变性
复性
-
复性(破坏较轻时)
杂交
杂交
-
胶体性质
分离
分子结构
一级
核苷酸在核酸链上的排列顺序为核酸的一级结构,核苷酸之间通过3′,5′磷酸二酯键连接。
蛋白质化学思维导图。1

谷氨酸(Glu) 天冬氨酸(Asp)
酸性氨基酸
氢基
甘氨酸(Gly)
乙酰胺基
天冬酰胺(Asn)
丙酰胺基 甲羟基
谷氨酰胺(Gln) 丝氨酸(Ser)
极性氨基酸介绍
1-乙羟基
苏氨酸(Thr)
甲巯基
半胱氨酸(Cys)
3-胍基正丙基
精氨酸(Arg)
咪唑基-4-甲基
组氨酸(His)
碱性氨基酸
4-氨基正丁基
极性
带电荷
正电荷 负电荷
不带电荷
非极性
脂肪族
芳香族
Tyr,Trp,Phe
杂环族
Pro,Trp,His
必需氨基酸
非必需氨基酸
多肽
方向性
10个以上氨基酸
肽
寡肽
少于10个
Lys,Arg,His Asp,Glu
分子结构
一级结构 二级结构
三级结构 四级结构
概述
定义
二级结构部件
α螺旋 β折叠
右手螺旋,3~6个氨基酸旋转一周,0.54nm,肽键平面与螺旋长轴平行,R基团在外 侧
赖氨酸(Lys)
极性氨基酸
血红蛋白β链第六位Glu被Val取代,血红蛋白易凝聚 镰刀形红细胞贫血症
关系 与疾病关系
一级结构与功能的关系 构象与功能的关系
结构与功能
二硝基氟苯法(DNFB)、二甲氨基萘磺酰氯法(DNS-Cl),Edman降解法、氨肽酶 法
N端分析
肼解法、羧肽酶法
C端分析
分离编码蛋白质的基因 测定DNA序列 排列出mRNA顺序 按照三联密码子原则推导出氨基酸系列
成锯齿状,顺反平行排列,反式稳定,ຫໍສະໝຸດ 在片层上下β转角 无规线团
第二十章蛋白质和核酸

R CH COOH NH2
OH
H
R CH COO
R CH COO
R CH COOH
NH2
H
NH3
OH
NH3
一般来说,氨基酸含氨基多,pI值较高,含羧基多者pI值较低 。
Honghe University Prof Guo Ya-li
O C
CO CO 茚三酮
H2O
O
C OH
C
+ RCHCOOH
C O OH
NH2
O C OH
C C O OH
水合茚三酮
CO
O C
C NC
CO
C HO
RCHO + CO
3 H2O
Honghe University Prof Guo Ya-li
3.氨基酸羧基的反应 (1)叠氮法合成肽
氨基酸分子中羧基的反应主要利用它能成酯、成酐、成酰胺的性质。 这里值得特别提出的是将氨基酸转化为叠氮化合物的方法(氨基酸酯 与肼作用生成酰肼,酰肼与亚硝酸作用则生成叠氮化合物)。
Honghe University Prof Guo Ya-li
三、氨基酸的制备
氨基酸的制取主要有三条途径:即蛋白质水解、有机合成和发酵法。 氨基酸的合成方法主要有三种: 1.由醛制备 醛在氨存在下加氢氰酸生成α-氨基腈,后者水解生成 α-氨基酸。 例如:
NH3, HCN
C6H5CH2CHO
C6H5CH2CHCN
反应是定量完成的,衡量的放出 N2,测定N2的体积便可计算出氨基酸 中氨基的含量。
α-NH2反应快,其他氨基不产生干扰。 不适用于脯氨酸
核酸及DNA思维导图脑图

核酸及DNA核酸核酸(nucleic acid)是以核苷酸为基本组成单位的生物大分子,具有复杂的空间结构和重要的生物学功能组成碱基(base)DNAATCG RNAAUCG碱基的酮基和氨基可以形成酮-烯醇互变异构体或氨基-亚氨基互变异构体,为形成氢键形成提供结构基础嘌呤的N-9原子或嘧啶的N-1原子连接核糖核糖(ribose)有β-D-核糖和β-D-2'-脱氧核糖之分脱氧核糖的化学稳定性优于核糖核苷(nucleoside)是碱基与核糖的缩合反应产物,核糖的C-1'原子和嘌呤的N-9原子或嘧啶的N-1原子形成了β-N-糖苷键天然情况形成反式构象核酸衍生物核苷酸ATP和GTP可以环化形成环腺苷酸(cAMP)和环鸟甘酸(cGMP)细胞信号传导过程中的第二信使,具有调控基因表达的作用辅酶1(NAD+)辅酶2(NADP+) 黄素腺嘌呤二核苷酸(FAD)辅酶A(CoA)是生物氧化体系的重要组成成分,传递质子或电子发挥重要作用碱基衍生物6-巯基嘌呤(6-MP) 阿糖胞苷(araC) 5-氟尿嘧啶(5-FU)干扰肿瘤核苷酸代谢,抗肿瘤磷酸二酯键DNA是多个脱氧核糖核苷酸聚合而成的线性生物大分子,脱氧核糖核苷酸之间是通过3’5’-磷酸二酯共价键连接方向DNA、RNA均为5‘→3’方向核酸的一级结构人们把RNA的核苷酸和DNA的脱氧核苷酸从5‘→3’的排列顺序定义为核酸的一级结构长度短于50个核苷酸的核酸片段称为寡核苷酸DNA的空间结构与功能DNA的二级结构是双螺旋结构DNA由两条多聚脱氧核苷酸链组成反向平行的右手螺旋一条链5‘→3’自上而下一条链5‘→3’自下而上直径2.37nm,螺距3.54nm互补碱基对AT两个氢键,CG三个氢键碱基对平面与螺旋结构的螺旋轴近乎垂直每一个螺旋有10.5个碱基对,每两个相邻碱基对之间的旋转角度为36两条多聚脱氧核苷酸链的亲水性骨架将互补碱基对包埋在内部两个碱基对平面重叠产生了碱基堆积作用与蛋白质螺旋对比双螺旋结构的多样性左手螺旋Z型-DNA右手螺旋B型-DNA相对湿度降低后仍稳定A型-DNADNA的多链结构Hoogsteen氢键含有三个碱基的C+GC平面,其中C+G之间是以Hoogsteen氢键结合的DNA三链结构的生成条件富含嘧啶的单恋环境为酸性嘧啶与双链中的嘌呤形成Hoogsteen氢键端粒(telomere)真核生物染色体3‘-端是一段高度重合的富含GT的片段可以自身回折形成一个称为G-四链的特殊结构核心是4个鸟嘌呤通过8对Hoogsteen氢键形成功能用来保护端粒的完整性DNA双链经过盘绕折叠形成致密的高级结构正超螺旋(positive supercoil)当盘绕方向与DNA双螺旋方向相同时,其超螺旋结构为正超螺旋,反之为负超螺旋自然状态下主要是负超螺旋封闭环状DNA具有超螺旋结构在大肠杆菌的环状DNA中,平均每200个碱基就有一个负超螺旋线粒体DNA也是具有封闭环状的双螺旋结构真核生物DNA被逐级有序地组装成高级结构DNA→核小体→染色体核酸的理化性质多元酸,具有酸性DNA为线性分子,粘度极大,粘度:RNA<DNA在260nm波长具有最大吸收峰,吸收强度由碱基共轭双键决定,可用作定性、定量的分析A260=1.0对应50ug/ml的双链DNA,40ug/ml的单链DNA,20ug/ul的寡核苷酸DNA变性(DNA denaturation)某些极端的理化条件可以断裂DNA双链互补碱基对之间的氢键以及破坏碱基堆积力,使一条DNA双链解离成为两条单链DNA的增色效应(hyperchromic effect)DNA解链过程中,包埋在双螺旋结构内部的碱基得以暴露,在260nm的吸光度增加解链温度(Tm)紫外吸光度的变化(△A260)达到最大变化值的一半时所对应的温度被定义为DNA的解链温度影响因素DNA越长Tm越高GC含量越高Tm越高离子浓度越高Tm越高复性与退火复性(renaturation)两条解离的DNA互补链可以重新互补配对形成DNA双链,恢复原来的双螺旋结构退火(annealing)热变性的DNA经缓慢冷却后可以复性但若变性后立即冷却至4度,则被固定至单链状态RNA的空间结构与功能mRNA特点占比最小,种类最多,寿命最短,半衰期最短真核生物mRNA的5’-端有帽结构5‘帽结构(5'-cap structure)大部分真核细胞mRNA的5’-端都有一个反式7-甲基嘌呤-三磷酸核苷(m7Gppp)的起始结构该结构可以与一类帽结合蛋白的分子结构形成复合体有助于维持mRNA的稳定性,协同mRNA从细胞核向细胞质转运,促进核糖体和翻译起始因子结合真核生物mRNA的3‘-端有多聚腺苷酸尾结构多聚腺苷酸尾/多聚尾(poly-tail)真核生物mRNA的3’-端是一段由80~250个腺苷酸连接而成的多聚腺苷酸结构与帽功能类似hnRNA细胞核内的初级转录产物为hnRNA,含有许多交替相隔的外显子(exon)和内显子(intron),外显子是构成mRNA的序列片段,内含子是非编码序列mRNA的核苷酸序列决定蛋白质的氨基酸序列一条成熟的真核mRNA包括5‘非翻译区5’帽结构到核苷酸序列中的第一个AUG(起始密码子)编码区(可读框ORF)起始密码子到终止密码子(UAA,UAG或UGA)3‘非翻译区可读框下游到多聚A尾tRNA转运RNA作为蛋白质合成的底物——氨基酸的载体参与蛋白质合成,为合成中的多肽链提供活化氨基酸特点微量,分子量最小稀有,稀有碱基最多特定的空间结构三叶草结构“三环一柄”(二级结构)靠近5‘端的是DHU环,靠近3’端的为TΩC环,位于上方的茎为氨基酸臂倒“L”型(三级结构)3‘端连接着氨基酸所有tRNA的3’端都是以CCA三个核苷酸结束的tRNA的反密码子能够识别mRNA的密码子rRNA核糖体RNA是细胞中含量最多的RNA,rRNA与核糖体蛋白结合形成核糖体三个重要结合部位A位结合氨酰-tRNA的氨酰位P位结合肽酰-tRNA的肽酰位E位释放已经卸载了氨基酸的tRNA排出位其余RNA及功能催化小RNA(核酶)催化特定RNA降解,在剪切修饰中有重要作用核仁小RNA(snoRNA)定位于核仁,参与rRNA的加工核小RNA(snRNA)参与真核细胞mRNA的成熟过程,切除内含子胞质小RNA(scRNA)引导含有信号肽的蛋白质进入内质网进行合成siRNA 降解外源mRNA,维持基因组稳定microRNA与mRNA结合,抑制或降解mRNA,调控生长发育piRNA调控基因沉默InRNA长非编码RNA协助基因调控circleRNA结合miRNA,解除基因抑制,提高基因表达水平。
高清版新课标高中生物思维导图
过程
光反应 暗反应
场所,条件 物质变化 能量变化
实质、意义
影响光合作用 的因素及应用
内部因素 外界因素
叶面积指数 叶龄 光照强度 温度 二氧化碳浓度 必需矿质元素
水
ATP的主要来源
概念
有氧呼吸
方式
比较
无氧呼吸
实质
意义
影响呼吸作用 的因素及应用
内部因素 环境因素
遗传因素 温度 氧气浓度 CO2浓度
含水量
DNA
分类 RNA
功能
糖类
元素 种类及作用
脂质
元素 种类及作用
有氧呼吸主要场所 光合作用的场所
线粒体 叶绿体
双层膜 细胞器
对来自内质网的蛋白质 进行加工、分类和包装
高尔基体
增大膜面积,与蛋白质、脂质 和糖类的合成有关,蛋白质 的运输通道
维持渗透压,使细胞膨胀
内质网 液泡
单层膜 细胞器
含有多种水解酶,可 分解细胞器和病毒
染色质
结构 功能
遗传物质的载体
是遗传信息库,是细胞代谢和遗传的控制中心
细胞膜 细胞壁
细胞的基 本结构
2/20
细胞骨架
组成 蛋白质纤维组成的网状结构
作用
在真核中维持细胞形态; 保持细胞内部结构的有序性
细胞质基质
成分
水、无机盐、脂质、糖类、 氨基酸、核苷酸和多种酶
状态 呈不断流动的胶质状
作用 活细胞代谢的主要场所
保护、物质交换、能量转换、 信息传递等;提供酶的附着位点; 使细胞内区域化
功能
生物膜系统
研究意义 实验:体验制备细胞膜的方法
纤维素和果胶 成分
保护和支持作用 功能
第04讲+蛋白质与核酸(精讲课件)-备战2024年高考生物一轮复习考点帮(新教材新高考)

这个侧链基团用R表示。各种氨基酸的区别在于R
基的不同。
HO
C C OH
羧基
R
侧链基团
考点2 蛋白质的基本组成单位—氨基酸
【特别提醒】 (1)氨基、羧基、R基的正确书写格式:—NH2、—COOH、—R(千万不要忘记在 原子团前面加“—”)。 ②结构通式及氨基和羧基不同表达形式的辨别
(2)部分氨基酸分子中含有一个以上的氨基或羧基,多出来的氨基或羧基位于R 基上。
(2023·黑龙江八校联合体高三联考)下图中甲是组成乙或丙的基本单位(单体)。下
列相关叙述错误的是( B )
A.如果甲中的m是U,则甲一定是丙的基本单位 B.如果甲中的m是G,则甲一定是乙的基本单位 C.如果甲中的a是脱氧核糖,则甲物质聚合成的大分子物质可以分布于线粒体和叶 绿体中 D.如果甲中的a是核糖,则甲物质聚合成的大分子物质可以分布于细胞核和细胞质
核糖
腺嘌呤(A),鸟 嘌呤(G),胞嘧 啶(C),尿嘧啶 (U)
考点5 核酸的组成、结构和功能
5、核酸的多样性和特异性 (1)多样性 4种核苷酸的数量不同和排列顺序的多样化。 (2)特异性 通过DNA指纹获得遗传信息的根本原因:生物的遗传信息储存在DNA分子中, 而且每个个体的DNA的脱氧核苷酸序列各有特点。
4、蛋白质结构多样性的原因 氨基酸的种类、数目和排列顺序不同,肽链的数目、盘曲、折叠方式及
其形成的空间结构千差万别。 每一种蛋白质分子都有与功能相适应的独特结构。如果结构改变,就可
能会影响其功能。
考点3 蛋白质的结构及其多样性
题型剖析
(2022·福建百校联考)科学研究发现,细胞内普遍存在被称为分子伴侣的一类蛋白 质,该类蛋白质能够识别并结合不完整折叠或装配的蛋白质,帮助这些多肽正确折 叠、转运或防止它们聚集,其本身不参与最终产物的形成(如下图),在生物体内发
核酸知识点总结图

核酸知识点总结图一、核酸的结构1. 核苷酸的结构核苷酸是核酸的基本组成单元,包括磷酸基团、五碳糖和碱基三部分。
在DNA中,糖是脱氧核糖;在RNA中,糖是核糖。
碱基分为嘌呤碱基和嘧啶碱基两类,嘌呤碱基有腺嘌呤(A)和鸟嘌呤(G),嘧啶碱基有胸腺嘧啶(T)(在DNA中)和胸腺嘧啶(U)(在RNA中)以及胞嘧啶(C)。
核苷酸是碱基和五碳糖的糖苷化产物,碱基与糖通过N-糖苷键相连。
2. 核酸的二级结构DNA的二级结构是由两股互补的链以双螺旋形式相互缠绕而成,肝氏结构为DNA最常见的二级结构形态。
RNA的二级结构更为多样,可以形成双股RNA结构和多股RNA结构。
具体的二级结构形式有很多,如折叠、打结、环形等。
3. 核酸的三级结构DNA的三级结构通常是一个肝氏螺旋形态,即多个二级结构相互缠绕而成。
RNA的三级结构呈现出多样性,可以形成复杂的空间结构,包括各种结构域和RNA酶等。
通过多种非共价键作用形成具有特定功能的特殊结构。
4. 结构特点(1)DNA的碱基配对规律:腺嘌呤与胸腺嘧啶之间通过三个氢键结合;鸟嘌呤与胞嘧啶之间通过两个氢键结合。
这种碱基配对规律保证了DNA在复制和转录时能够准确地传递遗传信息。
(2)RNA具有自身稳定性差的特点,易受酶的降解。
所以RNA的寿命相对较短。
二、核酸的功能1. 存储生物遗传信息核酸作为生物体内基因的物质基础,能够存储生物遗传信息,包括生物体形态、生长发育和功能表型等各种信息。
DNA分子中的基因序列编码了遗传信息,通过遗传物质的传递和表达,决定了生物个体的遗传特征。
2. 指导蛋白质的合成DNA通过转录合成RNA,再通过翻译合成蛋白质,这是中央法则的基本过程。
在这个过程中,DNA编码的遗传信息被复制和转录成RNA,再通过翻译转化成蛋白质。
蛋白质是生物体内最重要的功能分子,通过蛋白质的合成和活性发挥对生物体内各种生理过程的调控作用。
3. 调控生物体的生长和发育核酸通过编码蛋白质来控制生物体的生长和发育过程。
高中化学4.3蛋白质和核酸课件新人教版选修5 (1)

1.蛋白质为什么具有两性? 提示 蛋白质结构中有—NH2、— COOH。 2.蛋白质的盐析和变性对蛋白质的性质有何影响? 提示 盐析使蛋白质的溶解性减弱,但不影响化学性质 ;变性使蛋 白质的活性丧失。 3.蛋白质的颜色反应是物理变化,还是化学变化? 提示 化学变化。
探究一
探究二
名师精讲
1.蛋白质的水解 在酸、 碱或酶的作用下,肽键断裂,碳原子连接羟基,氮原子连接氢原子。
一
二
一、氨基酸
1.分子结构 氨基酸可看作是羧酸分子中烃基上的 H 被氨基取代后的产物,天然蛋 白质水解产生的氨基酸全为 α-氨基酸,其通式可写为 。
一
二
2.常见的氨基酸 俗名 结构简式 甘氨酸 H2N—CH2—COOH
丙氨酸 谷氨酸 苯丙氨酸
系统命名 氨基乙酸 α-氨基丙酸 2-氨基1,5-戊二酸 α-氨基苯丙 酸
天然蛋白质仅由碳、氢、氧、氮四种元素组成 ④ 氨基酸和蛋白质 Shp-2 B.②③ C.③④ D.①④
解析 :Shp-2 是蛋白质,故应为高分子化合物,且水解最终产物为氨基酸, ①②正确;天然蛋白质除含 C、H 、O、N 外还含有 S、P 等元素,③ 错;氨基 酸与蛋白质中都同时含有 —NH2 与— COOH,故不仅能与碱反应,也能与酸 反应,④错。 答案 :A
一
二
练一练 2
下图表示蛋白质分子结构的一部分,当蛋白质发生水解反应时,断裂的 键是( )
A.①② C.②
B.③ D.①②③④
解析 :蛋白质是氨基酸中氨基和羧基脱水形成肽键而形成,则蛋白质发 生水解反应时,是从肽键中断开“C—N”键。 答案 :C
一
二
练一练 3
中国科学家已找到白血病的致病元凶——蛋白质 Shp-2。下列关于蛋 白质 Shp-2 说法正确的是( ①它是高分子化合物 都只能与碱反应 A.①② ) ② 在一定条件下能水解最终生成氨基酸 ③
核酸和蛋白质的生物合成143页PPT

16、业余生活要有意义,不要越轨。——华盛顿 17、一个人即使已登上顶峰,也仍要自强不息。——罗素·贝克 18、最大的挑战和突破在于用人,而用人最大的突破在于信任人。——马云 19、自己活着,就是为了使别人过得更美好。——雷锋 20、要掌握书,莫被书掌握;要为生而读,莫为读而生。——布尔沃
END
核酸和蛋白质的生物合成
•
6、黄金时代是在我们的前面,而不在 我们的 后面。
•
7、心急吃不了ቤተ መጻሕፍቲ ባይዱ汤圆。
•
8、你可以很有个性,但某些时候请收 敛。
•
9、只为成功找方法,不为失败找借口 (蹩脚 的工人 总是说 工具不 好)。
•
10、只要下定决心克服恐惧,便几乎 能克服 任何恐 惧。因 为,请 记住, 除了在 脑海中 ,恐惧 无处藏 身。-- 戴尔. 卡耐基 。
思维导图在生物化学教学中应用

思维导图在生物化学教学中应用发表时间:2016-04-29T10:14:51.580Z 来源:《心理医生》2015年11期供稿作者:张雪莲[导读] 白城医学高等专科学校吉林白城 137000)在生物化学教学实践中,传统的课堂教学方式忽视了学生是学习主体,学生成为被动接受的知识容器,严重扼杀了学习主动性和创造精神。
张雪莲(白城医学高等专科学校吉林白城 137000)【中图分类号】R3 【文献标识码】A 【文章编号】1007-8231(2015)11-0236-02在生物化学教学实践中,传统的课堂教学方式忽视了学生是学习主体,学生成为被动接受的知识容器,严重扼杀了学习主动性和创造精神。
学生不能较好地辨别和建构概念与命题框架,死记硬背大量的化学代谢与化学反应,知识存储处于零星状态,没有形成知识网络。
学习过程中只重视模仿性做题,缺乏深入理解生物化学中的概念、规律,知识提取较难,仅靠课堂传授的知识是远远不能满足学生需要的。
因此,课堂教学要与时俱进,不仅要授之与鱼,更要授之与渔。
课堂教学要将以知识为中心转变为以能力中心,使学生自己学会学习,思维导图[1]可实现这一目标。
1.思维导图的制作思维导图可以手工制作,也可借助计算机运用各类思维导图软件。
现在制作思维导图的软件很多,非常容易掌握,不仅教师可以灵活使用,学生也可以很快掌握软件的使用,为学习提供了新的工具。
但限于学校条件,在课堂上只探讨如何让学生体验思维导图的手工制作。
1.1 制作准备几张白纸和多种颜色笔。
1.2 制作步骤⑴把主题画在纸的中央。
主题可用关键字和图像来表示。
关键字是表达核心意思的字或词,应该是具体的、有意义的。
这有助于我们进行回忆。
⑵考虑次主题,也就是在上一层主题下的延伸。
⑶在次主题后,罗列更为细节的要点。
这时不要强迫自己用一定的顺序或结构来罗列要点。
任何一个要点出现时,可用关键字的方式表达,并和最相关的次主题连接起来。
⑷总体联系:各级分支绘制完成后,要用箭头将相关的各个分支连接,使其相互联系,增强思维导图的整体性[2]。
