金刚石 石墨 碳60第二课时 (2)
《课题1 金刚石、石墨和C60》第2课时示范课教学课件【人教版化学九年级上册】

2C + O2 2CO
铺底色
圈画
1.氧气充足、燃烧充分时,碳燃烧生成二氧化碳。
2.氧气不充足、燃烧不充分时,碳燃烧生成一氧化碳。
注意:描述物质的化学性质时,要注意条件哦。如碳在常温下化学性质稳定;碳充分燃烧生成二氧化碳;不充分燃烧时则生成一氧化碳等。
碳单质的新结构形态,可在室温下转化为钻石
CO2
SO2
用Q-carbon制造钻石 科学们家从蓝宝石、玻璃或者塑料聚合物等基底材料着手,在其表面涂上一层无定形碳——即没有规则晶体结构的碳单质,然后采用单激光脉冲扫描这层无定型碳约200纳秒。在扫描过程中,碳温度会升至4000 K(约3727 ℃),然后迅速冷却。该操作过程均在恒定压力(大气压)下进行。最终我们会得到薄薄的一层Q-carbon,研究人员也能控制工艺过程,得到介于20 nm到500 nm之间任意厚度的碳层。 研究人员还可通过选择不同的基底材料以及改变激光脉冲的宽度来控制冷却的速度,从而在Q-carbon内部产生钻石结构。
金刚石 石墨 C60
这些单质都是由碳元素组成的,元素的化学性质与原子结构的最外层电子数的关系最密切,因此这些物质的化学性质在很大程度上是相似的。
A
还原性
先撤导气管
C + CO2 2CO Nhomakorabea通过本节课的学习,我们知道了:
课题1金刚石、石墨和C60
第2课时
01
常温下,碳的化学性质稳定
02
03
碳的还原性
古字画
档案材料
充分燃烧:
不充分燃烧:
碳与氧气反应
2C + O2 2CO
C + O2 CO2
人教版化学九年级上册6.1《金刚石、石墨和C60》(第二课时)教案

人教版化学九年级上册6.1《金刚石、石墨和C60》(第二课时)教案一. 教材分析《金刚石、石墨和C60》是人教版化学九年级上册的一章内容,主要介绍了金刚石、石墨和C60的结构、性质和用途。
本节课的内容是该章节的第二课时,主要通过实验和探究活动,让学生深入理解金刚石、石墨和C60的异同点,以及它们在现实生活中的应用。
二. 学情分析九年级的学生已经具备了一定的化学基础知识,对物质的基本性质和实验操作有一定的了解。
但是,对于金刚石、石墨和C60的详细结构和性质,以及它们的应用领域,可能还存在一定的疑问。
因此,在教学过程中,需要引导学生通过实验和探究活动,自主获取知识,提高他们的实践能力和解决问题的能力。
三. 教学目标1.理解金刚石、石墨和C60的结构和性质;2.掌握金刚石、石墨和C60的用途和应用领域;3.培养学生的实验操作能力和观察能力;4.提高学生的自主学习和合作学习的能力。
四. 教学重难点1.金刚石、石墨和C60的结构和性质;2.金刚石、石墨和C60的用途和应用领域;3.实验操作和观察能力的培养。
五. 教学方法1.实验法:通过实验让学生直观地观察金刚石、石墨和C60的结构和性质;2.问题驱动法:引导学生提出问题,通过实验和探究活动寻找答案;3.小组合作法:分组进行实验和探究活动,培养学生的合作能力;4.讨论法:引导学生进行讨论,分享自己的观点和经验。
六. 教学准备1.实验室器材:显微镜、石墨、金刚石、C60样品等;2.教学课件:PPT或者黑板;3.教学参考资料:相关的实验报告和论文。
七. 教学过程1.导入(5分钟)通过展示金刚石、石墨和C60的图片,引导学生思考它们之间的关系和特点。
2.呈现(10分钟)介绍金刚石、石墨和C60的结构和性质,以及它们在现实生活中的应用。
通过实验和观察,让学生直观地了解它们的异同点。
3.操练(15分钟)学生分组进行实验,观察金刚石、石墨和C60的结构和性质。
教师巡回指导,解答学生的问题。
《金刚石、石墨和C60》精品课件(创新版) 第二课时

谢谢观赏!
碳的还原性还表现在其他反应中,不仅可用于炼铜, 也可用于冶炼其他金属,如碳可用于炼铁。
2Fe2O3+3C
高温
4Fe+3CO2↑
在烧得很旺的炉子里(产生CO2)添上大量的新煤 后,温度为什么会降低?并且还容易有煤气生成? 在高温条件下 碳还能使二氧化碳转变成一氧化碳。
C+CO2
高温
2CO(吸收热量)
性质决定用途
可燃性——燃烧
还原性——冶炼金属
课堂小结
本节课我们主要学习了碳的化学性质,知道常温下碳的化学
性质不活泼,但在高温条件下碳能和氧气以及某些氧化物反应, 还分析得出了还原反应与还原性的概念。
课堂练习
1.下列现象中属于化学变化的是( D )
A.活性炭吸附有色、有毒的气体
B.铅笔把字迹留在纸上
件下制造出纳米级金刚石粉末。该成果发表在世界最权威的《科 学》杂志上,立即被科学家们高度评价为“稻草变黄金”。下列 说法不正确的是( B ) A.金刚石属于非金属单质 B.制造金刚石的过程中碳元素的化合价发生了改变 C.CCl4是一种化合物
D.制造金刚石的变化属于化学变化
6.用木炭还原氧化铜的实验如图。
演示实验
反应物、生成物、条件都已确定,你能写出反 【现象】澄清石灰水变浑浊, 试管内粉末中有红色物质生成。 应的化学方程式吗?
2CuO+C
高温
【结论】分析得出产物为二氧 2Cu +CO2↑ 化碳、铜。
注意事项
①酒精灯加网罩可使火焰集中并提高温度; ②试管口要略向下倾斜; ③装置的气密性要好;
④实验结束时,先撤出导气管,然后再熄灭酒精灯(防止澄清石灰水倒
流入热的试管致使试管破裂),待试管冷却后再把试管内的粉末倒在纸 上(防止生成的铜再被氧化成氧化铜)。
金刚石、石墨、C60(第2课时碳的化学性质)_刘琴

师:那位同学解开其中的“奥妙”——钻石恒久远,一颗永流传。
生:(抢答)碳具有稳定性。
生:应该是常温下具有稳定性。
师:不错,那请你们思考我们的周围还有那些事例能说明碳具有稳定性?请各组将你们从互联网上搜索的或其他方式总结的结果加以326592&cl=2&nc=1&lm=mp;fm=index&pv=&z=0&ie=utf-8&word=%E4%BC%98%E7%BE%8E%E5%8F%A4%E7%94%BB
二祖:排空气法收集……
三组:二组观点有问题,密度与空气密度接近,不易用此法收集,建议气球收集
/s?tn=98012088_1_hao_pg&ie=utf-8&bs=%E5%8F%8D%E5%BA%94%E7%89%A9%E7%9A%84%E9%87%8F%E4%B8%8D%E5%90%8C%2C%E7%94%9F%E6%88%90%E7%89%A9%E4%B8%8D%E5%90%8C&f=8&rsv_bp=1&wd=%E5%AF%86%E5%BA%A6%E4%B8%8E%E7%A9%BA%E6%B0%94%E5%AF%86%E5%BA%A6%E6%8E%A5%E8%BF%91%EF%BC%8C%E4%B8%8D%E6%98%93%E7%94%A8%E6%AD%A4%E6%B3%95%E6%94%B6%E9%9B%86%EF%BC%8C&rsv_n=2&rsv_sug3=1&rsv_sug4=94&inputT=1063
课题1 金刚石、石墨和C60(第二课时)教案

课题1 金刚石、石墨和C60(第二课时)教案[教学目标]:1、知识目标:(1)了解碳的各种单质的物理性质差异很大,却有相同的化学性质。
(2)了解单质碳在常温下的稳定性和高温时的化学活动性。
(3)掌握单质碳的可燃性和还原性。
(4)初步了解化学反应伴随的能量变化。
2、能力目标:培养学生观察、记忆、思维等能力。
3、情感目标:通过碳的充分与不充分燃烧,形成辨证地看待问题和分析问题的良好习惯。
[教学重点]:碳单质的可燃性和还原性。
[教学难点]:碳单质跟氧化铜、二氧化碳发生的化学反应。
[教学方法]:启发式教学。
[学法指导]:1、让学生学会化学实验的一般思路:原料装置操作现象。
2、引导学生学会解决问题的方法:提出问题,查阅资料,互相讨论,结论应用。
[课时]:1[课型]:新知识课。
[教学手段]:展示实物、投影仪。
[教学过程]:(复习提问)金刚石和石墨都是碳的单质,其物理性质有哪些显著的差异?为什么?其化学性质是否相同?(板书)一、单质碳具有相同的化学性质的原因是:因为它们都是有碳原子构成的。
(引入)金刚石、石墨的物理性质有很大的差异,但其化学性质却是相同的。
这节课,我们共同来研究单质碳的化学性质。
二、单质碳的化学性质:(展示)古代字画的图片(提问)古代的墨汁主要成份是碳单质,用墨汁写的字年深日久,纸都泛黄了,但字仍不褪色,为什么?(板书)1、常温下单质碳的化学性质稳定。
(讲解)在点燃或高温条件下,碳能跟许多物质反应。
现在大家一起回忆木炭在氧气中燃烧有哪些现象?其产物是什么?写出反应的化学方程式。
(小结)木炭在氧气中燃烧发生白光,放出热量,生成一种能使澄清石灰水变浑浊的气体(二氧化碳)。
化学方程式:C + O 2 CO 2 (提问)燃烧很旺的煤炉,封上封火盖时,可以观察到什么现象?为什么呢?写出反应的化学方程式。
(小结) 炉口有蓝色火焰产生,这是一氧化碳在燃烧。
封上封火盖前,氧气充足,碳燃烧生成了二氧化碳;封上封火盖后,氧气不充足,单质碳燃烧产生了CO 。
金刚石、石墨和C60(二)教案

课题1 金刚石、石墨和C60【第2课时】【教学目标】1.了解碳的重要化学性质2.能认真观察实验现象,掌握碳还原氧化铜的实验。
3.了解还原反应及碳的用途。
【教学重点】碳单质的化学性质【教学难点】碳和某些氧化物反应【教学方法】实验探究——分析——归纳【教具准备】木炭粉、氧化铜粉末、澄清石灰水、铁架台、网罩、试管、带导管的塞子、酒精灯。
【教学过程】[图片引入]为何我国古代一些名作历经几百年甚至几千年而依然色泽鲜艳不褪色?[设问]木制电线杆埋入地下部分的表面被稍稍烧焦碳化,为什么呢?[教师讲解并板书]二、碳的化学性质1、碳在常温下化学性质不活泼(稳定)。
[设问]若升高温度,又如何呢?[回顾提问]木炭在氧气中充分燃烧的现象和化学方程式[学生]木炭剧烈燃烧发出白光,放出热量, 生成一种能使澄清石灰水变浑浊的气体。
C+O 2===CO 2[板书]2、在高温下,碳的化学活动性增强。
(1)可燃性C+O 2===CO 2(充分燃烧)2C+O 2===2CO (不充分燃烧)[设问]利用木炭的这一性质可以作什么用途?[学生]作燃料[板书]用途1:作燃料(利用可燃性)[活动探究 实验6-2]木炭与氧化铜的反应[学生交流]实验现象:黑色粉末逐渐变成的红色固体,澄清石灰水变浑浊。
分析得到产物为二氧化碳和铜。
[板书]实验现象:黑色粉末逐渐变成的红色固体,澄清石灰水变浑浊。
化学方程式:C+CuO===Cu+CO2注意事项:a 、网罩的作用——集中火焰,提高温度。
b 、实验完毕时,应先将导气管从石灰水中拿出,再撤掉酒精灯[设问]从微观结构上看CuO 转变为Cu ,发生了什么变化,是谁导致了这种变化?[学生讨论] CuO 转变为Cu 失去了氧,是碳夺走了CuO 中的氧。
[讲解并板书] 点燃 点燃 点燃 点燃(2)还原性还原反应:含氧化合物里的氧被夺去的反应。
木炭具有还原性,作还原剂。
用途2:冶炼金属高温工业上炼铁:2Fe2O3+3C===4Fe+3CO2[总结并板书]一、碳的化学性质1.常温下:化学性质稳定高温下:化学性质活泼2、可燃性3、还原性二、还原性、还原反应[作业]课本P109 2、4、6。
新九年级化学上册第六单元课题1金刚石石墨和C60第二课时课件

操作步骤:
①气密性检验 ②装药 ③如图连接固定装置 ④点燃酒精灯加热 (观察现象) ⑤实验结束:先将导管 移出小试管,再停止 加热。
我会分析
—还原性
高温
C+2CuO===2Cu+CO2
CuO:我的氧不见了, 氧化性
我终于被还原了!
C: 我能夺取别人的氧,能把 还原性
别人还原,我的还原性很
厉害吧!
A.稳定性 B.吸附性
C.可燃性 D.还原性
5.下列各组物质中,具有可燃性 的一组物质是( C )
A. H2和O2 C. C和H2
B. H2和CO2 D. C和O2
请思考
有等质量的两份碳,分别燃烧生成
CO2和CO,消耗氧气的质量比
是 2:1
,生成CO2和CO
的质量比是 11 :7
。
有一包黑色粉末由氧化铜和木 炭混合而成,将其装入试管中加热 片刻,有红色物质生成,称剩余固 体质量,发现减轻了2.2g,则参加 反应的氧化铜和木炭的质量分别为 多少?
金刚石、石墨和C60
(第二课时)
金刚石失踪案
17世纪40年代,阳光明媚的夏日,意大利佛 罗伦萨科学院,几位院士围坐在花园中的一个 石桌旁,用放大镜观察、研究一小颗珍贵的金 刚石。当金刚石所处的位置与凸透镜的焦点吻 合时,金刚石折射出耀眼的强光,院士们纷纷 调头躲避。当他们回过头时,却意外地发现闪 闪发光的金刚石不见了。人们寻遍了周围的草 坪,一无所获。金刚石不翼而飞,成了一宗离 奇的失踪案,载入了佛罗伦萨科学院的大事记。
【作业】
《前沿》:
69页、70页
谢谢合作
木炭在氧气中不充分燃烧时,生成一氧化碳
方程式:
点燃
2C+O2===2CO
6.1 金刚石、石墨、C60(第二课时)--九年级化学上册教案
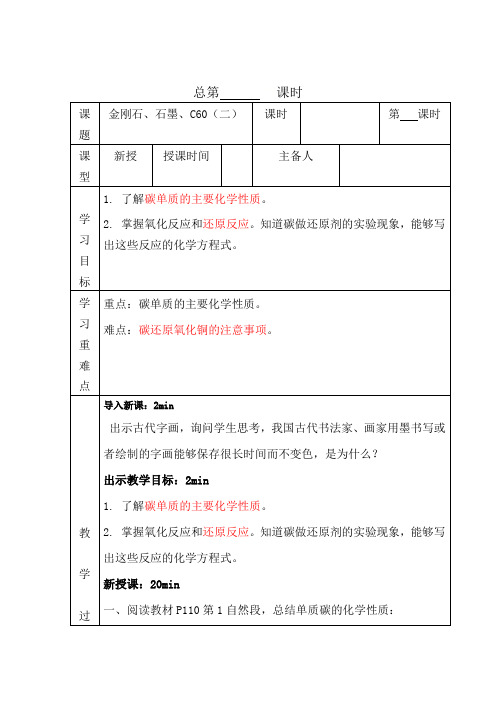
总第课时课题金刚石、石墨、C60(二)课时第课时课型新授授课时间主备人学习目标1. 了解碳单质的主要化学性质。
2. 掌握氧化反应和还原反应。
知道碳做还原剂的实验现象,能够写出这些反应的化学方程式。
学习重难点重点:碳单质的主要化学性质。
难点:碳还原氧化铜的注意事项。
教学过导入新课:2min出示古代字画,询问学生思考,我国古代书法家、画家用墨书写或者绘制的字画能够保存很长时间而不变色,是为什么?出示教学目标:2min1. 了解碳单质的主要化学性质。
2. 掌握氧化反应和还原反应。
知道碳做还原剂的实验现象,能够写出这些反应的化学方程式。
新授课:20min一、阅读教材P110第1自然段,总结单质碳的化学性质:程教学过程1、稳定性:常温下,碳的化学性质()。
2、可燃性:在点燃的条件下,单质碳能在氧气里燃烧,放出热量,故碳可做燃料。
氧气充足时,碳充分燃烧,化学方程式为:氧气不充足时,碳燃烧不充分,化学方程式为:3、还原性:实验现象:化学方程式:注意事项:1、酒精灯加网罩的目的是()2、大试管管口要(),防止()3还原反应:4、用途:()。
如还原氧化铁,化学方程式为训练展示:8min1、钻石恒久远,一颗永流传”这句广告词被美国《广告时代》评为20世纪的经典广告之一。
该广告能体现的钻石的性质是( )A.硬度大B.不能导电C.化学性质稳定D.熔点低2.下列说法中,正确的是( )A.金刚石、石墨都是由碳原子构成的,都很硬B.单质碳具有还原性C.用活性炭可除去硬水中的氯化钙杂质D.木炭燃烧时吸收大量的热3.下列关于碳单质的说法中正确的是()A.C60的相对分子质量为720B.金刚石、石墨和C60都由碳元素组成,结构相同C.木炭具有还原性,常温下可以将氧化铜中的铜还原出来D.石墨很软,不能用于制石墨电极1、在木炭还原氧化铜的实验中:(1)反应开始后,在盛澄清石灰水的试管中观察到的现象是_________________,. 2.用木炭还原氧化铜的实验如下图。
化学人教版九上精美课件:6.1.2 金刚石、石墨和C60(2)

2.高铁被誉为中国“新四大发明”之一。高铁动车与电路连接的是石墨电刷,
它没有体现出石墨具有的性质是( C )
A.导电性
B.滑腻感
C.还原性
D.稳定性
随堂演练
3.两份质量相等的木炭,一份燃烧全部生成二氧化碳,一份燃烧全部生成一氧
化碳,则两份木炭燃烧消耗氧气的质量比是( B )
A.1:2
B.2:1
C.3:8
单质碳的化学性质
知识梳理
常温下,碳的化学性质不活泼
炭化的木电线杆
铁路枕木被炭化
古书画保存至今
如果温度升高,碳的活泼性又如何呢?
知识梳理
你还记得木炭在氧 气中燃烧的现象吗?
单质碳的化学性质
木炭在氧气中的燃烧
知识梳理
碳与氧气的反应
实验现象:发出白光,生成能使澄清石灰水变浑浊的气体,放出热量。
知识梳理
单质碳的化学性质
还原反应
还原反应:含氧化合物中氧被夺去的反应。
木炭是使氧化铜还原为铜 的物质,它具有还原性
得氧
高温
C + 2CuO
2Cu + CO2 ↑
失氧
单质碳的化学性质
知识梳理
还原反应
应用1:碳的还原性可用于冶金工业。 如:焦炭可以把铁从它的氧化物矿石里还原出来。
高温
3C + 2Fe2O3
6.已知碳在一定条件下能够与氧化铜发生反应,该反应的化学方程式为:
C+2CuO 高温 2Cu+CO2↑,其中碳在该反应中作为( A )
A.还原剂 B.氧化剂 C.助燃剂
D.催化剂
课堂小结
课题1 金刚石、石墨和C60
第2课时
常温下,碳的化 学性原性
《金刚石、石墨和C60》第二课时参考教案

课题1 金刚石、石墨和C 60(第2课时)活动一:观察与思考师:(引言)我国是一个具有悠久历史文化的文明古国,在灿烂的历史长河中,涌现出了一大批赫赫有名的书画家,他们留下的传世之作经过几百甚至上千年的洗礼,流传于世幸存下来的已不多见,成为我国文化中的瑰宝。
下面两幅就是古代留下的珍贵字画。
请看屏幕:【屏幕投影】学生欣赏二幅古代字画图片:明代:董其昌 (学生对这两幅字画品头论足,交头接耳,赞不绝口。
)生:老师,我有一个问题,为什么明代董其昌的作品历经四百余年而依然笔峰清晰,漓江烟雨图保存到现在色泽鲜艳而不褪色呢?师:问得好!你们知道古代一些书法家、画家是用什么来书写或绘制字画的? 生:(异口同声)墨汁!师:墨汁又是用什么制成的?生:用炭黑来制成的。
活动二、交流师:炭黑的主要成分是碳。
古代字画保存几百年乃至上千年,纸或布都已开始腐烂破损,但墨色依然不变,这说明碳具有怎样的化学性质?猜猜看。
生:我想碳单质的化学性质应该是很稳定的。
师:都同意他的观点吗?(大部分同学点头同意)生:(立即反驳)不对,木炭可以在氧气中燃烧,怎么说它的化学性质稳定呢?我觉得应该是活泼的。
国画:漓江烟雨图(元朝)师;其实,这两位同学说得都有道理,但不够准确。
生:我们说碳单质的化学性质是稳定还是活泼应该是有条件的。
在常温下,碳的化学性质不活泼。
但在点燃条件下,碳能与氧气发生化学反应。
师:这位同学分析正确,我们在分析问题得出结论时,一定要注意将条件和结论有机地联系起来,辩证地看待问题,才不至于犯以偏概全的错误。
关于碳单质常温下的稳定性,在实际生活中有着广泛的应用。
你知道还有哪些应用吗?大家讨论。
生:我发现铁路枕木和街上木制电线杆表面都被烧焦碳化,我想这也是利用了碳单质常温下的稳定性。
枕木和木制电线杆表面碳化处理后,经得起日晒、风吹和雨打,都不容易起变化,可以有效地防止木头腐烂,虽然表面变得黑不溜秋,也不美观,但增加了使用的年限。
师:那么是什么决定了碳在常温下化学性质不活泼呢?元素的化学性质与元素原子结构中的哪部分关系最为密切?生:(齐声)最外层电子数。
金刚石、石墨和C60教案(第二课时)教案

课题1 金刚石、石墨和C60教案(第二课时)教学目标1、了解碳在常温与高温下,表现出不同的化学性质2、通过阅读,实验验证,分析对比等,掌握单质碳的化学性质--—稳定性,可燃性,还原性;3、通过阅读,实验验证,分析对比等,掌握单质碳的化学性质--—稳定性,可燃性,还原性;重点和难点重点:碳的化学性质难点:不同条件下碳的反应产物判断教学设计一、引入1、出示一幅字画照片,古代用墨书写,绘制的字画,虽经历数百年仍不褪色;又如金刚石琢磨而成的钻石,经风吹,日晒,雨淋仍不发生变化。
2、能否从碳原子的结构来分析为什么碳单质在常温下具有较为稳定的化学性质?3、你能否举出其他生活中的例子,说明碳在常温下的化学性质比较稳定。
4、木制的电线杆在埋入地下前,将其表面烧焦的目的是什么?5、碳单质是否在其它条件下,也保持稳定的化学性质呢?二、新授1、和氧气的反应------可燃性充分燃烧:C+O2点燃CO2不充分燃烧:2C+O2点燃2CO讨论:前面我们学习过一氧化碳是污染空气的一种气体,一氧化碳是有毒的气体,那么在冬天生火取暖时,特别是用煤炉取暖的时候,要注意什么问题?2、和某些氧化物反应----还原性碳除了有可燃性,在高温下还体现出还原性。
演示实验:碳还原氧化铜引导学生观察实验装置、操作及实验现象。
分析:反应中,碳得氧生成二氧化碳,氧化铜失氧生成铜。
化学方程式为:2CuO+C2Cu+CO2↑分析:物质跟氧发生的反应叫做氧化反应。
上述反应中,木炭夺取氧化铜里的氧使氧化铜失去了氧,变成了单质的铜。
这种含氧化合物里的氧被夺去的反应,叫做还原反应。
通常把夺取氧的物质叫还原剂;提供氧的物质叫氧化剂。
木炭在上述反应里是还原剂,它们具有还原性,使氧化铜还原成单质铜。
单质碳的还原性还可用于冶金工业。
例如,焦炭可以把铁从它的氧化物矿石里还原出来。
2Fe2O3+3C4Fe+3CO2↑三、巩固练习一、填空题。
1、碳原子的核电荷数为____,核外电子数为____,原子结构示意图为____。
金刚石、石墨与C60 PPT教学课件(第二课时) 人教版

•
5、心情就像衣服,脏了就拿去洗洗,晒晒,阳光自然就会蔓延开来。阳光那么好,何必自寻烦恼,过好每一个当下,一万个美丽的未来抵不过一个温暖的现在。
•
6、无论你正遭遇着什么,你都要从落魄中站起来重振旗鼓,要继续保持热忱,要继续保持微笑,就像从未受伤过一样。
•
7、生命的美丽,永远展现在她的进取之中;就像大树的美丽,是展现在它负势向上高耸入云的蓬勃生机中;像雄鹰的美丽,是展现在它搏风击雨如苍天之魂的翱翔中;像江河的美丽,是展现在它波涛汹涌一泻千里的奔流中。
•
10、有些事想开了,你就会明白,在世上,你就是你,你痛痛你自己,你累累你自己,就算有人同情你,那又怎样,最后收拾残局的还是要靠你自己。
•
11、人生的某些障碍,你是逃不掉的。与其费尽周折绕过去,不如勇敢地攀登,或许这会铸就你人生的高点。
•
12、有些压力总是得自己扛过去,说出来就成了充满负能量的抱怨。寻求安慰也无济于事,还徒增了别人的烦恼。
•
8、有些事,不可避免地发生,阴晴圆缺皆有规律,我们只能坦然地接受;有些事,只要你愿意努力,矢志不渝地付出,就能慢慢改变它的轨迹。
•
9、与其埋怨世界,不如改变自己。管好自己的心,做好自己的事,比什么都强。人生无完美,曲折亦风景。别把失去看得过重,放弃是另一种拥有;不要经常艳羡他人,人做到了,心悟到了,相信属于你的风景就在下一个拐弯处。
1、可燃性
点燃
C + O2 ===== CO2
(O2充足)
现象:①发出白光,②产生大量的 热,③生成的气体能使澄清的石灰 水变浑浊。
案情2介C绍+:O原2 =告点=宫=一燃=某=氧、2化刘CO某碳(诉中O称毒2:不引2充0发0足6巨年)1额月赔27偿日晚案,例原告一家三人在杨
人教版化学九年级上册《金刚石 石墨 C60》碳和碳的氧化物(第2课时)

自主探究
二、碳单质的化学性质
阅读教材110页,思考:
为什么我国书法家用墨写的字画能保存多年不褪色?
因为墨的主要成分是炭黑,碳在常温下化学性质稳定。
归纳总结 化学性质1 常温下碳的化学性质不活泼
既不容易得电 子,又不容易 失电子
温度升高,碳的活泼性增强 点燃条件下,有可燃性 高温条件下,有还原性
温故知新 化学性质2 碳的可燃性
4.待试管冷却倒出粉 末的目的:
探究实验
现
开始加热时导管口有无色气体放出,过一会 黑色粉末变为红色,石灰水变浑浊
象
开始加热时,试管中的空气因受热体积膨胀而
分
逸出,温度达到高温时,木炭与氧化铜反应,
析
生成的铜为红色固体,另一生成物为CO2
化学方程式:
合作交流
化学性质3 碳的还原性
物质和氧发生的化学反应叫做氧化反应。
目前世界上人工制得的最薄的材料,下列有关石墨片说法错误
的是( )
B
A.石墨片是一种单质
B.石墨片与C60是同种物质,具有导电性 C.在一定条件下,石墨片可还原氧化铜
D.石墨片在氧气中完全燃烧的产物是CO2
3.在木炭还原氧化铜的实验中:
(1)反应开始后,盛澄清石灰水的试管中观察到的现象是 ____澄__清__石___灰__水__变__浑___浊,说明反应中有______C生O成2 ,被加热的试管
本节课你学会了哪些知识? 收获了什么方法? 还有什么疑惑吗?
课堂达标
1.下列关于碳单质的说法中正确的是( C ) A.C60是由碳原子构成的 B.金刚石、石墨和C60都由碳元素组成,结构相同 C.木炭具有还原性,高温下可以将氧化铜中的铜还原出来 D.石墨很软,不能用于制石墨电极
人教版化学九年级上册《金刚石、石墨和C60》精品(第2课时)

的( B )
A、可燃性 B、还原性 C、稳定性 D、来源广
典型例题
3·木炭燃烧的产物是( C )
A.一定是.CO B.一定是CO2 C.可能是CO,也可能是CO2 D.一定是CO和CO2的混合物
小结: 1、得氧被氧化,发生氧化反应;失氧被还原,发生还原反应; 2、能提供氧的物质具有氧化性,作氧化剂,
能夺得氧的物质具有还原性,作还原剂。
一、单质碳的化学性质
生产和应用
a.焦炭炼铁 利用焦炭可以把铁矿石(假设含氧化铁)中的铁还
原出来。单质碳高温下也可以与二氧化碳反应生成
ቤተ መጻሕፍቲ ባይዱ
一氧化碳。 2Fe2O3+3C
2CuO + C
碳: 得到(或夺取)氧 发生氧化反应 具有还原性 用作还原剂
高温 2Cu +
氧化铜
CO2↑
失去(或提供)氧
发生还原反应
具有氧化性
用作氧化剂
一、单质碳的化学性质
含氧化合物中的氧被夺去的反应,叫还原反应。 (1)木炭使氧化铜还原成铜,其具有还原性。 (2)氧化铜使碳氧化成二氧化碳,其具有氧化性
高温
4Fe+3CO2↑
b.碳还原二氧化碳
C+CO2
高温
2CO
课堂小结
一、碳的化学性质 1.常温下:化学性质稳定 2.高温下:化学性质活泼
(1)跟氧气反应——可燃性 (2)跟某些氧化物反应——还原性
典型例题
1·2002年底江苏省考古专家对“泗水王陵”进行保护性挖掘,在考古的过程中发现
在棺室外围的土层中有厚厚的一层一千多年前的木炭,这表明木炭具有( C )
【知识学习】《金刚石、石墨和C60》教案(第2课时)

《金刚石、石墨和C60》教案(第2课时)本资料为woRD文档,请点击下载地址下载全文下载地址一、教学目标知识技能了解碳单质的化学性质,并能根据碳单质的性质认识其不同用途。
过程方法通过实验事实明白碳的化学性质的活泼和稳定都是相对的。
情感态度价值观通过对碳的不同单质有不同用途的探讨探究,体会性质决定用途,用途反映性质的学科思想。
【教学重点】物质的结构、性质和用途之间的相互关系。
碳与氧气及某些氧化物的反应——碳的可燃性和还原性。
【教学难点】碳与某些氧化物的反应。
二、学生认知分析对于碳单质的化学性质,学生有一定的了解,如在学习氧气的性质时,已经知道木炭可以在空气中或氧气中燃烧;对于碳单质的化学性质在常温下比较稳定,其实也易于接受,因为在学生的经验中,已知古代书法作品保存千年也不易褪色,以及档案材料都用碳素墨水书写等。
三、教学过程环节一、延续情境,引入新课教师活动学生活动设计意图上节课我们一起到卖“炭”翁的商店逛了逛,了解了碳单质的一些物理性质,今天我们继续到卖“炭”翁去看看有什么新的发现。
倾听,思考。
本节课的教学课堂仍设置在这个商店里。
学生在逛商场的过程中,经过讨论、探究,轻松、愉快的达到各项学习目标。
这种活泼开放的教学环境,给学生以新奇感,能激发学生学习兴趣,同时使学生感到,化学和生活是紧紧联系在一起的。
环节二、分析实例、总结性质教师活动学生活动设计意图【提问】我们首先来看看商店的镇店之宝---两幅古代字画吧,墨迹历经千年也不变色,大家讨论以下,为什么字画能保存这么长时间呢?【总结】用来书画的墨是由碳元素组成的,常温下碳[Xmy1] 的化学性质稳定。
回答:保存妥善,墨迹稳定。
设置一个这样的内容,既激发学生的民族自豪感,又培养了学生的创新意识,同时引出了碳的还原性,碳和氧化铜在高温条件下生成铜和二氧化碳。
【板书】二、碳的化学性质1.常温下稳定【讲述】碳并不是任何时候都这么稳定,出示图片:寒冷的冬天用烧火来取暖。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
碳的还原性
木炭是使氧化铜还原为铜的物质,木炭具 有还原性,作还原剂。
单质碳的还原性可用于冶金工业,如工业上 用焦炭还原氧化铁
3C+ 2Fe2O3 高温 4Fe + 3CO2↑
HOME
稳定性: 常温下,碳的化学性质不活泼
碳 的 化 学 性 质
C + O2 点燃 CO2(氧气充足)
可燃性 2C + O2 点燃 2CO(氧气不充足)
在温度升高的情况下,碳能跟很多物质发生 化学反应。
2.碳跟氧气的反应 C + O2 2C + O2
点燃
CO2
点燃
(充分燃烧) (不充分燃烧)
2CO
有毒
碳具有可燃性
燃烧 条件
化学方程式
结论
启示
在氧气 中充分 C + O 2 燃烧
点燃
CO2
燃烧不 点燃 2C + O2 2CO 充分
碳具有 书写方程 可燃性, 式一定要 条件不 注明反应 同,燃 条件,冬 第二课时
碳的化学性质
用碳笔画的古字画
1、常温下碳的稳定性
我国古代一些书法家、画家用 墨(用炭黑等制成)书写或绘制的 字画能够保存很长时间而不变色, 这是为什么呢?
这是因为在常温下,碳的化学性质 不活泼,碳受日光照射或与空气、水分 接触,都不容易起变化的缘故。
生活小运用【思考】 例如把木制的电线杆在埋入地下前, 将其表面烧焦,其目的是什么?
目的就是为了让电线杆不易腐烂,可 以保存久一些。
可是碳可以在氧气中燃烧, 怎么可以说它化学性质稳定呢?
请思考:
什么决定碳 在常温下性质 不活泼 ,而在高 温下性质活泼 呢? 元素的化学 性质和元素原 子结构中哪部 分关系最为密 切?
最外层电子数!
碳原子的最外层 电子数为4,既 不容易得到电子, 也不容易失去电 子,所以常温下 碳的化学性质比 较稳定
2CuO + C
现象
高温
2Cu + CO2↑
结论 有二氧化碳生成
澄清石灰水变成白色浑浊
黑色粉末变成红色物质
有铜生成
我会分析 观察这个方程式,看看有什么特点?
高温
C + 2 CuO
2 Cu + CO2
CuO:我的氧不见了,我终于被还原了! C:我能夺取别人的氧,能把别人还原,我的 还原性很厉害吧
含氧化合物里的氧被夺去的反应,就 叫做:还原反应。 例如:氧化铜失去氧变成铜单质, 我们就说它被还原了。
还原性 C + 2 CuO
高温
2 Cu + CO2
3.碳跟某些氧化物的反应(还原性)
C与CuO的反应
现象: 澄清的石灰水变浑浊, 试管内的黑色粉末变 成红色。
图上罩网罩了吗?
1.火焰上罩网罩的作用 是什么? 2.实验结束时,为什么 要先从石灰水中取出导 气管再熄灭酒精灯?
1. 因为木炭与氧化铜反 应的温度要求较高,用网 罩使火焰集中,提高温度。 2. 防止石灰水倒吸入热 的试管使试管炸裂。
