最新第一电离能教案知识讲解
高中化学 第1章 第3节 原子结构与元素性质 第1课时 电离能及其变化规律教案 高二化学教案

第1课时电离能及其变化规律[学习目标定位] 1.知道原子结构与元素性质间的关系规律。
2.正确理解元素电离能的含义及其变化规律,会用电离能的概念分析解释元素的某些性质。
一、元素的电离能及其变化规律1.元素第一电离能的概念与意义(1)概念:①电离能:气态原子或气态离子失去一个电子所需的最小能量。
符号:I,单位:kJ·mol-1。
②逐级电离能:第一电离能:处于基态的气态原子失去一个电子转化为正一价气态离子所需要的能量叫做第一电离能。
元素第一电离能符号:I1。
第二电离能:气态正一价离子再失去一个电子成为气态正二价离子所需的能量叫做第二电离能;第三电离能和第四、第五电离能依此类推。
通常情况下,第一电离能小于第二电离能小于第三电离能……(2)意义:可以衡量元素的原子失去一个电子的难易程度。
第一电离能数值越小,原子越容易失去一个电子;第一电离能数值越大,原子越难失去一个电子。
2.元素第一电离能变化规律(1)每个周期的第一种元素的第一电离能最小,最后一种元素的第一电离能最大,即一般来说,随着核电荷数的递增,元素的第一电离能呈增大趋势。
(2)同一族,从上到下第一电离能逐渐减小。
1.电离能数值的大小主要取决于原子的核电荷数、原子半径及原子的核外电子排布。
(1)核电荷数、原子半径对电离能的影响①同周期元素具有相同的电子层数,从左到右核电荷数增大,原子半径减小,I1总体上有增大的趋势。
碱金属元素的I1最小,稀有气体元素的I1最大。
②同主族元素从上到下,原子半径增大起主要作用,元素的I1逐渐减小。
(2)核外电子排布对电离能的影响某原子或离子具有全充满、半充满或全空时的电子排布时,电离能较大。
如第ⅡA族元素、第ⅤA族元素比同周期左右相邻元素的I1都大,原因是第ⅡA族元素最外层n s2全充满,第ⅤA族元素最外层n p3半充满,比较稳定。
各周期稀有气体元素的I1最大,原因是稀有气体元素的原子各轨道具有全充满的稳定结构。
第一电离能同主族的变化规律

第一电离能同主族的变化规律说到化学,很多人可能会觉得有些枯燥。
但其实,化学里的很多规律和变化,跟我们日常生活中的许多事情都息息相关。
今天,我们来聊聊第一电离能(也就是把一个电子从原子里搞出来所需要的能量)在同一主族元素中的变化规律。
这可是个既有趣又实用的知识点哦!1. 认识第一电离能先来个小科普吧。
第一电离能,顾名思义,就是把一个原子中的一个电子给“驱逐”出去时所需要的能量。
这个能量的大小和很多因素有关,比如原子内部的电子排布、原子的核电荷等等。
简单来说,电离能越大,说明原子的“护卫”越严,那个电子就越难被挤走。
2. 同主族元素的电离能变化规律好啦,进入正题了。
我们主要讲讲同一主族的元素第一电离能是怎么变化的。
说到主族,大家可以把它理解成周期表上竖着一列的元素。
这些元素有很多共同的性质,比如化学反应的特点,当然,第一电离能也是一样的。
2.1 由上而下逐渐减小如果你看周期表的那一列,应该会发现,从上往下的元素,第一电离能是逐渐降低的。
这是为什么呢?比如说,周期表的第一主族(就是那一列的最左边,氢、锂、钠、钾什么的),你会发现,氢的第一电离能非常高,而钾的则相对较低。
为啥?因为原子从上往下逐渐变大,电子离原子核越来越远,这样就需要的电离能就减少了。
就像你在沙发上躺着,离电视遥控器远了,自然就不想动了;电离能低了,电子自然也更容易被“抛弃”。
2.2 原子半径与电离能除了原子离核远,另一个原因就是原子半径增大。
原子半径的增大,导致核对外层电子的吸引力减小,电子就更容易被剥离。
这就好比你在宽敞的客厅里,你的狗狗跑来跑去,你自然不容易抓住它;但如果在狭小的房间里,你就容易把它抓住。
原子半径大,电子就“跑”得更远,抓住它们的难度也就小了。
3. 具体例子为了让大家更容易理解,我们可以举几个实际的例子。
比如,我们在主族元素中,氢、锂、钠、钾这些元素的电离能是逐渐降低的。
具体来说:3.1 氢元素氢元素只有一个电子,原子核对这个电子的吸引力非常强,因此它的第一电离能很高。
第一电离能教案教学内容

(2)元素第一电离能的意义:可以衡量元素的原子失去一个电子的难易程度。第一电离能数值越小,原子越容易失去一个电子;第一电离能数值越大,原子越难失去一个电子。
(3)气态一价正离子再失去一个电子成为气态二价正离子所需的最低能量叫做第二电离能,第三电离能和第四、第五电离能可以类推。由于原子失去电子形成离子后,若再失去电子会更加困难,因此同一原子的各级电离能之间存在如下关系:I1<I2<I3
第一电离能教案
课 题
元素第一电离能的周期性变化
备课时间
2015年 月 日
上课时间
2015 年 月 日
主备
田立国
审核
欧立国
教
学
目
标
知识技能
1.能表述元素第一电离能的含义。
2.熟知元素原子半径、元素的第一电离能的周期性变化规律。
3.能用元素的第一电离能说明元素的某些性质。
过程与方法
讲练结合
情感价值
体会科学家探索的过程
③具有全充满、半充满及全空的电子构型的元素稳定性较高,其电离能数值较大。如稀有气体的电离能在同周期元素中最大,N为半充满、Mg为全充满状态,其电离能均比同周期相邻元素大。
3.电离能的应用
(1)根据电离能数据,确定元素核外电子的排布。如Li:I1≪I2<I3,表明Li原子核外的三个电子排布在两个能层上(K、L能层),且最外层上只有一个电子。
【作业布置】
【课后反思】
2.元素第一电离能变化规律
(1)第一电离能的变化趋势如下图所示:
【学生活动】观察分析上图,同学们自己总结元素第一电离能的变化规律
①对同一周期的元素而言,碱金属元素的第一电离能最小,稀有气体元素的第一电离能最大;从左到右,元素的第一电离能在总体上呈现从小到大的变化趋势,表示元素原子越来越难失去电子。
元素第一电离能的周期性变化讲解

2.下列说法不正确的是( A ) A.同族元素,随着n的增加,I1逐渐增大 B.通常情况下,电离能I1<I2<I3 C.同周期元素,随着核电荷数的增加,I1 呈增大趋势
D.电离能越小,元素的金属性越强
作业
课本P29:1、3、4、9 练习册P10:4、5、11、13、19 预习P22:共价化合物、离子化合物、 化合价、离子键、共价键 小测准备:电子排布式等 阅读P22:化学史话
再失去的电子是能级较低的电子,且失 2.去In与电元子素后最离高子价所、带原正子电最荷外对层电电子子吸数引力
更“N交强界a流,2限+,与从为镁讨而:相易论使I邻形3电n”电成1钠离(离mM为能a能g易x越2)+相形,来差3成而越很N不大a大是。+,的M而地g3不方+?是 In
多级电离能数据
元素 In Na I1 496 I2 4 562
电离能/ I3 6 912 kJ·mol-1 I4 9 543
I5 13 353 I6 16 610 I7 20 114
Mg 738 1 451 7 733 10 540 13 630 17 995 21 703
Al 578 1 817 2 745 11 575 14 830 18 376 23 293
顺序排列
①K Na Li
Li >Na> K
②B C Be N N> C >Be> B
③He Ne Ar
He >Ne > Ar
④ Na Al S P P >S >Al> Na 4.练习册P9:例3 、4自主迁移3、4
多级电离能 (In )
1.各级电离能大小
I1 I2 I3 In In1
第一电离能 电负性教案
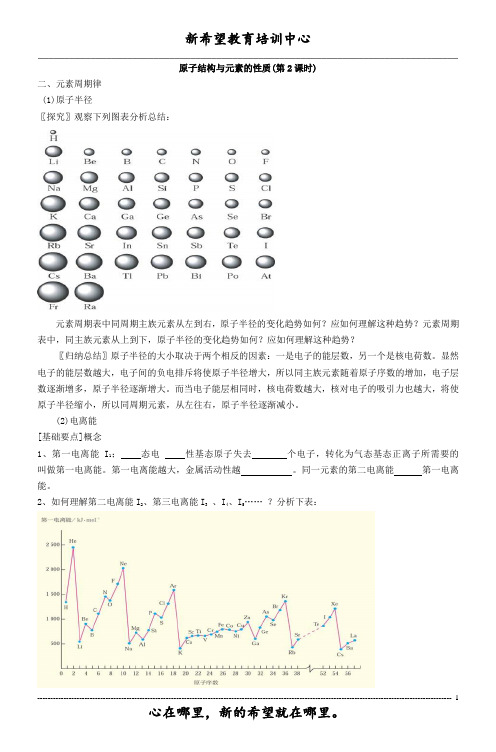
原子结构与元素的性质(第2课时)二、元素周期律(1)原子半径〖探究〗观察下列图表分析总结:元素周期表中同周期主族元素从左到右,原子半径的变化趋势如何?应如何理解这种趋势?元素周期表中,同主族元素从上到下,原子半径的变化趋势如何?应如何理解这种趋势?〖归纳总结〗原子半径的大小取决于两个相反的因素:一是电子的能层数,另一个是核电荷数。
显然电子的能层数越大,电子间的负电排斥将使原子半径增大,所以同主族元素随着原子序数的增加,电子层数逐渐增多,原子半径逐渐增大。
而当电子能层相同时,核电荷数越大,核对电子的吸引力也越大,将使原子半径缩小,所以同周期元素,从左往右,原子半径逐渐减小。
(2)电离能[基础要点]概念1、第一电离能I1;态电性基态原子失去个电子,转化为气态基态正离子所需要的叫做第一电离能。
第一电离能越大,金属活动性越。
同一元素的第二电离能第一电离能。
2、如何理解第二电离能I2、第三电离能I3、I4、I5……?分析下表:〖科学探究〗1、原子的第一电离能有什么变化规律呢?碱金属元素的第一电离能有什么变化规律呢?为什么Be 的第一电离能大于B ,N 的第一电离能大于O ,Mg 的第一电离能大于Al ,Zn 的第一电离能大于Ga ?第一电离能的大小与元素的金属性和非金属性有什么关系?碱金属的电离能与金属活泼性有什么关系? 2、阅读分析表格数据:Na Mg Al 各级电离能(KJ/mol)496 738 578 45621415 1817 6912 7733 2745 9543 10540 11575 13353 13630 14830 16610 17995 18376 201142170323293为什么原子的逐级电离能越来越大?这些数据与钠、镁、铝的化合价有什么关系? 数据的突跃变化说明了什么? 〖归纳总结〗1、递变规律周一周期同一族第一电离能从左往右,第一电离能呈增大的趋势从上到下,第一电离能呈减小趋势。
第一电离能同主族的变化规律

第一电离能同主族的变化规律嗨,大家好!今天咱们来聊聊化学里一个很有趣的概念——第一电离能,尤其是它在同主族元素中的变化规律。
别担心,我会用最简单的语言来讲解,希望你们能跟上我的节奏,一起深入探讨!1. 什么是第一电离能?首先,啥是第一电离能?其实,第一电离能就是把一个原子最外层的一个电子从它的原子里移走所需要的能量。
简单点说,就是你想把一个电子赶走,你得花多少钱。
越贵,说明这个电子越难被赶走。
2. 同主族元素的第一电离能规律好啦,搞懂了电离能的基本概念,我们来看看它在同主族元素中的变化规律。
2.1 第一电离能的总体趋势当我们沿着周期表的主族往下看,第一电离能的趋势是怎样的呢?一般来说,随着主族的增加,即从上到下,第一电离能是逐渐降低的。
这是什么原因呢?主要是因为,元素的原子半径变大了,外层电子离原子核越来越远,自然受到的吸引力就小了,所以比较容易被挤走。
2.2 影响电离能的因素除了原子半径,还有别的因素吗?当然有!比如说,原子核的正电荷也很关键。
原子核越大,正电荷越强,理论上应该更能吸引电子。
但是,实际情况是,虽然原子核的正电荷增加了,但电子离原子核更远了,电离能还是会降低。
这就像你想把一只远在高空的飞鸟抓住,难度会比你抓一只在地上的鸟大得多。
3. 实际例子为了让大家更容易理解,我来举几个例子。
3.1 氢、氦和锂比如氢、氦和锂这三个元素,氢的电离能是最高的,因为它只有一个电子,离原子核也很近。
氦的电离能虽然比氢稍低,但仍然比锂高。
为什么?因为氦的两个电子更紧密地围绕在原子核周围,不容易被移走。
而锂则不同,随着主族的增加,锂的第一电离能就低得多了,因为它的电子离原子核更远了。
3.2 钠、钙和镁再看钠、钙和镁。
钠的第一电离能比钙和镁高。
这是因为钠比钙和镁少一个电子层,电子离原子核比较近,抓得紧。
钙和镁由于多了一个电子层,外层电子距离原子核更远,电离能自然也低一些。
4. 总结好啦,今天我们通过几个例子和规律,一步一步揭开了第一电离能的神秘面纱。
高中化学必修一电离教案

高中化学必修一电离教案
一、概念引入
1. 以真空紫外灯对水进行电解实验,观察电解过程中氢气和氧气的产生。
2. 引导学生思考,电解水是如何产生氢气和氧气的?是不是水分子发生了电离?
二、电离的概念
1. 引导学生通过实验现象,理解电离的概念:电离是指分子或原子中的一个或多个电子脱
离原子而形成离子的过程。
2. 解释电离的类型:原子电离和分子电离。
三、电离的过程
1. 原子电离的过程:原子吸收能量后,电子从内层轨道跃迁到外层轨道,形成激发态原子,再脱离原子形成离子。
2. 分子电离的过程:分子受到能量激发后,成为高能量态,电子被脱离形成离子。
四、电离的影响
1. 电离在化学反应中的作用:电离是化学反应发生的基础,例如酸碱中电离产生的离子反应。
2. 电离在生物体系中的影响:生物体系中的细胞内外也发生着电离现象,控制细胞内离子
的浓度对生命活动至关重要。
五、练习与讨论
1. 讨论电离对化学反应的重要性。
2. 计算电离释放的能量。
六、实验
设计实验观察电解水过程,探究电离在实际应用中的作用。
七、课堂小结
通过本节课的学习,学生对电离的概念和过程有了更深入的理解,为之后学习相关知识打
下基础。
元素性质的递变规律第一电离能电负性PPT学习教案

s区 ⅠA、ⅡA族 ns1、ns2
p区 ⅢA~ⅦA族和0族元素 ns2np1~6
活泼金属(H除
外)
大多为非金属
d区 ds
ⅢB~ⅦB族和Ⅷ 族
ⅠB、ⅡB族
(n-1)d1~10ns1
~2
(n-1)d10ns1~2
区 镧系和锕系
f区
过渡元素 过渡元素
第22页/共55页
思考:为什么s区、d区、ds区的元素 都是金属(除H外)?
符号 单位:
第31页/共55页
概念应用
1、已知M(g)-e- →M +(g)时所需最低
738 KJ·mol-1
能量为738 KJ,则M元素的
2、已知Na元素的I1=496 KJ·mol-1,则Na (g) -e-
I1=
→Na
+(g)
时所需最低能.量为
496 KJ
.
第32页/共55页
问题探 究一
元素的第一电离能大小与原子 失去电子能力有何关系?
参考解答案释:同主族元素从上到下,随核电荷数增大
,原子半径逐渐增大,原子核对核外电子的吸引力 逐渐减小,原子失电子能力逐渐增大,第一电离能 逐渐减小。
第38页/共55页
4、同一周期第一电离能最小的是碱金 属元素,最大的是稀有气体元素。为什 么?
友情提示:从他们的原子外围电子排布式和 原子结构的特点思考。
d区元
ⅢB~ⅦB族和Ⅷ族元
素
素
它们的价层电子构型是(n-1)d1~10ns1~2
,最后1个电子基本都是填充在倒数第二层
(n-1)d轨道上的元素,位于长周期的中部
。这些元素都是金属,常有可变化合价,称
为过渡元素。它包括ⅢB~ⅦB族和Ⅷ族元
【精品】第一电离能教案(可编辑

第一电离能教案
------------------------------------------作者
------------------------------------------日期
系:I1<I2<I3
2.元素第一电离能变化规律
(1)第一电离能的变化趋势如下图所示:
【学生活动】观察分析上图,同学们自己总结元素第一电离能的变化规律
①对同一周期的元素而言,碱金属元素的第一电离能最小,稀有气体元素的第一电离能最大;从左到右,元素的第一电离能在总体上呈现从小到大的变化趋势,表示元素原子越来越难失去电子。
②同主族元素,自上而下第一电离能逐渐减小,表明自上而下原子越来越易失去电子。
③具有全充满、半充满及全空的电子构型的元素稳定性较高,其电离能数值较大。
如稀有气体的电离能在同周期元素中最大,N为半充满、Mg为全充满状态,其电离能均比同周期相邻元素大。
3.电离能的应用
(1)根据电离能数据,确定元素核外电子的排布。
如Li:I1≪I2<I3,表明Li原子核外的三个电子排布在两个能层上(K、L能层),且最外层上只有一个电子。
(2)根据电离能数据,确定元素在化合物中的化合价。
如K:I1≪I2<I3,表明K 原子易失去一个电子形成+1价阳离子。
(3)判断元素的金属性、非金属性强弱:I1越大,元素的非金属性越强;I1越小,元素的金属性越强。
【课堂小结】1.电离能数值的大小主要取决于原子的核电荷数、原子半径及原子的电子构型。
2.第一电离能的变化规律
【作业布置】【课后反思】。
教学课件第一电离能(标准)

第一电离能与元素性质的关系
02
CHAPTER
第一电离能的变化规律
随着原子序数的增加,第一电离能呈现先增加后减小的趋势。
总结词
在元素周期表中,随着原子序数的增加,元素的电子排布变得更加稳定,使得原子更难失去电子,因此第一电离能逐渐增加。然而,当原子序数达到一定值时,随着电子的增加,电子之间的排斥作用增强,使得原子更容易失去电子,第一电离能开始减小。
第一电离能的大小与原子的电子排布、原子半径、有效核电荷数等因素有关。
什么是第一电离能
第一电离能可用于判断元素的金属性或非金属性强弱,第一电离能越大,金属性越弱,非金属性越强。
第一电离能可用于预测元素在化合物中的表现形式,如金属元素通常以正价态出现,非金属元素通常以负价态出现。
第一电离能可用于研究元素周期表中元素的性质变化规律,如同一周期从左到右第一电离能呈增大趋势,同一主族从上到下第一电离能呈减小趋势。
详细描述
第一电离能随原子序数的变化
随着电子排布的增加,第一电离能呈现先增加后减小的趋势。
总结词
随着电子的增加,电子之间的排斥作用逐渐增强,使得原子更难失去电子,第一电离能逐渐增加。然而,当电子排布达到一定值时,电子之间的排斥作用过强,使得原子更容易失去电子,第一电离能开始减小。
详细描述
第一电离能随电子排布的变化
目前对于第一电离能的研究主要集中在单元素体系,对于多元素体系的研究相对较少,需要进一步拓展研究范围。
当前研究主要集中在实验测量和理论计算两个方面,但实验数据和理论预测存在一定偏差,需要进一步研究和验证。
第一电离能的大小受到多种因素的影响,如原子所处的电子构型、原子序数、同位素效应等,需要更深入的理论模型来描述这些因素。
高中化学电离能教案

高中化学电离能教案
一、教学目标:
1. 理解电离能的概念及重要性;
2. 掌握电离能的计算方法;
3. 能够分析电子亲和能的实验数据。
二、教学重点:
1. 电离能的定义和计算方法;
2. 电离能与原子结构的关系;
3. 电离能与元素的位置在周期表中的关系。
三、教学过程:
1. 引入:通过实验或示意图引入电离能的概念,让学生了解电离能的重要性和意义。
2. 概念讲解:解释电离能的概念及其在原子结构中的作用,引导学生理解电离能与电子亲
和能之间的关系。
3. 计算方法:讲解电离能的计算方法,并通过实例演示如何计算不同元素的电离能值。
让
学生掌握计算电离能的技巧。
4. 实验分析:引导学生分析电子亲和能的实验数据,让他们理解电离能与元素性质的关系。
5. 总结:总结电离能的概念和计算方法,强调电离能在化学研究中的重要性。
四、教学评估:
1. 复习练习:布置相关的练习题,让学生巩固所学知识;
2. 课堂讨论:组织学生讨论电离能对元素性质的影响,鼓励他们发表自己的见解;
3. 小测验:进行一次小测验,测试学生对电离能的理解程度。
五、作业布置:
1. 完成相关的练习题;
2. 阅读相关资料,进一步了解电离能的应用领域。
六、课后反思:
通过本节课的教学,学生对电离能的概念和计算方法有了更深入的理解,能够独立计算不同元素的电离能值,并理解电离能在化学领域的重要性。
同时,也要不断反思和改进教学方法,以提高教学效果。
【原创课件】第一电离能 电负性gyb

电负性的大小顺序为 D>C>B>A 。
9、在下列空格中,填上适当的元素符号。 (1) 在第3周期中,第一电离能最小的元素
是 Na ,第一电离能最大的元素是 Ar ; 电负性最小的元素是 Na ,电负性最大的 元素是 Cl 。
(2)在元素周期表中,第一电离能最小的元素
是 Cs ,第一电离能最大的元素是 He ; 电负性最小的元素是 Cs ,电负性最大的 元素是 F 。(不考虑放射形元素!)
三、第一电离能
1、定义:某元素的气态原子失去一个电子形成+1 价气态阳离子所需的最低能量。
2、符号:I1 单位:kJ/mol
M(g) - e– → M+(g)
I1
3、意义: 衡量元素的气态原子失去一个电子的难 以程度
I1 越小 I1 越大
原子越易失去一个电子 原子越难失去一个电子
4、同周期、同主族变化规律 同主族,从上→下, I1↓。 同周期 ,从左→右,I1呈增大趋势。 (ⅡA、ⅤA反常)
并用这些元素的电负性解释对角线规则。
解答:Li、Mg在空气中燃烧 的产物为Li2O、MgO, Be(OH)2、Al(OH)3都是两性 氢氧化物,H3BO3、H2SiO3都 是弱酸。这些都说明“对角线 规则”的正确性。
11、根据周期律对角线规则,金属铍与铝单质及其化合物
的性质相似,又知AlCl3熔沸点较低,易升华,试回答下 列问题:
10、A、B、C、D四种元素,已知A元素是自然界 中含量最多的元素;B元素为金属元素,已知它的 原子核外K、L层上电子数之和等于M、N层电子 数之和;C元素是第3周期第一电离能最小的元素, D元素在第3周期中电负性最大。 (1)试推断A、B、C、D四种元素的名称和符号。 A:O(氧) B:Ca(钙) C:Na(钠) D:Cl(氯)
元素第一电离能的周期性变化 教学设计

《元素第一电离能的周期性变化》教学设计一、教材分析地位和作用:元素第一电离能是元素的一个重要性质,此内容早在人教版(甲种本)中就有,新教材将其纳入《元素性质的递变规律》,使得元素的性质的知识学习更加完整。
本单元的知识内容是《化学2》专题1 第一单元核外电子排布与周期律的深化和拓展。
电离能、电负性是元素的重要性质,也是学习化学键、离子键和共价键的基础。
为有志于进一步深造化学相关专业的学生指导元素化合物知识和化学理论的学习打下坚实的基础。
二、目标分析1、知识与技能:理解第一电离能的概念和随原子序数递增呈周期性变化的规律,理解其本质是核外电子排布的周期性变化的结果。
2、过程与方法:能运用电离能的数据比较元素金属性的强弱,推测原子结构。
培养学生科学推理能力和综合运用知识解决问题的能力3、情感态度与价值观:养成实是求事的科学态度和思辨的科学精神。
三、教学重点难点重点:第一电离能的递变性难点:从电子构型的角度解释第一电离能的递变规律及特殊性四、教学方法1、以思维为核心,开展问题探究:通过分析数据图表,引导学生开展积极的思维活动培养学生科学推理能力。
2、以学生为主体,促进知识内化:通过组织讨论,发挥群体智慧,完成知识构建。
五、教学过程1、知识衔接,引入新课〔教师活动〕引导学生回忆学过的元素主要性质有哪些?他们各有怎样的递变规律?〔学生活动〕元素主要性质有金属性、非金属性、化合价、原子半径。
金属性:同周期从左到右逐渐减小,同主族从上到下逐渐增大;非金属性:同周期从左到右逐渐增大,同主族从上到下逐渐减小;主要化合价:同周期最高正价从+1到+7,负价从中部开始,-4到-1;原子半径:同周期从左到右逐渐减小,同主族从上到下逐渐增大。
〔教师活动〕引出元素的另一性质——第一电离能。
给出概念:气态原子失去一个电子形成+1价气态阳离子所需最低能量。
M(g)-e-→M+(g) 符号I1单位KJ•mol-1指出注意点,配以巩固练习。
第一电离能

目标要求: 能说出元素第一电离能的涵义,能应用
元素的电离能说明元素的某些性质。 本节重、难点: (1)电离能与元素性质的关系 (2)第一电离能的周期性变化
第一电离能
1、含义:气态电中性基态原子失去一个电子转化为气态基 态正离子所需要的最低能量。用符号I1表示,单位: kJ/mol
思 1.原子失去电子时,吸收还是放出能量? 考 2.第一电离能反映了原子得到还是失去电子倾向的大小?
根据电离能数据的突跃式变化,可确定元素常见 化合价。
练习
1.判断下列元素间的第一电离能的大小: Na > K; O < N; N > P; Mg > Al; S < P; Cl < Ar。
2.将下列元素按第一电离能由大到小的顺序排列
①K Na Li
Li >Na> K
②B C Be N
N> C >Be> B
b、第ⅡA元素>ⅢA的元素; N> C >Be> B
H 判断下列元素间的第一电离能的大小:
判断下列元素间的第一电离能的大小:
Kr
判断下列元素间的第一电离能的大小:
②B C Be N 1962年,英国化学家巴特列特将强氧化性的PtF6与O2反应,得到了O2PtF6,考虑到O的第一电离能和Xe相近,他仿照氧化O2的做法, 将PtF6与Xe混合,得到了第一个稀有气体化合物XePtF6。
回眸反思
1、什么是第一电离能? 2、如何比较第一电离能的大小? 3、第一电离能的影响因素有哪些? 4、电离能与元素的性质有什么联系?
作业:
•1、画出碱金属、卤族元素的第一电离能变 化图。
•2、画出第二、三周期元素的第一电离能变 化图。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
【学生活动】观察分析上图,同学们自己总结元素第一电离能的变化规律
①对同一周期的元素而言,碱金属元素的第一电离能最小,稀有气体元素的第一电离能最大;从左到右,元素的第一电离能在总体上呈现从小到大的变化趋势,表示元素原子越来越难失去电子。
②同主族元素,自上而下第一电离能逐渐减小,表明自上而下原子越来越易失去电子。
③具有全充满、半充满及全空的电子构型的元素稳定性较高,其电离能数值较大。
如稀有气体的电离能在同周期元素中最大,N为半充满、Mg为全充满状态,其电离能均比同周期相邻元素大。
3.电离能的应用
(1)根据电离能数据,确定元素核外电子的排布。
如Li:I1≪I2<I3,表明Li原子核外的三个电子排布在两个能层上(K、L能层),且最外层上只有一个电子。
(2)根据电离能数据,确定元素在化合物中的化合价。
如K:I1≪I2<I3,表明K 原子易失去一个电子形成+1价阳离子。
(3)判断元素的金属性、非金属性强弱:I1越大,元素的非金属性越强;I1越小,元素的金属性越强。
【课堂小结】1.电离能数值的大小主要取决于原子的核电荷数、原子半径及原子的电子构型。
2.第一电离能的变化规律
【作业布置】
【课后反思】
数学全真模拟试题八
一、选择题(每小题3分,共15题,45分)
1、设集合M={2|≥x x },N={51|≤≤-x x },则M ∪N =( )
A .{21|≤≤-x x }
B .{52|≤≤x x }
C .{1|-≥x x }
D .{5|≤x x } 2、1+x >2是x >1的( )
A .充分条件
B .必要条件
C .充要条件
D .不充分不必要条件 3、下列四组函数中,有相同图像的一组是( ) A .x x f =)(,2)(x x g =
B .x x f =)(,33)(x x g =
C .x x f sin )(=,)sin()(x x g +=π
D .x x f =)(,x
e x g ln )(=
4、若0)]lg[lg(lg =x ,则5
1-x
=( )
A .100
B .0.1
C .0.01
D .10 5、观察正弦型函数)sin(2ϕ+=wx y (其中w >0,ϕ<2
π
)在一个周期内的图像,可知:w 、ϕ分别为( )
3
π
-
A .w =2,ϕ=
3π B .w =2,ϕ=6π
C .w =21,ϕ=3π
D .w =21,ϕ=6
π
6、已知两点A (1,2),B ()2,5-,且3=,则C 点的坐标为( ) A .)3
5
,32(-
B .
(—8,11) C .(0,3) D .(2,1) 7、若a =(1,3),=(32,2),则a 与的夹角为( ) A .0
30 B .450 C .600 D .900 8、设),2
(
ππ
α∈,已知直线1l :03sin 1cos =+-+ααy x ,直线2l :αsin 1++y x —3=0,则
直线1l 与2l 的位置关系为( )。
