化工原理(第四版)习题解第六章蒸馏
化工原理第六章蒸馏

恒摩尔气流 恒摩尔液流
注意:V不一定等于V′,L不一定等于L′
溶液中两组分的摩尔汽化热相等,即rA rB; 因汽液两相温度不同而传递的热量可忽略; 假定 精馏塔保温良好,其热量损失可以忽略。
三、进料热状态参数q
1.进料热状况的定性分析:
A — — 过冷液体;
B — — 饱和液体;
加料板及其以下 ——提馏段
加料板以上 ——精馏段
间歇精馏:
——只有精馏段, 没有提馏段
第三节 双组分连续精馏的计算与分析
设计型计算: 操作型计算:
一、全塔物料衡算
F、D、W — kmol( A B) h
xF、xD、xW — kmolA kmol( A B) 总物料:F D W
Ln1 温度 易挥发汽化多
Vn yn
气相
液相
yn yn1 xn xn1
Ln1 x n1
Ln xn
n-1 n n+1
塔顶:纯A 塔釜:纯B
Vn1 y n 1
yn+1 tn+1 tn tn-1 xn
G O P
yn
t/℃
xn-1
0
x或y
1.0
加料位置 ——与原料液组成和温度相近的板上进料
240 101.33
pA
pB
0
,kPa ,kPa
101.33 116.9 135.5 155.7 179.2 204.2 40.0 46.0 54.0 63.3 74.3 86.0
0
温度℃
80.1
85
90
95
100
105
110.6 240
pA
0
,kPa
第六章 蒸馏(自化工原理)

汽液相平衡,是指溶液与其上方蒸汽达到平衡 汽液相平衡,是指溶液与其上方蒸汽达到平衡时 平衡时 气液两相间各组分组成的关系。 气液两相间各组分组成的关系。 理想溶液的汽液相平衡服从拉乌尔 拉乌尔(Raoult)定律 定律。 理想溶液的汽液相平衡服从拉乌尔(Raoult)定律。 因此对含有A 组分的理想溶液可以得出: 因此对含有A、B组分的理想溶液可以得出: PA=PAoxA 1a) (6-1a) PB=PBoxB= PBo(1-xA) 1b) (6-1b)
6.2 双组分溶液的气液相平衡
☺ ☺ ☺ ☺ ☺ ☺
6.2.1 理想溶液的气液相平衡 6.2.2 温度组成图(t-y-x图) 温度组成图(t6 . 2 . 3 y -x 图 6.2.4 挥发度与相对挥发度 6.2.5 非理想溶液的汽液相平衡 本节小结
6.2.1 理想溶液的气液相平衡(1)
☺
☺ ☺ ☺ ☺
t → x( y ) x− y
本节小结(2)
☺
☺ห้องสมุดไป่ตู้
☺
☺
2)在一定外压下,纯组分的饱和蒸汽压与外压 在一定外压下, 相等时,液体开始沸腾,其对应的温度称为沸点, 相等时,液体开始沸腾,其对应的温度称为沸点, 可见,外压一定时,纯组分的沸点为一定值。 可见,外压一定时,纯组分的沸点为一定值。 在一定外压下,液体混合物的沸腾温度称为泡点, 在一定外压下,液体混合物的沸腾温度称为泡点, 泡点与混合物的组成有关。 泡点与混合物的组成有关。 (t- y)图上可见 图上可见, 在(t-x-y)图上可见,表示不同组成液体混合物的 泡点温度( x=0到x=1.0)为泡点曲线。 泡点温度(从x=0到x=1.0)为泡点曲线。 在该曲线上,对应x=0(即 =0, =1.0)的温度为 在该曲线上,对应x=0(即xA=0,xB=1.0)的温度为 B组分的沸点;对应x=1.0(即xA=1.0,xB=0) 的温 组分的沸点;对应x=1.0(即 =1.0, 度曲线为A组分的沸点。 度曲线为A组分的沸点。
化工原理 第六章 蒸馏

相同时进行多次部分冷凝和部分汽
化。 精馏条件:塔顶的液体回流和塔 釜的产生的蒸汽回流。
29
t P=定值 t1
t P=定值 t1 t2 t3 1 2 3
xW x1
xF
y1
yF
x(y)
x1
x2 xF x3 y1
y2 y3 x(y)
图6-10 一次部分气化的图
图6-11 多次部分气化和冷凝的示意图
30
V HF 加料板F L’ hF V’ H F+1
L' L q F
L L q F
'
F L V ' V L'
V ' V (q 1)F
41
V F L V F L V (1-q)F F qF L L’ 汽液混合进料
V =V (1 q)F
V’
V’
L’ 冷液进料
p p xA p
0 A 0 B
0 A
0 B
0 B
0 P pB xA 0 0 p A pB
xB 1 x A
——泡点方程
若平衡的气相为理想气体,可用道尔顿分压定律:
0 pA pA yA x P P
yB 1 y A
——汽液两相平衡组成间的关系
0 0 0 pA pA p pB f A (t ) p f B (t ) —露点方程 yA xA 0 0 p p pA pB p f A (t ) f B (t )
3
传质过程或分离操作:物质在相间的转移过程。
蒸馏:将液体混合物部分气化,利用各组分的挥发 度不同的性质以实现分离目的的操作。
易挥发组分(轻组份):沸点低的组分 难挥发组分(重组份):沸点高的组分
【化工原理复习笔记】第六章 蒸馏

蒸馏⏹双组分溶液的气液相平衡拉乌尔定律由溶剂与溶质组成的稀溶液,在一定温度下汽液两相达到平衡时p A=p A o x Ap A:溶剂在汽相中的蒸气分压,kPap A∗:同温度下纯溶剂A的饱和蒸气压,kPax A:溶剂A在液相中的组成(摩尔分数)对于组分Bp B=p B∗x B=p B∗(1−x A)理想溶液的t−y−x关系式➢温度(泡点) — 液相组成关系式x=p−p B∗p A∗−p B∗x:液相中易挥发组分的摩尔分数p:总压,kPap A∗、p B∗:溶液温度t时,纯组分A、B的饱和蒸气压,kPa ➢恒压下t−y−x关系式y=p A∗x p若已知汽液相平衡温度t下的液相组成x,用上式就可求出与x平衡的汽相组成y ➢温度(露点) — 汽相组成关系式将上面两式合并y=p A∗p×p−p B∗p A∗−p B∗双组分理想溶液的汽液两相达到平衡时,总压p、温度t、汽相组成y及液相组成x的4个变量中,只要决定了两个变量的数值,其他两个变量的数值就被决定了。
相对挥发度与理想溶液的y−x关系式挥发度v挥发度是用来表示物质挥发能力大小的物理量,前面已提到纯组分液体的饱和蒸气压能反映其挥发能力。
理想溶液中各组分的挥发能力因不受其他组分存在的影响,仍可用各组分纯态时的饱和蒸气压表示,即挥发度v等于饱和蒸气压p∘v A=p A ov B=p B o相对挥发度α溶液中两组分挥发度之比称为相对挥发度αa=v Av B=p A op B o对于理想溶液,在操作温度范围内,取最低温度的α值与最高温度的α值之几何平均值理想溶液的汽液相平衡方程式非理想溶液汽液相平衡非理想溶液中各组分的蒸气分压不服从拉乌尔定律,他们对拉乌尔定律发生的偏差有正偏差与负偏差两大类。
实际溶液中,正偏差的溶液比负偏差者多蒸馏与精馏原理简单蒸馏与平衡蒸馏简单蒸馏:只适用于混合液中各组分的挥发度相差较大,而分离要求不高的情况,或者作为初步加工,粗略分离多组分混合液平衡蒸馏:为稳定连续过程,生产能力大。
化工原理习题蒸馏答案

第三部分蒸馏一、填空题1、蒸馏是用来分离均相液体混合物的单元操作。
2、含乙醇12%(质量百分数)的水溶液,其乙醇的摩尔分率为5.07%。
3、蒸馏操作是借助于液体混合物中各组分挥发度的差异而达到分离的目的。
4、进料板将精馏塔分为精馏段和提馏段。
5、理想溶液的气液相平衡关系遵循拉乌尔定律。
6、当一定组成的液体混合物在恒这一总压下,加热到某一温度,液体出现第一个气泡,此温度称为该液体在指定总压下的泡点温度,简称泡点。
7、在一定总压下准却气体混合物,当冷却到某一温度,产生第一个液滴,则此温度称为混合物在指定总压下的露点温度,简称露点。
8、理想溶液中各组分的挥发度等于其饱和蒸气压。
9、相对挥发度的大小反映了溶液用蒸馏分离的难易程度。
10、在精馏操作中,回流比的操作上限是全回流。
11、在精馏操作中,回流比的操作下限是最小回流比。
12、表示进料热状况对理论板数的影响的物理量为进料热状况参数。
13、q值越大,达到分离要求所需的理论板数越少。
14、精馏塔中温度由下而上沿塔高的变化趋势为逐渐降低。
15、当分离要求一定,回流比一定时,在五种进料状况中,冷液进料的值最大,此时,提馏段操作线与平衡线之间的距离最远,分离所需的总理论板数最少。
16、精馏过程是利用部分冷凝和部分汽化的原理而进行的。
精馏设计中,回流比越大,所需理论板越少,操作能耗增加,随着回流比的逐渐增大,操作费和设备费的总和将呈现先降后升的变化过程。
17、精馏设计中,当回流比增大时所需理论板数减小(增大、减小),同时蒸馏釜中所需加热蒸汽消耗量增大(增大、减小),塔顶冷凝器中冷却介质消耗量减小(增大、减小),所需塔径增大(增大、减小)。
18、分离任务要求一定,当回流比一定时,在5种进料状况中,冷液体进料的q 值最大,提馏段操作线与平衡线之间的距离最远, 分离所需的总理论板数最少。
19、相对挥发度α=1,表示不能用普通精馏分离分离,但能用萃取精馏或恒沸精馏分离。
化工原理-6章蒸馏

y x 1 ( 1)x
——相平衡方程
当 α为已知时,可用相对挥发度表示了气液相平衡关系。
当 1 当 1
y=x, 即相平衡时气相的组成与液相的组成相同, 不能用蒸馏方法分离。
则y>x,α愈大,y比x大的愈多,组分A和B愈易分离。
三、双组分理想溶液的气液平衡相图
双组分理想溶液的汽液平衡关系用相图表示比较直观、 清晰,而且影响蒸馏的因素可在相图上直接反映出来。蒸馏 中常用的相图为恒压下的温度-组成( t-x-y )图和气相-液 相组成( x-y )图。
当生产任务要求将一定数量和组成的原料分离成指定组成 的产品时,精馏塔计算的内容有:出液和塔釜残液的流量、塔 板数、进料口位置、塔高、塔径等。
6.4.1 全塔物料衡算
1.全塔物料衡算
单位时间为基准
总物料衡算: qn,F=qn,D+qn,W 易挥发组分物料衡算:
qn,FxF=qn,DxD+qn,WxW qn,F、qn,D、qn,W——流量,kmol/h
二、蒸馏的分类
1、按蒸馏方法:简单蒸馏、平衡蒸馏(闪蒸)、精馏、特殊精馏。 2、按操作压力:常压;减压;加压。 3、按原料液组分数:双组分蒸馏和多组分蒸馏 4、按操作方式:间歇蒸馏和连续蒸馏。
三、蒸馏操作的特点
优点:* 适用面广,液体混合物和气体混合物均可 * 操作流程较简单,无需其他外加介质
缺点:* 能耗大
一、利用饱和蒸气压计算气液平衡关系
法国物理学家拉乌尔在1887年研究含有非挥发性溶质的 稀溶液的行为时发现的,可表述为:“在某一温度下,稀溶 液的蒸气压等于纯溶剂的蒸气压乘以溶剂的摩尔分数”。
PA PA0 xA ——拉乌尔定律
pA0——纯组分A在溶液温度下的饱和蒸气压,Pa; xA——溶液中组分A的摩尔分数;
化工原理_大题第六章

第六章 习题4.在常压下将某原料液组成为0.6(易挥发组分的摩尔分数)的两组分洛液分别进行简单蒸馏和平衡蒸馏,若汽化率为1/3,试求两种情况下的釜液和馏出液组成。
假设在操作范围内气液平衡关系可表示为y=0.46x+0.549解:(1)简单蒸馏釜液由下式求得,即 bx m b x m m W F +-+--=21)1()1(ln 11ln ln 20.61210.5490.540.51ln 20.540.5490.5490.5483x w x dx x w -==-+-⨯⎰ 解得 20.498x = (即汽化液为1/3时的釜液组成)馏出液的平均组成,D m x 由一批操作的物料衡算求得1,1,120.60.498330.804D m D m w x w x =⨯-⨯= (2)平衡蒸馏 由题意知,q =2/3 2/30.62 1.8112/312/31F X q y x x x q q =-=-=-+----(1) 而0.460.549y x ==(2)联立(1),(2)解得0.509x = 0.783D y x == 说明:相同汽化率下,简单蒸馏得到的,D m x 高与平衡蒸馏的D x 。
这是由于平衡蒸馏实现了蒸馏过程的连续化造成了物料混合,从而影响了分离效果。
5..在连续精馏塔中分离由二硫化碳和四氯化碳所组成的混合液。
已知原料液流量为4000kg/h,组成为0.3(二硫化碳的质量分数,下同)。
若要求釜液组成不大于0.05,馏出液回收率为88%。
试求馏出液的流量和组成,分别以摩尔流量和摩尔分数表示。
解:由全塔物料衡算得 (以上标“'”表示质量流量)'''''''F D m F D W F x Dx Wx =+⎧⎨=+⎩由于'0.88''D F Dx F x =所以''0.88''''F F w F x F x D x =+0.12''0.1240000.32880/''0.05400028801120/0.88''0.8840000.3'0.94311200.943/760.97(0.943/760.057/154F w F D D F x kg h W x D F W kg hF x x D x ⨯⨯===-=-=⨯⨯=====+摩尔分数)平均千摩尔质量:0.97760.0315478.3/m M kg Kmol =⨯+⨯=馏出液的摩尔流量:1120/78.314.3/D Kmol h ==7. .对习题6中的溶液,若原料液流量为100kmol/h,馏出液组成为0.95,釜液组成为0.04(以上均为易挥发组分的摩尔分数),回流比为2.5。
化工原理复习必看第6章_蒸馏习题

1.蒸馏是分离的一种方法,其分离依据是混合物中各组分的,分离的条件是。
答案:均相液体混合物,挥发性差异, 造成气液两相系统(每空1分,共3分)2.在t-x—y图中的气液共存区内,气液两相温度,但气相组成液相组成,而两相的量可根据来确定。
答案: 相等,大于,杠杆规则(每空1分,共3分)3.当气液两相组成相同时,则气相露点温度液相泡点温度。
答案:大于(每空1分)4.双组分溶液的相对挥发度α是溶液中的挥发度对的挥发度之比,若α=1表示。
物系的α值愈大,在x—y图中的平衡曲线愈对角线。
答案:易挥发组分,难挥发组分,不能用普通蒸馏方法分离远离(每空1分,共4分)5.工业生产中在精馏塔内将过程和过程有机结合起来而实现操作的.而是精馏与普通精馏的本质区别。
答案:多次部分气化,多次部分冷凝,回流(每空1分,共3分)6.精馏塔的作用是。
答案:提供气液接触进行传热和传质的场所。
(2分)7.在连续精馏塔内,加料板以上的塔段称为,其作用是 ;加料板以下的塔段(包括加料板)称为________,其作用是。
答案:精馏段(1分)提浓上升蒸汽中易挥发组分(2分)提馏段提浓下降液体中难挥发组分(2分)(共6分)8.离开理论板时,气液两相达到状态,即两相相等,____互成平衡。
答案: 平衡 温度 组成 (每空1分,共3分)9. 精馏塔的塔顶温度总是低于塔底温度,其原因有(1) 和(2) 。
答案: 塔顶易挥发组分含量高 塔底压力高于塔顶(每空2分,共4分)10. 精馏过程回流比R 的定义式为 ;对于一定的分离任务来说,当R= 时,所需理论板数为最少,此种操作称为 ;而R= 时,所需理论板数为∞。
答案:R=DL∞ 全回流 R min (每空1分,共4分) 11. 精馏塔有 进料热状况,其中以 进料q 值最大,进料温度____泡点温度。
答案: 五种 冷液体 小于(每空1分,共3分)12. 某连续精馏塔中,若精馏段操作线方程的截距等于零,则回流比等于____,馏出液流量等于 ,操作线方程为 .答案: ∞ 零 y n+1=x n (每空1分,共3分)13. 在操作的精馏塔中,第一板及第二板气液两相组成分别为y 1,x 1及y 2,x 2;则它们的大小顺序为 最大, 第二, 第三,而 最小. 答案: y 1 y 2 x 1 x 2 (每空1分,共4分)14. 对于不同的进料热状况,x q 、y q 与x F 的关系为(1)冷液进料:x q x F ,y q x F ; (2)饱和液体进料:x q x F ,y q x F ; (3)气液混合物进料:x q x F ,y q x F f ; (4)饱和蒸汽进料:x q x F ,y q x F ; (5)过热蒸汽进料:x q x F ,y q x F ;答案:大于 大于(1分)等于 大于(1分)小于 大于(1分)小于 等于(1分)小于 小于(1分)(共5分)15. 精馏操作时,增大回流比R ,其他操作条件不变,则精馏段液气比VL( ),馏出液组成x D ( ),釜残液组成x W ( ).A 增加B 不变C 不确定D 减小答案: A A D(每空1分,共3分)精馏塔的设计中,若进料热状况由原来的饱和蒸气进料改为饱和液体进料,其他条件维持不变,则所需的理论塔板数N T ( ),提馏段下降液体流量L /( )。
化工原理 第六章 蒸馏(传质过程)

t
121.9℃
X=0.383
负偏差
x y
x y
y
y
x
x
19
挥发度与相对挥发度
挥发度:表示某种溶液易挥发的程度。 若为纯组分液体时,通常用其当时温度下饱和蒸 气压PA°来表示。 若为混合溶液时,各组分的挥发度,则用它在一 定温度下蒸气中的分压和与之平衡的液相中该组 分的 摩尔分数之比来表示, vA = pA / xA vB = pB / xB
演示
37
xn
xn 1 yn 1 yn
第四节 双组分连续精馏计算
38
物料衡算
F—原料(液)摩尔流量,kmol/h; D—馏出液摩尔流量,kmol/h; W—釜残液摩尔流量,kmol/h; 总物料衡算 易挥发组分的物料衡算
D xD F xF
F D W
D F ( xF xW ) xD xW
xn 1
n 1
yn xn yn 1
n
n 1
T-x(y) 图
t 假设蒸汽和液体充分接触,并在离 n 1 开第 n 层板时达到相平衡,则 yn 与 xn t n t n 1 平衡,且yn>yn+1,xn<xn-1。
这说明塔板主要起到了传质作用, 使蒸汽中易挥发组分的浓度增加, 同时也使液体中易挥发组分的浓度 减少。
t5 t4 t3 t2 t1
E D
C
B A
x(y)
温度-组成图( t-x-y 图)
12
上述的两条曲线将tx-y图分成三个区域。
液相线以下的区域 代表未沸腾的液体, 称为液相区 气相线上方的区域 代表过热蒸气,称为 过热蒸气区; 二曲线包围的区域 表示气液同时存在, 称为气液共存区。
化工原理(第四版)习题解第六章蒸馏
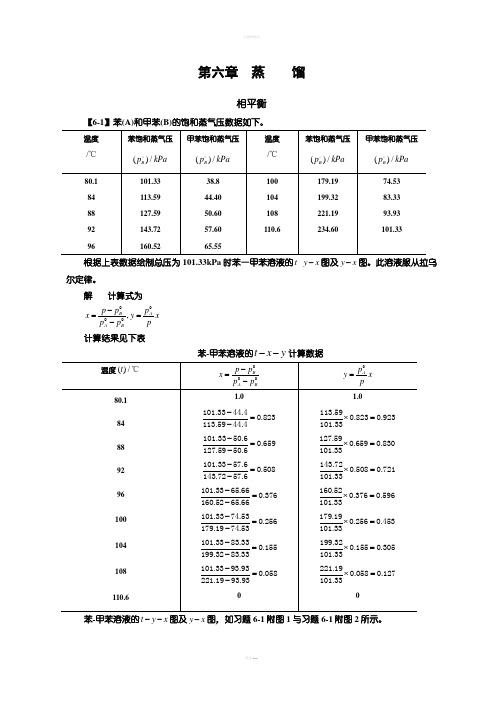
第六章 蒸 馏相平衡【6-1】苯(A)和甲苯(B)的饱和蒸气压数据如下。
101.33 38.8 179.19 74.53 根据上表数据绘制总压为101.33kPa 时苯一甲苯溶液的-t y x -图及y x -图。
此溶液服从拉乌尔定律。
解 计算式为,0000B AA Bp p p x y x p p p -==- 计算结果见下表苯-甲苯溶液的t x y --计算数据苯-甲苯溶液的t y x --图及y x -图,如习题6-1附图1与习题6-1附图2所示。
习题6-1附图1 苯-甲苯t-y-x 图习题6-1附图2 苯-甲苯y-x 图【6-2】在总压.101325kPa 下,正庚烷-正辛烷的汽液平衡数据如下。
温度/℃ 液相中正庚烷的摩尔分数()x汽相中正庚烷的摩尔分数()y温度/℃ 液相中正庚烷的摩尔分数()x 汽相中正庚烷的摩尔分数()y 98.4 105 1101.0 0.656 0.4871.0 0.81 0.673115 120 125.60.311 0.157 00.491 0.280 0试求:(1)在总压.101325kPa 下,溶液中正庚烷为0.35(摩尔分数)时的泡点及平衡汽相的瞬间组成;(2)在总压.101325kPa 下,组成.035x =的溶液,加热到117℃,处于什么状态?溶液加热到什么温度,全部汽化为饱和蒸气?解 用汽液相平衡数据绘制t y x --图。
(1) 从t y x --图上可知,.035x =时的泡点为113.8℃,平衡汽相的瞬间组成.053y =。
(2) .035x =的溶液,加热到117℃时为气液混合物,液相组成.024x =,汽相组成.040y =。
.035x =的溶液加热到118℃时,全部汽化为饱和蒸气。
习题6-2附图 正庚烷-正辛烷t-y-x 图【6-3】 甲醇(A)-丙醇(B)物系的汽液平衡服从拉乌尔定律。
(1) 试求温度80℃t =、液相组成.05x =(摩尔分数)时的汽相平衡组成与总压。
最新“化工原理”第6章《精馏》复习题.

《化工原理》第六章“精馏”复习题一、填空题1. 在汽-液相平衡的t-x-y 图中,沸点与液相组成的关系曲线,称为 _______ ,沸点与汽相组成的曲线,称为_____________ .( *** 答案*** 液相线(或泡点线)汽相线(或露点线))2. 在汽-液相平衡的t-x-y 图中, 液相线与汽相线将图平面平分为三个区:汽相线以上的区域称为_______ ,液相线以下的区域称为 _________ ,汽.液相线之间的区域为____________ .(*** 答案*** 汽相区液相区汽液共存区)3. 在y-x 图中,以A 组份标绘的平衡曲线在对角线的左上方,则表示A 组分比B 组分的挥发度______ •平衡曲线若在对角线的右下方,则表示A组分比B组分挥发度_____ .(***答案***高低)4. 精馏过程,就是利用混合液的各组分具有不同的__________________ ,利用_______________ 、_____________ 的方法,将各组分得以分离的过程• (*** 答案*** 沸点(或挥发度)多次部分汽化多次部分冷凝)5. 某泡点进料的连续精馏塔中,进料组成xf=0.35,系统的平均相对挥发度 a =2.44,当xf=0.93时,达到此分离要求的最小回流比Rmin=_____ . (*** 答案*** 1.66)6. 当塔板中上升的汽相与下降液相之间达到________ 时,该塔板称理论塔板。
*** 答案*** (相平衡)7. 分离某些a接近1的物系时,可采用一些特殊的精馏方法,如______ , __________ .(*** 答案*** 萃取精馏恒沸精馏)8. 分离要求一定。
当回流比为一定时,在五种进料状况中, ______ 进料的q值最大,其温度___________ , 此时,提馏段操作线与平衡线之间的距离________ , 分离所需的总理论板数_______________ 。
化工原理答案

第六章 蒸 馏11、在连续精馏操作中,已知精馏段操作线方程及q 线方程分别为y =0.8x +0.19;y = -0.5x +0.675,试求:(1)进料热状况参数q 及原料液组成x F ;(2)精馏段和提馏段两操作线交点坐标。
解:由q 线方程 y = -0.5x +0.675知5.01-=-q q 故q =1/3 又675.01=--q x F 故x F =0.675(1-q )=0.675×(1 -1/3)=0.45 因为精馏段操作线与提馏段操作线交点也是精馏段操作线与q 线的交点,所以y q = -0.5x q +0.675y q =0.8x q +0.18 联立求解 x q =0.373 y q =0.48912、用逐板计算习题10中泡点进料时精馏段所需理论板层数。
在该组成范围内平衡关系可近似表达为y =0.46x +0.545解:由习题10知 x F =0.4 、x D =0.95 、R =2.6设塔顶为全凝器,故y 1=x D =0.95由平衡关系 y 1=0.46x 1+0.545=0.95 得 x 1=0.88由精馏段操作线方程26.072.06.395.06.36.2111+=+=+++=+n n D n n x x R x x R R y 得 y 2=0.72×0.88+0.26=0.89又 0.46x 2+0.545=0.89 得 x 2=0.75同理 y 3=0.72×0.75+0.26=0.80又 0.46x 3+0.545=0.80得 x 3=0.55y 3=0.72×0.55+0.26=0.66又 0.46x 4+0.545=0.66得 x 4=0.25<x F∴ 精馏段理论板层数为3层,第四层为进料板。
13、在常压连续精馏塔中分离苯-甲苯混合液。
若原料为饱和液体,其中含苯0.5(摩尔分数,下同),塔顶馏出液组成为0.95,釜液组成为0.06,操作回流比为2.6。
化工原理下第六章 蒸馏习题课讨论题

第六章蒸馏习题课讨论题
某车间用一连续精馏塔,分离含苯0.4(摩尔分率,下同)的苯-甲苯混合液,进料量为100 kmol/h,进料状态为汽、液混合进料,其中含液体量为80%。
该塔在塔顶、塔底分别得含苯0.97和含甲苯0.97的产品。
现在精馏段某一板上取样分析,获得上升蒸汽的组成为0.82,下降液体的组成为0.7,并测得该板效率(汽相)为0.65,若该塔在最佳位置进料,操作条件下相对挥发度α可取为2.47,试求:
1.塔顶、塔底的产品流量;
2.塔的操作回流比以及该条件下的最小回流比;
3.若该塔有实际板20块,求该塔的总板效率;
4.精馏段、提馏段的汽相和液相流率;
5.为减小物耗,欲将釜液中苯含量降为0.5%,
①在操作上应采取什么措施,再沸器热负荷变化百分数;
②若对塔实施改造,应增加多少块实际板(效率同上);
③每年多回收苯多少吨;
④塔两端哪些参数会发生变化,如何变化,有何问题。
化工原理(第四版)习题解 第六章 蒸馏
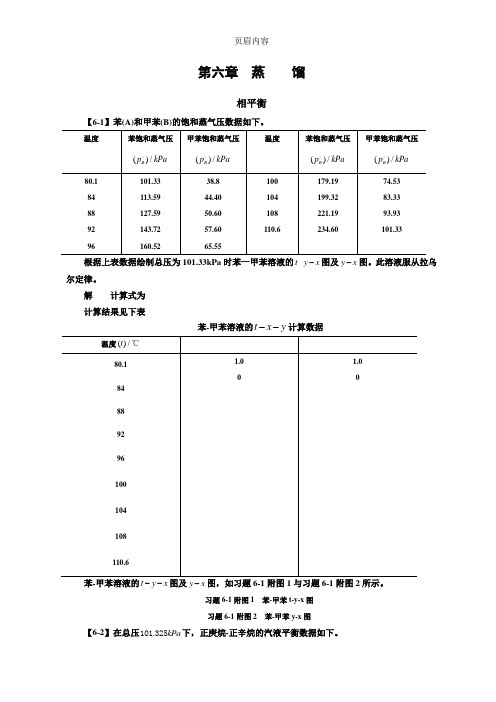
第六章 蒸 馏相平衡【6-1】苯(A)和甲苯(B)的饱和蒸气压数据如下。
)/B kPa )/B kPa )/B kPa )/B kPa 101.33 113.59 38.8 44.40179.19 199.32 74.53 83.33 根据上表数据绘制总压为101.33kPa 时苯一甲苯溶液的-t y x -图及y x -图。
此溶液服从拉乌尔定律。
解 计算式为 计算结果见下表苯-甲苯溶液的t x y --计算数据苯-甲苯溶液的t y x --图及y x -图,如习题6-1附图1与习题6-1附图2所示。
习题6-1附图1 苯-甲苯t-y-x 图 习题6-1附图2 苯-甲苯y-x 图【6-2】在总压.101325kPa 下,正庚烷-正辛烷的汽液平衡数据如下。
试求:(1)在总压.101325kPa 下,溶液中正庚烷为0.35(摩尔分数)时的泡点及平衡汽相的瞬间组成;(2)在总压.101325kPa 下,组成.035x =的溶液,加热到117℃,处于什么状态?溶液加热到什么温度,全部汽化为饱和蒸气?解 用汽液相平衡数据绘制t y x --图。
(1) 从t y x --图上可知,.035x =时的泡点为113.8℃,平衡汽相的瞬间组成.053y =。
(2) .035x =的溶液,加热到117℃时为气液混合物,液相组成.024x =,汽相组成.040y =。
.035x =的溶液加热到118℃时,全部汽化为饱和蒸气。
习题6-2附图 正庚烷-正辛烷t-y-x 图【6-3】 甲醇(A)-丙醇(B)物系的汽液平衡服从拉乌尔定律。
(1) 试求温度80℃t =、液相组成.05x =(摩尔分数)时的汽相平衡组成与总压。
(2) 试求总压为.10133kPa 、液相组成.04x =(摩尔分数)时的汽液相平衡温度与汽相组成。
(3) 试求液相组成.06x =、汽相组成.084y =时的平衡温度与总压。
组成均为摩尔分数。
用Antoine 方程计算饱和蒸气压(kPa) 甲醇 .lg ..15749971973623886A p t =-+丙醇 .lg .137514674414193B p t =-+式中t 为温度,℃。
化工原理学习指导 第6章 蒸馏 计算题答案.

化工原理学习指导 第6章 蒸馏 计算题答案6-31 某二元混合物蒸汽,其中轻、重组分的摩尔分数分别为0.75和0.25,在总压为300kPa 条件下被冷凝至40℃,所得的汽、液两相达到平衡。
求其汽相摩尔数和液相摩尔数之比。
已知轻、重组分在40℃时的蒸汽压分别为370kPa 和120kPa 。
解:两相中,720.01203701203000B0A 0B =--=--=p p p p x 888.0300720.03700A A =⨯===x p p p p y设汽相摩尔量为V ,液相摩尔量为L ,总量为F ,则L V F +=Lx Vy Fx F +=由以上两式可得:217.075.0888.072.075.0F F =--=--=x y x x L V 事实上,汽液平衡体系中,两相的摩尔量比值服从杆杠定律。
6-32 苯和甲苯组成的理想溶液送入精馏塔中进行分离,进料状态为汽液共存,其两相组成分别如下:5077.0F =x ,7201.0F =y 。
用于计算苯和甲苯的蒸汽压方程如下:8.2201211031.6lg 0A +-=t p5.2191345080.6lg 0B +-=t p其中压强的单位为Pa ,温度的单位为℃。
试求:(1)该进料中两组份的相对挥发度为多少?(2)进料的压强和温度各是多少?(提示:设进料温度为92℃) 解:(1)混合物中两组分的相对挥发度:49.25077.015077.07201.017201.011F F F F=--=--=x x y y α (2)设进料温度为92℃,则16.28.220921211031.6lg 0A =+-=pkPa 38.1440A =p 762.15.219921345080.6lg 0B =+-=pkPa 83.570B =p由此求得体系的相对挥发度为:496.283.5738.144'0B0A ===p p α 其值与(1)中所求相对挥发度足够接近,故可认为进料温度为92℃。
化工原理习题答案-第六章-第九章
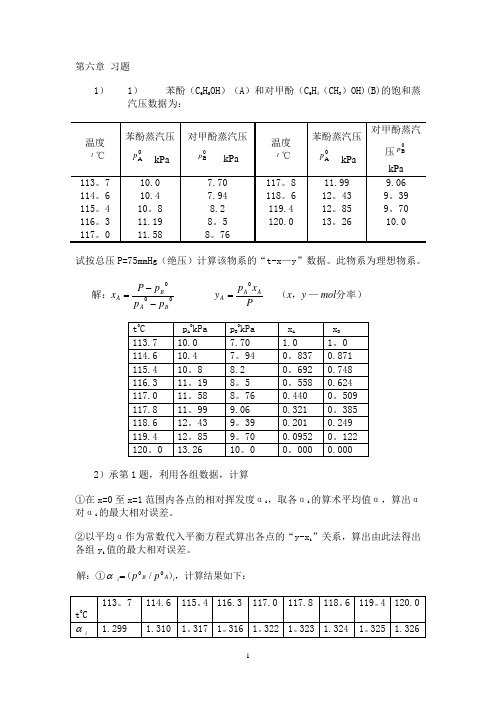
第六章 习题1)1) 苯酚(C 6H 5OH )(A )和对甲酚(C 6H 4(CH 3)OH)(B)的饱和蒸汽压数据为:试按总压P=75mmHg (绝压)计算该物系的“t-x —y ”数据。
此物系为理想物系。
分率)—,(解:mol y x P xp y p p p P x AA A BA BA 00=--=2)承第1题,利用各组数据,计算①在x=0至x=1范围内各点的相对挥发度αi ,取各αi 的算术平均值α,算出α对αi 的最大相对误差。
②以平均α作为常数代入平衡方程式算出各点的“y-x i ”关系,算出由此法得出各组y i 值的最大相对误差。
,计算结果如下:)(解:①i A B i p p 00/=α%46.1299.1299.1318.1318.1=-===∑最大误差niαα计,结果如下:按)()318.1112αααiii x x y -+=t 0C113。
7 114.6 115。
4 116.3 117。
0 117.8 118。
6 119。
4 120。
0 x i 1。
0 0。
837 0.692 0.558 0。
440 0。
321 0。
201 0。
0952y i1.0 0。
871 0.748 0。
625 0。
509 0.384 0.249 0.122 0最大误差=31060.2385.0385.0384.0-⨯-=-3)已知乙苯(A )与苯乙烯(B )的饱和蒸汽压与温度的关系可按下式算得:式中p 0的单位是mmHg,T 的单位是K.问:总压为60mmHg (绝压)时,A 与B 的沸点各为多少℃?在上述总压和65℃时,该物系可视为理想物系。
此物系的平衡汽、液相浓度各为多少摩尔分率?CK T T Ln B t p p CK T T Ln A t p p B B A A 00007.6985.34272.63/57.33280193.16608.6195.33495.59/47.32790195.1660)1==∴--====∴--==)(的沸点为,算得的令)(的沸点为算得的,令解:mmHgp Lnp KC t mmHg p A A 81.6895.5915.338/47.32790195.1615.33865602000=∴--====)(,)639.060557.081.68557.092.4881.6892.486092.4872.6315.338/57.33280193.1600=⨯==--==∴--=A A B B y x mmHgp Lnp )(4)苯(A)和甲苯(B)混合液可作为理想溶液,其各纯组分的蒸汽压计算式为式中p 0的单位是mmHg ,t 的单位是℃。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第六章 蒸 馏相平衡【6-1】苯(A)和甲苯(B)的饱和蒸气压数据如下。
温度/℃苯饱和蒸气压()/B p kPa甲苯饱和蒸气压()/B p kPa温度/℃苯饱和蒸气压()/B p kPa甲苯饱和蒸气压()/B p kPa80.1 84 88 92 96101.33 113.59 127.59 143.72 160.5238.8 44.40 50.60 57.60 65.55100 104 108 110.6179.19 199.32 221.19 234.6074.53 83.33 93.93 101.33根据上表数据绘制总压为101.33kPa 时苯一甲苯溶液的-t y x -图及y x -图。
此溶液服从拉乌尔定律。
解 计算式为,0000B AA Bp p p x y x p p p -==- 计算结果见下表苯-甲苯溶液的t x y --计算数据温度()/t ℃00BA Bp p x p p -=- 0A p y x p=80.1 84 88 92 96 100 104 108 110.61.0 (10133444)082311359444-=- (10133506)065912759506-=- (10133576)050814372576-=- (101336566)0376160526566-=- (101337453)0256179197453-=- (101338333)0155199328333-=- (101339393)0058221199393-=-1.0 (11359)0823092310133⨯= (12759)0659083010133⨯= (14372)0508072110133⨯= (16052)0376059610133⨯= (17919)0256045310133⨯= (19932)0155030510133⨯= (22119)0058012710133⨯=苯-甲苯溶液的t y x --图及y x -图,如习题6-1附图1与习题6-1附图2所示。
习题6-1附图1 苯-甲苯t-y-x 图习题6-1附图2 苯-甲苯y-x 图【6-2】在总压.101325kPa 下,正庚烷-正辛烷的汽液平衡数据如下。
温度/℃ 液相中正庚烷的摩尔分数()x汽相中正庚烷的摩尔分数()y温度/℃ 液相中正庚烷的摩尔分数()x 汽相中正庚烷的摩尔分数()y 98.4 105 1101.0 0.656 0.4871.0 0.81 0.673115 120 125.60.311 0.157 00.491 0.280 0试求:(1)在总压.101325kPa 下,溶液中正庚烷为0.35(摩尔分数)时的泡点及平衡汽相的瞬间组成;(2)在总压.101325kPa 下,组成.035x =的溶液,加热到117℃,处于什么状态?溶液加热到什么温度,全部汽化为饱和蒸气?解 用汽液相平衡数据绘制t y x --图。
(1) 从t y x --图上可知,.035x =时的泡点为113.8℃,平衡汽相的瞬间组成.053y =。
(2) .035x =的溶液,加热到117℃时为气液混合物,液相组成.024x =,汽相组成.040y =。
.035x =的溶液加热到118℃时,全部汽化为饱和蒸气。
习题6-2附图 正庚烷-正辛烷t-y-x 图【6-3】 甲醇(A)-丙醇(B)物系的汽液平衡服从拉乌尔定律。
(1) 试求温度80℃t =、液相组成.05x =(摩尔分数)时的汽相平衡组成与总压。
(2) 试求总压为.10133kPa 、液相组成.04x =(摩尔分数)时的汽液相平衡温度与汽相组成。
(3) 试求液相组成.06x =、汽相组成.084y =时的平衡温度与总压。
组成均为摩尔分数。
用Antoine 方程计算饱和蒸气压(kPa) 甲醇 .lg ..15749971973623886A p t =-+丙醇 .lg .137514674414193B p t =-+式中t 为温度,℃。
解 (1) 80℃t =)时,..1811,5093A B p kPa p kPa ==BA Bp p x p p -=-总压 ()()....18115093055093116A B B p p p x p kPa =-+=-⨯+= 汽相组成 (181105)0781116A p x y p ⨯=== (2) 已知..10133,04,求、p kPa x x y ==.10133p kPa =时,甲醇沸点为64.7℃,丙醇沸点为97.2℃,所求汽液相平衡温度必在64.7℃与97.2℃之间。
假设75℃t = 计算.1511,41A B p kPa p kPa == 液相组成 (1013341)054804151141B A Bp p x p p --===>-- 计算的x 值大于已知的x 值,故所假设的温度t 偏小,重新假设大一点的t 进行计算。
将3次假设的t 与计算的x 值列于下表,并在习题6-3附图1上绘成一条曲线,可知.04x =时的平衡温度.795℃t=。
习题6-3附表计算次数第一次第二次第三次假设/t℃75 80 85 x0.548 0.387 0.252习题6-3 附图1.795℃t=时,.1779Ap kPa=汽相组成....177904=070210133Ap xyp⨯==(3)已知..06,084,求,x y t p==计算().(.).().(.)1084106351061084ABp y xx yp--===--待求的温度t,就是/.35A Bp p=时的温度,用试差法计算。
假设..80℃,1811,5093A Bt p kPa p kPa===...181135565093ABpp==,大于3.5温度t越小,则/A BP p就越大,故所假设的t偏小。
假设..85℃,2159,6275A Bt p kPa p kPa===...21593446275ABpp==用比例内插法求/.=35A Bp p时的温度t......803535560056=858034435560116t---=---()...0056808580824℃0116t=+-⨯=在此温度下,..1972,5635A B p kPa p kPa ==,则 ./..1972355635A B p p == 故.824℃t =为待求的温度 总压 (197206)1409084A p x p kPa y ⨯=== 【6-4】 甲醇(A)-乙醇(B)溶液(可视为理想溶液)在温度20℃下达到汽液平衡,若液相中甲醇和乙醇各为l00g ,试计算汽相中甲醇与乙醇的分压以及总压,并计算汽相组成。
已知20℃时甲醇的饱和蒸气压为11.83kPa ,乙醇为5.93kPa 。
解 甲醇和乙醇的摩尔质量分别为32和46。
甲醇为易挥发组成,液相组成为 ///100320.591003210046x ==+ 摩尔分数甲醇分压 ..11830.59698A A p p x kPa ==⨯=乙醇分压 ()()..1=59310.59=243B B p p x kPa =-⨯- 总压 ...698243941A B p p p kPa =+=+= 汽相组成 (698)0742941y == 【6-5】总压为120kPa ,正戊烷(A)与正己烷(B)汽相混合物的组成为0.6(摩尔分数),冷却冷凝到55℃,汽液相呈平衡状态。
试求液相量与汽相量之比值(摩尔比)。
此物系为理想物系。
55℃下纯组务的饱和蒸气压分别为..18518,6444A B p kPa p kPa ==。
解 液相组成 (1206444)0.46185186444B A B p p x p p --===--汽相组成 (18518046)=071120A p x y p ⨯== 液相量L 与汽相量V 之比值 (07106)078606046s s y x L V x x --===--(摩尔比) 【6-6】利用习题6-1的苯一甲苯饱和蒸气压数据,(1)计算平均相对挥发度α;(2)写出汽液相平衡方程;(3)计算y x -的系列相平衡数据,并与习题6-1作比较。
解 (1) 80.1℃时 ...110133261388A Bp p α=== 110.6℃时 (22346)23210133α== 从计算结果可知,温度高,相对挥发度小。
平均...12261232246ααα==⨯= (2) 汽液相平衡方程.().246111146x xy x xαα==+-+ (3)计算y x -平衡数据,与习题6-1的计算结果接近。
/t ℃ 80.1 84 88 92 96 100 104 108 110.6 x 1 0.823 0.659 0.508 0.376 0.256 0.155 0.058 0 y10.920.8260.7180.5970.4580.3110.131【6-7】 甲醇和丙醇在80℃时的饱和蒸气压分别为181.lkPa 和50.93kPa 。
甲醇一丙醇溶液为理想溶液。
试求:(1) 80℃时甲醇与丙醇的相对挥发度α;(2)在80℃下汽液两相平衡时的液相组成为0.5,试求汽相组成;(3)计算此时的汽相总压。
解 (1)甲醇和丙醇在80℃时的相对挥发度 (181135565093)A B p p α=== (2) .05x = ...()(.).35560507811113556105x y x αα⨯===+-+-⨯(3) 总压 (181105)==1160781A p x p kPa y ⨯=物料衡算及恒摩尔流量假设【6-8】由正庚烷与正辛烷组成的溶液在常压连续精馏塔内进行分离。
原料的流量为5000kg/h ,其中正庚烷的质量分数为0.3。
要求馏出液中能回收原料中88%的正庚烷,釜液中正庚烷的质量分数不超过0.05。
试求馏出液与釜液的摩尔流量,及馏出液中正庚烷的摩尔分数。
解 先将质量流量换算为摩尔流量,质量分数换算为摩尔分数,再作物料衡算。
正庚烷()716C H 的摩尔质量/100A M kg kmol =,正辛烷()818C H 的摩尔质量/114B M kg kmol =。
(03)10003280307100114F x ==+ (00510000566005095)100114W x ==+ 原料的平均摩尔质量为().../1000328114103281094kg kmol ⨯+-=原料的摩尔流量 ..5000457/1094F kmol h == 将已知数.0328F x =(摩尔分数)、.00566W x =(摩尔分数)及./457F kmol h =,代入馏出液采出率计算式F W D W x x D F x x -=- (032800566)45700566D D x -=- ()1 并代入馏出液中正庚烷的回收率表达式.088D F Dx Fx = (0884570328)DDx =⨯ ()2 由式(1)与式(2)求得馏出液流量./139D kmol h =,馏出液中正庚烷的摩尔分数.0948D X =。
